Tema 1: La actividad Científica
La Medida
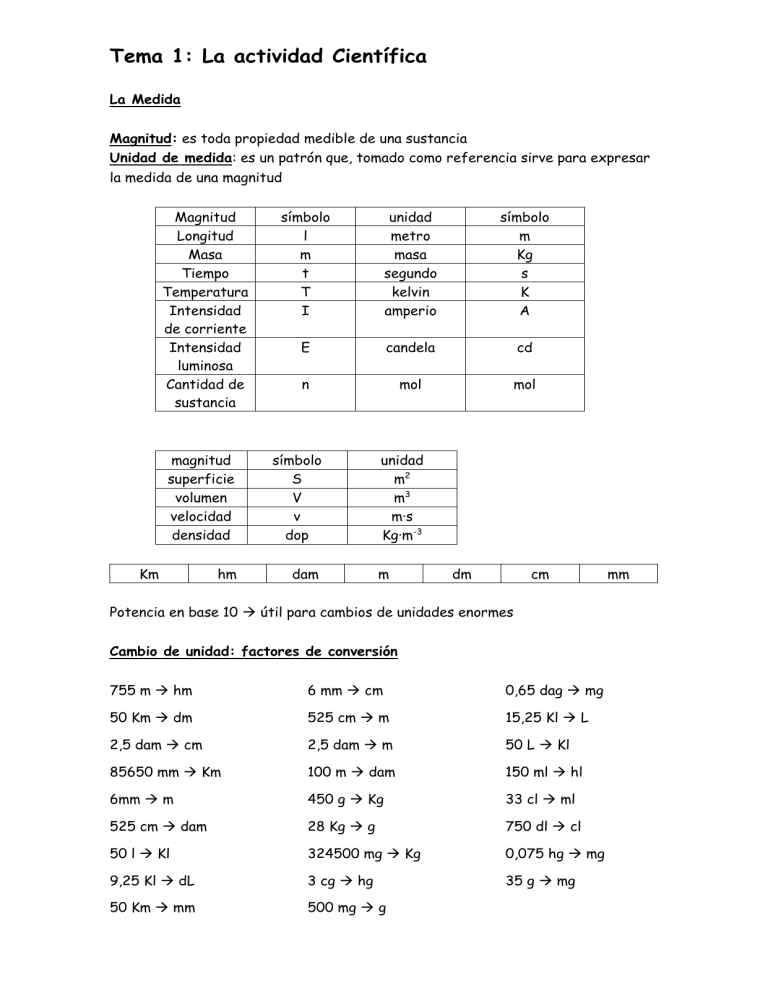
Magnitud: es toda propiedad medible de una sustancia
Unidad de medida: es un patrón que, tomado como referencia sirve para expresar
la medida de una magnitud
Magnitud
Longitud
Masa
Tiempo
Temperatura
Intensidad
de corriente
Intensidad
luminosa
Cantidad de
sustancia
símbolo
l
m
t
T
I
unidad
metro
masa
segundo
kelvin
amperio
símbolo
m
Kg
s
K
A
E
candela
cd
n
mol
mol
magnitud
superficie
volumen
velocidad
densidad
símbolo
S
V
v
dop
hm
dam
Km
unidad
m2
m3
m·s
Kg·m-3
m
dm
cm
Potencia en base 10 útil para cambios de unidades enormes
Cambio de unidad: factores de conversión
755 m hm
6 mm cm
0,65 dag mg
50 Km dm
525 cm m
15,25 Kl L
2,5 dam cm
2,5 dam m
50 L Kl
85650 mm Km
100 m dam
150 ml hl
6mm m
450 g Kg
33 cl ml
525 cm dam
28 Kg g
750 dl cl
50 l Kl
324500 mg Kg
0,075 hg mg
9,25 Kl dL
3 cg hg
35 g mg
50 Km mm
500 mg g
mm
Tema 2: La materia y sus estados
Materia: Es todo aquello que tiene masa y que ocupa un volumen. Una sustancia es
cada uno de los tipos de materia
Masa: Es la cantidad de materia que tiene un cuerpo.
Volumen: Es el espacio ocupado por un cuerpo.
Densidad: Es una magnitud física que indica la masa que tiene un cuerpo por unidad
de volumen. Sus unidades en el S.I. son el kg/m3.
d= m/v
Sustancias: cada uno de los tipos de materia
Propiedades de la materia: se clasifican en generales y especificas
Cualquier sustancia, en función de sus condiciones de temperatura o presión, puede
presentar 3 estados de agregación distintos: sólido, líquido, gaseoso.
Los estados de agregación.
Ley de Boyle-Mariotte. La presión y el volumen de un gas, a temperatura
constante, son inversamente proporcionales. A mayor presión, menor volumen y
viceversa.
P·V=constante
Ley de Charles-Gay-Lussac.
La temperatura y la presión en un gas, a volumen constante, son directamente
proporcionales. A mayor presión, mayor temperatura y viceversa.
P·T =constante
La temperatura y el volumen en un gas, a presión constante, son directamente
proporcionales. A mayor temperatura mayor volumen, y viceversa.
V·T=constante
Ley de gases ideales En la ley que refunde, en una sola, las dos anteriores
P0·V0 /T =constante
𝑷𝒐 𝑽𝒐
𝑻𝒐
=
𝑷𝟏𝑽𝟏
𝑻𝟏
1. Calcula la densidad de una roca sabiendo que su masa es 480 g
y ocupa 200 cm3. Expresa ese resultado en unidades del SI.
2. Un trozo de madera tiene una masa de 250 g y ocupa 400 ml.
a) Halla su densidad en el SI
b) Halla la masa de otro trozo de esa misma madera, cuyo volumen es de 25 cm3
3. Una escultura de cobre tiene una masa de 4500 g y ocupa 500 cm3.
Calcula la densidad del cobre.
4. Una medalla de oro que tiene una masa de 38 g y un volumen de
2 cm3, ¿está hecha totalmente de oro? Datos: doro= 19300 kg/m3
5. Calcula la densidad del dióxido de carbono (CO2), si 1 litro de
dicho gas tiene una masa de 1,9 g. Expresa el resultado en unidades del SI.
6. La densidad del corcho es 250 kg/m3
a) Calcula el volumen de trozo de corcho de masa 30 g
b) Calcula la masa de un trozo de corcho de volumen 44 cm3
propiedades con los estados de agregación
SÓLIDO
LÍQUIDO
GASEOSO
Las partículas están muy próximas entre sí.
Tiene forma y volumen fijo.
Sus partículas suelen estar muy ordenadas.
No son compresibles.
Tiene volumen fijo pero su forma depende
del contenedor.
Son muy poco compresibles.
Pueden expandirse muy pocos
Adoptan la forma del recipiente que los
contiene.
Sus partículas están unidas por fuerzas muy
débiles.
Sus partículas tienen un movimiento caótico.
No tiene ni forma ni volumen fijo.
Adoptan la forma del recipiente que los
contiene.










