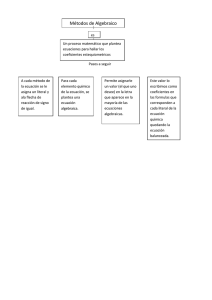
Área Académica: QUIMICA Tema: TIPOS DE BALANCEO DE ECUACIONES (tanteo, Algebraico y óxido reducción) Profesor: Q. LUCIANO HURTADO GONZALEZ Periodo: ENERO-JUNIO 2015 Tema: TIPOS DE BALANCEO DE ECUACIONES Abstract: Balancear una ecuación es realmente un procedimiento de ensayo y error, que se fundamenta en la búsqueda de diferentes coeficientes numéricos que hagan que el número de cada tipo de átomos presentes en la reacción química sea el mismo tanto en reactivos como en productos. Keywords: Método, Balanceo, Tanteo, Algebraico, Oxido redución 1. MÉTODO DEL TANTEO O INSPECCIÓN Este método es utilizado para ecuaciones sencillas y consiste en colocar coeficientes a la izquierda de cada sustancia, hasta tener igual número de átomos tanto en reactantes como en productos. EJEMPLO: N2 + H2 → NH3 Para balancearlos hay que colocar un coeficiente 3 al H2 y un coeficiente 2 al producto NH3: N2 + 3H2 → 2NH3 LA ECUACIÓN HA QUEDADO EQUILIBRADA. EL NÚMERO DE ÁTOMOS DE CADA ELEMENTO ES EL MISMO EN REACTIVOS Y PRODUCTOS. 2.- MÉTODO ALGEBRAICO. Para realizar este método de balanceo, se sugiere seguir los siguientes pasos: 1. Se asigna una literal a cada especie química de la reacción.(a,b,c,d,e,f,g….etc.) 2. Se establece una ecuación matemática para cada elemento participante en la reacción, utilizando las literales antes asignadas. 3. A la literal que más veces aparezca en las ecuaciones se le asigna el valor de 1 o a veces se puede asignar el valor de: 2 4.- Se resuelven algebraicamente los valores de las demás literales. 2.- MÉTODO ALGEBRAICO. 5.- Si los resultados obtenidos son fracciones se multiplica a todas por el mínimo común denominador, obteniendo de esta manera resultados enteros. 6.- Los valores así obtenidos corresponden a los coeficientes estequiométricos de cada especie química, por tanto se anotan en la reacción original. 7.- Comprueba ahora que la reacción se encuentre balanceada. 2.- MÉTODO ALGEBRAICO. Por ejemplo: Al + MnO2 ----------- Mn + Al2O3 Asignando literales. Al + MnO2 --------- Mn + Al2O3 a b c d Estableciendo una ecuación matemática para cada elemento: Al: a= 2d (especies en las que aparece y el número de átomos que hay) Mn: b =c O: 2b =3d 2.- MÉTODO ALGEBRAICO. Como la literal b aparece en dos ecuaciones le asignamos el valor de 1 y procedemos a resolver algebraicamente los otros valores: b =1 por lo tanto si: b =c entonces c = 1 Si 2b =3d entonces : 2= 3d y por lo tanto d = 2/3 Si a =2d entonces : a = 2(2/3) por lo tanto a = 4/3 Como tenemos fracciones, multiplicamos por el mínimo común denominador: A =4/3 x 3 = 4 B=1 x 3 = 3 C=1 x 3 = 3 D =2/3 x 3 = 2 2.- MÉTODO ALGEBRAICO. Por lo que los coeficientes estequiométricos, ya los obtuvimos, entonces procedemos a anotarlos en la reacción original: 4 Al + 3 MnO2 --------- 3 Mn + 2 Al 2O3 Si comprobamos la igualdad de átomos: Al: 4 contra 4: Mn: 3 contra 3; O: 6 contra 6 2.- MÉTODO ALGEBRAICO. Ejemplo 2 Para balancear de modo algebraico seguiremos los siguientes pasos: 1. Identificar reactivos y productos. 2. Al elemento que aparece la mayor cantidad de veces se le asigna el coeficiente 2. 3. Se asignan literales para cada componente. 4. Se resuelve sumando los valores de las literales de cada uno de los lados. 5. Colocar el respectivo coeficiente a cada compuesto. 2.- MÉTODO ALGEBRAICO. Ejemplo: C7 H 6O 2 O2 CO 2 H 2O a b c d C 7a 1c H 6a 2d O 2a 2b 2c d a2 c 7a 2d 6a 2a 2b 2c d c 7( 2) d c 14 d 6 2b 2c d 2a 2c d 2a b 2 b 15 6( 2) 2 De tal forma que al multiplicar los coeficientes de cada compuesto con el número de cada elemento, estos queden igual de cada lado: 2 C 7 H 6 O 2 15 O 2 14 CO 2 6 H 2 O C = 14 H = 12 O = 34 C = 14 H = 12 O = 34 3. MÉTODO DE OXIDO REDUCCIÓN Para utilizar éste método es necesario tener en cuenta que sustancia gana electrones y cual los pierde, además se requiere manejar los términos que aparecen en la siguiente tabla: CAMBIO EN ELECTRONES CAMBIO DE NÚMERO DE OXIDACIÓN Oxidación Perdida Aumento Reducción Ganancia Disminución Agente oxidante (sustancia que se reduce) Gana Disminuye Agente reductor (sustancia que se oxida) Pierde Aumenta BALANCEO ECUACIONES DE 3. MÉTODO DE OXIDO REDUCCIÓN Como los procesos de óxido-reducción son de intercambio de electrones, las ecuaciones químicas estarán igualadas cuando el número de electrones cedidos por el agente oxidante sea igual al recibido por el agente reductor. El número de electrones intercambiados se calcula fácilmente, teniendo en cuenta la variación de los números de oxidación de los elementos. 3. MÉTODO DE OXIDO REDUCCIÓN El mecanismo de igualación por el método de óxido-reducción es el siguiente : (a) Se escribe la ecuación del proceso.Se determina qué compuesto es el oxidante y el reductor, y qué átomos de estos compuestos son los que varían en su número de oxidación. Mn+4O2-2+ H+1 Cl-1 → Mn+2Cl2-1 + Cl20+ H2+1O-2 (b) Se calcula el número de oxidación de cada uno de estos átomos, tanto en su forma oxidada como reducida y se procede a escribir ecuaciones iónicas parciales. Mn+4+ 2Cl-1 + 2e-→ Mn+2 2e-→ Cl20 3. MÉTODO DE OXIDO REDUCCIÓN (c) Se establecen los coeficientes mínimos del oxidante y del reductor, de tal forma que el número total de electrones ganados y perdidos sea el mismo; para ello multiplicamos en las ecuaciones iónicas el número de electrones por los factores adecuados. (d) Se asignan como coeficientes de las sustancias afectadas en la ecuación, los factores que se utilizaron para que el número de electrones sea igual. MnO2 + 2HCl → MnCl2 + Cl2 + H2O (e) Por último el balanceo se determina por el método de inspección o ensayo y error. MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O 3. MÉTODO DE OXIDO REDUCCIÓN 3. MÉTODO DE OXIDO REDUCCIÓN (2) El esquema de igualación de electrones es como sigue: N+5 + 3e- → S-2 → N+2 S0 + (a) (b) - 2e (3) Para que el número de electrones ganados sea igual al de los perdidos, se multiplica la ecuación (a) por 2,y la ecuación (b) por3 2N+5 + 6e- → 6N+2 3S-2 → 3S0 + - 6e (a) (b) (4) Por tanto, el coeficiente del HNO3 y del NO es 2, y el del H2S y S es 3 en forma parcial, la ecuación esquemática es la siguiente; 2HNO3 + 3H2S→ 2NO + 3S + H2O 3. MÉTODO DE OXIDO REDUCCIÓN (5) Ajuste de H y O. Los átomos de H de la izquierda en la ecuación (2 de HNO3 y 6 del H2S) deberán formar 4H2O en la derecha de la ecuación. la ecuación final será: 2HNO3 + 3H2S→ 2NO + 3S + 4H2O Bibliografía: • UAEH, Educación Abierta y a Distancia, México 2002. • Química Mc Graw Hill, 2ª. Edición, México 1999 p.:633,480,493,690 (3) A. Chamizo, J.A.