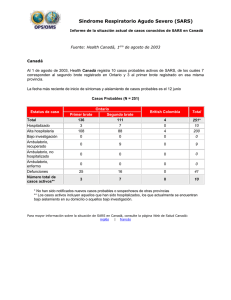
sars
Anuncio

Adaptado de Kamps-Hoffmann. www.SARSreference.com SARS Reference – 05/2003 Dr. Gustavo Reyes-Terán y colaboradores. Adaptado de: www.SARSReference.com por Kamps-Hoffmann et al. Flying Publishing Página 1 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Flying Publisher. Todos los derechos reservados Todo el material de este libro esta protegido por los derechos de autor. Ninguna parte de este libro puede ser reproducida y/o distribuida de manera alguna sin el permiso escrito del autor. Edición Mayo 2003. SARS Medicine es un campo siempre dinámico. Los autores y editores de SARSReference.com han hecho todo un esfuerzo para brindar información la cual está completa y es precisa hasta la fecha de publicación. Sin embargo, en vista de los rápidos cambios que ocurren en la ciencia médica, la prevención y política del SARS, así como la posibilidad de error humano, este texto pudiera contener errores técnicos, tipográficos o de otra índole. Se sugiere a los lectores revisar la información actual del producto brindada por el manufacturero de cada droga a ser administrada para verificar la dosis recomendada, el método y duración de la administración y las contraindicaciones. Es responsabilidad del médico tratante, el cual se basa en experiencia y conocimiento del paciente, determinar las dosis y el mejor tratamiento para el paciente. Por tanto, la información contenida es brindada “como es” y sin ninguna garantía. Los contribuyentes de este sitio, incluyendo el Grupo Amedeo y Flying Publisher, quedan exentos de cualquier responsabilidad por cualquier error u omisión, o por los resultados obtenidos por el uso de la información contenida en este manual. Kamps y Hoffman (eds.) Página 2 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Índice Capítulo 1: Resumen Capítulo 2: Cronología Referencias Capítulo 3: Virología Búsqueda del agente causal de SARS Descubrimiento de SARS Co-V Morfología Detección Estabilidad y resistencia Agente antiviral y resistencia Perspectivas Referencias Capítulo 4: Transmisión y prevención Vías de transmisión Condominios Amoy Gardens Factores que influyen en la transmisión Factores virales Factores del huésped Prevención Respuesta de los servicios de salud Control de infecciones en instalaciones de cuidado de salud Control de infección en albergues Referencias Capítulo 5: Epidemiología Lugar de propagación Propagación mundial Hong Kong, Febrero 2003 Vietnam, Febrero 2003 Toronto, Febrero 2003 Singapur, Febrero 2003 Beijing 2003, Abril 20 Otros Países SARS en Niños Perspectivas Referencias Capítulo 6: Definición de caso Definición de casos de la OMS Caso sospechoso Caso probable Criterios de exclusión Reclasificación de casos Definición de caso de la CDC Página 3 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Capítulo 7: Pruebas diagnósticas Pruebas de laboratorio Pruebas moleculares Aislamiento de virus Detección de anticuerpos Limitaciones Consideraciones de seguridad Perspectivas Tabla, figuras Capítulo 8: Diagnóstico Presentación Clínica Anormalidades en radiografía de tórax Curso clínico Diagnóstico Histopatología Biopsia de pulmón Hallazgos post-muerte Referencias Capítulo 9: Tratamiento Guías Referencias SARS pediátrico Referencias Página 4 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Prefacio Aproximadamente hace tres meses el SARS empezó a diseminarse alrededor de todo el mundo. Es la primera y nueva gran enfermedad infecciosa de este siglo y está tomando ventaja de las grandes oportunidades que los viajes internacionales ofrecen. Al momento de este escrito, 8 de mayo de 2003, más de 7,000 personas han sido infectadas en 29 países. Parece ser que en China, la enfermedad es de difícil control. Si no es controlada, el SARS cambiará la manera en la que vivimos nuestras vidas. La respuesta de la comunidad científica a esta nueva amenaza ha dejado sin aliento. La relación causal entre un coronavirus previamente desconocido y SARS fue establecida apenas un mes después de que la OMS desplegó una alerta global y convocó a aproximadamente 11 laboratorios reconocidos mundialmente en 9 países, a formar parte de un grupo de investigación multicéntrico para encontrar la etiología del SARS y simultáneamente desarrollar una prueba diagnóstica. La identificación temprana del virus, hace posible la investigación de compuestos antivirales y vacunas. La OMS, el CDC y las organizaciones nacionales se han encargado de difundir la información más reciente a todo el personal de la salud. La red de laboratorios creada por la OMS se aprovecha de la tecnología de comunicación avanzada (correo electrónico y portales de Internet) para que los resultados sobre la investigación en muestras clínicas de casos de SARS sean puestos a disposición en tiempo real. En la página de Internet de la OMS, la red de miembros comparte fotomicrografías electrónicas de los virus, secuencias de material genético para la identificación y caracterización de virus, aislados virales, y varias muestras de pacientes y de tejidos postmortem. Las muestras de un paciente pueden ser analizadas paralelamente por distintos laboratorios y los resultados pueden ser compartidos en tiempo real. Sin embargo, tal y como dijo Julie Gerberding del CDC: “ La velocidad del descubrimiento científico y la velocidad de las comunicaciones, son piedra angular en la respuesta ante el SARS y reflejan los grandes logros de la ciencia, tecnología y colaboración internacional. Sin embargo, a pesar de estos avances, existen aún algunas preguntas por contestar: ¿Somos acaso lo suficiente rápidos? ¿Podemos prevenir una pandemia de SARS?” No lo sabemos. Es la naturaleza de una epidemia ser impredecible. Lo que si sabemos es que se requieren de esfuerzos sin precedentes para darle forma a un mundo sin SARS. SARSReference.com acompañará a estos esfuerzos con actualizaciones mensuales a lo largo de la epidemia. Bernd Sebastián Kamps y Christian Hoffmann. www.HIVMedicine.com 8 de mayo de 2003. Página 5 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Capítulo 1. Resumen Traducción por: Dra. Alexandra Haddad Angulo. El síndrome agudo respiratorio severo (SARS) es una enfermedad respiratoria aguda causada por la infección con el virus del SARS (SARS-CoV). La fiebre, seguida de compromiso respiratorio rápidamente progresivo, es la clave de un complejo grupo de signos y síntomas, los cuales incluyen escalofrío, mialgias, cefalea e hiporexia. La mortalidad, inicialmente considerada como del 3%, pudiera llegar a ser hasta del 15%. La OMS estima que la proporción de casos letales por SARS varía de 0% a 50%, dependiendo en el grupo de edad afectado: menos del 1% en personas menores de 24 años; 6% en personas entre 25 y 44 años de edad; 15% en personas entre 45 y 64 años de edad y mayor al 50% en personas mayores de 65 años de edad. (WHO Update 49, http://www.who.int/csr/sarsarchive/2003_05_07a/en/). El agente etiológico del SARS es un coronavirus que fue identificado en Marzo del 2003. El cúmulo inicial de casos en el hotel y condominios de Hong Kong demuestran que la transmisión del virus del SARS es extremadamente eficiente. Se han reportado tasas de ataque hasta del 50%. El virus es predominantemente diseminado por medio de gotitas o por contacto directo o indirecto. También es vertido en heces y orina. El personal de la salud, doctores, enfermeras y los trabajadores de hospitales, son comúnmente infectados. En ausencia de medicamentos efectivos o vacunas contra el SARS, el control de la enfermedad está dado por la identificación precoz de los casos y su manejo apropiado, incluyendo el aislamiento del caso sospechoso y probable, así como el manejo de los contactos cercanos. En la gran mayoría de los países, estas medidas han prevenido la diseminación de los casos importados. Hasta ahora el régimen de tratamiento más eficaz para SARS, si es que existe, es desconocido. Para pacientes con deterioro progresivo, el tratamiento intensivo y de soporte es primordial. El tratamiento inmunomodulador con esteroides puede ser importante. Página 6 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Capítulo 2. Cronología Traducción por: Dra. Alexandra Haddad Angulo. 16 de noviembre 2002 Los casos iniciales de SARS aparecen al sur de China, en la Provincia de Guandong. 14 de febrero 2003 Un desplegado pequeño en los registros mensuales epidemiológicos (WER) reporta 305 casos y 5 muertes por un síndrome agudo respiratorio desconocido que ocurrió entre el 15 de noviembre de 2002 y el 9 de febrero de 2003 en la Provincia de Guandong, en China (WER 7/2003). La enfermedad se disemina en miembros del hogar y en el personal de la salud. Dos semanas después, a finales de febrero, el Ministerio de Salud de China reporta que el agente infeccioso causante del brote de neumonía atípica era probablemente Chlamydia pneumoniae. (WER 9/2003) 26 de febrero Por parte de Hong Kong y Vietnam, surgen reportes nuevos acerca de brotes de una forma severa de neumonía. El brote de Vietnam se remonta a un hombre de mediana edad que fue admitido en un hospital en Hanoi, con fiebre elevada, tos seca, mialgias y dolor faríngeo moderado. Posterior a su admisión, aproximadamente 20 miembros del personal de salud enfermaron con sintomatología similar. En algunos casos, este cuadro fue seguido por neumonía bilateral y progresión a síndrome de insuficiencia respiratoria progresiva aguda (SIRPA). 10 de marzo Dieciocho trabajadores de la salud, durante una guardia, en el Hospital Príncipe de Gales en Hong Kong, anuncian que están enfermos. En unas cuantas horas, se identifica que más de 50 miembros del personal de salud han tenido una enfermedad febril en los día previos. El 11 de marzo, veintitrés de ellos son admitidos al hospital, en observación, como medida de precaución. Ocho de ellos desarrollan signos radiológicos de neumonía. (Lee et al.) Los brotes, ambos en Hanoi y Hong Kong, parecen estar confinados al ambiente hospitalario. El personal de los hospitales pareciera estar expuesto a mayor riesgo. El nuevo síndrome es ahora llamado “Síndrome Agudo Respiratorio y Grave” o SARS. 12 de marzo La OMS emite una alerta global y tres días después realza la alerta de salud mundial sobre la misteriosa neumonía después de que en Singapur y Canadá también se identifican casos. La alerta incluye una extraña recomendación de urgencia para los viajeros internacionales, personal de la salud y autoridades sanitarias en la que se sugiere a todas las personas que viajen a áreas afectadas estar pendientes del desarrollo de sintomatología en un periodo de 10 días posteriores al regreso del viaje. (http://www.who.int/csr/sarsarchive/2003_03_15/en/). 17 de marzo La OMS convoca a 11 laboratorios líderes en nueve países a formar parte de la red multicéntrica de investigación en la etiología de SARS y desarrollo simultáneo de un examen diagnóstico. La red toma ventaja de la moderna tecnología de comunicación Página 7 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com (correo electrónico, páginas de Internet) para que los avances sobre las investigaciones en muestras clínicas de casos de SARS puedan ser compartidos en tiempo real (http://www.who.int/csr/sars/project/en/). En la página de la OMS, la red de miembros comparten fotomicrografías electrónicas de virus, secuencias de material genético para identificación y caracterización de virus, aislados virales, muestras variadas de pacientes y tejidos postmortem. Las muestras de un paciente pueden ser analizadas paralelamente por distintos laboratorios y los resultados compartidos en tiempo real. La meta: detección del agente causal del SARS y el desarrollo de una prueba diagnóstica. 19 de marzo Una semana después de la alerta global, la OMS publica una actualización de la situación, diciendo que las fallas de todo esfuerzo previo para detectar la presencia de bacterias y virus conocidos como causantes de enfermedades respiratorias, sugieren fuertemente que el agente causal pudiera ser un patógeno nuevo. 21 de marzo El centro para la prevención y el control de enfermedades, CDC por sus siglas en inglés, publica una descripción clínica preliminar del SARS (http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5212a5.htm). 24 de marzo Científicos del CDC y en Hong Kong anuncian que un nuevo coronavirus ha sido aislado de pacientes con SARS. (http://www.cdc.gov/od/oc/media/pressrel/r030324.htm). En unos cuantos días la secuencia del gen de polimerasa de coronavirus es comparado con aquellas cepas previamente caracterizadas y los científicos son capaces de demostrar que este virus es distinto a todos los patógenos humanos conocidos. Adicionalmente, el suero de los pacientes con SARS, es evaluado para detectar anticuerpos contra el nuevo coronavirus y la seroconversión es documentada en varios pacientes tanto en la fase aguda como de convalecencia. 26 de marzo La primera “mesa redonda” mundial sobre los aspectos clínicos y de tratamiento del SARS es llevada a cabo por la OMS. La reunión electrónica junta a 80 clínicos de trece países; un resumen sobre las discusiones y conclusiones está disponible en la página de SARS de la OMS, http://www.who.int/csr/sars/cliniciansconference/en/. Hasta ahora, un total de 1323 casos sospechosos, de los cuales 49 han fallecido, han sido reportados por ocho países. La transmisión local de SARS ha sido confirmada en Canadá, Hong Kong, Singapur, Taiwán y Vietnam. 28 de marzo El CDC reporta en su investigación a un grupo de 12 personas consideradas caso sospechoso/probable de SARS en Hong Kong que pueden ser rastreadas hacia atrás a un médico del sur de China que llegó el 21 de febrero 2003 y se hospedó en un hotel local (http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5212a1.htm) 30 de marzo El departamento de salud de Hong Kong emite una orden de aislamiento para prevenir la posterior diseminación del SARS. La orden de aislamiento pide que los residentes del edificio E de los Amoy Gardens permanezcan en su departamentos hasta la media Página 8 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com noche del 9 de abril (OMS, Update 15). Los residentes del edificio son posteriormente trasladados a campos rurales de aislamiento por 10 días. 31 de marzo La revista, New England Journal of Medicine, publica en Internet, dos artículos sobre los grupos de pacientes en Hong Kong y Toronto (Tsang, Poutanen). 2 de abril La OMS recomienda que las personas que planean viajar a Hong Kong y a la Provincia de Guangdong en China, consideren posponerlo a menos que sea esencial el viaje. (http://www.who.int/csr/sarsarchive/2003_04_02/en/). El reporte epidemiológico semanal de la OMS, publica una nueva definición de caso, recomienda medidas para prevenir la diseminación internacional del SARS y propone la implementación de un sistema de vigilancia global (ver: http://www.who.int/wer/pdf/2003/wer7814.pdf , que incluye una copia de la forma de reporte de caso). Esta sugerencia actualizada sobre viajes es el resultado de los nuevos acontecimientos, particularmente en Hong Kong, donde un aumento abrupto en los casos de SARS es detectado en una gran propiedad de 35 pisos, hogar de alrededor de quince mil personas. La OMS recomienda que los aeropuertos y las autoridades sanitarias de las áreas afectadas hagan investigaciones en pasajeros a viajes internacionales. Adicionalmente, la OMS está emitiendo guías para el manejo de posibles casos en vuelos internacionales, desinfección de aeronaves que lleven casos sospechosos y vigilancia de pacientes que han estado en contacto con casos sospechosos mientras realizan viajes internacionales. Aunque estas guías están principalmente dirigidas a viajes aéreos, los mismos procedimientos son recomendados para viajes terrestres y marítimos desde áreas afectadas. 8 a 10 de abril Tres grupos de investigación publican resultados que sugieren que un nuevo coronavirus es el agente etiológico del SARS (Peiris, Drosten, Ksiazek). Utilizando pruebas serológicas y la reacción en cadena de la polimerasa para transcriptasa reversa (RT-PCR) específica para el nuevo virus, un grupo de investigadores encontraron que 45 de 50 pacientes con SARS y ninguno de los controles, tenían evidencia de infección por el virus (Peiris). La examinación de cultivos por medio de microscopía electrónica revela los aspectos ultraestructurales característicos de los coronavirus. Con primers de RT-PCR específicos, varias secuencias de nucleótidos idénticos, son identificados en doce pacientes de distintos lugares; un hallazgo que es consistente con el punto de inicio de la epidemia (Ksiazek). En esputo, son encontradas grandes concentraciones de RNA viral de hasta cien millones de moléculas por mililitro (Drosten). 12 de abril Científicos canadienses anuncian la primera secuencia exitosa del genoma del coronavirus probablemente responsable de la epidemia global del SARS. Los científicos del CDC confirman estos reportes. La nueva secuencia tiene 29,727 nucleótidos, la cual concuerda bien con los límites de RNA de los coronavirus conocidos. Los resultados aparecen solo diez días después de que un grupo de diez científicos, apoyados por numerosos técnicos, empezaron a trabajar día y noche para hacer crecer cultivos celulares a partir de cultivos faríngeos, tomados de uno de los pacientes con SARS, en células Vero (células renales de mono verde africano) con el fin de reproducir el ácido ribonucléico (ARN) del coronavirus causante de la Página 9 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com enfermedad. (ver el desplegado http://www.cdc.gov/od/oc/media/pressrel/r030414.htm) de prensa 16 de abril La OMS anuncia que un nuevo patógeno, miembro de la familia de coronavirus, nunca antes visto en humanos, es la causa del SARS. Para probar la relación causal entre el virus y el SARS, los científicos tenían que cumplir con los postulados de Koch, los cuales estipulan que un patógeno debe cumplir con cuatro condiciones: debe ser encontrado en todos los casos de la enfermedad, debe ser aislado del huésped y crecer en cultivos puros, debe reproducir la enfermedad original al ser introducido a un huésped susceptible y debe ser encontrado en el huésped experimental, e cual fue también infectado (http://www.who.int/csr/sarsarchive/2003_04_16/en/). Para confirmar que el nuevo virus era efectivamente el causante de la enfermedad, los científicos de la Universidad de Erasmo de Rótterdam, en Holanda, infectaron monos con el patógeno. Encontraron que el virus causa síntomas similares – tos, fiebre, dificultad respiratoriaen los monos, como los causados en humanos con SARS, por lo tanto, esto provee fuerte evidencia científica que el patógeno es sin duda el agente causal. La gran velocidad con la cual se identificó al agente causal del SARS, a tan solo un mes desde que la OMS se percatara de la nueva enfermedad, fue posible gracias a la colaboración sin precedentes de trece laboratorios en diez países. 20 de abril El gobierno de China revela que el número de casos de SARS es mucho mayor que lo previamente reportado. Beijing tiene ahora 339 casos confirmados de SARS y 402 casos sospechosos. Diez días antes, el Ministro de Salud Zhang Wenkang admitía la existencia de únicamente 22 casos confirmados de SARS en Beijing. La ciudad cierra escuelas e impone estrictas medidas de cuarentena. Lo más preocupante es la evidencia de que el virus se está diseminando en el interior de China, donde los recursos médicos pudieran ser inadecuados. 23 de abril La OMS extiende sus recomendaciones de viaje relacionadas con el SARS a Beijing y a la Provincia Shanxi en China y a Toronto, en Canadá, aconsejando que todas las personas que planean viajar a estos destinos, lo pospongan a menos que sea estrictamente necesario. http://www.who.int/csr/sarsarchive/2003_04_23/en/ 27 de abril Aproximadamente tres mil caso de SARS han sido identificados en China. China cierra teatros, cafés Internet, discotecas y otros centros recreativos y suspende la aprobación de matrimonios como un esfuerzo para prevenir reuniones donde pueda diseminarse el SARS. Siete mil trabajadores de la construcción, trabajan día y noche para terminar un hospital con mil camas para pacientes con SARS en Beijing. El gobierno de Taiwán impone diez días de cuarentena para toda la gente proveniente de China, Hong Kong, Singapur, Vietnam y la ciudad canadiense de Toronto. 29 de abril El primer reporte de SARS en niños, publicado por la revista The Lancet (Hon), sugiere que los niños desarrollan una forma leve de la enfermedad con un curso clínico menos agresivo que aquél visto en adolescentes y adultos. Página 10 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com 30 de abril En Beijing, circulan los rumores sobre que las autoridades chinas pudieran estar listas para imponer medidas autoritarias para el control del SARS. El alcalde aún niega que Beijing, con una población de trece millones de habitantes, pronto será cerrada hacia el resto del mundo. Hong Kong reporta que un pequeño número de gente (menos de 10 de los más de 700, de acuerdo con un vocero de una autoridad hospitalaria) que previamente había sido diagnosticada como recuperada del SARS han enfermado nuevamente. En algunos casos, la enfermedad reinició a más de dos semanas de haber sido dados de alta. 1 de mayo El líder el grupo clínico de la OMS, Mark Salter, dice que la tasa de mortalidad está en 6%, pero pudiera alcanzar el 10%. 2 de mayo El hospital Xiaotangshan abre sus puertas para 156 pacientes de SARS a 15 hospitales de las áreas urbanas de Beijing. Este hospital fue construido por siete mil constructores en ocho días. Taiwán, que tiene una epidemia que evoluciona rápidamente, hoy tiene un total de 100 casos probables, con 11 casos nuevos comparado con el día de ayer. Ocho defunciones por SARS han ocurrido en Taiwán. 4 de mayo Los científicos del grupo de laboratorios colaboradores de la OMS reportan que el virus del SARS puede sobrevivir después secarse en superficies plásticas, por 48 horas; que puede sobrevivir en las heces por 2 días y en la orina por lo menos 24 horas; y que el virus puede sobrevivir por 4 días en las heces tomadas de pacientes que sufren de diarrea (WHO Update 47). 7 de mayo La OMS revisa los estimados iniciales de la tasa de letalidad de SARS. Ahora estima que la tasa de letalidad de SARS varía desde el 0% al 50% dependiendo del grupo de edad afectado, con un estimado total del 14% al 15%. Basado en evidencia nueva, la tasa de letalidad se estima en menos del 1% en personas menores a 24 años, 6% en personas de 25 a 44 años de edad, 15% en personas de 45 a 64 años y mayor al 50% en personas mayores a 65 años (Donnelly, WHO Update 49). Página 11 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Referencias 1. CDC. Update: Outbreak of Severe Acute Respiratory Syndrome - Worldwide, 2003. MMWR 2003;52:241-248. http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5212a1.htm 2. Chan-Yeung M, Yu WC. Outbreak of severe acute respiratory syndrome in Hong Kong Special Administrative Region: case report. BMJ 2003; 326: 850-2. http://bmj.com/cgi/content/full/326/7394/850 3. Donnelly CA, Ghani AC, Leung GM, et al. Epidemiological determinants of spread of causal agent of severe acute respiratory syndrome in Hong Kong. Lancet 2003; 361. Publicado en línea May 7, 2003. http://image.thelancet.com/extras/03art4453web.pdf 4. Drazen JM. Case Clusters of the Severe Acute Respiratory Syndrome. N Engl J Med 2003. http://content.nejm.org/cgi/reprint/NEJMe030062v2.pdf 5. Drosten C, Gunther S, Preiser W, Van Der Werf S, et al. Identification of a Novel Coronavirus in Patients with Severe Acute Respiratory Syndrome. N Engl J Med 2003. http://SARSReference.com/lit.php?id=12690091 6. Gerberding JL. Faster. but Fast Enough? Responding to the Epidemic of Severe Acute Respiratory Syndrome. N Engl J Med 2003. http://content.nejm.org/cgi/reprint/NEJMe030067v1.pdf 7. Hon KLE, Leung CW, Cheng WTF, et al. Clinical presentations and outcome of severe acute respiratory syndrome in children. Lancet, Publicado en línea el 29 de abril, 2003. http://image.thelancet.com/extras/03let4127web.pdf 8. Ksiazek TG, Erdman D, Goldsmith CS, Zaki SR, et al. A Novel Coronavirus Associated with Severe Acute Respiratory Syndrome. N Engl J Med 2003. http://SARSReference.com/lit.php?id=12690092 9. Lee N, Hui D, Wu A, Chan P, et al. A Major Outbreak of Severe Acute Respiratory Syndrome in Hong Kong. N Engl J Med 2003. http://SARSReference.com/lit.php?id=12682352 10. Peiris J, Lai S, Poon L, Guan Y, et al. Coronavirus as a possible cause of severe acute respiratory syndrome. Lancet 2003; 361: 1319-1325. http://SARSReference.com/lit.php?id=12711465 11. Poutanen SM, Low DE, Henry B, Finkelstein S, et al. Identification of Severe Acute Respiratory Syndrome in Canada. N Engl J Med 2003. http://SARSReference.com/lit.php?id=12671061 12. Tsang KW, Ho PL, Ooi GC, Yee WK, et al. A Cluster of Cases of Severe Acute Respiratory Syndrome in Hong Kong. N Engl J Med 2003. http://content.nejm.org/cgi/reprint/NEJMoa030666v3.pdf 13. WHO, WER 7/2003. Acute respiratory syndrome, China. Weekly Epidemiological Record 2003; 78: 41. http://www.who.int/csr/don/2003_03_12/en/ Página 12 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com 14. WHO, WER 9/2003. Acute respiratory syndrome, China – Update. Weekly Epidemiological Record 2003; 78: 57. http://www.who.int/csr/don/2003_03_12/en/ 15. WHO, WER 11/2003. Acute respiratory syndrome – China, Hong Kong Special Administrative Region of China, and VietNam. Weekly Epidemiological Record 2003; 78: 73-74. http://www.who.int/wer/pdf/2003/wer7811.pdf 16. WHO, WER 15/2003. WHO Multicentre Collaborative Networks for Severe Acute Respiratory Syndrome (SARS) diagnosis. Weekly Epidemiological Record 2003; 78: 121-122. http://www.who.int/wer/pdf/2003/wer7815.pdf 17. WHO Update 15: Situation in Hong Kong, activities of WHO team in China. March 31. http://www.who.int/csr/sarsarchive/2003_03_31/en/ 18. WHO Update 47: Studies of SARS virus survival, situation in China. May 5. http://www.who.int/csr/sarsarchive/2003_05_05/en/ 19. WHO Update 49: SARS case fatality ratio, incubation period. May 7. http://www.who.int/csr/sarsarchive/2003_05_07a/en/ Página 13 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Capítulo 3: Virología Wolfgang Preiser, Christian Drosten Traducción por: QC. Klintsy J. Torres Hernández La búsqueda del agente causal del SARS La epidemia de la neumonía atípica severa, la cual fue observada en la provincia China de Guandong y reportada internacionalmente el 11 de febrero de 2003, inicialmente se sospechó que estaba ligada a un nuevo virus de la influenza; para el 19 de febrero de 2003, algunos investigadores aislaron un virus de la influenza aviaria A (H5N1) de un niño en Hong Kong. Este virus fue similar al virus de la influenza originada en aves que causó la epidemia en humanos en Hong Kong en 1997 y se esperó una nueva epidemia de cepas semejantes. Sin embargo, la “gripe de aves” posiblemente ocurrió por una contaminación y pronto fue descartada como la causa del recientemente denominado Síndrome Respiratorio Agudo Grave o SARS (siglas en inglés). Las investigaciones fueron enfocadas a miembros de la familia Paramyxoviridae, después de que se encontraron partículas semejantes a los paramixovirus por microscopía electrónica en muestras respiratorias de pacientes en Hong Kong y Frankfurt am Main. Posteriores investigaciones mostraron que un metaneumovirus humano (hMPV; van den Hoogen) estaba presente en un sustancial número de muestras, aunque no en todos los pacientes con SARS reportados a la fecha. Posteriores pruebas no confirmaron estos hallazgos. Al mismo tiempo, China reportó la detección por microscopía electrónica de organismos semejantes a Chlamydia en pacientes que murieron por neumonía atípica durante la epidemia de Guandong. Nuevamente, los hallazgos no pudieron ser confirmados por otros laboratorios en pacientes con SARS, fuera de China, aunque se encontró una infección concurrente de Chlamydia pneumoniae en el paciente índice en Frankfurt am Main (Drosten). El 17 de Marzo de 2003, la Organización Mundial de la Salud (WHO) hizo un llamado a 11 laboratorios de nueve países para realizar una red para investigación multicéntrica sobre la etiología del SARS y simultáneamente desarrollar una prueba diagnóstica (http://www.who.int/csr/sars/project/en/). Los institutos miembros se comunicaban mediante regulares conferencias telefónicas (inicialmente diariamente) y mediante un sitio Web seguro e intercambio de datos, muestras y reactivos para facilitar y agilizar la investigación sobre la etiología del SARS. Descubrimiento del SARS Co-V El agente etiológico del síndrome respiratorio agudo grave (SARS) es un coronavirus identificado durante la tercera semana de Marzo del 2003, cuando los laboratorios de Hong Kong, Alemania y Estados Unidos encontraron evidencia de un nuevo coronavirus en pacientes con SARS. La evidencia incluía el aislamiento en cultivo celular, demostración por microscopía electrónica, demostración de secuencias genómicas específicas por reacción en cadena de la polimerasa (PCR) y por tecnología de microarreglos, así como pruebas de anticuerpos por inmunofluorescencia indirecta (Ksiazek, Drosten, Peiris). Página 14 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com El descubrimiento del nuevo agente infeccioso fue hecho en menos de dos semanas después que la red de laboratorios de la OMS mencionó su existencia. Tres semanas después, el 16 de abril de 2003, siguiendo una reunión de laboratorios colaboradores en Ginebra, la OMS anunció oficialmente que este nuevo Coronavirus, nunca antes visto en humanos o animales, es la causa del SARS. Este anuncio se realizó después de la investigación realizada por los 13 laboratorios participantes de 10 países, habían demostrado que el nuevo Coronavirus reunió los cuatro postulados de Koch, necesarios para demostrar la causa de la enfermedad: el patógeno debe ser encontrado en todos los casos de la enfermedad, debe ser aislado en cultivo puro, debe reproducir la enfermedad original cuando es introducido en un huésped susceptible y debe ser encontrado en el huésped experimental infectado. El nuevo virus fue denominado provisionalmente como Coronavirus asociado al SARS (SARS-CoV). Pronto, la secuencia completa del genoma del nuevo Coronavirus (Marra, Rota) fue publicada por un laboratorio canadiense y la CDC. Los datos de la secuencia del genoma de varias cepas de SARS-CoV reveló que el nuevo agente infeccioso no pertenece a ninguno de los grupos de Coronavirus conocidos, incluyendo dos Coronavirus humanos HCoV-OC43 y HCoV-229E (Drosten, Peiris, Marra, Rota), los cuales están moderadamente relacionados. Se ha propuesto que el nuevo virus determina una cuarta familia (grupo 4) (Marra). El análisis de la secuencia del SARSCoV es consistente con la hipótesis de que un virus de animales, cuyo huésped normal permanece aún desconocido, desarrolló la capacidad de infectar humano o ha sido capaz de atravesar la barrera de las especies (Ludwig). Morfología Las tinciones negativas por microscopía electrónica de transmisión de muestras de pacientes y de sobrenadantes de cultivo, reveló partículas semejantes a coronavirus, pleomórficas, con envoltura, de diámetros entre 60 y 130 nm. Muchas, aunque no todas las partículas virales, exhiben la apariencia característica de proyecciones de superficie, otorgándoles su nombre al virus (corona, del latín) (Ksiazek, Peiris). El examen de células infectadas de cortes ultrafinos mediante microscopía electrónica muestra partículas semejantes a coronavirus dentro de vacuolas citoplásmicas unidas a membranas y en la cisterna del retículo endoplásmico rugoso. La acumulación de partículas extracelulares acumuladas en grandes cantidades, se han observado en la superficie de la membrana plasmática (MMWR 2003; 52:241-248). Detección El SARS-CoV ha sido detectado en diferentes muestras, incluyendo extractos de tejido pulmonar y de riñón mediante cultivo de virus o PCR; muestras de lavado bronquioloalveolar por microscopía electrónica y PCR; así como muestras de esputo, frotis de tracto respiratorio superior, aspirado o muestras de lavado para PCR o aislamiento de virus (Ksiazek, Drosten). Altas concentraciones de RNA viral, por arriba de 10 millones de copias por mL se encontraron en muestras de esputo. También se detectó el RNA viral a muy bajas concentraciones en plasma, durante la fase aguda, así como en heces durante la fase de convalecencia, sugiriendo que el virus puede liberarse en heces durante prolongados periodos de tiempo (Drosten). Página 15 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Coronaviridae Los Coronavirus (orden Nidovirales, familia Coronaviridae, género Coronavirus) son miembros de una gran familia de virus RNA de cadena positiva, con envoltura, con capacidad de replicar en el citoplasma de células del animal huésped (Siddell). Existen tres grupos de Coronavirus conocidos; los grupos 1 y 2 contienen a virus de mamíferos, mientras que el grupo 3 contiene únicamente a virus de aves. Estos virus se han asociados a una variedad de enfermedades humanas y en animales domésticos, incluyendo gastroenteritis y enfermedades del tracto respiratorios superior y bajo. Mientras los Coronavirus en animales pueden causar enfermedades graves en animales (ejemplo, virus de la gastroenteritis transmisible porcina, virus de la hepatitis murina, virus de la peritonitis infecciosa felina, virus de la bronquitis infecciosa aviaria), las cepas humanas se asociaron previamente a enfermedades leves. Los Coronavirus humanos (HCoVs) se encontraron en el grupo 1 (HCoV-229E) y el grupo 2 (HCoV-OC43) y son la principal causa de enfermedad respiratoria leve (Makela). Ocasionalmente pueden causar enfermedad grave del tracto respiratorio bajo en niños y adultos, así como enterocolitis necrotizante en recién nacidos (McIntosh, ElSahly, Folz, Sizun). Los Coronavirus humanos conocidos son capaces de sobrevivir en superficies ambientales por más de 3 hrs. (Sizun). Los Coronavirus pueden ser transmitidos de persona a persona por gotitas de agua, contaminación de las manos, fomites (objetos inanimados que sirven como transporte de los virus) y aerosoles (Ljaz). Se ha visto al SARS-CoV como el primer Coronavirus que ocasiona enfermedad grave en los humanos. Estabilidad y resistencia El trabajo que se lleva a cabo para evaluar la estabilidad del SARS-CoV y su resistencia a factores ambientales y desinfectantes, es realizado por la red multicéntrica de colaboradores para diagnóstico de SARS de la OMS (ver resultados preliminares en la página de internet: http://www.who.int/csr/sars/survival_2003_05_04/en/index.html ). Se ha observado que es estable en heces y orina a temperatura ambiente por al menos 1 a 2 días. Se ha observado mayor estabilidad en heces de pacientes con diarrea (con pH más alto que en heces normales). En los sobrenadantes de cultivos con células infectadas, existe únicamente una mínima reducción en la concentración de virus después de 21 días a 4 °C y -80 °C. Después de 48 hrs. a temperatura ambiente, la concentración de virus se reduce únicamente un logaritmo, indicando que este virus es más estable a estas condiciones que los otros Coronavirus humanos conocidos. Sin embargo, el calentamiento a 56 °C inactiva rápidamente al SARS-CoV. Además, el agente pierde su capacidad infectiva después de la exposición a diferentes desinfectantes de uso común y reactivos fijadores. Agentes antivirales y vacunas Se han realizados esfuerzos en varias instituciones para ensayar el potencial efecto de agentes anti-SARS-CoV in vitro. La Ribavirina, un agente de “amplio espectro” que es activo contra varios virus RNA (Tam) también ha sido usado clínicamente en pacientes con SARS, sin embargo, no se ha observado eficacia in vitro. Asimismo, se llevan a cabo los esfuerzos para el desarrollo de una vacuna que ofrezca protección para prevenir la infección y/o enfermedad ocasionada pos el SARS-CoV. Aunque una Página 16 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com vacuna efectiva disponible no es esperada dentro de uno o dos años, ciertos rasgos alientan su fabricación: la relativa facilidad con que se propaga in vitro, así como la disponibilidad de vacunas contra Coronavirus de animales como virus de la bronquitis infecciosa aviaria, coronavirus de gastroenteritis transmisible en cerdos y virus de la peritonitis infecciosa felina. Perspectiva El descubrimiento del Coronavirus asociado al SARS fue el resultado del ejercicio de colaboración global sin precedentes, coordinado por la Organización Mundial de la Salud. El rápido éxito de esta enfoque a resultados de un esfuerzo de colaboración – más que un enfoque competitivo – por investigadores de alto nivel haciendo uso de técnicas disponibles desde cultivo celular y microscopía electrónica (Hazelton and Gelderblom), hasta técnicas moleculares, en disposición para tratar de identificar el nuevo agente. Esto demuestra como un esfuerzo extraordinariamente bien organizado puede ser capaz de dirigir o controlar la amenaza enfermedades infecciosas emergentes en el siglo XXI. El control de la epidemia del SARS requerirá el desarrollo de pruebas de laboratorio confiables, para establecer diagnósticos y monitorear la propagación del virus, así como el desarrollo de vacunas y componentes antivirales para prevenir y tratar esta enfermedad. Las vacunas son exitosas en la prevención de infecciones por Coronavirus en animales; así, el desarrollo de una vacuna efectiva contra este nuevo Coronavirus es una posibilidad realista. Sin embargo, la vacunación contra Coronavirus de enfermedades en animales no ha sido uniformemente exitosa. Como en el caso del desarrollo de cualquier vacuna, es necesario el tiempo. Los modelos animales adecuado deberán demostrar eficacia, y es necesario tiempo para demostrar la seguridad de las nuevas vacunas en humanos. Con la capacidad de los diferentes métodos de laboratorio, han surgido un alto número de importantes preguntas con respecto a la historia natural del SARS-CoV, y actualmente se conducen para responder con urgencia: ¿En que momento del curso de la enfermedad el virus se libera con facilidad? ¿Cuál es la concentración de virus en los diferentes compartimentos corporales? ¿Correlaciona la carga viral con la gravedad de la enfermedad o capacidad de transmisión? ¿Existen portadores sanos? ¿Si es así, existen grandes cantidades de virus en heces, suficientes para propagar la infección? ¿Existe excreción de virus durante la recuperación clínica? Si es así, ¿durante cuánto tiempo? ¿Es epidemiológicamente relevante? ¿Porqué los niños son menos propensos a desarrollar SARS? ¿Tienen un bajo índice de manifestaciones clínicas o poseen una relativa inmunidad contra SARS-CoV? ¿Cuál es la función de potenciales cofactores como Chlamydia spp, y metaneumovirus humano (hMPV)? ¿Están relacionados clínicamente a presentaciones graves de la enfermedad o a una alta propagación? ¿Cuál es el origen del SARS-CoV? ¿Qué animal sirve de reservorio, si es que existe? ¿Presenta transmisión entre especies y con el humano? Página 17 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com ¿Existen fuentes ambientales de transmisión de SARS-CoV, como alimentos, agua, desechos? ¿Qué tan estable es el SARS-CoV bajo diferentes condiciones? ¿Puede llevarse a cabo una desinfección eficiente? ¿Cuánto tiempo puede sobrevivir el virus en el ambiente, en superficies secas, en suspensión, incluyendo heces fecales? ¿Qué tan importante es la diversidad genética de las cepas de SARS-CoV? Figure 1. Micrografía electrónica de partículas semejantes a Coronavirus en cultivo celular; sobrenadantes de cultivos, posterior ultracentrifugación y tinción negativa con acetato de uranilo. (Fuente: Department of Virology, Bernhard Nocht Institute for Tropical Medicine; Director: H. Schmitz) Figura completas en: http://SARSReference.com/archive/coronavirus_em.jpg) Figura 2:Efecto citopático en cultivo células Vero por Coronavirus asociado a SARS 24 horas post-inoculación, para comparación: cultivo de células no infectadas (Fuente: Institute for Medical Virology, Director: H. W. Doerr; Figuras completa en: http://SARSReference.com/archive/cytopathiceffect.jpg; http://SARSReference.com/archive/uninfectedcells.jpg) Página 18 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Figura 3. Árbol filogenético de el Coronavirus asociado al SARS (Fuente: S. Günther, Department of Virology, Bernhard Nocht Institute for Tropical Medicine; Director: H. Schmitz; Figura completa: http://SARSReference.com/archive/phylogenetictree.jpg ) Referencias 1. Arbour N, Day R, Newcombe J, Talbot PJ. Neuroinvasion by human respiratory coronaviruses. J Virol 2000;74:8913-21. http://SARSReference.com/lit.php?id=10982334 2. Drosten C, Gunther S, Preiser W, et al. Identification of a NovelCoronavirus in Patients with Severe Acute Respiratory Syndrome. N Engl J Med [early online release 2003 Apr 10]. Disponible en: http://content.nejm.org/cgi/reprint/NEJMoa030747v2.pdf (accessed 2003 April 29) Página 19 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com 3. El-Sahly HM, Atmar RL, Glezen WP, Greenberg SB. Spectrum of clinical illness in hospitalized patients with "common cold" virus infections. Clin Infect Dis 2000;31:96-100. http://SARSReference.com/lit.php?id=10913403 4. Folz RJ, Elkordy MA. Coronavirus pneumonia following autologous bone marrow transplantation for breast cancer. Chest 1999;115:901-5. http://SARSReference.com/lit.php?id=10084516 5. Hazelton PR, Gelderblom HR. Electron microscopy for rapid diagnosis of infectious agents in emergent situations. Emerg Infect Dis. 2003; 9(3): 294-303. http://SARSReference.com/lit.php?id=12643823 6. Ijaz MK, Brunner AH, Sattar SA, Nair RC, Johnson-Lussenburg CM. Survival characteristics of airborne human Coronavirus 229E. J Gen Virol 1985;66:2743– 8. http://SARSReference.com/lit.php?id=2999318 7. Ksiazek TG, Erdman D, Goldsmith CS, Zaki SR, Peret T, Emery S, et al. A novel coronavirus associated with severe acute respiratory syndrome. N Engl J Med [early online release 2003 Apr 10]. Disponible en: http://content.nejm.org/cgi/reprint/NEJMoa030781v3.pdf (accessed 2003 April 24). 8. Ludwig B, Kraus FB, Allwinn R, Doerr HW, Preiser W. Viral Zoonoses – A Threat under Control? Intervirology 2003; 46: 71- 78. http://SARSReference.com/lit.php?id=12684545 9. Makela MJ, Puhakka T, Ruuskanen O, et al. Viruses and bacteria in the etiology of the common cold. J Clin Microbiol 1998;36:539-42. http://SARSReference.com/lit.php?id=9466772 10. Marra MA, Jones SJM, Astell CR, et al. The Genome Sequence of the SARSAssociated Coronavirus. Science 2003. Publicado en líncea el 1 de mayo 2003. http://www.sciencemag.org/cgi/content/abstract/1085953v1 11. McIntosh K. Coronaviruses. In: Mandell GL, Bennett JE, Dolin R, eds. Mandell, Douglas, and Bennett’s Principles and Practice of Infec-tious Diseases, 5th ed. Philadelphia: Churchill Livingstone, Inc., 2000. 12. Peiris JSM, Lai ST, Poon LLM, Guan Y, Yam LYC, Lim W, et al. Coronavirus as a possible cause of severe acute respiratory syndrome. Lancet [publicado en línea el 8 de abril, 2003]. Disponible en: http://image.thelancet.com/extras/03art3477web.pdf (accessed 2003 April 24). 13. Peiris JSM, Chu CM, Cheng VCC, et al. Prospective study of the clinical progression and viral load of SARS associated coronavirus pneumonia in a community outbreak. Lancet 2003. http://www.who.int/csr/sars/prospectivestudy/en/index.html 14. Rota PA, Oberste MS, Monroe SS, et al. Characterization of a Novel Coronavirus Associated with Severe Acute Respiratory Syndrome. Science 2003. Published online 1 May 2003. http://www.sciencemag.org/cgi/content/abstract/1085952v1 15. Siddell S, Wege H, ter Meulen V. The biology of coronaviruses. J Gen Virol. 1983; 64 (Pt 4): 761-776. Página 20 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com 16. Sizun J, Yu MW, Talbot PJ. Survival of human coronaviruses 229E and OC43 in suspension after drying on surfaces: a possible source of hospital-acquired infections. J Hosp Infect 2000;46:55–60. http://SARSReference.com/lit.php?id=11023724 17. Tam RC, Lau JY, Hong Z. Mechanisms of action of ribavirin in antiviral therapies. Antivir Chem Chemother. 2001; 12(5): 261- 272. http://SARSReference.com/lit.php?id=11900345 18. van den Hoogen BG, de Jong JC, Groen J, Kuiken T, de Groot R, Fouchier RA, Osterhaus AD. A newly discovered human pneumovirus isolated from young children with respiratory tract disease. Nat Med. 2001; 7(6): 719-724. http://SARSReference.com/lit.php?id=11385510 19. World Health Organization (WHO). Acute respiratory syndrome, China – Update. Weekly Epidemiological Record 2003; 78: 57. http://www.who.int/csr/don/2003_03_12/en/ 20. World Health Organization (WHO). Acute respiratory syndrome China, Hong Kong Special Administrative Region of China, and Viet Nam. Weekly Epidemiological Record 2003; 78: 73-74. http://www.who.int/wer/pdf/2003/wer7811.pdf 21. World Health Organization (WHO). WHO Multicentre Collaborative Networks for Severe Acute Respiratory Syndrome (SARS) diagnosis. Weekly Epidemiological Record 2003; 78: 121-122. http://www.who.int/wer/pdf/2003/wer7815.pdf Página 21 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Capítulo 4. Transmisión y Prevención. Traducción por: Dra. Elia Camacho Gutiérrez / Dra. Alexandra Haddad Angulo. El cúmulo inicial de casos en hoteles y condominios en Hong Kong han demostrado la eficiente transmisión del virus del SARS. La rápida diseminación de la enfermedad entre los trabajadores del área de la salud en Hanoi, Vietnam, y en hospitales en Hong Kong confirma la naturaleza altamente contagiosa del virus. El personal médico, doctores, enfermeras y trabajadores de los hospitales son comúnmente infectados. Como lo reportan las tasas de ataque, 50% (CDC, MMWR 2003: 52-226-8), el SARS pudiera llegar a ser la primer crisis de salud global del siglo XXI. Rutas de transmisión Los mecanismos de transmisión del virus no son comprendidos del todo aún. EL hecho de que la mayoría de las infecciones nuevas ocurriera en contactos cercanos de pacientes que no utilizaban medidas de protección respiratorias o de contacto, parece sugerir que el virus se disemina predominantemente a través de gotitas o por contacto directo o indirecto. (CDC, Seto). El virus infeccioso está presente a altas concentraciones en el tracto respiratorio de los pacientes (Drosten). Se han detectado bajas cantidades del RNA viral en las heces de los pacientes durante el periodo tardío de convalecencia (Drosten). Esto recuerda a las características de otros coronavirus (Cho), y por lo tanto las heces son potencialmente otra ruta de transmisión. La diseminación del SARS a través de la vía área no parece ser la principal fuente de transmisión. Sin embargo, es de consternar, la aparente facilidad de transmisión en algunos casos. En particular, el cúmulo de casos inicial que se originó en hotel M (CDC, MMWR 2003:52:241-248) y en el brote en los condominios Amoy Gardens (Región Administrativa Especial del Gobierno de Hong Kong) indican que la posibilidad de transmisión a través de la vía aérea del virus del SARS, aunque probablemente un raro evento, no puede ser descartada. La OMS hasta ahora no ha concluido que cualquier bien, producto o animales provenientes de áreas con brotes de SARS posean una amenaza de salud pública. No hay recomendaciones de restricción en este aspecto. Se encuentra información disponible sobre bienes y animales provenientes de áreas afectadas con SARS (http://www.who.int/csr/sars/goods2003_04_10). Condominios Amoy Gardens Hacia finales de Marzo de 2003, un brote de SARS ocurrió entre los residentes de los condominios Amoy Gardens, en Hong Kong. En menos de tres semanas, ya había un total de 320 casos de SARS. El brote hizo pensar en la posibilidad de una infección de origen ambiental. Los hallazgos preliminares sugieren que el probable caso índice del brote fue un paciente que padecía de insuficiencia renal crónica y que, además de la diseminación de persona a persona y a través del uso de servicios comunitarios, tales como elevadores y escaleras, el virus del SARS pudo haberse diseminado también por medio de los sistemas de drenaje de los edificios (para ver detalles Región Administrativa Especial del Gobierno de Hong Kong). Estos hallazgos fueron corroborados por los resultados de los estudios que indican que el virus del SARS Página 22 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com pudiera no ser matado por todos los detergentes de uso común y que pudiera sobrevivir al menos por 24 horas sobre una superficie plástica, a temperatura ambiente, y por hasta 4 días en evacuaciones diarreicas (WHO). Interesantemente, alrededor del 66% de los pacientes de los condominios Amoy Gardens, presentaron diarrea como sintomatología, comparado con el 2% a 7% de los casos en otros brotes. Factores que influyen en la transmisión Si la transmisión del patógeno viral desencadena las manifestaciones de la enfermedad, ello está determinado por múltiples interacciones, en aún un indefinido número de factores tanto virales como del huésped. Factores virales Hasta la fecha, no existe información si las diferentes cepas del virus del SARS pudieran tener diferentes grados de virulencia. Carga viral Como en otras enfermedades infecciosas, el tamaño del inóculo, esto es, el número de partículas infecciosas que se transmiten de persona a persona, es probablemente de suma importancia. La infectividad pudiera ser variable a través del tiempo, incluso durante la fase sintomática de la enfermedad. Incluso, los hallazgos preliminares de los análisis cuantitativos de RT-PCR secuenciales de los aspirados nasofaríngeos sugieren que la carga viral pudiera tener su pico máximo alrededor del día diez posterior al inicio de los síntomas y luego disminuir a los niveles obtenidos durante la admisión, ya hacia el día 15 (Peiris II). En un estudio, la enfermedad severa fue asociada con la adquisición de la enfermedad por medio de contacto en el hogar. Las personas infectadas de esta manera pudieran tener, una mayor dosis o duración a la exposición viral que las personas expuestas, por ejemplo, a través de contacto social (Peiris). Procedimientos diagnósticos y terapéuticos Los procedimientos diagnósticos y terapéuticos llevados a cabo dentro de los hospitales, tales como la inducción de esputo diagnóstico, broncoscopía, intubación endotraqueal y aspirado bronquial, son procedimientos que generan aerosoles potentes. En estas situaciones, las precauciones estándar no han sido reconocidas como medida efectiva para el control de infecciones (Seto). Al menos un serio brote en un hospital público en Hong Kong, pudo haber estado, dado por el uso de un broncodilatador (albuterol; 0.5 mg a través de un nebulizador con oxígeno a 6 litros por minuto, cuatro veces al día por un total de siete días), causando atomización de las secreciones infectadas (Lee). Por lo tanto, el uso de fármacos nebulizados, debe ser evitado en pacientes con SARS (Dwosh). Página 23 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Factores del huésped Existe evidencia creciente que el SARS tiene un curso clínico menos agresivo en niños comparado con adolescentes y adultos (Hon). Adicionalmente, en un estudio, ocho niños habían estado acudiendo a la escuela al inicio de la enfermedad y no existió evidencia de que hubieran diseminado la infección a sus compañeros de clase. Este hallazgo contrasta con la alta tasa de infección del SARS entre los adultos (Peiris, Lee). Aún falta por demostrar que, un curso clínico menos agresivo está asociado con una menor descarga viral del tracto respiratorio y por lo tanto un menor grado de infectividad. Prevención Respuesta nacional El foco primario de la vigilancia del SARS en países sin o con pocos casos de SARS radica en la identificación temprana y aislamiento de pacientes que tengan sospecha de SARS. En los países con un alto número de casos de SARS, los determinantes epidemiológicos clave de la magnitud y tiempo de la epidemia, incluyen el intervalo de tiempo entre la infección y el inicio de los síntomas, entre el inicio de los síntomas y la admisión al hospital, el grado y duración de la infectividad del agente y la extensión y mezcla entre personas infectantes y susceptibles, lo que da lugar a la transmisión del virus (Donnelly). La introducción temprana de procedimientos para la cuarentena del SARS deben ser considerados por las autoridades de salud. Durante el mes de marzo, las autoridades de salud de Singapur, Hong Kong y Canadá implementaron la cuarentena y medidas de aislamiento para limitar la diseminación del SARS. El 4 de abril del 2003 el SARS fue incluido en la lista de enfermedades que requieren cuarentena en EUA. Un acto presidencial dio al CDC la autoridad legal para implementar la cuarentena y medidas de aislamiento como parte de las medidas de control de enfermedades trasmisibles, si se requerían. Control de infecciones nosocomiales El personal de salud permanece en primera fila en la respuesta global al SARS. Están considerados en el riesgo para contraer SARS cuando hay exposición sin protección. Para proteger al personal y prevenir la diseminación de la enfermedad son esenciales las medidas estrictas para el control de infecciones y la educación pública (ChangYeung). Un estudio sugiere que la infección de SARS por gotas puede ser la vía de transmisión primaria del virus del SARS (Seto) dentro del ambiente hospitalario. En un estudio de casos y controles en cinco hospitales de Hong Kong, con 241 miembros infectados del personal hospitalario y 13 no infectados, con exposición a 11 pacientes índice documentada, se observó que no hubo infección en 69 trabajadores de la salud que reportaron el uso de mascarillas, guantes, batas y lavado de manos. Las mascarillas quirúrgicas y N-95 brindaron la mejor protección al personal de salud expuesto a diferencia de las mascarillas convencionales que no reducen significativamente el riesgo de infección (Seto). Página 24 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Como el SARS puede permanecer viable por varios días (WHO), las medidas de precaución, incluyendo la desinfección rigurosa y los procedimientos de higiene debieran brindar el más alto estándar de protección. Tabla 1 muestra un resumen de las precauciones para infección por gotas. obtener información detallada ver las guías del CDC abajo. Para Tabla 1: Precauciones para infección por gotas (de Chan-Yeung, brote de síndrome respiratorio agudo y grave en Hong Kong Región Especial Administrativa: reporte de caso) Los pacientes deben utilizar mascarillas N-95 cuando se presenten los primeros síntomas y se deben aislar inmediatamente (de preferencia en cuartos con presión negativa). Los trabajadores sanitarios deberán utilizar mascarillas similares junto con gorro, lentes, bata y guantes cuando se encuentren en contacto con estos pacientes. Se debe realizar desinfección diaria y terminal que incluya cuidadoso lavado y desinfección de la cama, barandales, piso y todo el equipo con solución de hipoclorito (1000 ppm). desinfectar diario Para pacientes intubados se debe utilizar un sistema de succión cerrado para evitar la dispersión aérea y diseminación de la enfermedad. La implementación de medidas agresivas de control de infecciones podría ser muy efectiva para prevenir las trasmisiones futuras del SARS. En un hospital se documentó la ausencia de transmisión desde un paciente posterior a implementar las estrictas medidas de control de infecciones que incluían la utilización de mascarillas N95, bata, guantes y lavado de manos antes y después del contacto con los pacientes (Hsu). En la comunidad se recomienda a los médicos utilizar mascarillas N-95 cuando revisen pacientes con síntomas respiratorios (Chan-Yeung). Los practicantes de control de infecciones, los médicos que proporcionan atención a pacientes sospechosos de SARS y personas que pudieron haber tenido contacto con casos sospechosos de SARS deben consultar frecuentemente las guías del CDC para el control de infecciones y manejo de exposición en SARS (SARS Infection Control and Exposure Management): Guía interina actualizada para el control de infecciones domésticas en la comunidad y en el cuidado de la salud para pacientes con sospecha de SARS. Se recomiendan precauciones mientras la epidemiología de la enfermedad incluido su transmisión sea mejor entendida (ver los detalles abajo). Guía interina para el uso de mascarillas para la prevención de la transmisión del SARS Precauciones para el control de infecciones para procedimientos generadores de aerosoles en pacientes con sospecha de SARS Precauciones para procedimientos como tratamientos con medicamentos aerolizados (Ej. Salbutamol), inducción de esputo diagnóstica, bronconscopía, succión de vía aérea e intubación endotraqueal. Guías Interinas de bioseguridad en laboratorios para manejo y procesamiento de especimenes asociados con SARS Página 25 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Unidad de Terapia Intensiva Se publicó por Li et al. un breve resumen de las medidas de control de infecciones en unidades de terapia intensiva (agrupando pacientes graves con SARS en una sola UTI, trasfiriendo los pacientes pre-existentes a centros no contaminados, restringir la UTI a pacientes con SARS, instruir al personal para la utilización de batas, guantes, gorros y mascaras en las áreas designadas antes de entrar a la unidad, asignación de enfermeras supervisoras, revisión para asegurar la correcta utilización de máscaras, uso de lentes y visores durante el contacto directo con el paciente, etc.). Triage La identificación de personas que podrían estar en riesgo de tener SARS desde su llegada a los establecimientos médicos es difícil y requiere cambios en la manera en que las evaluaciones médicas se conducen. Las guías interinas para Triage recomiendan que todos los pacientes ambulatorios sean revisados en busca de fiebre, síntomas respiratorios, viajes recientes y contacto cercano con pacientes sospechosos de SARS. Guía actualizada para el triage y la disposición de pacientes que podrían tener el síndrome respiratorio agudo y grave (SARS) para facilitar el escrutinio en el triage para identificar pacientes que podrían tener SARS de manera ambulatoria. (SARS) CDC: Guía actualizada interina para el control de infecciones en el ámbito comunitario y de atención de salud para pacientes con sospecha de SARS. Revisado: 1o de mayo del 2003 Revisar regularmente para actualizaciones en: http://www.cdc.gov/ncidod/sars/infectioncontrol.htm Para todos los contactos de pacientes con sospecha de SARS es imprescindible cuidadosa higiene de manos con agua y jabón, si las manos no están visiblemente sucias se pueden utilizar soluciones de base alcohol como alternativa para el lavado de manos. Buscar en www.cdc.gov/handhygiene para mayor información de higiene de manos. Para el paciente intrahospitalario: Si un paciente es admitido al hospital por sospecha de SARS se debe notificar de inmediato al personal encargado del control de infecciones. Las medidas de control de infecciones para el paciente internado incluyen: Página 26 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Precauciones estándar (p. Ej. Higiene de manos); junto con las precauciones estándar de rutina el personal sanitario debe utilizar protección ocular para todos los contactos con el paciente. Precauciones de contacto (p. ej. uso de bata y guantes para contacto con el paciente o su entorno) Precauciones respiratorias (p. ej aislamiento en un cuarto con presión negativa relativa al área circundante y el uso de mascarillas N-95 para las personas que entren al cuarto) Si no se pueden implementar completamente estas medidas los pacientes se deberán poner en un cuarto privado y todas las personas que entren deberán utilizar mascarillas N-95. Cuando sea posible se deberá realizar una prueba cualitativa para las mascarillas N-95, se puede obtener información detallada sobre estas pruebas en http://SARSReference.com/link.php?id=4. Cuando el personal de salud no tenga a su disposición mascarillas N-95 se podrán utilizar mascarillas quirúrgicas. Las medidas de precaución estándar, respiratorias y de contacto se deberán implementar en todos los pacientes sospechosos de SARS. Para el paciente extrahospitalario: Se debe interrogar a las personas que acudan en busca de atención médica por infección respiratoria aguda acerca de exposición con personas con SARS o viajes a lugares afectados por SARS. Si se sospecha SARS se debe proveer una mascarilla quirúrgica al paciente que cubra nariz y boca. Si no es posible poner una mascarilla al paciente, el paciente debe ser instruido para cubrirse la boca con un pañuelo desechable cuanto tosa, hable o estornude. Separar al paciente en la sala de espera lo antes posible, preferentemente en cuarto privado con presión negativa relativa al área circundante. Todo el personal de salud debe utilizar mascarillas N-95 mientras se encuentren atendiendo pacientes sospechosos de SARS. El personal de salud debe seguir las precauciones estándar (p. Ej. Higiene de manos), precauciones de contacto (p. Ej. Uso de bata y guantes para el contacto con todos los pacientes o su entorno) y utilizar protección ocular para todo contacto con los pacientes. Para mayor información ver las guías de Triage en http://www.cdc.gov/ncidod/sars/infectioncontrol.htm Página 27 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Para el entorno residencial o casero: Se recomienda el uso de mascarillas quirúrgicas para los pacientes sospechosos de SARS durante el contacto con otras personas en casa. Si el paciente no puede utilizar una mascarilla se recomienda que los miembros de la casa utilicen la mascarilla cuando se encuentren en contacto con el paciente. Los miembros de la casa en contacto con el paciente deben recordad la necesidad de la higiene de manos que incluya lavado con agua y jabón y en los casos en que las manos no se encuentren visiblemente sucias se podrán utilizar como alternativa las soluciones con base alcohol para su frotación. Para mayor información sobre las guías de miembros del hogar visitar el sitio web. Definición de Caso Sospechoso del Síndrome Respiratorio Agudo y Grave (SARS) El personal al cuidado de la salud deberá aplicar las medidas de control de infecciones apropiadas para cualquier contacto con pacientes en los que se sospeche SARS. La definición de caso sospechoso de SARS está sujeta a cambios, particularmente en lo concerniente a la historia de viajes ya que se puede reportar transmisión en nuevas áreas geográficas. La definición de caso más reciente de SARS se puede revisar en la página web del Síndrome Respiratorio Agudo y Grave, SARS Severe Acute Respiratoy Síndrome (SARS) case definition. Control de Infecciones en el Hogar Los trabajadores de la salud deben tener un alto índice de sospecha si ellos o miembros de su familia desarrollan fiebre u otros síntomas sugestivos del síndrome respiratorio agudo y grave. Deberán acudir a un hospital y no tratarse así mismos en casa y poner a su familia en riesgo (Chan-Yeung). Para prevenir transmisión secundaria, los contactos cercanos de pacientes con SARS deberán permanecer pendientes de la presencia de fiebre o síntomas respiratorios. Si los síntomas se presentaran, las personas expuestas deben evitar contacto con otras personas, buscar inmediatamente atención médica y practicar las recomendaciones para el control de infecciones que se sugieren a los pacientes con SARS. Los miembros del hogar y otros contactos cercanos de pacientes con SARS deben ser monitorizados activamente por el personal de salud pertinente. Consultar frecuentemente las guías del CDC “Guía para el control de infecciones y manejo de exposición del SARS”: Guía Interina de Control de Infecciones para pacientes sospechosos de SARS y sus contactos cercanos (ver abajo). Guía Interina para personas que pudieron haber estado expuestas a pacientes sospechosos de SARS Guía Interina para el manejo de exposiciones a SARS en el personal de salud y otras instituciones Página 28 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Contactos de casos probables deben ser aislados hasta que el periodo de incubación haya pasado. Después del contacto con pacientes con síntomas respiratorios, es necesario higiene de manos cuidadosa y lavado de manos con agua y jabón. CDC: Guía Interina de Precauciones para el Control de Infecciones para pacientes con sospecha de síndrome respiratorio agudo y grave (SARS) y sus contactos cercanos. Revisado el 29 de abril 2003 Revisar regularmente para actualizaciones en: http://www.cdc.gov/ncidod/sars/ic-closecontacts.htm Los pacientes con SARS representar un riesgo de transmisión a sus contactos tanto familiares como personal sanitario. El tiempo durante el cuál un paciente con SARS antes y después de presentar los síntomas puede trasmitir la enfermedad es desconocido todavía. Las siguientes medidas de control de infecciones se recomiendan para la convivencia en casa de los pacientes con sospecha de SARS. Estas recomendaciones se basan en la experiencia de los Estados Unidos hasta la fecha y se irán actualizando conforme se genere nueva información al respecto. 1. Los pacientes con SARS deben limitar sus interacciones fuera de su casa, que incluye no ir a trabajar, a la escuela, guarderías o cualquier otra área pública hasta 10 días después de que la fiebre haya remitido y los síntomas respiratorios ausentes o en mejoría. Durante este tiempo las precauciones para el control de infecciones se deben utilizar como se describe a continuación para minimizar el potencial de transmisión. 2. Todos los miembros del hogar de un paciente con SARS deberán seguir cuidadosamente las recomendaciones de higiene de manos (p. Ej. Lavado de manos frecuente o uso de geles con base alcohol), particularmente después de tener contacto con fluidos corporales (p. Ej. secreciones respiratorias, orina o heces). Para mayores detalles sobre la higiene de manos ver la “Guía para la higiene de manos en el ámbito del cuidado de la salud “. 3. utilizar guantes desechables cuando se tenga contacto directo con fluidos corporales de un paciente con SARS. Sin embargo, el uso de guantes no 1. sustituye la higiene de manos. Inmediatamente después de actividades que involucren el contacto directo con fluidos corporales se deben retirar y desechar los guantes y realizar un lavado de manos. Nunca se deben lavar o reusar los guantes. 4. Se le debe informar a cada paciente con SARS la manera para taparse la boca y nariz con un pañuelo facial cuando tosa o estornude. De ser posible deberá utilizar un cubrebocas quirúrgico (o de alta eficiencia) cuando tenga contacto con personas no infectadas para prevenir la diseminación de gotas infectactes. Cuando un paciente con SARS sea incapaz de utilizar el cubrebocas los familiares deberán utilizarla cuando tengan contacto cercano con el paciente. Página 29 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com 5. Se debe evitar compartir utensilios de cocina, toallas y ropa de cama entre pacientes con SARS y otras personas, a menos que se hayan lavado (con jabón y agua caliente). Las superficies contaminadas con fluidos corporales deben limpiarse con cualquier desinfectante casero de acuerdo a las instrucciones del fabricante, se deben utilizar guantes para realizarlo. 6. Los desechos de los familiares incluyendo mascarillas y pañuelos faciales que se hayan ensuciado con fluidos corporales de pacientes con SARS deben desecharse como basura normal. 7. Contactos cercanos o cohabitantes de pacientes con SARS deben ser monitorizados activamente por el departamento de salud local correspondiente. 8. Contactos cercanos o cohabitantes de pacientes con SARS deben estar alerta para detectar el desarrollo de fiebre o síntomas respiratorios y de presentarse deben buscar ayuda médica. Para una evaluación el médico debe estar informado que la persona es un contacto cercano de un paciente con SARS y se deben tomar las medidas necesarias para prevenir la trasmisión. Se deben seguir las precauciones recomendadas para pacientes con SARS para los contactos cercanos o cohabitantes de pacientes con SARS que desarrollan síntomas. 9. En este momento, en la ausencia de fiebre o síntomas respiratorios, las personas que cohabiten o los contactos cercanos de pacientes con SARS no requieren modificar sus actividades fuera de casa. Sitios relacionados: SARS Information for Patients and Their Close Contacts Página 30 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Referencias 1. CDC. Outbreak of Severe Acute Respiratory Syndrome - Worldwide, 2003. MMWR 2003;52:226-8. http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5211a5.htm 2. CDC. Update: Outbreak of Severe Acute Respiratory Syndrome - Worldwide, 2003. MMWR 2003;52:241-248. http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5212a1.htm 3. CDC. Infection Control Precautions for Aerosol-Generating Procedures on Patients who have Suspected Severe Acute Respiratory Syndrome (SARS). 23 de marzo 2003. http://www.cdc.gov/ncidod/sars/aerosolinfectioncontrol.htm (accessed May 3, 2003). 4. Chan-Yeung M, Yu WC. Outbreak of severe acute respiratory syndrome in Hong Kong Special Administrative Region: case report. BMJ 2003; 326: 850-2. http://bmj.com/cgi/content/full/326/7394/850 5. Cho KO, Hoet AE, Loerch SC, Wittum TE, et al. Evaluation of concurrent shedding of bovine coronavirus via the respiratory tract and enteric route in feedlot cattle. Am J Vet Res 2001; 62: 1436-41. http://SARSReference.com/lit.php?id=11560274 6. Donnelly CA, Ghani AC, Leung GM, et al. Epidemiological determinants of spread of causal agent of severe acute respiratory syndrome in Hong Kong. Lancet 2003; 361. Publicado en línea el 7 de mayo, 2003. http://image.thelancet.com/extras/03art4453web.pdf 7. Drosten C, Gunther S, Preiser W, et al. Identification of a Novel Coronavirus in Patients with Severe Acute Respiratory Syndrome. N Engl J Med [publicado en línea el 10 de abril,2003]. Disponible en: http://content.nejm.org/cgi/reprint/NEJMoa030747v2.pdf (accessed 2003 April 29) 8. Dwosh HA, Hong H, Austgarden D, Herman S, Schabas R. Identification and containment of an outbreak of SARS in a community hospital. CMAJ 2003; 168. Publicado en línea el 25 de abril,2003. http://SARSReference.com/link.php?id=2 9. Government of Hong Kong Special Administrative Region, Department of Health. Outbreak of Severe Acute Respiratory Syndrome (SARS) at Amoy Gardens, Kowloon Bay, Hong Kong. Main Findings of the Investigation. http://www.info.gov.hk/info/ap/pdf/amoy_e.pdf (accessed April 30) 10. Hon KLE, Leung CW, Cheng WTF, et al. Clinical presentationsand outcome of severe acute respiratory syndrome in children.Lancet, Pubilicado en líndea el 29 de abril, 2003. http://image.thelancet.com/extras/03let4127web.pdf 11. Hsu L-Y, Lee C-C, Green JA, Ang B, Paton NI, Lee L, et al. Severe acute respiratory syndrome (SARS) in Singapore: clinical features of index patient and initial contacts. Emerg Infect Dis 2003; 9. http://www.cdc.gov/ncidod/EID/vol9no6/03- 0264.htm Página 31 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com 12. Lee N, Hui D, Wu A, Chan P, et al. A Major Outbreak of SevereAcute Respiratory Syndrome in Hong Kong. N Engl J Med2003. http://SARSReference.com/lit.php?id=12682352 13. Li T, Buckley TA, Yap F, Sung J, Joynt GM. Severe acute respiratory syndrome (SARS): infection control. Lancet 2003; 361. http://SARSReference.com/link.php?id=6 14. Peiris JSM, Lai ST, Poon LLM, Guan Y, Yam LYC, Lim W, etal. Coronavirus as a possible cause of severe acute respiratory syndrome. Lancet [publicado en línea el 8 de abril, 2003]. Disponible en: http://image.thelancet.com/extras/03art3477web.pdf (accessed2003 April 24) 15. Peiris JSM, Chu CM, Cheng VCC, et al. Prospective study ofthe clinical progression and viral load of SARS associatedcoronavirus pneumonia in a community outbreak. Lancet 2003. http://www.who.int/csr/sars/prospectivestudy/en/index.html 16. Poutanen SM, Low DE, Henry B, Finkelstein S, et al.Identification of Severe Acute Respiratory Syndrome in Canada.N Engl J Med 2003. http://SARSReference.com/lit.php?id=12671061 17. Seto WH, Tsang D, Yung R, et al. Effectiveness of precautionsagainst droplets and contact in prevention of nosocomialtransmission of severe acute respiratory syndrome (SARS).Lancet 2003; 361: 1519–20. http://SARSReference.com/link.php?id=1 18. WHO. First data on stability and resistance of SARS coronaviruscompiled by members of WHO laboratory network. May 4, 2003. http://SARSReference.com/link.php?id=5. (accessed May 4). Página 32 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Capítulo 5: Epidemiología Traducción por: Dra. Elia Camacho Gutiérrez Hasta el 5 de mayo del 2003 se han diagnosticado más de 6,000 pacientes con Síndrome Respiratorio Agudo y Grave (SARS) en 29 países. Diseminación Local En noviembre del 2002 en la provincia de Guangdong al sur de China se reportaron algunos casos de una neumonía típica, altamente contagiosa y severa. Esta condición ha presentado una particular prevalencia entre personal al cuidado de la salud y sus familiares (algunos casos rápidamente fatales). Durante la primera semana de febrero hubo gran preocupación pública acerca de una misteriosa enfermedad respiratoria la cual aparentemente tenía alta mortalidad y causaba la muerte en horas. Entre los síntomas se incluían tos, fiebre y dificultad respiratoria (Rosling). Oficiales locales de salud reportaron a la OMS 305 casos relacionados con esta enfermedad desconocida con cinco muertes resultantes (WER /2003). Diseminación Global La diseminación global del SARS comenzó en Hong Kong el 21 de febrero del 2003 cuando un doctor de la provincia de Guangdong viajó a Hong Kong a visitar a su familia y se hospedó en el noveno piso de un hotel local (Hotel M). Días antes inició con malestar leve y durante su estancia estuvo gravemente enfermo hasta que fue admitido a un hospital el 22 de febrero muriendo al día siguiente. Hong Kong, febrero 2003 Al tiempo que murió se infectaron 10 personas que se habían hospedado en el mismo hotel (MMWR 2003;52:241-248). Estos individuos fueron responsables a su vez de los principales brotes en los hospitales de Hong Kong, Vietnam, Canadá, Singapur y los condominios Amoy Gardens en Hong Kong. Tan pronto se reconoció la extensión de la epidemia las autoridades sanitarias de Hong Kong implementaron procedimientos encaminados al control de infecciones en todos los hospitales de Hong Kong incluyendo protección respiratoria y de contacto para trabajadores del área de la salud, desinfección diaria de zonas afectadas y seguimiento de pacientes con SARS. Después de la fase inicial de aumento exponencial, la tasa de casos confirmados bajó a menos de 20 por día para el 28 de abril, posterior a la implementación de estos lineamientos (Figura 1). Hasta el 8 de mayo, se habían diagnosticado 1,637 casos probables de SARS en Hong Kong de los cuales han muerto 187. Página 33 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Figura 1. Casos nuevos de SARS en Hong Kong Al final de abril, el número diario de nuevos casos variaban entre 2 y 80 se observó un pico al final de marzo, lo cual es atribuible principalmente a los casos de los condominios Amoy Gardens. El promedio diario de nuevos casos reportado en las primeras 4 semanas de abril fue 39, 44, 30 y 22 respectivamente. Vietnam, febrero 2003 El brote de Vietnam comenzó el 26 de febrero cuando un hombre de negocios asiáticoamericano fue admitido a un hospital en Hanoi con fiebre alta, tos seca, mialgias y leve dolor de garganta. Previo a su llegada Hanoi había visitado Hong Kong donde tres días después de su llegada habían comenzado los primeros síntomas. Durante su visita a Hong Kong estuvo hospedado en el Hotel M, lugar donde estuvo el paciente índice del brote de Hong Kong. Para el 5 de marzo se identificaron los primeros casos probables de SARS secundario entre trabajadores del área de la salud en Hanoi y subsecuentemente 63 personas fueron infectadas. El gobierno de Vietnam implementó un sistema de control nacional que incluía seguimiento diario de los contactos de casos probables de SARS y vigilancia de casos sospechosos en la comunidad. El 28 de abril del 2003 la OMS retiró a Vietnam de la lista de países afectados, siendo el primer país en contener satisfactoriamente el brote, alcanzando 20 días consecutivos (la duración de 2 períodos de incubación) sin presentar casos nuevos. La ausencia de casos nuevos por un período consecutivo de 20 días en un país fue un indicador alentador acerca de que la detección apropiada junto con medidas de protección, siguiendo las recomendaciones de la OMS (WHO, 2003), fueron capaces de contener brotes y prevenir diseminación futura. Vietnam, uno de varios países afectados por diseminación local de SARS, ha implementado las siguientes medidas de detección y protección: identificación temprana de personas con SARS, incluyendo movimientos y contactos aislamiento efectivo de los pacientes con SARS en hospitales Página 34 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com protección apropiada al personal sanitario involucrado en el manejo de estos pacientes identificación y aislamiento de casos sospechosos de SARS escrutinio de viajeros internacionales reporte e intercambio de información oportuna y precisa entre autoridades y/o gobiernos. Toronto, febrero 2003 El SARS fue introducido a Toronto por una mujer de familia procedente de Hong Kong que había viajado a su casa para visitar parientes del 13 al 23 de febrero del 2003. Durante la visita a su hijo en Hong Kong, ella y su esposo se hospedaron en el Hotel M del 18 al 21 de febrero, al mismo tiempo y mismo piso en que el paciente índice del brote internacional estuviese hospedado. La mujer y su esposo sólo permanecían en el hotel de noche, el día lo pasaban visitando a su hijo. Regresaron el 23 de febrero a su departamento en Toronto, el cual compartían con otros 2 hijos, una nuera y un nieto de 5 meses de edad. Dos días después, la mujer desarrolló fiebre, anorexia, mialgias, dolor de garganta y tos leve no productiva. Murió 9 días después posteriores al inicio de los síntomas. Entre el 8 y 9 de marzo, 5 de los 6 miembros adultos de la familia presentaron síntomas de SARS (Poutanen). Hasta el 8 de mayo del 2003, se han diagnosticado 148 casos probables de SARS, la mayoría en Toronto, de los cuales han muerto 22. El 23 de abril, la OMS (update 37) incluyó Toronto entre las zonas para las que se habían de seguir recomendaciones para viajes internacionales, incluyendo que se pospusieran viajes excepto los imprescindibles. Cinco días después, Toronto fue retirado de estas listas con base en los siguientes cambios (WHO, update 42): disminución en la magnitud de casos probables de SARS; período de 20 días consecutivos libre de nuevos casos de transmisión local y la confirmación de ausencia de exportación de nuevos casos. Singapur, febrero 2003 El caso índice de SARS en Singapur fue una mujer de 23 años previamente sana, de origen chino quien estuvo hospedada en el noveno piso del hotel M durante sus vacaciones en Hong Kong del 20 al 25 de febrero del 2003 (Hsu). Desarrolló fiebre, cefalea y posteriormente tos seca el 25 y 28 de febrero respectivamente. Fue admitida a un hospital en Singapur el 1 de marzo. Durante un período de varios días ella infectó por lo menos a otras 20 personas. Posterior a implementar estrictas medidas para el control de infecciones se logró evitar que esta paciente trasmitiera la enfermedad a nuevas personas. Estas medidas incluían uso de máscaras N95, uso de batas y guantes, lavado de manos antes y después del contacto con los pacientes (Hsu). Hasta el 8 de mayo del 2003 se han diagnosticado 204 casos probables de SARS en Singapur de los cuales 26 han muerto. Página 35 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Beijing, 20 de abril 2003 Hasta mediados de abril, las autoridades chinas subestimaron la magnitud de la epidemia en Beijing, con sólo 37 casos reportados hasta el 19 de ese mes. En los siguientes 2 días, China anunció más de 400 casos nuevos de SARS (WHO, update 35). Reportes adicionales (WHO, update 37) indican que se ha diseminado el SARS a algunas provincias más pobres de China, incluyendo Guanxi oeste, Gansu norte y el interior de Mongolia. El 23 de abril, la OMS (WHO update 37) extendió el aviso de viaje relacionado al SARS hacia Beijing y la provincia de Shanxi en China, con la recomendación de posponer viajes a estos destinos excepto casos imprescindibles. Cuatro días después las autoridades Chinas cerraron teatros, los café internet, discotecas y otras actividades recreativas y suspendió la aprobación de matrimonios como un esfuerzo de prevenir reuniones en las que se pudiera diseminar el SARS. Hasta el 8 de mayo del 2003 se han diagnosticado 4,280 casos probables de SARS de los cuales han muerto 206. Taiwán, finales de abril 2003 Los primeros dos casos sospechosos de SARS fueron diagnosticados en una pareja el 14 de marzo del 2003. El hombre tenía el antecedente de un viaje en febrero a la provincia de Guangdong y Hong Kong. El 26 de marzo, un taiwanés, residente de los condominios Amoy Gardens en Hong Kong voló a Taiwán y tomó el tren a Taichung para celebrar un festival tradicional, el Qing Ming. El hermano del hombre fue el primer caso fatal de SARS en Taiwán y su compañero de tren también se infectó. El número de casos comenzó a incrementar las últimas semanas de abril. Personal de 3 hospitales se infectó. El 28 de abril, el gobierno taiwanés impuso una cuarentena obligatoria de 14 días a todos los viajeros provenientes de China, Hong Kong, Singapur, Macao y Toronto. Hasta el 8 de mayo del 2003, se han diagnosticado 116 casos sospechosos de SARS en Taiwán de los cuales 8 murieron. Otros países El número de casos probables de SARS reportados desde el primero de noviembre del 2002 al 5 de mayo del 2003 se muestran en la tabla 1 (actualizaciones disponibles en http://www.who.int/csr/sars/en/). Mapa de los casos probables acumulados reportados de SARS La distribución geográfica de los casos probables reportados de SARS el 5 de mayo del 2003 se encuentra disponible como archivo de referencia de SARS en: http://SARSReference.com/archieve/whomap2003_05_05b.gif Revisar actualizaciones en http://www.who.int/csr/sars/en/. Página 36 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com País No. Cumulativo No. de muertes de casos No. recuperados Alemania 7 0 7 Australia 4 0 4 Brasil 2 0 2 Bulgaria 1 0 0 Canadá 148 22 93 Corea 1 0 0 China 4,280 206 1,433 116 8 25 España 1 0 1 EUA 61 0 26 Filipinas 3 2 1 Francia 5 0 4 1,637 187 930 Indonesia 2 0 1 Inglaterra 6 0 6 Irlanda 1 0 1 Italia 9 0 4 Kuwait 1 0 1 Macao 1 0 0 Malasia 7 2 4 Mongolia 8 0 4 Nueva Zelanda 1 0 1 Polonia 1 0 0 Rumania 1 0 1 Singapur 204 26 149 Sudáfrica 1 1 0 Suecia 3 0 2 Suiza 1 0 1 Tailandia 7 2 5 Vietnam 63 5 58 6,583 461 2,764 China, Taiwán Hong Kong Total Nota: el número acumulado de casos incluye el de muertes. Tabla 1. Número de casos probables de SARS reportados desde el primero de noviembre del 2002 al 5 de mayo del 2003 Página 37 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com SARS en niños El SARS parece presentarse con un curso clínico menos agresivo en niños pequeños en comparación con adultos y adolescentes (Hon) (ver también el capítulo de SARS pediátrico). Hasta el 25 de abril, los niños menores de 15 años representaban sólo el 3% de todos los casos de SARS reportados en Hong Kong. La razón de esta situación es incierta hasta el momento. Edad Hombres Mujeres 0-14 3% 3% 15-24 4% 7% 25-34 10% 16% 35-44 9% 12% 45-54 6% 9% 55-64 4% 4% >65 9% 5% Total 44% 56% *Esta figura es ligeramente diferente a la sumatoria de los siete relevantes grupos etarios (por 1%) debido al redondeo. Perspectivas Hasta el momento en que se escribió este texto (8 de mayo) la mayoría de los países que han reportado casos probables de SARS se encuentran con un número pequeño de casos importados. Cuando se detectan oportunamente estos casos, se aíslan y se manejan de acuerdo a estrictos procedimientos para el control de infecciones, disminuye o desaparece el número de infecciones secundarias tanto al personal sanitario como a sus familias (Chan-Yeung). Los brotes de SARS parecen estar contenidos en Canadá, Singapur, Hong Kong y Vietnam pero no en China. El nuevo brote en Taiwán ha causado preocupación. Hasta el momento muchas preguntas que respectan al SARS permanecen sin respuesta. Aunque las evidencias epidemiológicas indican que el contacto cercano con los casos probables es el principal modo de transmisión se desconoce por qué algunas personas parecieran ser especialmente infectantes en comparación con la mayoría que no lo son. La transmisión aérea parece ser la excepción más que la regla de transmisión del SARS, no obstante podría ser la causa de la transmisión extensa en los edificios y otras áreas confinadas a Asia. Por qué el SARS ha impactado tan fuerte la vida pública en Beijing pero no en Shangai (WHO, update 40). Página 38 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Finalmente, ¿permanecerá el SARS confinado a las áreas donde se encuentra actualmente, o se diseminará alrededor del mundo?, ¿qué pasaría si el virus llega a África?, ¿el patrón de transmisión será diferente si el virus se introduce a poblaciones con alta prevalencia de personas inmunocomprometidas, por ejemplo personas infectadas por VIH? “Una vez más no sabemos. La naturaleza de las epidemias es ser impredecibles”. Bloom Referencias 1. Bloom BR. Lessons from SARS. Science 2003; 300:701. http://www.sciencemag.org/feature/data/sars/pdfs/se01.pdf 2. CDC. Update: Outbreak of Severe Acute Respiratory Syndrome Worldwide, 2003. MMWR 2003;52:241-248. http://www.cdc.gov/mmwr/preview/mmwrhtml/ mm5212a1.htm 3. Chan-Yeung M, Yu WC. Outbreak of severe acute respiratory syndrome in Hong Kong Special Administrative Region: case report. BMJ 2003; 326: 850-2. http://bmj.com/cgi/content/full/326/7394/850 4. Cho KO, Hoet AE, Loerch SC, Wittum TE, et al. Evaluation of concurrent shedding of bovine coronavirus via the respiratory tract and enteric route in feedlot cattle. Am J Vet Res 2001; 62: 1436-41. http://SARSReference.com/lit. php?id=11560274 5. Drosten C, Gunther S, Preiser W, et al. Identification of a Novel Coronavirus in Patients with Severe Acute Respiratory Syndrome. N Engl J Med [publicado en línea el 10 de abril, 2003]. Disponible en: http://content.nejm.org/cgi/reprint/ NEJMoa030747v2.pdf (accessed 2003 April 29) 6. Government of Hong Kong Special Administrative Region, Department of Health. Outbreak of Severe Acute Respiratory Syndrome (SARS) at Amoy Gardens, Kowloon Bay, Hong Kong. Main Findings of the Investigation. http://www.info.gov.hk/info/ap/pdf/amoy_e.pdf (accessed April 30). 7. Government of Hong Kong Special Administrative Region, Department of Health. SARS Bulletin, 29 April 2003 (accessed April 30) http://www.info.gov. hk/dh/diseases/ap/eng/bulletin0429.pdf 8. Health, Welfare & Food Bureau. SARS Bulletin 25 April 2003. (accessed on April 27) http://www.info.gov.hk/dh/diseases/ap/eng/bulletin0425.htm 9. Hon KLE, Leung CW, Cheng WTF, et al. Clinical presentations and outcome of severe acute respiratory syndrome in children. Lancet, Publicado en línea el 29 de abril, 2003. http://image.thelancet.com/extras/03let4127web.pdf 10. Hsu L-Y, Lee C-C, Green JA, Ang B, Paton NI, Lee L, et al. Severe acute respiratory syndrome (SARS) in Singapore: clinical features of index patient and initial contacts. Emerg Infect Dis 2003; 9. Accessed on May 1. http://www.cdc.gov/ ncidod/EID/vol9no6/03-0264.htm Página 39 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com 11. Lee N, Hui D, Wu A, Chan P, et al. A Major Outbreak of Severe Acute Respiratory Syndrome in Hong Kong. N Engl J Med 2003. http://SARSReference.com/lit.php?id=12682352 12. Peiris JSM, Lai ST, Poon LLM, Guan Y, Yam LYC, Lim W, et al. Coronavirus as a possible cause of severe acute respiratory syndrome. Lancet [publicado en líncea el 8 de abril, 2003]. Disponible en: http://image.thelancet.com/extras/03art3477web.pdf (accessed 2003 April 24). 13. Peiris JSM, Chu CM, Cheng VCC, et al. Prospective study of the clinical progression and viral load of SARS associated coronavirus pneumonia in a community outbreak. Lancet 2003. http://www.who.int/csr/sars/prospectivestudy/en/index.html 14. Poutanen SM, Low DE, Henry B, Finkelstein S, et al. Identification of Severe Acute Respiratory Syndrome in Canada. N Engl J Med 2003. http://SARSReference.com/lit.php?id=12671061 15. Rosling L, Rosling M. Pneumonia causes panic in Guangdong province. BMJ 2003:326:416. http://bmj.com/cgi/content/full/326/7386/416 16. WHO, WER 7/2003. Acute respiratory syndrome, China. Weekly Epidemiological Record 2003; 78: 41. http://www.who.int/csr/don/2003_03_12/en/ 17. WHO, WER 18/2003. Viet Nam SARS-free. Weekly Epidemiological Record 2003; 78: 145. http://www.who.int/wer/pdf/2003/wer7818.pdf 18. WHO Update 35: Update on China: New numbers, May Day holiday reduced. April 21. http://www.who.int/csr/sarsarchive/2003_04_21/en/ 19. WHO Update 36: Situation in Singapore http://www.who.int/csr/sarsarchive/2003_04_22/en/ and China. April 21. 20. WHO Update 37: WHO extends its SARS-related travel advice to Beijing and Shanxi Province in China and to Toronto Canada. April 23. http://www.who.int/csr/sarsarchive/2003_04_23/en/ 21. WHO Update 40: Situation in Shanghai, Hong Kong and Vietnam. April 26. http://www.who.int/csr/sarsarchive/2003_04_26/en/ 22. WHO. Viet Nam removed from list of affected countries, more than 5000 probable cases worldwide. April 28. http://www.who.int/csr/sarsarchive/2003_04_28/en/ 23. WHO Update 42: Travel advice for Toronto, situation in China. April 29. http://www.who.int/csr/sarsarchive/2003_04_29/en/ Página 40 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Capítulo 6: DEFINICION DE CASO Traducción por: Dra. Alexandra Haddad Angulo Definición de caso según la OMS Tal y como la Organización Mundial de la Salud (OMS) lo define, dentro de caso sospechoso se clasifica a aquél en el cual la persona presenta fiebre documentada (temperatura > 38 ° C), síntomas de las vías aéreas inferiores y haber estado en contacto con una persona que probablemente haya cursado con SARS o tener antecedente viaje a un área geográfica donde haya sido documentada la transmisión de la enfermedad. Un caso sospechoso con: 1) hallazgos compatibles con neumonía en la radiografía de tórax, 2) síndrome de insuficiencia respiratoria progresiva aguda (SIRPA) o 3) muerte por enfermedad respiratoria inexplicable en la cual la necropsia muestra hallazgos consistentes con SIRPA sin una causa identificable, es considerado un caso probable. La definición de caso de la OMS se encuentra disponible en la página de Internet: http://www.who.int/csr/sars/casedefinition/. Se recomienda que no se reclasifique a una persona dentro de la definición de caso mientras se esperan los resultados de los exámenes de laboratorio o en base a haber obtenido resultados negativos. Ver Uso de métodos de laboratorio para diagnóstico de SARS. Caso sospechoso 1. Aquella persona que presente, posterior al 1º. de noviembre de 2002: • fiebre elevada (> 38°C) • tos o dificultad respiratoria Y Y una o más de las siguientes características de exposición durante los 10 días previos al inicio de los síntomas: • contacto cercano2 con una persona que es considerada como caso sospechoso o probable de SARS; • antecedente de viaje, a un área con transmisión local reciente de SARS Página 41 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com • residencia en un área con transmisión local reciente de SARS. 2. Aquella persona con enfermedad respiratoria aguda inexplicable que resulte en la muerte posterior al 1º. de noviembre del 20021, pero no se le ha realizado necropsia Y • contacto cercano2 con una persona que es considerada como caso sospechoso o probable de SARS • antecedente de viaje, a un área con transmisión local reciente de SARS • residencia en un área con transmisión local reciente de SARS 1 El periodo de vigilancia inicia el 1º de noviembre de 2002 donde fueron identificados casos de neumonía atípica en China, ahora reconocidos como SARS. La transmisión internacional de SARS fue por primera vez reportada en Marzo de 2003, con inicio de los casos desde el mes de Febrero de 2003. 2 Contacto cercano: haber cuidado, vivido o tenido contacto directo con secreciones respiratorias o fluidos corporales de un caso sospechoso o probable de SARS. Caso probable 1. Un caso sospechoso con evidencia radiográfica de infiltrados consistentes con neumonía o síndrome de insuficiencia respiratoria progresiva aguda (SIRPA) en la radiografía de tórax. 2. Un caso sospechoso de SARS que sea positivo para coronavirus de SARS (SARS-CoV) por medio de una o más pruebas. Ver Uso de métodos de laboratorio para diagnóstico de SARS. 3. Un caso sospechoso con hallazgos en la necropsia compatibles de patología por SIRPA sin una causa identificable. Criterio de exclusión Debe excluirse el caso, si un diagnóstico alternativo puede explicar por completo su enfermedad. Página 42 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Reclasificación de caso Debido a que actualmente el SARS es considerado como un diagnóstico de exclusión, la clasificación de un caso reportado pudiera modificarse a través del tiempo. Sin embargo, el paciente debe ser manejado apropiadamente independientemente de la clasificación donde se encuentre. • El caso inicialmente reportado como sospechoso o probable, al cual se le atribuye un diagnóstico alternativo que explique completamente su enfermedad, debe ser descartado posterior a haber considerado cuidadosamente la posibilidad de coinfección. • Un caso sospechoso, después de haber sido estudiado minuciosamente, que cumpla con los criterios de caso probable, debe ser reclasificado como caso probable. • Un caso sospechoso con una radiografía de tórax normal, deberá ser tratado apropiadamente y monitorizado por 7 días. Aquellos casos cuya recuperación no sea adecuada deberán ser reevaluados con otra radiografía de tórax. • Aquellos casos sospechosos cuya recuperación sea adecuada, pero cuya enfermedad no pueda ser completamente explicada por un diagnóstico alternativo, deberán permanecer como sospechosos. • Un caso sospechoso que muera, en el cual no se lleve a cabo la necropsia, deberá permanecer clasificado como sospechoso. Sin embargo, si se identifica que este caso ha sido parte de una cadena de transmisión de SARS, el caso debe ser reclasificado como probable. • Si se lleva a cabo la necropsia y no se encuentra evidencia patológica de SIRPA, el caso deberá ser descartado. Definición de caso según el CDC El Centro para la Prevención y Control de Enfermedades (CDC por sus siglas en inglés) agregó los criterios de laboratorio como evidencia de infección por el coronavirus asociado a SARS (SARS-CoV) a la vigilancia provisional de definición de caso. Utilizando los criterios de laboratorio, un caso de SARS se confirma por medio de pruebas de laboratorio si se encuentra alguno de los siguientes: • Detección del anticuerpo contra SARS-CoV por inmunofluorescencia indirecta (IF) o por ensayo inmunoabsorbente ligado a enzimas (ELISA). • Aislamiento de SARS-CoV en cultivo de tejidos. Página 43 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com • Detección de RNA de SARS CoV por medio de reacción en cadena de la polimerasa de transcriptasa reversa (RT-PCR), que deberá ser confirmada por una segunda RT-PCR. Los resultados negativos de las pruebas de laboratorio para PCR, cultivo viral o exámenes de anticuerpos que hayan sido obtenidos dentro de los primeros 21 días de enfermedad, no descartan la posibilidad de infección por coronavirus. En estos casos, se requiere de una prueba de anticuerpos de alguna muestra obtenida después de los primeros 21 días de enfermedad para determinar la infección. La definición actualizada de caso según el CDC del día 29 de abril de 2003, se encuentra disponible en la página de Internet: http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5217a5.htm Página 44 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Capítulo 7: Pruebas diagnósticas Wolfgang Preiser, Christian Drosten Traducción por: Dr. Joaquín A. Zúñiga Ramos. Pruebas de laboratorio Debido a los esfuerzos de la Red Multicéntrica de Colaboración para pruebas de laboratorio para SARS, se ha desarrollado pruebas para el nuevo Coronavirus con rapidez sin precedentes (SARS: Laboratorio de pruebas diagnósticas – Abril 29, 2003; http://www.who.int/csr/sars/diagnostictests/en/ ). Las muestras de casos sospechosos y probables de SARS han sido probadas para SARS-CoV en varios laboratorios, incluyendo Canadá, Francia, Alemania, Hong Kong, Italia, Japón, Holanda, Singapur, Reino Unido y Estados Unidos. Sin embargo, hasta que la se estandarice la detección de virus o anticuerpos, y los métodos sean adecuadamente probados, el diagnóstico de SARS se basa en hallazgos clínicos y epidemiológicos. La revisión de definición de caso del 1 de mayo de 2003 (ver: http://www.who.int/csr/sars/casedefinition/en/) para la primer ocasión incluye resultados de laboratorio: caso sospechoso de SARS, que es positivo para SARS-CoV en uno o más ensayos, debe ser clasificado como caso probable. Hasta el momento, no existe un criterio definido para resultados de pruebas de SARS-CoV para confirmar o excluir el diagnóstico de SARS. Los resultados de laboratorio para otros agentes conocidos que son capaces de causar neumonía atípica, tales como Legionella pneumophila, virus de influenza y parainfluenza, Mycoplasma pneumoniae, etc., pueden servir como criterios de exclusión; de acuerdo con la definición de caso, se puede excluir si se explica totalmente la enfermedad de un paciente con un diagnóstico alternativo. Sin embargo, la posibilidad de una infección doble no debe ser descartada completamente. Pruebas moleculares El RNA específico para SARS-CoV puede ser detectado en varios tipos de muestras clínicas como sangre, heces, secreciones respiratorias o tejidos corporales mediante la reacción en cadena de la polimerasa (PCR). Un número de protocolos de PCR desarrollados por la red de laboratorios de la OMS están disponibles en la página de internet de la OMS (http://www.who.int/csr/sars/primers/en/). El kit de prueba de RTPCR 5´-nucleasa y controles negativos desarrollados por el Instituto Bernhard Nocht (http://www.bni-hamburg.de/), también se encuentra disponible http://www.artusbiotech.de). La preparación de un estándar inactivado con fines diagnósticos, se encuentra disponible en la Red Europea para Infecciones Virales Importadas (ENIVD; http://www.enivd.de). El ENIVD prepara un esquema para asesoramiento de calidad externa internacional para ensayos de SARS-CoV. A pesar de la alta sensibilidad, la prueba de PCR existente no puede determinar con exactitud la presencia de SARS-CoV en pacientes. Por otro lado, la contaminación de muestras en los laboratorios puede permitir la presencia de resultados falsos-positivos. La elaboración de estrictas guías de control de calidad de laboratorio y pruebas confirmatorias están siendo desarrolladas por la OMS Página 45 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com (http://www.who.int/csr/sars/labmethods/en/). Un resultado positivo válido de PCR indica que existe material genético (RNA) de SARS-CoV en la muestra. Sin embargo, no significa que el virus presente sea infeccioso o que se encuentre en grandes cantidades para infectar a otra persona. Los resultados negativos de PCR no excluyen SARS. Además existe la posibilidad de obtener resultados incorrectos, falsos-negativos (por pérdida de sensibilidad), muestras colectadas en tiempo en que el virus o el material genético no estuvieron presentes. Cultivo Viral La presencia de virus infeccioso puede ser detectada por inoculación de líneas celulares apropiada (Ej. Vero E6) con muestras del paciente (como secreciones respiratorias, sangre o evacuaciones) y propagar el virus in vitro. El virus, una vez aislado debe ser identificado como SARS-CoV, utilizando las siguientes técnicas. El cultivo celular es una prueba muy demandante, pero actualmente (con excepción de los ensayos en animales) únicamente sirve para demostrar la existencia de un virus vivo. Esta prueba ha sido desarrollada para usarse en condiciones de bioseguridad 3. Un cultivo positivo indica la presencia de SARS-CoV vivo en la muestra. Un resultado negativo, no excluye SARS (ver resultado negativo de la PCR). Detección de Anticuerpos Existen métodos para la detección de anticuerpos producidos en respuesta a la infección con el SARS-CoV. Diferentes isotipos de anticuerpos (IgM e IgG) aparecen y cambien sus niveles durante el curso de la infección. Estos anticuerpos pueden ser indetectables en las etapas tempranas de la infección. Usualmente la IgG permanece detectable después de la resolución del SARS. Se han desarrollado algunas técnicas para la detección de anticuerpos, sin embargo no están disponibles comercialmente: - Ensayo de inmunoabsorción ligado a enzima (ELISA): esta es una prueba que detecta una mezcla de anticuerpos de isotipo IgG e IgM en el suero de los pacientes con SARS y generalmente se pueden observar resultados confiables aproximadamente a los 21 días después del inicio del SARS - Ensayo de inmunofluorescencia (IFA): este ensayo requiere el uso de células infectadas por el SARS-CoV fijadas en una laminilla para su observación al microscopio; los anticuerpos del paciente se unen a los antígenos virales, estos anticuerpos son posteriormente detectados por un segundo anticuerpo de clase IgG y/o IgM marcado con un agente que emite fluorescencia al observarse en un microscopio de inmunofluorescencia. Esta prueba resulta positiva después de unos 10 días a partir del comienzo de la enfermedad. Los resultados pueden cuantificarse mediante diluciones seriadas del suero de los pacientes. Actualmente no se dispone con un equipo comercial que utilice este método. - Prueba de neutralización: esta prueba se utiliza para determinar y cuantificar por titulación la capacidad del suero de un paciente para neutralizar la capacidad infecciosa del SARS-CoV en un cultivo celular. Esta prueba esta recomendada para instituciones que cuenten con instalaciones de nivel 3 de bioseguridad. Página 46 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Interpretación Una prueba positiva de detección de anticuerpos indica la infección previa con SARSCoV. Seroconversión de negativo a positivo o un aumento en el título de anticuerpos cuatro veces mayor en relación a los niveles normales en un suero de paciente con infección aguda a una etapa convaleciente indica infección reciente. Puede encontrarse una prueba negativa hasta los 21 días de haber comenzado la enfermedad, si la prueba continúa negativa por un periodo mayor podría pensarse que SARS-CoV no es el responsable de la enfermedad. Hasta la fecha no hay datos de seroprevalencia contra SARS-CoV en ningún grupo control. Las pruebas de diagnóstico por medio de la detección de anticuerpos permiten el diagnóstico indirecto de la infección por SARS-CoV, pero no son útiles en la etapa aguda de la enfermedad Limitantes Es importante se cautelosos en la toma de decisiones en el manejo de pacientes basándose en resultados de ensayos virológicos. Para más detalles, revisar la update 39 de la OMS http://www.who.int/csr/sarsarchive/2003_04_25/en/. Los falsos negativos (resultado de baja sensibilidad, muestras incorrectas o fuera de tiempo, etc.) pueden dar un falso sentido de seguridad; en el peor de los casos pueden observarse en sujetos portadores de SARS-CoV capaces de infectar a otras personas. Para un mejor entendimiento de SARS, la OMS recomienda que se guarden muestras secuenciales de quienes se sospecha SARS e incluso de contactos cercanos, todo esto con la finalidad de un análisis posterior. Esto es particularmente importante en los primeros casos identificados en un país sin previos reportes de SARS. Deberá realizarse una recolección de datos clínicos e historia de contacto para tener un mejor entendimiento del patrón de diseminación viral y periodo de transmisión. Es importante poner especial atención en que las muestras de los pacientes sean adecuadas y estén en buen estado para la realización de cultivo viral, PCR, detección de antígenos, inmuno-tinción y/o pruebas de búsqueda de anticuerpos. La OMS también hace hincapié en que cada país designe un laboratorio de referencia para investigación y el envío de las muestras de pacientes con posible SARS. Consideraciones de bioseguridad A este respecto, ningún caso de SARS se ha reportado en personal que maneja el SARS-CoV en laboratorio. Además la OMS ha emitido una guía de manejo de muestras provenientes de pacientes con SARS o en todo caso material contaminado (25 de Abril, 2003; ver http://www.who.int/csr/sars/biosafety2003_04_25/en/). Es necesario tomar algunas medidas para prevenir la diseminación potencial por medio de gotas, aire o superficies y objetos contaminados, con particular énfasis en muestras que puedan emitir aerosoles. Para pruebas diagnósticas de rutina en suero y sangre que involucren la manipulación de virus inactivados (lisados, fijados u otros tratamientos), partículas virales y/o fragmentos no infecciosos del genoma viral, evaluación rutinaria de cultivos bacterianos o de hongos y finalmente empacamiento de muestras (dentro de un contenedor primario sellado y descontaminado) para su transportación a laboratorios de Página 47 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com diagnóstico para pruebas adiciones, deberán utilizarse prácticas adecuadas nivel 2 de bioseguridad. Cualquier procedimiento que pueda generar aerosoles necesariamente deberá efectuarse dentro de un gabinete de seguridad biológica y los trabajadores deberán usar protección en ojos, mascaras de alta eficiencia, además del equipo básico de protección como guantes, bata desechable impermeable. La manipulación in vitro de grandes concentraciones del agente etiológico como el cultivo celular, necesariamente debe ser manejado en un nivel 3 de bioseguridad tanto instalaciones de nivel 3 como prácticas especiales de nivel 3 de bioseguridad. Las regulaciones para agentes peligrosos del 2003 de la IATA (International Air Transport Association), para muestras que probablemente contengan el agente etiológico de SARS deben ser transportadas como: UN3373 “muestras de diagnóstico” cuando la finalidad de transportación sea para investigación o diagnóstico. Cuando las muestras a transportar, de forma deliberada puedan producir virus patogénicos como cultivos deben transportarse como: UN 2814 y marcadas como “Sustancia infecciosa, que afecta a humanos (Severe Acute Respiratory Síndrome virus)”. Todas las muestras deberán transportarse como UN3373 o UN 2814 y deben empacarse en tres contenedores. Para información detallada acerca de las prácticas de bioseguridad y prácticas de contención pueden ser encontradas en el manual de bioseguridad de la OMS, 2ª edición, disponible en la página de internet (http://www.who.int/csr/resources/publications/biosafety/Labbiosafety.pdf). Perspectivas Además de un diagnóstico rápido de infección por SARS, la disponibilidad de pruebas diagnósticas puede ser de mucha ayuda para resolver preguntas importantes como el periodo de diseminación viral (y comunicabilidad) durante la convalecencia la presencia del virus en diferentes fluidos corporales, heces y presencia de virus durante el periodo de incubación. A pesar de que las pruebas de laboratorio para SARS-CoV han sido desarrolladas bajo un buen grado de estandarización y control de calidad, es importante utilizarlas con sumo cuidado en las situaciones clínicas. Es muy recomendable verificar las recomendaciones actualizadas de la OMS y las organizaciones nacionales importantes donde se especifiquen y refieran a la disponibilidad y uso de estas pruebas. (Ver: http://www.who.int/csr/sars/labmethods/en/). Página 48 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Tabla 1.- Pruebas disponibles (Mayo 2003) para el diagnóstico de infección por coronavirus asociado a SARS. Método de Detección Tipo de muestra Detalles técnicos Importancia diagnóstica Detección de virus Uso de línea celular Vero; infraestructura y prácticas de nivel 3 de bioseguridad Indica la presencia de virus infeccioso; resultado negativo no excluye SARS Diferentes protocolos y secuencias de oligonucleótidos están disponibles en la página electrónica de la OMS+ Indica la presencia de genoma viral, no necesariamente de virus infeccioso; un resultado negativo no excluye SARS Ensayo de Suero inmunofluorescencia Detección de anticuerpos específicos de isotipo IgG e IgM o ambos La inmunofluorescencia para IgM es positiva después de 10 días del inicio de síntomas ELISA Suero El ELISA es positivo Detección de anticuerpos de isotipo después de 21 días del inicio de síntomas IgG o IgM o ambos Neutralización Suero Utilidad en Requiere investigación infraestructura y prácticas de nivel 3 de bioseguridad (virus “vivo”) Aislamiento viral en cultivo Muestras de tracto respiratorio: esputo, BAL Reacción en cadena Muestras de tracto de la polimerasa respiratorio: (PCR) esputo, BAL, hisopado faríngeo, lavado faríngeo, heces fecales Detección de anticuerpos Ver: “: "Severe Acute Respiratory Syndrome (SARS): Laboratory diagnostic tests" (http://www.who.int/csr/sars/diagnostictests/en/) +Ver: "PCR primers for SARS developed by the WHO Network Laboratories" (http://www.who.int/csr/sars/primers/en/) and "Recommendations for laboratories testing by PCR for presence of SARS coronavirus - RNA" (http://www.who.int/csr/sars/coronarecommendations/en/) Página 49 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Figura 1. Ensayo de Inmunofluorescencia (IFA): Células Vero infectadas con SARS-CoV, incubación con suero de paciente (dilución 1:50), obtenido 11 después del inicio de síntomas, se observa un patrón de fluorescencia citoplasmático (Fuente: Institute for Medical Virology, Director: W. Doerr) http://www.sarsreference.com/archive/verocells_patientserum.jpg Figura 2. Ensayo de Inmunofluorescencia (IFA): Células Vero infectadas con SARS-Cov, incubadas con un suero control negativo. (Fuente: Institute for Medical Virology, Director: W. Doerr) http://www.sarsreference.com/archive/verocells_controlserum.jpg Página 50 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Capitulo 8: Diagnóstico. Traducción por: Dr. Ricardo Stanley Vega Presentación clínica La presentación clínica del SARS es inespecífica. Los síntomas pueden semejar las otras formas de neumonía atípica la cual, usualmente, puede ser provocada por Legionella, Mycoplasma o Chlamydia. Después de un periodo de incubación de 2 a 10 días, el paciente desarrolla fiebre mayor a 38 grados centígrados asociada con otros síntomas y signos clínicos como son escalofríos, cefalea, somnolencia, malestar general y mialgias. (Ver cuadro 1) (CDC, Lee, Tsang, Peiris, Chan-Yeung) La producción de esputo, odinofagia, coriza, nausea, vomito y diarrea, la cual es menos común (Lee). Cuadro 1: Presentación de síntomas clínicos (%) Lee, et al. n=138 Peiris , et al n=50 Fiebre 100 100 Escalofrio 73 74 Tos 57 62 Mialgia 61 54 Malestar general nd 50 Rinorrea 23 24 Dolor de garganta 23 20 Taquipnea nd 20 Diarrea 20 10 Cefalea 56 20 El examen físico del paciente revela fiebre en la mayoría de los pacientes. Estertores inspira torios se pueden auscultar en la base de los pulmones y las sibilancias están generalmente ausentes. Las más comunes de las anormalidades de laboratorio incluyen linfopenia, leucopenia, trombocitopenia, niveles altos de deshidrogenasa láctica, aspartato aminotransferasa y creatincinasa (Lee, Tsang, Poutanen, Peiris, Chan-Yeung). (Ver cuadro 2. La leucopenia es generalmente provocada por disminución de los linfocitos en los primeros días posterior a su internamiento. En un estudio ninguno de los pacientes con elevación de los niveles de creatincinasa tuvo elevación anormal de creatincinasa fracción MB o troponina T, indicando que la fuente de creatincinasa fue poco probable ser de origen cardíaco. (Lee). Página 51 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Cuadro 2: Hallazgos de laboratorio (%) Lee, et al n= 138 Peiris , et al n=50 Leucopenia ( <3500 x mL) 34 26 Linfopenia (< 1000 x mL) 70 68 Trombocitopenia 45 40 Alanin-amino-transferasa elevada. 23 34 Creatincinasa elevada. 32 26 LDH elevada. 71 nd Hiponatremia 20 nd Hipopotasemia 25 nd Niveles de Dimero –D elevados. 45 nd Tiempo parcial de tromboplastina activado prolongado 43 nd Se desconoce la proporción de casos asintomático de esta infección. Una descripción comprehensiva del espectro de enfermedades clínicas del SARS es dependiente de un gran número de seroconvertidos en la población a la cual el virus del SARS se ha diseminado. Las pruebas diagnósticas futuras podrán hacer posible dichas investigaciones. Anormalidades radiográficas del tórax Las radiografías de tórax pueden ser normales durante el pródromo febril y a través del curso de la enfermedad; sin embargo, al inicio de la fiebre, la mayoría de los pacientes presentan una radiografía de tórax anormal con evidencia de consolidación de espacio aéreo. (Lee). Los hallazgos de la radiografía de tórax al inicio del cuadro clínico presentan opacidades pequeñas, unilaterales en parche, las cuales progresan al primer y segundo día llegando a ser opacidades bilaterales y generalizadas con áreas confluentes e intersticiales. En una cohorte de pacientes, 59 de 108 pacientes (54.6%) tienen lesiones unilaterales localizadas y 49 (45.4 %) tenían lesiones multifocales y/o bilaterales. Los hallazgos radiológicos inicial son indistinguibles a otras causas de neumonía. Existe una mayor frecuencia de presentación de dichas lesiones en las zonas periféricas del pulmón. Derrame pleural, cavitaciones y linfadenopatías mediastinales no se presentaron. (Lee). Los síntomas respiratorios y los signos auscultatorios son desproporcionalmente menores comparados con los hallazgos radiográficos. (Lee). En los pacientes que presentan deterioro clínico, las opacidades pulmonares pueden incrementarse en tamaño, extensión y severidad entre el día 7 y 10 posterior a su internamiento. (Tsang, Lee). Las anormalidades predominantes encontradas inicialmente en la tomografía axial computada de Tórax son áreas de consolidación subpleural localizadas con broncograma aéreo y áreas de vidrio despulido, con predilección por las zonas Página 52 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com posteriores de los pulmones. (Tsang). Las opacidades alveolares periféricas hacen recordar a las encontradas en Neumonías producidas por Bronquiolitis Obliterante y neumonías intersticiales agudas. Dilataciones bronquiales no se observan (Tsang). Radiológicamente, SARS pude ser indistinguible de otras formas severas de neumonía. Esto también se encuentra en los hallazgos de la tomografía computada con otras condiciones que resultan en enfermedad de espacio aéreo subpleural, tales como la neumonía con Bronquiolitis obliterante y neumonía intersticial aguda (Tsang) Un grupo de investigación de Hong Kong sugiere que las radiografías de tórax ofrecerían importantes claves diagnósticas, en particular, cuando después de una semana, las áreas de consolidación periféricas y unilaterales se vuelven bilaterales y la extensión de las opacidades pulmonares se correlaciona con el deterioro en la función respiratoria. (Lee). Curso Clínico La severidad de la enfermedad es altamente variable, presentándose desde síntomas leves a graves con falla respiratoria aguda (en más del 20%) y muerte. El deterioro clínico combinado con desaturación de oxigeno, necesidad de cuidados intensivos y soporte ventilatorio, generalmente ocurre entre el día 7 y 10 después del inicio de los síntomas. (Lee, Peiris). La mortalidad puede ser tan alta como el 50 %, dependiendo del grupo de edad afectado con una letalidad estimada de 14 a 15%. (Donnelly, WHO Update 49). La temperatura corporal normalmente permanece alta durante la evolución de le enfermedad. En el primer estudio de seguimiento, los pacientes presentaron fiebre recurrente (85.3%) al día 8.9 +/- 3.1 (rango 4-18), diarrea liquida (73.3%) al día 7.5 +/2.3 (rango 3-15), deterioro radiológico (80%) al día 7.4 +/- 2.2 (rango 3-13) y deterioro respiratorio (45.3%) al día 8.6 +/- 3 días (rango 5-19). (Peiris II). En 45.3% de los pacientes, una marcada mejoría de las lesiones iniciales correlacionaron con el aparecimiento de nuevos lesiones radiológicas en otros sitios. (Peiris II). La RT-PCR de los aspirados nasofaríngeos consistentemente demostró un pico de carga viral al día 10 y una disminución de los niveles al día 15. Estos hallazgos sugieren que el deterioro durante la segunda semana no puede estar relacionada con una descontrolada replicación viral pero puede ser causada por daño inmunopatológico. (Peiris II) Factores de riesgo que han sido asociados a deterioro clínico son resumidos en el cuadro 3: Página 53 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Cuadro 3: Factores de riesgo asociado con deterioro clínico. Autor n Lee , et al Peiris . et 138 al 50 Peiris II , et al 75 Factores de riesgo Edad avanzada, Neutrofilia, LDH alta. Edad avanzada, linfopenia grave, AAT alta , retraso ribavirina + esteroides Edad avanzada, infección por hepatitis B crónica. En un pequeño porcentaje de pacientes se ha descrito diferentes grados de fibrosis pulmonar posterior a su recuperación. Los mecanismos fisiopatológicos de estos hallazgos permanecen sin conocerse; sin embargo, el desarrollo de secuelas a largo tiempo requiere de cuidadoso seguimiento post tratamiento. Diagnóstico Pruebas de laboratorio menos específicas (PCR, Detección de Anticuerpos contra SARS-CoV, ver capitulo de” pruebas diagnósticas”) confirman la sospecha inicial de SARS, el diagnóstico de SARS es basado en los hallazgos clínicos de una neumonía atípica no atribuible a ninguna otra causa conocida y una historia de exposición a un caso sospechoso o probable de SARS o contacto con sus secreciones o líquidos corporales. La prueba diagnóstica inicial de un paciente sospechoso de SARS incluye radiografía de tórax, Oximetría de pulso, hemocultivos, Tinción de Gram y cultivo de la expectoración con pruebas para virus respiratorios como Influenza A y B y sincicial respiratorio; así como, una muestra de orina para antígeno de Legionella y neumococo deben ser consideradas. (CDC, http:// www.cdc.gov/ncidod/sars/diagnosis.htm). Se debe guardar cualquier muestra clínica disponible (respiratoria, sangre y suero) para posteriores pruebas hasta poder tener un diagnóstico específico. Muestras de suero sanguíneo en la etapa aguda y en la convaleciente (mayor a 21 días del inicio de los síntomas) deben ser guardadas en aquellos pacientes con criterios de definición de SARS. Las instrucciones específicas de colección de muestras en casos sospechosos de SARS están disponibles en Internet. En las etapas tempranas, el SARS puede ser difícil de diferenciarse de otras infecciones virales y el retraso en su diagnóstico contribuye a la diseminación de la epidemia. (Hsu). Página 54 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Histopatología Biopsia pulmonar El examen histopatológico de una muestra de parénquima pulmonar en un paciente con SARS muestra una inflamación intersticial leve con neumocitos esfacelados que presentan citomegalia, citoplasma granular anfofílico y núcleos grandes con nucleolos prominentes. No se encuentran células con inclusiones típicas de virus del herpes o adenovirus. (Peiris) Hallazgos Post-Mortem Evaluaciones histopatológicas post muerte de tejido pulmonar de aquellos pacientes que han fallecido de SARS mostraron daño alveolar difuso en diferentes niveles de progresión y severidad, consistentes con las manifestaciones patológicas de un Síndrome de Insuficiencia Respiratoria Aguda. (Ksiazek, Tsang, Poutanen). Los cambios incluyeron formación de membranas hialinas, infiltrados inflamatorios mononucleares intersticiales y descamación de neumocitos en el espacio alveolar. (Ksiazek). Había focos cicatrizales de tejido fibroelástico mixoide a nivel alveolar, lo cual corresponde, a la fase organizacional temprana del Síndrome de Insuficiencia Respiratoria Aguda. Septos interalveolares con leve engrosamiento e infiltrado mononuclear (Tsang). El examen del hígado reveló cambios grasos microvesiculares, hemorragias focales y necrosis hepática con cuerpos cicatrizales acidófilos. El bazo mostró grandes áreas de necrosis isquémica y linfocitos atípicos en las vainas periarteriolares (Poutanen). Referencias 1. CDC. Preliminary Clinical Description of Severe Acute Respiratory Síndrome. MMWR 2003 ; 52:255-6. http://www.cdc.gov/mmwr/preview/mmwrhtml/mm5212a5.htm. 2. Chan-Yeung M, Yu WC. Outbreak of severe acute respiratory syndrome in Hong Kong special Administrative Region: case report. BMJ 2003; 326:850-2. http://bmj.com/cgi/content/full/326/7394/850 3. Donnelly CA, Ghani AC, Leung GM, et al. Epidemiological determinants of spread of casual agent of severe acute respiratory syndrome in Hong Kong. Lancet 2003; 361. http://image.thelancet.com/extras/03art4453web.pdf 4. Hsu L-Y, Lee C-C, Green JA, Ang B, Paton NI, Lee L , et al. Severe acute respiratory síndrome (SARS) in singapore: Emerg Infect dis. 2003, 9. http://cdc.gov/ncidod/EID/vol9no6/030264.htm 5. Ksiazek, TG, Edman D, Goldsmith CS, Zaki SR, Peret T, Emery S, et al. A novel Coronavirus associated with severe acute respiratory syndrome. N Engl J Med( Early online release 2003 Apr 10). http:// SARSreference.com/lit.php?id=12690092 Página 55 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com 6. Lee N, Hui D, Wu A, Chan P, et al. A major outbreak of severe acute respiratory syndrome in Hong Kong. N Engl J Med 2003. http:// SARS Reference.com/lit.php?id=12682352 7. Peiris J, Lai S, Poon J, Guan Y, et al. coronavirus as a possible cause of severe acute respiratory syndrome. Lancet 2003; 361: 1319-1325. http://SARSReference.com/lit.php?id=12711465 8. Peiris J, Chu C, Cheng V, et al. Prospective study of the clinical progression and viral loadof SARS associated coronavirus pneumonia in a community outbreak.Lancet 2003.http:// www.who.int/esr/sars/prospectivestudy/en/index.html 9. Poutanen SM, Low DE, Henry B, Finkelstein S.et al Identification of severe acute respiratory syndrome in Canada. N Engl J Med , 2003. http:// SARSReference.com/lit.php?id=12671061 10. Tsang KW, Ho PL, Ooi GC, Yee Wk, et al. A cluster of cases of severe acute respiratory syndrome in Hong Kong. N Engl J Med 2003. http://SARSReference.com/lit.php?id=12671062 11. WHO Update 49: SARS case fatality ratio, incubation 7.http://www.who.int/esr/sarsarchive/2003_05_07a/en/ period. May Página 56 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Capítulo 9: Tratamiento Traducción por: Dra. Elia Camacho Gutiérrez. El régimen terapéutico más eficaz contra el SARS, si es que hay alguno, aún se desconoce. Para pacientes con deterioro evolutivo resultan de gran importancia las medidas de soporte. La ribavirina y los esteroides son los fármacos que se han utilizado más frecuentemente en los últimos meses desde el inicio de la epidemia del SARS. La ribavirina es un fármaco antiviral análogo de nucleósido purínico de amplio espectro, estructuralmente relacionado con la guanosina. Tiene actividad contra gran variedad de virus RNA y su uso habitual es en el tratamiento de hepatitis por virus C en combinación con interferón. El uso de esteroides tiene su fundamento en la observación de cambios en el tejido pulmonar sugestivos de que al menos parte del daño debe estar mediado por citocinas inducidas por el agente infectante. En términos generales se piensa que el uso de la combinación ribavirina y esteroides es el responsable de cierta mejoría clínica de los pacientes con SARS (Lee, Poutanen, Tsang). Sin embargo, algunos médicos no han observado beneficio clínico cuando se utilizan dosis del esteroide menores a las usadas en Hong Kong (Hsu). Los mejores resultados obtenidos del uso de la combinación ribavirina y esteroides han sido por mucho reportados en Hong Kong. Se ha sugerido el siguiente tratamiento empírico, inicialmente basado en la experiencia obtenida de un pequeño número de casos y subsecuentemente confirmado por resultados favorables en un pequeño número de casos y subsecuentemente confirmados por resultados favorables en una mayor proporción de pacientes (Tabla 1). Sin embargo, aún en Hong Kong, continúa el debate de continuar la utilización de Ribavirina como parte del régimen terapéutico. Algunos médicos han descontinuado el uso de la ribavirina mientras otros aún lo utilizan (Moira Chan-Yeung, comunicación personal, 5 de mayo). En Canadá, los oficiales de salud decidieron el 1º de mayo que el Programa de Acceso Especial (en Canadá la ribavirina parenteral no se encuentra aprobada para su venta) no permitiría el acceso de rutina a la ribavirina para el tratamiento del SARS (Health Canadá). Esta decisión se tomó posterior a la revisión de la experiencia clínica anecdótica contra otros coronavirus relacionados con el SARS Co-V, los resultados negativos in vitro de la ribavirina contra coronavirus relacionados con el SARS Co-V y el conocimiento de los reportes de efectos adversos serios e inesperados. Página 57 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Tabla 1: Tratamiento empírico contra el SARS* Fármaco Administración Ribavirina 8 mg/kg IV cada 8 horas ó 1.2 g VO cada 12 horas con un bolo inicial de 4 g (con función renal normal). Administrar por 7-14 días dependiendo de la respuesta y el tiempo de retiro de los corticoesteroides. Hidrocortisona 2mg/kg IV cada 6 horas o 4mg/kg IV cada 8 horas. Suspensión gradual 1 semana cuando haya mejoría clínica importante. Para pacientes con deterioro rápido usar metilprednisolona 10 mg/kg IV cada 24 horas por 2 días y después continuar con la hidrocortisona como se señala anteriormente. Antibacterianos Cobertura contra agentes de neumonía adquirida en la comunidad y atípicos por 7 a 14 días (levofloxacina y macrólidos). Los pacientes deben recibir profilaxis anti-ulcerosa y ser monitorizados con Hb, cuenta reticulocitaria, glucosa sérica y concentraciones de potasio. La eficacia de este régimen requiere seguimiento estricto. * Sugerido por las autoridades hospitalarias de Hong Kong (Chan-Yseung) Desde el reconocimiento de la ribavirina como teratógeno y capaz de causar efectos adversos severos, incluyendo anemia hemolítica severa (Koren), se le ha recomendado a los médicos que actualmente están tratando pacientes con ribavirina que re-evalúen estrictamente el riesgo/beneficio para cada paciente antes de continuarla. Otro fármaco antiviral, con licencia de uso contra influenza, el inhibidor de neuraminidasa oseltamivir (Tamiflu), no ha mostrado ninguna eficacia (Lee, Poutanen). Ventilación Mecánica Los pacientes que requieren ventilación mecánica generalmente llenan los criterios de SIRPA con infiltrados difusos en la radiografía de tórax e hipoxemia sin evidencia de falla ventricular izquierda. El manejo terapéutico es de soporte (Poutanen). El mejor abordaje para el soporte ventilatorio de pacientes con SARS no se conoce pero podría ser alguna estrategia neumoprotectiva que se ha observado disminuye la mortalidad en pacientes con SIRPA (ARDS Network, 2000). Guías Hasta el momento se han publicado pocas guías y lineamientos sobre el manejo del SARS hasta ahora (Ho, WHO). Página 58 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Los lineamientos de la OMS que se describen a continuación se encuentran en constante revisión y actualización de acuerdo a la información generada. Revisar regularmente el sitio web de la CDC para nuevas actualizaciones. http://www.who.int/csr/sars/magement/en/ OMS: Manejo de pacientes con Síndrome Respiratorio Agudo y Grave SARS Revisado: 11 de abril 2003 Manejo de Casos sospechosos y probables de SARS Hospitalización en cuarto aislado o con otros casos sospechosos o probables de SARS (ver Guías de Control de Infecciones Hospitalarias). Tomar muestras pertinentes (esputo, sangre, suero, orina) para excluir las causas comunes de neumonía (incluyendo gérmenes atípicos), considerar la posibilidad de coinfección con SARS y realizar los estudios radiológicos apropiados (Rx tórax) Tomar los siguientes exámenes de laboratorio para apoyar el diagnóstico clínico del SARS: BH, PFH, ES, QS, PCR y suero pareado (El suero pareado será importante para el entendimiento ulterior del SARS aún en aquellos pacientes que posteriormente no se consideren casos de SARS) Cobertura con antibióticos contra gérmenes de neumonía adquirida en la comunidad y por gérmenes atípicos desde el momento de su admisión. Mantener especial atención a intervenciones o terapias que puedan causar aerolización como el uso de nebulizaciones con broncodilatadores, fisioterapia pulmonar, broncoscopía, gastroscopía y otros procedimientos o intervenciones que puedan alterar el tracto respiratorio. Deben realizarse con las precauciones recomendadas (aislamiento, guantes, lentes, bata, mascarillas, etc.). Para el manejo del SARS se han empleado empíricamente ribavirina con o sin esteroides pero no se ha probado su efectividad. Se ha propuesto un estudio multicéntrico coordinado para establecer la efectividad de la terapia con ribavirina y otras posibles intervenciones. SARS por haber estado expuesta a un caso sospechoso o probable de SARS. Hasta el momento se considera exposición riesgosa aquellas actividades que incluyan cuidado, cohabitación o tener contacto directo con las secreciones respiratorias, fluidos corporales y/o excremento de un caso sospechoso o probable de SARS. Si el contacto desarrolla síntomas de la enfermedad deberá ser investigado por las autoridades sanitarias locales a cargo Definición de Contacto de SARS Un contacto es una persona que puede encontrarse en gran riesgo de desarrollar SARS. La información disponible hasta la fecha sugiere que dentro de las exposiciones riesgosas se encuentran cuidar, vivir con o tener contacto directo con secreciones respiratorias, fluidos corporales y/o excremento (pl ej. Heces) de un caso sospechoso o probable de SARS. Página 59 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Manejo de contactos de casos probables de SARS Proporcionar información del SARS a los contactos relacionado con los síntomas, modos de transmisión, etc. Recomendar aislamiento voluntario en casa con vigilancia activa durante 10 días Seguimiento diario (visitas domiciliarias o vía telefónica) por un miembro del equipo de salud pública responsable Registro diario de temperatura Definición de contacto de SARS Un contacto es una persona que puede estar en mayor riesgo de desarrollar Manejo de los Contactos de casos sospechosos de SARS Las siguientes medidas corresponden a las recomendaciones mínimas a seguir: Proporcionar información del SARS a los contactos relacionado con los síntomas, modos de transmisión, etc. Vigilancia pasiva por 10 días Si el contacto desarrolla cualquier síntoma, deberá reportarse vía telefónica con las autoridades sanitarias correspondientes El contacto puede continuar sus actividades cotidianas El primer síntoma más consistente parece ser la fiebre La mayoría de las autoridades sanitarias en otros países prefieren evaluar el riesgo para cada contacto de caso sospechoso o probable de SARS de manera individual siguiendo los lineamientos establecidos para establecer su manejo Suspensión del seguimiento Si un caso sospechoso o probable de SARS deja de cumplir los criterios establecidos y por lo tanto deja de ser un caso sospechoso o probable de SARS automáticamente se terminará la vigilancia de sus contactos. Página 60 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Referencias 1. Chan-Yeung M, Yu WC. Outbreak of severe acute respiratory syndrome in Hong Kong Special Administrative Region: case report. BMJ 2003; 326: 850-2. http://bmj. com/cgi/content/full/326/7394/850 2. Health Canada. Management of Severe Acute Respiratory Syndrome (SARS) in Adults: Interim Guidance for Health Care Providers. May 1, 2003 (accessed May 6) http://SARSReference.com/link.php?id=8 3. Ho W. Guideline on management of severe acute respiratory syndrome (SARS). Lancet 2003; 361. Published online April 8, 2003 (accessed May 5). http://image. thelancet.com/extras/03cmt89web.pdf 4. Hsu L-Y, Lee C-C, Green JA, Ang B, Paton NI, Lee L, et al. Severe acute respiratory syndrome (SARS) in Singapore: clinical features of index patient and initial contacts. Emerg Infect Dis 2003; 9. http://www.cdc.gov/ ncidod/ EID/vol9no6/03- 0264.htm 5. Koren G, Kong S, Knowles S, Phillips E. Ribavirin in the treatment or SARS: a new trick for an old drug? CMAJ 2003;168. Publicado en línea el 25 de abril, 2003. http://SARSReference.com/link.php?id=3 6. Lee N, Hui D, Wu A, Chan P, et al. A Mayor Outbreak of Severe Acute Respiratory Syndrome in Hong Kong. N Engl J Med 2003., http://SARSReference. Com/lit.php?id=12682352 7. Peiris J, Lai S, Poon L, Guan Y, et al. Coronavirus as a possible cause of severe acute respiratory syndrome. Lancet 2003; 361:1319-1325. http://SARSReference. Com/lit.php?id=12711465 8. Poutanen SM, Low DE, Henry B, Finkelstein S, et al. Identification of Severe Acute Respiratory Syndrome in Canada. N Engl J Med 2003. http://SARSReference.com/lit/php?id=12671061 9. Tsang KW, Ho PL, Ooi GC, Yee WK, et al. A Cluster of Cases of Severe Acute Respiratory Syndrome in Hong Kong. N Engl J Med 2003. http://SARSReference.com/lit.php?id=12671062 10. The Acute Respiratory Distress Syndrome Network. Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. N Engl J Med 2000;342:1301-8. http://SARSReference.com/lit.php?id=10793162 Página 61 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com SARS Pediátrico. Traducción por: Dra. Elia Camacho Gutiérrez. Sólo se ha reportado hasta el momento un estudio de SARS en niños. En todos los pacientes encontraron fiebre persistente, tos, cambios radiográficos evolutivos y linfopenia (Hon). Los pacientes adolescentes se presentaron con síntomas de malestar general, mialgias, escalofríos, similares a los presentados en adultos, mientras que los niños menores presentaban principalmente tos, escurrimiento nasal y ninguno tuvo escalofríos, mialgias o . Los niños fueron tratados con altas dosis de ribavirina, prednisolona oral o metilprednisolona intravenosa, sin efectos adversos a corto plazo: Tabla 1. Tratamiento de niños con SARS* Diagnóstico de SARS sospechado en Cefotaxima IV, claritromicina VO y admisión ribavirina VO**(40 mg/kg/día dividido en 2 o 3 dosis) Fiebre persistente >48 H Prednisolona oral **(0.5 –2 mg/kg) Pacientes con síntomas moderados o Ribavirina IV** (20 mg/kg/día, en 3 fiebre alta fluctuante y malestar general dosis) e hidrocortisona ** (2 mg/kg cada 6 h) inmediatamente después de su notorio admisión Fiebre persistente y empeoramiento Bolos de Metilprednisolona IV (10-20 clínico o radiológico mg/kg) *de Hsu: Clinical presentations and outcome of severe acute respiratory syndrome in children. **la ribavirina se administró por 1-2 semanas y los corticosteroides se fueron retirando en 2-4 semanas. Cuatro adolescentes requirieron oxígeno suplementario y dos, ventilación asistida, mientras ninguno de los niños menores requirieron oxígeno suplementario. El curso clínico fue mucho más leve y de menor duración entre los pacientes menores de 12 años de edad. Así mismo, los cambios radiológicos fueron de menor severidad y generalmente se resolvieron más rápidamente que en los adolescentes. Comparando adultos y adolescentes, el SARS parece tener un curso clínico menos agresivo en niños menores (Hon). Al tiempo de presentación de los primeros síntomas, ocho de los diez niños se encontraban asistiendo a la escuela. No hay evidencia de que ellos hayan diseminado la infección a sus compañeros. Este hallazgo es altamente contrastante con la experiencia reportada entre adultos portadores de SARS con alta tasa de infectividad (Hon). Página 62 de 63 Adaptado de Kamps-Hoffmann. www.SARSreference.com Referencias 1. Hon KLE, Leung CW, Cheng WTF, et al. Clinical presentations and outcome of severe acute respiratory syndrome in children. Lancet, Publicado en línea el 29 de abril, 2003. http://image.thelancet.com/extras/03let4127web.pdf Página 63 de 63