Obesidad y Síndrome de Apnea-Hipopnea Obstructiva del Sueño
Anuncio

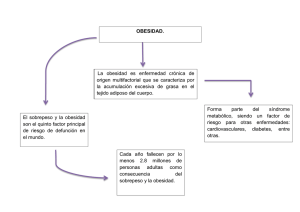
Obesidad y Síndrome de Apnea-Hipopnea Obstructiva del Sueño Introducción Guilleminault y cols, introdujeron el término síndrome de apnea del sueño (SAOS), Obstructive Sleep Apnea Syndrome, (OSAS), según la Academia Americana de disturbios del sueño (ASDA); para referirse a ventilaciones con pausas apneicas durante el sueño por más de 10 segundos y excesiva somnolencia durante el día, como consecuencia de una alteración anatómico-funcional de la vía aerodigestiva que conduce a la obstrucción del flujo aéreo. Hoy lo nombramos como "Síndrome de Apneas e Hipopnea Obstructiva del Sueño" (SAHOS); Block y cols; cuando el índice de apnea o hipopnea, (IAH) es superior a cinco por cada hora de sueño. El SAHOS se caracteriza por un cuadro de somnolencia y trastornos neuropsiquiátricos que pueden tener consecuencias sociolaborales importantes, accidentes de tráfico, laborales o el ausentismo laboral (por la somnolencia diurna), y consecuencias clínicas (Hipertensión Arterial, Infarto de miocardio, Accidente Vascular Cerebral, disminución de la líbido, depresión); constantes desaturaciones de la oxihemoglobina y despertares transitorios, dando lugar a un sueño fragmentado y poco reparador, con aumento en la aparición de cardiopatías. “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. Etiología La obesidad es un problema de salud creciente en nuestro país. Su forma más extrema u obesidad mórbida se asocia frecuentemente a Diabetes Mellitus No Insulina dependiente (DMNID), hipertensión arterial (HAS), hiperlipidemia, arteriosclerosis, enfermedades degenerativas y traumáticas, osteoarticulares, cáncer, trastornos sexuales, neuropsíquicos y alteraciones respiratorias. Estas últimas pueden constituir un cuadro grave e invalidante, capaz de llevar a los pacientes a la muerte por paro cardiorrespiratorio, conocidas como síndrome de Pickwick. Los niños obesos tienen una alta probabilidad de desarrollar trastornos de salud: asma, DMNID, HAS, cardiopatías, depresión, ansiedad, baja auto estima y apnea del sueño; afectando la memoria y la habilidad de aprender. La obesidad se asocia, en especial, con la apnea del sueño, cuando la parte superior de la faringe se relaja y colapsa a intervalos durante el sueño, impidiendo temporalmente el paso de aire. Cuando el cerebro es incapaz de enviar los impulsos adecuados a los músculos toracoabdominales para iniciar los movimientos ventilatorios, se refiere como apnea del sueño de origen central, (menos frecuente). Y periférica u obstructiva, cuando el aire no puede pasar por la nariz o la boca del paciente hacia o desde el exterior y mixtas. Una variante es el síndrome de resistencia de la vía aerodigestiva (UARS) en el cual los eventos patológicos se caracterizan por esfuerzo ventilatorio con microdespertares (RERAs), definida por la Academia Americana del Sueño (AASM), como causada por una obstrucción parcial de la vía aerodigestiva con un incremento en la amplitud del esfuerzo ventilatorio (presión intratoraccica negativa) llevando a una reducción en el flujo aéreo con una disminución del esfuerzo ventilatorio, asociado a microdespertares, y desaturación arterial de oxihemoglobina. “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. Epidemiología La apnea del sueño es una condición seria, potencialmente mortal, mas frecuente de lo que se cree. Afecta a algunas familias. Las personas más propensas a tener o desarrollar apnea del sueño son aquellas que: roncan sonoramente, tienen sobrepeso, padecen HAS, tienen algún defecto físico en la vía aerodigestiva, accidentes, principalmente en vehículo automotor y accidente vascular cerebral. Se produce en ambos sexos y en todos los grupos de edad, mas frecuente en hombres, poco diagnosticada en las mujeres. La asociación de SAOS y obesidad predomina en varones y mujeres postmenopáusicas. Afecta al 4% de los hombres y al 2% de las mujeres entre 30 y 60 años de edad. Bixler y cols., encontraron una prevalencia de SAOS en el 3.9% de los hombres y en el 1.2% de mujeres. El 20% de los hombres y el 30% de las mujeres sufren de obesidad. Por estadísticas mundiales se sabe que 3 a 5% de los obesos son mórbidos, con un Índice de Masa Corporal (IMC) mayor a 40 kg/m2. Entre 25 y 40% de los obesos mórbidos sufren alteraciones respiratorias significativas. Fisiopatogenía La mayoría de los pacientes con SAHOS presentan malformaciones maxilofaciales, (micrognatia o retrognatia), obstrucción de la vía aerodigestiva. Deformidad rinoseptal, Hipertrofia turbinal, Rinitis, Pólipos, Tumores, Hipertrofia adenoamigdalina, Macroglosia, Hipertrofia de la úvula; Obesidad, Hipotiroidismo, Cifoescoliosis y Acromegalia. La obesidad es causante de polipnea, disnea, esfuerzo ventilatorio, disminución de la capacidad respiratoria funcional, por el alto volumen de reservaba expiratorio; se asocia al cierre de unidades pulmonares periféricas, en especial en decúbito supino. Hipoventilación, somnolencia y retención de dióxido de carbono (pCO2 > 48 mm/Hg), “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. disminución de la distensibilidad de la pared torácica y aumento del trabajo respiratorio. Como consecuencia surgen hipoxia, hipertensión pulmonar, policitemia e insuficiencia cardiopulmonar; cuadro que mejora al disminuirse el peso corporal. Durante cada episodio apneico, el esfuerzo inspiratorio contra una vía aérea ocluida, se acompaña de aumento de la presión negativa del espacio pleural. A medida que la apnea persiste, la hipoxemia y la hipercapnia son más intensas, causando vasoconstricción pulmonar e hipertensión pulmonar transitoria. El estimulo del sistema simpático provoca HAS y aumento de la presión sistólica. La hipoxia y su subsecuente re-oxigenación, durante la noche, provoca cambios en la reperfucion, con producción de radicales libres, elevación de los títulos de citocinas inflamatorias, resistencia a la insulina, factor de necrosis tumoral (TNF- ), e interleucina-6 (IL-6). Cintra confirmo el papel del tabaquismo, hipercolesterolemia (LDL elevado y HDL bajos). DMNID, HAS, historia familiar, obesidad, inactividad física, síndrome metabólico, consumo de alcohol e incremento en la mortalidad de origen cardiovascular. Cuadro clínico: Los síntomas inician insidiosamente, presentes durante años antes de que el paciente decida buscar atención médica: ronquido, apneas, sueño inestable, cefalea matutina, incoordinación motora somnolencia diurna, (90 % de pacientes) alteraciones del talante y cognoscitivas; con repercusión psico-social y laboral. (Martínez). Algunas personas a menudo no se dan cuenta de ello excepto por síntomas prodrómicos, como cefalea matutina, sequedad orofaríngea, fatiga e irritabilidad. “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. Es necesario asentar, peso, talla, IMC, tensión arterial, perímetro cervical (> 44,5 cm. se asocia a SAHOS). Exploración de la vía aérea superior, simple y armada, anterior y posterior con nasofibroscopia. Diagnostico. El diagnostico se debe complementar con estudios básicos de laboratorio: biometría hemática completa, perfil tiroideo. Estudios de gabinete como radiografía de tórax AP y lateral, electrocardiograma (ECG), espirometría. Los médicos de atención primaria, los neumólogos, los neurólogos, los otorrinolaringólogos y otros médicos especialistas, deben intervenir en la realización de un diagnostico definitivo y en el establecimiento de un tratamiento. Los criterios diagnósticos del SAHOS, establecidos por consenso, exigen una sospecha clínica basada en la presencia de síntomas y una confirmación diagnóstica que se realiza mediante estudios del sueño. Una vez identificado al paciente con sospecha de SAHOS, este debe ser confirmado por medio de la polisomnografía durante el sueño (PSG), que consiste en el registro de parámetros fisiológicos, como electroencefalograma, electro-oculografía, electromiografía submentoniana y tibial, oximetría-capnometría, flujo aéreo oro-nasal, ronquido, movimientos torácicos, abdominales y electrocardiografía. Estos datos permiten afirmar el diagnóstico, aclarar de origen central o periférico y la valoración de la repercusión de las apneas e hipopneas sobre la función cardiorrespiratoria y la organización del sueño. “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. Complicaciones Las complicaciones circulatorias constituyen aumento en el volumen sanguíneo pulmonar, alto gasto cardiaco y elevación de la presión ventricular izquierda y del final de la diástole. Los pacientes obesos generalmente desarrollan hipoventilación y SAHOS con pobre respuesta compensatoria a la hipoxia e hipercapnea, resultando en hipoxemia, hipertensión pulmonar, astenia y adinamia progresiva, disnea y disminución a la tolerancia al ejercicio, disminución de la masa muscular y dolor articular. Complicaciones cardiovasculares Hipertensión arterial, arritmias cardiacas, coronopatia isquemica con la consecuente miocardiopatia isquemica, degenerando en insuficiencia cardiaca. SAHOS contribuye a la cardiopatía isquemica a través de varios mecanismos, como HAS y agregación plaquetaría. El gasto sanguíneo cerebral disminuye con cada evento de apnea, por la disminución en el gasto cardiaco, predisponiendo a sufrir eventos isquémicos en miocardio. Hipertensión El SAHOS es un factor desencadenante de HAS 42-47 con una prevalecía del 40 al 90%. Arritmias cardiacas Los pacientes con este síndrome experimentan arritmias ventriculares durante el sueño68, (0-15%). Guilleminault et al encontraron pausas sinusales (> 2.5 segundos), bloqueo atrioventricular de segundo grado, bradicardia sinusal en el 11%, 8%, y 7% de los pacientes, respectivamente “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. Diagnóstico diferencial El Síndrome de Prader-Willi (SPW), se caracteriza clínicamente por obesidad (después de los 2 años de edad), hipotonía, retraso mental, baja talla, manos y pies pequeños e hipogonadismo, somnolencia diurna y alteración del ciclo circadiano y del movimiento ocular rápido (REM) durante el sueño. Trastornos respiratorios durante el sueño que comprenden desde ronquidos hasta la apnea. (Clift–Nixon). Generalmente los pacientes con SPW son remitidos al endocrinólogo pediatra por obesidad. La obesidad es el factor más fuertemente asociado en los pacientes con SPW, pero también pudiera ser el elemento que aporta una mayor confusión para el análisis, ya que se ha observado que las anomalías cardiorrespiratorias en pacientes obesos con SPW no implican necesariamente una asociación entre la apnea nocturna y la morbilidad cardiorrespiratoria. Existen otros elementos como la enfermedad pulmonar obstructiva crónica asociada a la obesidad, que en ocasiones se subestima. (Fung) Otros diagnósticos diferenciales, incluyen, Insuficiencia cardiaca, asma bronquial, reflujo gastroesofágico, reflujo faringolaringeo, hipersomnia, síndrome de hipoventilación alveolar. Trastornos neurológicos, narcolepsia, síndrome de “piernas inquietas”, mioclonías, farmacoterapia lícita o ilícita, intoxicaciones (ej. etílica) “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. Tratamiento El tratamiento debe estar basado en datos obtenidos de la PSG, la magnitud de las complicaciones, la edad del paciente, su estado general de salud y su historia medica, la tolerancia a determinados medicamentos, procedimientos o terapias, expectativas para la trayectoria de la enfermedad y patología obstructiva ( Ej. deformación rinoseptal). El tratamiento se enfoca en dos aspectos: 1. Eliminar la obstrucción respiratoria completa o parcial (apnea o hipopnea) y la desaturación de oxigeno en la fase del sueño. 2. Lograr que el paciente duerma bien, mejorando su calidad de sueño y disminuyendo o eliminando los microdespertares (“arousals”). Tratamientos farmacológicos Generalmente los medicamentos no son eficaces en el tratamiento del SAHOS. La acetazolamida ha mostrado que reduce la frecuencia de apnea, pero no se asocia con mejorías en los síntomas, mal tolerado durante largos periodos. La progesterona, puede emplearse en casos de SAHOS asociados a hipercapnia diurna con o sin obesidad mórbida, su dosis habitual es de 20 microgramos cada 6 horas. Sin embargo, no hay ningún estudio con el suficiente número de casos que demuestre su eficacia a medio-largo plazo. La protiptilina, posee acción dilatadora sobre la vía aérea alta por su acción estimulante sobre la musculatura orofaríngea y suprime la fase REM del sueño. Estas propiedades permiten manejar casos leves de SAHOS, sobre todo si las apneas aparecen en fase REM, pero sus efectos anticolinérgicos limitan su beneficio. Ha demostrado producir mejorías en los síntomas pero no produce cambios en la frecuencia de apnea. “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. También se aconsejan medidas higiénico-dietéticas. o Evitar siestas prolongadas durante el día. o Practicar ejercicio físico de forma regular. o Acondicionar la habitación, ruidos, estímulos luminosos, temperaturas extremas. o Asociar la cama con el sueño: evitar ver la televisión, trabajar o cenar en la cama o Leer un poco o escuchar música. o Evitar cenas abundantes. o Ante la imposibilidad de conciliar el sueño, salir de la cama, hacer una actividad que distraiga y volver a la cama sólo si tiene sueño. o Perder peso. (incluso una perdida de tan solo un 10 por ciento del peso puede reducir el número de eventos de apnea en la mayoría de los pacientes) o Evitar tomar medicamentos relajantes (antidepresivos, ansiolíticos-sedantes, relajantes musculares, inductores del sueño) o No fumar. o Tratar todo trastorno que origine obstrucción nasal. o Dormir en decúbito lateral. o Adquirir una buena higiene del sueño o Evitar el consumo de alcohol y sustancias estimulantes y/o que contengan cafeína (café, te, cola). El tratamiento de elección del SAHOS, cuando no se encuentra una anomalía anatómica evidente susceptible de tratamiento quirúrgico, es la presión positiva continúa sobre la vía aérea (CPAP) administrada por vía nasal. (El uso del CPAP puede ayudar a disminuir la TA). En principio la terapéutica con CPAP no está indicada en la actualidad. Deberá individualizarse y aplicarse sólo en casos muy concretos y de un modo provisional. “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. Indicaciones de la CPAP IAH <30 sintomático IAH <30 con enfermedad cardiovascular asociada Es fundamental que el paciente sepa que la CPAP no es un tratamiento curativo EL CPAP mejora de forma significativa los síntomas de somnolencia diurna, funciones cognitivas, estado de ánimo y calidad de vida (Ballester). Mejora el rendimiento de los pacientes (American Academy of Otolaryngology−Head and Neck Surgery,) , y "normaliza" las cifras de riesgo de los conductores afectados por SAHS. Dispositivos intraorales Producen un adelantamiento mandibular aumentando el espacio retrofaríngeo. Pueden ser eficaces en SAHOS leve-moderado y constituyen una alternativa a considerar en pacientes que no toleren la administración de CPAP. En general son mal tolerados. Existen algunas evidencias que los aparatos linguales mejoran la somnolencia subjetiva y los índices de trastornos de la respiración durante el sueño sobre un control inactivo. Tanto la CPAP, como los aparatos linguales provocaron mejoras en los IAH en comparación con el valor inicial. La cirugía de la vía aérea superior y la maxilo-facial, está indicada cuando existen claras alteraciones anatómicas, de la vía aérodigestiva, tales como síndrome de obstrucción nasal, hipertrofia adenoamigdalina, cuerpos extraños, anomalías maxilo-faciales. Cuando no existan alteraciones de la vía aérodigestiva hay diversas opciones quirúrgicas: Uvulopalatofaringoplastia (UP3): consistente en la resección del tejido colapsable no muscular del paladar blando y tejidos orofaríngeos adyacentes, indicada en pacientes con valoración por Otorrinolaringología. “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. Cirugía de adelantamiento máxilo-mandibular y de avance geni-hioideo: eficaz en casos seleccionados. Traqueostomía: indicada en situaciones de gravedad extrema con fracaso y/o rechazo de cualquier otra medida terapéutica. Algunos pacientes pueden necesitar, además, otros tipos de cirugía Otorrinolaringológica: o Adenoamigdalectomia o Cirugías nasales como septoplastia o rinoseptoplastia, polipectomia, exéresis de tumores ya sea por vía endoscopia, vía Caldwell-Luc, vía Degloving; corrección de deformidades estructurales. o o La reconstrucción quirúrgica de las deformidades de la mandíbula Las intervenciones quirúrgicas para tratar la obesidad se recomiendan en ocasiones a pacientes con apnea del sueno que padecen obesidad patológica. “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. Bibliografía. 1. Guilleminault C. State of the art. Sleep and control of breathing. Chest 1978;73(2):293-9 2. Cutié O, Calvo E. Guías Clínicas 2005. Madrid;5 (29) 3. González P JF, Vera R. El aporte de la cirugía bariátrica en el tratamiento del síndrome de Pickwick. Rev. Chile Cir. 2003;55(1):9-13 4. Young T, Palta M, Dempsey J, Skatrud J, Weber S, Badr S. The occurrence of sleep-disordered breathing among middle-age adults. N Engl Med 1993; 328:1230-35. 5. Coma MJ, Terán J Santos, Alonso ML, Cordero J. La telemedicina en el diagnostico y tratamiento de los trastornos respiratorios del sueño. Unidad de Investigación y UTRS del Hospital General Yagüe. Burgos. España. Rev Electron Biomed / Electron J Biomed 2004;3:44-9. 6. Guilleminault C, Connolly SJ, Winkle RA. Cardiac arrhythmia and conduction disturbances during sleep in 400 patients with sleep apnea syndrome. Am J Cardiol 1983; 52: 490-4 7 Clift S, Dahlitz M, Parker JD. Sleep apnoea in the Prader-Willi syndrome. J Sleep Res 1994;3:121-6 8 Nixon GM, Brouillette RT. Sleep and breathing in Prader-Willi Syndrome. Pediatr Pulmonol 2002;34:209-17 9 Silvestri JM, Weese-Mayer DE. Respiratory control disorders in infancy and childhood. Curr Opin Pediatr 1996;8:216-20 “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. 10 Richards A, Quaghebeur G, Clift S, Holland A, Dahlitz M, Parkes D. The upper airway and sleep apnea in the Prader-Willi syndrome. Clin Otolaryngol 1994; 19:193-7 11 Beebe D, Gozal D. Obstructive sleep apnea and the prefrontal cortex: towards a comprehensive model linking nocturnal upper airway obstruction to daytime cognitive and behavioral deficits. J Sleep Res 2002;11:1-6 12 Nativio DG. The genetics, diagnosis, and management of Prader-Willi syndrome. J Pediatr Health Care 2002;16:298-303 13 Butler JV, Whittington JE, Holland AJ, Boer H, Clarke D, Webb T. Prevalence of, and risk factors for physical ill-health in people with Prader-Willi syndrome: a population-based study. Dev Med Child Neurol 2002;44:248-55 14 Holm VA, Cassidy SB, Butler MG, Hanchett JM, Greenswagg LR, Whittman BY. Prader-Willi syndrome: consensus diagnosis criteria. Pediatrics 1993;91:398-402 15 Richdale AL, Cotton S, Hibbit K. Sleep and behavior disturbance in Prader-Willi syndrome: a questionnaire study. J Intellect Disabil Res 1999;43:380-92 16 Laaban JP, Cassuto D, Orvoën-Frija E, Iiou MC. Cardiorrespiratory consequences of sleep apnoea syndrome in patients with massive obesity. Eur Respir J. 1998;11:20-7 17 High C. American Psychiatric Association, American Obesity Association, American Dietetic Association, American Public Health Association, National Institute for Health Care Management, American Academy of Child & Adolescent Psychiatry. The University of Texas School of Public Health, MayoClinic.com, At Health, Inc. Developed by Mental Health Association in Texas in collaboration with the Texas Department of State Health Services Border Children’s Mental Health Collaborative-El Paso, Texas; Youth Commission “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. 18 Ip MS, Lam B, Chan LY, Zheng L, Tsang KW, Fung PC. Circulation nitric oxide is suppressed in obstructive sleep apnea and is reversed by nasal continuous positive airway pressure. Am J Respir Crit Care Med 2000;162:2166-71 19 Fung KP, Lau SP, Chow OK, Lee J, Wong TW. Effects of overweight on lung function. Arch Dis Child 1990;65:512-5 19 Fung JW, Li TS, Choy DK, Yip GW, Ko FW, Sanderson JE. Severe obstructive sleep apnea is associated with left ventricular diastolic dysfunction. Chest. 2002;121:422-9 20 Lim J, Lasserson TJ, Fleetham J, Wright J. Aparatos bucales para la apnea obstructiva del sueño. En: La Bibliotheca Cochrane Plus; 2. Oxford Chichester, John Wiley & Sons, Ltd. 2005 21 Lyle DV. Obstructive Sleep apnea. Am Fam Physician 1999;15; 60(8):2279-86 22 Patel SR, White DP, Malhotra A, Stanchina ML, Ayas NT. Continuous positive airway pressure therapy for treating sleepiness in a diverse population with obstructive sleep apnea: results of a meta-analysis. Arch Intern Med 2003 Mar;163(5):565-71 23 American Academy of Otolaryngology−Head and Neck Surgery. Continuous Positive Airway Pressure (CPAP). AAO−HNS;2002 24 Marín JM, Arán X, Barbé F, Biurrum O, Fiz JA, Jiménez A, Canal JM, Terán J. Diagnóstico y tratamiento del síndrome de apnea obstructiva del sueño. En: Caminero JA, Fernández L. Recomendaciones SEPAR. Madrid; Doyma. 1998, 189-206 “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. 25 López A, Ruiz A, Morón A. Protocolo de actuación en el SAHS en el área 6 del IN SALUD. Área 6 de Madrid. Madrid: Gerencia de Atención Primaria/Clínica Puerta de Hierro 2004 26 Guilleminault C, Quera-Salva MA, Partinen M. Women and the obstructive apnea syndrome. Chest 1988;93: 104-109 27 Guilleminault C, Poyares D, Rosa A, Huang YS. Heart rate variability, sympathetic and vagal balance and EEG arousals in upper airway resistance and mild obstructive sleep apnea syndromes. Sleep Med. 2005; 6(5): 451-7 28 Guilleminault C, Kirisoglu C, Ohayon MM. C-reactive protein and sleep-disordered breathing. Sleep. 2004; 15; 27(8):1507-11 29 Ballester E, Badia JR, Carrasco E, de Pablo J, Fornas C, Rodríguez-Roisín R, Montserrat JM. Evidence of the effectiveness of continuous airway pressure in the treatment of sleep apnoea/hypopnoea syndrome. Am J Respir Crit Care Med 1999;159:495-501 30 Dumas F, Dalva P, Guilleminault C, Carvalho AC, Tufik S. Cardiovascular comorbidities and obstructive sleep apnea. Arq. Bras. Cardiol; São Paulo June 2006; 86(6) 31 Murray CJL, Lopez AD. The global burden of disease: a comprehensive assessment of mortality and disability from disease, injuries and risk factors in 1990 and projected to 2020. USA. Harvard School of Health; 1996 32 Avezum A, Piegas LS, Pereira JC. Fatores de risco associados com infarto agudo do miocárdio na região metropolitana de São Paulo. Uma região desenvolvida em um país em desenvolvimento. Arq Bras Cardiol. 2005; 84:206-13 “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. 33 Marin JM, Carrizo SJ, Vicente E, Agusti AGN. Long-term cardiovascular outcomes in men with obstructive sleep apnea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet. 2005; 365:1046-53 34 Kramer NR, Cook TE, Carlisle CC, Corwin RW, Millman RP. The role of the primary care physician in recognizing obstructive sleep apnea. Arch Intern Med. 1999; 159:965 35 Sleep-Related Breathing Disorders in Adults: Recommendations for syndrome definition and measurement techniques in clinical research. The report of an American Academy of Sleep Medicine Task Force. Sleep. 1999; 22:667-89 36 Vgontzas AN, Bixler EO, Chrousos GP. Sleep apnea is a manifestation of the metabolic syndrome. Sleep Med Rev. 2005;9(3):211-24 37 Vgontzas AN, Papanicolaou DA, Bixler EO, Kales A, Tyson K, Chrousos GP. Elevation of plasma cytokines in disorders of excessive daytime sleepiness: role of sleep disturbance and obesity. J Clin Endocrinol Metab. 1997; 82(5):1313-6 38 Fried SK, Bunkin DA, Greenberg AS. Omental and subcutaneous adipose tissues of obese subjects release interleukin-6: depot difference and regulation by glucocorticoid. J Clin Endocrinol Metab. 1998; 83(3):847-50 39 Vgontzas AN, Bixler EO, Chrousos GP. Metabolic disturbances in obesity versus sleep apnoea: the importance of visceral obesity and insulin resistance. J Intern Med. 2003; 254(1): 32-44 40 Arabi Y, Morgan BJ, Goodman B, Puleo DS, Xie A, Skatrud JB. Daytime blood pressure elevation after nocturnal hypoxia. J Appl Physiol. 1999; 87(2):689-98 “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. 41 Xie A, Skatrud JB, Puleo DS, Morgan BJ. Exposure to hypoxia produces longlasting sympathetic activation in humans. J Appl Physiol. 2001; 91(4): 1555-62 42 Belozeroff V, Berry RB, Khoo MC. Model-based assessment of autonomic control in obstructive sleep apnea syndrome. Sleep. 2003; 26(1): 65-73 43 Nieto FJ, Young TB, Lind BK, Shahar E, Samet JM, Redline S, et al. Association of sleep-disordered breathing, sleep apnea, and hypertension in a large community-based study. Sleep Heart Health Study. JAMA. 2000; 283(14): 182936 44 Peppard PE, Young T, Palta M, Skatrud J. Prospective study of the association between sleep-disordered breathing and hypertension. N Engl J Med. 2000; 342(19): 1378-84 45 Lavie P, Herer P, Hoffstein V. Obstructive sleep apnoea syndrome as a risk factor for hypertension: population study. B M J. 2000; 320(7233): 479-82 46 Silverberg DS, Oksenberg A, Iaina A. Sleep related breathing disorders are common contributing factors to the production of essential hypertension but are neglected, underdiagnosed, and undertreated. Am J Hypertens. 1997; 10(12 Pt 1): 1319-25 49 Fletcher EC. The relationship between systemic hypertension and obstructive sleep apnea: facts and theory. Am J Med. 1995; 98(2): 118-28 50 Hla KM, Skatrtud JB, Finn L, Palta M, Young T. The effect of correction of sleepdisordered breathing on BP in untreated hypertension. Chest. 2002; 122(4): 11112 “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C. 51 Logan AG, Tkacova R, Perlikowski SM, Leung RS, Tisler A, Floras JS, et al. Refractory hypertension and sleep apnoea: effect of CPAP on blood pressure and baroreflex. Eur Respir J. 2003; 21(2): 241-7 52 Hedner J, Darpo B, Ejnell H, Carlson J, Caidahl K. Reduction in sympathetic activity after long-term CPAP treatment in sleep apnoea cardiovascular implications. Eur Respir J 1995; 8: 222-9 53 Pepperell JC, Davies RJ, Stradling JR. Systemic hypertension and obstructive sleep apnoea. Sleep Med Rev. 2002; 6(3): 157-73 54 Pepin JL, Levy P. Pathophysiology of cardiovascular risk in sleep apnea syndrome (SAS). Rev Neurol. 2002;158: 785-97 55 Yokoe T, Minoguchi K, Matsuo H, Oda N, Minoguchi H, Yoshino G, et al. Elevated levels of C-reactive protein and interleukin-6 in patients with obstructive sleep apnea syndrome are decreased by nasal continuous positive airway pressure. Circulation. 2003; 107(8):1129-34 56 Kraiczi H, Caidahl K, Samuelsson A, Peker Y, Hedner J. Impairment of vascular endothelial function and left ventricular filling: association with the severity of apnea-induced hypoxemia during sleep. Chest. 2001; 119(4):1085-91 57 Shamsuzzaman AS, Gersh BJ, Somers VK. Obstructive sleep apnea: implications for cardiac and vascular disease. JAMA. 2003; 290(14):1906-14 58 Von Kanel R, Le DT, Nelesen RA, Mills PJ, Ancoli-Israel S, Dimsdale JE. The hypercoagulable state in sleep apnea is related to comorbid hypertension. J Hypertens. 2001; 19(8):1445-51 “Diplomado de Obesidad y Nutrición” Colegio Mexicano de Obesidad y Nutrición, A.C.