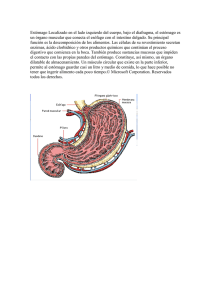
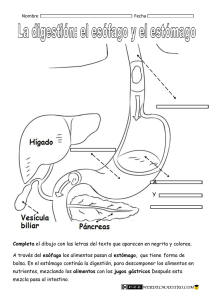
universidad regional autónoma de los andes “uniandes” facultad de
Anuncio

UNIVERSIDAD REGIONAL AUTÓNOMA DE LOS ANDES “UNIANDES” FACULTAD DE CIENCIAS MÉDICAS CARRERA DE MEDICINA PROYECTO DE INVESTIGACION PREVIO A LA OBTENCIÓN DEL TITULO DE MÉDICO CIRUJANO TEMA: FACTORES CLÍNICOS Y EPIDEMIOLÓGICOS DEL CÁNCER DE ESTÓMAGO EN PACIENTES ATENDIDOS EN EL CENTRO DE SALUD DEL CANTÓN QUERO, TUNGURAHUA. PERIODO 2010-2015. AUTORA: MARTÍNEZ SÁNCHEZ LETICIA MARICELA ASESOR: DR. VAYAS VALDIVIESO WALTER ALBERTO AMBATO – ECUADOR 2016 CERTIFICACIÓN DEL TUTOR Ambato, abril de 2016 Dra. Corona Gómez Armijos Rectora de Uniandes Presente, Estimada rectora, a través de la presente tengo a bien informarle que, en calidad de Tutor, he asesorado el desarrollo de la Tesis previa a la obtención del Título de Médico Cirujano titulada “Factores clínicos y epidemiológicos del cáncer de estómago en pacientes atendidos en el centro de salud del cantón Quero, Tungurahua. Período 2010-2015”, cuya autora es la señorita Leticia Maricela Martínez Sánchez, la cual reúne los requerimientos de orden teórico y metodológico, razón por la cual autorizo su presentación para el trámite legal correspondiente. Atentamente, __________________________ Dr. Walter Alberto Vayas Valdivieso Tutor de la tesis DECLARACIÓN DE AUTORÍA Ambato, abril de 2016 Dra. Corona Gómez Armijos Rectora de Uniandes Presente, Yo, Leticia Maricela Martínez Sánchez, declaro que soy el único autor de la tesis previa a la obtención del Título de Médico Cirujano titulada “Factores clínicos y epidemiológicos del cáncer de estómago en pacientes atendidos en el centro de salud del cantón Quero, Tungurahua. Período 2010-2015” y autorizo a la Universidad Regional Autónoma de los Andes, Uniandes, para que le dé a la misma el uso que estime pertinente. Para que así conste, firmo la presente, Atentamente, _____________________________ Leticia Maricela Martínez Sánchez Autora de la tesis DEDICATORIA Dedico este proyecto de tesis a Dios y a mis padres a mi esposo y de manera especial a mi Hija María de los Ángeles. A Dios porque ha estado conmigo a cada paso que doy, cuidándome y dándome fortaleza para continuar, a mis padres, quienes a lo largo de mi vida han velado por mi bienestar y educación siendo mi apoyo en todo momento, a mi esposo porque es el pilar fundamental de mi vida depositando su entera confianza en cada reto que se me presentaba sin dudar ni un solo momento en mi inteligencia y capacidad. Es por ellos que soy lo que soy ahora. Los amo con mi vida. LETICIA MARICELA MARTÍNEZ SÁNCHEZ AGRADECIMIENTO En primer lugar a Dios por haberme guiado por el camino de la felicidad hasta ahora; en segundo lugar a cada uno de los que son parte de mi familia a mi PADRE Luis Martínez, mi MADRE Gladys Sánchez, mi ESPOSO Byron Tustón, a mis hermanas Elena, Cecilia y Paulina; por siempre haberme dado su fuerza y apoyo incondicional que me han ayudado y llevado hasta donde estoy ahora. Por último a mis compañeros y amigos de tesis porque en esta armonía grupal lo hemos logrado y a mi asesor de tesis quién nos ayudó en todo momento, Dr. Walter Vayas. ÍNDICE PORTADA CERTIFICACIÓN DEL TUTOR DECLARACIÓN DE AUTORÍA DEDICATORIA AGRADECIMIENTO INDICE RESUMEN EJECUTIVO ABSTRACT INTRODUCCIÓN ................................................................................................... 1 1. ANTECEDENTES DE LA INVESTIGACIÓN ................................................... 1 2. PLANTEAMIENTO DEL PROBLEMA ............................................................. 4 3. FORMULACIÓN DEL PROBLEMA CIENTIFICO ............................................ 6 4. DELIMITACIÓN DEL PROBLEMA .................................................................. 7 5. OBJETO DE INVESTIGACIÓN Y CAMPO DE ACCIÓN ................................. 7 5.1 Objeto de investigación ................................................................................ 7 5.2 Campo de acción ......................................................................................... 7 6. IDENTIFICACIÓN DE LA LÍNEA DE INVESTIGACIÓN ..................................... 7 7. OBJETIVOS....................................................................................................... 7 7.1. Objetivo General ......................................................................................... 7 7.2. Objetivos Específicos .................................................................................. 7 6. PREGUNTAS CIENTÍFICAS .......................................................................... 8 9. JUSTIFICACIÓN DEL TEMA ............................................................................. 8 10. BREVE EXPLICACIÓN DE LA METODOLOGÍA INVESTIGATIVA EMPLEADA .............................................................................................................................. 8 7. RESUMEN DE LA ESTRUCTURA DE LA TESIS ........................................... 9 12. NOVEDAD CIENTFICA ................................................................................. 10 13. APORTE TEÓRICO ....................................................................................... 10 14. SIGNIFICACIÓN PRÁCTICA ......................................................................... 10 CAPÍTULO I ......................................................................................................... 11 MARCO TEÓRICO .............................................................................................. 11 1.1. PACIENTES Y ENFERMEDADES ............................................................ 11 1.1.1 Concepto de paciente y su clasificación ............................................... 11 1.1.2 Concepto de enfermedad ..................................................................... 13 1.1.3. Clasificación CIE-10 del cáncer gástrico ............................................. 13 1.2. Vivir con cáncer ......................................................................................... 13 1.3. Concepto de atención primaria de salud .................................................... 18 1.4. Acciones de prevención y promoción de salud .......................................... 18 1.4.1. Campañas de prevención ................................................................... 21 1.5. Principales funciones de los centros de atención primaria de salud en ..... 22 comunidades rurales ........................................................................................ 22 1.6. Morfofisiología gástrica .............................................................................. 24 1.7 Cáncer de estómago .................................................................................. 25 1.7.1. Definición de cáncer gástrico .............................................................. 25 1.7.2 Epidemiologia y factores de riesgo ...................................................... 26 1.7.3 Clasificaciones del cáncer gástrico ...................................................... 30 1.7.4. Cuadro clínico y diagnóstico ............................................................... 33 1.7.5. Prevención y tratamiento .................................................................... 40 Conclusiones parciales del capítulo ..................................................................... 40 CAPÍTULO II ........................................................................................................ 41 MARCO METODOLÓGICO Y EVALUACIÓN DE LOS RESULTADOS. .............. 41 Operacionalización de las variables de la investigación ................................... 43 Conclusiones parciales del capítulo ..................................................................... 71 CAPÍTULO III ....................................................................................................... 73 PLANTEAMIENTO DE LA PROPUESTA............................................................. 73 Objetivo de la propuesta ................................................................................... 73 Beneficiarios de la propuesta ........................................................................... 73 Desarrollo de la propuesta ............................................................................... 73 Guía de Prevención del Cáncer Gástrico y Educación para la Salud ................... 75 CONCLUSIONES GENERALES.......................................................................... 78 RECOMENDACIONES ........................................................................................ 79 BIBLIOGRAFÍA ANEXOS RESUMEN EJECUTIVO Cada año se diagnostican más de 85.000 nuevos casos de cáncer de estómago y 65.000 muertes por ésta afección en las Américas, dentro de los que se destaca Ecuador como uno de los países de mayor incidencia y mortalidad. Se realizó un estudio observacional descriptivo, transversal y retrospectivo, perteneciente a la línea de investigación de Salud Pública, sublínea enfermedades no transmisibles y crónicas degenerativas. El universo lo constituyeron todos los pacientes con diagnóstico conocido de cáncer gástrico del cantón Quero, provincia Tungurahua y la muestra se conformó con la totalidad de pacientes que fueron atendidos por esta condición en el Centro de Salud de dicho cantón durante el quinquenio 20102015. Predominaron los hombres de hasta 60 años con estado nutricional normal. Los principales factores de riesgo observados fueron alto consumo de tabaco, alcohol, alimentos ahumados, embutidos y conservados, antecedentes familiares de poliposis o cáncer intestinal, antecedentes personales de gastritis e infección con Helicobacter Pylori, desconocimiento de la enfermedad y poco interés por informarse. Se propuso una guía educativa de prevención del cáncer gástrico dirigida a toda la población del cantón Quero, provincia Tungurahua. Palabras claves: Cáncer gástrico, factores de riesgo de carcinoma gástrico ABSTRACT Each year more than 85,000 new cases of stomach cancer are diagnosed and this disease has caused 65,000 deaths in the America Continent. It is said that Ecuador stands out as one of the countries with the highest incidence mortality. A descriptive, cross-sectional and retrospective study in the stomach cancer has been done to a Public Health Center. This research for used on nontransmisible and chronic degenerative diseases. The universe taken into account in this research were all patients suffering from gastric cancer in the Quero Village, province of Tungurahua. Sample used contemplated all patients who had been treated in the Health Center during the period 2010-2015. The study was mainly made to men up to 60 years with normal nutritional status. The main risk factors detected were high consumption of snuff, alcohol, smoked foods, sausages and preserved food. It is also important to point out that the family background plays an important role when analyzing the mentioned disease. An educational guide on gastric cancer prevention has been designed to help entire population in the Quero Village due to the fact that there is little interest in preventing disease. Keywords: Gastric cancer, risk factors, gastric carcinoma, health Center INTRODUCCIÓN 1. ANTECEDENTES DE LA INVESTIGACIÓN El cáncer es tan viejo como la humanidad, habiéndose encontrado evidencias del mismo en tumores óseos fosilizados de momias egipcias. Aunque la palabra “cáncer” no era usada, la descripción más Antigua de la enfermedad data de alrededor de 3000 años AC, al aparecer el papiro de Edward Smith la descripción de 8 casos de tumores o úlceras de las mamas que fueron tratadas con cauterización, añadiendo que no hay tratamiento para tal condición (1). El término “cáncer” fue empleado por primera vez por médico griego Hipócrates, considerado el padre de la medicina, el cual uso los términos “carcinos” y “carcinoma”, que en griego significan “cangrejo”, para describir tumores ulcerosos y no ulcerosos, cuyos patrones de crecimiento recordaban la forma de un cangrejo. Posteriormente, el médico romano Celsio tradujo el término griego como “cáncer”, la palabra latina para cangrejo. Fue Galeno, otro médico romano, quien usó el término “oncos” (inflamación en griego) para describir tumores, convirtiéndose posteriormente en la raíz de la palabra oncología o estudio de los cánceres. Fue el cirujano escocés John Hunter, en el siglo XVIII, quien sugirió que algunos cánceres podrían ser curados con cirugía y no fue hasta prácticamente un siglo después, con el desarrollo de los métodos anestésicos, que la resección quirúrgica de cánceres que no invadían órganos vecinos se convirtió en una práctica regular. Los pioneros en la cirugía fueron Billroth en Alemania, Hardy en Londres y Halsted en Baltimore. Guillermo Stewart Halsted, profesor de cirugía de la universidad del John Hopkins, desarrolló la mastectomía radical, que no se modificado hasta la fecha. La idea que los cánceres se extendieran vía circulación de la sangre se le atribuye a Stephen Paget, cirujano inglés, esta comprensión de la metástasis se convirtió en un elemento clave en el reconocimiento de los 1 pacientes que pudieron y no pudieron beneficiarse de la cirugía, otra arma terapéutica se desarrolló en 1896 por un profesor alemán de la física, Roentgen de Wilhelm, descubrió las propiedades de los rayos X, la radioterapia comenzó con radio descubierto por Marie Curie, polaca que trabajaba en la Universidad de la Sorbona, París, y que curiosamente murió de leucemia. El descubrimiento de la quimioterapia fue casual en la Segunda Guerra Mundial al exponerse los soldados al gas mostaza que se convirtió en el primer medicamento para los cánceres ganglionares llamados linfomas. El cáncer de estómago o cáncer gástrico es un tipo de crecimiento celular maligno producido con capacidad de invasión y destrucción de otros tejidos y órganos, en particular el esófago y el intestino delgado. En las formas metastásicas, las células tumorales pueden infiltrar los vasos linfáticos de los tejidos, diseminarse a los ganglios linfáticos y, sobrepasando esta barrera, penetrar en la circulación sanguínea, después de lo cual queda abierto virtualmente el camino a cualquier órgano del cuerpo. A pesar de la disminución de la incidencia del carcinoma en los últimos años, esta enfermedad todavía es una de las causas de muerte más comunes por cáncer en todo el mundo, con cerca de un millón de muertes anualmente (1-5). El cáncer de estómago afecta principalmente a las personas de edad avanzada. Al momento del diagnóstico, la edad promedio de las personas es de 69 años. Alrededor de 6 de cada 10 personas diagnosticas con cáncer de estómago cada año tienen 65 años o más. El riesgo promedio de que una persona padecerá cáncer de estómago en el transcurso de su vida es de alrededor de 1 en 111. El riesgo es ligeramente mayor en los hombres que en las mujeres, y también puede ser afectado por un número de otros factores (6). Se ha señalado que el hecho de que las poblaciones que migran de un país con alta incidencia, a otro donde es baja, muestren a partir de la segunda generación, un descenso significativo de casos de cáncer gástrico, sugiere que la causa puede ser ambiental, y que existe un factor causal en los hábitos alimenticios. A pesar de que las diferencias internacionales en la incidencia son muy 2 pronunciadas, las variaciones con respecto al sexo son escasas, siguiendo una proporción de dos veces más frecuentes en los hombres que en las mujeres. La mayor incidencia por edad se encuentra entre los 50 y 70 años, con una incidencia máxima alrededor de los 60 años, siendo infrecuente antes de los 30 años (7, 8). Hasta finales de la década de los 30, el cáncer de estómago fue la causa principal de muertes por cáncer en los Estados Unidos. Actualmente, el cáncer de estómago está bien abajo en esta lista. No se conocen completamente las razones para este descenso, pero puede estar relacionado con el uso aumentado de la refrigeración para guardar alimentos. Esto causó una mayor disponibilidad de frutas y vegetales frescos y una disminución en el uso de alimentos salados y ahumados. Algunos médicos creen que el descenso también puede estar asociado con el uso frecuente de antibióticos para tratar las infecciones. Los antibióticos pueden destruir la bacteria llamada Helicobacter pylori (Hp), la cual se cree es una causa importante de cáncer de estómago. No obstante a su alta incidencia y mortalidad en el mundo, el cáncer gástrico ha sido poco estudiado comparado con otras patologías neoplásicas, y los resultados de las terapias siguen siendo pobres. Sin embargo, en la última década se han publicado los resultados de varios estudios que han demostrado un impacto favorable en sobrevida libre de progresión y en sobrevida global con terapias peri-operatorias y paliativas (10-13). El cáncer de estómago puede ser difícil de detectar en sus inicios ya que a menudo no hay síntomas, y en muchos casos, el cáncer se ha extendido antes de que se encuentre. Cuando ocurren los síntomas, son a menudo tan discretos que la persona no se preocupa por ellos. Unos de los aspectos claves para el éxito en el tratamiento del cáncer gástrico, es su detección precoz, porque si se diagnostica en estadios tempranos, es curable en más de 50% de los pacientes. Sin embargo, en la actualidad, la enfermedad en estadio inicial solo representa de 10 a 20% de todos los casos diagnosticados en los Estados Unidos. El resto de los pacientes padece enfermedad metastásica. Aún con enfermedad localizada, la 3 tasa de sobrevida a cinco años en pacientes con cáncer del estómago proximal solo alcanza entre 10 y 15%. Aunque el tratamiento de pacientes con cáncer gástrico diseminado puede lograr la paliación de los síntomas y cierta prolongación de la sobrevida, las remisiones prolongadas son poco frecuentes (12). 2. PLANTEAMIENTO DEL PROBLEMA Según reportes de la Organización Mundial de la Salud, a nivel mundial la mortalidad por cáncer aumentará un 45% entre 2007 y 2030, cuando pasará de 7,9 millones a 11,5 millones de defunciones, debido en parte al crecimiento demográfico y al envejecimiento de la población (10, 11). A nivel mundial, el cáncer gástrico es la cuarta causa de casos nuevos de cáncer por año, con aproximadamente 945,000 casos nuevos. La incidencia es muy variable en todos los países. Por ejemplo, reportes en USA hablan de una incidencia de 11.1; en Inglaterra la incidencia es de 22.1 y en Japón la incidencia alcanza 100.2 casos por 100,000 habitantes. Estos datos demuestran la gran variabilidad que existe entre distintas regiones con el paso del tiempo. Cada año se producen más de 85.000 nuevos casos de cáncer de estómago y 65.000 muertes por éste tipo de cáncer en las Américas, estimándose según proyecciones, que en el año 2030 se presentarán más de 138.000 casos nuevos y 107.000 muertes por cáncer de estómago en la región. El 60% de los nuevos casos y muertes por cáncer de estómago en las Américas se presentan en hombres, destacándose en Latinoamérica, Chile, Costa Rica y Ecuador por su mortalidad de más de 40 por 100,000 habitantes, mientras que Argentina, Cuba y Puerto Rico presentan tasas de mortalidad menores a la media latinoamericana. La mortalidad por cáncer gástrico en México alcanzó 5 por 100,000 habitantes, consolidándose como el tumor digestivo maligno más frecuente, con un 56% de incidencia en hombres y 44% en mujeres. 4 La Sociedad Ecuatoriana de Gastroenterología, en un estudio hecho en 2011, determinó que, por cada 100.000 habitantes mayores de 20 años, 30 mueren a causa de cáncer gástrico en Ecuador. Según un estudio de la Sociedad de Lucha Contra el Cáncer, SOLCA, entre 2004 y 2011 se detectaron 6.855 casos de cáncer gástrico, de los cuales el 59,6 por ciento corresponden a las mujeres y el 40,4 por ciento a hombres. Ecuador ocupa el primer lugar en incidencia en cáncer gástrico en Sudamérica, con una incidencia de 19.8% en mujeres, y una mortalidad masculina del 24.1% (14). En el año 2010 se produjeron en el país 57.940 defunciones es, de ellas el 2.8% correspondieron a cáncer gástrico. Este tumor ocupa el primer lugar en mortalidad entre todos los cánceres tanto en hombres como en mujeres. Su tasa de mortalidad se ha mantenido estable en los últimos 20 años (11.4 x 100.000 en 1980 y 11.9 en el 2010) mientras en los países desarrollados la tendencia es decreciente. De acuerdo a los reportes de la Dirección de Estadísticas del Ministerio de Salud Pública y el Instituto Nacional de Estadísticas y Censos (INEC), en el año 2006 se reportaron 728 pacientes con cáncer de estómago y en el 2010 fueron 679. Según la misma fuente, el cáncer gástrico ocupa el décimo segundo lugar entre las causas de mortalidad del Ecuador, con un estimado de 1567 defunciones por cada 100.000 habitantes (14-16). Tungurahua está entre las principales provincias del Ecuador con mayor incidencia por cada 100.000 habitantes de cáncer gástrico. En un estudio que abarcó el período de 1996 al 2000, se captaron y registraron 540 casos nuevos de cáncer en Tungurahua; 297 hombres y 243 mujeres: la edad promedio fue 66.9 años (rango: 17-98 años); la incidencia mayor entre los 70-74 años. El 56% de los casos fueron diagnosticados en Ambato; el 35% se presentó en agricultores (tasa 60.7 x 100,000), el resto en jubilados y trabajadores de servicios. El 17.7% de los tumores se localizaron en antro y píloro. En todos los casos el diagnóstico fue tardío (etapa III-IV). Estudios en la provincia de Tungurahua, hace referencia a que en esta provincia la mortalidad por cáncer gástrico se ha mantenido constantemente elevada desde 5 hace 30 años, ubicándose en tercer lugar entre las provincias del Ecuador, con una tasa de mortalidad de 23.1 x 100.000 habitantes, que duplica la tasa de mortalidad nacional por esta causa (12.6 x 100.000 habitantes), con una tendencia al incremento, pues se ha elevado de 11 x 100.000 Habitantes en 1965, a 23.1 x 100.000 en 1995 (7). En un estudio llevado a cabo en el cantón Quero en 1995, en el que se exploró una muestra de 429 sujetos mayores de 35 años mediante una encuesta socio económica, un estudio endoscópico y un estudio histopatológico de muestra de tejido gástrico previa prueba rápida de Ureasa para detección de Hp, se observó un 21.2% de antecedentes familiares de muerte por neoplasias malignas del estómago. La prevalencia de infección por Hp detectada por test de Ureasa fue del 95.9% entre los sujetos sometidos a endoscopia (205 personas). La prevalencia de lesiones premalignas fue de 20.2% (gastritis crónica atrófica, metaplasia intestinal, pólipos). En general se observa un alto consumo de carnes insuficientemente cocidas, y embutidos de preparación casera. La conservación de los alimentos se realizaba a temperatura ambiente, lo que debe ser tomado en cuenta por las observaciones de ocurrencia de procesos de descomposición de los alimentos y formación de radicales oxidantes principalmente nitrosoamidas, a temperaturas superiores de 2 grados centígrados (29). Todos estos elementos, sumado a la ausencia de publicaciones recientes sobre el cáncer en general y el carcinoma gástrico en particular en el cantón Quero, fueron la fuente de motivación para la realización del presente estudio. 3. FORMULACIÓN DEL PROBLEMA CIENTIFICO ¿Cuáles son los factores clínicos y epidemiológicos que influyen en la aparición de cáncer de estómago en los pacientes atendidos en el centro de salud del Cantón Quero, Tungurahua Periodo 2010-2015? 6 4. DELIMITACIÓN DEL PROBLEMA La investigación se llevó a cabo en el Centro de Salud del cantón Quero, provincia de Tungurahua y abarcó el quinquenio 2010-2015. 5. OBJETO DE INVESTIGACIÓN Y CAMPO DE ACCIÓN 5.1 Objeto de investigación Pacientes con diagnóstico de cáncer gástrico atendidos en Centro de Salud del Cantón Quero 5.2 Campo de acción Factores de riesgos clínicos y epidemiológicos del cáncer de Estómago. 6. IDENTIFICACIÓN DE LA LÍNEA DE INVESTIGACIÓN Línea de investigación: Salud Pública Sublínea: Enfermedades no transmisibles y crónicas degenerativas 7. OBJETIVOS 7.1. Objetivo General Determinar los factores de riesgo clínicos y epidemiológicos del cáncer de estómago para diseñar un programa de prevención y diagnóstico precoz de esta afección en el cantón Quero, provincia Tungurahua. 7.2. Objetivos Específicos Fundamentar teóricamente el cáncer de estómago, sus factores de riesgo y sus medidas de prevención. Caracterizar clínica y epidemiológicamente a los pacientes portadores de cáncer gástrico que reciben atención médica en el Centro de Salud de Quero Evaluar el nivel de conocimientos que tenían estos pacientes sobre los factores de riesgo del cáncer gástrico antes del diagnóstico 7 Identificar las principales medidas a aplicarse para la prevención y detección precoz del cáncer gástrico en Quero. 6. PREGUNTAS CIENTÍFICAS ¿Cuáles son los factores de riesgo que inciden en los pacientes con cáncer de estómago en el cantón Quero? ¿Qué nivel de conocimiento sobre los factores de riesgo y los síntomas del cáncer gástrico tenían estos pacientes antes del diagnóstico? ¿Qué medidas pueden tomarse para prevenir y diagnosticar precozmente el cáncer gástrico en el Centro de Salud del cantón Quero? 9. JUSTIFICACIÓN DEL TEMA Esta investigación resultó conveniente ya que permitió evaluar los principales elementos clínicos y epidemiológicos asociados al cáncer gástrico en pacientes del cantón Quero, dónde se ha reportado una alta incidencia de esta afección en el pasado. Presentó gran relevancia social e implicación práctica ya que sirvió de punto de partida para trazar estrategias de prevención y diagnóstico precoz del cáncer gástrico en el cantón Quero. Por otra parte, al no existir publicadas investigaciones recientes sobre esta importante temática en este centro de salud, le aporta un gran valor teórico a la investigación. 10. BREVE EXPLICACIÓN DE LA METODOLOGÍA INVESTIGATIVA EMPLEADA Se realizó un estudio observacional descriptivo, transversal y retrospectivo, perteneciente a la línea de investigación de Salud Pública, sublínea enfermedades no transmisibles y crónicas degenerativas. El universo de estudio fueron los pacientes con diagnóstico conocido de cáncer gástrico del cantón Quero, provincia Tungurahua y la muestra se conformó aleatoriamente con la 8 totalidad de pacientes que fueron atendidos por esta condición en dicha Institución, durante el período 2010-2015. En una primera etapa se consultó la bibliografía disponible sobre el tema de la investigación para obtener referentes teóricos actualizados sobre el tema. En un segundo momento se recolectaron los datos correspondientes a las variables a investigar revisando las historias clínicas de los pacientes y posteriormente se aplicó una encuesta a los mismos en visitas domiciliarias y el servicio de consulta externa. Posteriormente los datos obtenidos se depositaron en un formulario creado según la bibliografía consultada y los objetivos de la investigación, el cual se convirtió en la fuente primaria de información. El procesamiento estadístico de los datos se llevó a cabo empleando estadísticas descriptivas y distribuciones de frecuencia mediante fórmulas de un libro de Microsoft Excel. Los resultados se expusieron en tablas y gráficos. 7. RESUMEN DE LA ESTRUCTURA DE LA TESIS CAPÍTULO I. MARCO TEÓRICO 1.1. Pacientes y enfermedades 1.1.1 Concepto de paciente y su clasificación 1.1.2 Concepto de enfermedad 1.1.3. Clasificación CIE-10 del cáncer gástrico 1.2. Vivir con cáncer 1.3. Concepto de atención primaria de salud 1.4. Acciones de prevención y promoción de salud 1.4.1. Campañas de prevención 1.5. Principales funciones de los centros de atención primaria de salud en comunidades rurales 1.6. Morfofisiología gástrica 1.7 Cáncer de estómago 1.7.1 Definición de cáncer de estomago 1.7.2 Epidemiologia y factores de riesgo 1.7.3 Clasificaciones del cáncer gástrico 9 1.7.4 Cuadro clínico y diagnóstico 1.7.5. Prevención y tratamiento CAPÍTULO II. MARCO METODOLÓGICO Y EVALUACIÓN DE LOS RESULTADOS En este capítulo se expuso detalladamente la metodología investigativa empleada y se expusieron los resultados de la investigación CAPÍTULO III. PLANTEAMIENTO DE LA PROPUESTA En este capítulo se expuso y se describió la propuesta de la investigación. 12. NOVEDAD CIENTFICA De acuerdo al análisis de los factores de riesgo del cáncer gástrico que afectan a la población de Quero, se diseñó un programa de prevención y diagnóstico precoz, que constituye una herramienta novedosa para la prevención y el diagnóstico temprano del cáncer gástrico en el centro de salud del cantón Quero. 13. APORTE TEÓRICO Esta investigación aportará información nueva sobre los factores clínicos y epidemiológicos del cáncer gástricos en pacientes del cantón Quero, donde no se han publicados artículos recientes al respecto. Esto favorecerá al proceso prevención de cáncer gástrico mediante las acciones adecuadas en el centro de Salud de Quero. 14. SIGNIFICACIÓN PRÁCTICA Los resultados obtenidos en la investigación, servirá de base teórica para la aplicación práctica del programa de prevención y diagnóstico precoz del cáncer de estómago, que involucre a todos los sectores de la comunidad y al personal del Centro de Salud. Por otra parte, dotará a médicos, enfermeras, estudiantes de medicina e investigadores, de información actualizada y validada a nivel tanto nacional como internacional, que permitirá incrementar el conocimiento general sobre esta afección y facilitará las labores de prevención, diagnóstico y tratamiento. 10 CAPÍTULO I MARCO TEÓRICO 1.1. PACIENTES Y ENFERMEDADES 1.1.1 Concepto de paciente y su clasificación El paciente es aquella persona que sufre de dolor y malestar y que, por ende, solicita asistencia médica y está sometida a cuidados profesionales para la mejoría de su salud. La palabra paciente es de origen latín “patiens” que significa “sufriente” o “sufrido”. El individuo para adquirir la nominación de paciente debe pasar por una serie de etapas como: identificación de los síntomas, diagnóstico, tratamiento y resultado. De igual manera, el paciente posee una serie de derechos como: el derecho de ser informado de su enfermedad y posibles tratamientos para su cura, elegir al médico y a todo el equipo, recibir una asistencia médica eficaz y un trato digno por parte de los médicos y auxiliares. La palabra paciente se puede observar en diferentes contextos debido a la existencia de los diferentes tipos de pacientes. El paciente en estado crítico se caracteriza porque sus signos vitales no son estables y la muerte es un desenlace posible e inminente. El paciente paliativo indica que se encuentra en cuidados paliativos con el fin de buscar mejoría en enfermedades graves que ya no tienen cura posible. Los cuidados paliativos se presentan en enfermedades como: cáncer, sida, cardiopatía, demencia, entre otras. 11 El paciente en estado estuporoso identifica al individuo que presenta disminución en la lucidez mental y agilidad mental, pérdida de la agudeza mental y cambios en la consciencia. El paciente ambulatorio es el individuo que acude a un centro de salud con el fin de suministrar un tratamiento para la mejoría de la misma sin necesidad de ser internado o pasar la noche completa en el centro de salud u hospital. El paciente internado u hospitalizado es aquel que debe de pasar toda la noche o algunos días en el hospital debido al delicado estado de salud para el suministro de ciertos tratamientos y, en caso de ser necesario realizar una operación quirúrgica. El paciente cero indica a la primera persona confirmada de un nuevo virus o epidemia, se puede deducir que fue el primer infectado y debido a que posee el virus de forma más pura se puede hallar una cura o antivirus a la infección dada. El paciente geriátrico debe de cumplir con ciertas características como: ser mayor de 65 años, alto riesgo de dependencia, presencia de patología mental acompañante o predominante; los mismos son atendidos por un geriatra, persona especializada en prevenir, diagnosticar y tratar enfermedades en las personas de tercera edad, pueden ser vistas en su residencia u hospital. Actualmente, la palabra paciente se busca sustituir por usuario debido a su relación con la palabra paciencia. En virtud de ello, la palabra paciente se puede usar como adjetivo para señalar a una persona que actúa de manera relajada y tolerante. El término paciente es sinónimo de benévolo, pasivo, es por ello, que identifica a una persona que posee la capacidad de soportar algo o saber esperar, por ejemplo: un paciente puede esperar de forma paciente en el hospital por ser atendido por los médicos o enfermeros (30). 12 1.1.2 Concepto de enfermedad El término enfermedad proviene del latín infirmitas, que significa literalmente «falto de firmeza». La OMS define enfermedad como “Alteración o desviación del estado fisiológico en una o varias partes del cuerpo, por causas en general conocidas, manifestada por síntomas y signos característicos, y cuya evolución es más o menos previsible”. 1.1.3. Clasificación CIE-10 del cáncer gástrico En la clasificación internacional de las enfermedades CIE-10, el cáncer gástrico se codifica como C16 y sus variantes topográficas van desde C160 hasta C169. C160 Tumor maligno del cardias C161 Tumor maligno del fundus gástrico C162 Tumor maligno del cuerpo del estómago C163 Tumor maligno del antro pilórico C164 Tumor maligno del píloro C165 Tumor maligno de la curvatura menor del estómago, sin otra especificación C166 Tumor maligno de la curvatura mayor del estómago, sin otra especificación C168 Lesión de sitios contiguos del estómago C169 Tumor maligno del estómago, parte no especificada 1.2. Vivir con cáncer El cáncer es común. La mitad de todos los hombres y un tercio de las mujeres tendrán un diagnóstico de cáncer en su vida. Muchas personas con cáncer sobreviven. Millones de personas vivas hoy en día tienen historial de cáncer. Para la mayoría de las personas con cáncer, vivir con la enfermedad es el desafío más grande que jamás han enfrentado. Puede cambiar sus rutinas, roles y relaciones. Puede causar problemas de dinero y de trabajo. El tratamiento puede cambiar la forma en que se siente o su apariencia. Aprender más sobre las maneras en que puede ayudarse puede aliviar algunas de sus preocupaciones. El apoyo de los demás es importante. 13 Algunos pacientes que viven con cáncer tienen un grado bajo de sufrimiento y otros tienen grados alto de sufrimiento. El grado de sufrimiento varía desde la capacidad de adaptarse a vivir con un cáncer hasta padecer de un problema grave de salud mental como una depresión grave. Sin embargo, la mayoría de los pacientes con cáncer no muestran signos o síntomas de ningún problema específico de salud mental. Este sumario describe los grados menos graves de sufrimiento de los pacientes que viven con un cáncer: Adaptación normal: conducta por la que la persona realiza cambios en su vida para manejar una situación que causa tensión como, por ejemplo, un diagnóstico de cáncer. Cuando la persona tiene una adaptación normal, aprende correctamente a hacer frente al sufrimiento emocional y resuelve los problemas relacionados con el cáncer. Sufrimiento psicológico y social: afección por la que una persona tiene algunas dificultades para hacer cambios en su vida de modo de poder manejar una situación difícil como, por ejemplo, un diagnóstico de cáncer. Puede necesitar ayuda de un profesional para aprender nuevas habilidades para hacer frente a una dificultad. Trastorno de adaptación: afección por la que una persona tiene muchos problemas para hacer cambios en su vida a fin de poder manejar una situación difícil como, por ejemplo, un diagnóstico de cáncer. Se presentan síntomas tales como depresión, ansiedad u otros problemas emocionales, sociales o de comportamiento que empeoran la calidad de vida de la persona. Se pueden necesitar medicinas y ayuda de un profesional para hacer esos cambios. Trastorno de ansiedad: afección por la que una persona tiene un grado muy alto de ansiedad. Esto puede obedecer a una situación que causa tensión como, por ejemplo, un diagnóstico de cáncer o presentarse sin ninguna causa conocida. Los síntomas de un trastorno de ansiedad incluyen preocupación, miedo y pavor. Cuando los síntomas son graves, afectan la capacidad de una persona de tener una vida normal. Hay muchos tipos de trastornos de ansiedad: 14 Trastorno de ansiedad generalizada. Trastorno de pánico (afección que causa sentimientos súbitos de pánico). Agorafobia (miedo a los espacios abiertos o a las situaciones en las que puede ser difícil recibir ayuda en caso de ser necesario). Trastorno de ansiedad social: (miedo a situaciones sociales). Fobia específica (aversión a un objeto o situación específica). Trastorno obsesivo compulsivo. Trastorno por tensión postraumática. Casi la mitad de los pacientes con cáncer informan sentir mucho sufrimiento. Es más probable que los pacientes de cánceres de pulmón, páncreas y cerebro manifiesten sufrimiento pero, en general, el tipo de cáncer no determina una diferencia. Los factores que aumentan el riesgo de ansiedad y sufrimiento no siempre se relacionan con el cáncer. Los siguientes pueden ser factores de riesgo de grados altos de sufrimiento en los pacientes con cáncer: Dificultad para realizar las actividades de la vida diaria habituales. Síntomas físicos y efectos secundarios (como fatiga, náuseas y dolor). Problemas en el hogar. Depresión u otros problemas mentales o emocionales. Tener un grado más bajo de educación. Los pacientes encuentran que es más fácil adaptarse si pueden continuar con sus rutinas y trabajo habituales, seguir realizando actividades que les importan y hacer frente a la tensión en sus vidas. Hacer frente a situaciones difíciles es el uso de pensamientos y comportamientos para adaptarse a las situaciones que presenta la vida. La manera en que la gente hace frente a esas situaciones habitualmente se relaciona con las características de su personalidad (por ejemplo, si generalmente son optimistas o pesimistas, o son tímidos o sociables). Los métodos para hacer frente incluyen el uso de pensamientos o comportamientos en situaciones especiales. Por ejemplo, cambiar una rutina 15 diaria o un horario de trabajo para manejar los efectos secundarios del tratamiento del cáncer como mecanismo para hacer frente a una situación difícil. El uso de mecanismos para hacer frente a situaciones difíciles puede ayudar al paciente a lidiar con ciertos problemas, el sufrimiento emocional y el cáncer en su vida diaria. Los pacientes que se adaptan bien habitualmente participan mucho en hacer frente al cáncer. Ellos también continúan buscando el significado y lo que es importante en sus vidas. Los pacientes que no se adaptan bien se pueden distanciar de relaciones o situaciones, y se sienten sin esperanza. Se están realizando estudios para determinar el modo en que los diferentes tipos de métodos para hacer frente a situaciones difíciles afectan la calidad de vida de los sobrevivientes de cáncer. Todos los sobrevivientes de cáncer deben someterse a seguimiento. Saber qué esperar después del tratamiento del cáncer puede ayudarle a usted y a su familia a hacer planes, cambios de estilo de vida y tomar las decisiones importantes. Con frecuencia, el cáncer es una enfermedad de larga duración y las personas con esta enfermedad podrían recibir tratamiento durante muchos años. Algunas veces, aquellas personas cercanas apoyan mucho al paciente al principio, pero se alejan a medida que transcurren los meses o años que dura el tratamiento. Es comprensible llegar a sentirse mentalmente “desgastados” al estar apoyando a una persona con cáncer. Aun así, las personas con cáncer necesitan apoyo emocional durante toda la enfermedad. La mayoría de los supervivientes con cáncer vuelven a ser atendidos por sus médicos de atención primaria después del tratamiento. Es posible que su médico de atención primaria apenas conozca su experiencia con el cáncer, por lo que es esencial desarrollar un plan de seguimiento a largo plazo individualizado con el oncólogo antes de regresar a la atención primaria. Este plan debería incluir: El diagnóstico del cáncer 16 El tratamiento (incluido el momento de administración, la posología y la duración) Los posibles efectos secundarios del cáncer y del tratamiento Recomendaciones sobre la frecuencia de las visitas de seguimiento Tipos de pruebas que se realizarán durante las visitas Consejos para mantenerse sano y evitar las recidivas o los cánceres secundarios La mayoría de las directrices oficiales sobre el seguimiento se centran en los cinco primeros años de supervivencia. Las directrices para el seguimiento a largo plazo se basan en las opiniones fundamentadas de los oncólogos. (Hasta ahora, no hay estudios que demuestren formalmente que el seguimiento de estas directrices vaya a prolongar la vida de los supervivientes). Estas directrices recomiendan pruebas o procedimientos anuales para el seguimiento a largo plazo de cánceres concretos. El caso de los pacientes con cáncer en estadios terminales constituye un reto para los sistemas de salud, la familia y el propio paciente. Muchas veces no se sabe cómo actuar con estos pacientes que padecen enfermedades terminales o degenerativas, si sobreprotegiéndolos, o intentando que todo siga lo más normal posible. Las siguientes estrategias pueden ayudar a conocer las necesidades del paciente, facilitando la comunicación con el enfermo: Aliviar el dolor físico a toda costa. Ir con calma, dar tiempo al paciente para que asimile lo que implica la enfermedad que padece. Escuchar y compartir sus sentimientos y emociones. Intentar no interrumpir, a veces sólo necesita dar rienda suelta a sus emociones, no escuchar consejos o soluciones. No presuponer cómo pueden encontrarse y preguntarles cómo se les puede ayudar. 17 Respetar y tolerar los silencios. Respetar cuando no quiere hablar y estar disponible cuando desee hacerlo. Permitir el llanto. Facilita el desahogo. Evitar las frases hechas del tipo "ya verás como no es nada", "se positivo", "no puedes continuar así". Intentar permanecer tranquilo ante su irritación y esperar a que se le pase 1.3. Concepto de atención primaria de salud La atención primaria de salud es la asistencia sanitaria esencial accesible a todos los individuos y familias de la comunidad a través de medios aceptables para ellos, con su plena participación y a un costo asequible para la comunidad y el país. Es el núcleo del sistema de salud del país y forma parte integral del desarrollo socioeconómico general de la comunidad (33). Un sistema sanitario basado en la atención primaria de salud orienta sus estructuras y funciones hacia los valores de la equidad y la solidaridad social, y el derecho de todo ser humano a gozar del grado máximo de salud que se pueda lograr sin distinción de raza, religión, ideología política o condición económica o social. Los principios que se requieren para mantener un sistema de esta naturaleza son la capacidad para responder equitativa y eficientemente a las necesidades sanitarias de los ciudadanos, incluida la capacidad de vigilar el avance para el mejoramiento y la renovación continuos; la responsabilidad y obligación de los gobiernos de rendir cuentas; la sostenibilidad; la participación; la orientación hacia las normas más elevadas de calidad y seguridad; y la puesta en práctica de intervenciones intersectoriales (33). 1.4. Acciones de prevención y promoción de salud Desde la Conferencia Internacional sobre Atención Primaria de Salud, que se llevó a cabo en 1978 en Alma Ata, Rusia, las Conferencias Mundiales de Promoción de la Salud consecuentes, así como las resoluciones emitidas por la Organización Mundial de la Salud (OMS)/ Organización Panamericana de la 18 Salud (OPS) han marcado el camino y directrices sobre el desarrollo de Promoción de la Salud en el mundo (33). La prevención es sobre todo definida como la protección contra los riesgos y las amenazas del ambiente, lo que significa, inevitablemente la acción mancomunada de las Instituciones de Salud, de las comunidades, y de las personas que más que integrarlas, las instituyen. En la Primera Conferencia Internacional de Promoción de Salud, realizada en Ottawa en 1986 con el patrocinio de la OMS se señala que es necesario facilitar el proceso según el cual se puede movilizar "a la gente para aumentar su control sobre la salud y mejorarla…para alcanzar un estado adecuado de bienestar físico, mental y social… ser capaz de identificar y realizar sus aspiraciones, de satisfacer sus necesidades y de cambiar o adaptarse al medio ambiente". Para lograr verdaderamente esto es imprescindible comprender que el desarrollo de la Salud no se puede reducir a la lucha contra la enfermedad, a las prácticas clínicas tradicionales. La definición dada en la histórica Carta de Ottawa de 1986 dice que la promoción de la salud constituye un proceso político y social global que abarca no solamente las acciones dirigidas directamente a fortalecer las habilidades y capacidades de los individuos, sino también las dirigidas a modificar las condiciones sociales, ambientales y económicas, con el fin de mitigar su impacto en la salud pública e individual. La promoción de la salud es el proceso que permite a las personas incrementar su control sobre los determinantes de la salud y en consecuencia, mejorarla. Las áreas de acción que propone la Carta de Ottawa son: construir políticas públicas saludables, crear ambientes que favorezcan la salud, desarrollar habilidades personales, reforzar la acción comunitaria, reorientar los servicios de salud. En la Carta de Ottawa quedaron establecidas las cinco funciones básicas necesarias para producir salud: A) Desarrollar aptitudes personales para la salud La promoción de la salud proporciona la información y las herramientas necesarias para mejorar los conocimientos, habilidades y competencias 19 necesarias para la vida. Al hacerlo genera opciones para que la población ejerza un mayor control sobre su propia salud y sobre el ambiente, y para que utilice adecuadamente los servicios de salud. Además, ayuda a que las personas se preparen para las diferentes etapas de la vida y afronten con más recursos las enfermedades y lesiones, y sus secuelas. B) Desarrollar entornos favorables La promoción de la salud impulsa que las personas se protejan entre sí y cuiden su ambiente. Para ello estimula la creación de condiciones de trabajo y de vida gratificante, higiénica, segura y estimulante. Además, procura que la protección y conservación de los recursos naturales sea prioridad de todos. C) Reforzar la acción comunitaria La promoción de la salud impulsa la participación de la comunidad en el establecimiento de prioridades, toma de decisiones y elaboración y ejecución de acciones para alcanzar un mejor nivel de salud. Asimismo, fomenta el desarrollo de sistemas versátiles que refuercen la participación pública. D) Reorientar los servicios de salud La promoción de la salud impulsa que los servicios del sector salud trasciendan su función curativa y ejecuten acciones de promoción, incluyendo las de prevención específica. También contribuye a que los servicios médicos sean sensibles a las necesidades interculturales de los individuos, y las respeten. Asimismo, impulsa que los programas de formación profesional en salud incluyan disciplinas de promoción y que presten mayor atención a la investigación sanitaria. Por último, aspira a lograr que la promoción de la salud sea una responsabilidad compartida entre los individuos, los grupos comunitarios y los servicios de salud. E) Impulsar políticas públicas saludables La promoción de la salud coloca a la salud en la agenda de los tomadores de decisiones de todos los órdenes de gobierno y de todos los sectores públicos y privados. Al hacerlo busca sensibilizarlos hacia las consecuencias que sobre la salud tienen sus decisiones. También aspira a propiciar que una decisión sea más 20 fácil al tomar en cuenta que favorecerá a la salud. Así mismo promueve que todas las decisiones se inclinen por la creación de ambientes favorables y por formas de vida, estudio, trabajo y ocio que sean fuente de salud para la población. Del latín praeventio, prevención es la acción y efecto de prevenir (preparar con antelación lo necesario para un fin, anticiparse a una dificultad, prever un daño, avisar a alguien de algo). La prevención, por la tanto, es la disposición que se hace de forma anticipada para minimizar un riesgo. El objetivo de prevenir es lograr que un perjuicio eventual no se concrete. Esto se puede apreciar en los dichos populares “más vale prevenir que curar” y “mejor prevenir que curar”. Puesto en otras palabras, si una persona toma prevenciones para evitar enfermedades, minimizará las probabilidades de tener problemas de salud. Por lo tanto, es mejor invertir en prevención que en un tratamiento paliativo (33). 1.4.1. Campañas de prevención Las campañas de prevención sirven para transmitir al pueblo la preocupación que un grupo de personas con ciertos conocimientos específicos siente acerca de una problemática tal como una epidemia. Si bien la gente suele asociar los movimientos de este tipo con enfermedades, principalmente con el SIDA, también se llevan a cabo para generar conciencia acerca de otros temas, como por ejemplo las dislipidemias (33). La base de una campaña de prevención es conseguir que toda la población comprenda el mensaje y cambie los hábitos necesarios para mejorar su calidad de vida y la de aquellos que lo rodean. Por esa razón, es primordial utilizar un lenguaje accesible a todos, evitando los tecnicismos siempre que sea posible e intentando hacer hincapié en las consecuencias de no adoptar las propuestas (33). En los últimos años las definiciones de las Políticas de Salud han pasado a considerar especialmente el valor de las prácticas de Prevención. Estas han sido definidas sobre todo "como aquellas actividades que permiten a las personas tener estilos de vida saludables y faculta a las comunidades a crear y consolidar 21 ambientes donde se promueve la salud y se reduce los riesgos de enfermedad. La prevención implica desarrollar acciones anticipatorias. Los esfuerzos realizados para "anticipar" eventos, con el fin de promocionar el bienestar del ser humano y así evitar situaciones indeseables, son conocidos con el nombre de prevención. "Trabajar en prevención es trabajar con las causas reales o hipotéticas de algo que, de dejarlo pasar ahora para tratarlo después significaría un gran costo en dinero, en sufrimiento, en expectativas de vida". La prevención en el campo de la Salud implica una concepción científica de trabajo, no es sólo un modo de hacer, es un modo de pensar. Es también un modo de organizar y de actuar, un organizador imprescindible en la concepción de un Sistema de Salud. Un Sistema de Salud es más eficaz en la medida que prevenga más que cure; curar implica la inversión de una mayor cantidad de recursos económicos, de mayores gastos. Lo más importante es que es más eficaz porque, como se señala en el campo específico de las acciones profesionales del psicólogo, la prevención persigue "la identificación de aquellos factores que permitan promover la salud y la puesta en marcha de diferentes intervenciones, de cara a mantener saludables a las personas" y es precisamente el nivel de salud de las personas el máximo indicador de eficiencia de un sistema de salud cualquiera (33). 1.5. Principales funciones de los centros de atención primaria de salud en comunidades rurales Es el establecimiento de primer nivel de atención de salud y de complejidad orientado a brindar una atención integral de salud en sus componentes de Promoción, Prevención y Recuperación. Brinda consultas médicas ambulatorias diferenciadas en los consultorios de medicina, cirugía, ginecoobstetricia, pediatría y odontología. Además, debe contar con internamiento, prioritariamente en las zonas rurales y urbano-marginales. Por esta razón el Centro de Salud (CS), no se define por sus características técnicas, sino por su capacidad para establecer relaciones participativas con la población de la cual es responsable. En la visión de la OMS el CS es una 22 modalidad óptima de organización del primer nivel de atención en cualquier sistema racional de atención médica, público o privado. Los criterios para la planificación territorial de la distribución de los CS según el MSP de Ecuador incluyen las características demográficas y geográficas de la población, el perfil epidemiológico y el análisis de la oferta y la demanda. Teniendo en cuenta estos criterios de forma isócrona, el Centro de Salud de Quero, clasifica como un Centro de Salud Tipo C. Dentro de los principales objetivos del CS se encuentran: Brindar servicios de salud a través de una atención integral de salud. Desarrollar actividades preventivo-promocionales en la población a través de la participación de la comunidad organizada. Revalorar el sector salud en una localidad, mejorando la calidad de la atención médica. Desarrollar actividades de coordinación intersectorial buscando la participación de los actores sociales identificados con la problemática de salud. Las funciones de los centros de salud pueden resumirse en: Organizar, coordinar, dirigir, controlar, supervisar y evaluar la ejecución de todas las acciones de salud de su ámbito jurisdiccional. Promover la participación activa de la comunidad para la ejecución de las acciones de salud y de desarrollo integral. Desarrollar actividades de promoción de salud, prevención y recuperación de la enfermedad y de rehabilitación del paciente de acuerdo a la tecnología disponible. Realizar el análisis situacional de salud de la población y llevar a cabo la programación local de actividades con la participación de todos los actores sociales relevantes de la comunidad. Promover la concertación con otros sectores públicos y privados, con el gobierno local y con la comunidad, para compartir la responsabilidad de la ejecución de las acciones relacionadas con las condiciones de salud de la población y del medio ambiente. Hacer la referencia y contra-referencia de pacientes según la complejidad del caso y de acuerdo a las normas establecidas. Registrar, 23 consolidar y analizar la información bioestadística de los establecimientos de salud de su área de responsabilidad, incluyendo los hechos vitales de los derechos civiles y enviar el resumen respectivo a las instancias superiores correspondientes. Realizar visitas domiciliarias integrales de forma sistemática, priorizando de acuerdo a las necesidades de los programas. Participar conjuntamente con los representantes de la comunidad y de otros sectores públicos y privados de su ámbito en la administración del establecimiento y en las gestiones orientadas a la obtención y optimización de los recursos financieros, técnicos, logísticos y otros, a través de los canales respectivos. Capacitar a los técnicos de la atención primaria de salud voluntarios de la comunidad de forma permanente y de acuerdo a las necesidades de servicios. Supervisar, monitorear y evaluar las actividades de su establecimiento y de los puestos de salud de su jurisdicción. Facilitar y participar en la integración docencia-asistencia cuando las condiciones así lo requieran. Desarrollar actividades que promuevan la salud ambiental. Efectuar vigilancia epidemiológica de las enfermedades más prevalentes de la comunidad. 1.6. Morfofisiología gástrica El estómago es un órgano hueco del aparato digestivo. Tiene forma de “J” y está localizado en la parte superior y central del abdomen. Se encuentra muy próximo al diafragma y a otros órganos abdominales como el hígado, el páncreas, el bazo o el colon. Anatomía: Las partes más importantes del estómago son el cardias (zona de unión del esófago y el estómago), el cuerpo gástrico y el píloro (zona de unión del estómago con el intestino delgado). Tiene una porción curvada a la derecha (la curvatura menor) y otra a la izquierda (curvatura mayor). A las primeras tres partes del estómago (cardias, fondo, y cuerpo) algunas veces se les llama estómago proximal. Algunas células en estas partes del estómago producen ácido y pepsina (una enzima digestiva) que son las partes del jugo gástrico que ayudan a digerir los alimentos. También producen una proteína 24 llamada factor intrínseco, la cual el cuerpo necesita para la absorción de vitamina B12. A las dos partes inferiores (antro y píloro) se le llama estómago distal. El estómago tiene 3 capas: la mucosa (donde están las glándulas, que son un conjunto de células especializadas con una estructura característica), la muscular (donde están los músculos) y la serosa o peritoneo (membrana externa que rodea al estómago). Función: Los alimentos, después de ser masticados y lubricados con la saliva, descienden por el esófago hasta llegar al estómago donde se mezclan con los jugos gástricos y la mucina. Estas dos substancias producidas por las glándulas gástricas favorecen la digestión de los alimentos para extraer sus nutrientes esenciales. La pared gástrica tiene unos músculos (capa muscular) que se contraen y se relajan, “batiendo” los alimentos y mezclándolos con los jugos gástricos, facilitando así su digestión y desplazándolos hacia el píloro para que pasen al intestino delgado. 1.7 Cáncer de estómago El cáncer gástrico (adenocarcinoma) es el quinto tumor maligno más frecuente en el mundo. En el año 2012, se diagnosticaron cerca de un millón de casos nuevos. Existe una amplia variación geográfica en su presentación. Más de la mitad de los casos se concentran en Japón y China. También es un cáncer común en Sudamérica, Europa del Este y algunos países del Oriente Medio y, en cambio, es poco frecuente en Europa, Estados Unidos, Australia y África. El riesgo de desarrollar un cáncer gástrico aumenta a partir de los 50 años y es máximo en la séptima década de la vida. El cáncer gástrico es dos veces más frecuente en varones que en mujeres. 1.7.1. Definición de cáncer gástrico El término cáncer gástrico se refiere al crecimiento incontrolado de las células del estómago. Los tumores malignos pueden originarse en cada una de las tres capas: mucosa, muscular y serosa. Sus variedades histopatológicas incluyen al adenocarcinoma, que se origina en las glándulas y es el más frecuente: más del 25 95% de los cánceres gástricos son adenocarcinomas, mientras que los linfomas, los sarcomas y los melanomas son infrecuentes. Salvo en Japón, el carcinoma de estómago se encuentra en una fase evolutiva avanzada al momento del diagnóstico, con infiltración más allá de la submucosa e invasión de la pared gástrica. 1.7.2 Epidemiologia y factores de riesgo Los cánceres de estómago tienden a desarrollarse lentamente en un período de muchos años. Antes de que se forme un verdadero cáncer, a menudo ocurren cambios precancerosos en el revestimiento interno (mucosa) del estómago. Estos cambios tempranos casi nunca causan síntomas y, por lo tanto, no se detectan. Los tumores cancerosos que comienzan en diferentes secciones del estómago podrían producir síntomas diferentes y tienden a tener consecuencias diferentes. La localización del cáncer también puede afectar las opciones de tratamiento. Por ejemplo, los cánceres que se originan en la unión gastroesofágica son clasificados y tratados de la misma forma que los cánceres de esófago. Un cáncer que se origina en el cardias del estómago pero que está creciendo hacia la unión gastroesofágica también se clasifica por etapas y se trata como un cáncer de esófago. (Para más información, consulte el documento Cáncer de esófago). Los cánceres de estómago se pueden propagar (hacer metástasis) de varias maneras. Éstos pueden crecer a través de la pared del estómago e invadir los órganos cercanos. También pueden propagarse a los vasos linfáticos y a los ganglios linfáticos adyacentes. Los ganglios linfáticos son estructuras del tamaño de un fríjol que ayudan a combatir las infecciones. El estómago tiene una red muy rica de vasos linfáticos y de ganglios. Cuando el cáncer del estómago se torna más avanzado, puede viajar a través del torrente sanguíneo y propagarse a órganos como el hígado, los pulmones y los huesos. Si el cáncer se ha propagado a los ganglios linfáticos o a otros órganos, el pronóstico del paciente no es tan favorable. 26 Las causas exactas del cáncer gástrico no se conocen, aunque se sabe que existen unos factores de riesgo que favorecen su aparición. Los factores de riesgo son los agentes o condiciones que predisponen o aumentan las probabilidades de tener una determinada enfermedad. Los factores de riesgo para desarrollar cáncer gástrico son varios y no se excluyen entre sí: Edad: Las tasas del cáncer de estómago en las personas de más de 50 años aumentan bruscamente. La mayoría de las personas diagnosticadas con cáncer de estómago se encuentran entre los 60 y 89 años de edad. Origen étnico: En los Estados Unidos, el cáncer de estómago es más común entre los estadounidenses de origen hispano, las personas de raza negra y los asiáticos/isleños del Pacífico en comparación con las personas de raza blanca que no son de origen hispano. Geografía: A escala mundial, el cáncer de estómago es más común en Japón, China, Europa oriental y del sur y América Central y del sur. Esta enfermedad es menos común en África occidental y del sur, Asia Central y del sur, y Norteamérica. Factores nutricionales: Un riesgo aumentado de cáncer de estómago se ha visto en personas que llevan una alimentación que contiene grandes cantidades de alimentos ahumados, pescado y carne salada y vegetales conservados en vinagre. Los nitritos y nitratos son sustancias que se encuentran comúnmente en las carnes curadas. Ciertas bacterias, como la Helicobacter pylori, pueden convertir a los nitritos y nitratos en compuestos que han demostrado que causan cáncer de estómago en animales. Por otra parte, consumir muchas frutas, verduras y vegetales frescos parece reducir el riesgo de cáncer de estómago. Factores ambientales: Mala preparación de los alimentos, falta de refrigeración y aguas en mal estado (porque pueden tener altas concentraciones de nitratos o Helicobacter pylori). Tabaco: El hábito de fumar aumenta el riesgo de cáncer de estómago, particularmente para los cánceres de la sección superior del estómago cercana al 27 esófago. La tasa de cáncer de estómago es alrededor del doble para los fumadores Enfermedades o condiciones predisponentes: Existe una serie de condiciones y enfermedades, benignas o premalignas, que aumentan el riesgo de padecer cáncer gástrico. Las más destacadas son: • Linfoma gástrico: Las personas que han padecido cierto tipo de linfoma de estómago conocido como linfoma de tejido linfático asociado con la mucosa (MALT) tienen un riesgo aumentado de padecer adenocarcinoma del estómago. Probablemente esto se deba a que el linfoma MALT del estómago es causado por una infección con la bacteria H pylori. Cirugía gástrica previa: Para que aparezca un cáncer sobre el estómago residual (muñón), tiene que transcurrir más de 10 15 años. • Cirugía gástrica previa: Los cánceres de estómago son más propensos a originarse en las personas a las que se les ha extraído parte del estómago para tratar enfermedades no cancerosas como las úlceras. Esto puede deberse a que el estómago produce menos ácido, lo que permite que haya más bacterias productoras de nitritos. El reflujo de la bilis desde el intestino delgado hasta el estómago después de la cirugía podría también contribuir al riesgo aumentado. Por lo general, estos cánceres se desarrollan muchos años después de la cirugía. • Gastritis crónica atrófica: Puede ir degenerando hasta transformarse en cáncer. • Anemia perniciosa: Ciertas células en el revestimiento del estómago producen normalmente una sustancia llamada factor intrínseco (IF) que necesitamos para la absorción de vitamina B12 de los alimentos. Las personas que no tienen suficiente factor intrínseco pueden tener una deficiencia de vitamina B12, lo que afecta la capacidad del organismo de producir nuevos glóbulos rojos y puede también causar otros problemas. A esta condición se le llama anemia perniciosa. Además de la anemia (muy pocos glóbulos rojos), las personas con esta enfermedad presentan un mayor riesgo de cáncer de estómago. 28 • Pólipos gástricos: El riesgo de que se desarrolle un cáncer sobre un pólipo depende, entre otros factores, del tamaño del pólipo. A mayor tamaño, mayor riesgo. • Infección por Helicobacter pylori (H. Pylori): Las infecciones con la bacteria H pylori parecen ser la causa principal de cáncer de estómago, especialmente cánceres en la parte inferior (distal) del estómago. La infección por mucho tiempo del estómago con este germen puede conducir a inflamación (llamada gastritis atrófica crónica) y cambios precancerosos del revestimiento interno del estómago. Las personas con cáncer de estómago tienen una tasa más alta de infección con H pylori que las personas que no tienen cáncer. La infección con H pylori se asocia también con algunos tipos de linfoma de estómago. Aun así, la mayoría de la gente que es portadora de este germen en el estómago nunca desarrolla cáncer. • El sobrepeso o la obesidad es una posible causa de cánceres del cardias, aunque todavía no está claro cuán contundente es esta asociación. • Enfermedad de Menetrier (gastropatía hipertrófica): En esta afección el crecimiento excesivo del revestimiento del estómago causa grandes pliegues en el revestimiento y esto causa bajos niveles de ácido estomacal. Debido a que esta enfermedad se presenta en muy raras ocasiones, no se conoce exactamente cuánto aumenta el riesgo de cáncer de estómago. • Sangre tipo A: Los grupos de tipo de sangre se refieren a ciertas sustancias que normalmente están presentes en la superficie de los glóbulos rojos y otros tipos de células. Estos grupos son importantes para determinar la compatibilidad de la sangre en las transfusiones. Por razones desconocidas, las personas con el tipo de sangre A tienen un mayor riesgo de llegar a padecer cáncer de estómago. Factores genéticos o familiares • Factores genéticos: En casos poco frecuentes, el cáncer gástrico puede estar relacionado con factores genéticos. Por ejemplo, en el síndrome de cáncer gástrico difuso hereditario varios miembros de la familia desarrollan este tipo de cáncer y existe una mutación en un gen llamado cadherina. Otras afecciones 29 hereditarias que constituyen factores de riesgo son el Cáncer colorrectal hereditario sin poliposis (HNPCC), Poliposis adenomatosa familiar (FAP), BRCA1 y BRCA2, Síndrome de Li-Fraumeni y el Síndrome Peutz-Jeghers (PJS). • Factores familiares: La incidencia es 2-3 veces mayor en aquellas personas con varios familiares diagnosticados de cáncer gástrico, aunque no se identifique una alteración genética subyacente. 1.7.3 Clasificaciones del cáncer gástrico Los diferentes tipos de cáncer de estómago incluyen: Adenocarcinoma: Aproximadamente entre 90% y 95% de los cánceres del estómago son adenocarcinomas. Cuando se emplean los términos cáncer de estómago o cáncer gástrico casi siempre se refieren a un adenocarcinoma. Estos cánceres se originan en las células que forman la capa más interna del estómago (conocida como la mucosa). Linfoma: Se refiere a los tumores cancerosos del sistema inmunológico que algunas veces se detectan en la pared del estómago. Aproximadamente 4% de los cánceres de estómago son linfomas. El tratamiento y el pronóstico dependen del tipo de linfoma. Tumores del estroma gastrointestinal (GIST): Estos son tumores poco comunes que se originan en formas muy tempranas de células de la pared del estómago llamadas células intersticiales de Cajal. Algunos de estos tumores no son cancerosos (benignos), mientras que otros son cancerosos. Aunque los tumores estromales gastrointestinales se pueden encontrar en cualquier lugar del tracto digestivo, la mayoría se descubre en el estómago. Tumores carcinoides: Estos tumores se originan de células productoras de hormona del estómago. La mayoría de estos tumores no se propaga a otros 30 órganos. Los tumores carcinoides son responsables de aproximadamente 3% de los tumores cancerosos del estómago. Otros tipos de cáncer: Otros tipos de cáncer, como el carcinoma de células escamosas, el carcinoma de células pequeñas, y el leiomiosarcoma, también pueden originarse en el estómago, aunque estos cánceres ocurren con poca frecuencia. Clasificación Macroscópica para la Etapificación del Cáncer Gástrico Cáncer Incipiente (Clasificación japonesa): I Elevado IIa Levemente Elevado IIb Plano IIc Deprimido III Excavado o Ulcerado En tipos mixtos se colocará primero el que tiene mayor diámetro Cáncer Avanzado (Clasificación de Borrmann): Tipo I Lesión polipoidea, base ancha y bien demarcada de la mucosa alrededor Tipo II Similar a la anterior con ulceración central. Tipo III Ulcerado sin límites definidos, infiltrando la mucosa de alrededor. Tipo IV Difusamente infiltrante o Linitis plástica. Tipo V No asimilable a los anteriores Etapificación TNM (American Joint Comission on cancer, 1997) (T) Tumor primario TX: tumor Primario no puede evaluarse T0: Sin evidencia de tumor primario Tis: Carcinoma en situ: tumor d intra epitelial sin la invasión de la lámina propia T1: Tumor invade lamina propia o submucosa 31 T2: Tumor invade muscular propia o subserosa * (El tumor puede penetrar la muscular propia con extensión a los ligamentos gastrocólico o gastrohepático o al omentum mayor o menor sin perforar el peritoneo visceral que cubre estas estructuras. En este caso, el tumor es clasificado T2. Si hay perforación de peritoneo visceral que cubre los ligamentos gástricos u omentum el tumor debe ser clasificado T3). T3: Tumor penetra serosa (peritoneo visceral) sin invadir las estructuras adyacentes **(Las estructuras adyacentes al estómago incluyen bazo, colon transverso, hígado, diafragma, páncreas, la pared abdominal, la glándula suprarrenal, el riñón, intestino delgado y el retroperitoneo). *** (Extensión Intramural al duodeno o al esófago se clasifica por la invasión de mayor profundidad en cualquiera de estos sitios, incluso el estómago) T4: Tumor invade las estructuras adyacentes * * * (N) Linfonodos regionales Los linfonodos regionales son los nodos perigástricos, encontrados a lo largo de las curvaturas menor y mayor, y los nodos localizados a lo largo de las arterias gástricas izquierda, hepática, esplénica. Para pN, un espécimen de linfadenectomía regional contendrá ordinariamente por lo menos 15 ganglios linfáticos. El compromiso tumoral de otros ganglios linfáticos intra-abdominales, como hepatoduodenal, retropancreaticos, mesentéricos, y para-aórticos, se clasifica como metástasis a distancia. NX: Linfonodo no puede evaluarse N0 Sin metástasis a linfonodos regionales N1: Metástasis en 1 a 6 linfonodos regionales N2: Metástasis en 7 a 15 linfonodos regionales N3: Metástasis en más de 15 linfonodos regionales (M) Metástasis 32 MX: Metástasis no pueden evaluarse M0: Sin metástasis M1: Metástasis Estadios o etapas TNM Estadio 0: Tis N0 M0 Estadio IA: T1 N0 M0 Estadio IB: T1 N1 M0 T2 N0 M0 Estadio II: T1 N2 M0 T2 N1 M0 T3 N0 M0 Estadio IIIA: T2 N2 M0 T3 N1 M0 T4 N0 M0 Estadio IIIB: T3 N2 M0 Estadio IV: T1,T2,T3 N3 M0 T4 N1,N2,N3 M0 Cualquier T Cualquier N M1 1.7.4. Cuadro clínico y diagnóstico El cáncer gástrico puede no producir síntomas (es decir, ser asintomático) hasta que no está en una etapa avanzada. En los pacientes asintomáticos, el cáncer gástrico se diagnostica al realizar pruebas por otras enfermedades. Los síntomas suelen ser vagos e inespecíficos. Los más frecuentes son pérdida de peso, dolor abdominal, cambios de ritmo intestinal, pérdida de apetito y hemorragia. Las hemorragias pueden ser de varios tipos y causar anemia: • Pérdidas ocultas (microscópicas) de sangre por las heces • Hematemesis 33 • Melenas o hematoquecia También puede notarse náuseas y vómitos, sensación de plenitud precoz por falta de distensión de la pared gástrica, ascitis, cansancio y otros síntomas menos frecuentes. En los tumores de cardias se puede asociar disfagia. En los de estómago distal puede existir obstrucción del píloro. Estos síntomas no son exclusivos del cáncer gástrico, porque pueden aparecer en la úlcera gástrica o en otras enfermedades. Los signos pueden ser ninguno o alguno de los siguientes: nódulos, masas o empastamiento en el abdomen, organomegalias, ascitis, adenopatías en el cuello o en las axilas y otros signos menos frecuentes. Estos signos no son exclusivos de cáncer gástrico, pueden aparecer en otras enfermedades benignas o malignas. La detección temprana consiste en realizar pruebas para buscar la enfermedad en personas sin síntomas. En los países como Japón, en los que el cáncer de estómago es muy común, la realización de pruebas masivas de detección a la población ha ayudado a detectar muchos casos en una etapa temprana y curable. Es posible que las pruebas masivas de detección temprana hayan reducido la cantidad de personas que mueren a causa de esta enfermedad, aunque esto no se ha podido probar. Los estudios en los Estados Unidos han determinado que las pruebas de detección rutinarias en las personas que tienen un riesgo promedio de cáncer de estómago no son útiles porque esta enfermedad no es muy común. Por otra parte, las personas con ciertos factores de riesgo de cáncer de estómago podrían beneficiarse de las pruebas de detección. Por lo general, el cáncer de estómago se detecta cuando una persona acude al médico debido a que presenta signos o síntomas. El doctor anotará la historia médica y examinará al paciente. Si se sospecha cáncer de estómago, será necesario realizar pruebas para confirmar el diagnóstico. Al preparar la historia clínica, el médico hará preguntas acerca de los síntomas y posibles factores de riesgo para ver si ellos pudieran sugerir la presencia de un cáncer de estómago u otra causa. El examen físico provee a su médico la 34 información sobre su estado de salud en general, los posibles signos del cáncer de estómago y otros problemas de salud. Estudios endoscópicos Una endoscopia superior (también llamada esofagogastroduodenoscopia) es el estudio principal que se utiliza para detectar cáncer de estómago. Cuando se observa a través de un endoscopio, el cáncer de estómago puede tener el aspecto de una úlcera, de un pólipo, una masa protuberante o de áreas de mucosa engrosadas, difusas y planas conocidas como linitis plástica. Lamentablemente, a menudo los cánceres de estómago en el síndrome de cáncer gástrico difuso hereditario no se pueden observar durante una endoscopia. La endoscopia también se puede utilizar como parte de un estudio por imágenes especial conocido como ecografía endoscópica, en la que se coloca un transductor pequeño en la punta de un endoscopio que permite al médico observar las capas de la pared estomacal, así como los ganglios linfáticos cercanos y otras estructuras justo fuera del estómago. La calidad de la imagen es mejor en comparación con la ecografía convencional. Este procedimiento es más útil para ver cuánto se pudo haber propagado el cáncer hacia la pared del estómago, los tejidos circundantes y a los ganglios linfáticos cercanos. También puede ser usado para ayudar a guiar la aguja en un área sospechosa para obtener una muestra de tejido (biopsia con aguja guiada por ecografía endoscópica). Biopsia gástrica Las biopsias se hacen con más frecuencia durante la endoscopia superior. Si durante la endoscopia el médico observa cualquier área anormal en el revestimiento del estómago, se pueden pasar instrumentos por el endoscopio para tomar muestras y luego realizar una biopsia. Algunos cánceres de estómago se encuentran profundamente ubicados dentro de la pared del estómago, lo que puede dificultar realizar una biopsia con un endoscopio convencional. Si el médico sospecha que el cáncer podría estar más profundamente en la pared del estómago, se puede usar una ecografía 35 endoscópica para guiar una aguja delgada y hueca hacia la pared del estómago para obtener una biopsia. También se pueden obtener biopsias de áreas de posible propagación del cáncer, tal como ganglios linfáticos adyacentes o áreas sospechosas en otras partes del cuerpo. Si una muestra de biopsia contiene células de adenocarcinoma, puede que se hagan pruebas para determinar si contiene una cantidad muy elevada de una proteína promotora del crecimiento llamada HER2/neu (o simplemente HER2). El gen HER2/neu instruye a las células a producir esta proteína. A los tumores con niveles aumentados de HER2/neu se les conoce como positivos para HER2. Los cánceres de estómago que son positivos para HER2 pueden ser tratados con medicamentos que atacan la proteína HER2/neu, como trastuzumab (Herceptin®). A la muestra de biopsia se le pueden hacer pruebas de dos maneras diferentes: Inmunohistoquímica (immunohistochemistry, IHC): en esta prueba se aplican a la muestra anticuerpos especiales que se adhieren a la proteína HER2/neu, lo que causa que las células cambien de color si se presentan muchas copias de esta proteína. Este cambio de color se puede ver en el microscopio. Los resultados de la prueba se presentan como 0, 1+, 2+, o 3+. Hibridización fluorescente in situ (fluorescent in situ hybridization, FISH): esta prueba utiliza porciones fluorescentes de ADN que se adhieren específicamente a las copias del gen HER2/neu en las células, las que se pueden contar con un microscopio especial. Con más frecuencia, la IHC se hace primero. Si los resultados son 0 o 1+, el cáncer es HER2 negativo. Las personas con tumores HER2 negativos no son tratadas con medicamentos (como trastuzumab) que atacan la HER2. Si los resultados de la prueba indican 3+, el cáncer es HER2 positivo. Las pacientes con tumores HER2 positivos pueden ser tratadas con medicamentos, como con 36 trastuzumab. Cuando el resultado es 2+, la condición de HER2 del tumor no está clara. Esto a menudo conduce a evaluar el tumor con FISH. Estudios por imágenes Los estudios por imágenes utilizan ondas sonoras, rayos X, campos magnéticos o sustancias radiactivas para obtener imágenes del interior del cuerpo. Los estudios por imágenes se pueden realizar por un número de razones, incluyendo: Para ayudar a determinar si un área sospechosa pudiera ser cancerosa. Saber cuán lejos se propagó el cáncer. Ayudar a determinar si el tratamiento ha sido eficaz. Radiografía seriada del tracto gastrointestinal superior: Este estudio radiológico se realiza para examinar el revestimiento interno del esófago, el estómago y la primera parte del intestino delgado. Este estudio se usa con menos frecuencia que la endoscopia para detectar cáncer de estómago u otros problemas estomacales, ya que puede pasar por alto algunas áreas anormales y no le permite a los médicos tomar muestras de biopsia. Sin embargo, este estudio es menos invasivo que la endoscopia, y puede ser útil en algunas situaciones. Para este estudio, el paciente toma una solución caliza que contiene una sustancia llamada bario. El bario aplica una capa sobre el revestimiento del esófago, estómago y el intestino delgado. Entonces se toman varias radiografías. Debido a que los rayos X no pueden traspasar a través de la capa de bario, esto resaltará cualquier anomalía del recubrimiento de estos órganos. Para identificar los cánceres de estómago tempranamente, se usa una técnica de doble contraste. Con esta técnica, después de tragar la solución que contiene bario, se pasa un tubo delgado y se bombea aire al estómago, lo que hace que la capa de bario sea muy delgada y se puedan ver incluso anomalías pequeñas. Tomografía computarizada: La tomografía computarizada (computed tomography, CT) es un estudio de radiografía que produce imágenes transversales detalladas de su cuerpo. En 37 lugar de tomar una sola imagen, como se hace en una radiografía convencional, una tomografía computarizada toma muchas imágenes mientras gira a su alrededor. Luego, una computadora combina estas fotografías en imágenes de secciones transversales de la parte del cuerpo que se está estudiando. Se pueden emplear contrastes orales y/o intravenosos, lo que ayuda a delinear mejor las estructuras. La tomografía computarizada muestra el estómago con bastante claridad, y frecuentemente puede confirmar la localización del cáncer. Además, puede mostrar los órganos adyacentes al estómago, tal como el hígado, así como los ganglios linfáticos y los órganos distantes donde pudiese haber propagación del cáncer. La CT puede ayudar a determinar la extensión (etapa) del cáncer, y si la cirugía puede ser una buena opción de tratamiento. Las tomografías computarizadas pueden también ser usadas para guiar la aguja de una biopsia hacia un área donde se sospecha propagación del cáncer. Para este procedimiento, el paciente permanece en la camilla de tomografía mientras un médico mueve una aguja de biopsia hacia la masa a través de la piel. Las tomografías computarizadas se repiten hasta que la aguja esté dentro de la masa. Se extrae una muestra mediante una biopsia con aguja fina (un fragmento diminuto de tejido) o una biopsia por punción con aguja gruesa (un cilindro delgado de tejido) y se observa con un microscopio. Imágenes por resonancia magnética Las imágenes por resonancia magnética (magnetic resonance imaging, MRI) utilizan ondas de radio e imanes potentes en lugar de rayos X. La energía de las ondas de radio es absorbida por el cuerpo y luego liberada en un patrón formado por el tipo de tejido del cuerpo y por ciertas enfermedades. Una computadora traduce el patrón en una imagen muy detallada de las partes del cuerpo. Al igual que la CT, se inyectará un material de contraste, pero esto se usa con menos frecuencia. La mayoría de los médicos prefieren usar las pruebas de CT para observar el estómago. Sin embargo, los exámenes de MRI algunas veces pueden 38 proveer más información. Las MRI a menudo se usan para examinar el cerebro y la médula espinal. Tomografía por emisión de positrones En la tomografía por emisión de positrones (positron emission tomography, PET), se inyecta una sustancia radiactiva en una vena (usualmente un tipo de azúcar emparentado con la glucosa, conocido como FDG). (La cantidad de radiactividad que se emplea es muy poca y el cuerpo la eliminará más o menos el día siguiente). Debido a que las células cancerosas están creciendo más rápidamente que las células normales, hacen uso del azúcar mucho más rápido, por lo que absorbe el material radiactivo. Después de aproximadamente una hora, una cámara especial crea una fotografía de las áreas de radiactividad en el cuerpo. Algunas veces, la PET (por sus siglas en inglés) es útil para detectar propagación tumoral inadvertida. La imagen no es tan detallada como una CT o las MRI, pero proporciona información útil sobre todo el cuerpo. Aunque los estudios con PET pueden ser útiles para detectar áreas de propagación del cáncer, no siempre son útiles en ciertas clases de cáncer de estómago, ya que estos tipos no adquieren mucha glucosa. Algunas máquinas pueden hacer una PET y una CT al mismo tiempo (PET/CT scan). Esto permite al médico comparar las áreas de mayor radiactividad en la PET con la apariencia más detallada de esa área en la CT. La PET/CT podría ser más útil que la PET sola para el cáncer de estómago. Puede ayudar a mostrar si el cáncer se ha propagado del estómago a otras partes del cuerpo, en cuyo caso puede que la cirugía no sea un buen tratamiento. Radiografía de tórax Esta prueba puede mostrar si el cáncer se ha propagado a los pulmones. También podría determinar si hay enfermedades graves de los pulmones o el corazón. Esta prueba no se necesita si se ha hecho una CT del tórax. Otras pruebas Laparoscopia: Si este estudio se realiza, por lo general, se hace sólo después de que se haya encontrado el cáncer de estómago. Aunque la CT o el MRI pueden 39 crear imágenes detalladas del interior del cuerpo, éstos pueden pasar por alto algunos tumores, especialmente si son muy pequeños. Los médicos podrían realizar una laparoscopia antes de cualquier otra cirugía para ayudar a confirmar que un cáncer de estómago sigue solamente en el estómago y puede ser removido totalmente mediante cirugía. También se puede realizar antes de la quimioterapia, radiación, o ambas, si estas son planificadas antes de la cirugía. Durante la laparoscopia se puede realizar un lavado peritoneal diagnóstico en busca de células cancerosas. Algunas veces, esta prueba se combina con la ecografía para proveer una mejor imagen del cáncer. 1.7.5. Prevención y tratamiento El acápite de prevención y tratamiento del cáncer gástrico se abordará en el Capítulo II como parte de la propuesta. Conclusiones parciales del capítulo En este capítulo se expusieron referentes teóricos actualizados sobre el origen y evolución del problema de investigación, las diferentes posiciones teóricas sobre el tema, así como se abordaron aspectos generales del proceso saludenfermedad y el sistema de atención primaria de salud. 40 CAPÍTULO II MARCO METODOLÓGICO Y EVALUACIÓN DE LOS RESULTADOS. La presente investigación se llevó a cabo en el Centro de Salud del cantón Quero, provincia de Tungurahua, la cual es la segunda provincia en el Ecuador con mayor incidencia de cáncer gástrico por cada 100.000 habitantes. El Centro de Salud es tipo C y constituye el primer eslabón en la atención a la ciudadanía. Esta casa de salud cuenta con todos los servicios médicos básicos como Obstetricia, Odontología, Radiología, Pediatría, Rehabilitación y Emergencias las 24 horas. Cuenta con equipamiento médico de última tecnología y beneficia además a unas 50 mil personas de los cantones de Mocha y Cevallos. Tipo de estudio: Se realizó un estudio observacional descriptivo, transversal y retrospectivo, ya que la principal técnica empleada fue la observación y recolección directa de los datos que aparecían en la historia clínica de los pacientes y la aplicación de una encuesta a los casos con diagnóstico conocido de Cáncer Gátrico. Fue un estudio transversal y retrospectivo, ya que abarcó un determinado período de tiempo y se analizó un fenómeno del pasado reciente. La investigación se correspondió con la línea de investigación de Salud Pública, sublínea enfermedades no transmisibles y crónicas degenerativas de la Universidad regional autónoma de los Andes, UNIANDES El universo de estudio fueron todos los pacientes con diagnóstico conocido de cáncer gástrico del cantón Quero, provincia Tungurahua. La muestra se conformó aleatoriamente con la totalidad de pacientes que fueron atendidos por esta condición en el Centro de Salud del cantón, durante el período 2010-2015. 41 Los criterios de exclusión abarcaron a los pacientes ya fallecidos y aquellos pacientes cuyas historias clínicas no reunían la información útil para la investigación. La modalidad paradigmática de este tipo de investigación fue cuanti-cualitativa, con predominio cualitativo narrativo, ya que se recolectaron los datos de las historias clínicas de los pacientes para describirlos y analizarlos en base a la revisión teórica del tema a investigar. Dentro de los métodos empleados, estuvo el método histórico-lógico al consultar la bibliografía disponible sobre el tema de la investigación. En un segundo momento se recolectaron los datos correspondientes a las variables a investigar revisando las historias clínicas de los pacientes y aplicándoles una encuesta. Posteriormente los datos obtenidos se depositaron en un formulario creado según la bibliografía consultada y los objetivos de la investigación, el cual fue la fuente primaria de información. El procesamiento estadístico de los datos se llevó a cabo empleando estadísticas descriptivas y distribuciones de frecuencia mediante fórmulas de un libro de Microsoft Excel. Para interpretar los resultados se emplearon los métodos analítico-sintético e inductivo-deductivo. Los resultados obtenidos se mostraron en tablas y gráficos. 42 Operacionalización de las variables de la investigación Variable Definición Operacional Dimensiones Tipo de variable Indicador Escala Fuente de verificación 1. De <35 años____ Años cumplidos Edad hasta la fecha Cuantitativa - actual agrupada 2. De 36 a 50 años____ Proporción Continua 3. De 51 a 60 años____ 4. De 61 a 70 años____ Historia Clínica 5. >70 años____ Cualitativa Sexo Género biológico - individual Nominal Razón 1. Masculino Historia 2. Femenino Clínica dicotómica Antecedentes familiares de cáncer o poliposis intestinal Antecedentes patológicos familiares Cualitativa individual Nominal Razón 1. Si Historia 2. No Clínica dicotómica 43 1. Tabaco Consumo habitual Hábitos tóxicos de sustancias y Cualitativa - productos nocivos Nominal 2. Alcohol Porcentaje politómica 3. Café 4. Drogas Historia Clínica 5. Ninguno Consumo semanal 1. Ahumados y de alimentos y embutidos Hábitos fármacos Cualitativa alimentarios y reconocidos como Nominal farmacológicos factores de riesgo o politómica protectores de 2. Alimentos conservados Porcentaje 3. Frutas y vegetales 4. Pescado fresco Historia Clínica 5. Aspirina cáncer gástrico Estado nutricional Valoración nutricional según IMC *Desnutrido Cualitativa por exceso individual *Desnutrido Nominal por defecto politómica 1. Desnutrido (IMC < 18,5) 2.Normopeso (IMC 18,624,9) Proporción 3. Sobrepeso (IMC 2529,9) 4. Obeso (IMC ≥ 30) Historia Clínica 44 1. Gastritis crónica 2. Enfermedad Comorbilidades y antecedentes de riesgo Enfermedades crónicas con diagnóstico conocido *Transmisibles *No transmisibles úlceropéptica Cualitativa individual Nominal 3. Infección con Porcentaje Helicobacter pylori 4. Linfoma gástricos politómica Historia Clínica 5. Cirugía gástricas previas 6. Pólipos intestinales 7. Otras (Explicar) Síntomas y signos Síntomas y signos relacionados con la enfermedad Cualitativa individual Nominal politómica Porcentaje 1. Asintomático 2. Dolor abdominal 3. Dispepsia tipo ulcerosa 4. Saciedad precoz o plenitud posprandial 5. Anemia 6. Pérdida de peso 7. Ascitis 8. Tumor palpable 9. Disfagia 10. Otro (Explicar) Historia Clínica 45 1. <1 mes Tiempo de evolución con los síntomas Tiempo de 2. De 1 a 3 meses evolución con los Cuantitativa síntomas antes del continua Proporción diagnóstico 3. De 91 días a 6 meses Historia 4. De 181 días a 9 meses Clínica 5. De 271 días a 1 años 6. > 1 año 1. Endoscopia 2. Estudios radiológicos Medio Prueba diagnóstico del confirmatoria del hallazgo diagnóstico contrastados Cualitativa - Nominal Porcentaje politómica 3. Estudios tomográficos Historia 4. Estudios sonográficos Clínica 5. En el curso de otra cirugía 6. Otro (Explicar) Tipo de tumor Se transcribió directamente del resultado estudio histopatológico de la biopsia Cualitativa - nominal politómica Porcentaje Según la biopsia Historia Clínica 46 Tiempo de evolución desde el diagnóstico Tiempo transcurrido 1. < 1 año desde que se confirmó el - Proporción diagnóstico de 2. 1 a 3 años Historia 3. De 4 a 5 años Clínica 4. > 5 años cáncer 1. Cirugía Tratamiento El tratamiento recibido oncológico recibido Cualitativa - nominal politómica 2. Quimioterapia Porcentaje 3. Radioterapia 4. Hormonoterapia Historia Clínica 5.Combinaciones (explicar) 47 Se ha señalado que la edad media de aparición de un cáncer gástrico es 55 años. En el presente estudio la media de edad fue de 57 ± 2 años, observándose que más de la mitad de los casos (52,6%) acumulativamente, tenían edades hasta 60 años y llamando la atención que un 10,5% eran menores de 35 años (Tabla y Gráfico 1). Tabla y Gráfico 1 Distribución de pacientes según grupos de edades Grupo de edades Frecuencia Porcentaje <35 años De 36 a 50 años De 51 a 60 años De 61 a 70 años >70 años Total 6 15 9 15 12 57 10,5% 26,3% 15,8% 26,3% 21,1% 100,0% 16 15 Porcentaje acumulativo 10,5% 36,8% 52,6% 78,9% 100,0% 100,0% 15 14 12 12 10 9 8 6 6 4 2 0 <35 años De 36 a 50 años De 51 a 60 años De 61 a 70 años >70 años Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez Estudios realizados en países de alta incidencia de cáncer gástrico como Chile y Japón, donde se realizan cribados de la enfermedad a grandes grupos 48 poblacionales, apuntan que cada vez más se incrementa la incidencia de la enfermedad en pacientes jóvenes menores de 50 años (8, 9, 20, 22, 26, 28). En lo referente al sexo, existe coincidencia en múltiples estudios donde se ha observado mayor incidencia del cáncer gástrico en el sexo masculino. En el presente estudio, si bien hubo predominio masculino dentro de los pacientes con la enfermedad, esta diferencia no fue significativa, observándose una relación de 1,1:1 a favor de los hombres (Tabla y Gráfico 2). Tabla y Gráfico 2 Distribución de pacientes según el sexo Sexo Frecuencia Porcentaje Masculino Femenino Total 30 27 57 52,6% 47,4% 100,0% 27; 47% 30; 53% Masculino Femenino Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez 49 Esta observación está en correspondencia con los estudios de Tamayo y Robles en la provincia de Tungurahua desde la década de los 90 los 2000, los que reportaron una relación de 1,2 hombres por cada mujer afectados con cáncer gástrico (7, 15, 29). 50 Actualmente no se pueden desconocer los importantes avances que se van haciendo en la genética relacionada al cáncer. Observaciones clínicas señalan un mayor riesgo, en dos o tres veces a desarrollar cáncer gástrico cuando existen antecedentes familiares. Este hecho estuvo notablemente presente en la población estudiada, en la cual el 100% de los pacientes tenían algún antecedente de cáncer o pólipos intestinales en familiares cercanos (Tabla y Gráfico 3). Tabla 3 Distribución de pacientes según antecedentes familiares de cáncer o poliposis intestinal Antecedentes familiares Frecuencia Porcentaje Si 57 100,0% No 0 0,0% Total 57 100,0% de cáncer o poliposis intestinal 60 50 40 30 20 10 0 Si No Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez 51 Estudios realizados en Colombia, Perú, México y Chile reportan resultados similares que le dan peso al papel de la genética y la herencia en el incremento del riesgo de esta enfermedad (12, 16, 20, 21). 52 Es conocido que el riesgo de padecer cáncer gástrico está incrementado al doble en los fumadores crónicos, sobre todo los que comenzaron a fumar a edades tempranas. De igual forma, el consumo excesivo de alcohol se ha señalado como un factor que incrementa el riesgo de adquirir la enfermedad. En la serie estudiada, llamó la atención que solo un paciente declaró no tener ningún hábito tóxico. El resto reconoció que tenía uno o más, con predominio de consumo de café y tabaco. (Tabla y Gráfico 4). Tabla y Gráfico 4 Distribución de la frecuencia de hábitos tóxicos en los pacientes Ninguno Alcohol Tabaco Hábitos tóxicos Frecuencia Porcentaje Café 49 86,0% Tabaco 25 43,9% Alcohol 22 38,6% Ninguno 1 1,8% 1 (1,8%) 22 (38,6%) 25 (43,9%) Café -3 7 17 27 Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez 49 (86,0%) 37 47 57 53 El hecho de que muchos pacientes que no fuman adquieran cáncer gástrico, hace que muchas personas no comprendan o acepten el riesgo real demostrado en varios estudios, que ubican al paciente fumador de ambos sexos con el doble de posibilidades de adquirir la enfermedad con respecto a los no fumadores (6, 17, 29, 32). 54 Respecto a los factores alimentarios, en la población del estudio los resultados observados fueron un tanto controversiales, ya que, aunque casi la mitad de los pacientes consumía habitualmente ahumados y embutidos (43,9%) y más de la mitad consumía alimentos conservados (57,9%), los que se reconocen como alimentos perjudiciales; la gran mayoría manifestó que consumía frutas y vegetales, los que conjuntamente con los pescados frescos, se reconocen como alimentos protectores (Tabla y Gráfico 5). Tabla y Gráfico 5 Distribución de los hábitos alimentarios y farmacológicos entre los pacientes Hábitos alimentarios y farmacológicos (Consumo semanal de:) Frecuencia Porcentaje Alimentos conservados Ahumados y embutidos Frutas y vegetales Pescado fresco Aspirina 33 25 51 24 0 57,9% 43,9% 89,5% 42,1% 0,0% 100,0% 51 90,0% 50 80,0% 40 70,0% 33 30 60,0% 25 50,0% 24 40,0% 20 30,0% 20,0% 10 0 0 10,0% 0,0% Alimentos conservados Ahumados y embutidos Frutas y vegetales Frecuencia Pescado fresco Aspirina Porcentaje Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez 55 En varias publicaciones se habla de alimentos perjudiciales o inductores y otros protectores. Las nitrosaminas son productos de la mala conservación de los alimentos. Los nitratos se transforman en nitritos y estos por acción bacteriana en nitrosaminas que son consideradas carcinogenéticas. Esto se produce especialmente en alimentos mal conservados. Por otra parte, el aumento de alimentos conservados y no frescos, incrementa el riesgo de carcinoma gástrico. La ingestión elevada de sal (alimentos ahumados o conservados en salmuera o salados) se correlacionaría con un incremento en la posibilidad de desarrollar cáncer gástrico. Estos pacientes desarrollan una gastritis atrófica y la posibilidad de desarrollar cáncer gástrico sería el doble. Se ha señalado que el aumento del consumo de frutas frescas, vegetales crudos, pescado frescos tienen un efecto protector, al igual que algunos fármacos como la aspirina y FAINES (21). 56 La obesidad, sobre todo asociada a sedentarismo, ha sido señalada como un factor de riesgo de cáncer gástrico, sin embargo, en la práctica, la mayoría de los pacientes en los que se confirma diagnóstico de carcinoma gástrico, ya este se encuentra en una etapa avanzada con compromiso variable del estado nutricional. La Tabla y Gráfico 6 muestra el estado nutricional de los individuos de la serie. Tabla y Gráfico 6 Distribución de pacientes según su estado nutricional por IMC Estado nutricional Desnutrido Normopeso Sobrepeso Obeso Total Frecuencia 14 38 5 0 57 Porcentaje 24,6% 66,7% 8,8% 0,0% 100,0% 38 40 70,0% 66,7% 35 60,0% 30 50,0% 25 40,0% 20 15 30,0% 14 24,6% 20,0% 10 5 5 10,0% 8,8% 0 0 Desnutrido Normopeso Sobrepeso Frecuencia 0,0% Obeso 0,0% Porcentaje Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez Se observó predominio de pacientes normopeso con 66,7%. No se encontró ningún paciente obeso en la serie. Otros autores reportaron resultados similares (10, 11). 57 Son varias las enfermedades que han sido reconocidas como factores de riesgo del carcinoma gástrico en ambos sexos. En el presente estudio se observó como antecedente de riesgo, un marcado predominio de la gastritis crónica, con más de las tres cuartas partes de los casos y la infección con H. pylori, con un 56,1% (Tabla y Grafico 7). Tabla y Gráfico 7 Distribución de antecedentes personales de riesgo entre los pacientes Comorbilidades y antecedentes de riesgo Frecuencia Porcentaje Gastritis crónica Infección con Helicobacter pylori Pólipos intestinales Enfermedad úlceropéptica Linfoma gástricos Cirugía gástrica previa 43 32 18 16 6 2 75,4% 56,1% 31,6% 28,1% 10,5% 3,5% 80,0% 50 70,0% 43 60,0% 40 32 50,0% 30 40,0% 18 20 30,0% 16 20,0% 10 6 2 0 10,0% 0,0% Gastritis crónica Infección con Pólipos Enfermedad Helicobacter intestinales úlceropéptica pylori Frecuencia Linfoma gástricos Cirugía gástrica previa Porcentaje Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez 58 Otras series reportan una mayor incidencia y por ende un mayor papel en la carcinogénesis, a la infección por el H. Pylori, lo cual es perfectamente aceptable si se tiene en cuenta que la mayoría de las gastritis agudas y crónicas son producidas por este microorganismo (19, 24, 25). Lamentablemente, la mayoría de pacientes con cáncer gástrico pasan largos períodos asintomáticos al comienzo de su enfermedad y en muchas ocasiones el comienzo de los síntomas es indicador de enfermedad avanzada. Sin embargo, la falta de información, educación en temas de salud y de preocupación, puede llevar a que un paciente transite con síntomas sospechosos por largos períodos sin solicitar ayuda médica y en muchas ocasiones automedicándose. 59 En los pacientes de la serie, los síntomas predominantes antes del diagnóstico fueron el dolor abdominal difuso o epigástrico en más de dos tercios de los casos y la plenitud postprandial o saciedad precoz en el 56,1% (Tabla y Gráfico 8) Tabla y Gráfico 8 Distribución de síntomas entre los pacientes Síntomas y signos Frecuencia Porcentaje Dolor abdominal Saciedad precoz o plenitud pospandrial Disfagia Pérdida de peso Dispepsia tipo ulcerosa Anemia Ascitis Asintomático 40 70,2% 32 56,1% 21 18 12 7 7 3 36,8% 31,6% 21,1% 12,3% 12,3% 5,3% 45 80,0% 40 40 70,0% 35 32 60,0% 30 50,0% 25 21 40,0% 18 20 15 30,0% 12 10 7 3 5 0 20,0% 7 Dolor abdominal Saciedad precoz o plenitud pospandrial Disfagia Pérdida de peso Dispepsia tipo ulcerosa Frecuencia Anemia Ascitis Asintomático 10,0% 0,0% Porcentaje Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez 60 Matta de García, en Guatemala, encontró resultados similares, mientras que en la región europea, se reporta mayor incidencia de síntomas de dispepsia tipo ulcerosa, anemia y pérdida de peso. La presencia de ascitis denuncia una enfermedad avanzada metastásica (24, 27). 61 Un elemento importante que se tuvo en cuenta durante la investigación, fue precisamente el tiempo que pasaron los pacientes con síntomas digestivos sospechosos de cáncer gástrico antes de solicitar asistencia especializada. Llamó la atención el hecho de que casi la mitad de los pacientes (49,1%) estuvieron con algún síntoma digestivo por más de un año, mientras que el resto (50,9% acumulativo) permaneció con los síntomas de uno a 12 meses (Tabla y Gráfico 9) Tabla y Gráfico 9 Distribución de pacientes según tiempo de evolución de los síntomas Tiempo de evolución con los Frecuencia Porcentaje síntomas <1 mes De 1 a 3 meses De 91 días a 6 meses De 181 días a 9 meses De 271 días a 1 año > 1 año Total 3 2 2 10 12 28 57 5,3% 3,5% 3,5% 17,5% 21,1% 49,1% 100,0% Porcentaje acumulativo 5,3% 8,8% 12,3% 29,8% 50,9% 100,0% 100,0% 30 60,0% 25 50,0% 20 40,0% 15 30,0% 10 20,0% 5 10,0% 0 0,0% <1 mes De 1 a 3 meses De 91 días a De 181 días a De 271 días a 6 meses 9 meses 1 año Frecuencia > 1 año Porcentaje Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez 62 Múltiples estudios, sobre todo en Asia, han recalcado la importancia que tiene la detección del carcinoma gástrico en estadios iniciales (early cancer) para mejorar el pronóstico del paciente. Cuando el tumor rebasa la capa mucosa, ya se considera avanzado y se modifica sensiblemente su clasificación, tratamiento y pronóstico (9, 26, 27). Como sucede en la mayoría de las series, en la población estudiada el medio diagnóstico que se empleó en el 100% de los casos, fue la endoscopia superior (gastroduodenoscopia) con biopsia. La endoscopía de esófago estómago y duodeno con biopsia es el método estándar para el diagnóstico de cáncer gástrico. La técnica es altamente sensible cuando es realizada por especialistas con experiencia, y permite detectar lesiones en estadios precoces. Estudios realizados en Chile, país latinoamericano de alta incidencia de cáncer gástrico, han demostrado que es posible detectar aproximadamente un caso de cáncer por cada 40-50 procedimientos endoscópicos, cuando el tamizaje se focaliza en los adultos (>40 años) sintomáticos, y que alrededor de un 20% de los cánceres detectados de esta forma son incipientes y el 60% son resecables (18, 20, 22). 63 Respecto al tipo de tumor, se observó que en el 100% de los casos se trataba de adenocarcinomas gástricos avanzados con predominio del tipo Bormann III y Bormann IV, con 43,9% y 35,1% respectivamente (Gráfico 6). Tabla y Gráfico 10 Distribución de pacientes según la clasificación del tumor Clasificación del tumor Bormann I Bormann II Bormann III Bormann IV Bormann V Total Frecuencia 1 11 25 20 0 57 Porcentaje 1,8% 19,3% 43,9% 35,1% 0,0% 100,0% 30 50,0% 45,0% 25 25 40,0% 20 35,0% 20 30,0% 15 25,0% 11 20,0% 10 15,0% 10,0% 5 1 0 0 5,0% 0,0% Borrmmann I Borrmmann II Borrmmann III Borrmmann IV Borrmmann V Frecuencia Porcentaje Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez Este hecho indica que cuando hay demora en realizar la endoscopia, sobre todo si el paciente tiene factores de riesgo y síntomas asociados, el diagnóstico se confirma en etapas avanzadas de la enfermedad, limitando las posibilidades terapéuticas y empobreciendo el pronóstico (9, 23). 64 El pronóstico de pacientes con cáncer de estómago depende de la extensión del tumor e incluye tanto compromiso de ganglios como la extensión del tumor directa más allá de la pared gástrica. El grado tumoral también puede suministrar cierta información sobre el pronóstico. El cáncer de estómago distal localizado se puede curar en más del 50% de los pacientes. Sin embargo, actualmente la enfermedad en estadio inicial sólo representa del 10 al 20% de todos los casos. Los demás pacientes presentan enfermedad metastásica en sitios regionales o distantes. La tasa de supervivencia general (TSG) a cinco años de estos pacientes oscila entre ningún caso de supervivencia en pacientes con cáncer de estómago diseminado hasta casi 50% de supervivencia en pacientes con cáncer de estómago distal localizado limitado a una enfermedad regional resecable. Aún con enfermedad localizada visible, la tasa de supervivencia a cinco años en pacientes de cáncer de estómago proximal sólo alcanza entre 10 y 15%. Aunque el tratamiento de pacientes con cáncer de estómago diseminado puede dar como resultado la paliación de los síntomas y cierta prolongación de la supervivencia, las remisiones prolongadas son poco frecuentes. 65 El tiempo de evolución con la enfermedad con respecto al tratamiento recibido se muestra en la Tabla 1. Tabla 11 Distribución de pacientes según tratamiento recibido y tiempo de evolución desde el diagnóstico. Tratamiento recibido Cirugía Tiempo de evolución desde el diagnóstico <1 De 4 a 5 1 a 3 años > 5 años año años Total (%) 11 (19,3%) 3 7 1 0 Quimioterapia 0 2 0 0 2 (3,5%) Radioterapia 0 1 0 0 1 (1,8%) Cirugía + Quimioterapia 5 23 8 7 43 (75,4%) 7 (12,3%) 57 (100,0%) Total (%) 8 33 (57,9%) 9 (15,8%) (14%) Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez Se pudo observar que el 15, 8% de los casos (9 pacientes) se encontraba en el quinto año con su enfermedad. El 12,3% de los casos rebasaba los 5 años de supervivencia, probablemente por una acertada terapia combinada de cirugía + quimioterapia, la cual fue empleada en más de las tres cuartas partes de los casos. El 57,9% de los pacientes se encuentran entre 1 y 3 años de supervivencia. Estudios similares realizados en la provincia de Tungurahua en los años 90 y primer quinquenio de 2000, reportaron una mortalidad de 50% en el primer año 66 del diagnóstico, situación que ha mejorado drásticamente en los últimos años (7, 15, 29). 67 Como parte indispensable de la investigación, se decidió aplicar una encuesta a los pacientes para tener de primera mano la percepción de los enfermos sobre su grado de información y conocimientos sobre el cáncer gástrico, su prevención y tratamiento. Tabla y Gráfico 12 Resultados de las preguntas de la 1 a la 4 de la encuesta a los pacientes Pregunta 1. ¿Conocía usted lo que es el cáncer y sus síntomas? Perfectamente Poco más o menos No conocía Pregunta 2. ¿Conocía cómo prevenir el cáncer gástrico? Perfectamente Poco más o menos No conocía Pregunta 3. ¿Sabía qué hábitos de alimentación y consumo incrementan el riesgo de la enfermedad? Perfectamente Poco más o menos No conocía Pregunta 4. ¿Conocía otros factores de riesgo de la enfermedad? Perfectamente Poco más o menos No conocía Frecuencia Porcentaje 0 51 6 0,0% 89,5% 10,5% Frecuencia Porcentaje 0 33 24 0,0% 57,9% 42,1% Frecuencia Porcentaje 0 18 39 0,0% 31,6% 68,4% Frecuencia Porcentaje 0 32 25 0,0% 56,1% 43,9% 60 51 50 39 40 33 30 32 25 24 18 20 6 10 0 1 Perfectamente 2 3 Poco más o menos 4 No conozco Fuente: Formulario Elaborado por: Leticia Maricela Martínez Sánchez 68 Los resultados de las preguntas de la 1 a la 4 muestran claramente que aproximadamente la mitad de los pacientes consideraban que no tenían conocimientos sobre el cáncer gástrico y el resto que conocían poco al respecto. Tabla y Gráfico 13 Resultados de la pregunta 5 de la encuesta a los pacientes Pregunta 5. ¿Ha recibido alguna información por cualquier vía, Frecuencia Porcentaje sobre las enfermedades malignas por parte del personal del dispensario de salud? Con frecuencia 0 0,0% Esporádicamente 29 50,9% Nunca 28 49,1% 35 29 30 28 25 20 15 10 5 0 0 Frecuentemente Esporádicamente Nunca Fuente: Encuesta Elaborado por: Leticia Maricela Martínez Sánchez En la pregunta 5, el 49,1% de los casos manifestó no haber recibido información alguna sobre la enfermedad por parte del personal del Centro de salud. 69 Tabla y Gráfico 14 Resultados de la pregunta 6 de la encuesta a los pacientes Pregunta 6. ¿Considera necesario ser informado sobre cómo, prevenir, tratar y mejorar el cáncer en general? Totalmente Poco necesario No es necesario Frecuencia Porcentaje 28 29 0 49,1% 50,9% 0,0% 35 30 28 29 25 20 15 10 5 0 0 Totalmente Poco necesario No es necesario Fuente: Encuesta Elaborado por: Leticia Maricela Martínez Sánchez Finalmente, la gran mayoría de los pacientes (94,7%) coincidieron en que era totalmente necesario ser informado sobre cómo, prevenir, tratar y mejorar el cáncer en general y cáncer gástrico en particular. Estos resultados evidencian que aún hay mucho por hacer en nuestras comunidades en materia de promoción y prevención de salud, comenzando tal vez por el difícil proceso de hacer comprender a la población, la importancia de estar bien informados sobre cómo mantenernos sanos, saludables y prevenir enfermedades fatales y temidas como el cáncer gástrico. 70 Conclusiones parciales del capítulo En este capítulo se describió el contexto institucional donde fue llevada a cabo la investigación y explicó detalladamente la metodología investigativa empleada. De igual forma se analizaron y discutieron los resultados de la investigación. Estos aspectos se pueden resumir de la siguiente forma: 1. En el cantón Quero se ha observado y reconocido una elevada prevalencia de cáncer gástrico. 2. Se realizó una investigación observacional descriptiva con el objetivo de determinar los principales factores de riesgo que influyeron en los casos con esta afección atendidos en el Centro de Salud. 3. Más de la mitad de los pacientes con cáncer gástrico eran hombres menores de 60 años. 4. La totalidad de los casos tenían antecedentes familiares de poliposis intestinal o cáncer digestivo. 5. El consumo de tabaco se observó en el 43,9% de los pacientes. 6. Se observó un equilibrio entre los hábitos de consumir alimentos perjudiciales y protectores. 7. Dos tercios de los pacientes eran normopeso y el 24,6% tenía desnutrición según el IMC 8. Las enfermedades de riesgo predominantes fueron la gastritis crónica y la infección con Helicobacter pylori, con 75,4% y 56,1% respectivamente. 9. Más de la mitad de los pacientes llevaba más de un año con síntomas y los predominantes fueron el dolor abdominal y la plenitud postprandial con 70,2% y 56,1% respectivamente. 10. El método Gold estándar para el diagnóstico positivo en el 100% de los casos fue endoscopia superior con biopsia. 11. Más de las tres cuartas partes de los pacientes presentaron un cáncer gástrico avanzado entre los tipos Bormann III y Bormann IV respectivamente. 71 12. Predominaron los pacientes con sobrevida de 1 a 3 años y se observó un 12,3% de sobrevida mayor a 5 años. 13. El tratamiento mayormente empleado fue la combinación de cirugía y quimioterapia en el 75,4% de los pacientes. 14. Más de la mitad de los pacientes manifestaron no tener conocimientos sobre el cáncer gástrico, su diagnóstico, prevención y tratamiento. 72 CAPÍTULO III PLANTEAMIENTO DE LA PROPUESTA La propuesta concreta de la presente investigación fue la elaboración de una guía educativa de prevención del cáncer gástrico dirigida a toda la población del cantón Quero, provincia Tungurahua. Objetivo de la propuesta El objetivo principal de esta propuesta es facilitar un material didáctico que informe a la población de manera clara, comprensible y efectiva los principales hábitos y estilos de vida que constituyen factores de riesgo del cáncer digestivo en general y el cáncer gástrico en particular y como irlos modificando paulatinamente. Beneficiarios de la propuesta Los beneficiarios directos de esta propuesta son las poblaciones de las diferentes comunidades del cantón Quero, donde se ha reconocido una elevada prevalencia del cáncer gástrico. También resulta beneficiada la propia institución de salud, ya que, al disminuirse la incidencia de nuevos casos de cáncer gástrico, se disminuyen los gastos por tratamientos y procederes, así como las posibles demandas. Desarrollo de la propuesta Para el desarrollo de la propuesta, se realizó una exhaustiva revisión bibliográfica de artículos nacionales y extranjeros actualizados, los que sirvieron de referentes teóricos necesarios para llevar adelante el proyecto. Posteriormente se aplicó la encuesta a los pacientes, cuyos resultados, que se discuten en el siguiente 73 capítulo, validaron la necesidad de proponer una guía educativa de prevención del cáncer gástrico. En una etapa inicial se procederá a la selección de un número representativo de técnicos de atención primaria de salud (TAPS), que son aquellas personas de la comunidad que representan la diversidad étnica y cultural, que sean reconocidos y cuenten con el aval de las organizaciones comunitarias, los que serán el primer contacto con la comunidad y recibirán las capacitaciones sobre cómo prevenir y tratar el cáncer gástrico. Los TAPS ayudarán al personal sanitario del Centro de Salud en la planificación y ejecución de charlas, conferencias, talleres y actividades, donde se explique de manera clara, usando lenguaje asequible a las diferentes etnias de la población, los aspectos relacionados con la prevención, diagnóstico y tratamiento de esta afección. De igual forma los TAPS, conjuntamente con el personal médico y de enfermería del centro de salud, llevarán a cabo una campaña publicitaria sistemática donde se emplearán los medios de comunicación, carteles, trípticos y pancartas brindando información sobre la enfermedad. Además, se solicitará colaboración a las autoridades locales y a las organizaciones comunitarias para organizar y llevar a cabo actividades culturales y educativas que involucren a pacientes con cáncer gástrico y sus familiares. Se propone la creación de equipos de trabajo formados por un médico, una enfermera y un TAPS, para organizar una campaña de detección precoz del cáncer de estómago por las diferentes comunidades en coordinación con algún centro endoscópico e histopatológico de las instituciones del MSP y posteriormente realizar coordinaciones con las autoridades de salud provinciales para solicitar agilidad en el tratamiento oncológico. Las acciones terapéuticas se planificarán y realizarán siguiendo las pautas de los protocolos clínicos y terapéuticos para la atención del cáncer gástrico del Ecuador, de la Organización Panamericana de la Salud (OPS) y de la Organización Mundial de la Salud (OMS). 74 Después de elaborada la guía y un tríptico (Ver anexos), se presentará a las autoridades del Centro de Salud y se propondrá un programa de presentación, divulgación y discusión de la misma entre todo el personal sanitario del centro para de esta manera, garantizar su divulgación y disponibilidad en todas las comunidades. Guía de Prevención del Cáncer Gástrico y Educación para la Salud No existe una manera segura de prevenir el cáncer de estómago, aunque hay medidas que puede tomar y que podrían reducir su riesgo de padecerlo. Se piensa que el dramático descenso de la incidencia de cáncer de estómago en las últimas décadas se debe a que las personas han reducido muchos de los factores de riesgo conocidos relacionados con la alimentación. Esto incluye un mayor uso de la refrigeración para guardar alimentos en vez de preservarlos mediante el uso de sal, vinagre o ahumándolos. Para ayudar a reducir su riesgo, evite llevar una alimentación alta en productos ahumados o conservados en vinagre y carnes o pescado salados. Una alimentación rica en frutas, ensaladas y verduras frescas también puede disminuir el riesgo de cáncer de estómago. Las frutas cítricas (naranjas, limones y toronjas) pueden ser especialmente beneficiosas, aunque la toronja y el jugo de toronja pueden cambiar los niveles sanguíneos de ciertos medicamentos que esté tomando. Por lo tanto, es importante que hable con su médico antes de agregar toronja a su alimentación. La Sociedad Americana Contra El Cáncer recomienda comer alimentos saludables, enfatizando en aquéllos de fuente vegetal. Esto incluye comer al menos una cantidad de frutas y verduras equivalente a 2½ tazas todos los días. Escoger panes, pastas y cereales de granos enteros (productos integrales) en lugar de granos refinados, así como comer pescado, aves o habas en lugar de carnes rojas y procesadas puede que también sea útil para reducir el riesgo de cáncer. 75 Los estudios que han estado analizando el uso de suplementos dietéticos para reducir el riesgo de cáncer de estómago han arrojado resultados diversos hasta el momento. Algunos estudios han sugerido que las combinaciones de suplementos antioxidantes (vitaminas A, C, y E y el mineral selenio) pueden reducir el riesgo de cáncer de estómago en las personas con pobre nutrición. No obstante, la mayoría de las investigaciones que estudian a las personas que tienen una buena nutrición no han encontrado ningún beneficio en agregar pastillas de vitaminas a la alimentación. Se requiere realizar más investigación en esta área. Aunque algunos estudios a menor escala sugieren que tomar té, particularmente el té verde, puede que ayude a proteger contra el cáncer de estómago, la mayoría de los estudios a mayor escala no han encontrado esta relación. Puede que el sobrepeso o la obesidad contribuyan al riesgo del cáncer de estómago. Por otro lado, la actividad física puede ayudar a reducir su riesgo. La Sociedad Americana Contra El Cáncer recomienda mantener un peso saludable durante el transcurso de la vida al balancear el consumo calórico con la actividad física. Aparte de los posibles efectos sobre el riesgo del cáncer de estómago, bajar de peso y estar activo puede además tener un efecto sobre el riesgo de otros tipos de cáncer y problemas de salud. El uso de tabaco puede aumentar el riesgo de padecer cáncer de estómago proximal (la sección del estómago más cercana al esófago). El uso del tabaco aumenta el riesgo de muchos otros tipos de cáncer y es el responsable de aproximadamente una tercera parte de todas las muertes por cáncer. Todavía no está claro si las personas cuyos revestimientos del estómago han sido infectados crónicamente con la bacteria H pylori, pero que no tienen síntomas, deben ser tratadas con antibióticos. Esto se está estudiando actualmente. Algunos estudios preliminares han sugerido que administrar antibióticos a las personas infectadas con H pylori puede reducir el número de lesiones precancerosas en el estómago y puede reducir el riesgo de cáncer de estómago. Sin embargo, no todos los estudios han coincidido en esto. Se necesitan más 76 estudios para asegurarse de que ésta es la manera de prevenir el cáncer de estómago en las personas infectadas con H pylori. El uso de aspirina u otros agentes antiinflamatorios no esteroideos (NSAIDs), como el ibuprofeno o naproxeno, parece reducir el riesgo de cáncer de estómago. Estos medicamentos también pueden reducir el riesgo de pólipos en el colon y cáncer colorrectal. Sin embargo, pueden también causar sangrado interno grave (incluso fatal) y otros riesgos potenciales de salud en algunas personas. La mayoría de los médicos consideran cualquier reducción en el riesgo de cáncer un beneficio añadido para los pacientes que toman estos medicamentos por otras razones, como para tratar la artritis. No obstante, los médicos no recomiendan tomar rutinariamente agentes antiinflamatorios no esteroides específicamente para prevenir el cáncer de estómago. Los estudios todavía no han determinado en qué pacientes los beneficios de reducir el riesgo de cáncer sobrepasan los riesgos de sangrado. 77 CONCLUSIONES GENERALES 1. En la caracterización de los pacientes afectados con cáncer gástrico predominaron los pacientes del sexo masculino con edades de hasta 60 años, normopeso, fumadores, con más de un año de síntomas y carcinoma gástrico tipo Bormann IV. 2. Más de la mitad de los pacientes manifestaron no tener conocimientos sobre el cáncer gástrico y que no habían recibido información al respecto por parte del personal del centro de salud. 3. Los principales factores de riesgo de cáncer gástrico observados en la población estudiada fueron: Alto consumo de tabaco, alcohol, alimentos ahumados y conservados. Antecedentes personales de gastritis e infección con Helicobacter Pylori. Antecedentes familiares de poliposis o cáncer intestinal. Desconocimiento de la enfermedad. 78 RECOMENDACIONES Al finalizar el estudio se hacen las siguientes recomendaciones: 1. Realizar investigaciones similares en todos los cantones de Tungurahua por ser una de las provincias de mayor incidencia de cáncer de estómago en el país. 2. Organizar una campaña masiva de prevención y educación en salud sobre esta afección, apoyada en los medios de comunicación y rectorada por las autoridades de salud. 3. Divulgar la propuesta de la investigación por todos los centros asistenciales de atención primaria. 4. Organizar en la universidad un taller de actualización sobre prevención, diagnóstico precoz y tratamiento del cáncer gástrico destinado a todos los internos y médicos recién graduados. 79 BIBLIOGRAFÍA 1. Mandal A. Historia del Cáncer. Online. Publicado en febrero de 2014. Consultado en abril de 2016. Disponible en: http://www.news- medical.net/health/Cancer-History-(Spanish).aspx. 2. Palacios MAE. Historia del cáncer. Online. Publicado en mayo de 2015. Consultado en abril de 2016. Disponible en: http://www.laprensagrafica.com/2015/05/17/historia-delcancer#sthash.vyP7paRB.dpuf 3. Salaverry O. La etimología del cáncer y su curioso curso histórico. Rev. perú. med. exp. salud pública. 2013; 30(1):137-141. 4. Galindo F. Carcinoma gástrico. Cirugía Digestiva. 2009; II (223):1-31. 5. Galvão de Azevêdo I, Leal MCI, Oliveira TM, Pessoa de Araújo BM. Gastric cancer and associated factors in hospitalized patients. Nutr Hosp. 2015; 32 (1): 283-290. 6. Beltrán G.¿Está cambiando la epidemiología del cáncer de estómago en Colombia? Rev Col Gastroenterol. 2005;20 (1):5-6. 7. Aguilar A, Echeverria E, Tamayo L, Martinez N, Corral F, Yépez J, Cueva P. Cáncer gástrico en la provincia de Tungurahua, 1996-1998. Acta científica ecuatoriana. 2001; 7(1). 8. Burmeister L, Fernández P, Covacevich, R. Experiencia de 15 años en el manejo del cáncer gástrico incipiente. Rev. chil. Cir.1987; 39(1):23-9. 9. Maruyama K, Okabayashi K, Kinoshita T. Progress in gastric cancer surgery in Japan and its limits of radicality. World journal of surgery. 1987;11(4):418-425. 10. Oliveros Ricardo, Navarrera LF. Diagnóstico, estadificación y tratamiento del cáncer gástrico en Colombia desde 2004 a 2008 (REGATE -Colombia). Revista Colombiana de Gastroenterología. 2012;27(4):269-274. 11. Emura F, Oda I. Diagnóstico y tratamiento endoscópico del cáncer gástrico estado 0. ¿Qué hacer para que aumente más? Revista Colombiana de Gastroenterología. 2009; 24(4):333-335. 12. Gómez M, Otero W, Arbeláez V. Tratamiento endoscópico de cáncer gástrico temprano en Colombia con seguimiento a cinco años. Revista Colombiana de Gastroenterología. 2009; 24(4):347-352. 13. Alvarado TC, Venegas OD. Sobrevida de pacientes con cáncer gástrico en el Perú, 2009–2010. Rev Panam Salud Publica.2015; 37(3):133–9. 14. Cueva P, Yépez J. Registro Nacional de Cáncer Gástrico. Quito: SOLCA. 2010. 15. Tamayo L, Aguilar SA, Martínez N, Echeverría ME. Incidencia de cáncer gástrico Tungurahua. Primer quinquenio 1996-2000. Oncología 2003; 12(4): 237-245. 16. Espejo RH, Navarrete SJ. Cáncer Gástrico Temprano: estudio de 371 lesiones en 340 pacientes en el Hospital E. Rebagliati. Lima-Perú. Revista de Gastroenterología del Perú. 2005; 25(1):48-75. 17. Howson CP, Hiyama T, Wynder EL. The decline in gastric cancer: epidemiology of an unplanned triumph. Epidemiologic Reviews.1986; 8(1):1-27. 18. Wagner AD, Grothe W, Haerting J, Kleber G, Grothey A, Fleig WE. Chemotherapy in advanced gastric cancer: a systematic review and metaanalysis based on aggregate data. Journal of Clinical Oncology. 2006; 24(18): 2903-2909. 19. Meng W, Bai B, Sheng L, Li Y, Yue P, Li X, Qiao L. Role of Helicobacter pylori in gastric cancer: advances and controversies. Discov Med. 2015; 20 (111):285-93. 20. Donoso D, Sharp A, Parra BA, Roa A, Bächler JC, Crovari JP, Funke F, Pimentel R, Ibáñez F, Guzmán LS, Endoscopic submucosal dissection in early gastric cancer: Experience in 16 patients. Revista médica de Chile. 2015; 143(10):1277-1285. 21. Hernández RRU, López CL. Dieta y cáncer gástrico en México y en el mundo. Salud Pública de México. 2014;56(5):555-560. 22. Latorre SG, Álvarez OJ, Ivanovic ZSD, Valdivia CG, Margozzini MP, Chianale BJ, Miquel PJF. Cobertura de la estrategia preventiva de cáncer gástrico en Chile: resultados de la Encuesta Nacional de Salud 2009-2010. Revista médica de Chile. 2015; 143(9):1198-1205. 23. Dong JG, Kun Y, Wei HZ. Prognostic Value of Metastatic No.8p LNs in Patients with Gastric Cancer. Gastroenterology Research and Practice. 2015; 7. 24. Eurogast Study Group. An international association between Helicobacter pylori infection and gastric cancer. The Lancet. 1993; 341(8857): 13591363. 25. Gutiérrez B, Cavazza ME, Ortiz D, Correnti M, Vidal T, Mégraud F, Álvarez P. Seroprevalencia de la infección por Helicobacter pylori en pacientes con Gastritis Crónica, Úlcera Duodenal y Gástrica: Primer estudio de corte retrospectivo. Revista Cubana de Investigaciones Biomédicas. 2008; 27(2). 26. Japanese Gastric Cancer Association. Japanese gastric cancer treatment guidelines 2010 (ver. 3). Gastric cáncer. 2011; 2(14):113-123. 27. Matta de García VL, De León JL. Caracterización del cáncer gástrico en Guatemala. Revista Científica de la Facultad de Ciencias Químicas y Farmacia. 2015;25 (2). 28. Nakajima T. Gastric cancer treatment guidelines in Japan. Gastric cancer. 2002; 5(1):1-5. 29. Robles C, Tamayo L, Martínez N, Aguilar A, Lascano C. Epidemiología del Cáncer Gástrico en Tungurahua. Resultados del Cantón Quero. Revista SOLCA. 1995;4(1-2). 30. Pérez MG. Filosofía de la enfermedad: vulnerabilidad del sujeto enfermo. Arch. argent. pediatr. 2007; 105 (2): 134-142 31. Clasificación Internacional de Enfermedades 10°. CIE 10° REVISION. Online. Consultado en abril de 2016. Disponible en: http://www.sssalud.gov.ar/hospitales/archivos/cie_10_revi.pdf. 32. Roder DM. The epidemiology of gastric cancer. Gastric cancer. 2002; 5(1):5-11. 33. Manual del Modelo de atención integral de salud. MSP Ecuador. 2012 34. Instituto nacional del cáncer. USA: NCI; (actualizado 1ro de julio de 2015; consultado en abril 2016). Disponible en: http://www.cancer.gov/espanol/cancer/sobrellevar/sentimientos/ansiedadsufrimiento-pdq#section/_1 35. American Cancer Society. USA: ACS; (actualizado el 11 de febrero de 2016; consultado en abril de 2016). Disponible en: http://www.cancer.org/espanol/cancer/cancerdeestomago/guiadetallada/ca ncer-de-estomago-early-diagnosis ANEXOS Anexo 1. Formulario de consentimiento informado para participar en la investigación Título de la investigación: Factores clínicos y epidemiológicos del cáncer de estómago en pacientes atendidos en el centro de salud del cantón Quero, Tungurahua. Año 2014. Investigadora: Leticia Maricela Martínez Sánchez Sitio donde se llevará a cabo el estudio: Centro de salud del Catón Quero, provincia Tungurahua Entidad que respalda la investigación: Universidad Regional Autónoma de Los Andes. Uniandes. Usted ha sido invitado(a) a participar en la presente investigación que tiene como objetivo conocer los principales factores clínicos y epidemiológicos del cáncer de estómago en pacientes atendidos en el centro de salud del cantón Quero, Tungurahua, durante el quinquenio 2010-2015. Participarán en el estudio un total de 57 pacientes con diagnóstico conocido de cáncer gástrico del cantón Quero y durante el mismo solamente se le aplicará una encuesta anónima, con completa garantía de su privacidad, la cual contendrá datos generales suyos y en la que usted responderá preguntas cerradas que no afectarán su dignidad. El proyecto durará unos seis meses y se realizarán varias visitas en el terreno. Usted no corre ningún riesgo físico, ni psicológico participando en la investigación y no tendrá que realizar pago alguno. Tampoco recibirá ningún beneficio ni pago directo. La información obtenida será resguardada en los archivos y repositorios de la Universidad Regional Autónoma de los Andes, donde se podrá tener acceso a la misma a través de Internet. En cualquier momento, todas sus dudas serán aclaradas. Consentimiento por escrito: He leído, comprendido y discutido la información anterior con el investigador responsable del estudio y mis preguntas han sido respondidas de manera satisfactoria. Mi participación en este estudio es voluntaria, podré renunciar a participar en cualquier momento, sin causa y sin responsabilidad alguna. He sido informado y entiendo que los datos obtenidos en el estudio pueden ser publicados o difundidos con fines científicos y/o educativos. Acepto participar en este estudio de investigación _____________________________________ Firma del participante y Fecha Anexo 2. Ficha de recolección de datos UNIVERSIDAD REGIONAL AUTÓNOMA DE LOS ANDES UNIANDES. FACULTAD DE CIENCIAS MÉDICAS Ficha de recolección de datos. Título de la investigación: Factores clínicos y epidemiológicos del cáncer de estómago en pacientes atendidos en el centro de salud del cantón Quero, Tungurahua. Período 2010-2015. Investigadora: Leticia Maricela Martínez Sánchez Sitio donde se llevará a cabo el estudio: Centro de salud del Catón Quero, provincia Tungurahua Entidad que respalda la investigación: Universidad Regional Autónoma de Los Andes. Uniandes. No. Consecutivo: ________ Historia clínica: ______________________ I. Edad: II. Sexo 1. De <35 años____ 1. Masculino: ____ 2. De 36 a 50 años____ 2. Femenino: ____ 3. De 51 a 60 años____ 4. De 61 a 70 años____ IV. Hábitos tóxicos 5. >70 años____ 1. Tabaco___ 2. Alcohol___ III. Antecedentes familiares de cáncer o 3. Café___ poliposis intestinal 4. Drogas___ 1. Si___ 5. Ninguno___ 2. No___ V. Hábitos alimentarios y farmacológicos VI. Estado nutricional (Consumo semanal de:) 1. Desnutrido___ 6. Ahumados y embutidos___ 2. Normopeso_____ 7. Alimentos conservados___ 3. Sobrepeso____ 8. Frutas y vegetales___ 4. Obeso____ 9. Pescado fresco____ VIII. Síntomas y signos 10. Aspirina___ 1. Asintomático____ VII. Comorbilidades y antecedentes 2. Dolor abdominal____ de riesgo 3. Dispepsia tipo ulcerosa____ 1. Gastritis crónica__ 4. Saciedad precoz o plenitud 2. Enfermedad úlceropéptica__ posprandial___ 3. Infección con Helicobacter pylori__ 5. Anemia___ 4. Linfoma gástricos__ 6. Pérdida de peso___ 5. Cirugía gástrica previa__ 7. Ascitis____ 6. Pólipos intestinales___ 8. Tumor palpable___ 7. Otras (Explicar)__ 9. Disfagia____ 10. Otro (Explicar)___ IX. Tiempo de evolución con los síntomas X. Medio diagnóstico del hallazgo 1. <1 mes___ 1. Endoscopia___ 2. De 1 a 3 meses___ 2. Estudios radiológicos 3. De 91 días a 6 meses___ contrastados__ 4. De 181 días a 9 meses__ 3. Estudios tomográficos___ 5. De 271 días a 1 año___ 4. Estudios sonográficos 6. > 1 año______ 5. En el curso de otra cirugía__ 6. Otro (Explicar) XI. Tipo de tumor resultado de la biopsia) (Transcribir el X. Tratamiento recibido XII. Tiempo de evolución desde el 1. Cirugía____ diagnóstico 2. Quimioterapia__ 1. < 1 año 3. Radioterapia__ 2. 1 a 3 años 4. Hormonoterapia_ 3. De 4 a 5 años 5. Combinaciones (explicar)___ 4. > 5 años ANEXO 3 Encuesta a los pacientes Estimado paciente, esta es una encuesta anónima para determinar su nivel de conocimientos sobre el cáncer de estómago antes de habérsele realizado el diagnóstico. Se agradece que proporcione la respuesta que considere más adecuada a su realidad con la mayor sinceridad. 1. ¿Conocía usted lo que es el cáncer y sus síntomas? a. Perfectamente____ b. Poco más o menos___ c. No conocía____ 2. ¿Conocía cómo prevenir el cáncer gástrico? a. Perfectamente____ b. Poco más o menos___ c. No conocía____ 3. ¿Sabía qué hábitos de alimentación y consumo incrementan el riesgo de la enfermedad? a. Perfectamente____ b. Poco más o menos___ c. No conocía____ 4. ¿Conocía otros factores de riesgo de la enfermedad? a. Perfectamente____ b. Poco más o menos___ c. No conocía____ 5. ¿Ha recibido alguna información por cualquier vía, sobre las enfermedades malignas por parte del personal del dispensario de salud? a. Con frecuencia_____ b. Esporádicamente____ c. Nunca______ 6. ¿Considera necesario ser informado sobre cómo, prevenir, tratar y mejorar el cáncer en general? a. Totalmente___ b. Poco necesario___ c. No es necesario______