ESTUDIO CINÉTICO DE LA REACCIÓN ENTRE DE LA REACCIÓN
Anuncio

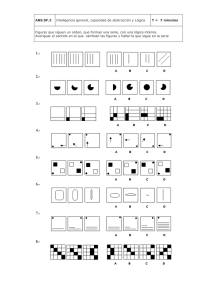
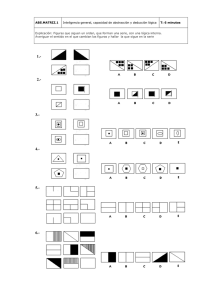
ESTUDIO CINÉTICO DE LA REACCIÓN ENTRE EL YODO Y LA ACETONA CATALIZADA POR ÁCIDO Laboratorio de Química Física I 2009-2010 Remedios González Luque 1 OBJETIVO Determinación de la ley de velocidad: órdenes de reacción y constante de velocidad absoluta de la reacción de yodación de la acetona en medio ácido mediante un procedimiento químico H CH 3 CO CH 3 I2 CH 3 CO CH 2 I HI v k abs [ Acet A ] [ H ] [I 2 ] Laboratorio de Química Física I 2009-2010 Remedios González Luque 2 ¿Porqué se utiliza un procedimiento químico? ¿De qué componente es fácil seguir su evolución? ¿Cómo lo haremos? H CH 3 CO CH 3 I2 CH 3 CO CH 2 I HI I2 I2 + 2 Na2S2O3 Na2S4O6 + 2 NaI ¿Qué otro método podríamos seguir? ¿Qué cambio observaremos? Laboratorio de Química Física I 2009-2010 Remedios González Luque 3 ¿Respecto a que componente expresaremos la ecuación de velocidad? H CH 3 CO CH 3 I2 CH 3 CO CH 2 I HI v d[I 2 ] k abs [ Acet ] [ H ] [I 2 ] dt ¿Qué condiciones deben cumplirse para seguir la evolución de la reacción respecto al yodo? [H ]o , [Acet]o [I 2 ]o v [H ], ] [Acet] ctes d[I 2 ] k ap [I 2 ] dt k ap k abs [Acet A ]o [H ]o Laboratorio de Química Física I 2009-2010 Remedios González Luque 4 ¿Porqué podemos suponer que el orden respecto al yodo es cero? rápido CH3-CO-CH3 + H+ CH3-COH + -CH3 CH3-COH=CH COH CH2 + I2 0 lento CH3-COH=CH2 + H + CH3-COCH COCH2I + IH rápido d[I 2 ] v k ap [I 2 ]0 k ap dt ¿Cómo podemos comprobar que el orden respecto al yodo es cero? I2 t 0 [I 2 ] [I 2 ]0 k ap t kap = -pendiente ¿Cómo vamos a seguir la evolución de la concentración de yodo? Laboratorio de Química Física I 2009-2010 Remedios González Luque t 5 I2 + 2 Na2S2O3 Na2S4O6 + 2 NaI Na2S2O3 1 n I 2 n Na 2S2 O 3 2 I 2 VI 2 1 Na 2S2O3 VNa 2S2 O 3 2 1 [S2O32 ] [ I 2 ]t Vt (S2O32 ) cte Vt (S2O32 ) 2 Valic (I 2 ) 1 [S2O32 ] cte 2 Valic (I 2 ) [I 2 ] [I 2 ]0 k ap t Laboratorio de Química Física I 2009-2010 Remedios González Luque 6 cte Vt (S2O32 ) cte V0 (S2O32 ) k ap t k ap 2 2 Vt (S2O3 ) Vo (S2O3 ) t cte Vt k’ap = -pendiente Vt Vo k 'ap t t kap k app cte k ap k abs [Acet]o [H ]o 1 [S2O32 ] cte 2 Valic (I 2 ) Laboratorio de Química Física I 2009-2010 Remedios González Luque 7 Vt Vt Vo k 'ap t k’ap = -pendiente t Ya sabemos como comprobar que el orden respecto al yodo es cero. ¿Cómo p podemos obtener el orden respecto p a la acetona y el yodo? y ¿Habéis hecho antes algo similar en otra experiencia? ¿Cómo lo hacíais? Estudio cinético de la decoloración de la fenolftaleina. Laboratorio de Química Física I 2009-2010 Remedios González Luque 8 Vacet VHCl Vt Serie 1 5 5 k'ap11 k Serie 2 15 3 k'ap2 Serie 3 15 5 k'ap3 k ¿Qué recta se corresponde con cada serie? -k’ap1 -k’ap3 ¿Porqué q se utilizan volúmenes iguales g de ácido y acetona en las diferentes series? V(HCl)1 = V(HCl) 3 -k’ap2 t [HCl]1 = [HCl] 3 Series 1 y 3 permiten determinar (orden acetona) V(Acet)2 = V(Acet)3 [Acet]2 = [Acet]3 S i 2 y 3 permiten Series it d determinar t i (orden ( d H+) ¿Cómo están relacionadas k’app y las concentraciones de ácido y acetona? Laboratorio de Química Física I 2009-2010 9 Remedios González Luque 1 [S2O32 ] cte 2 Valic (I 2 ) k ap i k abs [ Acet A ]o,i [H ]o,i (k ap )1 kap1 cte k abs [Acet]o,1 (k ap )3 kap 3 cte k abs [Acet] o3 o,3 k ap i kap i cte [[Acet]] o1 o,1 ln ln (kap )3 [Acet]o,3 (kap )1 [Acetona]i (moles acet)i g(Acet) / M r (g / mol) i VT VT [HCl] [Acet]o,1 o,1 [HCl]o,3 [Acet] o3 o3 o,3 ¿Cómo están relacionadas las concentraciones de acetona en el medio de reacción con los volúmenes de acetona utilizados tili d all preparar lla mezcla de reacción? Acet (Vacet )i riq(%) M r (g / mol o) [Acetona A ]i cte (Vacet )i VT Laboratorio de Química Física I 2009-2010 (V ) ln ln acet 1 (V ) (kap )3 acet 3 (kap )1 Remedios González Luque 10 ¿Cómo se determina el orden para el catalizador, H+? k ap i k abs [ Acet ] [ H ]o,i o,i (kap ) 2 k abs [Acet]o,2 (kap )3 k abs [Acet] o,3 k ap i kap i cte [HCl] o,2 ln ln (kap )3 [HCl]o,3 (kap ) 2 (VHCl )i [H ]o [H ]i cte(VHCl )i VT [HCl] [HCl] o,2 o,2 [HCl]o,3 [HCl]o,3 ¿Cómo están relacionadas las concentraciones de ácido á en el medio de reacción con los volúmenes de ácido utilizados tili d all preparar lla mezcla de reacción? (V ) ln ln HCl 2 ((V ) (kapp )3 HCl 3 Laboratorio de Química Física I 2009-2010 (kap ) 2 Remedios González Luque 11 ¿Cómo se determina la constante de velocidad, kabs? o k abs o k ap k abs [Acet] [H ] k ap k ap cte k abs k (abs)i k ap [Acet] [ H ]o o 1 [S2O32 ] cte 2 Valic (I 2 ) k 'ap cte [Acet]o [H ]o kap [S2O32 ] 1 i 2 [Acet]o,i [H ]o,i Valic ( I 2 ) k abs t ( 2,0.975) s(k abs ) k abs t (2,0.975) s(k absi ) 3 ¿Hemos cubierto los objetivos? Recapitulemos Laboratorio de Química Física I 2009-2010 Remedios González Luque 12 H CH 3 CO CH 3 I2 CH 3 CO CH 2 I HI d[ I 2 ] v k abs [Acet ] [ H ] [ I 2 ] dt VAcet VHCl Serie 1 5 5 k'ap1 Serie 2 15 3 k'ap2 Serie i 3 15 5 k'ap3 Vt k’op = -pendiente t kap [S2O32 ] 1 k abs 2 [Acet]o [H ]o Valic (I 2 ) Laboratorio de Química Física I 2009-2010 ¿Falta algo? Remedios González Luque 13 UNIDADES ml kap k app M k (abs)i Vt k’ap = -pendiente t-1 t t-1 M-1 t-1 k abs Vt Vo k 'ap t [I 2 ] [I 2 ]0 k ap t I2 t kap = -pendiente kap [S2O32 ] i 1 2 [Acet]o,i [H ]o,i Valic (I 2 ) t k abs k ap [Acet] o [ H ]o ¿Cómo vamos a realizar la experiencia? ¿Qué es lo primero que hacemos? Laboratorio de Química Física I 2009-2010 Remedios González Luque 14 PROCEDIMIENTO EXPERIMENTAL Comprobar el nivel de agua. Conectar el baño termostático. Comprobar la temperatura. temperatura ¿Hay que tener alguna ¿Qué hacemos a continuación? precaución? PREPARAR LAS DISOLUCIONES 1) I2 0.06 M. Preparada. ¿Cómo es el I2? ¿Cómo se p prepara p la disolución? ¿Porqué se da preparada? 2) 500 mL de Na2S2O3 0.005 M I 2(s) ¿Dónde se guarda la disolución de tiosulfato ? ¿porqué? ¿En q que balanza se p pesa el tiosulfato? O Laboratorio de Química Física I 2009-2010 +6 O - -2 S O I 2/I- (aq) S - OO S O O- Remedios González Luque 15 DISOLUCIONES 3) 250 mL de HCl 1.2 M (común a toda la mesa). EN LA VITRINA ¿Cómo se prepara? agua 4) 250 mL de AcNa al 2.5 % en peso ¿Para qué se utiliza está disolución? ¿Qué valor tiene la constante de equilibrio de esta reacción? ¿En que balanza b l n se s pesa p s el acetato? AcNa - Ac + + Na Ac- + H+ HAc K = 1/KHAc = 5 104 Laboratorio de Química Física I 2009-2010 Remedios González Luque 16 Una vez preparadas las disoluciones ¿Qué Q hacemos a continuación? VNaOH = 12 mL NaOH 1M VALORAR LA DISOLUCIÓN DE HCl ¿Porqué valoramos el HCl? ¿Con qué valoramos el HCl? Fenolftaleína ¿Qué indicador utilizamos? ¿Cuál á será á el pH en el punto de equivalencia? ¿Qué volumen de HCl utilizamos en la valoración? ¿Cómo mediremos este volumen? ¿Qué volumen de sosa se gastará en la valoración? ¿Cuántas valoraciones hacemos? HCl 1.2M 10 mL ¿En qué bureta? Laboratorio de Química Física I 2009-2010 Remedios González Luque 17 v k abs [ Acet ] [ H ] [I 2 ] Una vez valorado el HCl se realizan las tres series correspondientes a [H ]i cte(VHCl )i diferentes volúmenes de HCl y acetona. ¿Porqué se realizan tres series y [Acet]i cte (Vacet )i porqué estos volúmenes? VAcet*VHCl VAcet VHCl Serie 1 5 5 25 por la serie 1? p Serie 2 15 3 45 Serie 3 15 5 75 ¿Porqué es mas lenta ¿Porqué se comienza la serie 1? El volumen de yodo, es siempre el mismo ¿Porqué? Recordad que la reacción es de orden cero respecto al yodo ¿Qué implica esto? Si la velocidad de reacción no depende de la concentración de yodo ¿Qué sucedería si añadiéramos diferentes volúmenes de yodo? Laboratorio de Química Física I 2009-2010 Remedios González Luque 18 Serie 1: 5 mL de acetona y 5 mL de ácido clorhídrico 1 1.2 2 M ¿Cómo se p prepara p la mezcla de reacción? 5 mL HCl 1.2 M 5 mL acetona 100 mL 100 mL 50 mL agua g Erlenmeyer 250 mL ¿Qué hacemos mientras se alcanza el equilibrio térmico? Laboratorio de Química Física I 2009-2010 Remedios González Luque 19 Preparar los erlenmeyesrs con NaAc. ¿P ¿Porqué é hay h que tener t n preparados p p d s los l s erlenmeyers l nm s con n NaAc? N A ? ¿Con qué medimos los NaAc 10 mL de NaAc? . . . SIETE erlenmeyers con 10 mL NaAc ¿Cuándo se alcance el equilibrio térmico qué hacemos? 20 Laboratorio de Química Física I 2009-2010 Remedios González Luque ¿Dónde se añade el yodo? ¿En el baño? 10 mL I2 NO mezclar l vigorosamente 10 mL mezcla de reacción 110 mL 100 mL t=0 10 mL NaAc ¿Dónde se toman las alícuotas de la mezcla de reacción? ¿En el baño? t=t ¿Cuándo se toma tiempo cero? ¿Cuándo se toma el tiempo de reacción? Laboratorio de Química Física I 2009-2010 Remedios González Luque 21 Antes de continuar con la experiencia. ¿Estamos seguros que procedemos correctamente? I2 0.06M ACE TONA d= 0.7945 g/mL / riq = 99.5 %, Mr = 58.08 ¿Podemos ¿P d m s aplicar pli ell método de aislamiento de Ostwald? 1 HClserie tt 0 1.2 M 5 mL 1 Acet A tserie 13 . 611 M t 0 110 mL 5 mL 110 mL L 5.454 10 2 M 6.19 101 M HCl 1.2M I 2 t 0 0.06 M 10 mL 110 mL 5 mL acetona 13.611 M 110 mL ¿Cuáles serán las concentraciones de ácido y acetona en el medio de reacción. ó Cuestión ó 3? 5.45103 M ¿La concentración de yodo es mucho menor que la de ácido y acetóna? 10 mL I2 0.06M ??????? I 2 t 0 5.45103 M HCl t 0 5.45102 M Laboratorio de Química Física I 5 mL HCl 1.2 M 22 Remedios González Luque Hemos recogido la muestra de reacción en el erlenmeyers con acetato sódico ¿Es necesario valorar la muestra inmediatamente? ¿Cómo sabremos que hemos llegado al punto de equivalencia? ¿C ánd sse añade ¿Cuándo ñ d ell indi indicador? d ? Na2S2O3 ALMIDÓN ¿Cómo irá ¿Có i á cambiando el color de la muestra de reacción? 10 mL I2+almidón I2 23 Laboratorio de Química Física I Remedios González Luque ¿Cuántas muestras tomaremos y cada cuanto tiempo? ¿En las l s sucesivas s si s valoraciones l i n s gastaremos st m s más o menos volumen de tiosulfato? H CH 3 CO CH 3 I2 CH 3 CO CH 2 I HI ¿Cómo podemos saber si los volúmenes de lf que gastamos son correctos? tiosulfato ¿Qué volumen de tiosulfato se gastaría a t = 0? Cuestión 13 I2 + 2 Na2S2O3 Na2S4O6 n I2 VNa 2S2 O 3 1 n Na 2S2 O 3 2 2I 2 VI 2 Na 2S2O3 + 2 NaI I 2 VI 2 1 Na 2S2O3 VNa 2S2 O 3 2 VI 2 volumen de la alícuota que se valora I 2 concentracíón de yodo en el medio de reacción Remedios González Luque Laboratorio de Química Física I 24 t=0 Aalícuota de 10 mL VNa 2S2 O 3 2I 2 VI 2 Na2S2O3 Na N 2S2O3 ¿Cuál es [I2], ] [Na2S2O3] y VI2 ? 110 mL VI 2 I 2 t 0 0.06 M 10 mL 110 mL [Na2S2O3] = 0.005 M VNa 2S2 O 3 = Valícuota = 10 mL 5.4510 3 M 10 mL ¿Será esta concentración? 2 5.45 103 M 10 mL 5 10 3 21.8 mL M Laboratorio de Química Física I 2009-2010 Remedios González Luque 25 Una vez terminada la experiencia se realizan las series 2 y 3 Serie 2: 15 mL de acetona y 3 mL de ácido clorhídrico R Repetir ti ell experimento, i t según ú lo l indicado i di d para lla serie i 11, extrayendo las muestras cada 6 minutos. Serie 3: 15 mL de acetona y 5 mL de ácido clorhídrico Repetir el experimento, según lo indicado para la serie 1, extrayendo las muestras cada 4 minutos. ¿Porqué en estas series los intervalos de tiempo son menores? v k abs [ Acet A t ] [ H ] [I 2 ] VAcet VHCl VAcet*VHCl Serie 1 5 5 25 Serie 2 15 3 45 Serie 3 15 5 75 Laboratorio de Química Física I Remedios González Luque 26