tecnologia quimica
Anuncio

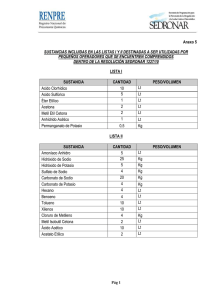
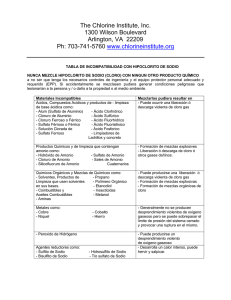
TECNOLOGIA QUIMICA UNIDAD 1 Industria basada en compuestos inorgánicos PRODUCCIÓN DE CLORO E HIDRÓXIDO DE SODIO • La industria cloro –alcali produce cloro Cl2 e hidróxido de sodio a partir de la electrólisis de una solución salina de NaCl. • En la electrólisis, se forma hidrógeno en el cátodo y cloro en el ánodo PRODUCCIÓN DE CLORO E HIDRÓXIDO DE SODIO • Electrolisis con celda de amalgama de mercurio • Fue el primer método empleado para producir cloro a escala industrial. • Se emplea un cátodo de mercurio y un ánodo de titanio recubierto de platino u óxido de platino. PRODUCCIÓN DE CLORO E HIDRÓXIDO DE SODIO • Proceso de Diafragma: En este proceso se emplean disoluciones acuosas de NaCl. Las celdas industriales de diafragma consisten en un depósito en el cual los ánodos se montan verticalmente y paralelos unos a otros. Los cátodos se sitúan entre los ánodos, son planos y de acero, recubiertos por fibras de asbesto impregnados con resinas flúor-orgánicas. PRODUCCIÓN DE CLORO E HIDRÓXIDO DE SODIO • Proceso de Membrana: En este proceso el cátodo y el ánodo se encuentran separados por una membrana conductora iónica que es impermeable al agua, pero es permeable al paso de iones. Acido clorhídrico • Acido Clorhídrico: El Cloruro de Hidrógeno se produce comercialmente por cualquiera de las siguientes vías: • Proceso Hargreaves : Este proceso está en desuso, debido a la dificultad de lograr Acido concentrado a partir de soluciones diluidas de gas y al incremento en la mano de obra. • Acido clorhídrico • Proceso Sintético: El Cloruro de Hidrógeno se puede sintetizar por la combustión de una mezcla controlada de Cloro e Hidrógeno. • Cloruro de Hidrógeno como Subproducto: La cloración de muchos químicos orgánicos genera Cloruro de Hidrógeno como subproducto. • R-H + Cl2 → R-Cl + HCl (Reacción 1) R-Cl + HF → R-F + HCl (Reacción 2) CARBONATO DE SODIO • Proceso Leblanc :Fue el primer proceso para obtener artificialmente carbonato de sodio (sosa).Haciendo reaccionar sal común (HCl)con ácido sulfúrico (H2SO4) para dar sulfato de sodio (Na2SO4)(1), que posteriormente se quema con carbón y piedra caliza para obtener carbonato de sodio (Na2CO3) CARBONATO DE SODIO • Proceso Solvay: El proceso Solvay utiliza sal común NaCl y piedra caliza CaCO3 como materias primas, el amoniaco NH3 también necesario para producir carbonato de sodio no se considera materia prima, ya que se regenerado y reciclado en el proceso. • • El proceso puede resumirse en la siguiente ecuación: • 2NaCl + CaCO3 Na2CO3 + CaCl2 HIERRO Y ACERO • El alto horno : El alto horno es la instalación industrial donde se transforma o trabaja el mineral de hierro. En general los altos hornos tienen un diámetro mayor a 8 m y llegan a tener una altura superior de los 60 m. Están revestidos de refractario de alta calidad HIERRO Y ACERO • Reducción directa del mineral de hierro : Para la producción del hierro también se puede utilizar el método de reducción directa, el que emplea agentes reactivos reductores como gas natural, coque, aceite combustible, monóxido de carbono, hidrógeno o grafito. El procedimiento consiste en triturar la merma de hierro y pasarla por un reactor con los agentes reductores, con lo que algunos elementos no convenientes para la fusión del hierro son eliminados HIERRO Y ACERO • El arrabio es un hierro de poca calidad, su contenido de carbón no está controlado y la cantidad de azufre rebasa los mínimos permitidos en los hierros comerciales. Sin embargo es el producto de un proceso conocido como la fusión primaria del hierro y del cual todos los hierros y aceros comerciales proceden. HIERRO Y ACERO HIERRO Y ACERO • Otros métodos de refinado del hierro • Método directo para fabricar hierro y acero a partir del mineral, sin producir arrabio. En este proceso se mezclan mineral de hierro y coque en un horno de calcinación rotatorio y se calientan a una temperatura de unos 950 ºC. El coque caliente desprende monóxido de carbono, igual que en un alto horno, y reduce los óxidos del mineral a hierro metálico HIERRO Y ACERO • Horno de hogar abierto : Es uno de los hornos más populares en los procesos de producción del acero. • Lingote al rojo vivo: El acero se vende en una gran variedad de formas y tamaños, como varillas, tubos, raíles (rieles) de ferrocarril o perfiles en H o en T. Estas formas se obtienen en las instalaciones siderúrgicas laminando los lingotes calientes o modelándolos de algún otro modo. HIERRO Y ACERO • El sistema de colada continua, en cambio, produce una plancha continua de acero con un espesor inferior a 5 cm, lo que elimina la necesidad de trenes de desbaste y laminado en bruto AMONIACO • El amoniaco, es uno de los productos intermedios más importantes de la industria química. • El NH3 se obtiene exclusivamente por el método denominado Haber-Bosh (Fritz Haber y Carl Bosh). El proceso consiste en la reacción directa entre el nitrógeno y el hidrógeno gaseosos, de acuerdo a la reacción: • • 3H (2)+ N (2) 2NH (3 ) +Calor ACIDO NÍTRICO • La materia prima para al producción de ácido nítrico corresponde al amoniaco que se produce en el proceso Haber – Bosch. El proceso implica tres reacciones: • Oxidación catalítica de amoníaco en aire • Oxidación de monóxido de nitrógeno • Absorción de dióxido de nitrógeno para producir el ácido. • La reacción global del proceso, es la siguiente: • • 1. NH3 (g)+ 2O2 (g)→HNO3(ac)+ H2O(l) UREA • La síntesis de urea a nivel industrial se realiza a partir de amoníaco (NH3) líquido y anhídrido carbónico (CO2) gaseoso. La reacción se verifica en 2 pasos. En el primer paso, los reactivos mencionados forman un producto intermedio llamado carbamato de amonio y, en la segunda etapa, el carbamato se deshidrata para formar urea. ABONOS NITROGENADOS • Sulfato de amonio. ( NH4)2SO4 • Se obtiene por la reacción del hidróxido de amonio con ácido sulfúrico • Nitrato de amonio (NH4)NO3 • Se obtiene a partir del ácido nítrico, usando el proceso Otsvald • Nitrato sódico NaNO3 • Se obtiene al reaccionar carbonato de sodio con ácido nítrico • Nitrato potásico. KNO3 • NaNO3 + KCl KNO3 + NaCl • INDUSTRIA DEL AZUFRE • Método Frasch: inventado en 1891 por el químico estadounidense Herman Frasch, éste método consiste en la inyección de agua sobrecalentada o de vapor de agua en las formaciones que contiene este elemento. • El azufre también puede extraerse de las piritas por destilación en retortas de hierro o arcilla refractaria, aunque con este proceso el azufre obtenido suele contener porciones de arsénico ÁCIDO SULFÚRICO • Cámaras de plomo :El proceso de cámaras de plomo es el más antiguo de los dos procesos y es utilizado actualmente para producir gran parte del acido consumido en la fabricación de fertilizantes. Este método produce un ácido relativamente diluido (62%-78% H2SO4) • Proceso de contacto : El proceso se basa en el empleo de un catalizador para convertir el SO2 en SO3, del que se obtiene ácido sulfúrico por hidratación Fósforo y derivados( Vía seca) • De la roca fosfórica se obtiene el fósforo elemental, mediante reducción con coque y en presencia de sílice en hornos eléctricos a más de 1.300°C, temperatura a la que escapa en forma de vapor junto con los gases del horno, condensando en electro filtros y siendo purificado a continuación. • Cloruros: Tricloruro y pentacloruro por combustión de fósforo blanco en atmósfera de cloro. • Óxidos: Pentóxido, por combustión de fósforo blanco en exceso de aire. Ácido fosfórico ( Vía húmeda) • El producto principal derivado de la roca fosfórica es el ácido fosfórico, que se produce masivamente por ataque directo de aquella con otro acido mas fuerte: sulfúrico, clorhídrico o nítrico, según procesos vía húmeda. • Ca5(PO4)3F + 5 H2SO4 → 3 H3PO4 + 5 CaSO4 ↓ + HF ↑ Ácido fosfórico ( Vía húmeda) • Proceso dihidrato: El proceso convencional consta de tres secciones principales: el ataque, donde tiene lugar la reacción sólido-líquido; la filtración, para separar el yeso del acido producido; y la concentración, en la que se lleva esta al 5254%, con la que se almacena. Ácido fosfórico ( Vía húmeda) • Procesos hemihidrato y anhidrita : La formación del sulfato cálcico hemihidrato en presencia de ácido débil (del orden del 30% P2O5) obliga a subir la temperatura en el ataque hasta casi 100°C, con graves problemas de corrosión, eliminando el enfriamiento evaporativo Ácido fosfórico ( Vía húmeda) • Proceso de horno de arco eléctrico : El proceso de horno eléctrico se basa en el hecho de que la sílice tiene propiedades de ácido fuerte a temperaturas elevadas. Si una mezcla de roca fosfórica, sílice y carbón se calienta a temperatura suficientemente alta, la sílice puede reemplazar al radical fosfato para formar un silicato de calcio, y el fósforo elemental puede destilarse de la mezcla reaccionante FOSFATOS Y FERTILIZANTES • Fosfatos: Se obtienen por la acción del ácido fosfórico con diferentes bases • Fertilizantes fosfatados: En general son productos obtenidos por acción de ácidos sobre minerales de fósforo (fosfatos), comprenden tanto a los fosfatos como a las sales derivadas del ácido empleado. Fertilizantes sólidos y líquidos • Dentro de los abonos minerales sólidos encontramos los abonos simples (un solo nutriente), compuestos (más de un nutriente) y blending (mezcla de los anteriores). • • Dentro de los abonos minerales líquidos encontramos los abonos simples y los compuestos. • Ejemplos: • KNO3 • (NH2)2CO • (NH4)2H2PO4 Cloruro de potasio y otros derivados del potasio • El cloruro de potasio se encuentra naturalmente como silvita, y puede extraerse de la silvinita. También puede extraerse de agua salada y puede producirse por cristalización, por flotación o por separación electrostática de minerales apropiados. Es un subproducto de la fabricación de ácido nítrico a partir de nitrato de potasio y ácido clorhídrico. • El potasio constituye del orden del 2,4% en peso de la corteza terrestre siendo el séptimo más abundante. Debido a su solubilidad es muy difícil obtener el metal puro a partir de sus minerales Cloruro de potasio y otros derivados del potasio • El potasio metal se usa en células fotoeléctricas. • El cloruro y el nitrato se emplean como fertilizantes. • El peróxido de potasio se usa en aparatos de respiración autónomos de bomberos y mineros. • El nitrato se usa en la fabricación de pólvora y el cromato y dicromato en pirotecnia. • El carbonato potásico se emplea en la fabricación de cristales. • La aleación NaK, una aleación de sodio y potasio, es un material empleado para la transferencia de calor. • Todos los fertilizantes de potasio se fabrican con salmueras o depósitos subterráneos de potasa. Las formulaciones principales son cloruro de potasio, sulfato de potasio y nitrato de potasio.