FORMULACIÓN INORGÁNICA
Anuncio

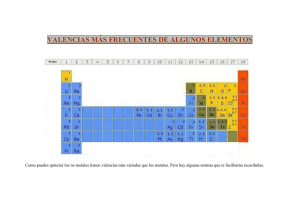
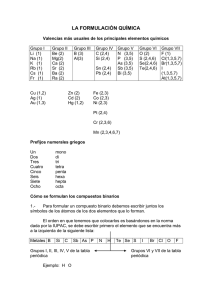
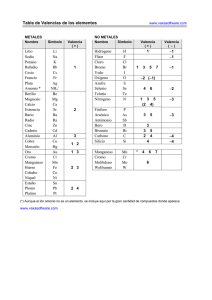
FORMULACIÓN INORGÁNICA SUSTANCIAS SIMPLES Las constituyen las agrupaciones de átomos de un mismo elemento. Constituyen, en general, la molécula del elemento. Existen elementos que pueden formar agrupaciones con distinto número de átomos. Cada una de estas agrupaciones recibe el nombre de estado o forma alotrópica. FORMULACIÓN Está constituida por el símbolo del elemento (E) afectado de un subíndice (n), según el número de átomos de la forma alotrópica: En Así por ejemplo, los gases nobles o inertes son todos monoatómicos y sus fórmulas serán: He, Ne, Ar, Kr, Xe, Rn También se formulan como moléculas monoatómicas los elementos que forman redes: Fe, Na, C, Si A temperatura ambiente y en estado libre, las sustancias simples gaseosas suelen llamarse gases elementales y su molécula es diatómica: H2, N2, O2, F2, Cl2 También son diatómicas, en estado libre y a temperatura ambiente las moléculas de los halógenos bromo y yodo: Br2, I2 A modo de ejemplo, algunas formas alotrópicas de sustancias simples que se pueden encontrar en la naturaleza son: Para el oxígeno: O2 y O3 Para el azufre: S2, S6, S8 Para el fósforo: P2, P4 1 NOMENCLATURAS La más usada para nombrar las sustancias simples es la TRADICIONAL (también llamada FUNCIONAL), que por lo general asigna a la sustancia el nombre del elemento químico correspondiente: sustancia He Ne Ar Kr Fe Na C Si H2 N2 O2 F2 Cl2 Br2 I2 O3 S2 S6 S8 P4 Nomenclatura tradicional (funcional) Helio Neón Argón Kriptón Hierro Sodio Carbono Silicio Hidrógeno Nitrógeno Oxígeno Flúor Cloro Bromo Yodo Ozono Azufre Azufre (romboédrico) Azufre (rómbico y monoclínico) Fósforo (blanco o rojo) También, aunque menos frecuente, se utiliza la nomenclatura SISTEMÁTICA para nombrar las sustancias simples. En esta nomenclatura todas las moléculas se nombran mediante un prefijo numeral según el número de átomos que la constituyen, seguido del nombre del elemento. sustancia Fe Na H2 N2 O2 O3 S6 S8 P4 Nomenclatura sistemática monohierro monosodio Dihidrógeno Dinitrógeno Dioxígeno Trioxígeno Hexaazufre Octaazufre Tetrafósforo 2 COMPUESTOS QUÍMICOS UNIONES ENTRE ÁTOMOS Los compuestos químicos están formados por uniones entre átomos. Los átomos, al combinarse, tienden a tener ocho electrones como máximo en su última órbita, o excepcionalmente dos. El resultado final de la combinación de átomos recibe el nombre de ENLACE QUÍMICO. La forma de conseguir los ocho electrones es la de ceder, captar o compartir electrones de la última órbita. Según el proceso que tenga lugar, se habla de enlace iónico o de enlace covalente. Enlace iónico: el cloro capta un electrón cedido por el sodio, obteniendo así 8 electrones en la última capa Enlace covalente: el oxígeno comparte dos electrones de su última capa con el único electrón de cada átomo de hidrógeno, de esta forma el oxígeno obtiene 8 electrones en su última capa y cada átomo de hidrógeno obtiene dos electrones Si queremos simbolizar un compuesto químico de forma eficaz debemos como mínimo dar una representación escrita de su unidad estructural, esto recibe el nombre de FÓRMULA QUÍMICA, que consta de los símbolos de los elementos componentes y subíndices numéricos que expresan la composición mas sencilla (fórmula empírica) del compuesto, así por ejemplo: CH4 Indica que la sustancia está compuesta de carbono e hidrógeno, en una proporción de cuatro átomos de hidrógeno por cada átomo de carbono. Fe2O3 Indica que la sustancia está compuesta de hierro y oxígeno, en una proporción de tres átomos de oxígeno por cada dos átomos de hierro. H2SO4 Indica que la sustancia está compuesta de hidrógeno, azufre y oxígeno en la proporción de un átomo de azufre por cada dos de hidrógeno y cuatro de oxígeno. VALENCIA O NÚMERO DE OXIDACIÓN Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es un número, positivo o negativo, que nos indica el número de electrones que gana, pierde o comparte un átomo con otro átomo o átomos al formar un enlace químico. 3 VALENCIAS DE LOS ELEMENTOS MÁS IMPORTANTES DEL SISTEMA PERIÓDICO. **Se reflejan aquí las valencias más usuales, cuando se estudian en profundidad se pueden encontrar variaciones o añadidos a las indicadas METALES VALENCIA 1 Litio Sodio Potasio Rubidio Cesio Francio Plata VALENCIAS 1, 2 Cobre Mercurio Li Na K Rb Cs Fr Ag Cu Hg VALENCIAS 2, 4 Platino Plomo Estaño Pt Pb Sn VALENCIA 2 Berilio Magnesio Calcio Estroncio Zinc Cadmio Bario Radio VALENCIAS 1, 3 Oro Talio Be Mg Ca Sr Zn Cd Ba Ra Au Tl VALENCIAS 2, 3, 6 Cromo Cr VALENCIA 3 Aluminio Al VALENCIAS 2, 3 Níquel Ni Cobalto Co Hierro Fe VALENCIAS 2, 3, 4, 6, 7 Manganeso Mn NO METALES. VALENCIA -1 Flúor F VALENCIAS ±2, 4, 6 Azufre Selenio Teluro VALENCIAS ±2, 4 Carbono S Se Te VALENCIAS ± 1, 3, 5, 7 Cloro Cl Bromo Br Yodo I VALENCIAS 1, 2, ± 3, 4, 5 Nitrógeno N VALENCIA 4 C Silicio Si VALENCIA -2 Oxígeno O VALENCIAS ±3, 5 Fósforo Arsénico Antimonio VALENCIA 3 P As Sb Boro B HIDRÓGENO. VALENCIA ±1 Hidrógeno H 4 FORMULACIÓN DE COMPUESTOS: EL “CRUCE” DE VALENCIAS Con los conceptos de enlace químico y valencia antes mencionados, es fácil deducir la fórmula de un compuesto químico. Basta tener en cuenta que la valencia nos indica el número de electrones puesto en juego en un enlace químico. Ejemplo: Para el compuesto óxido de sodio se puede resumir su formación como sigue: Un átomo de oxígeno puede captar dos electrones e incorporarlos a su última capa Un átomo de sodio puede ceder un electrón de su última capa valencia = -2 valencia = +1 De lo anterior vemos que para que sean captados dos electrones por un átomo de oxígeno es necesaria la participación de dos átomos de sodio, esto lo expresaremos mediante la siguiente fórmula química: Na2O indica que la sustancia está compuesta de oxígeno e hidrógeno en la proporción de un átomo de oxígeno por cada dos de sodio. En la práctica, para formular compuestos binarios se recurre al llamado “cruce de valencias”, que en el caso anterior sería lo siguiente: Observamos que al cruzar el valor absoluto de las valencias aparecen en la fórmula el número de átomos necesarios de uno y otro elemento que “satisfacen” las necesidades de electrones. Otros ejemplos serían los siguientes Fe+2 + Cl-1 FeCl2 C+4 + Br-1 CBr4 Ni3+ + O2- Ni2O3 Ca2+ + H1- CaH2 5 CALCULO DE LA VALENCIA CON LA QUE ACTÚA UN ELEMENTO EN UNA SUSTANCIA Muchas veces, cuando se nombra un compuesto, es necesario conocer la valencia con la que actúa alguno de los elementos en dicho compuesto. Es fácil calcular, para un compuesto determinado, las valencias si se aplica el principio de electroneutralidad: “La suma de los estados de oxidación (valencias) de todos los elementos químicos presentes en una fórmula debe dar cero”. Para calcular la valencia es necesario saber de memoria algunas valencias de elementos en las que apoyarnos: Oxígeno (O) Hidrógeno (H) Flúor (F) Grupo IA (alcalinos) Grupo IIA (alcalino-terreos) Grupo IIIA (terreos) Su valencia es generalmente -2 Valencias exclusivamente -1 ó +1 Siempre -1 Sólo tienen valencia +1 Sólo tienen valencia +2 Sólo tienen valencia +3 Ejemplos: Valencia del azufre en el SO3: 3 átomos de O Contribución del O: 3·(-2) = -6 1 átomo de S Contribución del S: 1· X = X ----------------------------------------------------------------Suma =0 -6 + X = 0 X = 6 La valencia con la que actúa el S es 6 Valencia del P en el compuesto H3PO4 4 átomos de O Contribución del O : 4·(-2) = -8 1 átomo de P Contribución del P : 1·X = X 3 átomos de H Contribución del H : 3·1 = 3 Suma =0 -8 + X + 3 = 0 X = 5 La valencia con la que actúa el P es 5 Estos sencillos cálculos permiten, a la hora de nombrar un compuesto, conocer la valencia con que actúan los elementos. 6 NOMENCLATURAS. Para nombrar los compuestos químicos inorgánicos se siguen las normas de la IUPAC (unión internacional de química pura y aplicada). Se aceptan tres tipos de nomenclaturas para los compuestos inorgánicos, la sistemática, la nomenclatura de stock y la nomenclatura tradicional. De forma general son como siguen (particularmente se irán desarrollando a medida que se vean las funciones químicas) 1. NOMENCLATURA SISTEMÁTICA. Para nombrar compuestos químicos según esta nomenclatura se utilizan los prefijos: MONO_, DI_, TRI_, TETRA_, PENTA_, HEXA_, HEPTA_..., indicativos del número de átomos de cada elemento presentes en la proporción de la sustancia. Cl2O3 Trióxido de dicloro I2O Monóxido de diyodo 2. NOMENCLATURA DE STOCK. En este tipo de nomenclatura, se utiliza el nombre específico de la función química (óxido, hidróxido, ácido, etc.) seguido del nombre del elemento que forma el compuesto indicando al final, en números romanos y entre paréntesis la valencia del elemento si este posee mas de una: Fe(OH)2 Hidróxido de hierro (II) Fe(OH)3 Hidróxido de hierro (III) SnS Sulfuro de estaño (II) Na2O Óxido de sodio 3. NOMENCLATURA TRADICIONAL (FUNCIONAL). En esta nomenclatura para poder distinguir con qué valencia actúan los elementos en un compuesto se utilizan una serie de prefijos y sufijos: Nº de valencias Orden de la valencia Prefijo Sufijo Ejemplo Nombres del elemento 1 valencia -ico Na+1 Sódico -oso -ico Co+2 Co+3 Cobaltoso Cobáltico 2 valencias menor mayor Hipo- 3 valencias menor intermedia mayor -oso -oso -ico N+1 N+3 N+5 Hiponitroso Nitroso Nítrico Hipo- 4 valencias menor intermedia menor intermedia mayor mayor -oso -oso -ico -ico Cl+1 Cl+3 Cl+5 Cl+7 Hipocloroso Cloroso Clórico Perclórico Per- 7 COMBINACIONES BINARIAS DEL OXÍGENO 1. ÓXIDOS METÁLICOS Están formados por la combinación de un metal con oxígeno. Su fórmula general es: M+X + O-2 M2Ox (“cruce” de valencias) En el caso de que x sea par se simplifica la fórmula Ejemplos: Al3+ + O2- Al2O3 Pb4+ + O2- Pb2O4 simplificar PbO2 Nomenclatura TRADICIONAL: ÓXIDO + METAL + -OSO(menor valencia)/-ICO (mayor valencia) Nomenclatura SISTEMÁTICA: PREFIJO Nº DE ATOMOS DE OXÍGENO + ÓXIDO DE + PREFIJO Nº ÁTOMOS METAL + NOMBRE DEL METAL Los prefijos utilizados son mono-, di-, tri-, tetra-, penta-,hexa-,hepta-, ... En muchas ocasiones se prescinde del prefijo mono-. Nomenclatura de STOCK: ÓXIDO DE + NOMBRE METAL + (valencia del metal con nº romanos) Si el metal sólo tiene una valencia, no es necesario indicarla. EJEMPLO Na2O FeO Fe2O3 TRADICIONAL Óxido sódico Óxido ferroso Óxido férrico SISTEMÁTICA Monóxido de disodio Monóxido de hierro Trióxido de dihierro STOCK Óxido de sodio Óxido de hierro (II) Óxido de hierro (III) 8 2. ÓXIDOS NO METÁLICOS Están formados por la combinación de un no metal con oxígeno. Su fórmula general es: M+X + O-2 M2Ox (“cruce” de valencias) En el caso de que x sea par se simplifica la fórmula Ejemplos: C+4 + O-2 C2O4 simplificar CO2 Cl+3 + O-2 Cl2O3 N5+ + 02- N2O5 Nomenclatura TRADICIONAL: ANHÍDRIDO + (PREFIJO) + NO METAL + SUFIJO. (Se tiende a sustituir la palabra ANHÍDRIDO por ÓXIDO). El prefijo y el sufijo dependen de las valencias que tenga el no metal. Número valencias Orden de la valencia Prefijo Sufijo del elemento 1 valencia -ico 2 valencias menor mayor -oso -ico menor intermedia mayor Hipo- 3 valencias -oso -oso -ico Hipo- 4 valencias menor intermedia menor intermedia mayor mayor -oso -oso -ico -ico Per- El caso del manganeso es especial: (tiene tres valencias con las que actúa como no metal: 4, 6 y 7) Menor (4) MnO2 Anhídrido manganoso Medio (6) MnO3 Anhídrido mangánico Mayor (7) Mn2O7 Anhídrido permangánico También el cromo tiene valencias en las que actúa como no metal (3 y 6) Menor (3) Cr2O3 Anhídrido cromoso Mayor (6) CrO3 Anhídrido crómico 9 Nomenclaturas SISTEMÁTICA y de STOCK: Igual que en los óxidos metálicos. COMPUESTO TRADICIONAL CO2 SISTEMÁTICA Anhídrido carbónico Cl2O3 Anhídrido hipocloroso Anhídrido cloroso Cl2O5 Anhídrido clórico Cl2O7 Anhídrido perclórico Cl2O STOCK Óxido de carbono Dióxido de carbono (IV) Monóxido de Óxido de cloro (I) dicloro Trióxido de dicloro Óxido de cloro (III) Pentóxido de Óxido de cloro (V) dicloro Heptóxido de Óxido de cloro (VII) dicloro COMBINACIONES BINARIAS CON EL HIDRÓGENO. 1. HIDRUROS METÁLICOS: Combinación de metal e hidrógeno. Su fórmula general es: M+x + H-1 MHx (“cruce” de valencias) Nomenclatura TRADICIONAL: HIDRURO + METAL + -OSO (menor valencia)/ -ICO (mayor valencia) Nomenclatura SISTEMÁTICA: PREFIJO Nº DE ATOMOS DE HIDRÓGENO +HIDRURO DE+ NOMBRE DEL METAL. Nomenclatura de STOCK: HIDRURO DE + NOMBRE DEL METAL + (valencia del metal con nº romanos) Si el metal sólo tiene una valencia, no es necesario indicarla. EJEMPLO AlH3 NiH2 NiH3 TRADICIONAL Hidruro alumínico Hidruro niqueloso Hidruro niquélico SISTEMÁTICA Trihidruro de aluminio Dihidruro de níquel Trihidruro de níquel STOCK Hidruro de aluminio Hidruro de níquel (II) Hidruro de níquel (III) 10 2. HIDRUROS NO METÁLICOS (volátiles): Combinación de no metal menos electronegativo que el hidrógeno (grupos IIIA, IVA y VA) , con el hidrógeno. Los no metales actúan con una única valencia (LA NEGATIVA) Nomenclatura TRADICIONAL: Son nombres tan conocidos que se siguen manteniendo en la actualidad. Grupo IIIA Grupo IVA Grupo VA BH3 borano CH4 metano NH3 amoníaco B2H6 diborano SiH4 xilano PH3 fosfina (fosfamina) AsH3 arsina (arsenamina) SbH3 estibina BiH3 bismutina Nomenclatura SISTEMÁTICA: Igual que para los hidruros metálicos. CH4 Tetrahidruro de carbono, NH3 Trihidruro de nitrógeno AsH3 Trihidruro de arsenico 3. HALUROS DE HIDRÓGENO Y ACIDOS BINARIOS (HIDRÁCIDOS) Combinación de no metales más electronegativos que el hidrógeno (grupos VIA y VIIA) con hidrógeno. Como gases se denominan haluros de hidrógeno y cuando están disueltos en agua presentan propiedades ácidas llamándose entonces ácidos hidrácidos. Su fórmula general es: X-y + H+1 HyX (Cruce de valencias .El no metal frente al hidrógeno utiliza su valencia más pequeña que se corresponde con la negativa) Grupo VIA (valencia -2) Grupo VIIA (valencia -1) S, Se, Te F, Cl, Br, I Nomenclatura TRADICIONAL (Cuando están en disolución acuosa): ÁCIDO + NOMBRE NO METAL + HÍDRICO Nomenclatura SISTEMÁTICA (Cuando están en estado gaseoso): NOMBRE NO METAL+ -URO DE + PREFIJO Nº H + HIDRÓGENO 11 Nomenclatura STOCK: Igual que la anterior, pero sin prefijos numéricos. NOMBRE NO METAL + -URO DE HIDRÓGENO EJEMPLO TRADICIONAL HCl Ácido clorhídrico H2S Ácido sulfhídrico SISTEMÁTICA Cloruro de hidrógeno Sulfuro de dihidrógeno STOCK Cloruro de hidrógeno Sulfuro de hidrógeno COMBINACIONES BINARIAS: SALES 1. SALES HIDRÁCIDAS. Combinación de un metal y un no metal. La fórmula general es: M+n + X-y MyXn (cruce de valencias: El no metal actúa con su valencia negativa frente al metal, que puede actuar con cualquiera de sus valencias) Grupo IVA Valencia (-4) Grupo VA Valencia (-3) Grupo VIA Valencia (-2) Grupo VIIA Valencia (-1) C N, P, As, Sb, Bi S, Se, Te F, Cl, Br, I Nomenclatura TRADICIONAL: NOMBRE NO METAL + URO + NOMBRE METAL + OSO (valencia menor) / ICO (Valencia mayor) Nomenclatura SISTEMÁTICA: PREFIJO Nº ÁT. NO METAL + NOMBRE NO METAL + -URO DE + PREFIJO Nº ÁT. METAL + NOMBRE DEL METAL. Nomenclatura STOCK: NO METAL + URO DE + NOMBRE METAL + (valencia del metal con nº romanos).Si el metal sólo tiene una valencia, no es necesario indicarla. 12 COMPUESTO AlCl3 Fe2S3 Na3N Ca2C TRADICIONAL Cloruro alumínico Sulfuro férrico Nitruro sódico Carburo cálcico SISTEMÁTICA Tricloruro de aluminio Trisulfuro de dihierro Trinitruro de sodio Carburo de calcio STOCK Cloruro de aluminio Sulfuro de hierro (III) Trinitruro de sodio Carburo de calcio 2. SALES VOLÁTILES Combinación de un no metal (que puede actuar con cualquiera de sus valencias positivas) y un no metal, más electronegativo, que actúa con su valencia negativa. Para formularlos se escribe siempre primero el que se encuentra más a la izquierda en la tabla periódica y si son del mismo grupo, se escribe primero el que está mas abajo en el grupo Se utiliza casi exclusivamente la nomenclatura SISTEMÁTICA: Igual que las sales hidrácidas. CCl4 Tetracloruro de carbono IF5 Pentafluoruro de yodo PCl3 Tricloruro de fósforo SiC Carburo de silicio (carborundo) CS2 Sulfuro de carbono COMBINACIONES BINARIAS: PERÓXIDOS. Son combinaciones de un metal con el grupo peróxido (O22-) que actúa con valencia –2. El subíndice 2 del grupo peróxido NUNCA SE SIMPLIFICA. M+x + O2-2 M2(O2)x (cruce de valencias. Si x es par, se simplifica con el subíndice 2 del metal M, a no ser que haya posibilidad de confundir con un óxido) Ejemplos: Li+1 + (O2)-2 Li2O2 Mg+2 + (O2)-2 Mg2(O2)2 MgO2 H+1 + (O2)-2 H2O2 Fe+2 + (O2)-2 Fe2(O2)2 FeO2 Fe+3 + (O2)-2 Fe2(O2)3 Sn+2 + (O2)-2 Sn2(O2)2 (aquí no se simplifica ya que se confundiría con SnO2, el óxido de estaño (IV) ) Sn+4 + (O2)-2 Sn2(O2)4 Sn(O2)2 Pb+2 + (O2)-2 Pb2(O2)2 (aquí no se simplifica ya que se confundiría con PbO2, el óxido de plomo (IV) ) 13 Nomenclatura TRADICIONAL: PERÓXIDO + NOMBRE METAL + -OSO (menor valencia)/-ICO (mayor valencia) Nomenclatura SISTEMÁTICA: Casi no se usa Nomenclatura STOCK: PERÓXIDO DE + NOMBRE DEL METAL + (valencia del metal con nº romanos) Si el metal sólo tiene una valencia, no es necesario indicarla. COMPUESTO Na2O2 BaO2 H2O2 FeO2 Sn(O2)2 Pb2(O2)2 TRADICIONAL STOCK Peróxido de Peróxido sódico sodio Peróxido de Peróxido bárico bario Peróxido de agua oxigenada hidrógeno Peróxido Peróxido de ferroso hierro (II) Peróxido Peróxido de estánnico estaño (IV) Peróxido Peróxido de plumboso plomo (II) COMBINACIONES TERNARIAS HIDRÓXIDOS Formados por un metal, oxígeno e hidrógeno, en los que el oxígeno y el hidrógeno forman una especie química llamada grupo hidroxilo (-OH) de valencia (-1). La fórmula general es: M+x + (OH)-1 M(OH)x (cruce de valencias. Si x = 1, se omite el paréntesis) Ejemplos: Na+1 + OH-1 NaOH Ca+2 + OH-1 Ca(OH)2 Cu+1 + OH-1 CuOH Cu+2 + OH-1 Cu(OH)2 14 Nomenclatura TRADICIONAL: HIDRÓXIDO + NOMBRE METAL + -OSO (menor valencia)/-ICO (mayor valencia) Nomenclatura SISTEMÁTICA: PREFIJO Nº DE -OH + HIDRÓXIDO DE + NOMBRE METAL Nomenclatura de STOCK: HIDRÓXIDO DE + NOMBRE METAL + (valencia del metal con nº romanos). Si el metal sólo tiene una valencia, no es necesario indicarla. EJEMPLO NaOH CuOH Cu(OH)2 Ca(OH)2 Fe(OH)3 TRADICIONAL SISTEMÁTICA Monohidróxido de Hidróxido sódico sodio Hidróxido Monohidróxido de cuproso cobre Hidróxido Dihidróxido de cúprico cobre Hidróxido de Dihidróxido de calcio calcio Trihidróxido de Hidróxido férrico hierro STOCK Hidróxido de sodio Hidróxido de cobre (I) Hidróxido de cobre (II) Hidróxido de calcio Hidróxido de hierro (III) ÁCIDOS OXÁCIDOS Formados por hidrógeno, no metal o un metal de transición (Cr, Mn,.,) y oxígeno. La fórmula general es: HaXbOc Para calcular la valencia del elemento X seguimos la regla de la electroneutralidad ya vista anteriormente: nº de át. de O • (-2) + nº de át. de H • (+1) + no át. de X • (v) = 0 Despejando, v es la valencia que buscamos. Ejemplo: Valencia del azufre en el H2SO3 3 át. De O · (-2) + 2 át de H · (+1) + 1 át de S · (v) = 0 -6 + 2 + v = 0 v = 4 15 1. OXÁCIDOS SIMPLES La regla práctica para formularlos consiste en sumar una molécula de agua al óxido no metálico correspondiente: Ejemplos: N2O3 + H2O H2N2O4 simplificando HNO2 N2O5 + H2O H2N2O6 simplificando HNO3 SO3 + H2O H2SO4 Nomenclatura TRADICIONAL: ÁCIDO + (PREFIJO)+ NOMBRE NO METAL+ SUFIJO también podemos decir que se nombran igual que el anhídrido del que provienen sustituyendo la palabra anhídrido por la palabra ácido) El prefijo y el sufijo dependen de las valencias que tenga el no metal o el metal de transición (Cr, Mn...) Número valencias Orden de la valencia Prefijo Sufijo del no metal 1 valencia -ico 2 valencias menor mayor -oso -ico menor intermedia mayor Hipo- 3 valencias -oso -oso -ico Hipo- 4 valencias menor intermedia menor intermedia mayor mayor -oso -oso -ico -ico Per- (Recordar que el caso del Mn, con tres valencias como no metal (4,6 y 7) es especial. Ver óxidos no metálicos.) Nomenclatura SISTEMÁTICA: PREFIJO Nº O + OXO +NOMBRE NO METAL +-ATO + (valencia no metal con nº romanos) +DE HIDRÓGENO Nomenclatura de STOCK: ÁCIDO+PREFIJO Nº ÁT. DE O + -OXO + NOMBRE NO METAL + -ICO (valencia del no metal con nº romanos) 16 EJEMPLO TRADICIONAL SISTEMÁTICA STOCK H2SO4 Ácido sulfúrico Tetraoxosulfato (VI) de hidrógeno Ácido tetraoxosulfúrico (VI) Otros ejemplos de oxácidos importantes son: EJEMPLO TRADICIONAL SISTEMÁTICO H2CO3 Ácido Trioxocarbonato (IV) de carbónico hidrógeno HNO2 Ácido nitroso Dioxonitrato (III) de hidrógeno HNO3 Ácido nítrico Trioxonitrato (V) de hidrógeno H2SO3 Ácido sulfuroso Trioxosulfato (IV) de hidrógeno HClO Ácido Monoxoclorato (I) de hipocloroso hidrógeno HClO2 Ácido cloroso Dioxoclorato (III) de hidrógeno HClO3 Ácido clórico Trioxoclorato (V) de hidrógeno HClO4 Ácido Tetraoxoclorato (VII) de perclórico hidrógeno H2CrO4 Ácido crómico Tetraoxocromato (VI) de hidrógeno H2MnO3 Ácido Trioxomanganato (IV) de manganoso hidrógeno H2MnO4 Ácido Tetraoxomanganato (VI) de mangánico hidrógeno HMnO4 Ácido Tetraoxomanganato (VII) de permangánico hidrógeno STOCK Ácido trioxocarbónico (IV) Ácido dioxonítrico (III) Ácido trioxonítrico (V) Ácido trioxosulfúrico (IV) Ácido monoxoclórico (I) Ácido dioxoclórico (III) Ácido trioxoclórico (V) Ácido tetraoxoclórico (VII) Ácido tetraoxocrómico (VI) Ácido trioxomangánico (IV) Ácido tetraoxomangánico (VI) Ácido tetraoxomangánico (VII) 2. OXÁCIDOS POLIHIDRATADOS Existen elementos que, con una misma valencia pueden formar series de oxácidos que se diferencian en el contenido de oxígeno e hidrógeno en la molécula. En los casos más sencillos se puede obtener la fórmula sumando una, dos o tres moléculas de agua a la molécula del anhídrido correspondiente: ANHÍDRIDO + nH2O OXÁCIDO POLIHIDRATADO (n = 1,2 ó 3) Ejemplos: P2O5 + 2 H2O H4P2O7 B2O3 + 3H2O H6B2O6 simplificar H3BO3 17 Nomenclatura FUNCIONAL: Se utiliza un prefijo indicativo del grado de hidratación META, PIRO Y ORTO (del prefijo ORTO se puede prescindir) según el elemento pertenezca a los grupos siguientes. GRUPO IIIA: Para el B (valencia 3): 1 molécula H2O prefijo META B2O3 + H2O H2B2O4 HBO2 ácido metabórico 3 moléculas H2O prefijo ORTO (se puede omitir) B2O3 + 3H2O H6B2O6 H3BO3 ácido (orto)bórico GRUPO IVA Para el Si (valencia 4): 1 molécula H2O prefijo META SiO2 + H2O H2SiO3 ácido metasilícico 2 moléculas H2O prefijo ORTO (se puede omitir) SiO2 + 2H2O H4SiO4 ácido (orto)silícico GRUPO VA Para P (valencias 1,3,5), As y Sb (valencias 3 y 5): 1 molécula H2O META 2 moléculas H2O PIRO 3 moléculas H2O ORTO (se puede omitir) Si lo hacemos por ejemplo para la valencia 5 del fósforo obtenemos: P2O5 + H2O H2P2O6 simplificar HPO3 ácido metafosfórico P2O5 + 2H2O H4P2O7 ácido pirofosfórico P2O5 + 3H2O H6P2O8 simplificar H3PO4 ácido (orto)fosfórico 18 Nomenclaturas de STOCK y SISTEMÁTICA: Se siguen las reglas ya vistas para los oxácidos simples, añadiendo, caso de ser necesario, un numeral que indique el número de átomos del no metal presentes en la molécula. Ejemplos: STOCK SISTEMÁTICA H3PO4 Ácido tetraoxofosfórico (V) Tetraoxofosfato (V) de hidrógeno H4P2O7 Ácido heptaoxodifosfórico (V) Heptaoxodifosfato (V) de hidrógeno 3. POLIÁCIDOS (ISOPOLIÁCIDOS) Son oxácidos en cuya molécula existe más de un átomo del no metal o átomo principal. Podemos escribir la fórmula, en los casos más sencillos, uniendo a una molécula de agua, las moléculas necesarias del anhídrido correspondiente. n·(ANHÍDRIDO) + H2O POLIÁCIDO (n = 1, 2, …) Ejemplos: 2B2O3 + H2O H2B4O7 2CrO3 + H2O H2Cr2O7 2SO2 + H2O H2S2O5 Nomenclatura FUNCIONAL: Se siguen las normas ya vistas para los oxácidos simples, utilizando un prefijo numérico que indique el número de átomos del elemento principal. Nomenclaturas de STOCK y SISTEMÁTICA: Se siguen las normas ya vistas. H2B4O7 H2Cr2O7 H2S2O5 TRADICIONAL Ácido tetrabórico STOCK Ácido heptaoxotetrabórico (III) Ácido dicrómico Ácido heptaoxodicrómico (VI) Ácido Ácido disulfuroso pentaoxodisulfúrico (IV) SISTEMÁTICA Tetraoxoborato (III) de hidrógeno Tetraoxodicromato (VI) de hidrógeno Pentaoxodisulfato (IV) de hidrógeno 19 SALES OXÁCIDAS NEUTRAS. Proceden de los ácidos oxácidos en los que se han sustituido TODOS los átomos de hidrógeno por un metal. La fórmula general se puede obtener de la siguiente manera: 1º Oxácido del que proviene la sal HaXbOc sustituye todos sus hidrógenos (XbOc)-a (“a” coincide con el número de H eliminados y será la valencia del grupo) 2º Combinación con el metal: (“cruce” de valencias) Mn+ + (XbOc)-a Ma(XbOc)n (a y n son simplificables) Ejemplos: Na+1 + HNO2 NaNO2 Mg+2 + HNO3 Mg(NO3)2 K+1 + H2SO4 K2SO4 Cu+2 + H2SO4 Cu2(SO4)2 simplificarCuSO4 Ca+2 + H3PO4 Ca3(PO4)2 Nomenclatura TRADICIONAL: Se utiliza el nombre del ácido de procedencia cambiando las terminaciones –oso/-ico por las terminaciones –ito/-ato. Valencias de procedencia Sufijo en el acido Sufijo en la sal pequeñas -oso -ito grandes -ico -ato Seguidamente se añade el nombre del metal con los sufijos – OSO(valencia menor)/ICO (valencia mayor): raíz elemento + (-ITO/-ATO) de + metal + (-OSO/-ICO) También se admite mezclar la nomenclatura tradicional con la de Stock y en este caso indicar la valencia del metal con nº romanos en lugar de las terminaciones –oso e –ico. raíz elemento + (-ITO/-ATO) de + metal + (valencia en números romanos) Nomenclatura SISTEMÁTICA-STOCK: PREFIJO Nº ÁT. DE O + -OXO + PREFIJO Nº ÁT. NO METAL + NOMBRE NO METAL + -ATO + (valencia del no metal con nº romanos) DE + PREFIJO Nº ÁT. METAL + NOMBRE DEL METAL 20 Nomenclatura SISTEMÁTICA-ESTEQUIOMÉTRICA: Igual que la sistemática-Stock pero prescindiendo de indicar la valencia del metal con nº romanos. Cuando resulta necesario utilizar dos prefijos juntos, se emplea bis-, tris-, tetraquis-… para el primero EJEMPLO TRADICIONAL SISTEMÁTICA-STOCK ESTEQUIOMÉTRICA K2CO3 Carbonato potásico o Carbonato de potasio Trioxocarbonato (IV) de potasio Trioxocarbonato de dipotasio EJEMPLO TRADICIONAL SISTEMÁTICA-STOCK ESTEQUIOMÉTRICA Fe2(SO3)3 Sulfito férrico o Sulfito de hierro(III) tetraoxosulfato (IV) de hierro (III) Tris(trioxosulfato) de dihierro EJEMPLO TRADICIONAL Ca3(PO4)2 (orto)fosfato cálcico o (orto)fosfato de calcio Tetraoxofosfato (v) de calcio Bis(tetraoxofosfato) de tricalcio SISTEMÁTICA-STOCK ESTEQUIOMÉTRICA EJEMPLO TRADICIONAL SISTEMÁTICA-STOCK ESTEQUIOMÉTRICA CuSO4 Sulfato cúprico o sulfato de cobre(II) Tetraoxosulfato (VI) de cobre (II) Tetraoxosulfato de cobre EJEMPLO TRADICIONAL SISTEMÁTICA-STOCK ESTEQUIOMÉTRICA NaNO2 Nitrito sódico o nitrito de sodio Dioxonitrato (III) de sodio Dioxonitrato de sodio 21 SALES ÁCIDAS DE OXÁCIDOS. Proceden de los ácidos oxácidos en los que se han sustituido parcialmente los átomos de hidrógeno por un metal. Ejemplos: Li+1 + H2SO4 LiHSO4 Na+1 + H2CO3 NaHCO3 Ca+2 + H3PO4 Ca(H2PO4) Ca+2 + H3PO4 Ca2(HPO4)2 simplificación CaHPO4 Nomenclatura TRADICIONAL: Igual que la de las oxisales pero añadiendo PREFIJO Nº DE H + HIDRÓGENO al principio del nombre. Se permite anteponer el prefijo bi- si se han sustituido la mitad de los hidrógenos del ácido del que proviene la sal Nomenclatura SISTEMÁTICA: Igual que la de las oxisales pero añadiendo PREFIJO Nº DE H + HIDRÓGENO al principio del nombre. EJEMPLO TRADICIONAL SISTEMÁTICA-STOCK ESTEQUIOMÉTRICA EJEMPLO TRADICIONAL SISTEMÁTICA (IUPAC) ESTEQUIOMÉTRICA EJEMPLO TRADICIONAL SISTEMÁTICA-STOCK ESTEQUIOMÉTRICA LiHSO4 Hidrógenosulfato lítico, hidrógenosulfato de litio bisulfato de sodio Hidrógenosulfato (VI) de litio Hidrógenotetraoxofosfato de disodio Fe (H 2 PO4)2 Dihidrógeno (orto)fosfato ferroso Dihidrógeno (orto)fosfato de hierro (II) dihidrógenotetraoxofosfato(V) de hierro (II) Bis(dihidrógenotetraoxofosfato) de hierro NaHCO3 hidrógeno carbonato sódico Hidrógeno carbonato de sodio Bicarbonato de sodio Hidrógenotrioxocarbonato (IV) de sodio Hidrógenotrioxocarbonato de sodio 22 EJEMPLO TRADICIONAL SISTEMÁTICA (IUPAC) ESTEQUIOMÉTRICA Fe (H 2 PO4)2 Dihidrógeno (orto)fosfato ferroso Dihidrógeno (orto)fosfato de hierro (II) dihidrógenotetraoxofosfato(V) de hierro (II) Bis(dihidrógenotetraoxofosfato) de hierro SALES ÁCIDAS DE HIDRÁCIDOS También pueden formarse sales ácidas a partir de los ácidos hidrácidos cuando la sustitución del hidrógeno es parcial: Ejemplos: K+1 + H2S KHS Sn2+ + H2S Sn(HS)2 Fe3+ + H2Se Fe(HSe)3 Nomenclaturas TRADICIONAL Y SISTEMÁTICA: Igual que lo visto para las sales ácidas de oxoácidos, salvo que ahora la terminación del no metal es –URO en vez de –ITO o -ATO EJEMPLO TRADICIONAL SISTEMÁTICA-STOCK ESTEQUIOMÉTRICA EJEMPLO TRADICIONAL SISTEMÁTICA-STOCK ESTEQUIOMÉTRICA EJEMPLO TRADICIONAL SISTEMÁTICA-STOCK ESTEQUIOMÉTRICA KHS Hidrógeno sulfuro potásico Bisulfuro de potasio Hidrógenosulfuro de potasio Hidrógenosulfuro de potasio Sn(HS)2 Hidrógeno sulfuro estannoso Hidrógeno sulfuro de estaño (II) Bisulfuro estannoso Hidrógenosulfuro de estaño (II) Bis(Hidrógenosulfuro) de estaño Fe(HSe)3 Hidrógeno seleniuro férrico Hidrógeno seleniuro de hierro (III) Hidrógenoseleniuro de hierro (III) Tris(hidrógenoseleniuro) de potasio 23