descargar documento
Anuncio

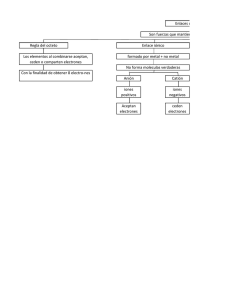
TEMA 5. Metabolismo – Reacciones en química orgánica Oxidaciones y reducciones Reacciones de formación y de ruptura de enlaces carbonocarbono. Nucleofilia y electrofilia. Isomerizaciones y eliminaciones. Sustituciones. Reacciones de transferencia de grupos. Ácidos y bases. Conceptos de Browsted-Lowry y de Lewis. El metabolismo es el conjunto de reacciones bioquímicas y procesos físico-químicos que ocurren en una célula y en el organismo. Reacciones químicas: Es el proceso por el cual se redistribuyen los átomos en un sistema material formado por una o más sustancias (llamadas reactivos) obteniéndose una o más sustancias con propiedades químicas diferentes (llamadas productos). Las reacciones químicas se representan mediante ecuaciones químicas. Tipos de reacciones Reacciones de oxidación-reducción Reacciones que forman o rompen enlaces carbonocarbono Reordenamientos internos, isomerizaciones y eliminaciones Reacciones de transferencia de grupos Reacciones de hidrólisis Reacciones de oxidación-reducción Son aquellas en las que hay transferencia de electrones entre los reactivos Oxidación: Una especie química (átomo o molécula) cede electrones a otra. Reducción: Una especie química (átomo o molécula) capta electrones de otra Zn0 + 2 HCl ZnCl2 + H2 En este tipo de reacciones de óxido-reducción, se observa claramente la transferencia de los electrones. El átomo de Zn, electricamente neutro, se oxida a Zn+2, mientras que el hidrógeno, que se encuentra oxidado en el HCl, gana electrones y por lo tanto, se reduce a hidrógeno molecular. Para analizar el estado de oxidación del carbono, hay que tener en cuenta la electronegatividad del átomo o de los átomos que se encuentran unidos al carbono. Para ello es conveniente representar las moléculas según las estructuras de Lewis. Se analizan los enlaces, y se identifica si el átomo que está unido al carbono es más o menos electronegativo que éste. Si el enlace está compartido por dos átomos iguales, se distribuyen equitativamente los electrones entre ellos. Recordemos el orden de electronegatividades: H<C<N<O Metano Etano (Alcano) Eteno (Alqueno) Etanol (Alcohol) Acetileno (Alquino) Formaldehído (Aldehído) Etanal (Aldehído) Acetona (Cetona) Ácido fórmico (Ac. carboxílico) Monóxido de carbono Ácido acético (Ác. carboxílico) Dióxido de carbono Metano Etano (Alcano) Eteno (Alqueno) Etanol (Alcohol) Acetileno (Alquino) Formaldehído (Aldehído) Etanal (Aldehído) Acetona (Cetona) Ácido fórmico (Ac. carboxílico) Monóxido de carbono Ácido acético (Ác. carboxílico) Dióxido de carbono Grado de Oxidación Alcano Alcohol Aldehído o cetona Ácido carboxílico Dióxido de carbono Ejemplo de una oxidación biológica Lactato Lactato deshidrogenasa Piruvato Tipos de reacciones Reacciones de oxidación-reducción Reacciones que forman o rompen enlaces carbonocarbono Reordenamientos internos, isomerizaciones y eliminaciones Reacciones de transferencia de grupos Reacciones de hidrólisis Recordar!!! En un enlace covalente simple, se comparten un par de electrones entre dos átomos. En algunas moléculas, hay átomos que presentan pares de electrones libres (no apareados). enúmero de enlaces pares de e- libres Los átomos de nitrógeno, de oxígeno y los halógenos (F, Cl, Br, I) normalmente tienen electrones no enlazantes (pares solitario o pares libres) en sus compuestos estables Ruptura homolítica Radical + Átomo de carbono hidrógeno Radicales carbono Ruptura heterolítica Carbanión + protón Homo: igual Hetero: distinto “lítica” proviene de “lisis” que significa ruptura Carbocatión + hidruro Carbanión + carbocatión Nucleofilia y Electrofilia Nucleófilo: “amante de los núcleos”, o sea, que tiene afinidad por las especies cargadas positivamente o con densidad de carga positiva. Son especies que donan pares electrones en una reacción química para formar un enlace. Ejemplos de nucleófilos : H2 O : Nucleofilia y Electrofilia Electrófilo: “amante de los electrones”, o sea, que tiene afinidad por los electrones. Son especies que aceptan pares electrones de un nucleófilo para formar un enlace en una reacción química. Ejemplos de electrófilos H+ protón CH3 H3C El carbono de un grupo carbonilo C+ CH3 carbocatión Reacción entre un nucleófilo (Nu:-), en este caso un carbanión y un electrófilo (E+), el carbono con densidad de carga positiva del grupo carbonilo. Por convención, las flechas para indicar el ataque, va dirigida desde el Nu:- al E+. Nu:- E+ Ejemplo de formación de enlace carbono-carbono. Reacción de adición Condensación aldólica Los enlaces carbono-carbono también pueden sufrir ruptura, dando lugar a dos moléculas a partir de una. Ejemplo de ruptura de enlace carbono-carbono. Reacción de adición Descarboxilación de un β-cetoácido Hay reacciones en las que se rompen y forman nuevos enlaces reemplazando uno de los sustituentes del carbono por otro sustituyente. Son reacciones de sustitución Reacciones de sustitución. Ejemplo: Tipos de reacciones Reacciones de oxidación-reducción Reacciones que forman o rompen enlaces carbonocarbono Reordenamientos internos, isomerizaciones y eliminaciones Reacciones de transferencia de grupos Reacciones de hidrólisis Isomerizaciones Glucosa-6-fosfato fosfohexosa isomerasa Fructosa-6-fosfato La conversión de Glu-6-P a Fru-6-P catalizada por una enzima llamada fosfohexosa isomerasa, es un paso clave en la vía glicolítica Eliminaciones Son reacciones que conducen a una olefina (alqueno) a través de la eliminación de una molécula de agua Tipos de reacciones Reacciones de oxidación-reducción Reacciones que forman o rompen enlaces carbonocarbono Reordenamientos internos, isomerizaciones y eliminaciones Reacciones de transferencia de grupos Reacciones de hidrólisis Reacciones de transferencia de grupos Adenina Ribosa glucosa Adenina Ribosa Glucosa-6-fosfato, un éster fosfato Tipos de reacciones Reacciones de oxidación-reducción Reacciones que forman o rompen enlaces carbonocarbono Reordenamientos internos, isomerizaciones y eliminaciones Reacciones de transferencia de grupos Reacciones de hidrólisis Reacciones de hidrólisis Ejemplos Acetil-CoA hidrólisis Ácido acético Reacciones de hidrólisis Acidez y Basicidad Ácidos Inorgánicos HCl Bases inorgánicas NaOH H2SO4 H3PO4 HBr HF Ca(OH)2 KOH Qué características tienen en común los ácidos inorgánicos? Todos ellos pueden ceder un H+ (protón) …y las bases o álcalis? Todas ellas pueden ceder HO o más ampliamente, pueden captar un H+. Ejemplo: HCl + NaOH NaCl + H2O Reacción de neutralización Según Bronsted-Lowry: Un ácido es una sustancia que cede iones hidrógenos (protones) H+ Una base es una sustancia que capta iones hidrógenos HCl + H2O ácido base Cl + H3 + O Base Ácido conjugada conjugado Como vimos en el ejemplo anterior el agua se comporta como una base porque capta un H+ del ácido clorhídrico. Pero el agua también puede comportarse como un ácido cediento un H+ H2O + B: HO + + HB Las sustancias que pueden comportarse como ácidos y como bases según las condiciones en las que se encuentren se denominan anfolitos El pH es una medida de la acidez o alcalinidad de una solución. El pH indica la concentración de iones hidronio [H3O+] presentes en determinadas sustancias. La sigla significa "potencial de hidrógeno" La escala de pH va de 0 a 14 en disolución acuosa, siendo ácidas las disoluciones con pH menores a 7 y alcalinas las que tienen pH mayores a 7. El pH = 7 indica la neutralidad de la disolución (donde el disolvente es agua). Una definición más útil en química orgánica es la propuesta por Gilbert N. Lewis. Según esta denición: Un ácido es una sustancia capaz de captar un par de electrones y una base es una sustancia capaz de ceder pares de electrones. Son ácidos orgánicos los siguientes grupos: O OH R R OH OH Ácidos carboxílicos Fenoles Alcoholes Son bases orgánicas los siguientes grupos: R OH R O O R' O R R H O R R O O R R OH R'' N R' R' OR' NH2 Todos estos compuestos tienen átomos con pares de electrones libres