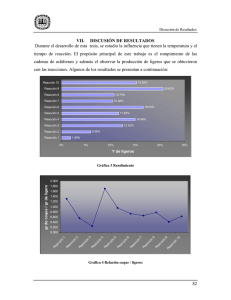
estudios de adsorción y desorción de asfaltenos y su fracción a2 en
Anuncio

UNIVERSIDAD SIMÓN BOLÍVAR DECANATO DE ESTUDIOS PROFESIONALES COORDINACIÓN DE LICENCIATURA EN QUÍMICA ESTUDIOS DE ADSORCIÓN Y DESORCIÓN DE ASFALTENOS Y SU FRACCIÓN A2 EN UNA INTERFASE TOLUENO-SÍLICE Por: Jonathan Da Silva Teixeira TRABAJO ESPECIAL DE GRADO Presentado ante la ilustre Universidad Simón Bolívar como requisito parcial para optar al título de Licenciado en Química Sartenejas, Abril de 2010 UNIVERSIDAD SIMÓN BOLÍVAR DECANATO DE ESTUDIOS PROFESIONALES COORDINACIÓN DE LICENCIATURA EN QUÍMICA ESTUDIOS DE ADSORCIÓN Y DESORCIÓN DE ASFALTENOS Y SU FRACCIÓN A2 EN UNA INTERFASE TOLUENO-SÍLICE Por: Jonathan Da Silva Teixeira Realizado con la asesoría de: Prof. Belsay Borges TRABAJO ESPECIAL DE GRADO Presentado ante la ilustre Universidad Simón Bolívar como requisito parcial para optar al título de Licenciado en Química Sartenejas, Abril de 2010 III RESUMEN En el presente trabajo se exponen los resultados obtenidos en el estudio de los procesos de adsorción y desorción de los asfaltenos y su fracción soluble en tolueno (A2) extraídos de los crudos Hamaca (n-C5, n-C6, n-C7), Boscán (n-C5, n-C7) y San Jacinto (n-C7) sobre superficies de gel de sílice, aplicando la técnica de espectrofotometría de absorción molecular UV-Visible. Primeramente, se obtuvieron las muestras de asfaltenos Boscán mediante la utilización de varias n-parafinas, encontrándose que la cantidad de asfaltenos aislados se incrementaba en función de la disminución del número de átomos de carbono del n-alcano. Luego, se realizó el fraccionamiento de los asfaltenos con p-nitrofenol. En el caso de los asfaltenos Hamaca no se logró obtener las fracciones esperadas, probablemente, debido a que estas moléculas pudieron ser oxidadas lentamente por el O2 atmosférico. En contraste, para los asfaltenos Boscán, los cuales fueron recién precipitados, se obtuvieron las fracciones correspondientes, tal que la cantidad de la fracción A1 fue superior a la cantidad de A2. Finalmente, se determinaron las isotermas de adsorción de las muestras bajo análisis, evidenciándose en todos los casos, que la cantidad de muestra adsorbida se incrementaba al aumentar el tiempo de contacto con la superficie adsorbente. Así mismo, las curvas reflejaron la formación de multicapas debido a la generación y adsorción de agregados asfalténicos. En cuanto al proceso de desorción, la cantidad desorbida resultó ser mucho menor que la cantidad adsorbida, por lo que se presume que la adsorción de asfaltenos es irreversible. La cantidad de asfaltenos adsorbidos se incrementaba con el aumento del tamaño de la cadena carbonada de la n-parafina utilizada para la precipitación de los asfaltenos. Por otro lado, se encontró que la solubilidad de los asfaltenos y su fracción A2 se redujo abruptamente luego del proceso de adsorción. Al analizar la influencia de la naturaleza de los asfaltenos en el proceso de adsorción, se observó que los asfaltenos San Jacinto (n-C7) tienden a adsorberse en mayor magnitud que los asfaltenos Hamaca y Boscán (n-C7), debido a su capacidad de formar agregados intermoleculares de grandes dimensiones. IV AGRADECIMIENTOS Llegamos hasta este punto del camino, un camino que ahora se torna diferente y que se constituye en el final de un eslabón y en el principio de toda una cadena de sueños … …Agradezco a todas las personas que me acompañaron en este viaje: A Dios, por estar conmigo en cada paso que doy, por fortalecer e iluminar mi mente y por haber puesto en mi camino a aquellas personas que han sido mi soporte y compañía durante todo el periodo de estudio. A la profesora Belsay Borges, por su incondicional apoyo en lo académico y su gran paciencia, además de su respaldo como amiga. A mis padres y a mis hermanos, por brindarme el cariño, la paciencia y la fuerza necesaria para salir adelante. V ÍNDICE GENERAL ÍNDICE DE TABLAS IX ÍNDICE DE FIGURAS X LISTA DE ABREVIATURAS Y SÍMBOLOS XIII INTRODUCCIÓN 1 CAPÍTULO I: MARCO TEÓRICO 4 1.1 El petróleo: Origen, localización y tratamiento……………………………………… 4 1.1.1 Propiedades del petróleo…………………………………………………….…… 7 1.1.1.1 Características físicas………………………………………………………... 8 1.1.1.2 Composición química……………………………………………………...… 10 1.2 Descripción de los asfaltenos………………………………………………………... 14 1.2.1 Composición química……………………………………………………………. 14 1.2.2 Fraccionamiento: A1 y A2……………………………………………………...… 18 1.3 Modelos de precipitación de asfaltenos……………………………………………… 20 1.3.1 Modelo termodinámico contínuo………………………………………………… 20 1.3.2 Modelo termodinámico coloidal………………………………………….……… 22 1.4 Factores que inducen la precipitación de asfaltenos…………………………………. 23 1.4.1Tipo de disolvente………………………………………………………………... 23 1.4.2 Relación disolvente/crudo……………………………………………………...... 25 1.4.3 Presión…………………………………………………………………………… 25 1.4.4 Temperatura……………………………………………………………………… 27 1.4.5 Naturaleza del crudo…………………………………………………………...… 28 1.5 Procesos Superficiales: Adsorción y desorción……………………………………… 29 1.5.1 Generalidades……………………………………………………………………. 29 1.5.2 Materiales adsorbentes…………………………………………………………... 30 1.5.3 Isotermas de adsorción…………………………………………………………... 31 1.5.4 Adsorción y desorción de asfaltenos………………………………...…………... 38 1.6 Espectrofotometría UV-Visible……………………………………………………… 42 1.6.1 Generalidades……………………………………………………………………. 42 1.6.2 Transiciones electrónicas……………………….……………………………….. 43 1.6.3 Espectrofotómetro UV-Visible……………………………….………………….. 44 1.6.4 Desviaciones de la Ley de Lambert-Beer………………………………….…….. 45 1.6.5 Espectroscopía de absorción aplicado al estudio de asfaltenos………………….. 46 VI CAPÍTULO II: SECCIÓN EXPERIMENTAL 48 2.1 Crudos…..……………………………………………………………...…………..… 48 2.2 Reactivos…..………..……………………………………………………………….. 49 2.3 Equipos…………………………………………………….………..……………..… 49 2.4 Metodología experimental…..………..………..………..…………………………… 51 2.4.1 Precipitación y obtención de asfaltenos…..………..………..…………………… 51 2.4.2 Fraccionamiento de asfaltenos con p-nitrofenol…..……………………………... 52 2.4.3 Determinación de las isotermas de adsorción de asfaltenos y su fracción A2 sobre superficies de gel de sílice………………………………………………… 54 2.4.3.1 Construcción analítica de las isotermas de adsorción……………………….. 55 2.4.3.2 Determinación de la solubilidad de los asfaltenos y su fracción A2…...…….. 56 CAPÍTULO III: RESULTADOS Y DISCUSIÓN 58 3.1 Proceso de precipitación de asfaltenos del crudo Boscán empleando como agentes precipitantes n-C5 y n-C7............................................................................................. 58 3.2 Obtención de las fracciones A1 y A2 de los asfaltenos usando PNF………………… 59 3.2.1 Fraccionamiento de los asfaltenos extraídos del crudo Hamaca (n-C5, n-C6 y n-C7)……………………………………………………………………………... 59 3.2.2 Fraccionamiento de los asfaltenos extraídos del crudo Boscán (n-C5 y n-C7)….. 61 3.3 Estudios de adsorción y desorción de asfaltenos sobre superficies de gel de sílice a diferentes tiempos de contacto…………………………............................................ 62 3.3.1 Isotermas de adsorción para asfaltenos del crudo Hamaca (n-C5, n-C6 y n-C7) sobre superficies de gel de sílice a 24, 48 y 72 h ………………………………... 62 3.3.2 Isotermas de adsorción para asfaltenos del crudo Boscán (n-C5 y n-C7) sobre superficies de gel de sílice a 24, 48 y 72 h……………………………………… 64 3.3.3 Isotermas de adsorción para la fracción A2 de los asfaltenos del crudo Boscán (n-C5 y n-C7) sobre superficies de gel de sílice a 24, 48 y 72 h………………... 66 3.3.4 Isotermas de adsorción para asfaltenos del crudo San Jacinto (n-C7) sobre superficies de gel de sílice a 24, 48 y 72 h………………………………............. 67 3.3.5 Influencia del agente precipitante en el proceso de adsorción de asfaltenos sobre superficies de gel de sílice a tiempos de contacto de 24, 48 y 72 h…………….. 72 3.3.5.1 Asfaltenos extraídos del crudo Hamaca (n-C5, n-C6 y n-C7)………….…… 72 3.3.5.2 Asfaltenos extraídos del crudo Boscán (n-C5 y n-C7)….…………………… 73 3.3.6 Comparación de las isotermas de adsorción de los asfaltenos Boscán y su fracción A2 (n-C5 y n-C7) sobre superficies de gel de sílice a tiempos de contacto de 24, 48 y 72 h …………………………………………………………………………... 75 VII 3.3.7 Influencia de la naturaleza de diferentes asfaltenos (n-C7) en el proceso de adsorción sobre superficies de gel de sílice a tiempos de contacto de 24, 48 y 72 h………………………………………………………………………………. 77 CONCLUSIONES 79 RECOMENDACIONES 81 REFERENCIAS BIBLIOGRÁFICAS 82 VIII ÍNDICE DE TABLAS Tabla 1.1 Relación elemental H/C de varios asfaltenos precipitados con n-pentano…...................................................................................................... 15 Tabla 1.2 Características de los diferentes tipos de adsorción…………………………. 29 Tabla 1.3 Contribución energética de las interacciones en el proceso de adsorción sobre una superficie de caolinita…………………………………………….. 39 Tabla 2.1 Propiedades de los crudos empleados……………………………………….. 48 Tabla 2.2 Propiedades fisicoquímicas de los reactivos empleados. …………………… 49 Tabla 3.1 Porcentajes de los asfaltenos del crudo Boscán obtenidos con n-C5 y n-C7.. 58 Tabla 3.2 Porcentajes de las fracciones A1 y A2 de los asfaltenos extraídos del crudo Boscán con n-C5 y n-C7………………………………………………...…… 62 Tabla 3.3 Valores de S A para los asfaltenos extraídos del crudo Hamaca (n-C5, n-C6 y n-C7).…………………………………………………………………….… 64 Tabla 3.4 Valores de S A para los asfaltenos extraídos del crudo Boscán (n-C5 y n-C7).………………………………………………………………………… 65 Tabla 3.5 Valores de S para la fracción A2 de los asfaltenos extraídos del crudo A Boscán (n-C5 y n-C7)………………………………………………..……… 67 Tabla 3.6 Valores de S A para los asfaltenos extraídos del crudo San Jacinto (n-C7)… 68 Tabla 3.7 Valores de X A y X D para los asfaltenos Hamaca (n-C6) y San Jacinto (n-C7)………………………………………………………………………… 71 IX ÍNDICE DE FIGURAS Figura 1.00 Distribución de las reservas de petróleo del mundo…............................... Figura 1.11 Procesos de extracción, producción, transporte y refinación del 1 petróleo…………………………………………………………………... 7 Figura 1.12 Esquema del método SARA……………………………………………... 11 Figura 1.13 Estructura hipotética de la ― Fracción Saturada‖ del petróleo……………. 11 Figura 1.14 Estructura hipotética de la ― Fracción Aromática‖ del petróleo………….. 12 Figura 1.15 Estructura hipotética de la ― Fracción de Resinas‖ del petróleo………….. 12 Figura 1.16 Estructura hipotética de la ― Fracción de Asfaltenos‖ del petróleo………. Figura 1.20 Estructura de los asfaltenos del crudo Athabasca propuesta por Strausz y 13 colaboradores…………………………………………………………..… 15 Figura 1.21 Estructura de los asfaltenos del crudo Cerro Negro propuesta por Acevedo y colaboradores………………………………………………… 16 Figura 1.22 Estructura de los asfaltenos de un crudo Venezolano propuesta por Murgich y colaboradores. (a) Bosquejo dimensional, (b) Bosquejo tridimensional……………………………………………………………. 16 Figura 1.23 Estructura de los asfaltenos propuesta por Strausz y colaboradores…….. 17 Figura 1.24 Formación de dímeros, trímeros y tetrámeros para una molécula de asfaltenos……………………………………………………………….. Figura 1.25 Estructuras de las fracciones de los asfaltenos propuestas por Acevedo y colaboradores. (a) Fracción A2, (b) Fracción A1………………………… Figura 1.26 18 19 Estructuras ― Tipo Rosario‖ de las fracciones de los asfaltenos propuestas por Acevedo y colaboradores. (a) Fracción A1, (b) Fracción A2………... 20 Figura 1.30 Modelo termodinámico continuo para la precipitación de asfaltenos…… 21 Figura 1.31 Modelo termodinámico coloidal para la precipitación de asfaltenos. (a) Acción peptizante de las resinas sobre los asfaltenos en la matriz del crudo, (b) Interacción de coloides...……………………………………... 22 Figura 1.32 Estructura coloidal de los asfaltenos en solución propuesto por Acevedo. 23 Figura 1.40 Efecto del número de carbonos del agente precipitante sobre la cantidad de componentes insolubles………………………………………………. Figura 1.41 Variación del contenido de asfaltenos precipitados con respecto a la cantidad de disolvente usado…………………………………………….. Figura 1.42 24 25 Efecto de la presión y la temperatura sobre la precipitación de asfaltenos……………………………………………………………….... 26 X Figura 1.43 Efecto de la temperatura sobre la precipitación de asfaltenos con distintos solventes……………………………………………………….. 28 Figura 1.44 Contenido de asfaltenos en crudos de diferente origen………………….. 28 Figura 1.50 Representación no lineal de la Isoterma de Langmuir…………………… 34 Figura 1.51 Representación lineal de la Isoterma de Langmuir…………………….… 35 Figura 1.52 Clasificación de las isotermas de adsorción propuesta por Giles y colaboradores…………………………………………………………..… 37 Figura 1.53 Isotermas de adsorción de asfaltenos sobre varios minerales obtenidas por Collins y colaboradores……………………………………………… Figura 1.54 38 Isotermas de adsorción para asfaltenos Furrial sobre gel de sílice obtenidas por Acevedo y colaboradores…………………………….…… 40 Figura 1.60 Espectro Electromagnético…………………………………………….… 42 Figura 1.61 Niveles de energía electrónicos de los orbitales moleculares…………… 43 Figura 1.62 Esquema de un espectrofotómetro UV-Visble………………………...… 44 Figura 1.63 Representación esquemática de la distribución de población de cromóforos en crudos y asfaltenos en el espectro electromagnético…….. 46 Figura 2.00 Esquema representativo del proceso de precipitación de asfaltenos…….. 52 Figura 2.10 Esquema representativo para el fraccionamiento de asfaltenos con PNF………………………………………………………………………. Figura 2.20 53 Esquema del estudio de adsorción y desorción de los asfaltenos y su fracción A2…………………………………………………………...…... 54 Figura 2.30 Modelo de la isoterma de adsorción construida…………………………. 57 Figura 3.00 Fraccionamiento de los asfaltenos del crudo Hamaca con PNF…………. 60 Figura 3.10 Isotermas de adsorción para asfaltenos Hamaca (n-C5) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h.…………………………… Figura 3.11 Isotermas de adsorción para asfaltenos Hamaca (n-C6) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h.………………………..….. Figura 3.12 63 Isotermas de adsorción para asfaltenos Boscán (n-C5) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h.…………………………………. Figura 3.14 63 Isotermas de adsorción para asfaltenos Hamaca (n-C7) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h.…………………………… Figura 3.13 62 64 Isotermas de adsorción para asfaltenos Boscán (n-C7) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h.…………………………..……… 65 Figura 3.15 Isotermas de adsorción para la fracción A2 de los asfaltenos Hamaca (n-C5) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h………. 66 XI Figura 3.16 Isotermas de adsorción para la fracción A2 de los asfaltenos Hamaca (n-C7) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h………. Figura 3.17 Isotermas de adsorción para asfaltenos San Jacinto (n-C7) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h……………………………. Figura 3.20 66 67 Superposición de las isotermas de adsorción para asfaltenos del crudo Hamaca obtenidos con diferentes agentes precipitantes. (a) 24 h, (b) 48 h, (c) 72 h......................................................................................... Figura 3.21 72 Superposición de las isotermas de adsorción para asfaltenos del crudo Boscán obtenidos con diferentes agentes precipitantes. (a) 24 h, (b) 48 h, (c) 72 h………………………………………………………... 73 Figura 3.22 Características de los asfaltenos extraídos con diferentes n-parafinas…... 74 Figura 3.30 Superposición de las isotermas de adsorción de los asfaltenos y su fracción A2 del crudo Boscán precipitados con n-C5. (a) 24 h, (b) 48 h, (c) 72 h…………………………………………………………………… 75 Figura 3.31 Superposición de las isotermas de adsorción de los asfaltenos y su fracción A2 del crudo Boscán precipitados con n-C7. (a) 24 h, (b) 48 h, (c) 72 h…………………………………………………………………… 76 Figura 3.40 Figura 3.41 Superposición de las isotermas de adsorción para asfaltenos de diferentes crudos precipitados con n-C7. (a) 24 h, (b) 48 h, (c) 72 h…… 77 Espectros de absorción UV-Visible de diferentes asfaltenos (n-C7)……. 78 XII LISTA DE ABREVIATURAS Y SÍMBOLOS A1 Fracción asfalténica insoluble en tolueno. A1-PNF Complejo insoluble formado cuando una solución de asfaltenos en tolueno es mezclada con una solución saturada de PNF en tolueno. A2 Fracción asfalténica soluble en tolueno. A2-PNF Complejo soluble formado cuando una solución de asfaltenos en tolueno es mezclada con una solución saturada de PNF en tolueno. Abs Absorbancia. ASTM American Society Tensting Materials. [C]A Concentración de muestra adsorbida. CD Concentración de muestra desorbida. CE Concentración teórica obtenida de la isoterma de adsorción asumiendo que el proceso de desorción es completamente reversible. [C]I Concentración inicial de las muestras. [C]R Concentración remanente. GE Gravedad Específica. Ir Intensidad del haz de referencia. Is Intensidad del haz de la muestra. K Constante de equilibrio. kA Constante de velocidad para el proceso de adsorción. kD Constante de velocidad para el proceso de desorción. l Camino óptico. mA Cantidad de muestra adsorbida. mD Cantidad de muestra desorbida. mR Cantidad de muestra remanente adsorbida que queda en la placa luego del proceso de desorción. mSílice Masa aproximada de una placa de gel de sílice 2x1 cm. n Número de moléculas adsorbidas. N Número total de sitios activos disponibles para la adsorción. n-Cx n-Parafina, donde x es el número de átomos de carbono del compuesto. PNF p-Nitrofenol. ppm Partes por millón. s Desviación Estándar XIII SA Solubilidad aparente de los asfaltenos y su fracción A2 en tolueno cuando la muestra está en contacto con la superficie del adsorbente. SARA Saturados, Aromáticos, Resinas y Asfaltenos. SO Solubilidad de los asfaltenos y su fracción A2 en tolueno a temperatura ambiente. VA Velocidad del proceso de adsorción. VD Velocidad del proceso de desorción. VS Volumen de la solución donde ocurren los procesos de adsorción y desorción. XA Cantidad de soluto adsorbido por unidad de masa del adsorbente. XD Cantidad de muestra desorbida por unidad de masa del adsorbente. XR Cantidad de muestra remanente adsorbida por unidad de masa del adsorbente. Θ Grado de recubrimiento. λ Longitud de onda. ε Coeficiente de absortividad molar. XIV INTRODUCCIÓN Justificación e importancia de la investigación El petróleo es un recurso natural no renovable que aporta el 36% del total de la energía que se consume en el mundo. Lo usamos para generar electricidad, obtener energía térmica para fábricas, hospitales y oficinas; y elaborar diversos lubricantes para maquinaría y vehículos. El total de recursos de petróleo del planeta es de aproximadamente 9-13 trillones de barriles. La mayor parte de estos recursos corresponde a hidrocarburos pesados, los cuales son difíciles y caros de producir (Figura 1.00). El hidrocarburo más viscoso, el bitumen, es un sólido a temperatura ambiente y se ablanda fácilmente cuando se calienta. Por lo general, mientras más pesado es el petróleo, menor es su valor económico, pues tienden a poseer mayores concentraciones de metales y otros elementos, lo que exige más esfuerzos y erogaciones para la obtención de productos utilizables y la disposición final de los residuos. Las fracciones de crudo más livianas y menos densas, derivadas del proceso de destilación simple, son las más valiosas. Con la gran demanda y los altos precios del petróleo, y estando en declinación la producción de la mayoría de los yacimientos de petróleo convencionales, la atención de la industria en muchos lugares del mundo se está desplazando hacia la explotación de petróleo pesados y extrapesados[1,2]. Figura 1.00. Distribución de las reservas de petróleo del mundo[2]. Los crudos pesados y extrapesados poseen un alto contenido de moléculas de asfaltenos. Usualmente, estos compuestos se definen de acuerdo a su solubilidad como: la fracción del petróleo insoluble en n-parafinas de bajo peso molecular[3]. Los asfaltenos pueden precipitar de forma espontánea en el crudo formando un sólido amorfo constituido por una mezcla de componentes de alto peso molecular y elevado contenido de heteroátomos. Son éstos sólidos 1 los responsables, en su mayoría, del taponamiento de las tuberías debido a las incrustaciones que se forman, obligando en muchos casos a paralizar el proceso de producción. Está problemática afecta a la industria petrolera en todos sus procesos: a nivel de yacimiento, los asfaltenos pueden alterar el flujo de la fase en el reservorio; en la producción, pueden tapar la salida del pozo; en el transporte, pueden precipitar en el oleoducto; y en la refinación, pueden envenenar los catalizadores. Así mismo, los asfaltenos provocan una alta contaminación ambiental ocasionada por la limpieza necesaria de todo el equipo de operación tras su deposición y adherimiento en las paredes del pozo[4,5]. Adicionalmente, su compleja estructura molecular no permite una fácil degradación por la acción de ciertos microorganismos[6]. Estos son fenómenos que han sido experimentados por la industria petrolera durante muchos años de operación. En el crudo, los asfaltenos están presentes como partículas coloidales dispersas en la fase oleosa (maltenos); las propiedades de estos coloides dependen del contenido de resinas y otros componentes del crudo. Las resinas son parte del medio oleoso, pero tienen elevada polaridad. Esta propiedad les facilita a las resinas ser fácilmente adsorbidas sobre los asfaltenos, actuando como neutralizante de carga o agente peptizante. Cualquier variación en la matriz del petróleo podría desestabilizar este sistema, promoviendo la interacción mutua entre las moléculas de asfaltenos; es decir, se generarían agregados asfalténicos de proporciones variables que inducen la precipitación de los mismos[3,7]. Se ha encontrado adsorción de asfaltenos en forma directa sobre superficies minerales y metálicas. En este sentido, se piensa que la tendencia de los asfaltenos a formar agregados intermoleculares está relacionada con su capacidad para la formación de multicapas sobre superficies sólidas[7,8]. La comprensión de estos fenómenos es de gran relevancia para tratar de evitar la precipitación y la consecuente adsorción de estos compuestos sobre las instalaciones con el correspondiente impacto negativo para la industria petrolera. A pesar de que son contundentes las evidencias encontradas sobre los asfaltenos por diferentes autores, el comportamiento de estos sistemas depende de muchos factores como: concentración, presión, temperatura y naturaleza del crudo, entre otras. Por esto es necesario seguir con trabajos de investigación orientados a la búsqueda de evidencias experimentales que permitan explicar el comportamiento de los asfaltenos y sus fracciones sobre superficies sólidas y su tendencia a formar agregados intermoleculares. 2 Objetivos de la investigación El objetivo general de este trabajo fue estudiar los procesos de adsorción y desorción de los asfaltenos y su fracción soluble en tolueno (A2), extraídos de crudos con diferentes agentes precipitantes, sobre superficies de gel de sílice; aplicando la técnica de absorción molecular UV-Visible. En aras de alcanzar la meta planteada, a continuación se destacan los objetivos específicos de esta investigación: Extraer los asfaltenos del crudo Boscán con n-C5 y n-C7. Aislar las fracciones A1 y A2 con p-nitrofenol de los asfaltenos Hamaca (n-C5, n-C6, n-C7) y Boscán (n-C5 y n-C7). Establecer la influencia del agente precipitante en el proceso de adsorción de los asfaltenos Hamaca (n-C5, n-C6, n-C7) y Boscán (n-C5 y n-C7) sobre superficies de gel de sílice a diferentes tiempos de contacto. Determinar la nueva solubilidad de los asfaltenos y su fracción A2 luego de la adsorción en la interfase tolueno-sílice a diferentes tiempos de contacto. Comparar el proceso de adsorción de los asfaltenos del crudo Boscán y su correspondiente fracción A2 (n-C5 y n-C7) sobre superficies de gel de sílice a diferentes tiempos de contacto. Indagar el efecto de la naturaleza de los asfaltenos Hamaca, Boscán y San Jacinto (n-C7) en el proceso de adsorción sobre superficies de gel de sílice a diferentes tiempos de contacto. 3 CAPÍTULO I MARCO TEÓRICO En este capítulo se establecen las bases teóricas que contextualizan el tema bajo investigación, con énfasis en las propiedades fisicoquímicas del petróleo, así como su composición. En particular, se describe la naturaleza de la fracción asfalténica del crudo. 1.1 El petróleo: Origen, localización y tratamiento El petróleo es una mezcla compleja en la que coexisten fracciones sólidas, líquidas y gaseosas. Principalmente, está conformado por compuestos denominados hidrocarburos, constituidos por átomos de carbono e hidrógeno, en su mayoría naftenos, parafinas y aromáticos. Además, presenta proporciones variables de compuestos azufrados, nitrogenados y oxigenados, así como metales (vanadio, níquel, hierro y plomo), dependiendo de su volatilidad, peso específico y viscosidad[9,10]. Existen varias teorías sobre la formación del petróleo. Sin embargo, la más aceptada es la teoría orgánica, la cual supone que se originó por la descomposición de restos de animales y plantas superiores acumuladas en el fondo de los mares, lagunas y en el curso inferior de los ríos. Esta materia orgánica se cubrió paulatinamente con capas cada vez más gruesas de sedimentos, al abrigo de las cuales, a determinadas condiciones de presión, temperatura y tiempo, se transformó lentamente en hidrocarburos. Estas conclusiones se fundamentan en la localización de los mantos petroleros, ya que todos se encuentran en terrenos sedimentarios. Además, los elementos químicos y moléculas complejas que constituyen el petróleo son característicos de los organismos vivientes (biomarcadores). Ahora bien, existen científicos que no aceptan esta teoría. Su principal argumento estriba en el hecho inexplicable de que si es cierto que existen más de 30.000 campos petroleros en el mundo entero, hasta ahora sólo 33 de ellos constituyen grandes yacimientos. De esos yacimientos, 25 se encuentran en el Medio Oriente y contienen más del 60% de las reservas probadas de nuestro planeta. Entonces, resultaría improbable que la mayoría de los animales hayan muerto en menos del 1% de la corteza terrestre[10-12]. 4 Por otro lado, la teoría inorgánica sostiene que el crudo se formaría netamente por reacciones químicas; es decir, sin la intervención de especies animales o vegetales. Se fundamenta en experimentos de laboratorio mediante los cuales carburos metálicos en presencia de agua generan hidrocarburos. En tal sentido, el agua se filtraría a las profundas capas terrestres y allí se formarían hidrocarburos de cadenas cortas, que luego por reacciones de polimerización producirían hidrocarburos cada vez más complejos. Sin embargo, estudios geológicos y químicos demuestran que los componentes del petróleo son ópticamente activos, lo cual no es característico de los compuestos inorgánicos[10-12]. Uno de los primeros pasos en la búsqueda del petróleo es la obtención de imágenes por medio de satélites, aviones o radares de una superficie determinada. Esto permite elaborar mapas geológicos en los que se identifican ciertas características, tales como: vegetación, topografía, corrientes de agua, tipos de roca, fallas geológicas, anomalías térmicas, etc. Esta información da una idea general de aquellas zonas que tienen condiciones propicias para la presencia de mantos sedimentarios en el suelo (geoquímica de superficie)[10-12]. Actualmente, el método más empleado para hallar el petróleo es la reflexión sísmica. Los movimientos sísmicos provocados con explosivos y pesadas planchas metálicas que se dejan caer en sitios muy localizados del suelo producen ondas sísmicas, las cuales son analizadas para conocer las particularidades del área del subsuelo estudiada. El petróleo puede estar en el mismo lugar donde se formó (en la roca madre) o haberse filtrado hacia otros reservorios por entre los poros o fracturas de las capas subterráneas[10-12]. Toda la información obtenida a lo largo del proceso exploratorio es objeto de interpretación en los centros geológicos y geofísicos de las empresas petroleras. Pero, en último término, la única forma de demostrar la existencia de petróleo en el subsuelo es perforando un pozo exploratorio. De hecho, casi todas las zonas petrolíferas del mundo fueron identificadas en un principio por la presencia de filtraciones superficiales, y la mayoría de los yacimientos fueron descubiertos por prospectores particulares que se basaban más en la intuición que en la ciencia. El tamaño de esos depósitos varía desde unas pocas decenas de hectáreas hasta decenas de kilómetros cuadrados. El tiempo de perforación de un pozo dependerá de la profundidad programada y las condiciones geológicas del subsuelo. La perforación se realiza por etapas, de tal manera que el tamaño del pozo en la parte superior es ancho y en las partes inferiores cada vez más angosto. Para proteger el pozo de derrumbes, filtraciones o cualquier otro problema propio de la perforación, se adhieren a las paredes del 5 hueco unos tubos de revestimiento con cemento especial que se inyecta a través de las mismas tuberías[10-12]. Una vez hallado, puede ser recuperado a través de la presión creada por el gas natural o agua dentro del yacimiento (producción primaria). También puede ser extraído mediante la inyección de agua, dióxido de carbono, polímeros y solventes que permitan, eventualmente, incrementar la presión artificialmente o reducir la viscosidad del mismo (recuperación mejorada). Si no existe esa presión, se emplean otros métodos de extracción. El más común ha sido el ―b alancín‖, el cual, mediante un permanente balanceo, acciona una bomba en el fondo del pozo que succiona el petróleo hacia la superficie. El crudo extraído, generalmente, viene acompañado de sedimentos, agua y gas natural, por lo que deben construirse previamente las facilidades de producción, separación y almacenamiento[11]. El petróleo es transportado por oleoductos de caudal continuo, que a menudo pueden llevar más de 500.000 barriles por día, o a través de buques oceánicos a las refinerías. El gas natural asociado que acompaña al petróleo se separa previamente y se envía a plantas de tratamiento para la recuperación mejorada o para evitar la subsidencia[11]. El petróleo es transformado a productos de gran valorización en refinerías. Las refinerías son muy distintas unas de otras, según las tecnologías y los esquemas de proceso que se utilicen, así como su capacidad. Existen refinerías simples y complejas. Las simples están constituidas solamente por algunas unidades de tratamiento, mientras que las refinerías complejas cuentan con un mayor número de estas unidades. El proceso de refinación empieza con la destilación o fraccionamiento del petróleo en varios cortes de hidrocarburos. La calidad de los productos resultantes depende de las características del crudo procesado. La mayor parte de los productos destilados y residuos, posteriormente, son transformados a través del craqueo, reformado, isomerización y otros procesos de conversión. Luego, estos derivados son sometidos a diversos tratamientos para remover constituyentes indeseables y mejorar el octanaje. Con estas etapas se pueden obtener desde gases ligeros, como el propano y el butano, hasta fracciones más pesadas, fuel-óleo y asfaltos, pasando por otros productos intermedios como la gasolina, el gasoil y los aceites lubricantes[11] (Figura 1.11). 6 Figura 1.11. Procesos de extracción, producción, transporte y refinación del petróleo. 1.1.1 Propiedades del petróleo El petróleo es muy complejo y, por tanto, exhibe una amplia gama de propiedades físicas, algunas de las cuales pueden correlacionarse entre sí. Mientras que propiedades como la viscosidad, densidad y coloración pueden variar extensamente, el análisis elemental varía sobre un intervalo estrecho para un gran número de muestras de petróleo. El contenido de carbono es relativamente constante, en tanto que el contenido de hidrógeno y de heteroátomos son los principales responsables de las diferencias entre muestras de petróleo[9.,10]. La evaluación del petróleo como materia prima para la obtención de ciertos derivados implica la evaluación de una serie de propiedades físicas. Cada crudo se compara con las otras materias primas disponibles y, basándose en la realización del producto se le asigna un valor[9,10]. 7 1.1.1.1 Características físicas Coloración: La mayor parte de la población tiende a pensar que el petróleo es de color negro. Sin embargo, pueden ser desde color ámbar, pasando por amarillo pálido, rojo y marrón, hasta llegar al negro. Los aceites de bajo peso específico son amarillos, los medianos ámbar, y los aceites más pesados son oscuros. Por luz reflejada, el aceite crudo es usualmente verde, debido a la fluorescencia. Por lo general, su tonalidad se oscurece con el aumento de su peso específico[9-12]. Olor: El olor del petróleo es de efluvio aromático como el de la gasolina, el queroseno u otros derivados. Si contiene elevadas proporciones de azufre, el olor llega a ser repugnante. Por otro lado, si el contenido de sulfuro de hidrógeno es muy alto, los vapores son irritantes, tóxicos y hasta mortíferos[9-12]. Análisis Elemental: El análisis del crudo a través de los porcentajes de carbono, hidrógeno, nitrógeno, oxígeno, y azufre es, quizás, el primer método usado para examinar la naturaleza general, y realizar una evaluación de la materia prima. Las proporciones atómicas de varios elementos respecto al carbono (H/C, N/C, O/C, y S/C) pueden caracterizar el petróleo. Además, contiene trazas de vanadio, níquel y otros metales, los cuales pueden tener graves efectos en el funcionamiento de catalizadores durante el proceso de refinación. Las proporciones de los elementos en el petróleo varían ligeramente sobre límites estrechos: - Carbono: 83 a 87%. - Hidrógeno: 10 a 14%. - Nitrógeno: 0,1 a 2%. - Oxígeno: 0,05 a 1,5%. - Azufre: 0,05 a 6%. - Metales: <1000 ppm[9-12]. Densidad: La densidad relativa del petróleo se mide empleando una escala arbitraria denominada gravedad °API (American Petroleum Institute), la cual establece la relación correspondiente de peso específico (GE) de los crudos con respecto al agua. La gravedad °API se puede medir a través de un hidrómetro. 8 La fórmula empleada para obtener este parámetro a 60 °F es la siguiente: 141,5 0 Gravedad API 0 GE 60 F 131,5 (1) Entonces, al agua a 60 °F le corresponde una gravedad °API de 10; líquidos menos densos que el agua tienen una gravedad °API mayor a 10 y líquidos más densos que el agua tienen una gravedad °API menor de 10. El peso específico depende intrínsecamente de la composición química del petróleo. Generalmente, se establece que el aumento de la concentración de compuestos aromáticos causa un incremento de la densidad, mientras que el aumento de concentración de compuestos saturados se traduce en una disminución de la densidad. La clasificación del petróleo de acuerdo a su gravedad °API se muestra a continuación: - Extrapesados: Menores o iguales a 9,9 °API. - Pesados: Entre 10 y 22,3 °API. - Medianos: Entre 22,3 y 31,1 °API. - Livianos: Mayores a 31,1 °API[9-12]. Viscosidad: La viscosidad es una medida de la resistencia interna al flujo, siendo de gran importancia en procesos operacionales de producción, transporte y refinación del petróleo. Usualmente, representa el tiempo necesario para que un volumen dado de aceite, a una temperatura definida, fluya a través de un pequeño orificio de dimensiones estándar. Se mide con un instrumento denominado viscosímetro[9-12]. La viscosidad de los crudos varía desde 0,2 hasta más de 1000 unidades de centipoise. Esta propiedad permite estimar la energía necesaria para transportar un crudo a través de un oleoducto, desde el yacimiento hasta la refinería. Los aceites compuestos de hidrocarburos de las series CnH2n-2 y CnH2n-4 son muy viscosos. Los crudos pesados están compuestos por gran cantidad de estos hidrocarburos. Es muy importante el efecto de la temperatura sobre la viscosidad de los crudos, en el yacimiento o en la superficie, especialmente concerniente a crudos pesados y extrapesados, ya que, a mayor temperatura, el petróleo fluye mucho mejor, lo cual es indicativo de que la viscosidad disminuye en gran medida[9-12]. 9 Volatilidad: La volatilidad es la capacidad que tiene una sustancia de evaporarse a una temperatura y presión determinada. El punto de ebullición de las moléculas orgánicas se incrementa con el número de átomos de carbono en las moléculas y, por lo tanto, con el incremento de la masa molecular y el número de electrones. Las moléculas más grandes y pesadas son atraídas entre sí, con fuerzas intermoleculares más fuertes que las que existen en las moléculas más pequeñas, necesitándose temperaturas mayores para vaporizar los componentes de mayor masa molecular debido a estas fuerzas intermoleculares intensas. Entonces, teniendo en consideración que el petróleo está constituido por una mezcla de hidrocarburos, cuando éste es sometido a calentamiento severo, los hidrocarburos más ligeros (1 a 5 átomos de carbono) son los primeros en evaporarse. La tendencia del petróleo a vaporizarse es la base del proceso de refinación[9-12]. 1.1.1.2 Composición química El petróleo constituye una mezcla de compuestos orgánicos con estructura variada y con diferentes pesos moleculares, por lo cual resulta difícil caracterizar todos sus componentes presentes. El procedimiento SARA permite separar los constituyentes del petróleo que ha perdido sus componentes gaseosos en cuatros grupos orgánicos definidos: Saturados, Aromáticos, Resinas y Asfaltenos. El análisis SARA se basa en la diferencia de solubilidad, polaridad y peso molecular de los constituyentes presentes en el petróleo. En dicho fraccionamiento, los asfaltenos se separan de los otros componentes por precipitación mediante el agregado de una n-parafina. Los componentes remanentes denominados maltenos se fraccionan en forma consecutiva mediante cromatografía líquida en columna abierta de alúmina o sílice. Cada componente se remueve de la columna mediante un lavado con un disolvente de polaridad específica. La elución de los hidrocarburos saturados se realiza con un n-alcano, la de los hidrocarburos aromáticos con una mezcla 2:1 en volumen de n-heptano y tolueno o 1:1 de n-alcano y diclorometano, y las resinas con una mezcla 1:1:1 de diclorometano, tolueno y metanol o con piridina (Figura 1.12). El rendimiento de cada una de las fracciones dependerá de su respectivo volumen de retención, que dependerá a su vez del adsorbente elegido y del poder de elución de los disolventes[11,13]. 10 Figura 1.12. Esquema del método SARA[13]. La ventaja del método SARA es que se trata de un procedimiento simple, que puede ser llevado a cabo en muchos laboratorios. No obstante, este análisis también plantea numerosas desventajas, que se ponen de manifiesto cuando se utiliza con fines ajenos a su objetivo original. En primer lugar, el petróleo muerto carece de los componentes gaseosos que están disueltos en los petróleos vivos y, por ende, los resultados no son representativos de la forma en que actuaría el petróleo bajo condiciones de yacimiento. Además, los métodos de laboratorio difieren considerablemente y la solubilidad de los asfaltenos varía con el tipo de n-alcano utilizado para precipitarlo. Esto significa que un mismo crudo podría tener dos o más resultados SARA, dependiendo de los disolventes empleados[13]. A continuación se describen los grupos orgánicos obtenidos con dicho análisis: Saturados: Los compuestos saturados son hidrocarburos no polares, sin dobles enlaces, que incluyen a los alcanos de cadenas lineales y ramificadas, así como a los cicloalcanos (Figura 1.13). La proporción de compuestos saturados en el crudo normalmente disminuye con el aumento del peso molecular de las fracciones, por lo que estos compuestos representan la fracción liviana del crudo. Representan entre 5-50% de la masa total del petróleo. Su relación H/C varía entre 1-2, con trazas de heteroátomos. Poseen un peso molecular entre 470-1200 g/mol y una densidad a 20°C entre 0,7-0,8 g/mL[14-16]. Figura 1.13. Estructura hipotética de la ― Fracción Saturada‖ del petróleo. 11 Aromáticos: Constituidos por polienos cíclicos conjugados que se caracterizan por su alta estabilidad. Generalmente, son moléculas de benceno que poseen ramificaciones o moléculas de estructuras similares al naftaleno y al antraceno, pero mucho más complejas (Figura 1.14). Junto con las resinas, son los componentes más abundantes del crudo, ya que representan entre 30-45% de la masa total del petróleo. Se presentan como materiales líquidos, de coloración variable entre amarrillo y rojo. Poseen un peso molecular entre 570-1500 g/mol y una densidad a 20°C entre 0,9-1,2 g/mL[14-16]. Figura 1.14. Estructura hipotética de la ― Fracción Aromática‖ del petróleo. Resinas: Representan la fracción no coloidal del crudo, constituyendo la transición entre la parte más polar (asfaltenos) y las fracciones relativamente no polares (maltenos). Las resinas son solubles en solventes como: tolueno, n-pentano, n-hexano y n-heptano, e insolubles en ácidos. Presentan una estructura intermedia entre los aceites y los asfaltenos (Figura 1.15); además, mantienen a estos últimos dispersos en el crudo, actuando así como surfactantes. Las resinas pueden ser adsorbidas sobre sílice, alúmina y otras superficies activas. Se presentan como materiales semisólidos, de color rojizo, de bajo punto de fusión y alto poder adhesivo. Poseen un peso molecular entre 780-2000 g/mol y su densidad a 20°C es inferior a 1,07 g/mL[14-16]. Figura 1.15. Estructura hipotética de la ― Fracción de Resinas‖ del petróleo. 12 Asfaltenos: Los asfaltenos típicamente son definidos como la fracción de crudo soluble en tolueno, benceno y tetrahidrofurano e insoluble en un exceso de n–parafinas (n-pentano, n-heptano, etc.). Los asfaltenos están constituidos por anillos aromáticos condensados ligados a cadenas alquílicas y cicloalcanos, además de compuestos heterocíclicos que poseen nitrógeno, azufre y oxígeno (Figura 1.16). Representan entre 2-20% de la masa total del petróleo. Poseen un peso molecular entre 800-3500 gr/mol y su densidad a 20°C es inferior a 1,2 g/mL[14-16]. Figura 1.16. Estructura hipotética de la ― Fracción de Asfaltenos‖ del petróleo. El azufre es el tercer constituyente atómico más abundante del petróleo. Está presente en todas las fracciones, desde las más livianas hasta las más pesadas. Los compuestos de azufre identificados en las fracciones ligeras y medias del crudo se pueden distribuir en cuatro clases generales: tioles, también llamados mercaptanos; sulfuros orgánicos e inorgánicos; disulfuros y derivados del tiofeno[17]. El nitrógeno se encuentra especialmente en las fracciones de alto peso molecular y alto punto de ebullición. Estos compuestos son, en forma general, de estructuras aromáticas policíclicas, las cuales podrían contener a su vez otros heteroátomos. En las fracciones livianas, se pueden hallar compuestos básicos de nitrógeno: quinolina y piridina. El resto, son moléculas no básicas conformadas por carbazoles e indoles; y la forma más predominante en las fracciones pesadas de asfaltenos son las porfirinas[15-17]. Por otra parte, el oxígeno está presente en forma de ácidos, alcoholes, cetonas y fenoles. Los compuestos particularmente característicos del oxígeno son los ácidos nafténicos [17]. También existen trazas de metales pesados en el petróleo, tales como: níquel, vanadio y plomo. Se encuentran retenidos en estructuras porfirínicas, formando enlaces de coordinación con los nitrógenos del pirrol, en una estructura planar y aromática con 18 electrones en el 13 anillo. Su origen se debe principalmente a reacciones químicas de intercambio que tuvieron lugar hace millones de años en las primeras etapas de descomposición de la materia orgánica. La comprobación de la existencia de estos compuestos en los asfaltenos se lleva a cabo mediante estudios de espectrofotometría UV-Visible. Éstas presentan una absorción característica en el rango de longitudes de onda comprendidos entre 390 y 420 nm[17]. Sin embargo, los metales no solamente están presentes en los asfaltenos en forma de metaloporfirinas, sino que también existen en una forma no coordinada. Constantinides y colaboradores (1967) afirman que el vanadio aparece como metaloporfirina en un crudo venezolano, en un porcentaje equivalente al 31% del total. El balance de masa indica que aproximadamente un 70% de este elemento está asociado a estructuras no porfirínicas. Se piensa que pueden aparecer en forma de naftenatos, los cuales se hacen más abundantes en la medida en que la gravedad °API decrece[18]. 1.2 Descripción de los asfaltenos 1.2.1 Composición química La estructura de los asfaltenos es muy diversa y depende intrínsecamente del crudo del cual provienen. En general, se considera que estos compuestos están constituidos por núcleos aromáticos condensados con cadenas alquílicas laterales y heteroátomos incorporados en muchas de las estructuras cíclicas. Los sistemas aromáticos condensados pueden tener desde 4 hasta más de 20 anillos bencénicos. El alto contenido de heteroátomos permite establecer ciertas similitudes entre los asfaltenos y el kerógeno (producto de la degradación de la materia orgánica por microorganismos) hasta el punto de que una de las hipótesis que intentan explicar el origen de los asfaltenos, los presentan como un estado de maduración intermedio entre el kerógeno y los hidrocarburos livianos. Ahora bien, las moléculas de asfaltenos poseen partes relativamente polares, dadas por los anillos aromáticos y los grupos funcionales, y partes apolares constituidas por las cadenas alifáticas; lo cual les permite presentar un comportamiento dual polar-apolar.[20-23]. A temperatura ambiente, los asfaltenos son sólidos compactos de color marrón-negruzco. Además, son infusibles, lo que significa que no poseen un punto de fusión definido, pero se descomponen frente al calor, dejando un residuo carbonoso. Presentan una proporción H/C 14 entre 0,98-1,20. De hecho, para asfaltenos precipitados con n-pentano presentan una relación H/C casi constante de 1,15; tal como es evidenciado en la tabla 1.1[22]. Tabla 1.1 Relación elemental H/C de varios asfaltenos precipitados con n-pentano[22]. Origen del Crudo Canadá Iraq Kuwait Iran Composición (%Peso) H C 8,0 79,5 7,9 81,7 7,9 82,4 7,5 83,4 Relación atómica H/C 1,21 1,16 1,14 1,07 La determinación de la estructura molecular promedio de los asfaltenos se realiza mediante diversas técnicas analíticas, tales como: difracción de rayos X, resonancia magnética nuclear, absorción óptica, espectroscopia molecular de fluorescencia, difracción de neutrones a pequeños ángulos, osmometría de presión de vapor, espectroscopía de masas, ultracentrifugación, electroforesis, dispersión dinámica de luz, cromatografía de impregnación de gel, entre otras. Dado que estos métodos investigan diversos aspectos de los asfaltenos bajo diferentes condiciones, no es sorprendente que hayan producido modelos dispares de las moléculas de asfaltenos[24-28]. Mediante un proceso denominado octilación, Strausz y colaboradores (1977) establecieron la estructura molecular de los asfaltenos del crudo Athabasca. Esta técnica permite la introducción de grupos n-octilos en la molécula de asfaltenos para evitar que existan interacciones y la formación de agregados asfalténicos. Entonces, propusieron una estructura formada por segmentos de azufre unidos entre sí, con un peso molecular aproximado de 6000 Daltons[29] (Figura 1.20). Figura 1.20. Estructura de los asfaltenos del crudo Athabasca propuesta por Strausz y colaboradores[29]. 15 Acevedo y colaboradores (1982) estudiaron la estructura molecular de la fracción asfalténica del crudo Cerro Negro proveniente de la Faja Petrolífera del Orinoco. De esta estructura, destacaron que las moléculas de asfaltenos pueden interaccionar a través de puentes de hidrógeno, fuerzas intermoleculares tipo ― dipolo-dipolo‖ y transferencia de carga[30] (Figura 1.21). Figura 1.21. Estructura de los asfaltenos del crudo Cerro Negro propuesta por Acevedo y colaboradores[30]. Murgich y colaboradores (1996) analizaron las fracciones de alto peso molecular de un crudo Venezolano por medio de ciertas técnicas: 1H-RMN, IR, osmometría de presión de vapor y análisis elemental. Las estructuras moleculares promedio de las resinas y asfaltenos fueron similares a otras reportadas en la literatura. No obstante, la comparación entre los bosquejos espaciales de los asfaltenos reveló que el número de sitios activos disponibles para la interacción de estas moléculas a través de puentes de hidrógeno fue menor a lo esperado, producto de efectos estéricos[31] (Figura 1.22). (a) (b) Figura 1.22. Estructura de los asfaltenos de un crudo Venezolano propuesta por Murgich y colaboradores. (a) Bosquejo dimensional, (b) Bosquejo tridimensional[31]. 16 Los modelos moleculares presentados hasta ahora indican que los asfaltenos poseen una condensación aromática extendida con cadenas alquílicas en su periferia, lo cual les confiere gran solubilidad en solventes como THF y tolueno. Sin embargo, una organización estructural muy diferente fue propuesta por Strausz y colaboradores (1999), utilizando como métodos la pirólisis y estudios selectivos de oxidación asfalténica. Al someter a calentamiento severo moléculas complejas se genera una amplia gama de productos, desde metano hasta residuos de carbono, cuestión que fue observada por los investigadores. Por lo tanto, concluyeron que los asfaltenos no necesariamente están constituidos por núcleos aromáticos de grandes dimensiones[32] (Figura 1.23). Figura 1.23. Estructura de los asfaltenos propuesta por Strausz y colaboradores[32]. 17 Debido a la presencia de anillos aromáticos condensados y heteroátomos, los asfaltenos pueden enlazarse entre sí a través de interacciones π-π o puentes de hidrógeno. Simulaciones computarizadas demuestran que la diferencia de energía de asociación entre dos monómeros y un dímero se encuentra entre 200-400 KJ/mol. Esta diferencia energética decrece a 40-200 KJ/mol cuando esta asociación es analizada en solventes como tolueno y n-heptano. La solubilidad de estos agregados asfalténicos disminuye con el incremento en la cantidad de moléculas asociadas [15] (Figura 1.24). Figura 1.24. Formación de dímeros, trímeros y tetrámeros para una molécula de asfaltenos[15]. 1.2.2 Fraccionamiento de los asfaltenos: A1 y A2 El fraccionamiento de los asfaltenos es de gran relevancia para lograr disminuir la complejidad y la polidispersidad de la muestra, haciendo más fácil el análisis de sus propiedades estructurales. Existen múltiples técnicas que se pueden utilizar para tal fin, como la cromatografía de intercambio iónico, cromatografía de adsorción, precipitación diferencial y diálisis[33-35]. Acevedo y colaboradores (2001) propusieron un método novedoso para el fraccionamiento de asfaltenos empleando p-nitrofenol (PNF). Básicamente, consiste en adicionar al medio en el cual se encuentran inmersas las moléculas de asfaltenos un compuesto capaz de generar dos 18 complejos de transferencia de carga, uno soluble y el otro insoluble en el medio de reacción. Luego, el agente acomplejante (p-nitrofenol) es removido mediante extracciones sucesivas ácido-base. Las fracciones obtenidas fueron llamadas como A1 y A2. De acuerdo a los resultados presentados por estos investigadores, la solubilidad en tolueno de la fracción A2 es mucho mayor que la fracción A1, a pesar de que sus pesos moleculares eran similares. De esta forma, concluyeron que los asfaltenos son una mezcla de compuestos con una gran diferencia de solubilidad, en donde la fracción A1 (insoluble) representa una fase coloidal dispersada por la fracción A2 (soluble). A continuación se muestran las estructuras propuestas por los investigadores para estas fracciones[34] (Figura 1.25). Figura 1.25. Estructuras de las fracciones de los asfaltenos propuestas por Acevedo y colaboradores. (a) Fracción A2, (b) Fracción A1[34]. Acevedo y colaboradores (2004) fraccionaron los asfaltenos del crudo Furrial con p-nitrofenol. Las fracciones fueron caracterizadas a través de análisis elemental, determinación de pesos moleculares y RMN. Entre los resultados más significativos se destacan: Diferencias entre la cantidad de hidrógenos aromáticosalto contenido de hidrógenos enlazados a carbonos alifáticos y diferencias entre la cantidad de carbonos aromáticos[35]. El bajo contenido de hidrógenos alifáticos y el alto contenido de hidrógenos aromáticos sugiere que la fracción A1 se encuentra conformada por un conjunto de anillos policíclicos aromáticos y unidades nafténicas. Por el contrario, el elevado contenido de hidrógenos alifáticos y de hidrógenos aromáticos, sugiere que la fracción A2 presenta una estructura conformada por una pequeña cantidad de anillos policíclicos unidos por cadenas alifáticas. Mediante el empleo de mecanismos moleculares para el cálculo de geometrías y energías óptimas se pudo proponer un nuevo modelo estructural para dichas fracciones[35] (Figura 1.26). 19 (a) (b) Figura 1.26. Estructuras ― Tipo Rosario‖ de las fracciones de los asfaltenos propuestas por Acevedo y colaboradores. (a) Fracción A1, (b) Fracción A2[35]. Los pesos moleculares y el contenido de heteroátomos de las fracciones resultaron ser similares. Así pues, la marcada diferencia de solubilidad obedece a la movilidad espacial de las estructuras en cuestión. La fracción A2 es más flexible que A1, lo cual le confiere mayor solubilidad y no le permite formar agregados intermoleculares de manera eficiente[35]. 1.3 Modelos de precipitación de asfaltenos El desarrollo de los modelos de precipitación de asfaltenos está basado en dos descripciones conceptuales de estas moléculas en solución. El modelo termodinámico continuo establece que los asfaltenos y las resinas son moléculas individuales disueltas en el crudo. Por otro lado, el modelo termodinámico coloidal establece que las resinas y los asfaltenos forman agregados dispersos en la matriz del petróleo[36-41]. 1.3.1 Modelo termodinámico contínuo El modelo termodinámico continuo, también conocido como modelo de solubilidad, predice el comportamiento de fase de los componentes orgánicos pesados dentro del crudo. Las propiedades de las fracciones pesadas y su dispersión en el crudo dependen de sus pesos moleculares y de la composición química del petróleo. La precipitación de los componentes con alto peso molecular involucra un cambio en el equilibrio molecular del sistema. Este modelo considera que la precipitación es un proceso reversible, ya que se asume que las 20 partículas de asfaltenos se dispersan y se estabilizan en el crudo. La disolución completa de los asfaltenos en algunos solventes orgánicos apoya esta suposición[36]. La proporción de moléculas polares y no polares, y la proporción de moléculas de alto y bajo peso molecular en una mezcla compleja como el petróleo, constituyen los principales factores responsables de mantener la solubilidad dual. La estabilidad del sistema se altera por la adición de solventes miscibles. Las moléculas polares y de alto peso molecular, como los asfaltenos, se separan de la mezcla en forma de líquidos o sólidos (precipitado) [36]. El primer modelo termodinámico continuo fue propuesto por Hirschberg y colaboradores (1984). Ellos describen el fenómeno de la precipitación de asfaltenos a través del equilibrio termodinámico reversible líquido-líquido de una mezcla de pseudo-componentes, los asfaltenos y el resto de las fracciones que constituyen el crudo, denominado solvente. Entonces, bajo ciertas condiciones de presión y temperatura, el petróleo se puede separar en dos fases líquidas, una de las cuales se constituye sólo por los asfaltenos, mientras que la otra por ambos componentes, pero en su gran mayoría por el solvente. La separación de fases es calculada mediante el modelo de Huggins-Flory, el cual establece que los asfaltenos son polímeros monodispersos en solución[37] (Figura 1.30). Este modelo es de fácil aplicabilidad y se pude emplear para hallar parámetros de solubilidad. Figura 1.30. Modelo termodinámico continuo para la precipitación de asfaltenos[37]. 21 1.3.2 Modelo termodinámico coloidal Los asfaltenos constituyen moléculas insolubles y dispersas en el crudo; asociándose en tres o cuatros moléculas para formar una micela o coloide. El modelo termodinámico coloidal, desarrollado por Leontaritis y Mansoori (1987), asume que los asfaltenos son partículas sólidas de diferentes tamaños suspendidas en forma de coloide en el crudo y estabilizados por las moléculas de resinas adsorbidas en la superficie de los asfaltenos. El tamaño de la micela de los asfaltenos y el espesor de la capa peptizante dependen de la composición del crudo, la temperatura y la presión[38]. Ahora bien, cuando a este sistema estable se le inyecta un solvente ionizador (n-pentano, tolueno, etc.) o existe alguna perturbación físico-química en el campo petrolífero, la concentración de moléculas de resina cambia. Por lo tanto, algunas resinas abandonan la micela, causando la interacción mutua entre asfaltenos. Cuando dos partículas de asfaltenos con movimiento Browniano presentan contacto en áreas libres de resina, quedan pegadas, formando un cúmulo que se difundirá en el sistema, con la probabilidad de adherirse a partículas individuales o a otros agregados asfalténicos de tamaño variable que se encuentren en el crudo. Conforme este proceso transcurre en el tiempo, el número de partículas individuales disminuye y, en consecuencia, ocurre la precipitación. A diferencia del modelo termodinámico contínuo, este modelo asume que las precipitación de asfaltenos es irreversible[39-41] (Figura 1.31). (a) (b) Figura 1.31. Modelo termodinámico coloidal para la precipitación de asfaltenos. (a) Acción peptizante de las resinas sobre los asfaltenos en la matriz del crudo, (b) Interacción de coloides[38]. 22 Acevedo (2001) propuso una perspectiva más amplia del modelo coloidal a través de la inclusión de las fracciones A1 y A2 de los asfaltenos en dicho sistema. De manera que para obtener un coloide estable en solución, las resinas no solamente deben adsorberse en la superficie, sino ser capaces de penetrar más allá de su superficie, generando un coloide de menor densidad molecular y menor tensión interfacial[42] (Figura 1.32). AR: Aromáticos S: Saturados R: Resinas Figura 1.32. Estructura coloidal de los asfaltenos en solución propuesto por Acevedo[42]. 1.4 Factores que inducen la precipitación de asfaltenos La precipitación de los asfaltenos se debe fundamentalmente a alteraciones en el balance que mantiene a los coloides en solución. Este proceso se pone de manifiesto en todas las fases de producción, transporte y procesamiento del crudo. Por esta razón, es considerado un problema de peso que afecta la industria petrolera. El contenido y la composición de los asfaltenos depende de las siguientes variables: tipo de disolvente, relación disolvente/carga, temperatura, presión y la naturaleza del crudo[43-49]. 1.4.1Tipo de disolvente La separación de los asfaltenos puede realizarse convenientemente por medio de hidrocarburos parafínicos de bajo peso molecular. La variación en el tipo de disolvente puede causar cambios significativos en su precipitación y caracterización. La capacidad del disolvente para precipitar asfaltenos se incrementa en el siguiente orden: iso-parafina < n-parafina < olefina terminal 23 Para explicar esta diferencia es necesario considerar el poder solvatante del disolvente, que para el caso de los disolventes parafínicos, éstos tienden a autoasociarse disminuyendo así su poder de solvatación; lo contrario sucede con los disolventes aromáticos que no se asocian[11]. Así mismo, la cantidad de asfaltenos se ve afectada por el número de átomos carbonos del disolvente. De acuerdo con esto, conforme se incrementa el número de carbonos de la n-parafina, la cantidad de asfaltenos que se obtiene tiende a ser menor. En la Figura 1.40 se puede observar la relación existente entre la cantidad de componentes insolubles y los diferentes disolventes empleados. La cantidad de asfaltenos precipitados con n-C5 es más del doble que la obtenida con n-C7. La forma de la curva se debe al incremento del poder solvatante de los n-alcanos vinculado al aumento del tamaño de la cadena carbonada[11]. Sin embargo, no sólo se ve afectada la concentración, sino también las propiedades de los asfaltenos. Por ejemplo, si se usa n-heptano, los asfaltenos son de alto peso molecular y mayor polaridad, en tanto que con n-pentano son menos polares y de peso molecular más bajo, aunque con n-pentano hay mayor cantidad de precipitado[11]. Figura 1.40. Efecto del número de carbonos del agente precipitante sobre la cantidad de componentes insolubles[11]. 24 1.4.2 Relación disolvente/crudo Speight y Moschopedis (1981) recomiendan que la relación disolvente/crudo para la precipitación de asfaltenos a nivel experimental con hidrocarburos ligeros sea de 40:1[22]. Esto también ha sido reportado por otros autores, aunque sugieren que para obtener realmente las máximas concentraciones de asfaltenos, se deben emplear relaciones de 60:1[46] (Figura 1.41). Figura 1.41. Variación del contenido de asfaltenos precipitados con respecto a la cantidad de disolvente usado. (—) Crudo Athabasca, (---) Crudo Maya. Disolvente: n-C5[46]. 1.4.3 Presión La presión es uno de los factores más importantes que influyen en la precipitación de asfaltenos. Durante los procesos operacionales, la caída de presión del crudo hasta su punto de burbuja provoca que los componentes más livianos, como las cadenas alquílicas, se expandan más que los componentes pesados. El incremento del volumen molar de estos compuestos continúa mientras que la presión del crudo desciende. A través de la despresurización por debajo del punto de burbuja, las cadenas livianas abandonan el fluido en forma de gas y, por lo tanto, disminuye la concentración de los n-alcanos en el crudo[36]. La disminución de la presión y del volumen molar de los compuestos livianos en el crudo se traduce en un descenso de la densidad del fluido y una correspondiente disminución de la solubilidad de los asfaltenos. La separación entre moléculas de la fase líquida del crudo y las 25 micelas de resina-asfalteno resulta mayor en densidades bajas, cuando las interacciones resultan menos atractivas. Por tal motivo, las moléculas de asfaltenos tienden a precipitar[36]. Bilheimer y colaboradores (1949) analizaron el efecto de la presión y la temperatura sobre la precipitación de asfaltenos a partir de mezclas de tetralina con n-alcanos. Los investigadores encontraron que tanto la solubilidad en n-pentano como en n-decano se incrementó con la presión, aunque la temperatura presentó un cambio más notorio. Para el n-pentano, la solubilidad de los asfaltenos aumentó con la temperatura en las dos presiones investigadas, mientras que con n-decano las curvas mostraron pendientes opuestas[46] (Figura 1.42). Figura 1.42. Efecto de la presión y la temperatura sobre la precipitación de asfaltenos. (—) Mezcla n-pentano/tetralina, (---) Mezcla n-decano/tetralina. (•) P=1,0 kg/cm2, (o) P=517,0 kg/cm2 [46]. El problema de los depósitos de asfaltenos por cambios de presión se produce cuando la presión natural del pozo se agota o cuando existe alguna modificación en las condiciones operacionales[46]. 26 1.4.4 Temperatura Lhioreau y colaboradores (1967) establecieron que al incrementar la temperatura, la cantidad de asfaltenos precipitados también aumentaba, para los casos en donde se empleó n-hexano y n-pentano como disolventes, en tanto que usando n-heptano había una disminución en el porcentaje de asfaltenos precipitados. La solubilidad de los asfaltenos del crudo ligero Kirkuk se incrementó con el aumento de la temperatura, y para los asfaltenos del crudo pesado Qaiyarah se observó un aumento de la solubilidad seguido por una reducción arriba de 23°C usando n-C5, n-C6 y n-C7[47]. Speight (2007) ha demostrado que la solubilidad de los asfaltenos se reduce a altas temperaturas, ya que se logra que la tensión superficial del agente precipitante disminuya, y con ello su poder de solvatación hacia las moléculas de asfaltenos, por lo cual éstas precipitan[11]. Feng y colaboradores (2001) realizaron estudios sobre el efecto de la temperatura en la precipitación de asfaltenos en un crudo Chino. Trabajaron en el intervalo entre 20-65°C usando varios disolventes (n-C5 a n-C12). En todos los casos, se observó que el contenido de asfaltenos disminuyó ligeramente (de 6,12 a 4,12% m/m) con el aumento de temperatura. Para muchos sistemas y moléculas se espera un incremento de la solubilidad cuando se incrementa la temperatura si no existen interacciones como enlaces de hidrógeno[48]. Andersen y colaboradores (1990) estudiaron el efecto de la temperatura sobre la precipitación de los asfaltenos de un residuo de Kuwait usando diferentes disolventes parafínicos (n-C5 a n-C8) a temperaturas desde 4ºC hasta la temperatura de reflujo del agente precipitante y encontraron que para todos los solventes usados, la cantidad máxima precipitada de asfaltenos se obtenía a aproximadamente 25ºC. Cuando la temperatura sube de 4ºC a 25ºC la viscosidad del medio disminuye, lo que conduce a la asociación de moléculas de asfaltenos. Aumentando la temperatura por arriba de los 25ºC, comienzan a romperse los enlaces que mantienen unidos a los agregados asfalténicos y la solubilidad se incrementa. También obtuvieron asfaltenos a partir de los aceites crudos Kuwait y Boscán usando n-heptano y trabajando en un intervalo de temperaturas de –2-80ºC. Los resultados mostraron una disminución en el contenido de asfaltenos con el incremento de la temperatura[44,49] (Figura 1.43). 27 Figura 1.43. Efecto de la temperatura sobre la precipitación de asfaltenos con distintos solventes. (—) Residuo de Kuwait, (---) Crudo Kuwait, (- — -) Crudo Boscán. Disolventes: (■) n-C5, (o) n-C6, () n-C7, () n-C8[49]. 1.4.5 Naturaleza del crudo La composición química del petróleo y la profundidad a la cual se extrae son factores relevantes que determinan la cantidad de asfaltenos obtenidos del mismo. Por ejemplo, el crudo California de USA tiene el doble de contenido de asfaltenos que el crudo Cerro Negro de Venezuela[22] (Figura 1.44). Figura 1.44. Contenido de asfaltenos en crudos de diferente origen[22]. 28 1.5 Fenómenos Superficiales: Adsorción y Desorción 1.5.1 Generalidades La adsorción es el proceso mediante el cual un átomo o una molécula de una sustancia se adhiere a la superficie de un sólido o en la interfase entre dos fluidos. La especie que se adsorbe se llama "adsorbato" y la fase sobre la cual ocurre el fenómeno se denomina "adsorbente"[50]. El proceso de adsorción culmina cuando la energía libre interfacial haya alcanzado un mínimo. Así mismo, cuando todos los sitios del sustrato están ocupados, o cuando el empaquetamiento de las moléculas adsorbidas produce fuerzas contrarias, la adsorción alcanza el equilibrio. En realidad, es un equilibrio dinámico entre el proceso de adsorción y el proceso opuesto llamado desorción, en el cual una molécula adsorbida regresa al seno del líquido[50-52]. Dependiendo de la magnitud de las energías involucradas en el proceso existen dos tipos de adsorción: adsorción física (Fisisorción) o adsorción química (Quimisorción). La adsorción física es producida por interacciones débilmente polarizantes tipo Van der Waals, en el cual la energía involucrada en el proceso no es lo suficientemente grande como para romper enlaces y, por tanto, la molécula conserva su identidad química. La adsorción química es producida por fuertes interacciones polarizantes, en donde la energía liberada en el proceso es capaz de disociar enlaces, de manera que la molécula adsorbida pierde su identidad química. En la tabla 1.2 se evidencian las diferencias más relevantes entre estos tipos de adsorción[50-52]. Tabla 1.2. Características de los diferentes tipos de adsorción[50-52]. Características Tipos de Adsorción Quimisorción Fisisorción Rango de temperaturas Ilimitado (depende de cada molécula) Próximo al punto de condensación del gas Entalpías de adsorción Amplio rango (40-800 KJ/mol) Bajas (5-40 KJ/mol) Naturaleza de la adsorción A menudo disociativa. No disociativa. Saturación Monocapa Multicapa Cinética de adsorción Variable. Suele ser un proceso activado. Rápida. No es un proceso activado. 29 1.5.2 Materiales Adsorbentes Los materiales sólidos empleados como adsorbentes son productos naturales o sintéticos. En cualquier caso, el proceso de fabricación ha de asegurar un gran desarrollo superficial mediante una elevada porosidad. Los adsorbentes naturales tienen pequeñas superficies. Los adsorbentes industriales de buena calidad pueden llegar a tener entre 1.000 y 1.500 m2/g. Además, deben ser de fácil regeneración a través de procesos de desorción y estables térmicamente[53]. Entre los adsorbentes más utilizados se pueden citar los siguientes: Gel de Sílice: Se produce normalmente por neutralización de una disolución de silicato sódico mediante un ácido mineral diluido. El material obtenido se calienta a unos 350ºC y resulta un producto duro, inerte, cristalino, no tóxico y muy poroso. Las superficies específicas que se dan para este adsorbente son superiores a 350 m2/g. Es un producto que se puede regenerar una vez saturado, si se somete a una temperatura entre 120-180ºC. Se utiliza para secar líquidos y gases, así como para la recuperación de hidrocarburos. Además, el gel de sílice puede diferenciar la adsorción de diferentes moléculas actuando como un adsorbente selectivo[53]. Alúmina activada: Es un adsorbente con buena resistencia mecánica y, por ello, muy adecuado para su utilización en lechos móviles. Se fabrica calentando los distintos hidratos de alúmina a velocidad controlada. El producto, amorfo y muy poroso, se utiliza para el secado de gases y líquidos, eliminar fluoruro y neutralizar aceites lubricantes[53]. Carbón activado: Se produce a partir de diversas sustancias carbonosas de origen animal, vegetal o mineral, por medio de procesos térmicos que implican la deshidratación del material y la calefacción en ausencia de aire, seguidos por el tratamiento oxidante (activación) a altas temperaturas. Está constituido por un aglomerado rígido de microcristales, cada uno de los cuales está formado por una pila de planos grafíticos. Cada átomo dentro de un determinado plano está unido a cuatro átomos de carbono adyacentes. Así, los átomos de carbono en los bordes de los planos presentan una alta disponibilidad. Se emplea para la extracción de metales, tratamiento del agua potable, limpieza de vertidos, purificación de la glicerina, entre otros usos[53]. 30 Tamices moleculares: Están formados por estructuras tetraédricas de alumino-silicatos (SiO2-AlO4). El entramado es muy regular, de forma tal que sólo pueden adsorberse aquellas moléculas con un tamaño suficientemente pequeño como para atravesar los poros de la estructura. La ventaja de los tamices moleculares es que pueden fabricarse a la medida de las aplicaciones deseadas. Se usan ampliamente en la industria del petróleo, especialmente para la purificación de corrientes de gas, y en los laboratorios de química para separar compuestos y secar reactivos[53]. 1.5.3 Isotermas de adsorción Los distintos sistemas heterogéneos en los que puede tener lugar la adsorción son: sólidoliquido, sólido-gas y líquido-gas. Es importante el carácter más o menos polar de las moléculas de adsorbato, así como el tamaño de las mismas. El soluto se adsorberá más fácilmente cuando la afinidad de aquél por la superficie sea superior a su afinidad por el disolvente. Por tanto, la energía de unión entre la superficie y la sustancia considerada depende de la naturaleza de los solutos que han de adsorberse. Así mismo, la cantidad de sustancia adsorbida varía con la temperatura y la concentración de adsorbato en la disolución[50]. Una forma relativamente sencilla desde el punto de vista experimental de distinguir entre los diferentes tipos de adsorción consiste en obtener una isoterma de adsorción, la cual no es más que una representación gráfica de la cantidad adsorbida de soluto relativo a la masa del adsorbente frente a la concentración del soluto en el equilibrio[50,51]. Langmuir (1916) desarrolló un modelo simple para tratar de predecir el grado de adsorción de un gas sobre una superficie como función de la presión del fluido. Este modelo supone que: - No hay interacción entre las partículas adsorbidas. - La superficie del adsorbente es uniforme y regular. - Las moléculas adsorbidas no tienen movimiento sobre la superficie. - Ocurre la formación de una única monocapa[50,51]. 31 Los procesos de adsorción entorno a una interfase sólido-líquido pueden representarse mediante la siguiente ecuación química[51]: (2) Donde: A simboliza al adsorbato, S es el adsorbente o sustrato y AS al complejo adsorbente-adsorbato. Los procesos de adsorción están caracterizados por el valor de las constantes de velocidad, k A y k D , respectivamente. Para expresar el grado de extensión de la adsorción se introduce la fracción de recubrimiento (θ). Teniendo en cuenta que sobre cada posición sólo puede adsorberse una molécula: n N (3) Donde: n es el número de moléculas adsorbidas y N es el número total de sitios activos disponibles para la adsorción. Si consideramos una cinética de primer orden respecto a cada miembro, se obtiene que la velocidad de adsorción VA es: VA k A.A.N .(1 ) (4) Donde: A es la concentración de la especie A en la fase líquida. La velocidad de desorción VD es proporcional al número de moléculas adsorbidas: VD kD .N . (5) En el equilibrio la velocidad de reacción directa e inversa son iguales, de manera que igualando las ecuaciones (4) y (5), se obtiene: k A.A.(1 ) kD . (6) 32 Agrupando términos y resolviendo: k A.A k A.A. kD . (7) k A.A. kD . k A.A (8) .(k A.A kD ) k A.A (9) k A .A k A .A k D (10) Sacando factor común : Despejando en la ecuación (9): Al sacar factor común k D en el denominador de la ecuación (10), se obtiene: kA .A kD kA .A 1 kD (11) Definiendo a la constante de equilibrio (K) como la relación: K kA kD (12) Introduciendo la relación (12) en (11) se obtiene la ecuación que define la Isoterma de Langmuir: K .A K .A 1 (13) 33 En la Figura 1.50 se muestra una representación de la isoterma de Langmuir en su forma no lineal: Concentración A Figura 1.50. Representación no lineal de la Isoterma de Langmuir[51]. De la gráfica se observa que si: K.A 1 = = 1 (Superficie muy recubierta) (14) 1 K.A = = K.A (Superficie poco recubierta) (15) La ecuación obtenida para la isoterma de Langmuir puede convertirse en su forma lineal si se considera la fracción de recubrimiento (), entonces: n K .A N K .A 1 (16) Elevando ambos miembros de la ecuación (16) a la (-1): N K .A 1 n K .A (17) 34 Reordenando la ecuación (17) se obtiene: A K .A 1 (18) A A (19) n K .N Finalmente: n N 1 K .N A continuación se muestra una representación gráfica de la isoterma de Langmuir en su forma lineal: [A]/n vs.[A] 1000 [A]/n 800 600 400 200 0 0 100 200 [A] 300 400 500 Figura 1.51. Representación lineal de la Isoterma de Langmuir. No obstante, otros investigadores a lo largo del tiempo han desarrollado distintos tipos de isotermas que responden a situaciones no ideales, como: Freundlich, Brunauer-Emmet-Teller (BET) y Temkin. Estas isotermas resultan ser más complejas que la propuesta por Langmuir, pues además de considerar que la superficie del adsorbente no es uniforme, existen interacciones entre las moléculas adsorbidas y la adsorción ocurre a través de la formación de multicapas[50-53]. 35 Giles y colaboradores (1960) desarrollaron una teoría básica para la clasificación de las isotermas de adsorción para disoluciones diluidas. Esta clasificación se basa en la forma de la parte inicial de la isoterma, y los subgrupos se diferencian en la forma de la curva a elevadas concentraciones[54] (Figura 1.52). Las isotermas propuestas por Giles y colaboradores son: Isoterma S: La curva es convexa respecto al eje de abscisas, por tanto, aumenta la facilidad de adsorción al aumentar la concentración. Las curvas S aparecen cuando las moléculas de soluto cumplen las siguientes condiciones: - Monofuncionalidad: Las moléculas monofuncionales son aquellas que poseen un claro residuo hidrófobo y una marcada localización de las fuerzas de atracción por el sustrato sobre una corta sección de su periferia, siendo adsorbidas como una sola unidad y no en forma de micelas. - Atracción intermolecular moderada. - Fuerte competición por los lugares de adsorción entre las moléculas de adsorbato y las del disolvente[54]. Isoterma L (Tipo Langmuir): Es la más común de todas. Es cóncava respecto al eje de las abscisas, por tanto, al aumentar la concentración se hace más difícil la adsorción. Los sistemas donde se dan estas curvas cumplen las siguientes características: - Las moléculas adsorbidas son muy semejantes y se adsorben en forma plana. - Sufren poca competencia del disolvente si se adsorben por un extremo. - Sustrato y soluto altamente polares o con gran atracción intermolecular[54]. Isoterma H: Es un caso particular de las isotermas L, ya que presenta elevados valores de la capacidad de adsorción, incluso para pequeñas concentraciones en la fase líquida. Por lo tanto, el soluto tiene tan alta afinidad, que en disoluciones diluidas es 36 completamente adsorbido. Esto da lugar a que la parte inicial de la isoterma sea vertical[54]. Isoterma C: Se caracteriza por presentar una relación constante entre la concentración en la fase adsorbida y líquida, hasta alcanzar un máximo, a partir del cual se transforma en una línea horizontal. Además esta isoterma puede ser explicada por la penetración del soluto en los microporos del sustrato, con lo cual se abren nuevos sitios de adsorción. Las condiciones que favorecen la aparición de las isotermas C son: - Un sustrato poroso con moléculas flexibles y regiones con distinto grado de cristalización. - Un soluto con mayor afinidad por el sustrato que el disolvente. - Mayor poder penetrante[54]. Figura 1.52. Clasificación de las isotermas de adsorción propuesta por Giles y colaboradores[54]. 37 1.5.4 Adsorción y desorción de asfaltenos Es de suma importancia estudiar los procesos de adsorción y desorción de los asfaltenos sobre superficies sólidas debido a que en los distintos yacimientos petrolíferos estas moléculas son fuertemente adsorbidos sobre dichas superficies. La adsorción de asfaltenos representa una herramienta para correlacionar su solubilidad y estructura molecular. Collins y colaboradores (1983) obtuvieron datos acerca de la adsorción de asfaltenos sobre varios minerales. Además, caracterizaron a los asfaltenos a través de análisis elemental y determinación de pesos moleculares. En todos los casos, se evidenció una adsorción tipo Langmuir con la formación de una monocapa (Figura 1.53). Por otro lado, se determinó el efecto del agua sobre la adsorción de asfaltenos en superficies de Caolinita, encontrándose una disminución en la cantidad de asfaltenos adsorbidos producto de la pre-adsorción de moléculas de agua[55]. Figura 1.53. Isotermas de adsorción de asfaltenos sobre varios minerales obtenidas por Collins y colaboradores[55]. Acevedo y colaboradores (1995) analizaron el comportamiento de los asfaltenos y resinas sobre superficies orgánicas e inorgánicas empleando espectrometría UV-Visible. Se construyeron isotermas de adsorción para asfaltenos provenientes de dos crudos inestables a la precipitación (Furrial y Ceuta) y asfaltenos de un crudo estable a la precipitación (Cerro Negro). Las isotermas correspondientes a los asfaltenos de crudos inestables evidenciaron la formación de multicapas, debido a las fuertes interacciones entre las moléculas de asfaltenos 38 presentes en solución y la consiguiente formación de agregados adsorbidos en la superficie. En cambio, los asfaltenos de crudos estables a la precipitación mostraron una adsorción tipo Langmuir en todo el intervalo de concentraciones estudiado[56]. Kokal y colaboradores (1995) analizaron la adsorción de asfaltenos sobre superficies minerales como: caolinita, berea, limestona y dolomita. Para ello, colocaron en contacto soluciones de asfaltenos en tolueno en un intervalo de concentraciones entre 0-1500 mg/L sobre 0,7 g de superficies minerales durante 48 horas. Se observó que la cantidad de asfaltenos adsorbida fue aproximadamente similar, presentándose isotermas de adsorción tipo Langmuir. Los investigadores establecieron que la cantidad de moléculas adsorbidas es proporcional al área superficial del mineral[57]. Acevedo y colaboradores (1998) estudiaron la adsorción de asfaltenos (Furrial, Jobo y Hamaca) disueltos en tolueno sobre superficies de vidrio mediante la técnica de deformación fototérmica superficial. Esta técnica permite medir directamente la cantidad de asfaltenos adsorbidos en la superficie del sólido. Después de un largo periodo de contacto, las isotermas de adsorción reflejaron la formación de multicapas en todos los casos examinados. El análisis de los resultados sugirió que este comportamiento en la adsorción pudiera estar relacionado con el aumento repentino de la concentración de agregados asfalténicos[58]. Murgich y colaboradores (1998) analizaron las interacciones existentes entre los asfaltenos y las resinas en una superficie mineral como la caolinita, a través de cálculos de dinámica molecular. Se estableció que las interacciones predominantes entre los adsorbatos y el adsorbente correspondían a fuerzas de atracción tipo Van der Waals, seguidos por fuerzas coulómbicas y, finalmente, puentes de hidrógeno. Por otro lado, se encontró que las resinas interaccionan más fuertemente con la caolinita que con las moléculas de asfaltenos, indicando que esta superficie puede perturbar los agregados orgánicos hallados en el petróleo[59] (Tabla 1.3). Tabla 1.3. Contribución energética de las interacciones en el proceso de adsorción sobre una superficie de caolinita[59]. Tipo de Interacción Van der Waals Coulómbicas Puentes de Hidrógeno Contribución (%) 60-70 20-30 5-10 39 León y colaboradores (2002) estudiaron la adsorción de resinas sobre asfaltenos provenientes de crudos venezolanos empleando espectrometría UV-Visible. Las formas de las isotermas de adsorción obtenidas fueron atribuidas a la formación de multicapas y a la penetración de las resinas en los microporos de la estructura de los asfaltenos. Los investigadores concluyeron que las resinas al adsorberse efectivamente sobre la superficie de los asfaltenos ayudan a los mismos a disolverse y difundirse en el disolvente[60]. Marczewski y colaboradores (2002) estudiaron los procesos de adsorción de soluciones de asfaltenos en tolueno sobre varias superficies minerales como: cuarzo, dolomita, calcita y caolinita; así como también en óxidos metálicos (Fe2O3 y TiO2). En todos los casos, las isotermas de adsorción presentaron una gran desviación respecto a la clásica isoterma de Langmuir. La presencia de varios escalones en estas curvas indica la formación de multicapas sobre la superficie de los adsorbentes y la interacción entre las moléculas del adsorbato[61]. Acevedo y colaboradores (2003) estudiaron los procesos de adsorción de asfaltenos provenientes del crudo Furrial, en tolueno sobre gel de sílice. Para ello, construyeron isotermas de adsorción a 6, 72 y 168 horas. Los investigadores establecieron que los procesos de adsorción de asfaltenos pueden ajustarse a una cinética irreversible de segundo orden, observándose una reducción de la constante de velocidad a medida que se incrementa la concentración de asfaltenos en el medio de reacción[62] (Figura 1.54). Figura 1.54. Isotermas de adsorción para asfaltenos Furrial sobre gel de sílice obtenidas por Acevedo y colaboradores[62]. 40 Liao y colaboradores (2005) estudiaron los procesos de adsorción y oclusión de asfaltenos provenientes de crudos del Congo y de Venezuela. Se usaron n-parafinas deuteradas de la forma n-C20D42 para simular la adsorción y oclusión característica de los asfaltenos en soluciones de tolueno. Los resultados experimentales indicaron que la abundancia de microporos que existen en la estructura interna de los asfaltenos permiten adsorber y ocluir otras fracciones del crudo. Los compuestos ocluidos no pueden ser intercambiados por otras moléculas del medio, ya que este proceso ocurre en el núcleo de los agregados asfalténicos. Sin embargo, la adsorción ocurre en la superficie del asfalteno y, por lo tanto, podrían originarse procesos de desorción; intercambiando una molécula adsorbida por otra presente en el medio[63]. Acevedo y colaboradores (2007) estudiaron la relación existente entre las propiedades físicas y químicas de los asfaltenos y su estructura ― Tipo Rosario‖. Con tal finalidad, los investigadores determinaron pesos moleculares y relacionaron las solubilidades de los asfaltenos y su fracción A2 a través de isotermas de adsorción en una interfase tolueno-sílice. Así mismo, se realizaron estudios de cromatografía de exclusión por tamaño y cálculos de mecánica molecular. Se evidenció que al irradiar moléculas de asfaltenos con una fuente láser, éstas se fragmentan por las cadenas alquílicas encargadas de unir los anillos aromáticos condensados. Por otra parte, las grandes variaciones de solubilidad obtenidos a través de isotermas de adsorción pueden ser fácilmente explicados mediante un mecanismo de plegamiento-desplegamiento. Los experimentos de cromatografía demostraron que la fracción A2, debido a su mayor flexibilidad, es capaz de atrapar más moléculas de p-nitrofenol que la fracción A1. La conformación desplegada de la fracción A2 presenta una solubilidad muy baja y comparable a la de la fracción A1 en tolueno, mientras que su conformación plegada es muy soluble en tolueno[64]. 41 1.6 Espectrometría UV-Visible 1.6.1 Generalidades Los métodos espectrométricos más ampliamente utilizados están relacionados con la radiación electromagnética, la cual es una combinación de campos eléctricos y magnéticos oscilantes, que se propagan a través del espacio transportando energía de un lugar a otro. El espectro electromagnético se extiende desde la radiación de menor longitud de onda, como los rayos gamma y los rayos X, pasando por la luz ultravioleta, la luz visible y los rayos infrarrojos, hasta las ondas electromagnéticas de mayor longitud de onda, como son las ondas de radio[65]. (Figura 1.60). Figura 1.60. Espectro Electromagnético. El principio de la espectrometría ultravioleta-visible involucra la absorción de radiación por una especie atómica o molecular, causando la promoción de un electrón de un estado basal a un estado excitado, liberándose el exceso de energía en forma de calor. La cantidad de energía térmica desarrollada en la relajación no es, habitualmente, detectable. Por ello, las medidas de absorción crean una mínima perturbación del sistema en estudio. El tiempo de vida de la especie excitada es breve (10-8 a 10-9 s). La longitud de onda (λ) se encuentra entre 190 y 800 nm[65]. Aunque esta técnica no puede proporcionar la identificación inequívoca de un compuesto orgánico, el espectro de absorción en las regiones del ultravioleta y visible es, sin embargo, útil para detectar la presencia de ciertos grupos funcionales que actúan como cromóforos. Por ejemplo, una banda de absorción débil en la región de 280 a 290 nm, que se desplaza hacia longitudes de onda más cortas cuando aumenta la polaridad del disolvente, indica firmemente la presencia de un grupo carbonilo. Más importante, sin embargo, son las aplicaciones de esta técnica en la determinación cuantitativa de compuestos que contienen grupos absorbentes[65]. 42 1.6.2 Transiciones electrónicas Las especies absorbentes que contienen electrones π, σ y n incluyen iones y moléculas orgánicas, así como algunos aniones inorgánicos. En absorción UV-Visible, pueden observarse distintas transiciones electrónicas[65] (Figura 1.61): Transiciones σ → σ*: En este caso, un electrón de un orbital σ enlazante de una molécula se excita al correspondiente orbital antienlazante mediante la absorción de radiación. Comparado con otras posibles transiciones, la energía requerida para que tenga lugar esta transición es grande, correspondiendo a una frecuencia radiante de la región ultravioleta de vacío. Por lo general, se dan en hidrocarburos que únicamente poseen enlaces σ (C-H o C-C)[65]. Transiciones n → σ*: Los compuestos saturados que contienen pares de electrones no compartidos son capaces de sufrir transiciones n → σ*. Estas transiciones requieren menos energía que las del tipo σ → σ* y se pueden producir por radiación de la región comprendida entre 150-250 nm. Los máximos de absorción tienden a desplazarse hacia longitudes de onda más cortas en presencia de disolventes polares[65]. Transiciones n → π* y π → π*: La mayoría de las aplicaciones de espectroscopia UV-Visible están basadas en transiciones que ocurren en esta zona con longitudes de onda entre 200-700 nm. Ambas transiciones requieren la presencia de grupos funcionales no saturados que aportan los electrones π. Las energías de excitación en las transiciones π → π* son medianamente altas, mientras que las transiciones n → π* son considerablemente menores[65]. Figura 1.61. Niveles de energía electrónicos de los orbitales moleculares[65]. 43 1.6.3 Espectrofotómetro UV-Visible Para medir el espectro UV-Visible de un compuesto, la muestra se disuelve en un disolvente que no absorba por encima de 190 nm. La muestra disuelta se coloca en una celda de cuarzo y parte del disolvente se coloca en una celda de referencia. Un espectrofotómetro de UV-Visible opera comparando la cantidad de luz transmitida a través de la muestra con la cantidad de luz del haz de referencia. El haz de referencia pasa a través de la celda de referencia para compensar cualquier absorción de luz debida a la celda y al disolvente[65,66]. El espectrofotómetro tiene una fuente que emite todas las frecuencias de luz UV. La luz pasa a través de un monocromador, que utiliza una red de difracción o un prisma para dispersar la luz, descomponiéndola en un amplio espectro y selecciona una longitud de onda. Esta única longitud de onda de luz se divide en dos haces, un haz pasa a través de la celda de muestra y el otro a través de la celda de referencia. El detector mide constantemente la relación de intensidad entre el haz de referencia (Ir) y el haz de la muestra (Is). Mientras el espectrofotómetro explora las longitudes de onda en la región UV, un registrador hace el gráfico (espectro) de la absorbancia de la muestra en función de la longitud de onda[66] (Figura 1.62). Figura 1.62. Esquema de un espectrofotómetro UV-Visble[66]. La absorbancia (Abs) de la muestra a una longitud de onda determinada viene dada por la Ley de Lambert –Beer: Ir Abs log .c.l Is (20) 44 Donde: c es la concentración de la muestra, l es el camino óptico y ε es el coeficiente de absortividad molar[66]. Si la muestra absorbe luz a una longitud de onda determinada, el haz de muestra es menos intenso que el de referencia y la relación Ir/Is es mayor que 1. La relación es igual a 1 cuando no hay absorción. La absorbancia, por lo tanto, es mayor que cero cuando la muestra absorbe y es igual a cero cuando no hay absorción. Las medidas de absorbancia espectrofotométricas se hacen, normalmente, a una longitud de onda correspondiente a un pico de absorción, ya que el cambio en la absorbancia por unidad de concentración es mayor en este punto, consiguiéndose la máxima sensibilidad. Además, la curva de absorción es, a menudo, plana en esta región; bajo estas circunstancias, se puede esperar una buena observación de la ley de Beer[65]. Un espectro de UV es un gráfico de la absorbancia en función de la longitud de onda. Las variables que suelen influir en el espectro de absorción de una sustancia incluyen la naturaleza del disolvente, el pH de la disolución, la temperatura y la presencia de sustancias interferentes. Los efectos de estas variables deben conocerse; y deben elegirse las condiciones para el análisis de manera que la absorbancia no se vea prácticamente afectada por las pequeñas e incontroladas variaciones en sus magnitudes[65,66]. 1.6.4 Desviaciones de la Ley Lambert-Beer La ley de Lambert-Beer predice que la densidad óptica es directamente proporcional a la concentración de las especies absorbentes. Las desviaciones pueden tener distintos orígenes, bien sea de tipo instrumental o las asociadas a las propiedades intrínsecas de la muestra: Dispersión de luz: Las muestras biológicas, frecuentemente turbias debido a macromoléculas u otros grandes agregados los cuales dispersan la luz. La densidad óptica resultante de la dispersión será proporcional a (dispersión Rayleigh), y puede ser fácilmente reconocida como una absorción de fondo, la cual se incrementa rápidamente a medida que la longitud de onda disminuye[67]. Fluorescencia: Si la densidad óptica de la muestra es elevada, y si la especie absorbente es fluorescente, esto puede producir una saturación del detector[67]. 45 Agregación: Si las especies absorbentes son parcialmente solubles puede ocurrir agregación de estas especies al incrementar la concentración. Los espectros de absorción de los agregados difieren de los espectros de los monómeros. Generalmente, es apreciable por un cambio de color en la solución[67]. Todas las desviaciones descritas con anterioridad corresponden a propiedades intrínsecas de las muestras. Aquellas asociadas a problemas instrumentales, como longitud de onda y densidad óptica elevada, se pueden corregir fácilmente a partir de los parámetros de los cuales dependen la absorbancia[67]. 1.6.5 Espectroscopía de absorción aplicado al estudio de asfaltenos Los métodos ópticos espectrales son usados como prueba directa de componentes aromáticos en crudos y asfaltenos. La relación que existe entre las dimensiones del anillo aromático y la longitud de onda de absorción facilita el análisis. Moléculas de gran tamaño presentes en asfaltenos y crudos, las cuales son difíciles de analizar por otros métodos, producen absorciones electrónicas a longitudes de onda largas, donde otras moléculas no producen absorción[67] (Figura 1.63). Figura 1.63. Representación esquemática de la distribución de población de cromóforos en crudo y asfaltenos en el espectro electromagnético[67]. 46 La absorción electrónica en crudos y asfaltenos exhibe, de forma sistemática, características como los anchos rangos espectrales, al igual que en sistemas como semiconductores. En crudos livianos se ha encontrado una disminución apreciable de cromóforos, indicando la presencia de grandes anillos aromáticos y, para asfaltenos, anillos aromáticos de menor tamaño, aún cuando las dimensiones exactas dependen del crudo[67]. Generalmente, los resultados experimentales están descritos por teorías que explican los fenómenos experimentales; a inicios de los noventa Mullins llevó a cabo un estudio sistemático de crudos y asfaltenos. Para ello, aplicó un conjunto de técnicas espectroscópicas que le permitió estudiar la distribución de cromóforos y espectros de adsorción de crudos y asfaltenos. La amplitud de los espectros de adsorción de los crudos presentó un incremento en el perfil de intensidad de los mismos; esto se debe al solapamiento de bandas de absorción de moléculas individuales de muchos de los componentes presentes en el crudo. Así mismo, exhiben absorciones electrónicas continuas, localizadas a diferentes longitudes de onda del espectro electromagnético cuya magnitud de intensidad crece a longitudes de ondas cortas, esto refleja la presencia de componentes aromáticos en crudos. El autor llegó a la conclusión de que los crudos pesados, los cuales son más densos, presentan bandas de absorción en el IR cercano; los crudos livianos absorben preferiblemente en el visible, al igual que los asfaltenos[67]. Basanta (1999) estudió el rendimiento cuántico de las soluciones de asfaltenos en tolueno. Para tal fin, obtuvo los espectros de absorción para dos crudos: Hamaca y Cerro Negro, encontrando que la similitud en ambos espectros pareciera indicar la presencia de los mismos cromóforos. Este hecho lo corroboró al estudiar la variación de la absorbancia en función de la concentración (Curva de calibración), evidenciando la similitud en las pendientes; es decir, en el coeficiente de absortividad de las soluciones en estudio, resultado que le permite extrapolar y afirmar la similitud que existe en el comportamiento de ambos crudos[68]. Los espectros UV-Visible no sólo dan información acerca de la densidad de población de ciertas estructuras, las medidas de absorción también permiten construir isotermas de adsorción; pues nos permite monitorear la cantidad de material que se adsorbe sobre una determinada superficie. Adicionalmente, permite indagar sobre las posibles interacciones existentes entre las moléculas de asfaltenos[67]. 47 CAPÍTULO II SECCIÓN EXPERIMENTAL Para lograr los objetivos que se han fijado en este trabajo, fue necesario realizar una serie de experimentos a escala de laboratorio. En este capítulo se va a desarrollar la metodología que se ha seguido para la realización de esos experimentos. Así, se va a efectuar una descripción de los crudos, reactivos y equipos experimentales utilizados. 2.1 Crudos Los asfaltenos fueron obtenidos mediante el método SARA aplicado a los siguientes crudos (Tabla 2.1): Crudo San Jacinto: Proveniente del norte de Perú. Fue suministrado por el laboratorio de fisicoquímica de hidrocarburos de la Universidad Simón Bolívar. Crudo Boscán: Proveniente del Campo Boscán ubicado en el Municipio Urdaneta en la Costa Occidental del Lago de Maracaibo, Venezuela. Fue suministrado por el laboratorio de fisicoquímica de hidrocarburos de la Universidad Simón Bolívar. Crudo Hamaca: Proveniente del Campo Ayacucho ubicado en la Faja Petrolífera del Orinoco, Venezuela. Fue suministrado por el laboratorio de fisicoquímica de hidrocarburos de la Universidad Simón Bolívar. Tabla 2.1. Propiedades de los crudos empleados[69,70]. Propiedades Gravedad API a 60 °F Gravedad Específica a 60/60 °F Asfaltenos (% m/m) San Jacinto 12,6 0,98 14,4 Boscán 10,1 1,06 15,2 Hamaca 9,0 1,01 14,0 El hecho fundamental de escoger estas tres muestras de petróleo radica en la disponibilidad inmediata que había en el laboratorio antes citado. Además, esta selección sirve para evaluar la naturaleza de crudos de distintas procedencias. 48 2.2 Reactivos En la tabla 2.2 se muestran los reactivos usados y sus propiedades fisicoquímicas más relevantes. Tabla 2.2. Propiedades fisicoquímicas de los reactivos empleados[71]. Propiedades Reactivos a Masa Molecular (g/mol) 92,14 120,19 119,38 139,11 39,99 72,15 86,18 100,21 Tolueno Cumeno Cloroformo p-nitrofenol Hidróxido de sodio n-pentano n-hexano n-heptano Densidad (g/cm3) 0,87 0,86 1,48 1,27 2,10 0,63 0,66 0,68 Pto. De Ebullición (°C) 110,80 152,70 61,05 279,0 1390,0 35,95 68,85 98,42 Pto. De Fusión (°C) -95,02 -96,10 -63,65 113,0 323,0 -129,85 -95,15 -96,61 a Todos los reactivos fueron de grado analítico. Como adsorbentes se emplearon placas de capa fina de gel de sílice de dimensiones 2x1 cm. 2.3 Equipos Rotaevaporador: Se emplea para separar, mediante vaporización y recondensación, los componentes líquidos de una mezcla, aprovechando las diferentes en sus puntos de ebullición. Este equipo está constituido por: - Cubeta metálica con resistencia eléctrica. - Dos balones que contendrán la mezcla y el producto destilado, respectivamente. - Tubo refrigerante. - Panel, con los controladores del equipo. La mezcla se introduce en un matraz giratorio y, paulatinamente, es calentada en un baño de agua. Los vapores generados llegan a un refrigerante por succión al vacío o 49 presión, donde se condensan y regresan a su estado líquido, siendo recolectados en un balón de vidrio fijo. Extractor Soxhlet: Este equipo se aplica a analitos que no se pueden separar por volatilización, pero sí son extraíbles empleando un disolvente orgánico adecuado. El esquema del instrumento es sencillo: - Un balón de fondo redondo que contendrá el disolvente orgánico volátil. - Un contenedor intermedio de vidrio, en el cual se coloca la muestra dentro de un cartucho poroso al disolvente. - Tubo refrigerante. El balón de fondo redondo es calentado con una manta calefactora hasta que el disolvente orgánico se evapora. El vapor del disolvente asciende por el brazo lateral del contenedor, llegando al refrigerante donde se condensa y cae en forma líquida dentro del cuerpo del extractor que contiene el dedal con la muestra. Luego, el analito disuelto pasa por un sifón el cual, al llenarse y desbordar, se descarga sobre el balón. Baño ultrasónico termostatizado: Este equipo emplea ondas de ultrasonido en el agua, a través de una serie de transductores para la limpieza de materiales de vidrios, desgasificación de líquidos a determinadas concentraciones, aceleración de procesos de suspensión de células, disolución de muestras, entre otros usos. Está constituido por: - Cubeta interior de acero inoxidable. - Resistencia eléctrica en el interior de la cubeta. - Generador de ultrasonido. - Panel de mando frontal, con interruptor general de puesta en marcha y termostato regulador de temperatura con escala graduada en Grados Celsius. 50 Espectrofotómetro UV-Visible (UV-160, SHIMADZU): Su funcionamiento fue descrito en la sección 1.6.3. Los componentes de este equipo de haz sencillo son: - Lámpara de Deuterio-Halógeno. - Porta muestras Cuvette-All. - Sistema óptico de lentes, elemento dispersor y espejos. - Celdas de vidrio de 0,2 cm. - Fotomultiplicador. 2.4 Metodología experimental Se llevaron a cabo tres procedimientos, los cuales son nombrados en orden estricto de realización: Precipitación y obtención de asfaltenos, fraccionamiento con p-nitrofenol y medición de las isotermas de adsorción. 2.4.1 Precipitación y obtención de asfaltenos La norma de la American Society Tensting Materials (ASTM), recomendada para la precipitación de asfaltenos a partir de crudos (ASTM-D6560)[72], es un procedimiento estándar ampliamente reconocido. Dicha norma específica añadir un volumen de n-parafina que es 40 veces el volumen de una alícuota de crudo. La mayoría de los crudos contienen entre 1-10 g de asfaltenos por cada 100 g de crudo. En tal sentido, se tomaron 100 g de crudo y se transvasaron a una fiola de 6 L. Se añadió 4 L de n-parafina caliente (50°C), de tal forma que la relación disolvente/crudo fuese de 40:1. Se tapó el frasco y se agitó la mezcla vigorosamente por 4 horas. El sistema resultante se dejó reposar durante un día. Posteriormente, se filtró por succión al vació para obtener los asfaltenos precipitados con un n-alcano. El proceso de filtración se repitió tres veces para de esta manera asegurar obtener la mayor cantidad posible. El precipitado se lavó con n-heptano (independientemente del n-alcano empleado en la precipitación) en un Extractor Soxhlet durante 5 días con la finalidad 51 de eliminar las resinas que co-precipitan con los asfaltenos. El solvente remanente en los asfaltenos se eliminó por evaporación en la estufa, donde se mantuvo a 30°C por 30 min. Luego, se trituraron en un mortero hasta reducirlos a un polvo fino y se envasaron en frascos pequeños de color ámbar (Figura 2.00). Los solventes usados en los procesos de precipitación y extracción son recuperados en un rotaevaporador bajo succión al vacío. Este procedimiento fue realizado para obtener los asfaltenos del crudo Boscán empleando como agentes precipitantes n-C5 y n-C7. Por otra parte, los asfaltenos del crudo Hamaca precipitados con n-C5, n-C6 y n-C7; y los asfaltenos del crudo San Jacinto precipitado con nC7 estaban disponibles en el laboratorio. En todos los casos fue necesario realizar la extracción Soxhlet para lavar los asfaltenos. Figura 2.00. Esquema representativo del proceso de precipitación de asfaltenos. 2.4.2 Fraccionamiento de asfaltenos con p-nitrofenol Para realizar el fraccionamiento de asfaltenos con p-nitrofenol se reprodujo el procedimiento experimental propuesto por Acevedo y colaboradores (2001)[34]. De tal forma, en un balón aforado de 100 ml se preparó una solución de 8 g/L de asfaltenos en cumeno saturada con PNF. Durante la preparación, parte de la solución se colocó en un baño 52 ultrasónico termostatizado a temperatura ambiente durante 10 minutos para promover una rápida disolución de las partículas de asfaltenos. La solución resultante se dejó reposar por 3 días. Posteriormente, se filtró por succión al vació el precipitado obtenido (A1-PNF). Este proceso se realizó tres veces con el fin de garantizar la total recuperación de esta fracción. Este sólido se disolvió en cloroformo y se realizaron extracciones sucesivas ácido-base con una solución acuosa de hidróxido de sodio al 5% en un embudo de decantación para eliminar el PNF presente. Se rotaevaporó el cloroformo y se obtuvo la fracción A1. Luego, se envasó en un frasco pequeño de color ámbar cerrado herméticamente. Por otra parte, se rotaevaporó la solución remanente que contiene al complejo de transferencia de carga (A2-PNF), para eliminar el cumeno. Finalmente, la fracción A2 se aisló empleando el mismo procedimiento seguido para la fracción A1 (Figura 2.10). Este procedimiento fue aplicado a los asfaltenos del crudo Hamaca (n-C5, n-C6 y n-C7) y a los asfaltenos del crudo Boscán (n-C5 y n-C7). Figura 2.10. Esquema representativo para el fraccionamiento de asfaltenos con PNF. 53 2.4.3 Determinación de las isotermas de adsorción de asfaltenos y su fracción A2 sobre gel de sílice Se prepararon soluciones de 25 mL de asfaltenos y su fracción A2 en tolueno en un intervalo de concentraciones comprendido entre 100-2000 mg/L. En la Figura 2.20 se indican las concentraciones de las soluciones de asfaltenos empleadas. Con una pipeta graduada, se tomaron por duplicado 7 mL de cada una de las soluciones preparadas y se colocaron en frascos pequeños color ámbar. Las soluciones remanentes se emplearon para la construcción de las curvas de calibración. Las soluciones contenidas en los viales se colocaron en contacto con placas de gel de sílice de dimensiones 2x1 cm durante intervalos de tiempo de 24, 48 y 72 horas. Los viales fueron tapados para evitar la natural evaporación del disolvente. Trascurrido el tiempo, las placas fueron extraídas y se dejaron secar durante 10 minutos a temperatura ambiente. Luego, se coloraron a desorber en otros viales que contenían 7 ml de tolueno durante el mismo tiempo empleado para la adsorción. Se midió la absorbancia de las distintas soluciones en un espectrofotómetro UV-Visible a 530 nm. Este procedimiento fue realizado para los asfaltenos del crudo Hamaca (n-C5, n-C6 y n-C7), los asfaltenos del crudo Boscán y sus correspondientes fracciones A2 (n-C5 y n-C7), y los asfaltenos del crudo San Jacinto (n-C7). Figura 2.20. Esquema del estudio de adsorción y desorción de los asfaltenos y su fracción A2. 54 2.4.3.1 Construcción analítica de las isotermas de adsorción El primer paso para la construcción de las isotermas de adsorción fue la obtención de las curvas de calibración. Para ello, se midió la absorbancia de las diluciones correspondientes a la solución patrón de asfaltenos, o bien, su fracción A2. Posteriormente, se graficó la absorbancia frente a la concentración de las muestras y se determinó la función matemática que correlaciona estas variables. De esta forma se obtuvo: Abs A m.C R b (21) Donde: m es la pendiente de la recta, b es la ordenada al origen y C R es la concentración de la muestra una vez finalizada la adsorción (Concentración remanente). Despejando C R en la ecuación (21): C R Abs A b m (22) La concentración inicial de las muestras, C I , viene dada por: C I C R C A (23) Donde: C A es la concentración de muestra adsorbida sobre la superficie de gel de sílice. Despejando C A en la ecuación (23): C A C I C R (24) C A mA (25) Así mismo, C A viene dado por: VS Donde: mA es la cantidad de muestra adsorbida (mg) y VS es el volumen de la solución donde ocurren los procesos de adsorción y desorción (0,007 L). 55 Despejando mA en la ecuación (25): mA C A .VS (26) Finalmente, se obtuvo la cantidad de soluto adsorbida por unidad de masa del adsorbente ( X A ): XA C A.Vs mA msílice msílice (27) Donde: msílice es la masa aproximada de una placa de gel de sílice 2x1 cm (0,018 g). La isoterma de adsorción se construyó al graficar el resultado de la ecuación (27) en función de la concentración remanente. 2.4.3.2 Determinación de la solubilidad aparente de los asfaltenos y su fracción A2 La solubilidad aparente ( S A ) de los asfaltenos y su fracción A2 en tolueno cuando la muestra está en contacto con la superficie de gel de sílice, se halló mediante la siguiente expresión[63]: SA C D .S C E o (28) Donde: S o es la solubilidad de los asfaltenos o su fracción A2 en tolueno a temperatura ambiente (aproximadamente 100 gr/L), C D es la concentración de muestra desorbida y C E es una concentración teórica obtenida de la isoterma de adsorción asumiendo que el proceso de desorción es completamente reversible[64]. La concentración de muestra desorbida se determinó de forma similar a C R empleando la curva de calibración. Entonces: C D Abs D b m (29) 56 La cantidad de muestra desorbida ( mD ) viene dada por: mD C D .VS (30) Ahora bien, la cantidad de muestra desorbida por unidad de masa del adsorbente ( X D ): XD C D .Vs mD msílice msílice (31) Por otro lado, la cantidad de muestra remanente adsorbida que quedaba en la placa luego del proceso de desorción ( mR ) se obtuvo de la siguiente forma: mR mA mD (32) Luego: XR mR m mD A msílice msílice (33) C E en la isoterma de adsorción Con la relación (33) se halló directamente (Figura 2.30). Figura 2.30. Modelo de la isoterma de adsorción construida[64]. 57 CAPÍTULO III RESULTADOS Y DISCUSIÓN A continuación, se presentan los resultados obtenidos con su respectiva discusión. En general, este capítulo se esquematiza siguiendo el orden estricto en que se realizaron los experimentos. Además, se adicionan detalles importantes que pudieron quedar implícitos en el capítulo anterior. 3.1 Proceso de precipitación de los asfaltenos del crudo Boscán empleando como agentes precipitantes n-C5 y n-C7 En la sección 1.4.1 se discutió el efecto de la naturaleza del disolvente en la precipitación de los asfaltenos. Las n-parafinas de bajo peso molecular inducen la precipitación de asfaltenos dispersos coloidalmente en la matriz del petróleo. Las resinas y otros compuestos aromáticos que funcionan como agentes peptizantes son parcial o totalmente disueltos en presencia de un exceso de n-parafinas. En la tabla 3.1 se muestran los porcentajes de asfaltenos precipitados con cada uno de los disolventes usados. Tabla 3.1. Porcentajes de los asfaltenos del crudo Boscán obtenidos con n-C5 y n-C7. Agente precipitante n-C5 n-C7 Volumen de n-alcano (V 1)ml 4000 4000 Masa de asfaltenos (m 0,0001)g 18,2923 9,0155 Asfaltenos (%)a 18 9 a Porcentaje de asfaltenos obtenidos en relación a la masa de crudo empleado (100,0 g) De acuerdo a los resultados, la cantidad de asfaltenos precipitados con n-C5 resultó ser el doble de la obtenida con n-C7. Por lo tanto, la cantidad de precipitado se incrementa cuando 58 disminuye el número de átomos de carbono de la n-parafina empleada, tal como es reportado en la literatura[11,73]. El proceso de desasfaltado siempre va acompañado de la coprecipitación de otras fracciones del crudo, debido al carácter polar de las fracciones pesadas y a su facilidad para formar puentes de hidrógeno[11,73]. Cabe señalar que los asfaltenos Boscán obtenidos con n-C7 eran de color negro, pero los asfaltenos obtenidos con n-C5, tenían una coloración tendiente hacia el marrón. Esta última característica se puede tomar como evidencia de la coprecipitación de otras fracciones del petróleo cuando se utilizan n-alcanos, siendo éste el hecho responsable de las diferencias en las cantidades de asfaltenos obtenidos. En resumen, la separación de la fracción asfalténica del petróleo depende del tipo y composición del agente precipitante. 3.2 Obtención de las fracciones A1 y A2 de los asfaltenos usando PNF Es ampliamente reconocido que los asfaltenos provenientes de diferentes crudos pueden tener propiedades muy distintas que hacen difícil establecer la estructura molecular de estos compuestos. Una forma expedita de facilitar la comprensión de sus propiedades químicas consiste en separarlos en varias fracciones. En tal sentido, se intentó realizar el fraccionamiento de asfaltenos con PNF. 3.2.1 Fraccionamiento de los asfaltenos extraídos del crudo Hamaca (n-C5, n-C6 y n-C7) De acuerdo al procedimiento estándar para el fraccionamiento de asfaltenos con PNF propuesto por Acevedo y colaboradores[34], es viable preparar la solución de asfaltenos usando como disolventes tolueno o cumeno. Debido a su mayor disponibilidad, se optó por realizarlo empleando tolueno. Se preparó la solución de asfaltenos del crudo Hamaca en tolueno saturada con PNF (8 g/L). La solución resultante se dejó reposar durante 3 días, al cabo de los cuales no se obtuvo la precipitación del complejo A1-PNF. 59 Por lo tanto, se realizaron una serie pasos para promover dicha precipitación: Se dejó la solución en reposo por más tiempo (1 semana aproximadamente). Se tomó una alícuota correspondiente a la mitad del volumen total de la solución de asfaltenos saturada con PNF y se colocó en reflujo durante 30 min. Se modificó la cantidad de PNF empleada. Se preparó una nueva solución de asfaltenos, pero esta vez usando cumeno como disolvente. En la Figura 3.00 se muestra un breve esquema sobre la metodología usada para el fraccionamiento de los asfaltenos del crudo Hamaca. Figura 3.00. Fraccionamiento de los asfaltenos del crudo Hamaca con PNF. Probablemente, el fallido fraccionamiento de los asfaltenos del crudo Hamaca pudo deberse a que estas moléculas sufrieron reacciones de oxidación progresiva que terminaron por modificar su estructura molecular, producto de que habían sido aislados hace mucho tiempo y no fueron conservados bajo atmósfera inerte. La reacción principal en el fraccionamiento de asfaltenos que conduce a la formación del precipitado involucra moléculas en fase coloidal. En consecuencia, la formación del complejo de transferencia de carga (A1-PNF) dependería de la capacidad del p-nitrofenol de penetrar la periferia del coloide, cuestión que difícilmente ocurrió en estos asfaltenos dadas las circunstancias antes señaladas. 60 Se ha demostrado que los asfaltenos pueden oxidarse por la actividad metabólica de ciertos microorganismos, produciendo estructuras con grupos ceto e hidroxilo. La biodegradación de asfaltenos es un proceso que ocurre de forma natural en el petróleo, pero en bajos porcentajes, ya que la capa peptizante de resinas actúa como inhibidor de la acción de estos agentes microbianos. Los hidrocarburos saturados son los más propensos a la oxidación y le siguen los hidrocarburos aromáticos. Es importante señalar que los microorganismos son capaces de utilizar los asfaltenos como fuente de carbono y energía, ya que estos compuestos contienen carbono, hidrógeno, azufre, nitrógeno, y oxígeno, que son los elementos necesarios para el desarrollo de cualquier organismo[6,74]. La oxidación observada como consumo de oxígeno en ausencia de microorganismos puede explicarse en función de la composición química de los asfaltenos, susceptibles de reaccionar con el oxígeno disuelto en el medio mineral. Así mismo, se ha determinado que los asfaltenos, una vez aislados de la matriz del crudo con n-alcanos, pueden ser oxidados a elevadas temperaturas, o bien, si son expuestos al O2 atmosférico durante largos periodos de tiempo a bajas temperaturas[75]. Quintero (2001) estudió la oxidación de asfaltenos provenientes del crudo Furrial en solución de diclorometano, usando ozono como agente oxidante y variando el tiempo de suministro de ozono, manteniendo constante la concentración de asfaltenos. Los productos obtenidos fueron sometidos a diversas técnicas: Análisis elemental, FT-IR, 1H-RMN y osmometría de presión de vapor. Los resultados obtenidos muestran que los asfaltenos son susceptibles a las reacciones con ozono, y que a partir de 7 minutos de reacción, se comienzan a observar los cambios, los cuales se incrementan a medida que se incrementa el tiempo de ozonólisis. Los espectros de FT-IR mostraron señales típicas de grupos carbonilos y de OH asociado. Por su parte, los espectros 1H-RMN mostraron una señal a 9,8 ppm, atribuible a protones aldehídicos[76]. 3.2.2 Fraccionamiento de los asfaltenos extraídos del crudo Boscán (n-C5 y n-C7) El fraccionamiento de asfaltenos del crudo Boscán (n-C5 y n-C7) se llevó a cabo empleando como disolvente cumeno y siguiendo el procedimiento descrito en la sección 2.4.2; sin mayores inconvenientes. En la tabla 3.2 se muestran los porcentajes obtenidos de las fracciones A1 y A2. 61 Tabla 3.2. Porcentajes de las fracciones A1 y A2 de los asfaltenos extraídos del crudo Boscán con n-C5 y n-C7. Agente precipitante n-C5 n-C7 Fracción A1 (%)a 61 58 Fracción A2 (%)a 39 42 a Porcentaje obtenido respecto a la cantidad inicial de asfaltenos. Las proporciones de las fracciones obtenidas resultaron ser similares a las reportadas en la literatura[34,77], siendo la fracción A1 mayoritaria con respecto a la fracción A2. En cuanto a la influencia del agente precipitante empleado para la obtención de los asfaltenos en el fraccionamiento con PNF, no se puede establecer una correlación directa puesto que las cantidades obtenidas resultaron ser muy similares. 3.3 Estudios de adsorción y desorción de asfaltenos sobre superficies de gel de sílice a diferentes tiempos de contacto A continuación se muestran las isotermas de adsorción de las muestras bajo estudio. Cabe destacar que cada punto graficado corresponde al promedio de dos mediciones relativas a cada una de las soluciones preparadas. 3.3.1 Isotermas de adsorción para asfaltenos del crudo Hamaca (n-C5, n-C6 y n-C7) sobre superficies de gel de sílice a 24, 48 y 72 h. XA (mg Muestra/g Sílice) XA vs. [C]R 100,00 90,00 80,00 70,00 60,00 50,00 40,00 30,00 20,00 10,00 0,00 0,00 (Hamaca n-C5) 24 h 48 h 72 h 500,00 1000,00 1500,00 2000,00 [C]R (mg/L) Figura 3.10. Isotermas de adsorción para asfaltenos Hamaca (n-C5) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h. 62 XA (mg Muestra/g Sílice) XA vs. [C]R 100,00 90,00 80,00 70,00 60,00 50,00 40,00 30,00 20,00 10,00 0,00 0,00 (Hamaca n-C6) 24 h 48 h 72 h 500,00 1000,00 1500,00 2000,00 [C]R (mg/L) Figura 3.11. Isotermas de adsorción para asfaltenos Hamaca (n-C6) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h. XA vs. [C]R (Hamaca n-C7) XA (mg Muestra/g Sílice) 100,00 90,00 80,00 70,00 60,00 24 h 48 h 50,00 40,00 72 h 30,00 20,00 10,00 0,00 0,00 500,00 1000,00 [C]R (mg/L) 1500,00 2000,00 Figura 3.12 Isotermas de adsorción para asfaltenos Hamaca (n-C7) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h. 63 En la tabla 3.3 se muestran las solubilidades aparentes de los asfaltenos extraídos del crudo Hamaca. Tabla 3.3. Valores de S A para los asfaltenos extraídos del crudo Hamaca (n-C5, n-C6 y n-C7). Agente Precipitante Hora (h) 24 48 72 24 48 72 24 48 72 n-C5 n-C6 n-C7 a Valor promedio de S A a s (g/L) 1,0 0,4 1,6 0,4 1,9 0,5 0,7 0,1 1,1 0,4 2,0 0,5 1,1 0,3 1,5 0,1 1,5 0,3 SA 3.3.2 Isotermas de adsorción para asfaltenos del crudo Boscán (n-C5 y n-C7) sobre superficies de gel de sílice a 24, 48 y 72 h XA (mg Muestra/g Sílice) XA vs. [C]R 100,00 90,00 80,00 70,00 60,00 50,00 40,00 30,00 20,00 10,00 0,00 0,00 (Boscán n-C5) 24 h 48 h 72 h 500,00 1000,00 1500,00 2000,00 [C]R (mg/L) Figura 3.13. Isotermas de adsorción para asfaltenos Boscán (n-C5) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h. 64 XA (mg Muestra/g Sílice) XA vs. [C]R 110,00 100,00 90,00 80,00 70,00 60,00 50,00 40,00 30,00 20,00 10,00 0,00 0,00 (Boscán n-C7) 24 h 48 h 72 h 500,00 1000,00 1500,00 2000,00 [C]R (mg/L) Figura 3.14. Isotermas de adsorción para asfaltenos Boscán (n-C7) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h. En la tabla 3.4 se muestran las solubilidades aparentes de los asfaltenos extraídos del crudo Boscán. Tabla 3.4. Valores de S A para los asfaltenos extraídos del crudo Boscán (n-C5 y n-C7). Agente Precipitante Hora (h) 24 48 72 24 48 72 n-C5 n-C7 a Valor promedio de S A a s (g/L) 1,3 0,4 1,3 0,3 1,6 0,5 1,1 0,5 1,1 0,3 1,6 0,3 SA 65 3.3.3 Isotermas de adsorción para la fracción A2 de los asfaltenos del crudo Boscán (n-C5 y n-C7) sobre superficies de gel de sílice a 24, 48 y 72 h. XA (mg Muestra/g Sílice) XA vs. [C]R 110,00 100,00 90,00 80,00 70,00 60,00 50,00 40,00 30,00 20,00 10,00 0,00 0,00 (A2 -Boscán n-C5) 24 h 48 h 72 h 500,00 1000,00 [C]R (mg/L) 1500,00 2000,00 Figura 3.15. Isotermas de adsorción para la fracción A2 de los asfaltenos Boscán (n-C5) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h. XA (mg Muestra/g Sílice) XA vs. [C]R 100,00 90,00 80,00 70,00 60,00 50,00 40,00 30,00 20,00 10,00 0,00 0,00 (A2 -Boscán n-C7) 24 h 48 h 72 h 500,00 1000,00 1500,00 2000,00 [C]R (mg/L) Figura 3.16. Isotermas de adsorción para la fracción A2 de los asfaltenos Boscán (n-C7) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h. 66 En la tabla 3.5 se muestran las solubilidades aparentes de las fracciones A2 de los asfaltenos del crudo Boscán. Tabla 3.5. Valores de S A para la fracción A2 de los asfaltenos extraídos del crudo Boscán (n-C5 y n-C7). Agente Precipitante Hora (h) 24 48 72 24 48 72 n-C5 n-C7 a Valor promedio de S A a s (g/L) 1,1 0,3 1,1 0,2 1,4 0,3 1,1 0,2 1,3 0,3 1,5 0,2 SA 3.3.4 Isotermas de adsorción para asfaltenos del crudo San Jacinto (n-C7) sobre superficies de gel de sílice a 24, 48 y 72 h XA vs. [C]R (San Jacinto n-C7) 160,00 XA (mg Muestra/g Sílice) 140,00 120,00 100,00 24 h 80,00 48 h 60,00 72 h 40,00 20,00 0,00 0,00 200,00 400,00 600,00 800,00 1000,00 1200,00 1400,00 [C]R (mg/L) Figura 3.17. Isotermas de adsorción para asfaltenos San Jacinto (n-C7) sobre gel de sílice a tiempos de contacto de 24, 48 y 72 h. 67 En la tabla 3.6 se muestran las solubilidades aparentes de los asfaltenos del crudo San Jacinto. Tabla 3.6. Valores de S A para los asfaltenos extraídos del crudo San Jacinto (n-C7). Agente Precipitante Hora (h) n-C7 24 48 72 a Valor promedio de S A a s (g/L) 1,1 0,4 1,5 0,3 1,6 0,3 SA Probablemente, el tiempo de contacto del sistema sea uno de los factores más relevantes en el proceso de adsorción. La mayoría de los fenómenos de adsorción requieren una cantidad de tiempo considerable para alcanzar el equilibrio. Por lo general, mientras mayor sea el tiempo de adsorción mayor será el porcentaje de adsorbato que es removido del seno de la solución, a menos que se alcance la condición de equilibrio, en la que las velocidades de adsorción y desorción se igualan. Por ejemplo, a una concentración de 2000 mg/L la cantidad de asfaltenos del crudo Hamaca (n-C5) adsorbidos por gramos de sílice fue de 40,38; 62,93 y 88,58 mg/g para tiempos de contacto de 24, 48 y 72 h, respectivamente. Es decir, que a dicha concentración inicial hubo un incremento gradual de la cantidad adsorbida aproximado de 23 mg/g en función del tiempo de contacto asfaltenos-sílice. Ahora bien, si para estos mismos asfaltenos consideramos una concentración inicial mucho menor (200 mg/L), la cantidad de asfaltenos adsorbidos también se incrementa con el tiempo, pero en menor magnitud. Obviamente, a bajas concentraciones hay menor cantidad de moléculas en solución, por lo tanto, la adsorción es menor en relación a elevadas concentraciones. Tendencias similares fueron encontradas para asfaltenos Boscán (n-C7) y para las fracciones asfalténicas A2 del crudo Boscán (n-C5 y n-C7). Sin embargo, resultaría ambiguo señalar que la tendencia general es el aumento ― gradual o proporcional‖ de la masa adsorbida en función del tiempo, puesto que en la mayoría de los sistemas tratados está situación no sucede exactamente. Para los asfaltenos Boscán (n-C5) la cantidad de adsorbato que se encuentra en la interfase tolueno-sílice luego de 48 h es ligeramente mayor a la obtenida a 24 h, mientras que a 72 h este incremento es más pronunciado. En el caso de los asfaltenos San Jacinto (n-C7), existe un rango de concentraciones (400-800 mg/L) en el que la cantidad adsorbida es similar a 48 y 72 h. 68 Entonces, el tiempo de contacto del sistema es un factor relevante en la adsorción de asfaltenos sobre superficies minerales, por cuanto alcanzar el equilibrio es un proceso lento que requiere más de 72 h. Por otra parte, no se puede establecer una correlación precisa en cuanto al incremento de la cantidad adsorbida con el tiempo, ya que existen otras variables que inciden de forma significativa en este proceso, entre las cuales se pueden mencionar: la composición química de los asfaltenos, la naturaleza del adsorbente y disolvente, y la temperatura. Otro aspecto importante a ser resaltado es la forma de las isotermas de adsorción obtenidas. Todas las curvas resultaron ser cóncavas respecto al eje de las abscisas, con presencia de escalones a concentraciones elevadas (formación de multicapas), por lo tanto, de acuerdo a la clasificación propuesta por Giles y colaboradores se tratan de isotermas tipo L-3. Este sistema cumple con las siguientes características: Las moléculas de adsorbato son muy similares y se adsorben en forma plana. Hay poca competencia por los sitios de adsorción entre los asfaltenos y el disolvente (tolueno). Los asfaltenos (adsorbato) y la superficie de sílice gel (adsorbente) son altamente polares. Los asfaltenos son moléculas planas con sistemas aromáticos condensados, los cuales pueden ser interconectados por cadenas alifáticas. Un conjunto de estas moléculas pueden ser aglutinadas por interacciones π-π, las cuales son importantes fuerzas intermoleculares no-covalentes, causados por el solapamiento de los orbitales π, o por puentes de hidrógeno. Diversos autores postulan que la formación de multicapas está relacionado a las interacciones asfaltenos-asfaltenos en tolueno, por lo que, la adsorción de agregados está vinculado a la formación de agregados en solución[78-80]. A fin de estudiar las posibles interacciones soluto-soluto, muchos autores han realizado experimentos de adsorción de asfaltenos y resinas sobre material orgánico e inorgánico, midiendo la concentración en equilibrio de la solución después de la adsorción y calculando la cantidad de asfaltenos que se adsorben sobre la superficie. Los autores construyeron isotermas de adsorción observando de forma general, que a bajas concentraciones los asfaltenos se adsorben mostrando un comportamiento tipo Langmuir; pasada esta concentración los 69 asfaltenos se adsorben formando multicapas[67]. Así mismo, se han reportado isotermas de adsorción tipo H para tiempos de contacto grandes, las cuales son un caso particular de las isotermas tipo L[62]. Ranaudo (1997), usando la técnica de absorción molecular UV-Visible, construyó isotermas de adsorción para asfaltenos provenientes de distintos crudos venezolanos: Furrial, Hamaca y Cerro Negro. Las curvas obtenidas (Concentración de equilibrio en el sólido vs. Concentración de equilibrio de asfaltenos en solución) le permitieron concluir de forma general para los asfaltenos estudiados la existencia de tres regiones: una primera región (C < 500 mg/L) correspondiente a alta dilución donde predominan especies monoméricas; el comportamiento tipo Langmuir le permite reafirmar tal evidencia; una segunda región (500 < C < 2500 mg/L) donde la concentración relativa de monómeros es menor que la anterior, pero con una concentración significativa de agregados y, finalmente, una tercera región (C > 2500 mg/L) donde la concentración de monómeros es prácticamente nula[81]. De acuerdo a los resultados obtenidos, el intervalo de concentraciones para la formación y adsorción de agregados asfalténicos de gran tamaño varía de acuerdo al tipo de asfaltenos y el agente precipitante empleado. En todos los casos examinados, se observó un comportamiento tipo Langmuir a bajas concentraciones, por lo cual, la adsorción de pequeños agregados y moléculas individuales (monómeros) es viable hasta que la superficie de gel de sílice sea cubierta o saturada. En este sentido, se encontró que el valor de saturación; es decir, la cantidad de asfaltenos adsorbidos por gramos de sílice necesarios para formar una monocapa, se incrementa con el tiempo y varía en función de la composición química de los asfaltenos. El intervalo del valor de saturación estuvo comprendido entre 30-75 mg/g. En cuanto al proceso de desorción de asfaltenos, se evidenció que la cantidad desorbida por gramos de sílice se incrementa al aumentar la concentración inicial de la solución de asfaltenos, lo cual no resulta sorprendente, pues a elevadas concentraciones, se adsorben agregados asfalténicos de gran tamaño; es decir, hay un mayor número de moléculas adsorbidas que pueden ser removidas de la superficie de sílice. Así mismo, se notó que la cantidad desorbida se incrementaba muy poco después de 24 h en relación a la cantidad adsorbida para el mismo tiempo de contacto. Para fines ilustrativos, este hecho se muestra en la tabla 3.7 para dos asfaltenos distintos. 70 Tabla 3.7. Valores de X A y X D para los asfaltenos Hamaca (n-C6) y San Jacinto (n-C7). Asfaltenos Hamaca n-C6 Tiempo de Contacto (h) 24 48 72 24 San Jacinto n-C7 48 72 C I (mg/L) 100 1500 100 1500 100 1500 100 1500 100 1500 100 1500 XA (mg/g) 20,50 51,78 24,73 58,33 24,10 62,98 16,41 83,13 18,96 127,60 26,86 148,02 XD (mg/g) 0,51 4,31 0,79 8,02 0,85 8,41 0,19 4,13 0,24 5,10 0,25 5,54 Al comparar las magnitudes de X D y X A , se puede observar que el proceso de desorción ocurre de forma menos eficiente que el proceso de adsorción, llegando a un punto en el cual resulta difícil la remoción de las moléculas de asfaltenos de la superficie del adsorbente. Las concentraciones experimentales medidas después del proceso de desorción ( C D ) son mucho menores a las concentraciones teóricas obtenidas de las isotermas de adsorción ( C E ) En consecuencia, el proceso de adsorción de asfaltenos es prácticamente irreversible. Estudios cinéticos de segundo orden corroboran la no reversibilidad de dicho proceso[62]. En las tablas 3.3-3.6 se muestran los resultados del análisis de solubilidad de las distintas muestras. Como fue explicado anteriormente, los valores de S A representan estimados de la solubilidad de los asfaltenos y su fracción A2 en tolueno cuando la muestra está en contacto con la superficie adsorbente. En todos los casos examinados, la solubilidad se redujo considerablemente. En resumen, las isotermas de adsorción reflejaron la formación de monocapas a concentraciones bajas (C < 700 mg/L) y multicapas a concentraciones elevadas. La formación de multicapas apuntaría hacia la generación y adsorción de agregados asfalténicos. Debido a que no se determinó la entalpía de adsorción, no se puede establecer el tipo de adsorción que se establece en la interfase tolueno-sílice. 71 3.3.5 Influencia del agente precipitante en el proceso de adsorción de asfaltenos sobre superficies de gel de sílice a tiempos de contacto de 24, 48 y 72 h Por lo general, los asfaltenos son obtenidos con n-parafinas de bajo peso molecular en proporciones variables, dependiendo del tamaño de la cadena carbonada. Esto podría indicar que el tipo de moléculas que conforman los asfaltenos varían según el solvente utilizado para su precipitación. En tal sentido, en está sección se busca establecer si el agente precipitante afecta de alguna forma el proceso de adsorción de asfaltenos sobre superficies sólidas. 3.3.5.1 Asfaltenos extraídos del crudo Hamaca (n-C5, n-C6 y n-C7) En la Figura 3.20 se muestran las isotermas de adsorción de los asfaltenos del crudo Hamaca (n-C5, n-C6 y n-C7) para diferentes tiempos de contacto. Figura 3.20. Superposición de las isotermas de adsorción para asfaltenos del crudo Hamaca obtenidos con diferentes agentes precipitantes. (a) 24 h, (b) 48 h, (c) 72 h. En los tres casos examinados, se percibe un comportamiento muy similar de las curvas a concentraciones bajas, por cuanto están casí superpuestas. Por consiguiente, en este intervalo de concentraciones (C < 500-900 mg/L), donde se presume que sólo existen especies monoméricas y pequeños agregados, la adsorción de asfaltenos es independiente de la naturaleza del agente precipitante. A concentraciones mayores, donde la presencia de agregados de gran tamaño es importante, las tendencias de las curvas son distintas. Durante 72 un tiempo de adsorción de 24 h, se observa que la cantidad adsorbida por gramos de sílice se incrementa considerablemente en función del agente precipitante. Específicamente, la cantidad de asfaltenos adsorbidos aumenta con el incremento del número de átomos de carbono de la n-parafina utilizada para precipitar los asfaltenos. Esta misma tendencia se evidencia tras 48 h de contacto, pero la magnitud del incremento en la adsorción es menor. A 72 h, hay mayor adsorción de los asfaltenos Hamaca n-C7, seguidos por los asfaltenos n-C5 y n-C6. 3.3.5.2 Asfaltenos extraídos del crudo Boscán (n-C5 y n-C7) En la Figura 3.21 se muestran las isotermas de adsorción de los asfaltenos del crudo Boscán (n-C5 y n-C7) para diferentes tiempos de contacto. Figura 3.21. Superposición de las isotermas de adsorción para asfaltenos del crudo Boscán obtenidos con diferentes agentes precipitantes. (a) 24 h, (b) 48 h, (c) 72 h. Al igual que la adsorción de los asfaltenos Hamaca, las isotermas son similares a concentraciones bajas. A concentraciones mayores, la cantidad adsorbida por gramos de sílice varía en relación al tiempo de contacto y al agente precipitante. A 24 h, la isoterma de los asfaltenos Boscán n-C5 se encuentra ligeramente por encima de la isoterma de los asfaltenos Boscán n-C7 en el intervalo de concentraciones comprendido entre 500-1600 mg/L. Al transcurrir el tiempo, esta situación cambia, de tal forma que la cantidad 73 adsorbida se incrementa con el aumento del tamaño de la cadena carbonada del agente precipitante. Al comparar los resultados obtenidos para los asfaltenos Hamaca y Boscán, se puede establecer que a elevadas concentraciones, la cantidad adsorbida por unidad de masa del adsorbente se incrementa en el siguiente orden: X A (n-C5) < X A (n-C6) < X A (n-C7) Probablemente, este patrón está relacionado con las propiedades químicas de los asfaltenos. Centeno (2004) afirma que no sólo la concentración de asfaltenos se ve afectada por el tipo de n-parafina utilizada en la precipitación, sino también sus propiedades químicas. Existe una significativa diferencia de los asfaltenos precipitados con n-C7 respecto a los precipitados con n-C5, la relación H/C de los primeros es más baja, lo que indica su alto grado de aromaticidad. Las relaciones N/C, O/C y S/C son usualmente más altas en los asfaltenos n-C7, lo cual le confiere una alta proporción de heteroátomos[3,82]. En la Figura 3.22 se muestran las principales características de los asfaltenos extraídos con diferentes n-parafinas y su relación con el peso molecular. Asfaltenos n-C5 Asfaltenos n-C7 Peso Molecular Polaridad y Aromaticidad Figura 3.22. Características de los asfaltenos extraídos con diferentes n-parafinas[3]. Entonces, los asfaltenos n-C7 son capaces de formar agregados de mayores dimensiones que los asfaltenos n-C6 y n-C5, debido a su alta aromaticidad que le confiere altas interacciones π-π. Por lo tanto, la cantidad adsorbida se incrementa en el orden antes descrito. 74 Así mismo, el alto contenido de heteroátomos permite una mayor interacción con la superficie polar de sílice, por cuanto se podrían generar numerosos enlaces de hidrógeno. 3.3.6 Comparación de las isotermas de adsorción de los asfaltenos Boscán y su fracción A2 (n-C5 y n-C7) sobre superficies de gel de sílice a tiempos de contacto de 24, 48 y 72 h. Al comparar las isotermas de adsorción obtenidas para los asfaltenos Boscán y su correspondiente fracción A2 (Figuras 3.30 y 3.31) se evidencia un comportamiento similar de dichas curvas a concentraciones bajas. Adicionalmente, se observa la formación de multicapas a concentraciones elevadas, las cuales se acentúan en función del tiempo de contacto. En principio, es de esperarse que las moléculas de A2 tengan menor tendencia a formar agregados intermoleculares en solución que los mismos asfaltenos, debido a su gran flexibilidad molecular[64]. Se presume que la formación de multicapas en el caso de las moléculas de A2 puede deberse a que éstas, al adsorberse sobre la superficie de sílice gel, generan nuevos sitios activos para la adsorción. En otras palabras, una vez formada la monocapa, las moléculas de A2 adheridas al adsorbente permiten que otras moléculas homólogas puedan ser adsorbidas, probablemente, originado por interacciones π-π o puentes de hidrógeno. Figura 3.30. Superposición de las isotermas de adsorción de los asfaltenos y su fracción A2 del crudo Boscán precipitados con n-C5. (a) 24 h, (b) 48 h, (c) 72 h. 75 Figura 3.31. Superposición de las isotermas de adsorción de los asfaltenos y su fracción A2 del crudo Boscán precipitados con n-C7. (a) 24 h, (b) 48 h, (c) 72 h. En cuanto a la solubilidad aparente de los asfaltenos Boscán y su fracción A 2 después del proceso de desorción (Tablas 3.4 y 3.5), se evidencia un cambio drástico de dicho parámetro. Por ejemplo, a 48 h de contacto la solubilidad de los asfaltenos Boscán (n-C5) se redujo 77 veces, en tanto que para su fracción A2 se redujo 91 veces. Por lo tanto, se sugiere que las variaciones en la solubilidad de ambas muestras pueden deberse al cambio conformacional de la fracción A2, de una estructura plegada en solución a una estructura desplegada después del proceso de adsorción. Es decir, luego de la adsorción del confórmero plegado, un lento proceso de desplegamiento es promovido por la superficie del adsorbente. Este cambio conformacional es producto de su alta flexibilidad, favoreciendo que el sistema llegue a su estado de menor energía, tal como es descrito por Acevedo y colaboradores a través de estudios de mecanismos moleculares[64]. 76 3.3.7 Influencia de la naturaleza de diferentes asfaltenos (n-C7) en el proceso de adsorción sobre superficies de gel de sílice a tiempo de contacto de 24, 48 y 72 h. En esta sección se pretende evaluar el comportamiento del proceso de adsorción de asfaltenos extraídos de crudos de distintas procedencias. En otras palabras, se busca establecer alguna correlación entre la composición química de los asfaltenos y su actividad interfacial. Las isotermas de adsorción de los distintos asfaltenos obtenidos con n-C7 son presentados en la Figura 3.40. Figura 3.40. Superposición de las isotermas de adsorción para asfaltenos de diferentes crudos precipitados con n-C7. (a) 24 h, (b) 48 h, (c) 72 h. Al comparar las curvas obtenidas, se observa la gran tendencia que tienen los asfaltenos San Jacinto (n-C7) de adsorberse sobre una superficie activa de sílice gel en relación a los asfaltenos Hamaca (n-C7) y Boscán (n-C7). Para estos asfaltenos en particular, la cantidad adsorbida por gramos de sílice se incrementa en el siguiente orden: X A (A. Boscán) < X A (A. Hamaca) < X A (A. San Jacinto) En el caso de los asfaltenos San Jacinto (n-C7), es evidente el comportamiento tipo Langmuir a concentraciones inferiores a 800 mg/L. Al término de dicha concentración, la cantidad de moléculas adsorbidas se incrementa abruptamente, probablemente, debido a la formación de multicapas. En contraste, para los asfaltenos Hamaca y Boscán (n-C7), el comportamiento tipo Langmuir se prolonga hasta concentraciones mayores (1400 mg/L). 77 Estas diferencias podrían ser explicadas en términos de la capacidad de estos asfaltenos de formar agregados en solución, lo cual está íntimamente vinculado a la estructura molecular de los mismos. Tal y como se mencionó con anterioridad, la espectrometría UV-Visible no puede proporcionar la identificación inequívoca de un compuesto en particular, sin embargo, es útil para detectar la presencia de ciertos grupos funcionales denominados cromóforos[65]. Para tal fin, se obtuvieron los espectros de adsorción UV-Visible de los asfaltenos diluídos en tolueno a una concentración de 1500 mg/L. El intervalo espectral estuvo comprendido entre 503-1000 nm (Figura 3.41). Abs. vs. λ 2,4 2 Asfaltenos San Jacinto (n-C7) Asfaltenos Hamaca (nC7) Asfaltenos Boscán (n-C7) Abs. 1,6 1,2 0,8 0,4 0 503 603 703 803 λ (nm) 903 1003 Figura 3.41. Espectros de absorción UV-Visible de diferentes asfaltenos obtenidos con n-C7. La gran similitud en los espectros de absorción obtenidos para los asfaltenos Hamaca y Boscán (n-C7), permite sugerir que la distribución de cromóforos es la misma, a diferencia de los asfaltenos San Jacinto (n-C7) cuyo espectro es relativamente distinto. Los máximos de adsorción observados corresponden a la región donde sistemas aromáticos de uno y dos anillos condensados absorben radiación. Esto evidencia la presencia de transiciones electrónicas de baja energía[67]. Los elevados valores de absorbancia de los asfaltenos San Jacinto (n-C7) en la región del IR cercano (800-2500 nm) reflejan la presencia de sistemas aromáticos condensados de mayores dimensiones respecto a los demás asfaltenos. Por ende, los asfaltenos San Jacinto (n-C7) podrían ser capaces de formar más eficientemente interacciones π-π; es decir, se generarían agregados asfalténicos de gran tamaño, lo cual incrementaría su actividad interfacial en medios porosos. 78 CONCLUSIONES Se corroboró que la cantidad de asfaltenos extraídos de la matriz del crudo se incrementa con la disminución del número de átomos de carbono de la n-parafina utilizada para su precipitación. El porcentaje de asfaltenos Boscán precipitados con n-C5 fue de 18 %, en tanto que para su homólogo precipitado con n-C7 fue de 9 %. El tiempo de almacenamiento de los asfaltenos afecta la viabilidad del fraccionamiento de estas moléculas con PNF, lo cual podría deberse a la oxidación de estas moléculas. El porcentaje de la fracción A1 de los asfaltenos Boscán obtenido fue aproximadamente de 60%, mientras que para la fracción A2 fue de 40%. Las isotermas de adsorción de los asfaltenos reflejaron la formación de multicapas, probablemente, debido a la generación de agregados asfalténicos en solución. Por otra parte, el tiempo de contacto resultó ser un factor fundamental en el proceso de adsorción, ya que al transcurrir el tiempo se incrementaba la cantidad de muestra adsorbida. El proceso de desorción ocurrió de forma menos eficiente que el proceso de adsorción, llegando a un punto en el cual resulta difícil la remoción de las moléculas de asfaltenos de la superficie del adsorbente. En consecuencia, el proceso de adsorción de asfaltenos resultó ser, prácticamente, irreversible. El tipo de agente precipitante no sólo afecta la cantidad de asfaltenos extraídos sino también su composición química, lo cual puede generar variaciones significativas en el proceso de adsorción. La cantidad de asfaltenos adsorbidos se incrementaba con el aumento del tamaño de la cadena carbonada de la n-parafina. La fracción A2 de los asfaltenos Boscán tiene una gran tendencia a formar multicapas. Probablemente, esto puede deberse a la generación de nuevos sitios activos, promovidos por estas mismas moléculas a través de interacciones de tipo Van der Waals o puentes de hidrógeno. 79 La disminución de la solubilidad de los asfaltenos y su fracción A2, se debe al cambio conformacional que sufren estas últimas moléculas, promovido por la superficie adsorbente. Por lo tanto, las moléculas de A2 adoptan una conformación plegada en solución, en tanto que luego del proceso de adsorción adoptan una conformación desplegada. Los asfaltenos San Jacinto (n-C7) tienden a adsorberse en mayor magnitud que los asfaltenos Hamaca y Boscán (n-C7), generado por su capacidad de formar agregados intermoleculares de grandes dimensiones. 80 RECOMENDACIONES Analizar las placas de gel de sílice, una vez que ha ocurrido la adsorción de los asfaltenos y su fracción A2 a través de microscopía electrónica, de manera de obtener mayor evidencia experimental acerca de la estructura que adoptan las distintas moléculas una vez que han sido adsorbidas. Realizar estudios de elipsometría para determinar el espesor de las películas formadas en la superficie del adsorbente con la finalidad de verificar la adsorción de agregados asfalténicos. Comparar la reproducibilidad de los resultados obtenidos empleando otra técnica analítica, como la deformación fototérmica superficial. Dicha técnica permite medir directamente la cantidad adsorbida y es capaz de analizar de un amplio rango de concentraciones (0-10000 mg/L) Aplicar la metodología empleada sobre otra fracción del petróleo con el fin de determinar los valores de S A y compararlos con los obtenidos para la fracción asfalténica. Estudiar los procesos de adsorción y desorción de asfaltenos y su correspondiente fracción A2 sobre superficies minerales en función de la temperatura. Analizar las muestras de asfaltenos empleadas mediante análisis elemental o IR con la finalidad de establecer diferencias en cuanto a sus propiedades fisicoquímicas, que permitan dar mayor evidencia en cuanto al proceso de agregación de los asfaltenos. 81 REFERENCIAS BIBLIOGRÁFICAS [1] Saban, M.; Vitorovic, O.; Vitorovic, D. Characterization of heavy crude oils and petroleum residues. Editorial Technip, Francia. pp. 32-41 (1984). [2] Badry, R.; Baker, A.; Brown, G.; Calvo, R.; Hughes, T. Oilfield Review. 2006, 18, 38-59. [3] Delgado, J. Asfaltenos: Composición, agregación y precipitación. Cuaderno FIRP, Universidad de los Andes, Venezuela. pp. 1-30 (2006). [4] Buckley, J.; Lord, D. Petrol. Sci. Eng. 2003, 39, 261. [5] Allenson, S.; Zhang, Dan.; Kabir, S. Oilfield Review. 2007, 19, 24-47. [6] Pineda, G.; Howard, A. Rev. Latin. Microb. 2001, 43, 143-150. [7] Narve, A. Characterization of crude oil components, asphaltene aggregation and emulsion stability by means of near infrared spectroscopy and multivariate. Department of Chemical Engineering, Norwegian University of Science and Technology. pp. 2-58 (2002). [8] López, F.; Carbognani, L.; Stull, C.; Pereira, P.; Spencer, R. Energy Fuels. 2009, 23, 1901-1908. [9] Selley, R. Elements of petroleum geology. Academic press, USA. (1998). [10] Gruse, W. Chemical technology of petroleum. McGraw-Hill, USA. (1960). [11] Speight, J. The chemistry and technology of petroleum. CRC press, USA. (2007). [12] Atkinson, G.; Zuckerman, J. Origin and Chemistry of Petroleum. Pergamon Press, USA. (1981). [13] Wauquier, J. El refino del petróleo. Editorial Technip, Francia. pp. 82 (1994). [14] Mullis, O.; Sheu, E.; Hammami, A.; Marshall, A. Asphaltenes, heavy oils and petroleomics. Springer, USA. pp 677 (2007). [15] Lesueur, D. Advances in Colloid and Interface Science. 2009, 145, 42–82. [16] Corbett, L. Anal Chem. 1969, 41, 576–9. [17] Wauquier, J. Crude oil petroleum products process flowsheets. Editorial Technip, Francia. (1995). [18] Constantinides, G.; Arich, G. Non hydrocarbon compounds in petroleum. Elsevier, Amsterdam. pp.109 (1967). [19] Whiele, I. Fluid Phase Equilibria. 1996, 17, 201-210. [20] Groenzin, H. Petroleum Science and Technology. 2001, 19, 219-230. [21] Alayon, M. Asfaltenos: Ocurrencia y floculación. Cuaderno FIRP, Universidad de los Andes, Venezuela. pp. 3-38 (2004). 82 [22] Speight, J.; Moschopedis, S. American Chemical Society. 1981, 195, 10-17. [23] Long, R. Advances in Chemistry Series. 1981, 195, 17. [24] Guilherme, B. Petroleum Science and Technology. 2001, 19, 34-43. [25] Groenzin, H.; Mullins, O. Energy Fuels. 2000, 14, 677-684. [26] Branco, V.; Mansoori, G.; De Almeida, X.; Park, S.; Manafi, H. Petroleum Science and Engineering. 2001, 32, 217. [27] Vansal, B. Petroleum Science and Technology. 2004, 22, 1401-1426. [28] Dickie, J.; Yen, T. Analytical Chemistry. 1967, 39, 1847-1852. [29] Strausz, P.; Ignasiak, T.; Kemp-Jones, V. J. Org. Chem. 1977, 42,312-320. [30] Acevedo, S.; Gutiérrez, B. Acta Cient. Ven. 1982, 33, 440. [31] Murgich, J.; Rodríguez, J.; Aray, Y. Energy & Fuels. 1996, 10, 68-76. [32] Strausz, P.; Faraji, F.; Louren, E. Energy & Fuels. 1999, 13, 207-227. [33] Acevedo, S.; Escobar, G.; Ranaudo, M.; Piñate, J.; Amorín, A. Energy & Fuels. 1997, 11, 774-778. [34] Gutiérrez, L.; Ranaudo, M.; Méndez B. y Acevedo, S. Energy & Fuels. 2001, 15, 624-628. [35] Acevedo, S.; Escobar, O.; Echeverria, L.; Gutiérrez, L.; Méndez; B. Energy & Fuels. 2004, 18, 305-311. [36] Ospino, T. Aspectos generales del daño de formación por depositación de asfaltenos en yacimientos de petróleo. Trabajo de grado, Universidad Nacional de Colombia. pp. 7-30 (2009). [37] Hirschberg, A., Jong, L., Schipper, B., Maijer, J. SPE J. 1984, 283-293. [38] Leontaritis, K., Mansoori, A. Asphaltene flocculation during oil production and processing: A thermodynamic colloidal model. SPE Int. Symp. Oilfield Chemisty. (1987). [39] Victorov, A.; Firoozabadi, A. AIChE Journal. 1996, 42, 1753. [40] Lian, H., Lin, R.; Yen, F. Fuel. 1994, 73, 423. [41] Victorov, A.; Smirnova, N. Fluid Phase Equilibria. 1999, 158, 471–480. [42] Acevedo, S. Sociedad Ven. Química. 2001, 24, 33 [43] Speight, J. G., Long, R. B., Trowbridge, T. Fuel. 1984, 63, 616-620. [44] Andersen, S.; Birdi, K. Fuel Sci. Tech. Int. 1990, 8, 593-615. [45] Ancheyta, J.; Centeno, G.; Trejo, F.; Marroquín, G.; García, J.; Tenorio, E.; Torres, A. Energy & Fuels. 2002, 16, 1121-1127. [46] Bilheimer, J.; Sage, H.; Lacey, N. Petrol. Trans. AIME. 1949, 290. [47] Lhioreau, C.: Briant, J.: Tindy, R. Rev. Inst. Fr. Pet. 1967, 22, 797. 83 [48] Feng, H.; Min, T. Fluid phase equilibria. 2001, 192, 13-25. [49] Andersen, S. Fuel Sci. Tech. Int. 1994, 12, 51-74. [50] Castellan, G. Fisicoquímica. Editorial Addison Wesley, México. pp. 455-457. (1987). [51] Atkins, P. Fisicoquímica. Editorial Oxford., España (2006). [52] Levine, I. Fisicoquímica. Editorial McGraw-Hill, España. (1999). [53] Masel, R. Principles of adsorption and reaction on solid surfaces. John Wiley Sons, Inc. pp. 108-113 (1996). [54] Giles, C.; Smith, D. J. Chem. Soc. 1960, 3976-3993. [55] Collis, S.; Melrose, J. Society of Petroleum Engineers. 1983, 249-256. [56] Acevedo, S.; Ranaudo, M.; Escobar, G.; Gutierrez, L.; Ortega, P. Energy & Fuels. 1995, 74, 595-598. [57] Kokal, T.; Tang, L.; Scharm, S. Colloid Surf. A: Physicochem. Eng. Aspects. 1995, 94 253. [58] Sócrates, A.; Castillo, J.; Fernándes, A.; Ranaudo, M. Energy & Fuels. 1998, 12, 386390. [59] Murgich, J.; Rodríguez, J. Energy & Fuels. 1998, 12, 339-343. [60] León, O.; Rogel, E.; Dambakli, G.; Acevedo, S.; Carbognani, L.; Espidel, J. Langmuir. 2002, 18, 5106-5112. [61] Marczewski, W.; Szymula, M. Colloids and Surfaces. 2002, 208, 259–266. [62] Acevedo, S.; Ranaudo, M.; García, C.; Castillo, J.; Fernández, A. Energy & Fuels. 2003, 17, 257-261. [63] Liao, Z.; Zhou, H.; Graciaa, A. Energy & Fuels. 2005, 19, 180-186. [64] Acevedo, S.; Castro, A.; Negrin, J.; Fernández, A.; Escobar, G.; Piscitelli, V. Energy & Fuels. 2007, 21, 2165-2175. [65] Skoog, D.; Holler, J.; Nieman, A. Principios de Análisis Instrumental. Editorial Mc Graw Hill, España. pp. 322-351 (2001). [66] Wade, L. Química Orgánica. Editorial Pearson Prentice Hall, España. pp. 666-669 (2004). [67] Goncalves, S. Estudio óptico de los procesos de agregación y adsorción de asfaltenos. Tesis de grado, Universidad Central de Venezuela. (2002). [68] Basanta, C. Medidas del rendimiento óptico cuántico de fluorescencia, en soluciones de asfaltenos provenientes de crudos venezolanos en solventes orgánicos. Tesis de grado, Universidad Central de Venezuela (1999). [69] Borges, B.; Del Carpio, E.; Navarro, U. Estudio morfológico de los asfaltenos mediante microscopía electrónica de barrido. Universidad Simón Bolívar. (2009). 84 [70] Carnahan, N. Energy & Fuels. 1999, 13, 309-314. [71] Fichas Internacionales de Seguridad (IPCS). http://training.itcilo.it/actrav_cdrom2/es/osh/kemi/alpha2.html.Consultado: 28/01/2010. [72] Norma ASTM-D6560. [73] Pillon, Z. Petroleum Science and Technology. 2001, 19, 673-68. [74] Thouand, G.; Bauda, P.; Oudot, J.; Kirsch, G.; Sutton, C.; Vidalie, J. Can. J. Microbiol. 1999, 45, 106-115. [75] Yarranton, H.; Beck, J.; Svrcek, Y. Energy & Fuels. 2002, 16, 462-469. [76] Quintero, E. Caracterización estructural de los productos de ozonólisis de asfaltenos extraídos del crudo Furrial. Tesis de grado, Universidad Central de Venezuela (2001). [77] Rodríguez, P. Estudio de la morfología de coloides de las fracciones A1 y A2 de los asfaltenos del crudo Hamaca. XIII Congreso Venezolano de Microscopía y Microanálisis. (2008) [78] Rogel, E. Langmuir. 2004, 20, 1003-1012. [79] Simón, S.; Jestin, J.; Palermo, T.; Barré, L. Energy & Fuels. 2009, 23, 306-313. [80] Corvis, Y.; Cousin, F.; Jestin, J.; Barré, L. Langmuir, 2009, 25, 3991-3998. [81] Ranaudo, M. Estudio de fenómenos interfaciales de asfaltenos y otras fracciones de petróleo. Tesis de grado, Universidad Central de Venezuela (1997). [82] Centeno, G.; Trejo, F.; Ancheyta, J. Rev. Soc. Quím. Méx. 2004, 48, 179-188. 85