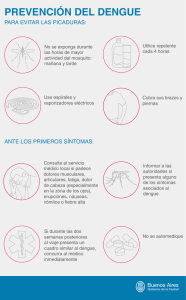
Proyecto de Control y Prevención de Enfermedades Metaxénicas
Anuncio

SERVICIO NACIONAL DE CONTROL DE ENFERMEDADES TRANSMITIDAS POR VECTORES ARTROPODOS “SNEM” PROYECTO DE VIGILANCIA Y CONTROL DE VECTORES PARA LA PREVENCION DE LA TRANSMISION DE ENFERMEDADES METAXENICAS EN EL ECUADOR. 2013-2017 Guayaquil, Marzo 2013 PROYECTO DE VIGILANCIA Y CONTROL DE VECTORES PARA LA PREVENCION DE LA TRANSMISION DE ENFERMEDADES METAXENICAS EN EL ECUADOR 1. DATOS GENERALES DEL PROYECTO 1.1 Nombre del Proyecto Vigilancia y Control de Vectores para la Prevención de la Transmisión de Enfermedades Metaxénicas en el Ecuador. CUP. 123200000.0000.374492 1.2 Unidad Ejecutora Servicio Nacional de Control de Enfermedades Transmitidas por Vectores Artrópodos (SNEM) “Dr. Juan Montalván Cornejo”. 1.3 Cobertura y Localización: La cobertura del proyecto se enmarca a la estructura organizacional del Estado que contempla nueve zonas territoriales, distribuidas de la siguiente manera: Zona I: Carchi, Esmeraldas Sucumbíos e Imbabura. Sede: Ibarra. Zona II: Pichincha, Orellana y Napo: Sede: Tena. Zona III: Pastaza, Cotopaxi, Tungurahua y Chimborazo. Sede: Riobamba. Zona IV: Santo Domingo de los Tsáchilas y Manabí. Sede: Portoviejo. Zona V: Los Ríos, Santa Elena, Bolívar, Guayas y Galápagos. Sede: Milagro. Zona VI: Morona Santiago, Cañar y Azuay. Sede: Cuenca. Zona VII: El Oro, Zamora y Loja. Sede: Loja. Zona VIII: Duran, Samborondón y el Distrito Metropolitano de Guayaquil. Sede: Guayaquil. Zona IX: Sangolquí y Distrito Metropolitano de Quito. Sede: Quito. Tabla 1: Zona I ZONA I: CARCHI,ESMERALDAS, SUCUMBÍOS E IMBABURA PROVINCIA CARCHI CANTONES PARROQUIAS MIRA (CHONTAHUASI) CONCEPCION MIRA JIJON Y CAAMAÑO JUAN MONTALVO ESMERALDAS CAMARONES CRNEL. CARLOS CONCHA TORRES CHINCA ESMERALDAS ESMERALDAS MAJUA SAN MATEO HABITANTES 5.994 2.807 2.071 1.308 Dengue Paludismo Chagas Leishmaniasis 161.868 2.817 2.354 4.552 2.534 5.739 TABIAZO 2.660 TACHINA 3.983 VUELTA LARGA 2.997 ELOY ALFARO VALDEZ (LIMONES) ENFERMEDADES METAXENICAS Dengue Paludismo Leishmaniasis Chagas Oncocercosis 6.226 1 ANCHAYACU ATAHUALPA BORBON LA TOLA LUIS VARGAS TORRES MALDONADO PAMPANAL DE BOLIVAR SAN FRANCISCO DE ONZOLE SANTO DOMINGO DE ONZOLE SELVA ALEGRE TELEMBI COLON ELOY DEL MARIA SAN JOSE DE CAYAPAS TIMBIRE MUISNE BOLIVAR DAULE GALERA MUISNE QUINGUE (OLMEDO PERDOMO SALIMA SAN FRANCISCO SAN GREGORIO SAN JOSE DE CHAMANGA ROSA ZARATE (QUININDE) CUBE QUININDE CHURA (CHANCAMA) MALIMPIA VICHE LA UNION SAN LORENZO ALTO TAMBO ANCON (PICHANGAL) CALDERON CARONDELET 5 DE JUNIO SAN LORENZO CONCEPCION MATAJE SAN JAVIER DE CACHAVI SANTA RITA TAMBILLO TULULBI URBINA ATACAMES LA UNION ATACAMES SUA TONCHIGUE TONSUPA RIOVERDE CHONTADURO RIOVERDE 4.733 17.772 5.292 19.924 25.096 1.871 1.814 628 1.730 416 2.354 1.475 664 1.639 1.743 2.295 761 16.855 2.540 3.449 8.001 10.681 4.964 3.222 CHUMUNDE 3.512 LAGARTO 5.674 MONTALVO 4.009 ROCAFUERTE SUCUMBIOS 2.537 1.454 7.696 4.366 352 1.861 1.118 1.430 1.934 1.166 5.639 1.410 1.513 1.037 8.880 1.039 2.153 1.733 574 1.117 2.809 5.915 4.254 67.259 7.590 LA CONCORDIA LA CONCORDIA NUEVA LOJA DURENO LAGO AGRIO GENERAL FARFAN EL ENO 5.488 42.924 57.727 2.756 6.769 6.636 Dengue Paludismo Leishmaniasis 2 IMBABURA PACAYACU JAMBELI STA. CECILIA LUMBAQUI EL REVENTADOR GONZALO PIZARRO GONZALO PIZARRO PUERTO LIBRE PUERTO EL CARMEN DEL PUTUMAYO PALMA ROJA PUTUMAYO PUERTO BOLIVAR PUERTO RODRIGUEZ SANTA ELENA SHUSHUFINDI LIMONCOCHA PAÑACOCHA SHUSHUFINDI SAN ROQUE SAN PEDRO DE LOS COFANES SIETE DE JULIO LA BONITA EL PLAYON DE SAN FRANCIS SUCUMBIOS LA SOFIA ROSA FLORIDA SANTA BARBARA EL DORADO DE CASCALES CASCALES SANTA ROSA DE SUCUMBIOS SEVILLA TARAPOA CUYABENO CUYABENO AGUAS NEGRAS ATUNTAQUI IMBAYA ANTONIO ANTE SAN FRANCISCO DE NATABUE SAN JOSE DE CHALTURA SAN ROQUE TOTAL DE HABITANTES 8.249 3.315 6.292 3.225 1.501 2.955 918 3.451 3.954 279 496 1.994 26.376 6.817 860 3.136 3.326 3.813 811 1.414 104 382 679 7.574 781 2.749 5.278 392 1.463 23299 1279 5651 3147 10142 766.262 Chagas Fiebre Amarilla Dengue Paludismo Chagas Leishmaniasis Fuente: Estadística INEC y SNEM Tabla 2: Zona II PROVINCIA PICHINCHA ORELLANA ZONA II: PICHINCHA, ORELLANA Y NAPO CANTONES PARROQUIAS SAN MIGUEL DE LOS BANCOS SAN MIGUEL DE LOS BANCOS MINDO PEDRO VICENTE PEDRO VICENTE MALDONADO MALDONADO PUERTO QUITO PUERTO QUITO PUERTO FRANCISCO DE ORELLANA DAYUMA TARACOA ALEJANDRO LABAKA EL DORADO EL EDEN ORELLANA GARCIA MORENO INES ARANGO LA BELLEZA NUEVO PARAISO SAN JOSE DE GUAYUSA SAN LUIS DE ARMENIA NUEVO ROCAFUERTE CAPITAN AUGUSTO RIBADENEYRA AGUARICO CONONACO SANTA MARIA DE HUIRIRIMA HABITANTES 13.731 3.842 12.924 20.445 45.163 6.298 2.616 1.237 1.639 900 1.091 3.038 4.133 2.717 1.951 2.012 1.024 701 519 729 ENFERMEDADES METAXENICAS Dengue Paludismo Leishmaniasis Chagas Dengue Paludismo Leishmaniasis Chagas Fiebre Amarilla 3 NAPO TIPUTINI YASUNI LA JOYA DE LOS SACHAS ENOKANQUI POMPEYA SAN CARLOS LA JOYA DE LOS SACHAS SAN SEBASTIAN DEL COCA LAGO SAN PEDRO RUMIPAMBA TRES DE NOVIEMBRE UNION MILAGREÑA LORETO AVILA PUERTO MURIALDO LORETO SAN JOSE DE PAYAMINO SAN JOSE DE DAHUANO SAN VICENTE DE HUATICOCHA TENA AHUANO CHONTAPUNTA TENA PANO PUERTO MISAHUALLI PUERTO NAPO TALAG ARCHIDONA ARCHIDONA COTUNDO SAN PABLO DE USHPAYACU CARLOS JULIO AROSEMENA CARLOS JULIO AROSEMENA TOLA TOTAL HABITANTES 1.597 277 17.934 2.362 1.204 2.846 3.353 1.861 1.993 3.138 2.900 4.227 4.331 3.375 3.125 5.047 1.058 33.934 5.579 6.687 1.392 5.127 5.393 2.768 11.689 8.376 4.904 3.664 Dengue Paludismo Leishmaniasis Chagas Fiebre Amarilla 276.851 Fuente: Estadística INEC y SNEM Tabla 3: Zona III PROVINCIA PASTAZA ZONA III: PASTAZA, COTOPAXI, TUNGURAHUA Y CHIMBORAZO CANTONES PARROQUIAS PUYO CANELOS DIEZ DE AGOSTO FATIMA MONTALVO (ANDOAS) POMONA RIO CORRIENTES PASTAZA RIO TIGRE SARAYACU SIMON BOLIVAR TARQUI TENIENTE HUGO ORTIZ VERACRUZ (INDILLAMA) EL TRIUNFO MERA MERA MADRE TIERRA SHELL SANTA CLARA SANTA CLARA SAN JOSE ARAJUNO ARAJUNO CURARAY HABITANTES 36.659 2.173 1.144 863 3.849 237 235 656 2.556 5.682 3.831 1.048 1.758 1.325 1.521 1.588 8.752 2.830 735 3.806 2.685 CHIMBORAZO CUMANDA CUMANDA 12.922 COTOPAXI LA MANA LA MANA 36.254 ENFERMEDADES METAXENICAS Dengue Paludismo Leishmaniasis Chagas Fiebre Amarilla Dengue Paludismo Leishmaniasis Chagas Dengue 4 PANGUA PUJILI GUASAGANDA PUCAYACU EL CORAZON MORASPUNGO PINLLOPATA RAMON CAMPAÑA PUJILI ANGAMARCA GUANGAJE LA VICTORIA PILALO TINGO ZUMBAHUA TOTAL DE HABITANTES 3.908 2.054 6.565 12.376 1.030 1.994 33.430 5.249 8.026 3.016 2.640 4.051 12.643 230.091 Paludismo Leishmaniasis Chagas Fuente: Estadística INEC y SNEM Tabla 4: Zona IV PROVINCIA SANTO DOMINGO MANABI ZONA IV: SANTO DOMINGO DE LOS TSACHILAS Y MANABÍ CANTONES PARROQUIAS SANTO DOMINGO DE LOS COLORADOS ALLURIQUIN PUERTO LIMON SANTO DOMINGO LUZ DE AMERICA SAN JACINTO DEL BUA DE LOS TSACHILAS VALLE HERMOSO EL ESFUERZO SANTA MARIA DEL TOACHI PORTOVIEJO ABDON CALDERON ALHAJUELA (BAJO GRANDE) CRUCITA PORTOVIEJO PUEBLO NUEVO RIOCHICO (RIO CHICO) SAN PLACIDO CHIRIJOS CALCETA BOLIVAR MEMBRILLO QUIROGA CHONE BOYACA CANUTO CONVENTO CHONE CHIBUNGA ELOY ALFARO RICAURTE SAN ANTONIO EL CARMEN EL CARMEN WILFRIDO LOOR MOREIRA SAN PEDRO DE SUMA FLAVIO ALFARO FLAVIO ALFARO SAN FRANCISCO DE NOVILLO ZAPALLO JIPIJAPA AMERICA JIPIJAPA EL ANEGADO JULCUY LA UNION HABITANTES 305.632 9.725 9.344 10.881 11.718 9.335 5.763 5.615 223.086 14.164 3.754 14.050 3.169 11.757 7.687 2.362 33.415 3.553 3.767 74.906 4.501 10.355 6.578 6.360 7.832 7.920 8.039 77.743 4.586 6.692 18.536 2.779 3.689 49.076 3.060 6.864 2.175 1.941 ENFERMEDADES METAXENICAS Dengue Paludismo Leishmaniasis Chagas Dengue Paludismo Leishmaniasis Chagas 5 MEMBRILLAL PEDRO PABLO GOMEZ PUERTO DE CAYO JUNIN JUNIN MANTA MANTA SAN LORENZO SANTA MARIANITA MONTECRISTI MONTECRISTI LA PILA PAJAN CAMPOZANO PAJAN CASCOL GUALE LASCANO PICHINCHA PICHINCHA BARRAGANETE SAN SEBASTIAN ROCAFUERTE ROCAFUERTE SANTA ANA DE VUELTA LARGA AYACUCHO SANTA ANA HONORATO VASQUEZ LA UNION SAN PABLO BAHIA DE CARAQUEZ SUCRE CHARAPOTO SAN ISIDRO TOSAGUA TOSAGUA BACHILLERO ANGEL PEDRO GILER SUCRE BELLAVISTA 24 DE MAYO NOBOA ARQ. SIXTO DURAN BALLEN PEDERNALES COJIMIES PEDERNALES 10 DE AGOSTO ATAHUALPA OLMEDO OLMEDO PUERTO LOPEZ PUERTO LOPEZ MACHALILLA SALANGO JAMA JAMA JARAMIJO JARAMIJO SAN VICENTE SAN VICENTE CANOA TOTAL DE HABITANTES 1.005 3.564 3.398 18.942 221.122 2.647 2.708 67.842 2.452 12.266 8.507 7.192 3.931 5.177 17.416 7.567 5.261 33.469 22.298 7.423 5.886 6.466 5.312 26.112 20.060 10.987 28.174 3.885 6.282 13.426 4.920 6.548 3.952 33.640 13.708 5.212 2.568 9.844 10.928 4.989 4.534 23.253 18.486 15.138 6.887 1.737.793 Fuente: Estadística INEC y SNEM Tabla 5: Zona V PROVINCIA LOS RIOS ZONA V: LOS RIOS, SANTA ELENA, BOLIVAR, GUAYAS Y GALAPAGOS CANTONES PARROQUIAS BABAHOYO CARACOL BABAHOYO FEBRES CORDERO (LAS JUNTAS) PIMOCHA LA UNION BABA BABA GUARE ISLA DE BEJUCAL HABITANTES 96.956 5.112 17.985 21.026 12.697 18.843 11.447 9.391 ENFERMEDADES METAXENICAS Dengue Paludismo Leishmaniasis Chagas 6 MONTALVO PUEBLOVIEJO QUEVEDO URDANETA VENTANAS VINCES PALENQUE BUENA FE VALENCIA MOCACHE QUINSALOMA SANTA ELENA SANTA ELENA LIBERTAD SALINAS CHILLANES SAN JOSE DE CHIMBO ECHEANDIA BOLIVAR SAN MIGUEL CALUMA LAS NAVES ALFREDO MORENO BALAO BALZAR COLIMES GUAYAS DAULE EL EMPALME BAQUERIZO MONTALVO PUEBLOVIEJO PUERTO PECHICHE SAN JUAN QUEVEDO SAN CARLOS LA ESPERANZA CATARAMA RICAURTE VENTANAS ZAPOTAL VINCES ANTONIO SOTOMAYOR PALENQUE SAN JACINTO DE BUENA FE PATRICIA PILAR VALENCIA MOCACHE QUINSALOMA SANTA ELENA ATAHUALPA COLONCHE CHANDUY MANGLARALTO SIMÓN BOLIVAR SAN JOSE DE ANCON LA LIBERTAD SALINAS ANCONCITO JOSE LUIS TAMAYO CHILLANES SAN JOSE DEL TAMBO SAN JOSE DE CHIMBO ASUNCION (ASANCOTO) MAGDALENA (CHAPACOTO) SAN SEBASTIAN TELIMBELA ECHEANDIA SAN MIGUEL BALSAPAMBA BILOVAN REGULO DE MORA SAN PABLO SANTIAGO SAN VICENTE CALUMA LAS NAVES 24.164 13.376 4.674 18.427 158.694 10.028 4.853 8.591 20.672 45.651 20.900 55.443 16.293 22.320 50.870 12.278 42.556 38.392 16.476 53.174 3.532 31.322 16.363 29.512 3.296 6.877 95.942 34.789 11.822 22.064 1.700 1.437 403 860 909 281 1.000 1.500 1.433 786 902 363 1.659 584 341 2.246 1.596 ALFREDO BAQUERIZO MORENO 25.179 BALAO BALZAR COLIMES SAN JACINTO DAULE JUAN BAUTISTA AGUIRRE LAUREL LIMONAL LOS LOJAS VELASCO IBARRA 20.523 53.937 17.307 6.116 87.508 5.502 9.882 8.774 8.660 47.667 Dengue Paludismo Leishmaniasis Chagas Dengue Paludismo Leishmaniasis Chagas Dengue Paludismo Leishmaniasis Chagas 7 EL TRIUNFO MILAGRO NARANJAL NARANJITO PALESTINA PEDRO CARBO SANTA LUCIA URBINA JADO YAGUACHI PLAYAS SIMON BOLIVAR CORONEL MARCELINO MARIDUEÑA LOMAS DE SARGENTILLO NOBOL GENERAL ANTONIO ELIZALDE ISIDRO AYORA SAN CRISTOBAL GALAPAGOS ISABELA SANTA CRUZ GUAYAS (PUEBLO NUEVO) EL ROSARIO EL TRIUNFO MILAGRO CHOBO MARISCAL SUCRE (HUAQUES) ROBERTO ASTUDILLO NARANJAL JESUS MARIA SAN CARLOS SANTA ROSA DE FLANDES TAURA NARANJITO PALESTINA PEDRO CARBO VALLE DE LA VIRGEN SABANILLA SANTA LUCIA EL SALITRE (LAS RAMAS) GENERAL VERNAZA LA VICTORIA (ÑAUZA) JUNQUILLAL YAGUACHI NUEVO GRAL. PEDRO J. MONTERO YAGUACHI VIEJO (CONE) VIRGEN DE FATIMA GENERAL VILLAMIL SIMON BOLIVAR CRNEL.LORENZO DE GARAICOA 17.579 9.205 44.778 145.025 5.421 5.365 10.823 39.839 6.427 6.516 5.444 10.786 37.186 16.065 31.317 5.230 6.889 38.923 28.117 9.511 6.470 13.304 26.617 8.195 11.957 14.189 41.935 14.585 10.898 CORONEL MARCELINO MARIDUEÑA 12.033 LOMAS DE SARGENTILLO NARCISA DE JESUS 18.413 19.600 GENERAL ANTONIO ELIZALDE 10.642 ISIDRO AYORA PUERTO BAQUERIZO MORENO EL PROGRESO ISLA SANTA MARIA (FLOREANA) PUERTO VILLAMIL TOMAS DE BERLANGA PUERTO AYORA BELLAVISTA SANTA ROSA TOTAL DE HABITANTES 10.870 6.672 658 145 2.092 164 11.974 2.425 994 2.121.141 Dengue Fuente: Estadística INEC y SNEM Tabla 6: Zona VI ZONA VI: MORONA SANTIAGO, CAÑAR Y AZUAY PROVINCIA MORONA SANTIAGO CANTONES MORONA PARROQUIAS MACAS ALSHI GENERAL PROAÑO SAN ISIDRO SEVILLA DON BOSCO SINAI ZUÑA (ZUÑAC) CUCHAENTZA HABITANTES 19.176 425 2.590 785 13.413 766 223 1.785 ENFERMEDADES METAXENICAS Dengue Paludismo Leishmaniasis Chagas Fiebre Amarilla 8 GUALAQUIZA LIMON INDANZA PALORA SANTIAGO SUCUA HUAMBOYA SAN JUAN BOSCO TAISHA LOGROÑO PABLO VI TIWINTZA CAÑAR LA TRONCAL RIO BLANCO GUALAQUIZA AMAZONAS (ROSARIO DE CUYES) BERMEJOS BOMBOIZA CHIGUINDA EL ROSARIO NUEVA TARQUI SAN MIGUEL DE CUYES EL IDEAL GENERAL LEONIDAS PLAZA G. INDANZA SAN ANTONIO SAN MIGUEL DE CONCHAY SANTA SUSANA DE CHIVIAZA YUNGANZA PALORA (METZERA) ARAPICOS CUMANDA SANGAY 16 DE AGOSTO SANTIAGO DE MENDEZ COPAL CHUPIANZA PATUCA SAN LUIS DE EL ACHO TAYUZA SAN FRANCISCO DE CHINIMB SUCUA ASUNCION HUAMBI SANTA MARIANITA DE JESUS HUAMBOYA CHIGUAZA SAN JUAN BOSCO PAN DE AZUCAR SAN CARLOS DE LIMON SAN JACINTO DE WAKAMBEIS SANTIAGO DE PANANZA TAISHA HUASAGA MACUMA TUTINENTZA PUMPUENTSA LOGROÑO YAUPI SHIMPIS PABLO VI TIWINTZA SAN JOSE DE MORONA LA TRONCAL MANUEL J. CALLE PANCHO NEGRO 1.992 9.228 412 223 4.623 552 608 511 184 821 3.981 1.363 2.157 405 772 1.044 3.947 482 345 1.172 990 3.008 480 467 2.133 618 1.510 1.079 12.619 1.903 2.891 905 2.538 5.928 2.177 265 793 204 469 5.949 1.509 3.885 4.641 2.453 2.053 1.777 1.893 1.823 4.721 2.274 42.610 2.765 9.014 Dengue Paludismo 9 Leishmaniasis Chagas SANTA ISABEL ABDON CALDERON AZUAY ZHAGLLI CAMILO PONCE ENRIQUEZ CAMILO PONCE ENRIQUEZ EL CARMEN DE PIJILI TOTAL DE HABITANTES SANTA ISABEL 11.607 4.631 2.155 17.404 4.594 242.720 Dengue Paludismo Leishmaniasis Chagas Fuente: Estadística INEC y SNEM Tabla 7: Zona VII PROVINCIA EL ORO ZONA VII: EL ORO, ZAMORA CHINCHIPE Y LOJA CANTONES PARROQUIAS MACHALA MACHALA EL RETIRO ARENILLAS CHACRAS ARENILLAS PALMALES CARCABON PACCHA AYAPAMBA CORDONCILLO ATAHUALPA MILAGRO SAN JOSE CERRO AZUL BALSAS BALSAS BELLAMARIA CHILLA CHILLA EL GUABO BARBONES (SUCRE) EL GUABO LA IBERIA TENDALES RIO BONITO HUAQUILLAS HUAQUILLAS MARCABELI MARCABELI EL INGENIO PASAJE BUENAVISTA CASACAY PASAJE LA PEAÑA PROGRESO UZHCURRUMI CAÑA QUEMADA PIÑAS CAPIRO LA BOCANA PIÑAS MOROMORO PIEDRAS SAN ROQUE SARACAY PORTOVELO CURTINCAPA PORTOVELO MORALES SALATI SANTA ROSA BELLAVISTA SANTA ROSA JAMBELI LA AVANZADA SAN ANTONIO HABITANTES 241.606 4.366 21.326 1.538 3.244 736 2.311 1.387 1.003 472 365 295 5.630 1.231 2.484 29.980 5.707 3.709 5.137 5.476 48.285 5.198 252 53.485 6.541 2.457 3.601 3.967 916 1.839 17.401 1.870 1.365 1.371 569 867 2.545 9.996 510 667 1.027 52.863 2.835 1.718 2.068 2.090 ENFERMEDADES METAXENICAS Dengue Paludismo Leishmaniasis Chagas 10 ZARUMA LAS LAJAS ZAMORA CHINCHIPE NANGARITZA ZAMORA YACUAMBI YANTZAZA EL PANGUI CENTINELA CONDOR PALANDA PAQUISHA LOJA LOJA DEL TORATA VICTORIA BELLAMARIA ZARUMA ABAÑIN ARCAPAMBA GUANAZAN GUIZHAGUIÑA HUERTAS MALVAS MULUNCAY GRANDE SINSAO SALVIAS LA VICTORIA LA LIBERTAD EL PARAISO SAN ISIDRO ZAMORA CUMBARATZA GUADALUPE IMBANA SABANILLA TIMBARA SAN CARLOS DE LAS MINAS ZUMBA CHITO EL CHORRO LA CHONTA PUCAPAMBA SAN ANDRES GUAYZIMI ZURMI NUEVO PARAISO 28 DE MAYO LA PAZ TUTUPALI YANZATZA CHICAÑA LOS ENCUENTROS EL PANGUI EL GUISMI PACHICUTZA TUNDAYME 1.953 3.187 2.322 10.559 1.684 995 3.045 1.704 1.996 1.185 845 1.336 748 2.632 802 761 599 13.387 4.416 2.857 1.126 584 960 2.180 6.878 1.230 216 261 118 416 2.598 2.004 594 3.153 2.043 639 12.356 2.661 3.658 4.988 1.604 1.290 737 ZUMBI 6.479 PALANDA EL PORVENIR DEL CARMEN SAN FRANCISCO DE VERGEL VALLADOLID LA CANELA PAQUISHA BELLAVISTA NUEVO QUITO CHANTACO CHUQUIRIBAMBA EL CISNE GUALEL JIMBILLA MALACATOS (VALLADOLID) 3.701 1.484 1.318 1.231 355 1.452 301 2.101 670 1.405 927 1.174 634 4.054 Dengue Paludismo Leishmaniasis Chagas Fiebre Amarilla Dengue Paludismo Leishmaniasis Chagas Fiebre 11 CALVAS CATAMAYO CELICA CHAGUARPAMBA ESPINDOLA GONZANAMA MACARA PALTAS PUYANGO SARAGURO SOZORANGA ZAPOTILLO PINDAL SAN LUCAS SAN PEDRO DE VILCABAMBA SANTIAGO TAQUIL (MIGUEL RIOFRIO) VILCABAMBA (VICTORIA) YANGANA (ARSENIO CASTILLO) QUINARA EL LUCERO EL TAMBO GUAYQUICHUMA SAN PEDRO DE LA BENDITA ZAMBI TNTE. MAXIMILIANO RODRIG CHAGUARPAMBA BUENAVISTA EL ROSARIO SANTA RUFINA AMARILLOS AMALUZA BELLAVISTA JIMBURA SANTA TERESITA 27 DE ABRIL EL INGENIO EL AIRO GONZANAMA CHANGAIMINA (LA LIBERTAD NAMBACOLA PURUNUMA (EGUIGUREN) SACAPALCA LARAMA LA VICTORIA SABIANGO (LA CAPILLA) CATACOCHA CANGONAMA GUACHANAMA LAURO GUERRERO ORIANGA SAN ANTONIO CASANGA YAMANA ALAMOR CIANO EL ARENAL EL LIMO (MARIANA DE JESUS) MERCADILLO VICENTINO SARAGURO SOZORANGA NUEVA FATIMA TACAMOROS ZAPOTILLO CAZADEROS GARZAREAL LIMONES PALETILLAS BOLASPAMBA PINDAL CHAQUINAL 2.663 734 782 2.087 2.723 865 788 1.154 2.639 218 906 330 326 2.040 691 282 689 377 1.959 1.330 1.320 1.000 1.189 1.066 568 1.436 1.568 2.576 245 1.235 615 887 371 1.255 724 1.483 1.040 1.004 621 1.028 708 4.729 813 559 1.351 669 722 5.156 2.144 514 1.597 2.411 668 1.015 1.024 1.499 619 3.229 620 12 12 DE DICIEMBRE QUILANGA FUNDOCHAMBA SAN ANTONIO DE LAS ARADAS OLMEDO LA TINGUE QUILANGA OLMEDO TOTAL DE HABITANTES 1.077 1.550 201 719 2.350 380 782.035 Fuente: Estadística INEC y SNEM Tabla 8: Zona VIII ZONA VIII: DURAN, SAMBORONDÓN Y D.M. DE GUAYAQUIL CANTONES GUAYAQUIL DURAN SAMBORONDON PARROQUIAS HABITANTES GUAYAQUIL JUAN GOMEZ RENDON (PROGR MORRO POSORJA PUNA TENGUEL ELOY ALFARO (DURAN) SAMBORONDON TARIFA 2.291.158 11.897 5.019 24.136 6.769 11.936 235.769 51.634 15.956 2.654.274 TOTAL DE HABITANTES ENFERMEDADES METAXENICAS Dengue Paludismo Leishmaniasis Chagas Fuente: Estadística INEC y SNEM Tabla 9: Población Nacional ZONAS ZONA I: CARCHI,ESMERALDAS, SUCUMBÍOS E IMBABURA ZONA II: PICHINCHA, ORELLANA Y NAPO ZONA III: PASTAZA, COTOPAXI, TUNGURAHUA Y CHIMBORAZO ZONA IV: SANTO DOMINGO DE LOS TSACHILAS Y MANABÍ ZONA V: LOS RIOS, SANTA ELENA, BOLIVAR, GUAYAS Y GALAPAGOS ZONA VI: MORONA SANTIAGO, CAÑAR Y AZUAY ZONA VII: EL ORO, ZAMORA CHINCHIPE Y LOJA ZONA VIII: DURAN, SAMBORONDÓN Y D.M. DE GUAYAQUIL TOTAL HABITANTES HABITANTES 766.262 276.851 230.091 1.737.793 2.121.141 242.720 782.035 2.654.274 8.811.167 Fuente: Estadística INEC y SNEM 1.4 Monto El monto total requerido para el Proyecto es de $98´774.113 dólares americanos, con recursos fiscales. Tabla 10: Presupuesto 2013-2017 Años 2013 2014 2015 2016 2017 TOTAL Monto $12´074.883 $18´079.353 $21´621.646 $22´861.234 $24´136.998 $98.774.113 1.5 Plazo de Ejecución El Plazo de ejecución es del 2013-2017, 60 meses (5 años). 13 1.6 Sector y Tipo de Proyecto Ministerio de Salud Pública (SNEM)-Proyecto de Apoyo Social. N° 2 2. SECTOR SALUD SUBSECTORES/ TIPOS DE INTERVENCIÓN 2.6 Otros DIAGNÓSTICO Y PROBLEMA 2.1 Descripción de la Situación Actual del Área de Intervención del Proyecto. La República del Ecuador se encuentra ubicada en el sur oeste de América, bordeada por el Océano Pacífico, limitando al norte con Colombia y por el sur y el oriente con el Perú. Su superficie territorial es de 256.370 kilómetros cuadrados. Su población se estima en 14´448.499 habitantes según el último Censo 2010 realizado por el INEC, correspondiendo el 50,4% a mujeres y 49.6% a hombres según Censo de población y vivienda 2010. La mayoría de la población, el 62,8%, vive en zonas urbanas; la densidad poblacional es de 55,8 habitantes por km2, considerada la más alta de América del Sur. La distribución de la población no es homogénea y se encuentra concentrada en los polos de desarrollo de las principales provincias: Guayas 25 % y Pichincha 18 %, y en especial en las ciudades de Quito y Guayaquil1. La tasa de crecimiento es de 1.47%, con una natalidad de 203 nacimientos por cada 1.000 h. y de mortalidad de 5 por cada 1.000 h. La expectativa general de vida al nacer es de 75 años, misma que llega a 78 años en las mujeres y 72 años para los hombres. Los grupos étnicos son: mestizos 71,9%, indígenas 7%, blancos 6,1%, afroecuatoriano 7,2% montubios 7,4% y otros 0,4%. El 95% practica la religión católica y el 5% otras religiones o ninguna. Los idiomas oficiales son el español, el kichwa y el shuar. Cerca de un millón de ecuatorianos son analfabetos, según el VII Censo de Población y VI de Vivienda 2010 determinando que el 6,8% de personas de entre 15 y más años no sabe leer ni escribir. Ese porcentaje representa a 984.878 habitantes de los 14’483.499 con los que cuenta el país.1 Figura 1: Distribución Analfabetismo en el Ecuador Fuente: Censo de Población y Vivienda 2010 –INEC. Elaboración: Diario El Universo 1 Instituto Nacional de Estadísticas y Censos INEC – SISTEMA INTEGRADO DE INDICADORES SOCIALES DEL ECUADOR versión 2010. 14 La población económicamente activa del Ecuador según el Censo del 2010 es de: sector terciaros (servicios) 46,1%; sector primario (agricultura y ganadería) 21,8% y sector secundario (industria) 16,8%. Este proyecto está enfocado al sector pobre del país, siendo la pobreza el principal síntoma del subdesarrollo. Para medir el avance o retroceso de la pobreza se lo mide a través de necesidades básicas insatisfechas (NBI), el cual tiene como objetivo principal, identificar qué hogares no logran satisfacer un conjunto de necesidades consideradas básicas, utilizando la información censal disponible. 2 Según la encuesta condiciones de vida del año 2010, en el país 60,1% de las personas viven en condiciones de pobreza NBI y un 26.8 % vive en extrema pobreza. Figura 2: Pobreza por Necesidades Básicas Insatisfechas (NBI) en el Ecuador - 2010 Fuente: Censo de Población y Vivienda Elaboración: Ministerio Coordinador de Desarrollo Social-SIISE La pobreza nacional en 2010 disminuyó en 3,3 puntos porcentuales respecto al 2009 y con respecto al 2006 la reducción fue de 4,8 puntos porcentuales. La pobreza nacional urbana se redujo entre septiembre de 2009 y septiembre de 2011 en 7,4 puntos porcentuales. La extrema pobreza a nivel nacional en el 2010 se redujo en 2,3 puntos porcentuales con respecto al 2009 y con respecto al 2006 la reducción fue de 3,8 puntos. Debemos considerar a las enfermedades de transmisión vectorial como patologías emergentes y re-emergentes que históricamente han presentado un comportamiento endémico – epidémico y siguen constituyendo un problema de salud pública en el Ecuador por ser la mayoría potencialmente letales; sin embargo, gracias a las actividades realizadas por el MSP – SNEM se han mantenido fuera de la lista de las principales causas de mortalidad y morbilidad en el país, como se puede apreciar en las figuras 3 y 4. 2 Fuente: INEC, Metodología pobreza NBI-2010 15 Figura 3: Principales Causas de Mortalidad General Año 2010 Actualizar datos Figura 4: Diez N° Orden Gráfico N° 6 Diez Principales Causas de Morbilidad Principales CausasAño de2011 Morbilidad Lista Internacional Detallada - CIE-10 Número de Egresos Causas % Tasa ** 34.778,00 3,07% 22,78 2° J18 Neumonía, Organis mo no Es pecificado A09 Diarrea y Gas troenteritis de Pres unto Origen Infeccios o 32.106,00 2,83% 21,03 3° K80 Colelitias is 31.183,00 2,75% 20,43 4° K35 Apendicitis Aguda 27.946,00 2,47% 18,31 5° O06 Aborto no Es pecificado 23.356,00 2,06% 15,30 6° O47 Fals o Trabajo de Parto 14.551,00 1,28% 9,53 7° K40 Hernia Inguinal 14.475,00 1,28% 9,48 8° O34 Atención Materna por Anormalidades Conocidas o Pres untas de los Órganos Pelvianos de la Madre 12.193,00 1,08% 7,99 9° S06 Traumatis mo Intracraneal 11.814,00 1,04% 7,74 10° N39 Otros Tras tornos del Sis tema Urinario 11.537,00 1,02% 7,56 O80 Parto Único Es pontaneo 120.148,00 10,60% O82 Parto Único por Ces área 70.492,00 6,22% 980,00 0,09% 1° O81, O83,O84 Otros Partos Signos y Hallazgos Anormales Clínicos y de Laboratorio, NCOP (CAP. XVIII) Las Demás Caus as de Morbilidad Total de Egresos Hospitalarios Población Es timada Año 2011 1/ 33.588,00 2,96% 694.409,00 61,26% 1.133.556,00 100,00% Año 2011 Tasa de Morbilidad a Nivel Nacional 22,78 21,03 20,43 18,31 15,30 9,53 1° 2° 3° 4° 5° 6° 9,48 7° 7,99 7,74 7,56 8° 9° 10° Causas Principales 15.266.431,00 a) 1/ Ecuador: Estimaciones y Proyecciones de Población 2010 - 2020. INEC ** Tasas por 10.000 habitantes Fuente: Anuario de estadísticas hospitalarias: camas y egresos - INEC 2011 El Censo del 2010 indica que un 12.5% de las viviendas del país tienen características físicas inadecuadas utilizando variables en relación a material predomínate en: techo, paredes exteriores Figura 5: Características de los Hogares en el Ecuador y piso: Fuente: Censo de Población y Vivienda 2010 –INEC. 16 Existen viviendas sin servicios de: agua potable por red pública (72%), alcantarillado (53,6%), energía eléctrica (93,2%), servicio telefónico (33,4%), recolección basura por carro recolector (77%). Figura 6: Cobertura de servicios básicos de la vivienda Fuente: Censo de Población y Vivienda 2010 –INEC. A pesar del mejoramiento evidente de las condiciones de vida y vivienda en los últimos años en nuestro país, aún se mantienen factores que influyen en la ocurrencia de las enfermedades transmitidas por vectores en áreas urbano –marginales y rurales del país ya que persisten las condiciones bio - ecológicas para la vida y desarrollo de artrópodos de importancia médica en aproximadamente el 70% de la extensión territorial del país. En la siguiente tabla se indica el número de casos registrados por el MSP en relación a las enfermedades transmitidas por vectores en el Ecuador durante el período 2002 a 2012. Tabla 11: Número de casos registrados por el MSP en relación a las enfermedades transmitidas por vectores en el Ecuador 2002 a 2012 CASOS ECUADOR MALARIA DENGUE NO GRAVE DENGUE GRAVE CHAGAS LEISHMANIASIS ONCOCERCOSIS FUEBRE AMARILLA 2002 88.038 13.596 111 12 1.253 0 0 2003 51.345 7.306 23 25 1.336 0 0 2004 28.730 6.522 64 22 2.494 0 0 2005 17.050 14.455 334 11 1.925 0 0 2006 9.863 6.810 179 20 1.536 0 0 2007 8.464 10.253 334 37 1.185 0 0 2008 4.986 2.840 31 62 1.479 0 0 2009 4.126 6.213 31 99 1.735 0 0 2010 1.888 17.823 307 167 1.629 0 2011 2012 1.232 558 7.659 17.116 307 294 110 76 1.403 935 0 0 0 2 Fuente: SIVE Alerta y Dpto. Estadística SNEM Elaborado: Ing. Cinthia Mosquera Zúñiga 2.2 Identificación, descripción y diagnóstico del problema MALARIA/PALUDISMO La malaria o paludismo es una enfermedad causada por un parásito del género Plasmodium. Existen más de 150 especies de Plasmodium que infectan diferentes vertebrados, pero solamente cuatro (P. Falciparum, P. Vivax, P. ovale y P. malariae) infectan al hombre. Las dos especies más comunes son: o P. falciparum - que tiene una distribución global y es la especie más agresiva, que puede causar la muerte sino es tratado a tiempo el paciente. 17 o P. vivax - de igual distribución que la especie anterior que produce infecciones debilitantes y recurrentes, raramente es causa de mortalidad. El paludismo es una enfermedad febril aguda. Los síntomas aparecen a los 7 días o más (generalmente entre los 10 y los 15 días) de la picadura del mosquito infectado. Puede resultar difícil reconocer el origen palúdico de los primeros síntomas (fiebre, dolor de cabeza, escalofríos, sudoración y vómitos). Si no se trata en las primeras 24 horas, el paludismo por P. falciparum puede agravarse, llevando a menudo a la muerte. Los niños de zonas endémicas con enfermedad grave suelen manifestar una o más de las siguientes presentaciones sindrómicas: anemia grave, sufrimiento respiratorio relacionado con la acidosis metabólica o paludismo cerebral. En el adulto también es frecuente la afectación multiorgánica. En las zonas donde el paludismo es endémico, las personas pueden adquirir una inmunidad parcial, lo que posibilita la aparición de infecciones asintomáticas. Perfil Epidemiológico de la Malaria Desde el año 2003 se observa un decrecimiento muy significativo de la incidencia de malaria en el Ecuador, en aquel año (2003)se reportaron 51.345 casos de paludismo, de los cuales 10,656 corresponde a P. falciparum y 40,689 a P. vivax de un total de 432.033 láminas examinadas lo que determinó los siguientes indicadores malariométricos IPA: 6,7; ILP: 11.9; FRIF: 20.8 y el IAES: 5.7 comparados con el año 2012 en el cual se reportaron 558 casos de los cuales 80 corresponden a P. falciparum y 478 a P. vivax de un total de 446. 509 láminas examinadas reportando los siguientes indicadores IPA: 0.07; ILP: 0.12; FRIF: 14,34 y el IAES: 6 (Tabla No. 12). Tabla 12: Comparación de número de casos con indicadores malariométricos Período 2003-2012 AÑOS POBLACIÓN MALARICA MUESTRAS HEMATICAS IAES* 2003 2004 2005 2006 2007 2008 2009 2010 2011 2012 7.619.834 7.619.834 7.544.719 7,603,438 7,794,946 7,794,946 7,794,946 7,821,223 7,821,223 7,821,223 432.033 349.539 349.308 318.307 352,426 384,800 446,74 481,251 460,6 446,509 5.7 4.6 4.6 4.2 4.5 4.9 5.7 6.2 6 6 TOTAL DE CASOS 51.345 28.730 17.050 9.863 8,194 4,891 4,126 1,888 1,232 558 IPA** X MIL HAB. 6.7 3.8 2.3 1.3 1.1 0.6 0.5 0.2 0.16 0.07 ILP*** 11.9 8.2 4.9 3.1 2.4 1.3 0.9 0.4 0.27 0.12 INFECCIONES FALCIPARUM NUMERO % 10,656 20.8 5,891 20.5 2,212 13.0 1,596 16.2 1,158 13.7 396 8.1 551 13.4 258 13.7 296 23.88 80 14.34 VIVAX 40,689 22,839 14,838 8,267 7,306 4,495 3,575 1,63 936 478 Fuente: Estadística del SNEM IAES* = Índice Anual de Exploración Sanguínea (Organización Panamericana de la Salud (OPS) recomienda que un buen muestreo hemático de pacientes febriles sospechosos de Malaria es entre 6% y 8% de la población de las zonas de transmisión). IPA** Índice parasitario anual (Número de casos confirmados con diagnostico microscópico de Malaria / población en riesgo X 1.000) ILP*** Índice de láminas positivas (Número de láminas positivas / Número de láminas examinadas x 100). En base a estos datos podemos indicar que existe una reducción 99% de la morbilidad palúdica desde el año 2003 comparativamente con el año 2012, como se muestra en la gráfica a continuación: 18 Figura 7: Número de casos de Malaria Periodo 2003-2012 Fuente: Estadística del SNEM Mecanismo de Transmisión El paludismo se transmite principalmente por la picadura de mosquitos del género Anopheles. La intensidad de la transmisión depende de factores relacionados con el parásito, el vector, el huésped humano y el medio ambiente. En el mundo hay unas 20 especies diferentes de Anopheles que tienen importancia local. Todas las especies importantes como vector pican por la noche. Estos mosquitos se crían en agua dulce de poca profundidad (charcos, campos de arroz o huellas de animales). La transmisión es más intensa en lugares donde los vectores tienen una vida relativamente larga que permite que el parásito tenga tiempo para completar su desarrollo en el interior del mosquito, y cuando el vector prefiere picar al ser humano antes que a otros animales. La transmisión también depende de condiciones climáticas que pueden modificar el número y la supervivencia de los mosquitos, como el régimen de lluvias, la temperatura y la humedad. En muchos lugares la transmisión es estacional, alcanzando su máxima intensidad durante la estación lluviosa e inmediatamente después. Se pueden producir epidemias de paludismo cuando el clima y otras condiciones favorecen súbitamente la transmisión en zonas donde la población tiene escasa o nula inmunidad, o cuando personas con escasa inmunidad se desplazan a zonas con transmisión intensa, como ocurre con los refugiados o los trabajadores migrantes. Al margen de la vía natural de transmisión existen otras posibilidades: a) Por medio de transfusión sanguínea de los parásitos. Es muy importante excluir a los donantes de riesgo. En este caso, y para individuos con P. falciparum, si no es detectado y tratado de manera definitiva no podrá ser donante durante un año, para P. vivax en al menos tres años. b) Por medio de accidentes de laboratorio y cirugía, jeringas no esterilizadas, etc. c) Paludismo congénito y neonatal: Es muy raro y la transmisión vertical a través de la placenta se puede diagnosticar cuando se detectan parásitos en el recién nacido 19 durante los siete primeros días de vida o posterior, siempre y cuando no haya posibilidad de nuevas picaduras infectivas para el niño. Factores de Riesgo El Anopheles, vector transmisor de la malaria, pertenece a la clase Insecta, orden Diptera, de la familia Culicidae, subfamilia Anophelinae, constituida por 3 géneros, aproximadamente 10 subgéneros y 532 especies en el mundo. Entre las especies más importantes que se hallan en el país, en la región costa predominan se encuentran An. albimanus, An. pseudopunctipennis, y en la región amazónica el An. Nuñeztovari y el An. trinkae. Como factores que influyen en la transmisión de la malaria, podemos citar: Contacto entre el mosquito y los humanos Existencia de una relación en tiempo y espacio, entre el mosquito y los casos locales de malaria Las glándulas salivales del mosquito contienen esporozoitos (estadio infectante para el humano). Dentro de los elementos de información entomológica para demostrar lo anterior incluye: Presencia y abundancia del mosquito anofeles. Especies existentes en cada área. Dispersión de las especies vectoras. El comportamiento de alimentación del vector: donde y cuando pica/ se alimenta un mosquito, la fuente de ingesta sanguínea y presencia de fuentes de azúcar. Índice de infección natural por especie. Edad y paridad de la población del mosquito. Hábitos de reposo (Endofilia o exofilia) Con lo anteriormente expuesto, se puede obtener el dato más importante sobre un insecto incriminado como vector que es la denominada capacidad vectorial. Los principales factores ambientales que afectan la transmisión de la malaria incluyen: Lluvia: En regiones tropicales y subtropicales las variaciones en la precipitación son responsables de la estacionalidad de la mayoría de especies de mosquitos. La lluvia propicia la presencia criaderos temporales que son críticos para el aumento de la densidad en la población de algunas especies vectores y por consiguiente favorece la transmisión. Temperatura y humedad: En las regiones templadas, la temperatura es el principal factor determinante que afecta la dinámica de población de anofelinos, este efecto parece es menos evidente en climas tropicales. Los mosquitos anofeles se vuelven inactivos a temperaturas bajas. El agua a temperatura más fría puede retardar el desarrollo y surgimiento de las larvas. 20 Sin embargo, la longevidad de los mosquitos disminuye significativamente a temperatura por arriba de los 35º y a humedad relativa por debajo del 50%. Altitud: Se conoce que la transmisión del paludismo tiende a caer a medida que aumenta la altura. Generalmente no se encuentra anofelinos por encima de los 2.000 metros. La temperatura disminuye un promedio de 6.5ºC por cada 1000 metros y esta disminución desacelera el desarrollo de los parásitos de la malaria dentro del mosquito afectado. Factores antropogénicos y demográficos: incluyen el tipo de construcción de la casa, actividades humanas que promueven la disponibilidad de criaderos, pobreza y comportamiento relacionado con el nivel de entendimiento de los riesgos de transmisión de malaria, así como las prácticas socio culturales. Análisis de Intervenciones Previas y Resultados Obtenidos Figura 8: Análisis de Intervenciones Previas y Resultados Obtenidos Malaria Entre las estrategias relacionadas con la reducción de la transmisión de la malaria en el Ecuador, se pueden indicar las siguientes: Mejoramiento de la oferta de diagnóstico microscópico, tanto de gota gruesa y pruebas de diagnóstico rápido (PDR). En el año 1998 existían 86 puestos de diagnósticos microscópico de Paludismo y en la actualidad existen 264, estratégicamente ubicados en zonas de riesgo y adicionalmente en aquellos de lugares de difícil acceso el diagnostico se realiza con pruebas rápidas (PDR) mismas que se distribuyen en un número aproximado de 200.000 anuales. Control de calidad en la gestión de diagnóstico microscópico de malaria: Se realiza supervisión y monitoreo de los puestos de diagnósticos y de los técnicos, de acuerdo a las normas de gestión de garantía en la calidad de diagnóstico. Disponibilidad de la gestión de medicamentos antimaláricos: Selección, adquisición, almacenamiento y distribución de medicamentos de acuerdo al Manual de Políticas Antimaláricas. Tratamiento integral, seguimiento y adherencia de los casos positivos. Control y seguimiento de pacientes considerados en riesgo como menores de 5 años, embarazadas y adultos mayores. Rociado residual selectivo, intradomiciliar y secuencial. 21 Dotación de mosquiteros impregnados con insecticida larga duración (MTILD) a la población de riesgo de transmisión de malaria. Evolución de Indicadores y metas de Malaria periodo 2007-2012 Durante la ejecución del Proyecto Control de Malaria-Paludismo del 2007-2012, basado en los componentes: Diagnóstico precoz y tratamiento oportuno de casos, Disminución de la población adulta del mosquito anofeles y Fortalecimiento de la vigilancia epidemiológica, se logró cumplir con los objetivos y metas programadas, observándose una notable disminución de la transmisión del Paludismo del Ecuador de 8.194 a 558 casos. Por estos logros el Ecuador ha sido considerado por varias ocasiones como Campeón en la LUCHA CONTRA LA MALARIA EN LAS AMERICAS en los años 2008 y 2011. Componentes 1: Diagnóstico precoz y tratamiento oportuno de casos 2: Disminución de la población adulta del mosquito anopheles 3: Fortalecimiento de la vigilancia epidemiológica Fuente: Tabla 13: Evolución de Indicadores y metas de Malaria periodo 2007-2012 Indicador Años 2007 2008 2009 2010 Meta 400.000 305.479 420.000 480.000 Muestras Resultado 352.426 384.800 439.181 481.251 examinadas 88,11% 125,97% 104,57% 100,26% Alcance % Casos 8.464 4.986 4.126 1.888 Casos diagnosticados diagnosticados y Casos tratados 8.464 4.986 4.126 1.888 tratados Alcance % 100% 100% 100% 100% Rociado de casas con insecticida de acción residual Dotación de mosquiteros impregnados con insecticida 2011 480.000 460.760 2012 490.000 459.803 95,99% 93,84% 1.232 592 1.232 100% 592 100% Meta 79.259 83.221 87.328 90.000 45.000 21.000 Resultado 66.578 309.750 145.991 43.914 27.688 21.384 Alcance % 84,00% 372,20% 167,18% 48,79% 61,53% 101,83% Meta 15.000 139.120 89.028 40.000 40.000 40.000 Resultado Alcance % 15.000 100,00% 139.120 100,00% 89.028 100,00% 40.000 100,00% 40.000 100,00% 47.345 118,36% Estadísticas del Proyecto Malaria Aunque en la actualidad solo 10 de 22 provincias con riesgo de transmisión de la Malaria reportan casos, es necesario indicar que todas ellas tienen condiciones sociales, ambientales, demográficas propicias para la ocurrencia de la enfermedad, por ende las medidas de prevención y control deben mantenerse de manera permanente con las estrategias anteriormente indicadas. Ver anexo 1 y 2. Persistencia en el Ecuador La persistencia de la malaria en el Ecuador está influenciada por los siguientes aspectos, que son de carácter no modificable y que se detallan a continuación: 1. La regiones naturales del territorio continental como Costa, Amazonía, Sierra con estribaciones y valles subtropicales andinos, presentan condiciones propicias para la existencia y reproducción del anofeles, entre ellas citamos: altitud menor a 2.000(msnm), temperatura ambiente (15 – 40ºC), humedad relativa (moderada a alta), 22 pluviosidad (moderada a alta), flora y fauna, presencia de fenómenos climatológicos ocasionales (ENOS) y el calentamiento global. 3 2. Las desigualdades sociales expresada en Indicadores socioeconómicos altos, tales como: pobreza, movimientos migratorios, asentamientos no planificados en sitios rurales/selváticos (colonización), deforestación acumulación de agua, poca o escasa cultura de prevención de enfermedades. 4 3. El agente infeccioso (plasmodium) que permanece en el humano, y en el portador asintomático, puede permanecer desde los pocos meses hasta los 5 años.5 DENGUE El dengue es una infección viral transmitida por la picadura de las hembras infectadas de mosquitos del género Aedes que después de un período de incubación de 4 a 10 días, puede presentar un amplio espectro de manifestaciones clínicas, a menudo con evolución clínica y resultados impredecibles.3 La actual clasificación recomendada por la Organización Mundial de la Salud en el 2009 es Dengue sin signos de alarma, Dengue con signos de alarma y Dengue grave.3 El virus del dengue (DEN) es un virus de ARN, que abarca cuatro distintos serotipos (DEN-1, DEN 2, DEN 3 y DEN -4) que están estrechamente relacionados y pertenecen al género Flavivirus, familia Flaviviridae.3 Aunque la mayoría de los pacientes presentan infecciones asintomáticas o subclínicas y se recuperan después de un curso clínico benigno y de resolución espontanea, una pequeña proporción progresa a una enfermedad grave, caracterizada principalmente por aumento de la permeabilidad vascular, con hemorragia o sin ella. La rehidratación intravenosa es el tratamiento de elección; esta intervención puede reducir la tasa de letalidad a menos de 1% en los casos graves. Resulta difícil determinar cuál grupo progresa de la forma no grave a la grave de la enfermedad, lo que genera una gran preocupación pues el tratamiento apropiado puede evitar que se desarrollen condiciones clínicas más graves y salvar la vida de los pacientes.3 Los pacientes con manejo ambulatorio deben evaluarse diariamente en la unidad de salud, siguiendo la evolución de la enfermedad y vigilando los signos de alarma y las manifestaciones del dengue grave, es importante no administrar ácido acetil salicílico (ASPIRINA), ni otros antiinflamatorios no esteroides (AINES) ni corticoides.3 Los factores individuales de riesgo determinan la gravedad de la enfermedad e incluyen infección secundaria, edad, raza y posibles enfermedades crónicas (asma bronquial, anemia de células falciformes y diabetes mellitus). Los niños pequeños, en particular, pueden tener menor capacidad que los adultos para compensar la extravasación de plasma capilar y, por consiguiente, están en mayor riesgo de choque por dengue.6 3 Aguilar M, Veloz R., Castro E., Bretas G. Propuesta de Eliminación de la malaria en la Republica http://www.siise.gob.ec/siiseweb/siiseweb.html?sistema=1# 5 Guía Para La Atención Clínica Integral Del Paciente Con Malaria. Colombia 2010 4 6 Guías de atención para enfermos de dengue en la región de las Américas --La Paz: OPS/ OMS, 2010 23 Perfil Epidemiológico del Dengue en el Ecuador El Dengue, desde su aparición a finales del año 1.988 e inicios de 1.989, se ha constituido en el más grave y prioritario problema epidemiológico para la salud pública en el país en lo que respecta a enfermedades de transmisión vectorial, representando una significativa carga social y económica para el Estado debido a la ocurrencia cíclica de grandes epidemias con presencia de casos graves y muertes por esta enfermedad, sumado a esto, existe una condición de híper – endemicidad viral, puesto que el INHMT, ha reportado la circulación de los 4 serotipos del virus del dengue en el país. Figura 9: Comportamiento del Dengue en el Ecuador Periodo 2001-2012 Conportamiento del Dengue en el Ecuador período 2001 - 2012 20000 18000 16000 Casos de Dengue 14000 12000 10000 8000 6000 4000 2000 0 Casos Dengue 2001 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011 2012 13596 7306 10726 6522 14455 6810 10253 2840 6213 17823 7659 17116 Fuente: SIVE – MSP Figura 10: Mapa Viral de Serotipos del Dengue en el Ecuador durante 2005-2011* Fuente: INSPI 24 La enfermedad guarda relación con la dispersión del vector y otros factores ambientales, socioeconómicos y culturales en las localidades de áreas tropicales, subtropicales de las regiones Costa, Sierra (valles interandinos), Amazonía y Galápagos, donde se dan condiciones propicias para la reproducción del Aedes aegypti. Figura 11: Evolución histórica de Localidades con Aedes aegypti en el Ecuador Periodo 1987-2012 EVOLUCIÓN DE LOCALIDADES CON AEDES AEGYPTI EN EL ECUADOR - PERÍODO 1987 - *2012 1600 # LOCALIDADES POSITIVAS 1400 1200 1000 800 600 400 200 0 LOCALIDADES 1987 1988 1989 1990 1991 1992 1993 1994 1995 1996 1997 1998 1999 2000 2001 2002 2003 2004 2005 2006 2007 2008 2009 2010 2011 *2012 4 22 62 126 200 277 329 380 405 435 477 487 496 518 522 534 634 640 710 787 918 1008 1118 1167 1358 1470 P rograma de Control del Aedes aegypti del S NE M , año 2012 (parcial a junio) Mecanismo de Transmisión El vector principal del dengue es el mosquito Aedes aegypti. El virus se transmite desde las personas infectadas a las sanas por medio de la picadura de mosquitos hembras infectadas luego de la ingesta de sangre de una persona enferma y tras un periodo de incubación extrínseco (en la mosquito) que dura entre 4 y 10 días esta puede transmitir el agente patógeno durante toda su vida. Las personas enfermas pueden ser infectantes para las hembras Aedes aegypti, desde un día antes de la aparición de los signos y síntomas hasta 4 o 5 después, lo que se conoce como período de viremia. El mosquito Aedes aegypti vive en hábitats urbanos y se reproduce principalmente en recipientes artificiales. A diferencia de otros mosquitos, este se alimenta durante el día; los periodos en que se intensifican las picaduras son al inicio de la mañana y el atardecer, antes de que oscurezca. 25 Factores de Riesgo7 Figura 12: Factores de Riesgo, transmisión Endemo-Epidémica de Dengue Análisis de Intervenciones Previas y de Resultados Obtenidos Figura 13: Análisis de Intervenciones Previas y de Resultados Obtenidos Dengue 7 Fuente: OPS-Organización Panamericana de la Salud. 1995. Dengue y dengue hemorrágico en las Américas: guías para su prevención y control. Washington DC: OPS. Publicación científica N° 548 26 Dado que no existe vacuna, ni tratamiento específico para el Dengue, la estrategia está orientada al control del vector de esta enfermedad. En este sentido el MSP a través del Servicio Nacional de Eliminación de la Malaria (SNEM), ejecuta intervenciones con insecticidas; principalmente la aplicación del larvicida Temephos al 1 % (fase acuática) en todos los recipientes útiles que contengan o puedan contener agua a nivel domiciliar; además de la destrucción mecánica de una serie de recipientes inservibles en su gran mayoría sirven como criaderos del Aedes aegypti. Complementariamente se realizan trabajos de control del vector en fase adulta a través de las fumigaciones realizadas con equipos portátiles y montados en vehículos en el interior y alrededor de los domicilios para reducir los índices de infestación y control de brotes y epidemias. Las medidas anti-vectoriales son reforzadas por actividades de comunicación y movilización social, incluidas las de Educación para la Salud. En relación a los índices de infestación vectorial durante el periodo 2007-2012 conforme se describe en la tabla a continuación, el índice de Breteau (número de depósitos con Aedes aegypti / número de casas inspeccionadas por 100) ha oscilado en un rango de 16.7 a 21.9 y el índice de casa (número de casas con Aedes aegypti / número de casas inspeccionadas por 100) de 11.0 a 13.4, mismos que se consideran altos o compatibles con la transmisión del Dengue, dado que según la OMS indica para que no exista riesgo de transmisión el índice de casa debe ser ≤5% y el de Breteau ≤3%. Figura 14: Actividades de Vigilancia y Control conforme a la situación del Aedes aegypti y del Dengue 27 Figura 15: Índice de Densidad y correspondencia con los índices de Casas, Recipientes y Breteau (extractado de Brown, 1974) Tabla 14: Evolución de los índices de infestación vectorial por Aedes aegypti en ecuador Periodo 2003-2012 ACTIVIDADES EJECUTADAS DE CONTROL LARVARIO DEL AEDES – PAIS AÑOS AÑO - 2003 AÑO - 2004 AÑO - 2005 AÑO - 2006 AÑO - 2007 AÑO - 2008 AÑO - 2009 AÑO - 2010 AÑO - 2011 AÑO - 2012 TOTAL No. No. Localidades Áreas 356 125 299 450 556 550 605 608 836 695 542 406 982 1.257 1.348 1.253 1.463 1.787 2.094 1.211 CASAS Inspeccionadas 1.189.169 583.876 1.470.953 1.661.244 1.631.183 1.371.134 1.659.411 2.148.048 2.235.078 2.670.151 16.620.247 DEPOSITOS Positivas 127.875 92.640 174.479 191.198 179.149 183.280 222.449 250.274 298.262 307.677 2.027.283 Inspeccionados 9.428.530 5.221.514 13.172.078 14.441.376 14.553.608 12.013.825 13.497.481 17.414.690 19.047.001 21.934.317 140.724.420 Positivos 193.206 144.914 270.020 288.716 272.173 303.810 341.137 392.540 490.007 485.422 3.181.945 Índices Aedes % Tratados (larvicida) 1.651.299 357.475 2.016.955 2.610.370 2.308.661 1.943.691 2.268.324 2.509.407 2.639.527 3.486.736 21.792.445 Breteau 16,2 24,8 18,4 17,4 16,7 22,2 20,6 18,3 21,9 18,2 19,1 Fuente: Proyecto control de Dengue SNEM. Índice de Breteau (número de depósitos con Aedes aegypti / número de casas inspeccionadas x 100). Índice de casa (número de casas con Aedes aegypti / número de casas inspeccionadas x 100) La OMS indica que para que no exista riesgo de transmisión el índice de casa debe ser ≤4% y el de Breteau ≤5%. En relación a los indicadores y metas propuestas en el proyecto Control del Dengue durante el periodo 2007-2012, se observa cumplimiento de las metas programadas durante los últimos tres años, en los componentes: Eliminar los criaderos del Aedes aegypti en la fase acuática y Disminuir la población adulta del mosquito Aedes aegypti en las áreas de riesgo. 28 Casa 10,8 15,9 11,9 11,5 11 13,4 13,4 11,7 13,3 11,5 12,2 Tabla 15: Evolución de Indicadores y metas de Dengue Periodo 2007-2012 Componentes Indicador Años 2007 2008 2009 2010 2011 2012 1: Eliminar los criaderos del Aedes aegypti en la fase acuática Casas Intervenidas con aplicación de larvicida Meta 1.691.118 1.775.674 621.486 1.500.000 2.148.048 2.000.000 Resultado 1.332.313 1.407.335 1.571.886 2.148.048 2.233.643 2.600.634 Alcance % 78,78% 79,26% 252,92% 143,20% 103,98% 130,03% Meta Resultado 667.457 - 735.871 - 750.000 768.820 1.000.000 1.148.561 848.024 836.576 800.000 1.165.665 2: Disminuir la población adulta del mosquito Aedes aegypti en las áreas de riesgo. Casas Fumigadas Manzanas Fumigadas Alcance % 0,00% 0,00% 102,51% 114,86% 98,65% 145,71% Meta Resultado 300.955 356.815 316.003 290.079 331.803 406.909 500.000 404.589 404.589 312.218 350.000 309.626 Alcance % 118,56% 91,80% 122,64% 80,92% 77,17% 88,46% Fuente: Estadísticas del Proyecto Dengue En cuanto al número de casos registrados de Dengue y Dengue Grave durante el periodo 2002 a 2012, conforme se indica en la tabla 11 el Dengue ha presentado un comportamiento endémico-epidémico, ocasionando graves repercusiones sociales y económicas constituyéndose hasta la actualidad en uno de los principales problemas de salud pública para el país al igual que en otros países de América y del Mundo, donde el control de la enfermedad no ha sido posible. Esta aparente contradicción del cumplimiento de las metas del proyecto vs. Ocurrencia de epidemias de Dengue en el país, podrían ser explicadas en base a los siguientes aspectos: 1. La programación de las actividades no se han ajustado a las reales necesidades operativas de control del Aedes aegypti en el país. 2. Han existido restricciones económicas en las asignaciones presupuestarias en el Ministerio durante el periodo 2007-2012, a pesar de haber presentado propuestas ajustadas a las reales necesidades del país. 3. La persistencia de la transmisión de enfermedad obedece a factores de carácter: sociales, económicos, culturales y ambientales, sobre los cuales el proyecto no puede o incide en forma mínima. LEISHMANIASIS La Leishmaniasis es una afección tegumentaria de los mamíferos incluido el humano, causada por parásitos del genero Leishmania, transmitida por dípteros de la familia Psichodidae, generos Phlebotomus en el viejo mundo y Lutzomyia en el Nuevo Mundo; puede ser una enfermedad zoonotica o antroponotica. Esta enfermedad representa un problema de salud pública en el Ecuador, por su gran dispersión en 23 de las 24 provincias del país, afectando a las personas más pobres de sectores rurales que viven en áreas ecológicamente propicias para su transmisión entre los 300 a 1.500 metros sobre el nivel del mar (valles interandinos subtropicales) y de acuerdo a la estratificación se estima una población con riesgo de transmisión de aproximadamente 3´500.00 habitantes. 29 La enfermedad produce lesiones deformantes y/o mutilantes, que generan en los pacientes problemas de carácter psicológico, producen aislamiento y pérdida de la capacidad productiva de las personas, de la familia y la comunidad. Perfil epidemiológico de Leishmaniasis Las diversas formas clínicas de la Leishmaniasis constituyen un serio problema de salud pública en los países donde es endémica. La Organización Mundial de la Salud (OMS), en la matriz de énfasis estratégico del programa de investigación en enfermedades tropicales (Tropical Disease Research), ha clasificado la Leishmaniasis en la categoría I como una enfermedad emergente y sin control. En los últimos años refleja un incremento de la transmisión de la enfermedad, que se puede atribuir a diversos factores, entre otros, al aumento de las actividades humanas en ambientes silvestres en donde existe la transmisión enzoótica, la adaptación de los vectores al peri domicilio y domicilioi.En la periferias de Alausi, Paute y Huigra, se han reportados casos en niños menores de un año sin antecedentes de viajes a zonas rurales (Hashiguchi et al. 1991). El conocimiento actual sobre la epidemiología de la leishmaniasis en Venezuela, Colombia, Ecuador, Perú y Bolivia nos indica que los vectores flebótominos pertenecen a varias especies del género Lutzomyia. La mayoría de los casos de leishmaniasis cutánea son causados por parásitos del subgénero Viannia y solo una minoría evoluciona a una complicación mucosa, metastásica o no metastásica.ii Los demás son causados por parásitos del subgénero Leishmania. En el Ecuador la enfermedad muestra una gran dispersión y según el MSP durante el periodo de 2002 al 2012, se han registrado casos en 23 de las 24 provincias del país (excepto Galápagos), con un promedio de 1.537 casos anuales y una tasa de incidencia que oscila en un rango de 6,14 a 19,15 por 100.000 habitantes. Figura 16: Número de casos y tasas de Leishmaniasis en el Ecuador Periodo 2002-2012 La transmisión de la Leishmaniasis en el Ecuador, puede presentar dos patrones: 1) brotes asociados a la incursión del humano en un hábitat silvestre con transmisión natural como la tala de bosques, construcción de carreteras, áreas nuevas de colonización, o en el caso de migración a áreas endémicas para realizar trabajos como la extracción de oro, madera, recolección de café, sembrío de arroz, incursiones militares, entre otros. 2) transmisión en 30 asentamientos urbanos cuando los vectores y reservorios se acercan a los domicilios rodeados de floresta, en este patrón, algunos mamíferos domésticos podrían tener un papel importante como reservorios. (En esta segunda forma es probable que en el futuro el humano se convierta en reservorio del parásito). La Leishmaniasis constituye un problema de salud pública en el Ecuador, debido a su amplia distribución principalmente a nivel rural de las regiones Costa y Amazonia (a partir de los 300 metros), Sierra (valles Andinos con una altitud entre los 1.200 a 2.400 metros sobre el nivel del mar). La distribución de la enfermedad coincide con la presencia de bosques tropicales y subtropicales que son los nichos ecológicos apropiados para la presencia del vector y reservorios. Mecanismo de Transmisión Las especies de Leishmania poseen un ciclo de vida similar; es importante el conocimiento de cada una de ellas para poder entender y aplicar ciertas medidas de prevención y control. En general se pueden producir dos ciclos (como se muestra en la imagen a continuación): a) uno silvestre donde la Leishmania circula entre los reservorios naturales, manteniendo el ciclo con la participación de vectores propios de la zona, y b) en que los vectores infectados pueden atacar al humano y a los animales domésticos o peri domésticos como los perros a partir de cuyas lesiones se han logrado infectar a flebotominos y los equinos, cuyo rol es aún discutido. Otros mamíferos peri-domiciliarios como las ratas o animales silvestres que se acercan al hábitat humano, pueden participar en el ciclo evolutivo. Figura 17: Mecanismo de transmisión de Leishmaniasis 31 Factores de Riesgo Esta enfermedad presenta varios factores de riesgo, entre ellos están: Medio Ambiente y Ocupación.- La residencia en áreas endémicas y movimientos migratorios internos exponen al humano al contacto del vector. La Leishmaniasis también puede considerarse como una enfermedad ocupacional, debido a que está directamente relacionada con actividades laborales en zonas donde esta enfermedad es endémica, sobre todo en bosques y plantaciones de clima tropical, subtropical y valles Andinos. Los cambios ambientales rompen el equilibrio natural de las especies, favoreciendo o perjudicando el normal desarrollo de los ciclos de vida de las mismas, es así que la modificación en territorio por la tala de bosques, inundaciones, construcción de represas, carreteras etc. puede aumentar el riesgo de contraer la enfermedad. Los estudios realizados, demuestran que la Leishmaniasis tiene alta vulnerabilidad debido a que la transmisión del parasito puede ser influenciada por los cambios de clima, ya que se acentuara o disminuirá a medida que se produzcan alteraciones en la humedad y temperatura. Vivienda e Higiene.- La vivienda rodeada de vegetación, también está asociada a un mayor riesgo de transmisión de la enfermedad, porque permite que el vector ingrese fácilmente a los hogares. Las viviendas rústicas y los bajos niveles de higiene aumentan los riesgos de transmisión domiciliaria y peri domiciliaria, una reciente investigación en el noroccidente de Pichincha, muestran que el mayor riesgo para adquirir la Leishmaniasis está asociada con personas que viven en casas cuyas paredes exteriores o pisos están construidos de madera o caña guadua, material que deja espacios en su estructura por donde el vector puede pasar. La ubicación de los servicios higiénicos o letrinas fuera de la casa puede favorecer la exposición al vector. Urbanización.- En algunas zonas endémicas el patrón epidemiológico de la Leishmaniasis está extendiéndose de una transmisión silvestre a una transmisión peri-urbana y urbana como ha sido demostrado en Alausí y Huigra (Gómez E. Hashiguchi Y.). Edad y Género.- De acuerdo a la información registrada en el Ministerio de Salud Pública del Ecuador el mayor número de casos se produce en el grupo etario de entre 15 a 44 años de edad del sexo masculino, sin embargo esto depende de cada zona endémica ya que existen algunas donde los más afectados son los niños, por la acción intra-domiciliaria del vector o por tratarse de zonas endémicas muy antiguas. 32 Figura 18: Análisis de Intervenciones Previas y su Efectividad de Leishmaniasis Durante los años 2011 y 2012 el proyecto de Leishmaniasis ha garantizado el abastecimiento oportuno de los medicamentos específicos para el tratamiento de la enfermedad a todas las Unidades Operativas de Salud ubicadas en áreas de transmisión. De un total de 286 Microscopistas-SNEM, a través del proyecto se ha logrado capacitar en el diagnóstico microscópico de Leishmaniasis cutánea a un total de 187 (65%) hasta mayo del 2012, logrando mejorar la oferta de diagnóstico y tratamiento de esta patología en las áreas de transmisión del país. El control vectorial no es considerado dentro del proyecto en razón de que el vector tiene hábitos silvestres. Dado que el vector es de hábitos silvestres y por ende no es posible su control, la principal estrategia está orientada a medidas de prevención de la picadura del vector para lo cual se debe realizar actividades permanentes de educación para la salud, hasta la presente fecha existen 576 líderes comunitarios en medidas de prevención, control y vigilancia comunitaria de esta enfermedad. Sin embargo, para el manejo de los pacientes se ha trabajado en incrementar la oferta de diagnóstico y tratamiento rápido de los casos, a través de la capacitación de la red de Microscopistas-SNEM ubicados en las áreas de salud a nivel nacional, lo que ha permitido mejorar la vigilancia epidemiológica de la enfermedad. Además el proyecto ha garantizado el abastecimiento oportuno de los medicamentos específicos (antimoniales pentavalentes) para el tratamiento a todas las Unidades Operativas de Salud ubicadas en áreas de transmisión. También contamos con tratamientos alternativos para las Leishmaniasis no severas, en las que no se requiere el uso de antimoniales. CHAGAS La Enfermedad de Chagas o Tripanosomiasis Americana es transmitida en su mayor porcentaje (80%) por insectos hematófagos obligatorios de la subfamilia triatominae, conocidos comúnmente en el Ecuador como chinchorros. El agente causal es el protozoo polimórfico parásito Trypanosoma cruzi, el cual debido a su diversidad genética, ha sido clasificado en dos grandes grupos: T cruzi I y T. cruzi II. El T. cruzi es un parásito de mamíferos que tiene como 33 hospedero invertebrado (vector) a varias especies de la familia Reduviidae, hemípteros hematófagos Esta enfermedad se presenta con mayor frecuencia en las comunidades rurales donde las condiciones de las viviendas y situación socio económica son muy precarias, por ello a la Enfermedad de Chagas se la denomina también la enfermedad de la pobreza o enfermedad olvidada. La población vulnerable y en riesgo de trasmisión de Chagas se estima en 3´500.000 habitantes, esto es el 25% de la población del Ecuador. Las formas clínicas son la Aguda (Subaguda y moderada) casi exclusiva de niños y menores de 15 años, y la crónica (asintomática y sintomática) que usualmente se presenta en mayores de 15 años y adultos. En la forma clínica crónica sintomática debemos señalar dos cuadros: La Cardiopatia chagásica y los megas viscerales. Las manifestaciones clínicas más importantes de la miocardiopatía chagásica son la insuficiencia cardíaca, los trastornos del ritmo, los bloqueos aurícula-ventriculares y las embolias pulmonares. Estas patologías deben ser tratadas por el especialista en cardiología. A nivel del aparato digestivo, son frecuentes los trastornos del peristaltismo y el reflujo gastroesofágico dando como resultado trastornos como estreñimiento y esofagitis por reflujo. Los Megas son el nivel más grave de la enfermedad de Chagas a nivel digestivo. De igual manera como en el caso anterior esto debe ser manejador el especialista en gastroenterología. Perfil Epidemiológico de la Enfermedad de Chagas Figura 19: Número de casos de la Enfermedad de Chagas Periodo 1990-2012 La incidencia de la Enfermedad de Chagas, en ausencia de medidas de control, fue estimada en aproximadamente 36 por 100.000 habitantes, es decir 4400 nuevas infecciones/año y una mortalidad anual de 1300 personas. El número absoluto de pacientes con formas crónicas sintomáticas probablemente se acerca a los 35.000 casos; de ellos, más de 30.000 casos sufren cardiopatías y unos 1700 casos de enfermedad digestiva. La carga social de la enfermedad se cuantificó en términos de pérdidas económicas de aproximadamente 23 millones de 34 dólares/año y de pérdidas de años de vida ajustados por discapacidad (AVADs) de aproximadamente 35.000 AVADs/año. Según la información del área de epidemiología del Ministerio de Salud Pública (MSP) las tasas de prevalencia conocidas en todo el país durante el período de 1990 al 2010 oscilan en un rango de 0,17 a 1,16 por 100.000 habitantes, con una tendencia al incremento en los últimos 3 años, lo que obedece a búsqueda activa de casos. De acuerdo a investigaciones efectuadas se estima que la prevalencia de la enfermedad probablemente es del 1,38% de la población general (0,65 % en la Sierra, 1,99% en la Costa y 1,75% en la Amazonía), considerándose que en nuestro país existirían aproximadamente 197.000 Chagásicos8. La mayoría son seropositivos asintomáticos, que en su mayoría jamás desarrollarán la enfermedad. Estos datos corresponden a muestreos serológicos hechos con una sola prueba (se necesitan 2 de 3 pruebas de método diferentes) Aproximadamente 8.5 millones de personas habitan en zonas de riesgo, donde la transmisión vectorial existe con certeza o es probable que exista; estas zonas de riesgo incluyen cantones de 22 provincias. Alrededor de 3 a 5 millones de personas son consideradas especialmente vulnerables debido a la ecología, las características de sus viviendas o a su situación económica. Las provincias históricamente más afectadas por esta patología son Loja, El Oro, Manabí y Guayas; en los años 2008 y 2009 el 80% de los casos nuevos de Chagas registrados a nivel nacional corresponden a las Provincias de Orellana y Sucumbíos. Mecanismos de Transmisión Transmisión por el insecto vector: La transmisión vectorial de la enfermedad de Chagas es la vía de contagio más común, (80%). El Trypanosoma cruzi, cumple dos ciclos evolutivos, uno en el chinchorro y otro en el hombre. Transmisión por transfusión sanguínea: en las ciudades se observa una cifra cada vez mayor de donantes infectados, los cuales han pasado sus primeros años de vida en las zonas endémicas. Esta forma de transmisión tiene un período de incubación más prolongado, alrededor de 40 días Transmisión congénita: Los microorganismos pueden atravesar la placenta y producir infección congénita (en 2% a 8% de los embarazos en mujeres infectadas). La detección del Chagas congénito debe efectuarse en los servicios de Ginecología, Obstetricia, Neonatología y Pediatría. Infección accidental en el laboratorio: es infrecuente, representa sin duda un riesgo muy real de contraer la enfermedad de Chagas. Los accidentes de laboratorio generalmente se deben a punciones con agujas infectadas, contacto con materiales contaminados, aspiración de cultivos de T. cruzi al trabajar con pipetas y salpicaduras de suspensiones de T. cruzi en las conjuntivas. 8 Fuente: Control de la Enfermedad de Chagas en el Ecuador OPS/OMS-MSP, Diciembre 2002 - Febrero 35 Transmisión oral: mediante investigaciones epidemiológicas de dos brotes independientes de enfermedad de Chagas aguda en Colombia se han obtenido pruebas sumamente convincentes de la transmisión oral a través de la ingestión de alimentos contaminados. Transmisión por trasplante de órganos: El trasplante de órganos de donantes infectados es una nueva forma de transmisión de Trypanosoma cruzi, que ha sido objeto de escasa atención. Los pacientes que han recibido órganos de donantes con enfermedad de Chagas crónica han sufrido episodios agudos de laenfermedad y el parásito ha sido aislado de la sangre periférica. Se han registrado algunos casos fatales, en los cuales se han aislado parásitos en varios órganos. Además, como los receptores de los órganos están sometidos a terapia inmunosupresiva, aumenta enormemente su susceptibilidad a la infección con los parásitos del donante. De igual manera, si los receptores son Chagásicos crónicos, pueden sufrir un agravamiento de la infección como resultado del tratamiento inmunosupresivo. Otra forma de clasificación internacional mente aceptada es la siguiente: a. Transmisión vectorial: La enfermedad de Chagas o Tripanosomiosis Americana se produce por la infección con Trypanosoma cruzi, parásito unicelular que se transmite a través de un insecto hematófago (que se alimenta de sangre). Este insecto, llamado popularmente “chinchorro”, puede compartir la vivienda con el hombre, y la especie más importante es el Triatoma dimidiata y Rhodnius ecuadoriensis. b. Transmisión no vectoriales: No participa el insecto, son: a) Por transfusión de sangre, b) Congénita: transmisión de la madre infectada a su hijo, durante el embarazo y/o parto. c) Por transplantes de órganos, d) Accidentes de laboratorio. e) Otros: oral, lactancia. Cuanto más alto sea el número de personas con Trypanosoma cruzi circulante, mayor será la posibilidad de transmisión y riesgo de infección. Factores de Riesgo Considerando que la mayoría de los casos se producen por transmisión vectorial, definitivamente los ambientes que sean hábitats adecuados para el triatomino vector promueven la probabilidad de infección de Chagas. Esto significa que viviendas con paredes de madera o lodo, con techos de paja, son hábitats que promueven la domicialización del vector. Casas en zonas rurales y de baja renta, se prestan para convertirse en hábitats del vector transmisor. 36 Por ser una zoonosis, la presencia de probables reservorios silvestres o domésticos, en los alrededores o dentro de la vivienda, constituye otro factor de riesgo. Otro factor de riesgo es la recepción de transfusiones sanguíneas, trasplante de órganos o transmisión congénita, en el caso que el donante o la madre estén infectados con la enfermedad de Chagas. Figura 20: Análisis de Intervenciones Previas y los Resultados Obtenidos de Chagas La estrategia está orientada a la interrupción de la transmisión vectorial de la enfermedad en las áreas con vectores a nivel nacional mediante búsqueda intra y peridomiciliaria y aplicación de insecticidas de acción residual, posterior a lo cual hay se continúan realizando actividades de vigilancia entomológica para evitar la reinfestación domiciliaria. Búsqueda activa de casos a través de estudios serológicos realizados sobre todo en la población escolar o menores de 15 años de edad, coordinación con el INSPI para pruebas confirmatorias y tratamiento de los mismos a través de unidades de salud del MSP, efecto para el cual se realizan eventos de Capacitación a los equipos de salud sobre, diagnóstico, tratamiento, vigilancia epidemiológica, vigilancia entomológica y medidas de prevención y control de enfermedades metaxénicas. Tabla 16: Casos confirmados de la Enfermedad de Chagas por provincia Período 2008 - 2012 PROVINCIAS Orellana Manabí Guayas Loja Sucumbíos El Oro Morona Santiago Los Ríos Pastaza Pichincha Napo Cañar Sto. Domingo Esmeraldas TOTALES AÑO 2008 AÑO 2009 AÑO 2010 AÑO 2011 30 54 66 0 10 0 37 25 1 16 29 40 0 4 13 0 7 22 10 0 1 0 8 34 8 1 0 6 0 0 1 4 4 0 1 0 0 0 0 0 1 1 1 0 0 0 1 0 0 1 0 0 0 0 0 1 62 99 167 110 Fuente: Proyecto Chagas del SNEM/MSP AÑO 2012 29 10 29 0 1 1 0 3 0 3 0 0 0 0 76 37 Caso confirmado: Se considera caso confirmado de Chagas aquel en que se detectare el parasito directamente en su circulación periférica (fase aguda) y a aquel paciente que resultare positivo en dos de tres pruebas serológicas con métodos diferentes (fase crónica asintomática y sintomática). Tabla 17: Evolución de Indicadores y metas de Chagas Periodo 2007-2012 Componentes Indicador Componente IEC Capacitación a estudiantes de colegios y escuelas Aumentar la cobertura de diagnóstico y tratamiento Muestras sanguíneas examinadas Casas visitadas Búsqueda entomológica Interrumpir la transmisión vectorial en las áreas con vectores domiciliados Casas rociadas Años 2007 2008 2009 2010 2011 2012 Meta - 44.022 9.000 11.000 - - Resultado Alcance % - 44.022 100,00% 12.418 137,98% 11.902 108,20% - - Meta - 6.139 9.000 10.000 8.000 8.000 6.139 100,00% 23.718 9.477 105,30% 45.240 7.406 74,06% 15.539 7.470 93,38% 20.000 9.895 123,69% 20.000 Resultado 10.567 23.718 45.240 Alcance % 88,06% 100,00% 100,00% Meta 1.000 1.000 4.000 Resultado 917 917 3.605 Alcance % 91,70% 91,70% 90,13% Fuente: Estadísticas del Proyecto Chagas 15.539 100,00% 3.000 2.641 88,03% 19.117 95,59% 2.000 1.986 99,30% 23.277 116,39% 20.000 21.993 109,97% Resultado Alcance % Meta 12.000 En relación a los indicadores y metas propuestas en el proyecto Control del Chagas durante el periodo 2007-2012, se observa el cumplimiento de las metas programadas, en los componentes: Información Educación y Comunicación, Aumento de cobertura en diagnóstico de tratamiento de Chagas e Interrupción la transmisión vectorial en las áreas con vectores domiciliados. El índice de infestación vectorial durante el periodo 2010-2012 conforme se describe en la tabla, se han encontrado altos índices de infestación (viviendas con triatominos / viviendas visitadas x 100) en las Provincias de Guayas, Manabí, El Oro y Loja, donde se visitaron comunidades con antecedentes históricos de presencia de triatominos. Tabla 18: Índices de Infestación y especies de Triatominos por Provincias Periodo 2010-2012 AÑOS 2010 PROVINCIAS INDICE DE INFESTACION GUAYAS MANABI 5,60 15,56 EL ORO 1,90 R. ecuadoriensis, P. rufotuberculatus LOJA GUAYAS 6,24 2,01 R. ecuadoriensis, P. rufotuberculatus, T. corrioni EL ORO LOJA 0,41 5,53 R. ecuadoriensis, P. rufutuberculatus, T. carrioni GUAYAS 2,43 T. dimidiata EL ORO 0,10 R. ecuadoriensis, P. rufutuberculatus, T. carrioni LOJA 3,57 P. rufutuberculatus, T. carrioni,P. chinai 2011 2012 ESPECIES ENCONTRADAS T. dimidiata R. ecuadoriensis T. dimidiata P. rufutuberculatus, T. carrioni,P. chinai Fuente: Programa Nacional de Control y Vigilancia de la Enfermedad de Chagas 38 ONCOCERCOSIS La Oncocercosis (ceguera de los ríos) es una enfermedad parasitaria transmitida de persona a persona por medio de la picadura del vector del genero Simulium. La onchocerca volvulus en estado adulto se ubica en nódulos u oncocercomas, tienen un periodo de vida de 9 a 14 años. Las principales lesiones que presenta la enfermedad en el aspecto dérmico varían desde algunas pápulas (el prurito resultante puede ser muy intenso) hasta cambios atróficos pigmentarios y crónicos de la piel como excoriaciones con pústulas, liquenificación, paquidermia, atrofia focal, regional o general, cambios pigmentarios, piel de leopardo y hasta fase leonina. En el aspecto ocular las microfilarias causan lesiones como la queratitis punteada que se presenta como una infiltración inflamatoria numular aguda evanescente alrededor de las microfilarias muertas. También se pueden hallar microfiliarias vivas en la córnea, se pueden observar circulando en el fluido acuoso detrás de la córnea. La queratitis esclerosante es una de las manifestaciones inflamatorias que puede causar la ceguera irreversible. El impacto sobre la economía familiar es alto ya que en caso de que la Oncocercosis avance a un estadío en que provoque ceguera al huésped, inmediatamente causaría la discapacidad física para poder trabajar, tomando en cuenta que la zona de riesgo es rural, esto imposibilitaría completamente a la persona de buscar trabajo y alimento, siendo una carga para su familia Como producto de una serie de acciones exitosamente ejecutadas por el proyecto desde hace varios años, en el 2008, se inició el proceso de Certificación de Eliminación de la Oncocercosis en el Ecuador, sustentado en acciones de vigilancia epidemiológica. En los años 2012 y 2013, se realizarán Evaluaciones Epidemiológicas a Profundidad: Parasitológicas, Oftalmológicas y Entomológicas, en las Comunidades Centinelas de los Focos Endémicos. Perfil Epidemiológico de la Oncocercosis Las zonas en riesgo identificadas para la enfermedad tomando en cuenta los factores ambientales y hábitat del vector son las comprendidas en la cuenca del Rio Santiago. Identificadas en el mapa a continuación. Figura 21: Perfil Epidemiológico de la Oncocercosis 39 Los focos endémicos de Oncocercosis en el Ecuador se encuentran geográficamente ubicados en el Noroccidente de la Provincia de Esmeraldas y en la Provincia de Santo Domingo de los Tsáchilas. Se estima que la población en riesgo es de 26.684 personas que habitan en 119 comunidades localizadas en 18 parroquias, 5 Cantones y 2 Provincias y el vector más importante es el Simulium Exiguum. Para la enfermedad de la Oncocercosis, toda la población que vive en la zona identificada está en riesgo, no existe una vulnerabilidad mayor por grupo de edad, sexo o etnia, más bien la vulnerabilidad está sujeta al tiempo de exposición a los lugares abiertos (cerca del río) y al número de picaduras del vector. El Programa Nacional de Eliminación de la Oncocercosis (PNEO-E) realizó evaluaciones detenidas a profundidad en comunidades centinelas para evaluar el impacto que la distribución masiva de ivermectina (del año 1990 hasta 2009) ha tenido sobre la Oncocercosis en el Ecuador. El método de evaluación sobre comunidades centinelas ha sido recomendado por la OMS para una medición a profundidad de los programas de distribución de ivermectina (WHO, 1995). Además, se realizaron evaluaciones a profundidad en comunidades extra centinelas seleccionadas para verificar las observaciones obtenidas en las comunidades centinelas. Los aspectos evaluados fueron oftalmológicos, parasitológicos, y entomológicos. Mecanismo de Transmisión Como muestra la figura a continuación, la onchocerca volvulus entra al cuerpo de las personas a través de la picadura de una mosca del género Simulium la cual desarrolla su etapa larvaria en los riachuelos correntosos y limpios. La mosca hembra se infecta cuando, buscando alimentación de sangre humana, pica a una persona infectada e ingiere microfilarias. Estas microfilarias, ya dentro de la mosca, evolucionan hasta transformarse en larvas infectivas (larvas de tercer estadío o L3). Estas larvas pueden ser inoculadas en un nuevo huésped en el momento en que los insectos vuelvan a picar. Figura 22: Mecanismo de Transmisión de la Oncocercosis 40 Factores de Riesgo El foco endémico principal ha sido delimitado en la cuenca del río Santiago en el cantón Eloy Alfaro de la provincia de Esmeraldas, existen focos satélites en los cantones Río Verde y Quinindé de la misma provincia y otro en Santo Domingo de los Tsáchilas debidos a la migración de la población. Esmeraldas es la provincia de la costa ecuatoriana que se encuentra más al este. El territorio es llano, con pequeñas colinas de un máximo de 30 msnm. Pequeñas elevaciones existentes. El clima de Esmeraldas varía desde tropical subhúmedo, subtropical húmedo y subtropical muy húmedo, con una temperatura media de 23 °C. El sistema hidrográfico del Río Santiago nace en la cordillera occidental en los páramos de Piñán. Sus afluentes son los Ríos Wimbí, Bogotá, Tululbí y el Palaví. Los Ríos Santiago y Cayapas riegan toda la zona norte de la provincia, y son navegables en la mayoría de su extensión. La composición étnica del foco endémico de oncocercosis en la provincia de Esmeraldas consiste principalmente de dos grupos: el grupo indígena de los Chachi y el grupo afroecuatoriano. En los últimos años la población mestiza ha ingresado al área endémica, y en Santo Domingo de los Tsáchilas, está el grupo indígena de los Tsáchilas en las dos comunidades del foco en esta provincia. Figura 23: Análisis de Intervenciones Previas y su Efectividad de Oncocercosis Desde el año 2004 no se detectaron más pacientes; tras cuatros años de vigilancia la instancias internacionales Organización Panamericana de la Salud y la OEPA (Onchocerciasis Elimination Program for the Americas), declararon eliminada la transmisión de la enfermedad y se entró en nueva fase de vigilancia hasta el año 2012 para declarar eliminada la enfermedad y alcanzar la correspondiente Certificación de Eliminación, éxito atribuible a la administración de un medicamento (Ivermectina) de manera semestral a toda la población en riesgo en el área endémica de nuestro país. Ver anexo 3. 41 Tabla 19: Evolución de Indicadores y metas del Proyecto de Oncocercosis Periodo 2007-2012 Componentes Indicador Años 2007 2008 2009 2010 2011 2012 Tratamiento semestral con ivermectina Número de entradas a las comunidades para dar tratamiento con ivermectina Meta 238 168 168 - - - Resultado 238 159 168 - - - Alcance % 100% 95% 100% - - - Meta 119 84 84 84 84 84 Paquete multipropósito Número de entradas a las comunidades con paquete multipropósito (consultas por demanda, odontología, multivitaminas, vacunación etc) Resultado 119 75 84 84 84 80 Alcance % Numero de comunidades con evaluación entomológica Evaluaciones entomológicas Numero de estudios PCR 100% 89% 100% 100% 100% 95% Meta - 4 - 3 - 8 Resultado - 4 - 3 - 8 Alcance % - 100% - 100% - 100% Meta - 1 - 1 - 1 Resultado - 1 - 1 - 1 100% - 100% Alcance % 100% Fuente: Estadísticas del Proyecto Oncocercosis FIEBRE AMARILLA La fiebre amarilla es una enfermedad viral aguda (flavivirus), transmitida por la picadura de mosquitos infectados, que en su forma severa o hemorrágica se caracteriza por presentar fiebre, postración, ictericia (hepatitis), toxemia, nefritis (albuminuria) y hemorragias, pudiendo llegar en estos casos la mortalidad al 50%. La evolución histórica de la fiebre amarilla urbana en la ciudad de Guayaquil durante el período de 1740 a 1919, con elevadas tasas de mortalidad es un recordatorio de la gravedad del riesgo de reurbanización de la fiebre amarilla en el Ecuador. Los principales vectores de la enfermedad son los mosquitos de los géneros Haemagogus y Sabethes a nivel selvático y Aedes aegypti a nivel urbano. Se destaca además al Aedes albopictus como otro eficiente vector de la fiebre amarilla y que podría servir de nexo entre los ciclos selváticos y urbanos para la reurbanización de la enfermedad debido a su capacidad para adaptarse a ambientes silvestres y urbanos, sin embargo este último no se ha reportado aún en el Ecuador pero existe en los países vecinos de Perú, Colombia y Brasil. La principal estrategia de prevención la constituye la vacunación anti amarilica del 100 % de la población en zonas endémicas y la implementación de la vigilancia entomo - epidemiologica de los vectores de la fiebre amarilla, con la finalidad de contar con información útil sobre los mismos y determinar oportunamente el riesgo de reurbanización de la fiebre amarilla selvática. Las poblaciones con mayor riesgo de transmisión son las rurales y en segundo lugar las urbanas de las provincias de la Región Amazónica donde viven alrededor de 739.814 habitantes. No hay tratamiento curativo para la fiebre amarilla, el tratamiento es sintomático y de sostén. 42 Perfil epidemiológico de la Fiebre Amarilla Según los datos estadísticos del área de Epidemiología del Ministerio de Salud Pública, desde el año 2002 hasta el año 2011 no se registraron nuevos casos de fiebre amarilla selvática en el País. En el año 2012 se reportaron casos sospechosos de síndrome febril ictero - hemorrágico de los cuales se conformaron dos por medio del CDC de Atlanta y el Instituto Nacional de Salud e Investigaciones del Ecuador (INSPI), situación que se evidencia en el siguiente gráfico: Figura 24: Casos de Fiebre Amarilla Selvática en Provincias de la Región Amazónica del Ecuador Periodo 1990 – 2012 Fuente: Anuario de Epidemiología – MSP Mecanismo de Transmisión El virus de la fiebre amarilla es un arbovirus del género Flavivirus y los principales vectores de la enfermedad son los mosquitos de los géneros Haemagogus y Sabethes a nivel selvático y Aedes aegypti a nivel urbano, que transmiten el virus de un huésped a otro, principalmente entre los monos, pero también del mono al hombre y de una persona a otra. Los mosquitos se crían en las casas (domésticos), en el bosque (salvajes) o en ambos hábitats (semidomésticos). Existen tres ciclos de transmisión: Fiebre amarilla selvática: En las selvas tropicales lluviosas el virus de la fiebre amarilla circula entre animales silvestres principalmente los monos y eventualmente el hombre a través de los mosquitos (géneros Haemagogus y Sabhetes. Fiebre amarilla intermedia: Ocurre en las fincas periféricas a las comunidades selváticas participando los mismos protagonistas con excepción de que el Aedes aegypti que es el vector urbano se infecta de animales silvestres que se acercan a los asentamientos, existiendo el riesgo de que a partir de aquí se extienda a las zonas urbanas. Fiebre amarilla urbana: Cuando las personas infectadas introducen el virus en zonas con gran densidad de mosquitos Aedes y con personas no inmunes se producen grandes epidemias urbanas. 43 Factores de Riesgo La gran dispersión y elevados índices de infestación vectorial del Aedes aegypti a nivel nacional. Las personas que por diversas razones ingresan a las áreas de transmisión selvática (turistas, colonizadores, cazadores, mineros, personal de las Fuerzas Armadas, explotación de petróleo), pueden tener una participación importante en transportar el virus de la fiebre amarilla desde un ambiente selvático al sector urbano donde el Aedes aegypti transmitirá la enfermedad. Figura 25: Análisis de Intervenciones Previas y su Efectividad de Fiebre Amarilla Deficientes coberturas de inmunizaciones antiamarílicas. En el componente entomológico el SNEM conjuntamente con las Direcciones Provinciales de Salud (DPS), han sentado las bases para la implementación de un sistema de vigilancia entomológica de los vectores selváticos de esta enfermedad en las provincias de la Amazonía y en el ámbito urbano las actividades son las que corresponden a la vigilancia y control del Aedes aegypti. En la siguiente tabla se evidencia un parcial cumplimiento de las metas en el año 2011 y el total cumplimiento de las mismas en el año 2012 en cada uno de los componentes: Vigilancia Entomológica del Vector de Fiebre Amarilla en áreas de riesgo priorizadas del país, Vigilancia Entomológica del Vector de Fiebre Amarilla y Fortalecimiento del sistema de información que contribuya a la respuesta temprana de los equipos de salud ante una situación de riesgo de transmisión en las zonas vulnerables. 44 Tabla 20: Evolución de Indicadores y metas del Proyecto de Fiebre Amarilla Periodo 2011-2012 Componentes Vigilancia Entomológica del Vector de Fiebre Amarilla en áreas de riesgo del país. Vigilancia Entomológica del Vector de Fiebre Amarilla en áreas de riesgo del país. Fortalecer el sistema de información que contribuya a la respuesta temprana de los equipos de salud ante una situación de riesgo de transmisión en las zonas vulnerables. Indicador Años 2011 2012 Número de personas capacitadas en Vigilancia entomológica para la Fiebre Amarilla. Puestos de vigilancia Entomológico de Fiebre Amarilla instalados Meta Resultado 160 110 180 232 Alcance % 68,75% 128,89% Meta Resultado Alcance % Meta 5 3 60,00% 7 6 6 100,00% 6 Resultado 6 7 Alcance % 85,71% 116,67% Talleres de capacitación al personal SNEM en diversas Zonas Fuente: Estadísticas del Proyecto Fiebre Amarilla Es importante continuar con la implementación de la vigilancia entomo epidemiológica de los vectores de la fiebre amarilla, con la finalidad de contar con información útil sobre los mismos y determinar oportunamente el riesgo de reurbanización de la fiebre amarilla selvática. Por ser un proyecto de reciente implementación en el país y debido a las escasas asignaciones presupuestarias, no se ha podido establecer una adecuada línea de base de la vigilancia entomológica que es el principal eje de acción propuesto de este proyecto. ENFERMEDADES METAXENICAS COMO UN PROBLEMA DE SALUD PÚBLICA Se estima que una gran parte de nuestro territorio (Costa, Amazonía, estribaciones y valles subtropicales Andinos y región Insular), presentan condiciones ambientales y ubicación geográfica propicias para la existencia y reproducción de vectores transmisores de enfermedades metaxénicas: Latitud 35 ºN a 35 ºS, altitud (msnm), temperatura ambiente (15 – 40ºC), humedad relativa (moderada a alta), pluviosidad (moderada a alta), tipo de vegetación y fauna, presencia de fenómenos climatológicos ocasionales (fenómeno del niño), calentamiento global.9 Otros factores que influyen para la persistencia de transmisión de estas enfermedades son: Pobreza, movimientos migratorios, asentamientos no planificados, viviendas precarias, falta de infraestructura sanitaria, déficit de agua potable o con disponibilidad intermitente, recolección inadecuada o inexistente de desechos sólidos, recipientes inservibles en los patios de las casas, valores culturales tradicionales, escaso conocimiento y participación comunitaria en actividades de prevención y control y comportamiento humano que influye en el modelo de transmisión vectorial correspondiente de las áreas endémicas de estas patologías.10 Los reservorios de estas enfermedades pueden ser humanos, animales o ambos y en nuestro país existen los tres tipos de acuerdo a cada patología. Por ejemplo, en el dengue se ha considerado que el reservorio es solo humano y la enfermedad no es susceptible al 9 Julio Álvarez Crespo, Historia de la Medicina Tropical Ecuatoriana, Vol. 1 Enfermedades Infecciosas y tropicales, de Gerrant (Edición 2002) 10 45 tratamiento por lo que no es factible cortar la transmisión de la enfermedad, pero adicionalmente existe un factor que no ha sido estimado, así desde el año 1996 por investigaciones científicas publicadas se ha confirmado la transmisión transovárica en el vector, lo que podría explicar la aparición explosiva de casos después de períodos de silencio epidemiológico, situación que indica que en nuestro país se deben realizar investigaciones relacionadas con este aspecto, puesto que incriminaría también al vector como reservorio de esta enfermedad.11 Otro aspecto a considerar es que las asignaciones presupuestarias a los Proyectos operativos de prevención y control no han sido suficientes para cubrir las reales necesidades operativas a nivel nacional, sobre todo los relacionados al Dengue, Leishmaniasis, Chagas y Fiebre Amarilla y además no se ha contado con la información científica derivada de la investigación nacional ya que esta es muy escasa o no existe y esto ha impedido que los programas se estructuren de acuerdo a nuestra realidad. Dado el carácter multifactorial de los modelos de transmisión y mientras las condiciones señaladas anteriormente se mantengan, las enfermedades metaxénicas continuarán siendo un problema de salud pública en nuestro país así como en todos los países con áreas tropicales y subtropicales del mundo, problemática que debe ser enfrentada a través de proyectos bien estructurados y con suficientes recursos económicos para actuar sobre aquellos factores que pueden ser modificables o susceptibles de controlar. 11 ta Lecture Notes on Tropical Medicine, de G. V. Gill y N: J. Beeching, 5 edición. 46 Figura 26: Árbol de Problema POBLACION EN RIESGO DE TRANSMISION DE ENFERMEDADES VECTORIALES EN EL ECUADOR Aumento de la morbi–mortalidad por dengue Persistencia de la transmisión de la malaria en el Ecuador Déficit de cobertura para la interrupción de la transmisión vectorial y Sub-registros de casos de Chagas Presencia de casos de Leishmaniasis cutánea y Subregistros de casos Incidencia de casos Fiebre Amarilla selvática en áreas urbanas Posible reintroducción del parasito ONCHOCERCA VOLVULUS en áreas endémicas para Oncocercosis. MORBI - MORTALIDAD POR ENFERMEDADES DE TRANSMISION VECTORIAL Presencia de vectores transmisores de enfermedades metaxénicas en el Ecuador Dispersión del mosquito Aedes aegypti transmisor del Dengue Presencia de focos de transmisión activa con dispersión de casos de paludismo Deficiencia de infraestructura higiénico-sanitaria Ineficiente manejo de desechos solidos Falta de Aplicación de las ordenanzas municipales por los gobiernos locales Condiciones socioeconómicasculturales desfavorables Inadecuada construcción de viviendas en zonas de riesgo Condiciones climatológicas adversas Falta de sensibilidad y poco compromiso de la ciudadana en la aplicación de medidas de prevención y control vectorial. Calentamiento global Desconocimiento del riesgo de transmisión de las enfermedades vectoriales Contaminación del medio ambiente Presencia del vector transmisor de la Enfermedad de Chagas Existencia del vector transmisor de la Leishmaniasis Riesgo de Urbanización de la transmisión del ciclo selvático de la Fiebre Amarilla por presencia del Aedes aegypti Interrupción de las actividades de vigilancia epidemiológica y entomológica para la certificación de la eliminación de la Oncocercosis. 47 Figura 27: Árbol de Objetivo CONTROL DEL RIESGO DE TRANSMISION DE ENFERMEDADES VECTORIALES EN LA POBLACION DEL ECUADOR Disminución de la morbi–mortalidad por dengue clásico y grave Aumento de cobertura para la interrupción de la transmisión vectorial y mejoramiento de los registros de casos de Chagas Fase de Preeliminación de la transmisión de la malaria en el Ecuador Disminución de casos de Leishmaniasis cutánea y mejoramiento en los registros de casos Evitar la incidencia de casos Fiebre Amarilla selvática en áreas urbanas Eliminar la reintroducción del parasito ONCHOCERCA VOLVULUS en áreas endémicas para Oncocercosis. DISMINUCION DE LA MORBI - MORTALIDAD POR ENFERMEDADES DE TRANSMISION VECTORIAL Prevención, control y vigilancia de los vectores transmisores de enfermedades metaxénicas en el Ecuador Controlar los índices de infestación del mosquito Aedes aegypti en las áreas de mayor riesgo de transmisión del Dengue en el Ecuador. Eficiente infraestructura higiénico-sanitaria Eficiente manejo de desechos solidos Fortalecimiento de la vigilancia epidemiológica para diagnostico precoz y tratamiento oportuno. Correcta aplicación de las ordenanzas municipales por los gobiernos locales Mejoramiento de las condiciones socio-económicasculturales Adecuada construcción de viviendas en zonas de riesgo Empoderamiento, sensibilización y compromiso de la ciudadanía en la aplicación de medidas de prevención y control vectorial. Conocimiento del riesgo de transmisión de las enfermedades vectoriales Pronostico oportuno de Condiciones climatológicas adversas las Calentamiento global Aplicación de medidas de control para disminuir los riesgos por Contaminación del medio ambiente Interrumpir la transmisión vectorial de la Enfermedad de Chagas en áreas prioritarias con vectores domiciliados a través de la vigilancia epi-entomológica permanente. Vigilancia epi-entomológica permanente para disminuir la transmisión de la Leishmaniasis cutánea Vigilancia y control de la dispersión del Aedes aegypti en localidades cercadas a áreas selváticas con riesgo de transmisión de Fiebre Amarilla. Sostenibilidad de las actividades de vigilancia epidemiológica y entomológica para la certificación de la eliminación de la Oncocercosis. 48 2.2 Línea Base del Proyecto de Vigilancia y Control de Vectores para la Prevención de la transmisión de enfermedades metaxénicas en el Ecuador Línea de base proyecto Control de Malaria 2012 El Índice Anual de Exploración Sanguínea (I.A.E.S) de 446.509 personas que se examinaron representan el 6% de la población en riesgo de transmisión 2012. El Índice Parasitario Anual (I.P.A). a nivel nacional de una población en riesgo de 7.821.223 representa el 0.07 por cada 1.000 habitantes. El índice de láminas positivas (I.L.P) de un total de 446.509 láminas tomadas, fue de 0.12%(558 casos). La frecuencia relativa de infecciones a P. falciparum (F.R.I.F) fue del 14.34% (80/478). Del total de los 478 casos de infecciones por P. vivax del país, aproximadamente el 80% se concentran en las Provincias de Guayas (43%), Los Ríos (14%), Orellana (16%) y Pastaza (8%) Del total de los 80 casos de infecciones por P. falciparum del país, aproximadamente el 85% se concentran en Esmeraldas (55%), Guayas (18%) y Los Ríos (13%). Línea de base proyecto Control de Dengue 2012 Índice de Breteau (número de depósitos con Aedes aegypti / número de casas inspeccionadas x 100) ha oscilado en un rango de 18.2%. Índice de casa (número de casas con Aedes aegypti / número de casas inspeccionadas x 100) de 11.5%. Incidencia de Dengue de los últimos 5 años, siendo 17.116 los casos reportados durante el año 2012. Figura 28: Incidencia de Dengue por Provincias Periodo 2008-2012 49 Línea de base proyecto Control de Leishmaniasis 2012 941 casos registrados en 22 provincias del Ecuador. 6 especies de leishmania identificadas en el país hasta el 2012. 822 personas capacitadas sobre cómo implementar normas de diagnósticos y tratamientos de la Leishmaniasis cutánea. Línea de base proyecto Control de Chagas 2012 76 casos de Chagas confirmados y tratados por los médicos de las Unidades Operativas de Salud. 23.277 casas visitadas de localidades vulnerables donde se realizó búsqueda, captura y clasificación del vector transmisor de la Enfermedad de Chagas. 21.993 unidades domiciliarias rociadas en el (intra y peridomiciliar) con insecticidas de acción residual. Línea de base proyecto Oncocercosis en el Ecuador 2012 Ceros casos de Oncocercosis en las 119 comunidades históricamente endémicas del Cantón Eloy Alfaro-Provincia de Esmeraldas como resultado de la cobertura total de tratamiento. Vigilancia Epidemiológica en los pobladores y vectores para identificar una posible reintroducción de la enfermedad y mantener la certificación de la eliminación de la enfermedad. o 68.311 simulidos (moscas) recolectados para estudios de PCR mediante evaluación entomológica en 4 comunidades centinelas y 4 comunidades extracentinelas. o Estudio PCR: Reacción en cadena de la polimerasa (Polymerase Chain Reaction), para detección del parasito Onchocerca volvulus en simulidos, cuyo resultado fue 0% de tasa de infectividad. Línea de base proyecto Control de Fiebre Amarilla 2012 Dos de casos de fiebre amarilla en la provincia de Napo. 232 Personas capacitadas en Vigilancia entomológica para la Fiebre Amarilla en las 6 provincias de las Amazónicas. 60 larvitrampas instaladas como complemento a la vigilancia entomológica, distribuidas en las 6 provincias de la amazonia. 2.4 Análisis de oferta y demanda El total de habitantes del país 14´483.499, hombres 7´177.683 y mujeres 7´305.816. Distribución: 61.1% población urbana y 38,9% población rural, de acuerdo al Censo Nacional efectuado en el año 2010. 50 Figura 29: Población del Ecuador Fuente: Censo de Población y Vivienda 2010 –INEC. Figura 30: Población por grupos de edades Fuente: Censo de Población y Vivienda 2010 –INEC. Demanda Referencial: tomando como referencia los 226 cantones que tiene el Ecuador (Censo de Población y Vivienda 2010-INEC), el área de influencia del proyecto se estima en 162 cantones que presentan condiciones ambientales propicias para el desarrollo de vectores transmisores de: Dengue, Malaria, Chagas, Leishmaniasis, Fiebre Amarilla y Oncocercosis en las regiones costa, amazónica, insular y valles subtropicales de la región Interandina con una población estimada de 8´811.167 habitantes que representan el 61% de la población total (datos estadísticos del SNEM). Tabla 21: Cantones con presencia de Enfermedades Metaxénicas PROVINCIAS CANTONES CARCHI IMBABURA ESMERALDAS SUCUMBIOS PICHINCHA NAPO ORELLANA 1 1 8 7 3 3 4 POBLACION REFERENCIAL 12.180 43.518 534.092 176.472 50.942 89.513 136.396 51 PASTAZA COTOPAXI CHIMBORAZO TUNGURAHUA MANABI STO. DOMINGO DE LOS TSACHILAS GUAYAS LOS RIOS STA. ELENA BOLIVAR GALAPAGOS AZUAY CAÑAR MORONA SANTIAGO EL ORO LOJA ZAMORA CHINCHIPE TOTAL 4 3 1 83.933 133.236 12.922 17.000 1.369.780 368.013 3.645.483 778.115 308.693 18.000 25.124 40.391 54.389 147.940 600.659 90.000 91.376 8´811.167 22 1 25 13 3 6 3 2 1 12 14 16 9 162 Fuente: Proyecto Control de Dengue, INEC 2010 Figura 31: Cantones con presencia de Enfermedades Metaxénicas Fuente: Proyecto Control de Dengue, INEC 2010 Tabla 22: Población Referencial por proyecto ENFERMEDADES METAXÉNICAS PROVINCIAS POBLACIÓN REFERENCIAL DENGUE MALARIA CHAGAS LEISHMANIASIS FIEBRE AMARILLA ONCOCERCOSIS 23 22 22 22 6 2 8´811.167 7´821.223 7´821.223 7´821.223 739.814 672.241 Fuente: Proyectos-SNEM, INEC 2010 52 Población demandante potencial de Control de Dengue se estima en 6´210.168 habitantes de los cantones y parroquias donde el proyecto va a intervenir con el componente 1: Vigilancia epidemiológica y entomológica fortalecida, para controlar y/o disminuir los índices de infestación del mosquito Aedes Aegypti y otros vectores transmisores de Dengue y Fiebre Amarilla, que corresponde al 70% de la población referencial, a partir del año 2015 se plantea cubrir las 7 ciudades que actualmente son intervenidas con el proyecto Participación comunitaria para el control biológico del Aedes aegypti con Bactivec. Población demandante potencial de Control de Malaria a pesar de los logros alcanzados en la lucha contra esta enfermedad, en el Ecuador existen las condiciones ambientales y demográficas favorables para la ocurrencia de esta enfermedad, por ende las estrategias de prevención y control deben fortalecerse para lograr la Pre-eliminación de la Malaria. Se estima una población demandante potencial para esta patología de 5´083.196 habitantes donde el proyecto intervendrá con el componente 2: Disminuida la incidencia de Malaria con IPA < 1 x 1000 habitantes en el Ecuador hasta el año 2017, que corresponde al 65% de la población referencial. Población demandante potencial para el Control de Chagas son las poblaciones que se encuentra en areas potenciales de transmisión de la Enfermedad de Chagas de las Regiones Amazónicas (Sucumbíos, Orellana, Napo, Pastaza, Morona y Zamora) y Extra Amazónicas (Guayas, Manabí, Los Ríos, Santo Domingo) que equivale el 41% de la población referencial donde se empleara la estrategia de la Ruta Inversa12 (estrategia mediante estudios serológicos en la población escolar de las localidades rurales donde existe el riesgo de transmisión de la Enfermedad de Chagas y si se detectan casos se realiza actividades de exploración y encuestas entomologías para la búsqueda, captura y clasificación de chinchorros). Población demandante potencial de Leishmaniasis corresponde al 40% de la población referencial en base a los factores de riesgos (medio ambiente, viviendas y demográficos) de las áreas rurales de las 22 provincias en riesgo. Población demandante potencial de Fiebre Amarilla la población que se encuentra potencialmente en riesgo de transmisión son las areas rurales y en segundo lugar las urbanas de la Región Amazónica donde se estima que bien alrededor de 452.664 habitantes. Población demandante potencial de Oncocercosis las zonas en riesgo identificadas para la ocurrencia de esta enfermedad es el Noroccidente de la Provincia de Esmeraldas y la Provincia de Santo Domingo de los Tsáchilas tomando en cuenta los factores ambientales y hábitat del vector. Se estima que la población en riesgo es de 26.684 personas que habitan en 119 comunidades localizadas en 18 parroquias, 5 Cantones y 2 Provincias. 12 Fuente: Libro “PROGRAMA REGIONAL PARA EL CONTROL DE LA ENFERMEDAD DE CHAGAS EN AMÉRICA LATINA” Carlos Antonio Silveira. 53 ENFERMEDADES METAXÉNICAS DENGUE MALARIA CHAGAS LEISHMANIASIS FIEBRE AMARILLA ONCOCERCOSIS Tabla 23: Población Potencial por proyecto POBLACIÓN PROVINCIAS HOMBRES POTENCIAL 23 6210168 3.042.982 22 5.083.196 2.490.766 22 1.418.943 695.282 22 1.402.500 687.225 6 452.664 221.805 2 26.684 13.075 Fuente: Proyectos-SNEM, INEC 2010 MUJERES 3.167.186 2.592.430 723.661 715.275 230.859 13.609 Población demandante efectiva corresponde al 100% de la población potencialmente en riesgo de transmisión de las enfermedades metaxénicas (Dengue, Chagas, Leishmaniasis, Malaria y Oncocercosis). OFERTA Las acciones de control de vectores de enfermedades metaxénicas en el Ecuador son realizadas por el Servicio Nacional de Control de Enfermedades Transmitidas por Vectores Artrópodos (SNEM), y hasta la actualidad es la institución responsable de este tipo de intervenciones a nivel del país. El proyecto de Participación comunitaria para el control biológico del Aedes aegypti mediante el uso de Bactivec (bacillus thuringiensis israelensis) se ejecuta para el control larvario en las ciudades de Guayaquil, Manta, Montecristi, Jaramijo, Machala, Huaquillas y Santo Domingo, lo que representa una población potencial de 712.505 viviendas (3´328.442 habitantes). Se debe indicar que en estas mismas ciudades es necesario ejecutar otras actividades para el control del mosquito adulto, mismas que se describen a continuación: 1. Control del mosquito Aedes aegypti mediante fumigación intradomiciliar con insecticida piretroides con equipo portátil. 2. Control del mosquito Aedes aegypti mediante fumigación con insecticida órgano fosforado espacial a ultra bajo volumen con máquinas montadas en vehículos. 3. Control del mosquito Aedes aegypti mediante fumigación peri domiciliar y en terrenos baldíos con termonebulizadoras con insecticida órgano fosforado. 4. Vigilancia epidemiológica 5. Vigilancia entomológica DEMANDA INSATISFECHA Después del análisis entre la demanda efectiva y la oferta de servicio se estableció que la demanda insatisfecha que existe para estas enfermedades vectoriales es igual que la demanda efectiva debido que no existe otra institución que ofrezca este tipo de intervenciones en el país. Se debe mantener la misma población de demanda insatisfecha debido que el proyecto de Participación comunitaria para el control biológico del Aedes aegypti mediante el uso de 54 Bactivec (bacillus thuringiensis israelensis) se enfoca en la participación comunitaria para efectuar el control del vector en su fase larvaria lo que no excluye la existencia del mosquito adulto que obliga al uso o empleo de otros métodos de control que se incluye en el presente proyecto. 2.5 Identificación y caracterización de la población objetivo El presente proyecto plantea cubrir la demanda insatisfecha en su totalidad considerando que no existe otro oferente, de acuerdo al siguiente detalle: Tabla 24: Población Objetivo del proyecto PROYECTO DENGUE MALARIA CHAGAS LEISHMANIASIS FIEBRE AMARILLA ONCOCERCOSIS POBLACIÓN OBJETIVO 6´210.168 5.083.196 1.418.943 1.402.500 452.664 26.684 Fuente: Proyectos-SNEM, INEC 2010 Ofreciendo los servicios que se describen a continuación: 1. Diagnóstico microscópico confirmatorio a pacientes clínicamente sospechosos de Malaria, Leishmaniasis y Enfermedad de Chagas, mediante la red de 286 puestos de diagnóstico. 2. Tratamiento oportuno a pacientes confirmados con Paludismo, Chagas y Leishmaniasis. 3. Control y seguimiento de pacientes para garantizar una adherencia adecuada al tratamiento de enfermedades metaxénicas con énfasis en Paludismo, Chagas y Leishmaniasis. 4. Aplicación de larvicida en las viviendas de las areas intervenidas por el proyecto para eliminación de la fase acuática del vector del Dengue; exceptuando el 70% de las ciudades de Manta, Montecristi, Jaramijó, Santo Domingo, Machala, Huaquillas y Guayaquil. 5. Fumigación de viviendas, terrenos baldíos y manzanas para la eliminación de vectores en estado adulto. 6. Rociado intra-domiciliar selectivo con insecticida de acción residual para control de enfermedades transmitidas por vectores con énfasis en Malaria y Chagas. 7. Entrega de mosquiteros tratados con insecticida de larga duración para evitar el contacto hombre-vectores. 8. Vigilancia y evaluación de las diferentes actividades realizadas para control vectorial. 9. Colocación de trampas en sitios centinelas de las áreas de riesgo en la amazonia para tener información oportuna de los mosquitos vectores 55 10. 11. 12. 13. 14. 15. haemagogus, sabethes y A. albopictus, transmisores de la fiebre amarilla selvática. Distribución de materiales de comunicación y educación para la salud, con contenidos de orientación comunitaria para prevención y control de enfermedades metaxénicas. Difusión a la comunidad sobre medidas de prevención de enfermedades transmitidas por vectores a través de medios de comunicación masivos. Acciones de comunicación y movilización social (ACMS) para la prevención y control de enfermedades metaxénicas en el Ecuador. Capacitación de los equipos de salud sobre, diagnóstico, tratamiento, vigilancia epidemiológica, vigilancia entomológica y medidas de prevención y control de enfermedades metaxénicas. Monitoreo y supervisión de actividades de vigilancia y control de los diferentes componentes del proyecto. Gestión para la adquisición, almacenamiento y dotación de medicamentos, equipos, maquinas, insecticidas e insumos utilizados para el tratamiento y control de las enfermedades transmitidas por vectores. 3. OBJETIVO DEL PROYECTO 3.1 Objetivo General y Objetivo Específicos. Objetivo General.Controlar y/o eliminar la transmisión de Enfermedades metaxénicas en las poblaciones que habitan en las zonas tropicales y sub tropicales del país mediante actividades de vigilancia epidemiológica y entomológica e intervenciones con participación intra e intersectorial y comunitaria. Objetivo específicos: Fortalecer la Vigilancia epidemiológica y entomológica, para controlar y/o disminuir los índices de infestación del mosquito Aedes Aegypti y otros vectores transmisores de Dengue y Fiebre Amarilla. Mantener la incidencia de Malaria IPA< 1 x 1.000 hasta el año 2017. Interrumpir la transmisión vectorial de la Enfermedad de Chagas en áreas con vectores domiciliados y ampliar la cobertura para el diagnóstico precoz y tratamiento oportuno de los casos detectados. Disminuir la incidencia de la Leishmaniasis cutánea mediante promoción y prevención fundamentadas en la vigilancia epidemiológica integral en áreas endémicas de transmisión del país. Mantener en cero los casos de Oncocercosis y la certificación definitiva de la eliminación de la Enfermedad. 56 3.2 Indicadores de Resultado: Disminución del índice de breteau en áreas de riesgo en ≤ 5 hasta el año 2017. Disminución del índice de casa en áreas de riesgo ≤ 3 hasta el año 2017. Mantener el IAES (INDICE ANUAL DE EXPLORACION SANGUINEA) entre 6% a 8% hasta el año 2017. Mantener el ILP (INDICE DE LAMINAS POSITIVAS) < 1 hasta el año 2017. Mantener una cobertura por encima de 15.000 muestras serológicas tomadas para detectar la Enfermedad de Chagas anualmente hasta el año 2017. 100% de los casos confirmados de la Enfermedad de Chagas tratados hasta el año 2017. Disminución de los índices de infestación de triatominos en el intra y peri domicilio a cero hasta el año 2017. Disminución de la incidencia de Leishmaniasis < 20% hasta el año 2017. 15 áreas endémicas intervenidas en promoción para la salud y prevención de la transmisión de la Leishmaniasis hasta el año 2017. Índice de transmisión del Onchocerca volvulus (enfermedad eliminada) < 0.05 % hasta el año 2017. 57 Tabla 25: MATRIZ DE MARCO LOGICO 2013-2017 Resumen Narrativo de Objetivos Indicadores Verificables Objetivamente Medios de Verificación Supuestos FIN: Disminución de la incidencia del Dengue no menos de un 40% al 2017 en relación al histórico de los últimos 5 años Mantener la incidencia de Malaria IPA< 1 x 1.000 100% de pacientes confirmados con Chagas y tratados Reducir el riesgo de adquirir enfermedades metaxénicas, basado en la garantía de los derechos de salud. SIVE ALERTA, fichas epidemiológicas e historias clínicas SIVE MAE 2, SIVE ALERTA, formularios OC19, Fichas epidemiológicas y control de calidad Pruebas confirmatorias INSPI, fichas epidemiológicas e historias clínicas Fenómenos climatológicos adversos , no aumentan inesperadamente los casos de Dengue Fenómenos climatológicos adversos como el Fenómeno del Niño, no aumentan inesperadamente los casos de malaria Accesibilidad al tratamiento y adherencia del 100% por parte de los pacientes Accesibilidad al tratamiento y adherencia del 100% por parte de los pacientes Vacunación anti amarilica del 100 % de la población en zonas endémicas e implementación de la vigilancia entoepidemiológica de los vectores de la fiebre amarilla 100% de los casos diagnosticados y tratados con Leishmaniasis Fichas epidemiológicas e historias clínicas Incidencia de Fiebre Amarilla en Cero SIVE ALERTA, fichas epidemiológicas e historias clínicas Incidencia Oncocercosis en Cero Entregar informes a las comunidades el éxito de la eliminación de la enfermedad y cierre del proyecto Participación activa de los actores para actividades de vigilancia entomológica Formularios AA2A para verificación Formularios AA2A para verificación SIVE MAE 2 y formularios OC19 Disponibilidad de recursos humanos e insumos Disponibilidad de recursos humanos e insumos Disponibilidad de recursos humanos e insumos. PROPÓSITO (u Objetivo General): Controlar y/o eliminar la transmisión de Enfermedades metaxénicas en las poblaciones objeto de acción del proyecto mediante actividades de vigilancia epidemiológica y entomológica e intervenciones con participación intra e intersectorial. Disminución del índice de breteau en áreas de riesgo en ≤ 5 Disminución del índice de casa en areas de riesgo en ≤ 3 IAES (INDICE ANUAL DE EXPLORACION SANGUINEA) entre 6% a 8% 58 ILP (INDICE DE LAMINAS POSITIVAS) < 1 SIVE MAE 2, formularios OC19 y Control de calidad Disponibilidad de insumos. Disminución de los índices de infestación de triatominos en el intra y peri domicilio a cero Formularios de visitas entomológicas Disponibilidad de recursos humanos e insumos 15 areas endémicas intervenidas en promoción para la salud y prevención de la transmisión de la Leishmaniasis Informes de actividades verificables Cambio de comportamiento para prevenir el contacto hombre-vector Índice de transmisión del Onchocerca volvulus (enfermedad eliminada) < 0.05 % Informes de vigilancia epidemiológica y entomológica Participación activa de los actores para actividades de vigilancia epidemiológica y entomológica Disminución de los Índices aedicos Formularios AA2A para verificación Disponibilidad de recursos humanos e insumos Cero casos de Malaria hasta el año 2017 SIVE MAE 2, SIVE ALERTA, formularios OC19, Fichas epidemiológicas y control de calidad Fenómenos climatológicos adversos como el Fenómeno del Niño, no aumentan inesperadamente los casos de malaria 15.000 muestras serológicas anuales tomadas para detectar la Enfermedad de Chagas anualmente hasta el año 2017 Informe y registro del muestreo Disponibilidad de recursos humanos e insumos. 100% casos confirmados de la Enfermedad de Chagas tratados hasta el año 2017 Fichas de pacientes Disponibilidad de medicamento y profesionales con amplios conocimientos en enfermedades vectoriales. 15.000 Unidades Domiciliarias inspeccionadas, rociadas y número de triatominos capturados e identificados en localidades programadas anuales hasta el 2017 Informe entomológico Personal adecuado para el puesto de trabajo COMPONENTES (resultados u objetivos específicos): COMPONENTE U OBJETIVO ESPECIFICO UNO Vigilancia epidemiológica y entomológica fortalecida, para controlar y/o disminuir los índices de infestación del mosquito Aedes Aegypti y otros vectores transmisores de Dengue y Fiebre Amarilla. COMPONENTE U OBJETIVO ESPECIFICO DOS Disminuida la incidencia de Malaria con IPA < 1 x 1000 habitantes en el Ecuador hasta el año 2017 COMPONENTE U OBJETIVO ESPECIFICO TRES Transmisión vectorial de la Enfermedad de Chagas interrumpida en áreas con vectores domiciliados y mejorando la detección y tratamiento oportuno de casos COMPONENTE U OBJETIVO ESPECIFICO CUATRO 59 Disminuida la incidencia de la Leishmaniasis cutánea mediante promoción y prevención fundamentadas en la vigilancia epidemiológica integral y educación para la salud en áreas endémicas de transmisión del país. Disminución de la incidencia de Leishmaniasis < 20% hasta el año 2017. Informes de actividades Educación y participación activa de la población para evitar contacto hombrevector y domiciliación COMPONENTE U OBJETIVO ESPECIFICO QUINTO Eliminación de la Oncocercosis Certificada parte de la OMS año 2013 ACTIVIDADES 1.1 Visitas domiciliarias para eliminación de criaderos de Aedes aegypti en fase larvaria integrando a la familia 1.2 Fumigación intradomiciliar de viviendas para el control del mosquito Aedes aegypti y otros en fase adulta 1.3 Fumigación de Manzanas con máquinas de ultra bajo volumen para el control del mosquito Aedes aegypti y otros en fase adulta 1.4 Estudios de la eficacia de los plaguicidas utilizados para el control vectorial 1.5 Talleres de capacitación sobre el manejo clinico de pacientes con Dengue dirigido a los equipos de salud a nivel nacional 1.6 Implementar puestos para vigilancia entomológica y monitoreo de vectores de dengue y fiebre amarilla 1.7 Difusión de medidas de prevención y control del dengue 1.8 Edu-comunicación a nivel intra e intersectorial, para ejecutar medidas de prevención y control del dengue 1.9 Talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento en enfermedades metaxénicas al personal del Sector Salud y equipos multidisciplinario 1.10 Sala de entrenamiento de manejo de pacientes con dengue Entregar informes a las comunidades el éxito de la eliminación de la enfermedad y cierre del proyecto MEDIOS DE VERIFICACION 34 visitas multiprósito ejecutadas en localidades programadas PRESUPUESTO TOTAL 2013 2014 2015 2016 Disponibilidad económica oportuna SUPUESTOS 2017 57.706.372 6.827.917 9.281.071 13.050.793 13.849.501 14.697.091 Formularios para registro de visitas domiciliarias Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 17.353.882 1.532.968 3.972.011 3.717.483 3.944.993 4.186.427 Formularios para registro de casas fumigadas Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 3.371.747 496.646 602.327 713.062 756.701 803.011 Formularios para registro de manzanas fumigadas Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 166.826 70.016 49.000 15.000 15.918 16.892 Informe de Estudio de susceptibilidad Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 587.990 104.760 111.171 116.730 123.874 131.455 Informe de actividades, registro de asistencia y fotos. Profesionales con amplios conocimientos en enfermedades vectoriales. 60.337 10.750 11.408 11.978 12.711 13.489 Informe de puestos de vigilancia instalados Personal Técnico con amplia experiencia y conocimiento y flujo financiero adecuado 271.241 20.000 60.000 60.000 63.672 67.569 Contratos 70.047 12.480 13.244 13.906 14.757 15.660 Informe de actividades, actas de compromisos y fotos. Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 579.381 66.800 114.800 124.800 132.438 140.543 Informe de actividades, registro de asistencia y fotos. Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 20.000 0 0 Informe del Personal de salud capacitado Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 20.000 0 0 60 Monitoreo de mensajes educativos en medios de comunicación contratados 1.11 Control vectorial de casos de Dengue (control de focos y brotes) 1.12 Monitoreo y Supervisión de actividades de prevención y control del Dengue TOTAL COMPONENTE 1 2.1 Toma de muestra hemática a febriles sospechosos de paludismo y adopción de esquemas terapéuticos altamente eficaces 86.934 0 6.496.828 1.149.756 86.771.584 10.292.093 20.000 21.000 22.285 1.220.121 1.294.792 1.374.034 15.475.153 19.139.544 20.310.884 1.488.602 421.485 243.500 258.402 274.216 2.2 Fortalecimiento del Sistema de Gestión de calidad del diagnóstico microscópico de malaria. 116.425 12.600 37.500 26.530 19.898 2.3 Monitoreo, Supervisión y Evaluación de actividades de campo en la vigilancia epientomológica para malaria 183.894 32.544 34.536 36.649 38.892 39.328 6.960 7.386 7.838 8.318 2.4 Control de brotes de malaria 23.649 Análisis de Casos de Dengue 1.458.125 Informe de actividades Se fortalecen las actividades de Formularios OC 19 (Registro diagnóstico y tratamiento por las 290.998 de muestras hemáticas instituciones prestadoras de servicios de tomadas) salud Informes de evaluaciones Red de laboratorio adecuadamente pre y post test. Informe de diagnosticando casos de paludismo. 19.898 Evaluación de Evaluación de competencias competencias. desarrollada. Profesionales con amplios 41.272 Informe de actividades conocimientos en enfermedades vectoriales. 8.827 Informe de control de brote 1.336.630 387.944 411.686 260.000 179.000 98.000 2.6 Vigilancia epidemiológica para la eliminación de la malaria 1.941.322 200.305 423.164 413.464 438.768 465.621 690.207 198.530 155.840 95.377 131.215 109.245 46.648 3.000 5.400 12.000 12.734 13.514 1.056.715 3.600 240.305 255.012 270.618 287.180 79.109 14.000 14.857 15.766 16.731 6.978.880 1.280.968 1.574.173 1.381.038 1.390.390 2.8 Reuniones semestrales de análisis epidemiológico de malaria con los niveles correspondientes 2.9 Caracterización de focos de transmisión: nuevo potencial, nuevo activo, activo residual, residual no activo, endémicos y libres de transmisión 2.10 Vigilancia Entomológica de Malaria TOTAL COMPONENTE 2 Profesionales con amplios conocimientos en enfermedades vectoriales 21.553.910 2.5 Distribución de mosquiteros según requerimiento epidemiológico 2.7 Rociado de viviendas para control casos de malaria Equipo Técnico cuenta con la información necesaria Formularios de entrega de mosquiteros, formulario de monitoreo de mosquiteros, hojas de egreso y kardex Informe de actividades, registro de asistencia y fotos. Formularios R1 (Registro de Casas Rociadas) Informes de reunión, rutinas de análisis epidemiológicas Informes de focos investigados, formularios de investigación completa y registros de mapas 17.755 Informes, protocolos. 1.352.309 61 Brotes adecuadamente controlados Se fortalecen las acciones de mejoramiento de cobertura con MTI Personal Técnico con experiencia Personal adecuado para el puesto de trabajo Oportuno trabajo coordinado con los equipos zonales responsable del componente Vigilancia entomológica desarrollada en pre-eliminación Vigilancia entomológica desarrollada en pre-eliminación 3.1 Creación a nivel zonal de núcleos de trabajo para priorizar distritos, orientar acciones para la detección y manejo de casos (prioridad niño), aplicación de manuales de normas y procedimientos (protocolos) de diagnóstico, tratamiento etiológico y manejo de las complicaciones cardiacas y/o digestivas además identificar probables brotes de chaguas por vía oral. 3. 2 Fortalecer la capacidad de laboratorio a nivel distrital y/o zonal en métodos parasitológicos para el diagnóstico de Chagas agudo, serológicos y confirmatorios. 3.3 Dar continuidad al tamizaje universal en donantes de sangre optimizando calidad en las acciones y correcta derivación del paciente para confirmación diagnóstica y atención médica. 3.4 Garantizar disponibilidad del medicamento para tratamiento etiológico 3.5 Vigilancia entomológica integral funcionando para el fortalecimiento de la capacidad de respuesta local, protocolos de encuestas triatominicas para estandarizar su aplicación y levantamiento de líneas de base. 3.6 Acciones de comunicación y movilización social para fortalecer la vigilancia entomológica de notificación de triatominos, con participación comunitaria (actores sociales y locales) 3.7 Monitoreo y Supervisión de actividades de campo y de vigilancia ento-epidemiológica para Chagas TOTAL COMPONENTE 3 4.1 Vigilancia y monitoreo entomológicos del vector trasmisor de Leishmaniasis en las zonas endémicas del país 4.2 Diagnóstico oportuno de los pacientes positivos para su tratamiento Informes y actas de 790.437 0 180.366 191.404 203.118 248.971 22.400 51.700 54.864 58.222 61.785 21.912 0 5.000 5.306 5.631 5.975 8.000 0 0 8.000 0 2.463.377 174.111 522.376 554.345 588.271 43.824 0 10.000 10.612 11.261 72.044 12.780 13.562 14.392 15.273 3.648.565 209.291 783.004 838.924 881.776 98.434 17.420 18.486 19.617 20.818 884.084 156.458 166.033 176.194 186.978 trabajo. Aprobación de la creación de los núcleos de trabajo en las coordinaciones zonales. Informes y registros diagnóstico Laboratorial. Actas de conformación de equipos técnicos para el diagnóstico laboratorial. Informes de cruz roja y bancos de sangre Actas de convenios aprobados por la autoridad competente. 215.549 creación de núcleos de Informes de balances de 0 medicamentos antichagasicos 624.274 Informes y registros entomológicos. Informes y registros de 11.951 actividades de comunicaciòn social Informe y analisis de las 16.037 actividades de monitoreo y supervisión 935.570 22.092 Informe de # ejemplares de cada especie capturados 198.421 Registro contable 62 Certificaciones de disponibilidad económica y existencia del medicamento en el mercado internacional. Disponibilidad económica para contratación de Talento Humano y compra de insumos. Disponibilidad econòmica Profesionales con amplios conocimientos en enfermedades vectoriales. Condiciones atmosféricas desfavorables y alteraciones del hábitat (deforestación, fumigaciones etc.) Monitoreo de mensajes educativos en medios de comunicación contratados 4.3 Evaluación y Capacitación a los profesionales de Salud en diagnóstico, tratamiento, vigilancia y medidas de prevención y control de la Leishmaniasis. 75.436 4.4 Actualización del personal Microscopistas en el diagnóstico de Leishmaniasis cutánea por examen directo de la lesión 42.380 4.5 Coordinación intra e intersectorial, para ejecutar medidas de prevención y control en base a los datos de la vigilancia 17.856 3.160 3.353 3.559 3.776 4.6 Monitoreo y Supervisión del Componente logístico y técnico 30.796 5.450 5.784 6.137 6.513 6.912 Informe de actividades Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 136.907 0 31.240 33.152 35.181 37.334 Informe de actividades Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 1.285.891 203.338 247.022 262.140 278.183 89.193 89.193 0 0 0 89.193 89.193 98.774.113 12.074.883 0 18.079.353 0 21.621.646 0 22.861.234 4.7 Edu-comunicación a la comunidad en areas de riesgo en los métodos de prevención contacto hombre-vector TOTAL COMPONENTE 4 5.1 Visitas Comunitarias Multipropósito a las comunidades bajo Vigilancia Epidemiológica para Oncocercosis TOTAL COMPONENTE 5 TOTAL PROYECTO Listas de asistencia del 13.350 14.167 15.034 15.954 16.931 personal capacitados, fotos, Disponibilidad económica deficiente informes Informe de actividades, 7.500 7.959 8.446 8.963 9.512 registro de asistencia y fotos. Informe de actividades, 4.008 actas de compromisos y fotos. Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 295.208 0 Informe de actividades 0 24.136.998 63 Personal Técnico con amplia experiencia, conocimiento y flujo financiero adecuado 4. VIABILIDAD Y PLAN DE SOSTENIBILIDAD 4.1 Viabilidad técnica COMPONENTE 1. Vigilancia epidemiológica y entomológica fortalecida, para controlar y/o disminuir los índices de infestación del mosquito Aedes Aegypti y otros vectores transmisores de Dengue y Fiebre Amarilla. El Dengue en el Ecuador persiste como uno de los principales problemas de salud pública al igual que en otros países de América y del mundo donde el control de la enfermedad no ha sido posible. Esta situación es preocupante si consideramos que existe una condición de híper – endemicidad viral con la circulación de los 4 serotipos del virus del dengue, la gran dispersión con altos índices de infestación vectorial y la presencia de factores ambientales, socio-económicos y culturales en las poblaciones de áreas tropicales, subtropicales de las regiones Costa, Sierra (valles interandinos), Amazonía y Galápagos que propician y perpetúan la transmisión de la enfermedad. No obstante los esfuerzos realizados durante muchos años por el MSP, el Dengue mantiene un comportamiento endémico-epidémico hasta los actuales momentos, destacándose entre los posibles factores causales de esta situación los siguientes: a) La programación de las actividades no se han ajustado a las reales necesidades operativas de control del Aedes aegypti en el país por restricciones económicas, b) La persistencia de la transmisión de enfermedad obedece a factores de carácter: sociales, económicos, culturales y ambientales, sobre los cuales el proyecto no puede o incide en forma mínima. Por las razones expuestas y sin superponerse al proyecto comunitario de control del Aedes aegypti con biolarvicida, se propone la ejecución de un plan que considere acciones ajustadas a las reales necesidades operativas a nivel nacional que aunque represente una mayor inversión para el estado, sirva para controlar de manera eficaz la transmisión de la enfermedad y/o reducir al mínimo el impacto de probables epidemias de Dengue en el país, basado en las actividades que son parte habitual de los programas de control y que se describen a continuación: Visitas domiciliarias para eliminación de criaderos de Aedes aegypti en fase larvaria con participación activa de la comunidad. Fumigación intradomiciliar de viviendas para el control del mosquito Aedes aegypti y otros en fase adulta. Fumigación de Manzanas con máquinas de ultra bajo volumen para el control del mosquito Aedes aegypti y otros en fase adulta. Monitoreo y supervisión de actividades de prevención y control del Dengue. Estudios de la eficacia de los insecticidas utilizados para el control vectorial. Capacitación sobre el manejo clínico de pacientes con Dengue dirigido a los equipos de salud a nivel nacional. 64 Implementación de puestos de Vigilancia Entomológica para la detección de vectores de dengue y fiebre amarilla. Difusión de medidas de prevención y control del dengue. Educación y comunicación a nivel intra e intersectorial, para ejecutar medidas de prevención y control del dengue. Talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento en enfermedades metaxénicas al personal del Sector Salud y equipos multidisciplinario Sala de entrenamiento de manejo de pacientes con dengue. Control vectorial de casos de Dengue (Control de focos y brotes) 1.1 Visita domiciliarias para eliminación de criaderos de Aedes aegypti en fase larvaria con participación activa de la comunidad. ACTIVIDAD METODOLOGÍA INSUMOS DESCRIPCIÓN DE REQUERIMIENTOS 634 Bachilleres para el año 2013 797 Bachilleres para el año 2014 Contratación de recursos 1375 Bachilleres para el año 2015 humanos 1375 Bachilleres para el año 2016 Visita 1375 Bachilleres para el año 2017 personalizada casa a casa por Adquisición de Temephos Temephos al 1% GT. 1.1 Visitas el visitador. Las al 1% domiciliarias para adquisiciones Piquetas, mochilas, linternas, pilas, pipetas, eliminación de se harán a viales para toma de muestras larvarias, tableros, criaderos de través de los crayones, lápices, tizas, esferográficos, lupa, Herramientas de trabajo Aedes aegypti en procesos de flexómetro, calculadora, borradores, cucharas, fase larvaria con portal de tachos, cuadernos, formularios, alcohol, frascos participación compras y materiales educativos. activa de la públicas y la Uniformes de campo y Uniformes completos, gorras, chalecos, comunidad. contratación administrativos camisetas del personal a Prendas de protección Mascarillas, botas, cascos, guantes través de la red socio empleo Vehículos (combustible, Mantenimiento de Adquisición de 40 Camionetas 4x4 vehículos, repuestos, pago de seguro) Metodología de inspección de viviendas para trabajos de control del Aedes aegypti Toda persona que trabaje como visitador dentro en el proyecto de control del Aedes aegypti debe cumplir las siguientes obligaciones: a) Descubrir criaderos de Aedes aegypti. b) Destruir los criaderos de Aedes aegypti. c) Capacitar a las familias para evitar la formación de criaderos de Aedes aegypti. Ingreso a la vivienda Para entrar a una vivienda el visitador debe anunciar su visita llamando a la puerta de la casa, saludando cortésmente, explicando el motivo de su presencia y pidiendo permiso para realizar la visita a nombre del MSP, actividad que siempre debe ser realizada con personas adultas a quienes adicionalmente presentará su carnet de identidad. 65 Secuencia de la visita Concedido el permiso para la visita, el visitador iniciará la inspección, siempre por el fondo de la casa o sea el patio, para seguir por la cocina y recorrer luego el comedor y las demás dependencias de la casa. En las inspecciones al interior de las habitaciones, el visitador deberá pedir siempre a una de las personas de la casa que haga el favor de acompañarlo, principalmente a las alcobas privadas. En las piezas de vivienda común, en los cuartos de los hoteles, pensiones, hospedajes, etc. en los baños o inodoros siempre deberá tocar la puerta y anunciar su entrada. Inspección de criaderos Todos los recipientes que contengan o pudieran contener agua deberán ser cuidadosamente examinados, debiendo suponerse siempre que cualquiera de ellos puede constituir un criadero o foco de mosquitos. Los criaderos inspeccionados positivos o negativos deben ser registrados en el respectivo formulario en base a la siguiente clasificación. 1.- Tanques elevados. 2.- Tanques bajos: de metal, plástico o cemento 3.- Depósitos de barro 4.- Barriles, toneles, tinas de madera o 5.- Depósitos artificiales, especiales diversos. 6.- Llantas 7.- Canales de los techos 8.- Árboles y plantas bromeliáceas u otras semejantes. 9.- Pozos y aljibes 10.-Otros depósitos, pozos negros Destrucción y tratamiento de criaderos y/o Depósitos. El tratamiento de un foco o criadero será hecho tratando el depósito con el larvicida usado por el proyecto, o bien con la destrucción del depósito, si este es inservible, mediante el uso de la piqueta. Dosificación del larvicida El temephos en su formulación en granos de arena, tiene excelente acción larvicida residual, con una persistencia promedio de 90 días, que bajo ciertas circunstancias puede ser más larga. Sin embargo por razones operacionales y debidas a las agresiones que sufre el insecticida, conviene repetir cada dos meses el tratamiento de los depósitos de agua en las casas. El temephos es utilizado como larvicida en los depósitos de agua para uso doméstico, inclusive agua de beber en una concentración de 1 ppm (una parte por millón). La dosis básica es de 1 gramo por cada 10 litros de agua. (Ver anexo actividad 1.1) 66 Terminada la inspección, el visitador dará un mensaje educativo orientado a promover que las familias se encarguen de evitar que el vector del Dengue se reproduzca en sus viviendas y que deben de hacer en caso de que alguien se enferme, luego saldrá de la vivienda y entrará en la siguiente casa que debe inspeccionar, tomando en consideración todo lo indicado anteriormente. El visitador nunca debe pasar de una propiedad a otra aprovechando la existencia de cualquier comunicación interior que exista entre ellas. En cada una de las visitas el visitador mantendrá reuniones de carácter educativo con los habitantes de las viviendas a fin de promover cambios de conducta de riesgo e inducir a las personas para que progresivamente asuman la responsabilidad de controlar el Aedes aegypti en sus casas con la intencionalidad final de que el control de este vector se realice de manera exclusiva solo con actividades de tipo físico realizadas por ellos y sin la necesidad de utilizar productos biológicos o químicos, objetivo que se pretende alcanzar de manera progresiva, aceptándose una participación gradual de las personas en un rango de 30 a 45 % al final del proyecto en el año 2017. Alcanzar este nivel de éxito es difícil y complejo en razón de que depende de varios factores que influyen en el logro de una respuesta favorable de parte de la comunidad, entre los cuales se pueden considerar aspectos relacionados a los emisores del mensaje educativo, los inherentes a la cultura y disposición de las personas que receptan la información y los de carácter ambiental, económicos y sociales que influyen en el comportamiento de las personas Los procesos de adquisición del larvicida temephos al 1%, vehículos e insumos necesarios para que los visitadores e inspectores desarrollen su actividad de manera adecuada se efectuarán a través del portal de compras públicas, mientras que la contratación del personal se realizará a través de la red socio empleo. Para más detalle de la metodología de la actividad, ver anexo 1.1 1.2 Fumigación intradomiciliar de viviendas para el control del mosquito Aedes aegypti y otros en fase adulta ACTIVIDAD METODOLOGÍA Fumigación intradomiciliar de viviendas. Las 1.2 Fumigación adquisiciones se intradomiciliar de harán a través de viviendas para el los procesos de control del portal de compras mosquito Aedes públicas y la aegypti y otros en contratación del fase adulta personal a través de la red socio empleo INSUMOS Contratación de recurso humano DESCRIPCIÓN DE REQUERIMIENTOS 303 Bachilleres para el año 2013 276 Bachilleres para el año 2014 392 Bachilleres para el año 2015 392 Bachilleres para el año 2016 392 Bachilleres para el año 2017 Adquisición de Deltametrina líquida al 2,5% Deltametrina líquida al 2,5% Herramientas de trabajo Mochila, tablero, formulario, lápices, borrador, esferográfico, franela, detergente, crayones Uniformes de campo y administrativos Uniformes completos, gorras, chalecos, camisetas Prendas de protección Mascarillas, botas, cascos, guantes, protectores de oído 67 Metodología de Fumigación intradomiciliar de viviendas para el control del Aedes aegypti La fumigación de los patios y el interior de las viviendas (fumigación intradomiciliar) es la medida más recomendada durante las epidemias de Dengue y consiste en la aerolización o aplicación de un insecticida líquido en forma de millones de gotas diminutas de 0,1 a 50 micras (tamaño óptimo de 15 a 20 μm), que permanecen suspendidas en el aíre por un período de 2 a 3 horas período en el cual al ponerse en contacto con los mosquitos los eliminan. La velocidad de caída de las gotitas depende de su masa; por ejemplo una gotita de 20 μm de diámetro cae a 0,012 metros por segundo, de manera que tarda 14 minutos en descender 10 metros en el aire quieto, mientras que las gotitas de 100 μm descienden a 0,279 metros por segundo y tardarán sólo 36 segundos en recorrer la misma distancia. Todas las personas que intervienen en actividades de fumigación intradomiciliar deben llevar ropa, guantes y gafas protectores para evitar el contacto con el insecticida y posibles intoxicaciones. Dado que las gotas pulverizadas son tan pequeñas que se pueden inhalar, el operador debe utilizar una mascarilla adecuada, cuyo filtro se ha de cambiar periódicamente de acuerdo con las instrucciones del fabricante. El equipo impulsado por un motor es muy ruidoso, de manera que el operador debería tener los oídos protegidos. Las máquinas que se utilizan ara esta actividad son portátiles y pequeñas, con un peso de 6-11 kg, impulsadas por un motor eléctrico y su caudal de 1- 4 litros por hora, se controla mediante una válvula dosificadora. El personal que realiza este trabajo requiere capacitación sobre las medidas de seguridad que se han de adoptar. Se aplican varias normas: Cortar toda la corriente eléctrica en el interruptor principal. Apagar la cocina y esperar a que se enfríe antes de pulverizar. Proteger todos los recipientes de agua y los productos alimenticios de la vivienda a fumigar. Cubrir los recipientes con peces. Asegurarse de que todos los ocupantes y los animales estén fuera de la casa durante la fumigación y que permanezcan fuera hasta 30 minutos después de su conclusión. Garantizar que se ventile la casa antes de volver a entrar en él. Cerrar todas las puertas y ventanas antes de la pulverización y mantenerlas así hasta 30 minutos después de su conclusión, para garantizar una eficacia máxima. Los operadores encargados de la fumigación deben caminar hacia atrás, alejándose de la niebla, para reducir al mínimo la exposición. En edificios pequeños de un solo piso se puede pulverizar desde la puerta de entrada o por una ventana abierta sin tener que entrar en todas las habitaciones del mismo, siempre que se pueda conseguir una dispersión adecuada de las gotitas de insecticida. En edificios grandes de un solo piso puede ser necesario pulverizar habitación por habitación, comenzando por la parte trasera del edificio y avanzando hacia la delantera. 68 En edificios de varios pisos, la pulverización se realiza desde el piso superior hacia la planta baja y desde la parte trasera del edificio hacia la delantera. Esto garantiza en todo momento la buena visibilidad del operador. En teoría, debe hacerse un mínimo de tres tratamientos sucesivos a intervalos máximos de 7 días si se desea que el virus sea eliminado tanto de humanos como de mosquitos, siendo necesaria la evaluación entomológica para valorar el grado de reducción de la población de mosquitos antes y después de la(s) aplicación(es). Para más detalle de la metodología de la actividad, ver anexo 1.2. 1.3 Fumigación de Manzanas con máquinas de ultra bajo volumen para el control del mosquito Aedes aegypti y otros en fase adulta ACTIVIDAD METODOLOGÍA Fumigación de Manzanas con 1.3 Fumigación máquinas montadas de Manzanas con en vehículos desde máquinas de la calle. Las ultra bajo adquisiciones se volumen para el harán a través de los control del procesos de portal mosquito Aedes de compras públicas aegypti y otros en y la contratación del fase adulta personal a través de la red socio empleo INSUMOS Contratación de recurso humano Adquisición de Malathion Líquido al 96% G.T, Herramientas de trabajo Uniformes de campo y administrativos Prendas de protección Maquinarias y repuestos Vehículos ( combustible, Mantenimiento de vehículos, repuestos, pago de seguro) DESCRIPCIÓN DE REQUERIMIENTOS Bachilleres Malathion Líquido al 96% G.T, Tableros, formularios, lápices, borradores, esferográficos, franela, detergente, jabón, protectores de oído Uniformes completos, gorras, chalecos, camisetas Mascarillas, botas, cascos, guantes máquinas UBL arrastre y kit de repuestos Camionetas 4x4 Metodología de Fumigación de manzanas para el control del Aedes aegypti La fumigación de manzanas se realiza a través de máquinas o equipos pesados instalados en vehículos que fraccionan y lanzan un chorro de insecticida desde el nivel del suelo con gotas muy pequeñas de volumen ultra reducido o de ultra bajo volumen (UBV), cubriendo fácilmente una faja de 90 metros de ancho, mismas que caen lentamente con desplazamientos laterales permitiéndoles penetrar a los patios posteriores y al interior de las viviendas En la actualidad es uno de los métodos más empleados para el control de mosquitos en fase adulta que transmiten enfermedades como el Dengue y la Malaria y además se utiliza para el control del mosquito culex, que sin estar involucrado en la transmisión de enfermedades en nuestro medio por ahora, constituyen una amenaza potencial, en razón de que son transmisores de otras patologías que pueden presentarse en cualquier momento (Encefalitis de San Luís, Encefalitis Venezolana, Virus del Nilo Occidental entre las principales) y porque adicionalmente son los insectos que mayores problemas de molestia pública ocasionan a la comunidad. 69 Las personas que intervienen en actividades de fumigación de las manzanas, (chofer y operador), deben llevar ropa, guantes y gafas protectores para evitar el contacto con el insecticida y posibles intoxicaciones, utilizar mascarillas adecuadas para gases cuyo filtro se ha de cambiar periódicamente y utilizar protectores de oídos debido a que el motor es muy ruidoso. Para la ejecución de la actividad se deben tener en consideración varios aspectos técnicos: Descarga ml/ minuto: calibrar la máquina para que aplique 127 ml de insecticida por minuto (4.3 onzas fluidas/minuto) (En el caso de Malathión líquido al 96% G.T.) Velocidad del vehículo: usualmente 10 km/hora o 100 m en 36 segundos; (6.2 millas/hora). El tiempo teórico para rodear una manzana de 90 x 90 cm, sin interrupciones es de 2 minutos y 40 centésimos. Horario de las aplicaciones: de preferencia dentro de los siguientes periodos: 05H30 a 09H30 am y de 05H00 a 09H00 pm. Este horario no está relacionado con las horas actividad del vector sino con los periodos del día en que las condiciones climáticas son más favorables. Temperatura del insecticida: no deberá sobrepasar los 35 °C (95°F) para disminuir el riesgo de que las gotas menores se eleven a las capas superiores de la atmosfera; Velocidad del viento: inferior a 10 km /hora, si el viento es muy fuerte debe interrumpirse la aplicación. Dirección del chorro de insecticida: hacia el interior de la manzana de casas, manteniendo el sistema de descarga a 45° sobre la horizontal. Recorrido del vehículo: para el control del Aedes aegypti, rodear cada manzana aplicando insecticida en sus cuatro caras. Un aspecto muy importante es que este tipo de fumigaciones permite realizar en poco tiempo una gran cobertura de viviendas por día a diferencia de las fumigaciones realizadas con equipo portátil (fumigaciones intradomiciliares). En circunstancias y horarios normales un generador de aerosoles instalado en un vehículo trata entre 1600 y 1800 casas/día u 80 a 85 manzanas en 7 horas de trabajo efectivo dividida en dos turnos al amanecer y al anochecer, siendo posible programar 8000 casas/ciclo/generador como mínimo que serán cubiertas en 5 días de trabajo. Se requiere la adquisición de insecticidas piretroides líquidos en una cantidad que permita atender las necesidades nacionales en caso de que se presente una epidemia de Dengue de gran magnitud, esto en razón de que es importante tener una reserva de este insumo de manera estratégica y porque los procesos de adquisición tardan alrededor de 3 a 4 meses para ser concretados lo que no daría tiempo de reaccionar ante situaciones de emergencia. Para más detalle de la metodología de la actividad, ver anexo 1.3. 70 1.4 Monitoreo y supervisión de actividades de prevención y control del Dengue ACTIVIDAD DESCRIPCIÓN DE REQUERIMIENTO 1.4 Monitoreo y supervisión de actividades de prevención y control del Dengue De acuerdo a la normativa vigente del presupuesto se considerará el rubro para las actividades relacionadas con monitoreo y evaluación: Gastos de movilización, viáticos y subsistencias, pasajes al interior. Metodología para el Monitoreo y supervisión de actividades de prevención y control del Dengue El monitoreo constituye una actividad importante para evaluar el avance y cumplimiento de las acciones programadas en el componente permitiendo decidir medidas dirigidas a realizar correctivos en caso de que estos sean necesarios. La supervisión de actividades debe realizarse de manera periódica a fin de evaluar el avance de las actividades y determinar si se están cumpliendo o no de acuerdo a lo programado en el componente 1 del proyecto, esto es; el fortalecimiento de la Vigilancia epidemiológica y entomológica para controlar y/o disminuir los índices de infestación del mosquito Aedes Aegypti y otros vectores transmisores de Dengue y Fiebre Amarilla. La supervisión puede ser realizada de manera directa e indirecta. Directamente a través del respectivo coordinador del componente quien deberá movilizarse regularmente de acuerdo a un itinerario, o; indirectamente delegando funciones a través de los jefes u otros funcionarios de las Zonas operativas del SNEM a nivel nacional de acuerdo a la actividad que se quiera supervisar: Visitas domiciliarias para eliminación de criaderos de Aedes aegypti en fase larvaria con participación activa de la comunidad. Fumigación intradomiciliar de viviendas para el control del mosquito Aedes aegypti y otros en fase adulta. Fumigación de Manzanas con máquinas de ultra bajo volumen para el control del mosquito Aedes aegypti y otros en fase adulta. Monitoreo y supervisión de actividades de prevención y control del Dengue. Estudios de la eficacia de los insecticidas utilizados para el control vectorial. Capacitación sobre el manejo clínico de pacientes con Dengue dirigido a los equipos de salud a nivel nacional. Implementación de puestos de Vigilancia Entomológica para la detección de vectores de dengue y fiebre amarilla. Difusión de medidas de prevención y control del dengue. Educación y comunicación a nivel intra e intersectorial, para ejecutar medidas de prevención y control del dengue. Talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento en enfermedades metaxénicas al personal del Sector Salud y equipos multidisciplinario Sala de entrenamiento de manejo de pacientes con dengue 71 1.5 Estudios de la eficacia de los insecticidas utilizados para el control vectorial ACTIVIDAD METODOLOGÍA INSUMOS DESCRIPCIÓN DE REQUERIMIENTOS Papeles impregnados con insecticida estandarizados y dosificados (Kits OMS) Conos estandarizados por OMS prueba biológica de pared Efectuar pruebas de Jaulas de exposición para las pruebas de biosusceptibilidad en valoración espacial e intra domiciliar estado larvario y de Kits OMS para determinar susceptibilidad del adultos utilizando Materiales 1.5 Estudios de la de Temephos insumos y siguiendo laboratorio eficacia de los directrices técnicas entomológica Formularios entomológicos insecticidas de la OMS. Las Goteros 3ml, capsulas de porcelana, capturadores utilizados para el adquisiciones se de succión, laminas y laminillas cubre objeto, control vectorial harán a través de los solución fisiológica, algodón, alcohol, cloroformo, procesos de portal jeringuillas de 1ml, tul, recipientes plásticos para de compras públicas recolectar mosquitos, bandejas de hierro enlosado, y de la OPS. cintas de embalaje y cintas de papel Equipos Microscopios compuestos, estereoscopios con micrómetro ocular, cámara de cuello de cisne para microscopio, balanza gramatoria. Metodología para evaluar la eficacia de los insecticidas utilizados para el control vectorial Se realiza para garantizar la eficacia letal de los insecticidas en los artrópodos blancos del control y para orientar o referenciar las adquisiciones relacionadas a los mismos. Para evaluar la eficacia letal se realizan de manera regular las pruebas de susceptibilidad del vector a los insecticidas utilizados para su control a fin de detectar cuando el insecticida no produce los efectos deseados debido a la presencia de especímenes resistentes, lo que permitirá decidir oportunamente las medidas correctivas. En cualquier circunstancia conviene descubrir la resistencia en fase larvaria y en fase de mosquito adulto con la mayor rapidez posible antes que se haya extendido ampliamente entre la población de vectores. Para descubrir la resistencia, es necesario: a) Determinar el grado de susceptibilidad de las larvas o mosquitos adultos de la especie considerada. b) Realizar comprobaciones periódicas del grado de susceptibilidad. Las pruebas deben ser hechas continuamente y con la periodicidad correspondiente a nivel de todas las áreas del país con presencia del vector del Dengue, con suficiente número de larvas o mosquitos adultos y la alerta de una posible resistencia se da cuando regularmente aparecen sobrevivientes ante una exposición diagnóstica correctamente seleccionada. Para más detalle de la metodología de la actividad, ver anexo 1.5. 72 1.6 Talleres de capacitación sobre el manejo clínico de pacientes con Dengue dirigido a los equipos de salud a nivel nacional. ACTIVIDAD METODOLOGÍA 1.6 Talleres de Capacitación basada capacitación en la simulación de sobre el manejo casos clínicos clínico de Dengue: 1) Dengue pacientes con sin signos de Dengue dirigido a alarma, 2) Dengue los equipos de con signos de salud a nivel alarma y, 3) Dengue nacional grave INSUMOS DESCRIPCIÓN DE REQUERIMIENTOS Recursos Humanos Profesionales capacitadores expertos en manejo de pacientes con Dengue Equipos Laptop, proyector, puntero laser, Materiales e insumos Pizarra, borradores, marcadores de tiza líquida, vestuario, muñeca, pelucas, escritorio, dos sillas, una camilla, tensiómetro, estetoscopio, solución salina, lactato, dextrosa, equipo de venoclisis, catéteres, esparadrapo. Metodología para la ejecución de Talleres de capacitación sobre el manejo clínico de pacientes con Dengue. Los talleres de capacitación tienen como objetivo capacitar a profesionales de salud en el diagnóstico y tratamiento adecuado y oportuno del Dengue con la finalidad de reducir la ocurrencia de casos graves y muertes por esta enfermedad tomando como documento de referencia la Guía de manejo de dengue de la OPS/OMS. Esta actividad es realizada de manera continua por un equipo de capacitadores nacionales especialistas en el manejo de esta enfermedad conformado por profesionales pediatras y médicos clínicos de adultos, en razón de que existe una alta rotación de los profesionales de salud y porque cada año coincidiendo con la temporada de lluvias se incrementa la transmisión del Dengue, enfermedad que representa uno de los principales problemas de salud pública en el contexto de las enfermedades transmitidas por vectores en el Ecuador. La metodología de enseñanza se basa en la simulación de casos clínicos de acuerdo a la actual clasificación del Dengue: 1) Dengue sin signos de alarma, 2) Dengue con signos de alarma y, 3) Dengue grave, efectuada por promotores de salud (actores) lo que ha generado un gran nivel de aceptación permitiendo mejorar la atención y una gran interacción entre los docentes y los asistentes con excelentes resultados. El escenario se monta en el auditorio donde se efectúa el taller y para el efecto se utiliza un escritorio dos sillas, una camilla, tensiómetro, estetoscopio, un paciente (actor), un familiar (actor), una enfermera (actriz), un médico en entrenamiento (evaluado) y un médico docente (evaluador de conocimiento). 73 1.7 Implementar puestos de Vigilancia Entomológica para la detección de vectores de dengue y Fiebre amarilla. ACTIVIDADES METODOLOGÍA Iinstalación de puestos centinelas (ovitrampas, larvitrampas) en lugares seleccionados y 1.7 Implementar captura puestos de sistemática e Vigilancia identificación Entomológica de mosquitos para la detección involucrados en la de vectores de transmisión del dengue y fiebre Dengue y Fiebre amarilla amarilla. Adquisición de insumos a través de los procesos del portal de compras públicas. INSUMOS DESCRIPCIÓN DE REQUERIMIENTOS Recipientes de plástico negro de 1 o 2 litros boca ancha, baja lenguas, cinta aislante negra. Caña guadua, sierras de corte redondo 3 pulgadas, sierras de disco manuales, machetes, linternas de mano o frente, pilas, cuerdas plásticas, alambre Insumos para galvanizado, clavos, martillos, alicate muestreo Trampas de luz modelo CDC entomológico urbano y Marcadores permanentes Pinturas, brochas, diluyente selvático Recipiente plásticos boca ancha de 0,5 litros para adecuación y manejo de larvas en laboratorio Viales plásticos de 5cm Plataformas plegables portátiles para ascenso y trabajo en árbol Uniformes de Uniformes completos, gorras, camisetas, chalecos campo Herramientas de Mochilas, tableros, formularios, lápices, borradores, trabajo esferográficos, franela, detergente, jabón Prendas de Mascarillas, botas, cascos, guantes de hule, protección impermeables Metodología para la Implementación de puestos de Vigilancia Entomológica para la detección de vectores de dengue y fiebre amarilla La vigilancia entomológica está dirigida a las formas inmaduras de los vectores (huevos, larvas) o las formas maduras es decir los mosquitos adultos. La vigilancia proporciona información sobre la densidad y el movimiento de las poblaciones de vectores y es esencial para los programas de control de las enfermedades metaxénicas tropicales ya que sin la misma es imposible diseñar y planificar las intervenciones a realizarse. Sirve para anticipar la presencia de mosquitos en lugares estratégicos, para lo cual se instalan puestos centinelas (ovitrampas, larvitrampas) en lugares seleccionados, situación que es aplicable al mosquito Aedes albopictus conocido vector de Dengue, Fiebre amarilla y Encefalitis en Asia, presente en muchos países del continente americano, pero no detectado aun en el Ecuador. En nuestro país el vector del Dengue y de la Fiebre amarilla urbana es el Aedes aegypti, mientras que a nivel selvático las especies responsables de transmisión de Fiebre amarilla pertenecen a los géneros Haemagogus y Sabethes. Muestreo de Adultos (imagos) Se hace mediante la captura sistemática (trampas de luz, cebos animales) de mosquitos en las ciudades y demás asentamientos humanos y en el campo (bosques o selvas primarias o 74 secundarias), luego se procede a la identificación y contaje de los imagos capturados tomando nota de todas las condiciones climáticas o atmosféricas que puedan registrarse. La periodicidad con que se haga depende de los recursos disponibles. Se sacan promedios semanales. Adicionalmente se establece la relación mosquito/hombre/hora y sus hábitos de picadura para orientar las medidas de prevención y control. Muestreo de formas inmaduras (huevos y larvas) Las formas inmaduras se muestrean a través de “ovitrampas” y “larvitrampas” y pueden utilizarse tanto a nivel urbano, periurbano, selvático, aeropuertos, puertos marítimos y terminales terrestres Internacionales. 1.8 Difusión de medidas de prevención y control del dengue. ACTIVIDADES METODOLOGÍA INSUMOS Campañas educativas de prevención de enfermedades vectoriales 1.8 Difusión de medidas de prevención y control del dengue Diseño, elaboración y difusión del material de comunicación y educación. Adquisición de insumos a través del portal de compras públicas. Monitoreo y evaluación del cumplimiento del contrato y del impacto en la población Equipos: DESCRIPCIÓN DE REQUERIMIENTOS Contratación de medios de comunicación radiales Diseño, elaboración, producción y reproducción de cuñas radiales. Validación de cuñas radiales Material para diseñar, elaborar y tabular encuestas para valorar el grado de conocimiento y participación comunitaria en el control vectorial. Laptop, radio-grabadoras que cuenten con amplitud modulada (A.M), resmas de papel bond A4 Investigación del impacto de las campañas radiales Contratación de empresa consultora en la población. Metodología de la actividad El MSP a través del SNEM, es responsable de mantener correctamente informada a la ciudadanía a través de campañas de difusión sostenida de mensajes educativos a través de medios radiales y escritos de prevención y control de esta enfermedad, generando mecanismos que permitan incentivar la cooperación comunitaria a fin de que participe activamente en la lucha contra el Dengue con énfasis en la destrucción de criaderos en el intra y peri-domicilio. Esta labor informativa se complementa con la capacitación de públicos que sirven de multiplicadores del mensaje: comunicadores sociales que trabajan en los medios radiales, TV y prensa escrita; líderes comunitarios, personal de salud; educación, actores principales locales, provinciales y nacionales, etc. La utilización de medios alternativos, como twitter, correo electrónico, teléfonos convencionales y celulares; son otras formas de informar diariamente a la ciudadanía y medios de comunicación. 75 Estas actividades dirigidas a promover la participación comunitaria en la lucha anti-vectorial, son reforzadas con acciones que involucran la movilización social a través de mesas de trabajo intra e intersectoriales para la coordinación y ejecución de “mingas sanitarias”. Para más detalle de la metodología de la actividad, ver anexo 1.8. 1.9 Edu-comunicación a nivel intra e intersectorial, para ejecutar medidas de prevención y control del dengue ACTIVIDAD 1.9 Edu-comunicación a nivel intra e intersectorial, para ejecutar medidas de prevención y control del dengue DESCRIPCIÓN DE REQUERIMIENTOS INTRASECTORIAL Coordinación dentro del MSP (nivel central, zonal y distrital, INSPI, Dirección Nacional de Control Vectorial) INTERSECTORIAL Organizaciones gubernamentales (educación, gobiernos locales, agricultura, vivienda, comunidad organizada, promotores de salud). Metodología para la Implementación de actividades educativas y de comunicación a nivel intra e intersectorial para ejecutar medidas de prevención y control del dengue. El control de las enfermedades vectoriales debe ser siempre integral por lo que se requiere la participación activa y coordinada de todas las dependencias del MSP en especial aquellas que están ubicadas en zonas y distritos de riesgo y la acción de socios estratégicos gubernamentales y no gubernamentales como: OPS, Ministerio de educación, gobiernos locales, Ministerio de Vivienda, Ministerio de Defensa, Ministerio de Coordinación y Desarrollo Social, comunidad organizada, etc. En este sentido la coordinación del proyecto debe promover la ejecución de reuniones a través de “mesas multisectoriales” con participación de todos los actores que sean requeridos en un momento dado para la solución de problemas relacionados con la eliminación de criaderos del vector del Dengue o aquellos que estén vinculados con la atención de los enfermos. Este tipo de actividades serán implementadas a nivel de las Coordinaciones Zonales y en sus respectivas provincias y se realizarán de manera regular en base a un itinerario elaborado especialmente para este fin. Un aspecto que es fundamental en el control del vector del Dengue es la coordinación con el Ministerio de Educación a fin de promover la firma de convenios que permitan realizar algunas acciones de prevención y control del Dengue con énfasis en el control vectorial en cada uno de los establecimientos educativos “Escuelas sin Aedes” y en las viviendas de los alumnos, quienes a su vez serán los impulsores para generar cambios de conducta en sus familias y evitar la reproducción del vector del Dengue en sus viviendas., actividad que se propondrá debe tener una calificación en alguna materia a manera de estímulo del estudiante. El acercamiento y coordinación con los gobiernos locales permitirá efectuar acciones más puntuales relacionadas con la recolección y disposición final de desechos sólidos, 76 principalmente llantas y su participación en las actividades que se realicen periódicamente a través de mingas comunitarias para eliminación de criaderos en la comunidad. Es importante considerar que el proyecto busca cambiar progresivamente las conductas de riesgo que tienen las personas en todas las áreas de transmisión del país, para lo cual es importante que además del sector educativo se coordinen acciones con las organizaciones comunitarias para este mismo fin. 1.10 Talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento en enfermedades metaxénicas al personal del Sector Salud y equipos multidisciplinario ACTIVIDADES INSUMOS 1.10 Talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento en enfermedades metaxénicas al personal del Sector Salud y equipos multidisciplinario Combustibles DESCRIPCIÓN DE REQUERIMIENTOS Hojas, cuadernos, lápices, esferográficos, carpetas, borradores, CDs, borrador de pizarra, marcadores, pizarra acrílica, cinta embalaje Folletos, dípticos, afiches, trípticos, rotafolios, guías para promotores de salud Gasolina Equipos Proyector, laptop, puntero laser Suministros de oficinas Materiales didácticos Metodología para la realización de talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento en enfermedades metaxénicas Dado el gran nivel de rotación de médicos, enfermeras, promotores de salud, personal contratado para actividades relacionadas con el control del vector del Dengue a nivel nacional, es necesario efectuar los talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento de enfermedades metaxénicas, para que ellos funcionen adicionalmente como replicadores de conocimientos a la comunidad y en sus respectivas viviendas. En general las actividades de control requieren de conocimientos técnicos teóricos y prácticos para la correcta ejecución de las medidas de prevención y control del Dengue, particular por el cual todos los talleres que se efectúen deben tener estas consideraciones. Previa coordinación los participantes serán reunidos en los locales con que cuenta el MSP en las diferentes provincias del país (DPS, SNEM, INSPI, otros) y se dictarán las respectivas charlas en cada uno de los temas de interés para el proyecto, esto es: Temas Vigilancia epidemiológica Medidas de prevención y control del Dengue Diagnóstico y tratamiento Contenidos principales Situación epidemiológica actual del Dengue y otras metaxénicas en el Ecuador Vigilancia de casos, etiológica y entomológica de enfermedades metaxénicas Control Integral de enfermedades metaxénicas (Métodos: Físico, químico, Biológico, cultural, legal). Métodos de diagnóstico, esquemas de tratamiento de enfermedades metaxénicas Con la finalidad de valorar un antes y después se realizarán las respectivas pruebas de evaluación de conocimientos. 77 1.11 Sala de entrenamiento de manejo de pacientes con dengue ACTIVIDADES INSUMOS Recursos Humanos Equipos 1.11 Sala de entrenamiento de manejo de pacientes con dengue Materiales e insumos Espacio físico DESCRIPCIÓN DE REQUERIMIENTOS Profesionales capacitadores expertos en manejo de pacientes con Dengue Laptop, proyector, puntero laser, simulador Simuladores, pizarra, borradores, marcadores de tiza líquida, escritorio, sillas, camas, camillas, tensiómetros, estetoscopios, solución salina, lactato, dextrosa, equipo de venoclisis, catéteres, algodón, frascos, charol de paro, aparato de cardioversión, EKG, esparadrapo, soporte para soluciones, medicamentos, laboratorio, aparato para lectura de placas de Rx, etc. Aula (¿Hospital, SNEM, Universidad?) Metodología para la implementación de una sala de entrenamiento de manejo de pacientes con Dengue. Durante las últimas décadas, los laboratorios de simulación se han constituido en una herramienta didáctica utilizada para la enseñanza de la medicina. Con la simulación, los estudiantes pueden aprender en una forma práctica procedimientos, y afianzar conceptos clínicos como apoyo de las diferentes asignaturas. Se sabe de las ventajas que ofrecen estos espacios, pero aún faltan docentes que crean en sus bondades y desarrollen de manera sistemática, una verdadera incorporación de la simulación en su práctica docente En consideración a que en nuestro país se ha evidenciado que los fallecimientos por Dengue se han debido en algunos casos a errores cometidos durante la realización de un procedimiento del actuar médico, resulta indispensable generar espacios donde los médicos y enfermeras en formación universitaria, rurales o tratantes de las unidades de salud participen en eventos de esta naturaleza, particular por el cual es necesario implementar una sala de entrenamiento en el manejo de pacientes con dengue a nivel pediátrico y adultos a fin de contribuir a disminuir los errores, producto de la misma condición humana y evitar al máximo la ocurrencia de casos graves y muertes por esta enfermedad, efecto para el cual se cuenta con capacitadores nacionales de Dengue interesados en desarrollar este componente lo que permitiría el adecuado entrenamiento de nuestros médicos y enfermeras en el país, con énfasis en las provincias con mayores problemas de transmisión de Dengue. La sala de entrenamiento basada en la simulación clínica como una herramienta del proceso enseñanza- aprendizaje es una estrategia para evitar o disminuir las iatrogenias que se derivan del mal entrenamiento en algunos procedimientos (Ruiz-Parra A, 2009). Sin embargo, estos espacios no deben considerarse únicamente como un lugar para el desarrollo de habilidades y destrezas, sino también como espacios integradores entre el conocimiento y la praxis. Para la implementación de esta sala se requiere inicialmente realizar las respectivas coordinaciones a nivel nacional con Universidades que vienen trabajando en este sentido o a nivel Internacional para establecer acciones a seguir y estimar algunos costos de manera real , 78 entendiéndose que esta actividad demandaría una implementación y desarrollo de manera progresiva. 1.12 Tratamiento focal de los casos de dengue La probabilidad para que el virus del dengue se transmita de una persona enferma se da dos días antes que se presente la fiebre y durante los tres primeros días de fiebre, es por lo que la prevención secundaria del dengue debe realizar en estos tres primeros días, de ahí la importancia de que los pacientes acudan oportunamente, no se automediquen, faciliten la dirección exacta y el medico reporte inmediatamente a l SNEM para realizar el tratamiento focal. Debido a que el mosquito Aedes aegypti es de hábitos doméstico y su rango de vuelo es generalmente de 100 metros, por lo que el tratamiento focal de los casos de dengue se debería realizar mínimo en la manzana del paciente y las que están alrededor; lo que daría 6 manzanas de trabajo y si se considera que cada una tiene 20 casas, nos daría un total de 120 casas. El trabajo debe realizarse al mismo tiempo, la eliminación del mosquito en su fase acuática como área: Fumigación intradomiciliar con motomochila e insecticida piretroide; un pareja de fumigadores Inspección de viviendas para la búsqueda y Tratamiento criaderos y depósitos potenciales; cuatro visitadores ( rendimiento 30 casa por jornada) Coordinar con el equipo de salud del sector para que se realice la búsqueda de febriles, seguimiento del paciente y sospechosos, toma de muestra sanguínea al 6 día de fiebre del paciente para confirmar diagnóstico En caso de brotes (más de tres casos autóctonos) tomar muestras sanguíneas a pacientes y sospechosos durante los tres primeros días de fiebre para identificar serotipo circulante. 79 COMPONENTE 2 Disminuida la incidencia de Malaria a cero casos autóctonos en el Ecuador hasta el año 2017. ACTIVIDADES: ACTIVIDADES 2.1 Toma de muestra hemática a febriles sospechosos de paludismo y adopción de esquemas terapéuticos altamente eficaces METODOLOGÍA INSUMOS Materiales laboratorio para diagnóstico de malaria Toma de muestra hemática a febriles. Las adquisiciones se harán a través de los procesos de portal de compras públicas y de la OPS. Tratamiento medicamentos antimalaricos DESCRIPCIÓN DE REQUERIMIENTOS Láminas cubre objeto 22x22mm Pruebas rápidas Lancetas estéril descartables con capuchón Alcohol al 70% ciento por litro Algodón hidrófilo Adquisición de mascarilla quirúrgica descartable Pañuelos faciales caja de 100 Tachos para cortapunzantes Guantes de examinación descartables Porta láminas Pipetas pasteur plásticas 3 ml Laminas porta objeto Papel absorbente Tiras adhesivas (curitas) Giemsa 500 ml Metanol por litros Dotación de insumos, reactivos, para examen de gota gruesa a embarazadas P. vivax Cloroquina Fosfato Tabletas 250 mg. Primaquina Adultos Tabl. 15 mg. Primaquina Infantil Tabl. 7,5 mg P. Falciparum Artemeter: 20mg + Lumefantrine 120mg. (tratamiento Infantil, niños, adolescentes y adultos) Clindamicina clorhidrato 300 mg Quinina Sulfato de 300 mg Casos Graves Artesunato 60 mg/ml ampolla Metodología para obtención de la muestra Disponer de un espacio limpio, ordenado y horizontal. Así también, los materiales previstos para realizar una gota gruesa, tomar las precauciones y medidas de bioseguridad adecuadas. Después que los datos del paciente han sido registrados apropiadamente en el formato de registro (formulario OC-19), las muestras de sangre se procesan de la siguiente manera: Sostenga la mano menos utilizada del paciente, con la palma hacia abajo, y seleccione el dedo índice; para esto haga que el paciente extienda el dedo seleccionado y flexione los demás. En niños pequeños se puede usar el dedo gordo del pie, el talón o el lóbulo de la oreja. 80 Limpie el dedo, (o el sitio de punción) con una torunda de algodón ligeramente humedecida en alcohol para retirar la suciedad y la grasa de la yema del dedo, luego seque el dedo con un algodón seco y limpio, estimulando la circulación de la sangre. Sostenga el dedo del paciente, tomándolo por sus lados y manteniendo una suave presión para favorecer la salida de sangre. Tome la lanceta y realice una dígito-punción en el pulpejo del dedo a la altura del nacimiento de la uña. Asegúrese de que la punta de la lanceta penetre totalmente en el dedo y esté ubicada en sentido contrario a las huellas dactilares. Presione el dedo, deje salir la primera gota de sangre y elimínela con una torunda de algodón seca. Asegúrese que ningún resto de algodón permanezca en el dedo, que pueda mezclarse posteriormente con la sangre. Luego, en una lámina portaobjetos colectar dos gotas de sangre, una para la gota gruesa que debe ser aproximadamente como el de la cabeza de un fósforo y se ubica entre el primer y segundo tercio de la lámina. La tercera gota que servirá para el frotis, es más pequeña y se coloca de 0.5 a 1cm de distancia de la gota gruesa. Limpie la sangre restante del dedo con una torunda de algodón humedecida en alcohol, e indique al paciente que la presione en el lugar de la punción por 5 minutos. Pasos para la realización de Pruebas de Diagnóstico Rápido de malaria (PDR): Selección de sitio de trabajo y revisión de materiales e insumos Registro de información de pacientes Marcar la lámina y prueba rápida con el código del paciente Limpieza del dedo (selección del dedo a puncionar) Correr prueba rápida de acuerdo a las indicaciones de la prueba rápida Lectura de prueba rápida 81 El SNEM como entidad encargada del control de enfermedades metaxénicas en la actualidad posee una red de Laboratorios también llamados Puestos de Diagnostico Microscópico (PDM) distribuidas en las distintas provincias y Zonas Maláricas, según se detalla en cuadro ajunto, lo cual hace posible que se mantenga la vigilancia pasiva de la malaria en nuestro país y esta actividad es complementada por la incorporación de las unidades operativas del MSP. ZONAS SNEM No. Microscopistas o PDM I Santo Domingo II Napo- Pastaza III Guayas- Santa Elena- Cañar IV Loja Zamora V Los Ríos-Cotopaxi-Bolívar VI Manabí VII Esmeraldas VIII El Oro –Azuay IX Sucumbíos- Orellana X Moriona Santiago XI Área Metropolitana Guayaquil-Duran TOTAL 17 14 22 3 21 36 54 20 28 9 23 247 Tratamiento a casos positivos de malaria En nuestro país se han aplicado esquemas de tratamiento altamente eficaces para pacientes con malaria de acuerdo a la especie diagnosticada, éstos cuentan con el aval de la Organización Panamericana de la Salud a través del proyecto RAVREDA-AMI desde el año 2005. No se ha evidenciado falla terapéutica de estos medicamentos en la cura del paludismo lo que hace factible que estos fármacos continúen siendo usados en las unidades operativas públicas y privadas del territorio nacional. Además su proceso de adquisición se lo realiza a través de Organización Panamericana de la Salud (OPS), el Fondo Estratégico Internacional y el Sistema Nacional de compras públicas. ESQUEMA PARA PACIENTES POSITIVOS A P. VIVAX 82 ESQUEMA PARA PACIENTES POSITIVOS FALCIPARUM ESQUEMA # 2 GRUPOS DE EDAD ARTEMETER+LUMEFANTRINA* Número de tabletas y tiempo aproximado de dosificación Edad En años Peso en Kg. 0H00 8H00 5 - 14 1 1 1 3 a 8 15 - 24 2 2 9 a 14 25 - 34 3 > 14 > 34 4 <3 24H00 36H00 48H00 60H00 1 1 1 2 2 2 2 3 3 3 3 3 4 4 4 4 4 DOSIS DE PRIMAQUINA AL 4 DIA De 6 a 11 años 1 Inf. De 1 a 2 años 1 1/2 Inf. De 3 a 6 años 1 Ad. De 7 a 11 años 1 1/2 Ad. De 12 a 14 años 2 Ad. De 15 o más años 3 Ad. DOSIS 0.75 mg/kg/dia TRATAMIENTO DE MALARIA GRAVE CON ARTESUNATO PRESENTACION PREPARACION Polvo para inyecciones de 60 mg de Artesunato anhidro en ampollas de 1 ml + bicarbonato de sodio al 5% en ampollas de 0,6 ml El polvo para inyección se debe disolver en 1 ml de solución de bicarbonato de sodio, agitar de 2-3 minutos y esperar hasta que se disuelva completamente, obteniendo una solución clara y libre de partículas, de no ser así, debe desecharse dicha preparación. Inserte la aguja de la jeringuilla para extraer el aire inmerso. DOSIS INICIAL 2.4 mg/kg i.v. o i.m. DOSIS DE MANTENIMIENTO 2.4 mg/kg i.v. o i.m., a las 12 y 24 horas, después de la primera administración FICHA TECNICA SOBRE USO DE ARTESUNATO Información general El artesunato es un hemisuccinato derivado de la artemisinina soluble en agua. Es inestable en solución neutra y la fórmula inyectable debe prepararse inmediatamente antes del uso. Después de la administración parenteral, se hidroliza rápidamente para transformarse en un metabolito de dihidroartemisinina activo. Se ha señalado que el artesunato elimina la fiebre en enfermos con paludismo falciparum grave de 16 a 25 horas después de la administración parenteral. Aplicaciones Por vía parenteral: tratamiento del paludismo falciparum grave en zonas donde hay indicios de resistencia a la quinina. La cura radical se consigue con la administración subsiguiente de un ciclo completo de un antipalúdico oral eficaz. Para administración IV (intravenoso): La preparación se mezclara con 5 ml. de solución salina o de solución glucosada al 5% en el vial, la solución resultante contendrá 10 mg de Artesunato por mililitro (para un volumen total de 6ml.) Extraiga la cantidad necesaria de la solución de Artesunato del vial en una jeringuilla y adminístrela muy lentamente a una velocidad aproximada de 3-4 ml/min. Para administración IM (intramuscular): Añada 2ml aproximadamente de solución salina o de solución glucosada al 5% en el vial, la solución resultante contendrá 20 mg. de Artesunato por 83 mililitro (para un volumen total de 3ml.) Extraiga la cantidad necesaria de la solución de Artesunato del vial en una jeringuilla e inyecte de acuerdo a las normas establecidas. Contraindicaciones Hipersensibilidad al medicamento o reacciones alérgicas anteriormente reportadas Precauciones El polvo para inyección es difícil de disolver y se debe poner cuidado en asegurarse de que está disuelto completamente antes de su administración parenteral. Debe utilizarse siempre inmediatamente después de la reconstitución. Si la solución está turbia o precipita, se debe descartar la preparación parenteral. Embarazo y Lactancia Se tiene escasa experiencia con respecto al empleo de este fármaco en el embarazo, pero la preparación parenteral no debe dejar de administrarse si se considera que puede salvar la vida de la madre. Se recomienda usarlo durante el primer trimestre de gestación solo si el beneficio es mayor al riesgo. Efectos adversos Puede producirse una fiebre de origen medicamentoso. Se ha observado neurotoxicidad en estudios sobre animales, pero no en los seres humanos. Dada la incertidumbre acerca de los efectos tóxicos, se debe actuar con cautela cuando se aplica un tratamiento de más de tres días. Se ha observado cardiotoxicidad después de la administración de dosis elevadas. Conservación Se deben conservar en recipientes bien cerrados y frescos, al abrigo de la luz. Sobredosis Puede causar reticulocitopenia transitoria cuando se administra más de 3.75 mg/kg. Interacciones El uso concomitante con mefloquina puede mejorar el efecto curativo. CASOS ESPECIALES EN MALARIA En malaria por P falciparum en EMBARAZADAS utilizar: Quinina Oral 10mg/kg/en tres tomas x 7 días + Clindamicina Oral 10mg/kg cada/12 horas por 5 días. Menores de 6 meses: Quinina Oral 8 mg/kg cada 8h x 7 dias + Clindamicina Oral x 5 días (10 - 20mg/kg/día). PRESENTACION: Clindamicina Frasco x 80 ml. Cada 5 ml. equivalen a 75 mg. de Clindamicina Base 84 2.2 Fortalecimiento del Sistema de Gestión de Calidad del diagnóstico microscópico de Malaria. El país cuenta con un Manual Operativo Estándar para la gestión de la garantía de la calidad en el diagnóstico microscópico de la malaria, realizado con la participación de técnicos nacionales y con la consultoría de un técnico de Organización Panamericana de la Salud (OPS). Se realizan las siguientes tareas: 1. Cumplimiento de la Norma y sus estándares técnicos 2. Cumplimiento de los Procedimientos Operativos Estándar (POE) 3. Evaluación de la Competencia Profesional 4. Implementación de un Programa de Capacitación en base a los resultados de la evaluación de la competencia profesional, a la Norma Técnica y a los POE Elementos de la Gestión de Garantía de la Calidad (GGC) Este grafico muestra los elementos de la Gestión de Garantía de la Calidad (GGC) para el diagnóstico microscópico de la malaria. POE: procedimientos operativos estándar, EID: validación de láminas diagnosticadas, EED: evaluación externa del desempeño. La Norma y estándares técnicos son el conjunto de lineamientos técnicos que regulan el ejercicio del diagnóstico microscópico de la malaria, desde la selección y capacitación del personal, la estructura y funcionamientos de los puestos de diagnóstico, la lectura de las muestras, hasta el registro y canalización de la información. Los procedimientos operativos estándar describen los diferentes procedimientos relacionados al diagnóstico microscópico con suficiente detalle para ser reproducidos de forma estandarizada por el personal y se encuentran contenidos en el Manual de Procedimientos Operativos Estándar (Manual POE). 85 Control de Calidad Es un proceso sistemático y continuo en los Puestos de Diagnóstico Microscópicos (PDM) que permite de manera simultánea medir la exactitud y precisión de las pruebas, la calidad de los equipos, instrumentos reactivos, el desempeño personal y un control de resultados emitidos. Conjunto de acciones que se aplican durante la ejecución de cada prueba para asegurar que los resultados, productos o servicios pueden ser entregados. Para evaluar la calidad de los PDM se utilizan siguientes métodos: 1. 2. 3. 4. 5. Control de calidad interno Evaluación indirecta Auditoría Supervisión directa Evaluación externa del desempeño. Todas estas actividades se realizan de forma sistemática y periódica en los niveles zonales a través de los revisores de microscopistas quienes evalúan y realizan el control de calidad para el aseguramiento de un diagnóstico certero, además ante cualquier duda se cuenta con el nivel central o se solicita apoyo internacional ya que el Ecuador es miembro de la los países de la Región que llevan el control de la malaria a través de OPS/OMS. 2.3 Monitoreo, Supervisión y Evaluación de actividades de campo en la vigilancia epientomológica para malaria. Esta actividad se realiza desde los niveles correspondientes de acuerdo a las líneas de acción, es decir desde el nivel zonal al nivel operativo, y desde el nivel central hasta el nivel zonal con el propósito de optimizar el buen uso de los recursos desde el punto de vista técnico y operativo. Tiene su base en los siguientes conceptos detallados y ejemplificados en el siguiente cuadro: CONCEPTO El monitoreo/supervisión es el seguimiento rutinario de los elementos clave del desempeño del componente Malaria. Es una actividad continua que usa la recolección sistemática de datos. La evaluación es la valoración puntual del cambio en los resultados del componente Malaria. Es el diagnóstico de un proyecto finalizado o en curso. Objetivo es lo que se quiere lograr con el componente. Siempre se lo redacta en infinitivo. La estrategia es el método o forma de actuación a seguir, para lo cual se realizan varias actividades. EJEMPLOS Visitas periódicas a unidades ejecutoras para seguimiento de una actividad a su cargo. 1. Análisis y explicación de los resultados finales del componente vs. metas planteadas. 2. Monitoreo & Evaluación a la red de diagnóstico de laboratorio de malaria y tomadores de muestra en los niveles zonales, distrital y local. 3. Evaluación de competencias. Interrumpir la transmisión de la malaria a cero casos autóctonos. 1. 2. Diagnóstico integral: Microscópico, Genotipificacion del parasito Tratamiento oportuno: Estudio de la calidad de los medicamentos antimalaricos con BIO-LAB. Estudio de eficacia de los tratamientos, Resistencia temprana. 86 3. 4. 5. Actividad es un conjunto de tareas efectuadas durante la implementación del componente. Los indicadores son unidades de medida que proporcionan información para monitorear y evaluar. Producto de un proyecto se refiere al bien o servicio generado por las actividades Los medios de verificación son los instrumentos que permiten comprobar el estado de los indicadores Seguimiento de casos con la implementación de la Ficha epidemiológica de investigación. Uso de Mosquiteros impregnados. Rociado selectivo secuencial en localidades con reporte de casos. 1. Realización de ciclos de talleres. 2. Aplicación test de conocimientos. 1.Índicadores malariometricos: IPA,ILP,FRIF,IAES. 2. Indicadores Entomológicos: IPH, IPHN, Densidad larval. 1. Plan de M&E para el componente. 2. Personas capacitadas. 1: Estadística de Morbilidad 2. Lista de asistentes/participantes firmada Los resultados son los cambios resultantes en las vidas de las personas que usan los productos del componente (efecto o impacto). La fuente de datos es el lugar (físico) donde se encuentran los datos que permiten verificar el estado del indicador Cambios de comportamiento (uso de Mosquitero Tratado con Insecticidas – MTI). La meta describe los cambios que generará el proyecto en un determinado plazo, implica un nivel y cronograma. Eficacia es la capacidad de alcanzar lo propuesto. Eficiencia es la capacidad de alcanzar lo propuesto con el mínimo de recursos. 1: IPA <1. 2: ILP <5 3: IAES: 6-10% de la población en riesgo. El tiempo programado es igual al tiempo de ejecución. Calidad es el estándar previsto para los productos, servicios o indicadores definidos. Equidad es la característica de un indicador que involucra nociones de justicia e igualdad social con valoración de la individualidad. Tratamiento de la Malaria de acuerdo a normas nacionales del MSP 1: SIVEMAE 2: INEC Ejecución presupuestaria acorde a lo programado (100%) 1. Niños menores de cinco años tratados acorde a pautas nacionales 2. Mujeres embarazadas con al menos un examen de hematozoario en sus controles prenatales. De acuerdo a la normativa vigente del presupuesto del componente se considerará el rubro para las actividades relacionadas con monitoreo y evaluación de gastos de movilización, viáticos y subsistencias, pasajes al interior (terrestre, aéreo y marítimo) y combustible en los niveles locales y zonales. 2.3 Control de Brotes malaria Se define como brote de malaria a uno o más casos de plasmodium falciparum autóctono que se presentan en un área geográficamente determinada sin que haya ocurrencia de casos en los últimos cinco años y de dos o más casos de plasmodium vivax autóctono que se presentan en un área geográficamente definida en el transcurso de un tiempo determinado. Definición de caso (programas de eliminación) Autóctono: Es un caso adquirido a través de la picadura de un mosquito infectado en una área delimitada geográficamente, sin que haya pernoctado fuera de su localidad durante el último mes. 87 Importado: Es todo caso que puede proceder de un área remota del país o fuera del mismo a una localidad sin transmisión de malaria. Inducido: Es un caso, cuyo origen se puede remontar a una transfusión de sangre o de otra forma de inoculación parenteral, y no por la transmisión normal de un mosquito infectado. Introducido: Es un caso cuyo origen antecede (primera generación) a partir de un caso importado. Asintomático: Es cualquier caso sin síntomas clínicos y que ha sido confirmado mediante el examen microscópico de los parásitos del plasmodium. Investigación del caso: Es la recopilación de información específica, que permite clasificar un caso de malaria por su origen de infección: autóctono, importado, inducido, y/o introducido. Diagnostico; Por PDR confirmados por microscopia. Tratamiento observado de acuerdo a la especie de plasmodium Seguimiento de los casos confirmados para los controles Control Plasmodium falciparum Plasmodium vivax Primero 5to. día 8vo. día Segundo 7mo. día 15vo. dia Tercero 14vo. dia 21vo. dia Cuarto 21vo. dia 28vo. dia Quinto 28vo. dia Estudio de colaterales mediante la implementación de la ficha epidemiológica de seguimiento de casos. Rociado secuencial (tres ciclos en el año) de manera selectiva en área de transmisión mediante la aplicación de insecticida de acción residual intradomiciliar (RRI). Dotación de mosquiteros (MTI) impregnados de larga duración. 2.5 Distribución de mosquiteros según requerimiento epidemiológico ACTIVIDADES 2.5 Distribución de mosquiteros según requerimiento epidemiológico METODOLOGÍA A través de los procesos de portal de compras públicas. INSUMOS Adquisición mosquiteros insecticida duración de DESCRIPCIÓN DE REQUERIMIENTOS de con Mosquiteros tratados con insecticida (tamaño larga familiar largo) Para un control eficaz y poder alcanzar las Metas de Desarrollo del Milenio para 2015, el Programa Global de Malaria recomienda 3 intervenciones principales: 1. Diagnóstico y Tratamiento con antimaláricos eficaces 88 2. Distribución de MTILD, con cobertura total de las poblaciones expuestas al riesgo de malaria 3. Rociamiento residual intradomiciliario, para reducir y eliminar la transmisión de malaria Directrices para la distribución de mosquiteros usadas en el país son: 1. Selección de localidades endémicas y poblaciones de alto riesgo de transmisión de malaria. 2. Distribución e instalación gratuita en las viviendas previo censo de la localidad. 3. Diseminación de material educativo junto con el mosquitero, con énfasis en las buenas prácticas de lavado. 4. Adecuados diagnóstico y tratamiento como parte integral de la intervención. 5. Encuestas de uso. La OPS recomienda las siguientes características de Mosquiteros: PARAMETRO Material Hilo Insecticida Malla Forma disponible Colores Tamaño Certificación Empaquetado Registro Sanitario ESPECIFICACIÓN 100% Polietileno o 100% Poliéster 75-100 denieres Piretroide de Acción Residual ( entre 1 y 2 años) y/o que resista como promedio entre 15-20 lavadas 156 orificios/pulgadas cuadrada Rectangular Indistinto 130x180x150 cm 160x180x150 cm 190x180x150 cm OPS/OMS Al vacío en fundas biodegradables. Registro Sanitario Vigente Emitido por el INSPI 89 2.6 Vigilancia epidemiológica para la eliminación de la malaria Necesidades Descripción de requerimientos Spots publicitario para la Contratación de medios de comunicación locales. eliminación de la malaria Talento humano para acciones de Contratación de 50 personas para formación de vigilancia epidemiológica vigilantes epidemiológicos comunitarios. Suministros Materiales de oficina, Material didáctico: dípticos, trípticos, volantes, afiches, licencias de los software Uniformes de campo Uniformes completos, gorras, chalecos, camisetas. Spots publicitarios que permitan difundir, publicar y socializar información específica referente a la fase de pre-eliminación de la enfermedad, la que tiene que ser sustentable y sostenible para lograr modificar conductas de riesgo a conductas saludables y consecuentemente la eliminación de la malaria. Paralelamente a la difusión de la campaña de mensajes, se debe reforzar esta actividad con la producción y reproducción de materiales educativos relacionados a la prevención del paludismo. La formación de vigilantes epidemiológicos, se hace necesaria para complementar la acciones de comunicación y movilización social, que garanticen el propósito del componente de comunicación. Para esta actividad se cuenta con personal técnico que actuará como facilitador en los talleres de formación de vigilantes epidemiológicos, cuya acción principal se centra en la vigilancia de la no reintroducción del paludismo en los sitios seleccionados para la certificación de eliminación de la malaria, así como la coordinación de las actividades en los niveles administrativos y comunitarios. Usando el sistema portal de georeferenciación a través de dispositivos GPS. Con el propósito de asegurar el mantenimiento de la vigilancia epidemiológica se prevé la adquisición del mantenimiento de las licencias del software de información que se emplea en el sistema nacional, el mismo que tiene el avalado por la OPS. 2.7 Rociado de viviendas para la intervención de casos de malaria ACTIVIDADES 2.7 Rociado de viviendas para la intervención de casos de malaria METODOLOGÍA INSUMOS Las adquisiciones se Prendas de protección harán a través de los procesos de portal Uniformes de campo de compras públicas y de la OPS. Movilización DESCRIPCIÓN DE REQUERIMIENTOS Mascarillas para insecticidas (con protector ocular), botas de cuero, guantes de hule. Uniformes completos, gorras, chalecos, camisetas Vehículo de la Institución Metodología del Rociado de viviendas Asegurar la aplicación correcta y segura de un insecticida residual en las superficies interiores de las viviendas sobre las áreas en que los vectores del paludismo suelen reposar. 90 Preparaciones – La vivienda Informar al jefe de familia sobre el programa de rociado y sobre el propósito del rociamiento, dándole tiempo para preparar y desocupar la casa. Los moradores DEBEN salir de la vivienda antes del rociado. Los cuartos ocupados por personas enfermas que no puedan moverse NO deberán ser rociados. Sacar de la casa todos los artículos domésticos, incluyendo agua, alimentos, utensilios de cocina y juguetes. Mover y cubrir o sacar los muebles para permitir el fácil acceso para rociar las paredes. Los artículos que no puedan ser removidos deberán ser cubiertos. Enjaular o atar a las mascotas y animales domésticos fuera de la casa. Preparaciones – El equipo El rociado residual de insecticidas en superficies interiores de las viviendas es normalmente realizado a través del empleo de bombas aspersoras de compresión de operación manual. Antes de iniciar la operación de rociado, el equipo debe ser revisado. Una bomba aspersora en malas condiciones puede dar resultados pobres o una sobre dosificación. Mezcla, técnicas de rociado y manejo Prepare el insecticida de acuerdo a las instrucciones del fabricante. El insecticida se puede mezclar por separado en otro recipiente y verter en la bomba aspersora. Bolsitas solubles en agua, tabletas e insecticidas granulados se añaden directamente al tanque lleno de agua. Estas formulaciones se mezclan fácilmente con agua y reducen los riesgos asociados con el manejo y mezcla en un recipiente por separado. El contenido de la aspersora debe ser mezclado perfectamente agitando el tanque antes de iniciar el rociado. 91 El rociado se aplica en franjas verticales de 75 cm de ancho. Las franjas deben sobreponerse por 5 cm. Rocíe del techo al piso, utilizando un movimiento hacia abajo hasta completar una franja. Dé un paso lateral y rocíe hacia arriba del piso al techo. La velocidad del rociado debe ser de un metro por cada 2.2 segundos, es decir, 4.5 segundos por cada pared de 2 metros de alto. El cronometraje puede ser auxiliado contando mentalmente “mil uno - mil dos - mil tres - …”. Ajuste el procedimiento contando mentalmente de acuerdo al lenguaje local. Se recomienda el uso de la “válvula de control de flujo (CFV)” ya que reducirá la necesidad de rebombeo y producirá una cantidad uniforme de insecticida que se deposita sobre la pared. La válvula se ajusta quitando primero el cuerpo de la boquilla. Adapte una arandela al final de la CFV atornillándola al cuerpo de la boquilla. La punta y la tapa de la boquilla están atornilladas atrás sobre la abertura final de la CFV. Con una “CFV roja” que opera a 1.5 bar (21 psi), la descarga será de 580 ml / min y 30 ml/ m2 a la misma velocidad del rociado. Preparación del insecticida a rociar La cantidad de formulación de insecticida necesario para la preparación de una carga se basa en la tasa promedio de descarga y la velocidad de la aplicación. Con una presión funcional de entre 25 y 55 psi y a una velocidad estándar de aplicación, la tasa de aplicación será de 40 ml/m2. Esto significa que 8 litros (8,000 ml) de la suspensión de rociado pueden ser aplicados a 200 m2 (cálculo: 8000 ml/40 ml/m2 = 200 m2). 92 Ejemplo 1: Para aplicar 2 g de ingrediente activo / m2 se requiere 400 g de ingrediente activo en el tanque (cálculo: 2 gr / m2 x 200 m2 = 400 g). Por lo tanto para una formulación de insecticida al 50% en polvo humectable, 800 g del producto formulado deben ser mezclados con agua para dar 8 litros de suspensión (cálculo: 400 g / 0.50 = 800 g). Ejemplo 2: Para aplicar 0.05 g de ingrediente activo / m2 se requiere de 10 g de ingrediente activo en el tanque (cálculo: 0.050 g/m2 x 200 m2 = 10 g). Por lo tanto para un insecticida formulado al 2.5% en polvo humectable, 400 g del producto formulado deben ser mezclados con agua para dar 8 litros de suspensión (cálculo: 10 g / 0.0025 = 400). Nota 1. La cantidad de ingrediente activo (i.a.) en formulaciones líquidas (p. ej. EC, SC) puede ser expresada como peso/peso (p/p) o peso/volumen (p/v). En el último caso, el cálculo procede como en los ejemplos anteriores. Como, en el caso de p/p, al consultar la etiqueta cuidadosamente, se hará, también dando la cantidad de ingrediente activo por litro. Convierta esta cantidad a porcentaje antes de proceder con los cálculos, como se indicó anteriormente. Por ejemplo, si la etiqueta indica que contiene 100 g de i.a. / L se convierten en 100 g/L a por ciento. (Cálculo: 100g/1000ml = 10%). Note 2: En algunos países se utilizan las bombas aspersoras de 10 l de capacidad. Con tal capacidad del tanque, el rociado de suspensión cubre 250 m2, aplicando 40 l/ m2. Nota 3: Con la CFV roja, la proporción de aplicación será de 30 ml/m2 y, por lo tanto, 8 litros de suspensión pueden ser rociados en 266 m2, a la misma velocidad de rociado (cálculo: 8000 ml/ 30 ml / m2 = 266 m2). Para aplicar 2 g de ingrediente activo / m2 se requiere de 532 g de i.a. en el tanque (cálculo: 2 g X 266 m2 = 532 g). Para una formulación de insecticida del 50% de polvo humectable, por lo tanto, 1,064 g del producto formulado deberá ser mezclado con agua, para dar 8 litros de suspensión (cálculo: 532 g / 0.50 = 1064 g). (Ver anexo 2.7) 2.8 Reuniones de análisis epidemiológico de la malaria desconcentrados a nivel nacional. con los niveles Reuniones con participación de los Coordinadores Zonales, Dirección General, Subdirección Técnica, Epidemiologia Nacional, Líderes de componentes y autoridades del Ministerio de Salud Pública, tienen como propósito entre otros, realizar las siguientes actividades: Incidencia de los últimos 5 años y estratificación en los niveles provincial, cantonal. Parroquial y local. Revisión del Canal endémico. Inventario de establecimientos de salud en los distintos niveles que reportan de manera oportuna, precisa y completa la información de las enfermedades metaxénicas con énfasis en malaria. Inventario de puestos comunitarios activos e implementados niveles que reportan de manera oportuna, precisa y completa la información de las enfermedades metaxénicas con énfasis en malaria. Red de diagnóstico FODA. (No. PDM activos, elaboración de paneles) 93 Distribución de Mosquiteros Tratados con Insecticida (inventario/saldo)-Pruebas de Diagnóstico Rápido. Seguimientos de casos con el uso de la Ficha de investigación epidemiológica. Georeferenciación de casos en localidades con transmisión. Medidas de intervención con la aplicación del rociado residual en áreas de transmisión Seguimiento de casos/porcentaje de cumplimiento acorde a la normativa Elaboración de paneles de Plasmodium en los niveles zonal, provincial, distrital y local. Control de calidad efectuado a las muestras sanguíneas para diagnóstico de malaria en los niveles correspondientes. Identificación de requerimientos y necesidades. 2.8.1 Reuniones Técnicas de coordinación con países en zonas de frontera para la implantación conjunta de estrategias de control y/o eliminación de malaria Nuestro país como ente encargado del control de malaria es miembro de los países de la Región que luchan contra esta enfermedad lo que hace insoslayable la participación de un equipo técnico del SNEM delegado por la máxima autoridad en reuniones binacionales de carácter anual con el propósito de evaluar las acciones de manera conjunta que se desarrollan en materia de control y/o eliminación de malaria. 2.9 Caracterización de focos de transmisión: nuevo potencial, nuevo activo, activo residual, residual no activo, endémicos y libres de transmisión Se define al Foco de malaria a toda localidad situada en un área actual o anteriormente malárica en la que existen de forma continua o intermitente los factores necesarios para la transmisión malárica: población, vectores y una ecología apropiada. Se detallan a continuación los diferentes tipos de focos y sus características. TIPOS DE FOCOS Inactivos Focos Residuales Activos Potenciales Focos Nuevos Activos CARACTERÍSTICAS Interrupción de la transmisión; recaídas de casos antiguos únicamente Interrupción incompleta de la transmisión; recaídas y nuevos casos (autóctonos) Existencia de casos importados; presencia del vector pero sin transmisión efectiva Existencia probada de transmisión; casos importadas y casos nuevos (introducidos y autóctonos) Sobre la base de la investigación, en el ámbito operativo, el foco también se puede clasificar en uno de los siguientes: Foco endémico: La transmisión se produce y no se controla eficazmente, y si las intervenciones de control de la malaria se están ejecutando, el efecto no ha sido suficiente para reducir la transmisión a niveles bajos. 94 Libre de transmisión: Es cuando no se presenta transmisión local durante los últimos 2 años en un área con una historia de la malaria y las condiciones adecuadas para la transmisión. 2.10 Vigilancia entomológica adecuada en fase de eliminación de la malaria. La Vigilancia Entomológica en malaria es un proceso continuo de recolección sistemática, tabulación, análisis e interpretación de la información sobre algunos aspectos de la biología y bionomía del Anopheles para la toma de decisiones en el control regular y contingencial de estos vectores. A fin de realizar estas actividades se debe disponer de profesionales capacitados, auxiliares de entomología y operarios de control de vectores idóneos, que tengan continuidad dentro del programa, una infraestructura técnica, logística adecuada, un subsistema de información básico, estandarización de métodos y procedimientos técnicos que garanticen el logro de los objetivos, calidad técnica y la consistencia de los resultados. En el país se ha desarrollado una vigilancia entomológica de forma parcial para la pre eliminación de la malaria, esto debido a que en los niveles desconcentrados no se cuenta con personal técnico calificado, solo son auxiliares que apoyan en el campo operativo, sin embargo, las directrices se emiten desde el nivel central a fin de contar con indicadores que orienten las actividades de control de forma óptima en base a los lineamientos que pronuncia la OPS/OMS. Se cuentan en la actualidad con indicadores entomológicos básicos tales como: tasa de picadura, densidad de adultos en reposo, densidad de larvas, mortalidad en pruebas de susceptibilidad y mortalidad en bioensayos, los cuales se describen en el siguiente cuadro. INDICADOR Tasa de picadura CALCULO Numero de mosquitos/hombre/hora Densidad de adultos en reposo Numero de mosquitos/Total de casas Densidad de larvas Total larvas/ Total cucharonadas X 100 cucharonadas/1m². Mortalidad en pruebas de susceptibilidad Número de individuos expuestos muertos/ Número de individuos expuestos X100 INTERPRETACION Permite calcular la antropofilia, endofagia y exofilia del vector. El valor corresponde al número de mosquitos que se acercan a picar a un hombre expuesto en el lapso de una hora. Permite calcular el riesgo de adquirir la enfermedad por la frecuencia de picadura del vector. Permite calcular la endofilia del vector. Se puede interpretar como el número de mosquitos vectores que ingresan y reposan dentro de la vivienda. Permite calcular la densidad larvaria relativa del criadero por m² y medir la residualidad de las acciones de control dirigidas a las fases inmaduras. Permite calcular la proporción de mosquitos que mueren en el bioensayo y permite calcular alteraciones de susceptibilidad VARIOS Otros indicadores relacionados se consideran a: Índice de picadura Hora noche (IPHN), Índice de esporozoitos, Tasa de fecundidad, entre otros. 95 Mortalidad en bioensayos de pared y mosquiteros Distribución geográfica de los vectores , diversidad de hábitats y adaptación ecológica Número de individuos control muertos/ Número de individuos control X100 Número de individuos expuestos muertos/ Número de individuos expuestos X100 Número de individuos control muertos/ Número de individuos control X100 Numero de poblaciones y sub-poblaciones de mosquitos vectores en áreas estratificadas de riesgo de malaria. al ingrediente activo empleado en el control vectorial. Permite calcular la proporción de mosquitos que mueren posterior a las intervenciones con MTI y rociado intradomiciliar y medir la residualidad de las acciones. Aplicación de técnicas moleculares para el Diagnostico de complejo de especies cripticas También contamos con protocolos emitidos desde el nivel central de acuerdo a la realidad local, se cita a continuación: PROTOCOLO PARA CARACTERIZACION DE CRIADEROS. La estimación de la densidad larvaria en los criaderos es relativa y es solo valida si el mismo procedimiento y equipo de colecta es usado cada vez en el mismo tipo de criadero. Variaciones temporales en la densidad pueden ser muy marcadas y esto debe ser tenido en cuenta. El método de colecta descrito puede no dar una idea real, especialmente en casos de criaderos muy grandes, pero si es cuidadosamente realizado bajo condiciones estandarizadas en criaderos seleccionados, pueda dar una idea aproximada de los cambios relativos en el número de larvas. Materiales y Métodos Aplicables 1. 2. 3. 4. Reconocimiento Geográfico. Georeferenciación de los criaderos. El cucharon debe ser inclinado sobre la superficie del agua. La colecta de larvas debe ser realizada en lugares distantes hasta máximo 2 km de las viviendas. Se escoge un punto de exploración cercano a la orilla (punto inicial), donde se realizarán diez cucharonadas, luego se continuará al siguiente punto del mismo criadero (donde se realizarán otras 5 cucharonadas) y de esta manera se continúa la exploración por la orilla del criadero, cuando sea posible. 5. Caracterización geográfica y de algunas variables climáticas (si hay facilidad) del área de estudio. 6. Medición de la Superficie Activa de Criadero 7. Se recomienda un total de 10 puntos explorados por criadero (100 cucharonadas) como mínimo, sin embargo, el total puntos para evaluar el criadero dependerá del tamaño del mismo. Como ya se indicó si el criadero tiene menos de cinco metros se 96 8. 9. 10. 11. trabajará con un punto por metro, para criaderos más extensos se trabajará en un punto cada 5 o 10 metros. El mismo número de cucharonadas (10) deberá ser mantenido para cada sitio de captura en las observaciones subsiguientes. Para el cálculo de la densidad larvaria se debe calcular la suma del 1 y 2 estadio y la del 3 y 4 estadio de cada especie colectada por el número de cucharonadas Identificación, caracterización, mapeo de criaderos positivos y determinación de densidad larvaria (estadios). Manejo de Formularios Entomológicos OBTENCION DEL INDICE DE DENSIDAD LARVARIA PERIMETRO DEL CRIADERO (EN METROS) Menor o igual 20 m No. CUCHARONADAS 1 cucharonada cada / metro De 21 – 99 m De 100 – 1000 m Mayor de 1000 m 1 cucharonada cada / 2 mts 1 cucharonada cada / 5 mts 1 cucharonada cada / 10 mts Máximo hasta 100 cucharonadas Total de larva colectadas DENDIDAD LARVAS POR CUCHARONADA= -------------------------------------- x 0.01 Rangos de la densidad larvaria de anopheles (larva x cucharonada MUY BAJA 0-1 Larva / cucharonada BAJA 2-5 Larva / cucharonada MEDIANA 6-20 Larva / cucharonada ALTA >21 Larva / cucharonada Fuente: OPS-OMS / MOVIMONDO – MINSA / NIC COMPONENTE 3 Transmisión vectorial de la Enfermedad de Chagas interrumpida en áreas con vectores domiciliados y mejorando la detección y tratamiento oportuno de casos Actividad 3.1 Creación a nivel zonal de núcleos de trabajo para priorizar distritos, orientar acciones para la detección y manejo de casos (prioridad niño), aplicación de manuales de normas y procedimientos (protocolos) de diagnóstico, tratamiento etiológico y manejo de las complicaciones cardiacas y/o digestivas además identificar probables brotes de Chagas por vía oral. 97 Actividad Metodología Insumos Descripción de requerimiento REGION AMAZONICA 6 profesionales (uno por provincia) para Sucumbíos, Orellana, Napo, Pastaza, Morona y Zamora que realizaran las siguientes actividades: a.- Vigilancia Epidemiológica Integral de 3.1 Creación a nivel Chagas en la región amazónica y coordinar zonal de núcleos de acciones intra e intersectorial (con las trabajo para priorizar dependencias del MSP y organizaciones distritos, orientar involucradas en el control de Chagas). acciones para la b.- Mantener la coordinación con las zonas y el detección y manejo de programa. casos (prioridad niño), c.- Información epidemiológica y de novedades Se adquieren Contratación aplicación de en su área de acción. a través del de personal manuales de normas y portal de procedimientos REGION EXTRA-AMAZONICA compras (protocolos) de 4 profesionales (uno por provincia) para públicas y diagnóstico, Manabí, Guayas, Los Ríos y Santo Domingo sistema tratamiento etiológico que realizaran las siguientes actividades: esipren y manejo de las a.- Vigilancia Epidemiológica Integral de complicaciones Chagas y coordinar acciones intra e cardiacas y/o intersectorial (con las dependencias del MSP y digestivas además organizaciones involucradas en el control de identificar probables Chagas). brotes de Chagas por b.- Mantener la coordinación con las zonas y el vía oral. programa. c.- Información epidemiológica y de novedades en su área de acción. Prendas de Mandil, mascarillas, visores plásticos, guantes protección quirúrgicos, gafas protectoras Movilización Vehículo de la Institución. Metodología: En cada una de las Coordinaciones Zonales de la Región Amazónica y Extra-Amazónica se formaran núcleos técnicos para el control y vigilancia de la Enfermedad de Chagas. El profesional responsable de las investigaciones serológicas tiene además la responsabilidad de coordinar con las autoridades respectivas (Zonas y Distritos) las acciones y estrategias que se emprenderán en las distintas localidades donde se realizaran las actividades. Los operadores de campo cumplirán actividades de control y vigilancia, las mismas que serán el producto de los resultados que den las encuestas serológicas. (Método Ruta Inversa); por lo que las acciones de vigilancia entomológica sean selectivas. Los núcleos técnicos Zonales recibirán capacitación que tiene como propósito conocer protocolos, Normas y procedimientos para el control de Chagas por parte del MSP y lograr mediante reuniones técnicas de trabajo que los equipos de conducción de Distritos y Circuitos cumplan y hagan cumplir los procedimientos para lograr su estandarización. 3.2 Fortalecer la capacidad de laboratorio a nivel distrital y/o zonal en métodos parasitológicos para el diagnóstico de Chagas agudo, serológicos y confirmatorios. 98 Actividad 3. 2 Fortalecer la capacidad de laboratorio a nivel distrital y/o zonal en métodos parasitológicos para el diagnóstico de Chagas agudo, serológicos y confirmatorios. Metodología Insumos Materiales didácticos suministros Se adquieren a través del Materiales laboratorio portal de compras publicas Prendas protección Movilización Descripción de requerimiento Guías, Protocolos, Fichas, Folletos, Dípticos, y otros. y Cuadernos espirales universitarios, plumas, lápices, CD, borradores. Reactivos para Chagas: Elisa, HAI, IFI. Giemsa, papel filtro Tubos tapas rojas, agujas tomas múltiples, viales plásticos de 2ml con tapa rosca, puntas amarillas, de puntas azules, cajas térmicas descartables, algodón, alcohol, fundas rojas y negras, torniquete plano, guardianes, Marcador para CD, Pipetas Pasteur Plásticas, tubos heparinizados para microhematocrito, Laminas porta objeto, Láminas cubre objeto, Micropipeta 100-1000ul. de Mandil, mascarillas, visores plásticos, guantes quirúrgicos, gafas protectoras Vehículo asignado al programa. Metodología de laboratorio para el diagnóstico de la enfermedad de Chagas. El diagnóstico de laboratorio de la Enfermedad de Chagas, depende de la fase clínica de la enfermedad en la que se encuentre el paciente. En aquellos pacientes que se sospeche están en periodo agudo, deberán realizarse los exámenes directos lo antes posible, puesto que el estado febril es la mejor forma y segura de encontrar parásitos y para la serología se deberá esperar a lo menos 15 días. No es necesario que el paciente este en ayunas en el momento de tomarse la muestra. Las herramientas de diagnóstico pueden ser divididas en: 1. Técnicas de demostración directa del parásito o métodos parasitológicos. 2. Métodos inmunológicos. 3. Procedimientos con base en la identificación de sus productos genómicos o moleculares. 1. METODOS PARASITOLÓGICOS. 1.1. Métodos Directos: Frotis. Examen directo de sangre en fresco. Micro hematocrito. Técnica de Strout. Quantitative buffy coat (QBC). 1.2. Métodos Indirectos: Xenodiagnóstico. 99 Hemocultivo. 2. MÉTODOS INMUNOLÓGICOS Reacción de fijación del complemento (Guerrero Machado). Inmunofluorescencia Indirecta. ELISA. Hemoaglutinación Indirecta. Western blot 3. MÉTODOS MOLECULARES PCR. 1. MÉTODOS PARASITOLÓGICOS. 1.1. Métodos parasitológicos directos: En las situaciones en que las parasitemias son altas como en la fase aguda de la enfermedad, el frotis y el examen en fresco son buenos métodos para identificar el parasito. Si las manifestaciones clínicas han estado presentes por más de 30 días, es posible una caída de la parasitemia, recomendándose entonces emplear las técnicas de micro hematocrito y QBC. Una vez visualizado el parasito, está confirmado el diagnóstico, no habiendo necesidad de otros exámenes. Frotis y gota gruesa El frotis de sangre periférica y gota gruesa (fijación y tinción por Giemsa) permiten evaluar la morfología de los trypomastigotes circulantes (formas alargadas de 15delgadas, provistas de membrana ondulante con flagelo anterior, núcleo central, kinetoplasto voluminoso posterior rojo-morado y citoplasma azulado); la sensibilidad de esta técnica es menor del 60%, pero es de utilidad para el diagnóstico diferencial con T. rangeli (más delgado y largo, con kinetoplasto pequeño puntiforme). Técnica: Coloración del frotis de sangre periférica con Giemsa y examen microscópico de la placa para visualizar el parásito. Es un método simple y sencillo en las situaciones en que la parasitemia es elevada como en la fase aguda. Técnica para colecta de material: Material utilizado Lanceta Algodón 100 Alcohol Laminas porta objeto (limpias y secas) Guantes Formulario. Colorantes. Agua destilada. Procedimiento Hacer desinfección del dedo índice o anular con alcohol y algodón. Con la lanceta realizar la punción en un costado del dedo elegido. Presionar el dedo suavemente hasta forma una gota, la cual será eliminada con un algodón seco. Presionar nuevamente el dedo hasta formar una gota. En una lámina porta objeto colocamos dos gotas y con una se procede a hacer el extendido o frotis y con la otra se prepara la gota gruesa. Dejar secar al ambiente, hasta que la sangre este completamente seca. Una vez seca procedemos a realizar la tinción. Preparamos el colorante: 1 gr. de azul de metileno en 250 ml de agua destilada, una vez preparada la colocamos en un vaso. Sumergimos la lámina en el azul de metileno por un segundo. Luego en un vaso colocamos agua destilada, sumergimos la lámina en el agua destilada por un segundo. La placa la colocamos en una superficie no muy plana con la cara que contiene el frotis hacia abajo. En una probeta pequeña se mezclan 2 ml de agua destilada y 4 gotas de Giemsa. Procedemos a verter el preparado a un lado de la lámina hasta que la cubra totalmente. Esperamos 15 minutos. Enjuagamos la lámina en el vaso que contiene agua destilada por un segundo. Escurrimos en una esponja. Dejamos secar al ambiente. Cuando este la placa completamente seca procedemos a enfocar en el microscopio en objetivo de 40x o 100x. 101 En la observación microscópica deben buscarse en forma de trypomastigotes en forma de S o C, alargados de 15-20mm, más o menos delgadas, provistos de membrana ondulante con flagelo anterior, núcleo central, kinetoplasto voluminoso posterior rojo-morado y citoplasma azulado. Examen directo en sangre fresca. El examen microscópico directo en fresco puede usarse para detectar la presencia de parásitos hemoflagelados móviles (ocular 10x y objetivo 40x); debe repetirse 4 veces diarias por 4 a 5 días, lo que genera una sensibilidad del 80-90%. Técnica: Consiste en examinar una gota de sangre obtenida por punción de la yema del dedo colocada en una lámina porta objeto y cubierta con una laminilla. Se trata de visualizar los movimientos del tripomastigote a 400 aumentos. Es necesario examinar 100 campos microscópicos para poder descartar la presencia del parásito. Esta técnica es más sensible que el frotis. Material utilizado Lanceta Algodón Alcohol Laminas porta objeto (limpias y secas) Guantes Laminilla cubre objeto Procedimiento Hacer desinfección del dedo índice o anular con alcohol y algodón. Con la lanceta realizar la punción en un costado del dedo elegido. Presionar el dedo suavemente hasta forma una gota, la cual será eliminada con un algodón seco. Presionar nuevamente el dedo hasta formar una gota. En una lámina porta objeto colocamos la gota, le colocamos el cubre objeto. Observamos en el microscopio en objetivo de 40x o 100x. Microhematocrito Técnica: Colectar sangre en un tubo capilar y centrifugar. El buffy coat (camada leucocitaria presente entre los glóbulos rojos y el plasma) es examinado al microscopio a fin de visualizar el movimiento del tripomastigote. La sensibilidad de este método puede llegar al 90 %. Técnica de Strout Este método concentra los elementos parasitarios mediante centrifugación. La especificidad es del 100% y la sensibilidad es del 95 %. Material utilizado 102 Procedimiento Guantes Aguja vacutainer de 3cm o 5cm Tubo tapa roja Alcohol Algodón Campana Colecta de sangre (mínimo 3 ml), sin anticoagulante Dejarlo a 37ºC durante 2 horas para la formación y retracción del coagulo. Recoger el líquido en un tubo y centrifugar (5 minutos a 400 rpm). El suero obtenido transferirlo a otro tubo y someterlo a centrifugación (10minutos a 400g aprox 2000rpm). El sobrenadante constituido por suero límpido, se elimina y se hace una preparación en fresco con la última gota del sedimento. Se toma este material con una pipeta y se procede a colocarlo en una lámina porta objeto. Se la cubre con una laminilla y se observa al microscopio en objetivo de 40x o 100x. Quantitative Buffy Coat (QBC) Técnica: Se toma sangre en un tubo capilar de QBC recubierto con naranja de acridina (colorante fluorescente) el mismo que es centrifugado. Los parásitos teñidos entonces pueden ser observados con luz ultravioleta en la interface entre los glóbulos rojos y el plasma. La sensibilidad de este método llega al 90 %. 1.2. Métodos parasitológicos Indirectos: La limitación de estos métodos es su baja sensibilidad lo que compromete el diagnóstico y control terapéutico de la enfermedad. Xenodiagnóstico El fundamento de este es la simulación en el laboratorio, de las condiciones naturales del ciclo evolutivo del T. cruzi en los triatominos hasta entonces libres de infección. Presenta un 100 % de sensibilidad en la fase aguda. Técnica: Se realiza con ninfas de tercer estadio criadas en laboratorio y alimentadas con sangre de aves para garantizar que no estén infectadas previa a la aplicación sobre el antebrazo del paciente por 30 minutos. Después de 30 a 60 días se examina microscópicamente el contenido intestinal del triatomino y se determina la presencia del parásito. Sus limitaciones son las reacciones locales de hipersensibilidad, el tiempo que toma para obtener resultados (90 días) y su no aceptación por algunos pacientes por lo que cada vez es menos utilizada. 103 Hemocultivo La positividad de esta prueba puede variar de 0 % a 99 %. Esta discrepancia puede ser justificada según la fase de la enfermedad en la que se hace la investigación (aguda, indeterminada o crónica) y por el protocolo adoptado. En general, los procedimientos adoptados para elevar la positividad de este examen son: Utilización del medio LIT (liver infusión tryptose). Utilización de hemocentrigugación (buffy coat). Alargamiento del tiempo de cultivo por 120 días. Disminución del tiempo de procesamiento. Disminución de la manipulación de las muestras de sangre. Elevación del número de muestras colectadas. Elevación del volumen de sangre colectado (30 ml). La técnica de Hemocultivo ha mostrado ser un método indirecto razonable para la detección de tripanosoma cruzi, teniendo su uso primario en la fase aguda. 2. MÉTODOS INMUNOLÓGICOS Reacción de fijación del complemento (Guerrero Machado). Este método se basa en el hecho de que una reacción antígeno – anticuerpo puede semejar la unión de proteínas del sistema de complemento, que se unen a la fracción Fc del anticuerpo y se activan en cascada para la formación de una estructura molecular. Técnica: El suero del paciente es adicionado al medio que contiene antígenos tripanosómicos. Si hubiera anticuerpos anti – T. cruzi en el suero adicionado, la unión consiguiente deberá fijar y consumir las proteínas del sistema de complemento presentes. Se adicionan glóbulos rojos de carnero y hemolisinas (anticuerpos anti glóbulos rojos de carnero) al medio. Habiendo sido consumido el complemento en la reacción, no habrá lisis de los glóbulos rojos adicionados y por lo tanto el resultado será positivo. Actualmente y sobre todo en Brasil existe el consenso de abandonar este método. Inmunofluorescencia Indirecta Es uno de los métodos más utilizados para el diagnóstico de Chagas, siendo con el ELISA y la hemaglutinación indirecta, uno de los más recomendados por la Organización Mundial de la Salud (OMS) para el diagnóstico de esta enfermedad. Técnica: Un anticuerpo conjugado a una molécula de fluoresceína y un anticuerpo anti – T. cruzi son adicionados a una lámina conteniendo el suero del paciente. Si el complejo antígeno tripanosómico -T. cruzi – IgM/anti.T. cruzi estuvieran presentes en la muestra, el anticuerpo 104 anti-IgM anti – T. cruzi se unirá a la fracción Fc de la IgM de este complejo. El anticuerpo conjugado a la fluoresceína se ligará a la fracción FC del anticuerpo anti – IgM anti- T. cruzi, produciendo una fluorescencia característica visible con el microscopio. Su sensibilidad varía de 93 al 100 % y su especificidad es de 99,7 %. Pueden ocurrir resultados falsos positivos en infecciones por Leishmania. ELISA (ENZIME – LINKED INMUNOSORBENT ASSAY) Es uno de los métodos más utilizados para el diagnóstico de Chagas y se basa en una reacción antígena – anticuerpo con formación de complejos, en que la presencia y concentración del antígeno son determinadas. Fundamentos del Método En esta técnica cualitativa para la detección de anticuerpos anti-T. cruzi, la muestra se diluye en el soporte en el que se encuentran inmovilizados antígenos recombinantes, obteniéndose un método de 3ª generación. Estos antígenos se obtiene por técnica de ADN recombinante a partir de proteínas específicas de los estadios espimastigote y tripomastigote del T. cruzi, correspondientes a zonas altamente conservadas entre distintas cepas. Si la muestra contiene los anticuerpos específicos, estos formaran un complejo con los antígenos y permanecerán unidos al soporte. La fracción no unida se elimina por lavado tras lo que se agregan anticuerpos anti-inmunoglobulina humana conjugados con per oxidasa. En los casos en que se haya unido el conjugado habrá aparición de color celeste. La fracción se detiene con ácido sulfúrico, con lo que el color celeste vira al amarillo. Reactivos Provistos Poli cubeta sensibilizada: con antígenos recombinantes de T. cruzi Conjugado: anti – inmunoglobulinas humanas (cabra) conjugadas con per oxidasa Revelador A: peróxido de hidrogeno Revelador B: tetrametilbencidina Stopper: ácido sulfúrico 2N Buffer de lavado concentrado: cloruro de sodio 1,4 mol/1 en buffer fosfatos 100mmol/l Diluyente de muestras Control positivo Control negativo Adhesivos para sellar la policubeta Material no proviso Micropipetas capaces de medir los volúmenes indicados. Reloj alarma o cronometro Estufa a 37ºC 105 Espectrofotometro para lecturas de poli cubeta (opcional) Estabilidad e instrucciones de almacenamiento de las muestras Los reactivos provistos son estables en refrigerador (2-10 ºC) hasta la fecha de vencimiento indicada en la caja. No congelar. Buffer lavado: estable 3 meses a temperatura ambiente. Poli cubeta sensibilizada: las tiras de pocillos inmovilizados se proveen cerradas al vacio y con desecante. No abrir el envoltorio hasta el momento de usar, ni antes que haya tomado temperatura ambiente, de lo contrario se favorecerá la humectación del contenido. Las tiras de pocillos no utilizadas deben conservarse dentro del sobre con el desecante, cerrado con cinta autoadhesiva y a2-10 ºC. Las tiras conservadas en estas condiciones pueden ser utilizadas dentro de los 5 meses posteriores mientras no se supere la fecha de vencimiento del equipo. Estabilidad e instrucciones de almacenamiento del Kit Los reactivos provistos son estables en refrigerador (2-10 ºC), hasta la fecha de vencimiento indicada en la caja Buffer de lavado estable 3 meses a temp. Ambiente Poli cubeta sensibilizada No abrir el envoltorio de los pocillos hasta el momento de usar ni antes que haya tomado temperatura ambiente. Las tiras que no se utilizan deben conservarse dentro del sobre con el desecante, cerrado con cinta autoadhesiva y a 2-10 ºC. Procedimiento: Llevar a temperatura ambiente los reactivos y las muestras antes de iniciar la prueba. Una vez iniciado el procedimiento debe completarse sin interrupción. Procesar simultáneamente 2 controles positivos (CP) 3 negativos (CN) y los desconocidos (D). Al depositar la muestra y/o controles sobre el diluyente de muestra, debe asegurarse de colocar los mismos en el seno del líquido y no sobre las paredes o el fondo del pocillo. Enjuagar la pipeta con el diluyente dispensado en el pocillo para asegurar la correcta homogenización. En los pocillos a utilizar de la policubeta colocar: 106 Diluyente de muestra Control positivo Control negativo muestra CP 200ul CN 200ul 10ul 10ul - 10ul - Mezclar aplicando suaves golpes en los laterales de la policubeta cargados las muestras en cada tira. Para evitar la evaporación, cubrir la placa e incubar en la estufa 30 minutos a 37 ºC. Luego aspirar cuidadosamente el líquido de cada pocillo recibiéndolo en un recipiente para desechos biológicos que contenga 5% de hipoclorito sódico. A continuación lavar 5 veces con buffer de lavado empleando aproximadamente 300ul/vez/pocillo. Después de cada lavado, el líquido se descartará también en el recipiente con hipoclorito. Opcionalmente, emplear lavador automático. Al finalizar el ultimo lavado, eliminar por completo el líquido residual, invirtiendo la policubeta y golpeándola varias veces sobre papel absorbente, ejerciendo una leve presión con la mano sobre los laterales mayores del soporte, para evitar la caída de las tiras de pocillo: Conjugado D 200ul 1 gota 1 gota 1 gota En caso de utilizar micropipeta automática, dispensar 50ul. Mezclar aplicando suaves golpes en los laterales de la policuebta durante 10 segundos. Para evitar la evaporación, cubrir la placa e incubar durante 30 minutos en estufa a 37ºC. Luego aspirar el líquido de los pocillos, recibiéndolo en el recipiente con hipoclorito y lavar según se indicó más arriba. Al finalizar el último lavado, eliminar por completo el líquido residual, invirtiendo la policubeta y golpeándola varias veces sobre papel absorbente, ejerciendo una leve presión con la mano sobre los laterales mayores del soporte, para evitar la caída de las tiras de pocillos. Luego agregar en cada pocillo: Revelador A 1 gota 1 gota 1 gota Revelador B 1 gota 1 gota 1 gota En caso de utilizar micropipeta automática, dispensar 50ul. Mezclar aplicando suaves golpes en los laterales de la policubeta durante 10 segundos. Incubar 30 minutos a temperatura ambiente y luego agregar: 107 Stopper 1 gota 1 gota 1 gota En caso de utilizar micropipeta automática dispensar 50ul. Mezclar aplicando suaves golpes en los laterales de la policubeta durante 10 segundos. Leer en espectrofotómetro a 450nm o bicromatica a 450/620-650nm o evaluar el resultado a simple vista por comparación con los controles positivos y negativos. HEMOAGLUTINACIÓN INDIRECTA Prueba de hemaglutinación indirecta para la detección de anticuerpos contra el Tripanosoma cruzi, se considera una técnica sencilla con limitaciones operativas, pero de adecuada sensibilidad y especificidad. Reactivos provistos Reconstituyente HAI: Antígeno HAI: liofilizado de GR. De carnero sensibilizados con antígenos citoplasmáticos de T. cruzi. GR no sensibilizados: suspensión al 1% de eritrocitos de carnero no sensibilizados, para control de heterofilia. Buffer HAI: solución fisiológica tamponada con fosfatos a pH 7,5, con colorante inerte. Solución Proteica: solución de albúmina bovina al 10%. 2. Mercaptoetanol: ampolla con 2-mercaptoetanol (2-ME). Control Positivo: suero inactivado conteniendo anticuerpos contra Tripanosoma cruzi. Control Negativo: suero no reactivo, inactivado. Reactivos no provistos Solución fisiológica Procedimiento: Seleccionar una policubeta con pocillos sin usar de fondo en U. Para eliminar la carga electrostática es necesario pasar un trapo húmedo por la base de la misma. TITULACION SIN 2 – ME 1. Dispensar 25 ul (microdilutor o micropipeta) de diluyente de sueros HAI en todos los pocillos a usar (6diluciones). 2. Colocar 25 ul de suero en el primer pocillo homogenizar aspirando y eliminando. Realizar las diluciones pasando de pocillo en pocillo y los últimos 25 ul descartarlos. 3. Utilizar controles. 4. Colocar en los pocillos con las diluciones ½ y ¼ 25 ul de GR. no sensibilizados (control de heterofilia). 5. En el resto de pocillos, agregar una gota 25 ul de antígeno HAI (frasco ámbar ya preparado y dura par 40 determinaciones aprox. 6. Mezclar aplicando suaves golpes en los laterales de la policubeta. 108 7. Dejar en reposo 90 minutos protegiendo la policubeta de vibraciones. 8. Leer. Preparación de los Reactivos: Diluyente de suero HAI para más o menos 6 determinaciones. Estable en el refrigerador por 5 días a partir de la fecha de preparación a temp. De 2 a 10ºC. Solución proteica + Buffer HAI Mezclar rotular y fechar 20 ul 1 ml 5 días de estabilidad Antígeno HAI (frasco ámbar + reconstituyente). Papel filtro Materiales Hojas de registro de encuestados Escribir los datos en las hojas de registro antes de tomar muestras Papel filtro Wathman No. 1 con área demarcada con lápiz (cuadrado de 15 x 15 mm.) para llenar con sangre capilar Medidas de Bioseguridad: USO DE GUANTES Procedimiento: Anotar en la ficha los datos indicados Doblar cada papel filtro por la mitad sin tocar el cuadro demarcado y anotar el código de identificación Los papeles deben estar sobre una superficie limpia Limpiar el dedo con alcohol Pinchar con la lanceta y llenar el cuadrado marcado en papel filtro Colocar los papeles sobre la mesa hasta que se sequen Colocar las muestras ya secas y cruzadas para evitar contacto entre ellas Guardarlas en una bolsa plástica con sus correspondientes datos Enviar al laboratorio lo más pronto, protegiéndolas del calor, humedad y algún otro factor que las deteriore En el laboratorio deberán mantenerse en refrigeración hasta el momento de realizar las pruebas serológicas. 109 WESTERN BLOT Es una técnica para la detección de proteínas antigénicas tripanosómicas en la sangre del paciente a través de anticuerpos anti – T. cruzi marcados, útil para la confirmación de resultados obtenidos con los otros métodos inmunológicos Técnica: La muestra, conteniendo una mezcla de antígenos tripanosómicos es desnaturalizada y sometida a electroforesis en gel de poliacrilamida con SDS (sodium dodecyl sulphate) y entonces sus diversas fracciones son separadas de acuerdo con el peso molecular y la carga eléctrica. Estas fracciones son transferidas a partir de este gel para una membrana de soporte a través de capilaridad (bloting) o electroforesis. El patrón de separación obtenido en el gel de poliacrilamida será mantenido en la membrana de soporte. Anticuerpos anti –T. cruzi serán incorporados a la membrana de soporte. Si fueran radio marcados, el complejo proteína antigénica tripanosómica/anticuerpo anti – T. cruzi será visible por auto radiografía; si fueran marcados por enzima, serán visibles como una quimioluminiscencia registrada en película fotográfica. 3. MÉTODOS MOLECULARES PCR (Reacción en cadena de Polimerasa). PCR es una técnica utilizada en biología molecular capaz de amplificar una secuencia conocida de DNA. Se trata de un examen molecular con base al conocimiento previo de una secuencia de DNA de hasta 1 kb, característica de la especie o célula que se desea detectar, y en la síntesis de una secuencia complementaria denominada praimer (primer) o iniciador. El primer se debe parear con el segmento correspondiente de una de las astas de DNA estudiado si la misma realmente existe en la muestra, posibilitando su detección. En la fase crónica la PCR puede ser útil como prueba confirmatoria con una sensibilidad descrita de 96,5 % a 100 % en pacientes con serología positiva y de 4,3 % a 46, 2 % en pacientes con serología no conclusiva. Para esta prueba se utiliza sangre total con anticoagulante cantidad mínima: 1 ml. Se excluye el uso de heparina. También, se puede recolectar sangre total con guanidina (1:4) y sangre en papel filtro. Resumen sobre métodos de diagnóstico de la Enfermedad de Chagas: MÉTODO DE LABORATORIO Frotis y gota gruesa Examen directo de sangre en fresco. ESPECIFICACION Son altamente sensibles y específicos en la fase aguda. Una vez visualizado el parasito, está confirmado el diagnostico, no habiendo necesidad de otros exámenes. Micro hematocrito. Técnica de Strout. Quantitative buffy coat (QBC). Xenodiagnóstico Presenta un 100 % de sensibilidad en la fase aguda. Se encuentra en desuso. Hemocultivo La positividad de esta prueba puede variar de 0 % a 99 %. 110 Inmunofluorescencia Indirecta. ELISA Papel filtro Su sensibilidad varía de 93 al 100 % y su especificidad es de 99,7 %. Pueden ocurrir resultados falsos positivos en infecciones por Leishmania. Este método se detectara en fluidos biológicos como suero, sangre o plasma. Son altamente específicos y altamente sensibles. Son altamente específicos y altamente sensibles. Método de hemaglutinación indirecta Prueba de hemaglutinación indirecta para la detección de anticuerpos contra el Tripanosoma cruzi, se considera una técnica sencilla con limitaciones operativas, pero de adecuada sensibilidad y especificidad. WESTERN BLOT PCR Pruebas rápidas Es una técnica para la detección de proteínas antigénicas tripanosómicas en la sangre del paciente a través de anticuerpos anti – T. cruzi marcados. Útil para la confirmación de resultados obtenidos con los otros métodos inmunológicos. En la fase crónica la PCR puede ser útil como prueba confirmatoria con una sensibilidad descrita de 96,5 % a 100 % en pacientes con serología positiva. Son pruebas auxiliares Resultados en 10 a 20 minutos. No necesita de equipos y reactivos sofisticados. Se puede realizar en un área pequeña. No requiere equipo especial para conservación de la muestra. Ideal para sitios con pocas muestras. Puede realizarse en plasma, suero, sangre venosa y/o capilar. 4. Aspectos a considerar para la conservación y transporte de muestras: Suero o plasma: Conservación: A más 4 ºC por un máximo de 5 días y congelada a menos 20 ºC, dependiendo del examen que se quiere realizar. Transporte: En tubo plástico con tapa hermética con las medidas necesarias de bioseguridad y para mantener la temperatura. El tubo con la muestra deberá ser rotulado correctamente. Sangre total para Métodos Directos Conservación: A más 4 ºC por un máximo de 3 días. Transporte: En tubo plástico con tapa hermética con las medidas necesarias de bioseguridad y para mantener la temperatura. 111 En caso de envió de las muestras al SNEM, deberán llegar al laboratorio los viales herméticamente cerrados con todas las medidas de bioseguridad previamente y correctamente rotulados. La identificación corresponderá con la hoja de registro de las personas muestreadas y deberán ser enviadas en cadena de frio, vendrá señalado en aquella hoja la procedencia de las muestras como: provincia, cantón, parroquia, localidad y el nombre de la escuela si el muestreo es dirigido a la población escolar. 5. Funciones y responsabilidades de los laboratorios de diagnóstico de Chagas. Los laboratorios emitirán un reporte de los resultados de las pruebas realizadas al laboratorio del nivel central del SNEM y este a su vez al Epidemiólogo del Programa Nacional de Chagas. Los laboratorios locales según su capacidad realizaran el diagnostico de las enfermedades sujetas a vigilancia como: Paludismo, Chagas y Leishmaniasis. Los resultados reactivos deberán ser confirmados por el l laboratorio de referencia nacional Instituto de Higiene. El laboratorio del nivel central realizara el control de calidad de los procedimientos de laboratorio a toda la red de laboratorios de Chagas a nivel nacional del Ministerio de Salud Pública envió de las muestras al SNEM, deberán e bioseguridad previamente y correctamente rotulados. La identificación 6. Medidas de bioseguridad en los Laboratorios Conducta Individual: Toda persona debe lavarse las manos antes y después de manipular un paciente o material potencialmente infeccioso. Evite el contacto de piel o mucosas con sangre o sus derivados, mediante el uso de guantes desechables. Los momentos en los cuales se estará en posible riesgo son: toma de la muestra a los pacientes, manejo de muestras o en superficies contaminadas con material biológico. Si presenta lesiones de piel o mucosa, evitar el contacto con los pacientes o material potencialmente contaminante. En el laboratorio es necesario usar mandil, uniforme u otra vestimenta para protección apropiada. Prohibido ingerir alimentos en el laboratorio. Todo el personal dedicado a labores de manejo de residuos debe contar con un esquema de vacunación completo contra el Tétanos y Hepatitis B. Prohibido maquillarse en el laboratorio. De llegar a tener un accidente de laboratorio como la posible inoculación de material contaminado por la punción con un objeto corto punzante o lanceta usada y con sangre visible, debe informarlo inmediatamente a su jefe inmediato o al departamento de salud ocupacional antes de 24 Horas de ocurrido el evento, para proceder según normas. Además de la anterior medida en caso de exposición tenga presente el lavado del área expuesta. 112 a) Exposición percutánea: lave inmediatamente el área expuesta con agua y jabón germicida, si la herida está sangrando, apriétela y estimule el sangrado, siempre que el área corporal lo tolere y aplique solución desinfectante después de concluido el lavado. b) Exposición de mucosas: lave profusamente el área con agua limpia o solución salina estéril. c) Exposición en piel no intacta: lave el área profusamente con solución salina estéril y aplique solución antiséptica. d) Exposición en piel intacta: lave abundantemente el área con agua y jabón. Manejo del paciente, desechos y sitio de trabajo. Paciente Emplear técnicas de limpieza en la toma de muestra. Siempre usar hojas de bisturí y/o lancetas desechables y nuevas para la toma de la muestra de cada paciente. Desechos Desechar el material contaminado (hojas de bisturí, gasa, lancetas) en recipientes adecuados o fundas plásticas destinadas para este propósito. De presentarse la ruptura de material de vidrio contaminado con sangre o fluidos corporales, adicione hipoclorito de sodio al 0,5%, deje media hora y recoja los fragmentos de escoba y recogedor para su disposición final. Sitio de Trabajo Se debe mantener el laboratorio limpio, aseado y ordenado. La superficie de trabajo debe descontaminarse regularmente con una solución de hipoclorito de sodio al 5%. En caso de derrame o contaminación con sangre o fluidos corporales, se deben aplicar con elementos absorbentes y sustancias desinfectantes la solución ya indicada por el lapso de 30 minutos, lavar luego con abundante agua y jabón. TECNICAS DE DIAGNOSTICO DE LABORATORIO Y SU SEGUIMIENTO TECNICAS DE DIAGNOSTICO Gota fresca Concentración Strout Hemocultivo Xenodiagnóstico PCR Pruebas Serológicas (HAI, ELISA, IFI) FORMAS CLINICAS DE LA ENFERMEDAD DE CHAGAS AGUDA (+) (++) (+++) (+++) (++++) (-) Inicio (++) Después de 15 días CRONICA - PORTADOR (-) (-) (+-) (+) (++) (++++) CONGENITA (+++) (+++) (+++) (+++) (++++) IgG(+) Madre IgM (+) Recién nacido 3.3 Dar continuidad al tamizaje universal en donantes de sangre optimizando calidad en las acciones y correcta derivación del paciente para confirmación diagnóstica y atención médica. 113 Actividad Metodología 3.3 Coordinar con la Cruz Roja y Bancos de Sangre la derivación de sero-reactivos a Chagas Coordinación con bancos de sangre Insumos Descripción requerimiento Suministros Papelería de Metodología Se llevara a cabo con el 100% de tamizaje serológico para detectar Ac anti T cruzi a los donantes en la Cruz Roja y Bancos de sangre del país y control de calidad establecido (PEED). Se coordinara y receptara información de la Cruz Roja y Bancos de Sangre del país en relación al tamizaje de Ac Anti T. cruzi. Se coordinara con las Instituciones pertinentes, para establecer un proceso de educación continua al personal de laboratorio. Receptar información de Monitoreo y evaluación del desempeño de los laboratorios que participan en el control de calidad (PEED). Sistematizar la información y dar seguimiento a los donantes seropositivos. Es la segunda vía de transmisión de T cruzi a humanos (alrededor del 16% de casos de EC). Su importancia es mayor en áreas urbanas libres de vectores, pero que han sido receptoras de inmigrantes procedentes de áreas endémicas. Así el control serológico de las donaciones a Bancos de sangre es el complemento necesario de todo programa de control de vectores y de hecho en Ecuador existe la obligación legal de analizar todas las donaciones de sangre para detectar la presencia de anticuerpos anti-T. cruzi. 3.4 Garantizar disponibilidad del medicamento para tratamiento etiológico Actividad 3.4 Garantizar disponibilidad del medicamento para tratamiento etiológico Metodología Se adquieren a través de la Organización Panamericana de la Salud (OPS) Insumos Descripción requerimiento Medicinas Nifurtimox de Metodología Esta actividad se llevara a cabo mediante el procedimiento de compras públicas a través de la importación directa mediante la participación de la OPS. Existen dos alternativas de tratamiento etiológico: Nifurtimox y Benznidazole; El procedimiento para la adquisición del Benzonidazole es mediante compras públicas; en el caso del medicamento Nifurtimox, se lo solicita a la OPS Regional con sede en Montevideo-Uruguay, para lo cual se hace el requerimiento en base a la producción de casos y saldos de medicamentos. Es importante 114 indicar que el pedido de los medicamentos se la hace basada en el promedio de los registros históricos de pacientes con diagnostico confirmatorio de la enfermedad de Chagas; Para dar cumplimiento de la propuesta del Gobierno Nacional que todo caso diagnosticado debe ser tratado. Índice de infección humana activa: No. de niños menores de 15 años positivos X 100 No. de niños menores de 15 años tamizados Índice de infección en donantes de sangre: No. de donantes positivos No. de donantes tamizados X 100 Índice de curación postratamiento: No. de pacientes con negativización serológica No. de pacientes tratados X 100 El diagnóstico de la Enfermedad de Chagas considera los siguientes criterios: Epidemiológico Clínico Laboratorial. Epidemiológico: Lugar de residencia del paciente. Determinar si es área endémica de la enfermedad. Tipo de vivienda, de caña, madera y con techo de cade. Antecedentes de viajes a zonas endémicas de Chagas. Antecedentes de transfusiones de sangre o hemocomponentes 90 días previos a la consulta. Mujeres embarazadas provenientes de áreas de riesgo. Probabilidad de infección accidental: personal profesional y auxiliar de laboratorio manipulando material contaminado con T. cruzi. Antecedentes de trasplante de órganos de donantes con enfermedad de Chagas. Clínico: Historia Clínica (Anamnesis), Examen Físico Búsqueda de signos y síntomas de sospecha como: Fiebre inespecífica y variable Hepatomegalia y esplenomegalia Linfadenopatía Signo de chagoma (reacción inflamatoria en sitio de picadura) Signo de romaña (edema unilateral de ambos párpados) Carditis, miocarditis Dilatación cardíaca Trastornos del ritmo Megacolon 115 Megaesófago Meningo-encefalitis Laboratorio: Es fundamental para el diagnóstico definitivo de la enfermedad. Las técnicas de diagnóstico difieren de acuerdo a la fase o evolución de la enfermedad. Fase Aguda: Se inicia con el aparecimiento de los primeros signos y síntomas y dura aproximadamente 30 días. Técnicas de Diagnóstico: o Gota gruesa o Método de Strout o microStrout o Xenodiagnóstico o Hemocultivo: o PCR Tratamiento de la enfermedad de Chagas El tratamiento de los individuos infectados por el Tripanosoma cruzy puede abordarse de dos maneras diferentes: Etiológico y Sintomático. Es importante tener en cuenta que más de la mitad de los individuos infectados transcurren en la forma indeterminada de la fase crónica, es decir sin presentar manifestaciones clínicas y sin saber que son portadores de la infección. En esta fase el diagnóstico se realiza de manera accidental por donación de sangre, o por chequeo anual o por imposiciones laborales. Tratamiento Etiológico: Objetivos: a) Lograr la eliminación del parásito del organismo, b) Prevenir el aparecimiento de las complicaciones cardíacas, digestivas y otras. c) Evitar el agravamiento de las lesiones existentes. d) Garantizar la cura total del paciente Deben recibir tratamiento etiológico todos los pacientes que presenten Enfermedad de Chagas en su forma Aguda sin excepción pero también deben recibir tratamiento etiológico pacientes infectados por tripanosoma cruzi en las siguientes condiciones: Infección crónica indeterminada (recomendada de acuerdo a los criterios actuales a todas las edades) y de manera exclusiva en niños y menores de 15 años según normas internacionales. Infección crónica indeterminada de larga data y sintomáticos en mayores de 15 años y adultos previa evaluación del médico especialista, Infección congénita, Infección aguda secundaria a accidentes ocupacionales, trasplantes y transfusiones, Tratamiento Sintomático: 116 Objetivo: Evitar el agravamiento de las lesiones existentes que pueden poner en peligro la vida del paciente chagásico. Básicamente las complicaciones principales que se presentan en la enfermedad de Chagas son a nivel sistema cardiovascular y del aparato digestivo. Las manifestaciones clínicas más importantes de la miocardiopatía chagásica son la insuficiencia cardíaca, los trastornos del ritmo, los bloqueos auriculo-ventriculares y las embolias pulmonares. Estas patologías deben ser tratadas por el especialista en cardiología. A nivel del aparato digestivo, son frecuentes los trastornos del peristaltismo y el reflujo gastroesofágico dando como resultado trastornos como estreñimiento y esofagitis por reflujo. De igual manera como en el caso anterior esto debe ser manejador el especialista en gastroenterología. PROTOCOLOS DE TRATAMIENTO DE LA ENFERMEDAD DE CHAGAS BENZNIDAZOL (BNL) Considerada como droga de elección) Adultos y personas mayores de 15 años: 5-7 mg/Kg/día, c/8-12 hrs. durante 30-60 días. Niños de 15 años o menos: 5-10 mg /Kg/día, c/8-12 hrs. Durante 60 días. Escolares y adolescentes con peso de hasta 40Kg: 7.5 mg/Kg/cada 8-12 horas. Dosis diaria máxima: 400 mg. (si la dosis es mayor de 400 mg. hay riesgo de RAM). Presentación: tabletas ranuradas de 100 mg. Suspensión. NIFURTIMOX (NFX) Adultos: y niños mayores de 15 años: 8-10 mg/Kg/8 horas día durante 60-90 días Niños de 15 años o menos: 10-15 mg/Kg/día cada 8 horas (revisar con protocolo actual). Contraindicaciones de tratamiento: No se recomienda tratamiento para la enfermedad de Chagas en las siguientes condiciones: Embarazo Lactancia Insuficiencia hepática Insuficiencia renal Insuficiencia cardiaca Afecciones respiratorias severas Hipersensibilidad a cualquier componente de los medicamentos REACCIONES ADVERSA A LOS MEDICAMENTOS Tanto el Nifurtimox como el Benznidazol pueden producir efectos adversos y reacciones de toxicidad en el paciente, entre las cuales podemos mencionar: 117 1. Trastornos digestivos como epigastralgias, nausea, vómito, pérdida de peso hiporexia etc. Básicamente más frecuentes con el uso de NFX. 2. Alteraciones hematológicas como leucopenia, plaquetopenia y agranulocitosis y púrpura. Es poco frecuente la depresión medular intensa. 3. Dermopatia por hipersensibilidad poco frecuente, se presenta en un 30% de los pacientes tratados. Generalmente aparece a partir del noveno día de tratamiento y en ocasiones es tan intensa que amerita suspender el tto. 4. Polineuropatía, guarda relación con la dosis utilizada, a mayor dosis mayor probabilidad de aparecimiento de polineuropatía. 5. Anafilaxia con edema generalizado, fiebre, adenomegalias y artromialgias. Monitoreo del tratamiento: a) Monitoreo Clínico: Examen físico completo enfatizando en la búsqueda de reacciones adversas por lesiones cutáneas, neurológicas y alteraciones gastrointestinales. Debe ser semanal. Se recomienda que la primera semana el monitoreo clínico sea diario. El manejo hospitalario, es a criterio medico según el estado del paciente y la imposibilidad de asegurar el monitoreo. b) Monitoreo Bioquímico: Pruebas Basales: Hemograma, Pruebas de función hepática (TGO; TGP), creatinina. Repetir estas pruebas durante el tratamiento (aproximadamente a la mitad del inicio del mismo) y en el post tratamiento (15 días después). c) Monitoreo Parasitológico: Examen parasitológico basal de inicio y al 1er y 3er mes post tratamiento (Directo, Strout, Frotis). d) Monitoreo Serológico: Las pruebas serológicas (IFI, ELISA) deben ser basales, al año, a los dos años y al tercer año post tratamiento en los casos de Chagas agudo. Para los pacientes con Chagas crónico indeterminado las pruebas serológicas deben ser anuales, hasta los 2 años post tratamiento. 3.5 Vigilancia entomológica integral funcionando para el fortalecimiento de la capacidad de respuesta local, protocolos de encuestas triatominicas para estandarizar su aplicación y levantamiento de líneas de base. 118 Actividad Metodología Insumos Descripción de requerimiento REGION AMAZONICA CONTRATACION DE: 30 Operadores de campo (5 por cada provincia) para Sucumbíos, Orellana, Napo, Pastaza, Morona y Zamora. CAPACITACION EN: a.- Educación Comunitaria en el conocimiento de la enfermedad de Chagas para su prevención, en las localidades de mayor riesgo. b.- Búsqueda y captura de vectores de la enfermedad de Chagas, codificación y preparación de muestras. c.- Intervenciones para el control de Chagas (rociado selectivo cuando fuese necesario). PARA QUE REALICEN LA PROMOCION, PREVENCION Y LA VIGILANCIA ENTOMOLOGICA DE CHAGAS. Contratación de personal 3.5 Vigilancia entomológica integral funcionando para el fortalecimiento de la capacidad de respuesta local. REGION EXTRA-AMAZONICA CONTRATACION DE: 20 Operadores de campo (5 por cada provincia) Manabí, Guayas, Los Ríos y Santo Domingo. CAPACITACION EN: a.- Educación Comunitaria en el conocimiento de la enfermedad de Chagas para su prevención, en las localidades de mayor riesgo. b.- Búsqueda y captura de vectores de la enfermedad de Chagas, codificación y preparación de muestras. c.- Intervenciones para el control de Chagas, rociado selectivo en domicilio (intra y peri-domicilio) d.- Priorizar las provincias de Manabí (valle del Rio Portoviejo), Guayas (Cantones Guayaquil y sus parroquias rurales Progreso y Posorja; Playas, Pedro Carbo). Provincias en que la meta propuestas es la eliminación del vector domiciliado Triatoma dimidiata. PARA QUE REALICEN LA PROMOCION, PREVENCION Y LA VIGILANCIA ENTOMOLOGICA DE CHAGAS. Sistema que detecta factores de riesgo para contraer Chagas en los distintos estadíos y habitad del vector Equipos rociado de Para que estas actividades aprendidas las realicen en sus labores Mochilas, linternas, pilas, capturadores, fundas de plástico, Herramientas frascos de transporte y conservación, tela tul, bandas de latex, de trabajo crayones, tiza, lápiz, franelas, pinzas de captura, fundas para pesar insecticida. Uniformes completos, gorras, cascos, camisetas, botas de Uniformes de cuero, cascos, guantes de cuero, guantes de hule. campo y Mascarillas para insecticidas (con protector ocular y filtro de Prendas de carbono activado), mascarillas desechables, visores protectores Protección transparentes, y quirúrgicos, Franela. Materiales Toalla, Jabón tocador, detergente. de aseo Insecticida Deltametrina al 5% polvo mojable Movilización Vehículo de la Institución, 119 Metodología BUSQUEDA ACTIVA La visita domiciliaria comenzara con una explicación clara del trabajo que va a ser llevado a cabo a las personas responsables de la casa, destacando la importancia preventiva de la visita. La investigación debe iniciarse en el cuarto de acceso, comenzando hacia la izquierda y continuar en sentido de las macillas del reloj. Inspeccionar detenidamente, muebles, utensilios, adornos en las paredes etc. La aplicación del irritante de los insectos cuando se utilice, será simultánea. Se continuara en los siguientes cuartos en la misma secuencia. Luego se realizara la investigación en las paredes externas de la casa. La investigación en el peridomicilio debe comenzar con la revisión detallada de los lugares en que algunos animales domésticos, en especial aves (gallinas, palomas, pavos, etc.), son mantenidos y tiene sus nidos deben revisarse montones de leñas o materiales de construcción, cercas, muros y otros lugares de abrigo. Cuando el objetivo sea la detección de casas positivas para su rociamiento inmediato (en la mayoría de los casos), la inspección se realizara hasta que se encuentre un triatomino vivo o un huevo embrionado (tiempo límite: 30 minutos por vivienda). Para determinar la densidad de las colonias del vector, la investigación se realizara con tiempo previamente determinada (hora/hombre), capturando todos los ejemplares identificados. (Basados en la guía operacional para el control de la enfermedad de Chagas en el Ecuador del Dr. Marcelo Aguilar, Fernando Abad y otros). Rociado de viviendas (intra y peridomiciliar) con insecticidas de acción residual para el control vectorial Metodología Aplicación de insecticida Antes de la aplicación, todos los muebles y otros objetos deben ser apartados para dejar libres las superficies que serán rociadas. Se debe tener especial cuidado de proteger los alimentos y los utensilios usados para el almacenamiento y cocción de los mismos. Además, debe evitarse que personas o animales domésticos entren en contacto con el insecticida el operador deberá usar equipos de protección (guantes, mascarillas, ropa que cubra todas las extremidades, vaselina para protección de la piel. Los insecticidas recomendados son los piretroides sintéticos: Deltametrina: 25mg de i.a./m2 (100g de productos al 5% en una bomba Hudson de 8 litros; rociado de 40ml/m2). La aplicación comprende las paredes internas y externas de la casa y los muebles (al menos la superficies que están en contacto con las paredes). Especialmente, deben rociarse las 120 estructuras de las camas y en el peridomicilio, todos los anexos posible (nidos de aves, corrales, pilas de leña o materiales de construcción, cercas, etc). (Basados en la guía operacional para el control de la enfermedad de Chagas en el Ecuador del Dr. Marcelo Aguilar, Fernando Abad y otros). Eliminación de Triatoma dimidiata.-Inspección de viviendas y peridomicilios; rociamiento con piretroides de unidades domiciliares infestadas (Deltametrina al 5% polvo mojable); en cuatro ciclos semestrales (mínimo 2 ciclos). Visitas periódicas a las zonas intervenidas, con reinspección y tratamiento de focos, hasta que los resultados de las búsquedas sean negativos. Deberán rociarse todas las viviendas de las localidades infestadas por T. dimidiata priorizadas. En todos los casos se aplicará el principio de realizar visitas periódicas (al menos semestrales) para reevaluar la situación y proceder a eliminar los focos residuales si los hubiera. En ciertos casos, y en particular en determinadas áreas urbanas, el control efectivo de T. dimidiata se verá dificultado por la existencia de casas con subpisos (espacios entre el terreno y el piso de la vivienda, generalmente de tablas de madera) en los que es físicamente imposible realizar acciones de búsqueda y rociado y en los que se refugian marsupiales, roedores y, muy probablemente, los triatominos asociados a ellos. Se sugiere que, en estos casos, podrían utilizarse (al menos de forma experimental) potes fumígenos formulados a base de piretroides sintéticos; la eficacia podría ser mayor si se utilizaran lonas para sellar, en la medida de lo posible, el espacio a ser tratado. El desarrollo de estrategias complementarias, en particular la detección de focos con participación comunitaria. Los componentes de esta estrategia son tres: (i) la comunidad debe saber qué vigilar y por qué hacerlo; (ii) la comunidad debe saber cómo notificar los focos y a quién hacerlo; y (iii) el sistema debe estar preparado para ofrecer una respuesta rápida y eficiente a todas las notificaciones (incluso en el caso de que los insectos sean identificados como inocuos – por ejemplo, chinches no hematófagas); La garantía de respuesta inmediata (no más de una semana desde la notificación) por parte del sistema, que consistirá en: (i) identificación de los insectos, (ii) en caso de tratarse de triatominos, verificación de la infección natural, (iii) visita a la unidad domiciliar: inspección, rociamiento, eliminación de microhábitats infestados, programación de visitas de reevaluación, (iv) si el foco de T. dimidiata es confirmado, los procedimientos descritos deberán aplicarse al resto de unidades domiciliares de la comunidad; por último, (v) siempre que sea posible, búsqueda activa de casos entre los habitantes que refieran contacto con vectores, sus familiares u otros habitantes de la vivienda y en toda la población infantil de la localidad y (vi) manejo clínico adecuado de casos positivos; La incorporación de un componente de manejo ambiental doméstico y peridoméstico, en particular dirigido a (i) la eliminación de cercos de piñuela, sustituyéndolos por otros construidos con materiales refractarios a la infestación (alambre y estacas o cercas vivas de piñón), (ii) la eliminación de otros microhábitats potencialmente peligrosos (acumulaciones de leña, maderos, ladrillos etc.) y (iii) el control de poblaciones de mamíferos oportunistas (en especial marsupiales y roedores), bien directamente o bien limitando la disponibilidad de 121 refugios en los que éstos puedan establecer sus madrigueras y de alimento para los mismos (gestión de residuos); En situaciones especialmente graves, como las que se dan cuando determinados ciudadanos se niegan a colaborar con las actividades de control en propiedades con alto riesgo de infestación, debería hacerse uso de los recursos legales disponibles para imponer medidas de inspección sanitaria (y, en ciertos casos, de defensa civil) en aplicación de las normativas municipales, provinciales y/o nacionales pertinentes. Control sostenible de las poblaciones domésticas y peridomésticas de Rhodnius ecuadoriensis El control de R. ecuadoriensis requerirá estrategias basadas en la combinación de acciones de control químico (que deben ser implementadas siguiendo los principios de contigüidad espacial y continuidad temporal mencionados antes), de manejo ambiental y de vigilancia entomológica con participación comunitaria; El manejo adecuado de palmas de tagua cercanas a las viviendas (eliminando la materia vegetal muerta que se acumula en las copas y troncos) puede reducir las probabilidades de infestación, y debe por tanto ser estimulado; se podrían considerar estrategias alternativas o complementarias, como la eliminación de palmas de alto riesgo no utilizadas o la aplicación de insecticidas en las copas de las palmeras (siguiendo recomendaciones del Ministerio de Agricultura o de instituciones de investigación agraria, y siempre de acuerdo con las normas que regulan el uso de pesticidas); La eliminación de cercos de piñuela o de nidos de ardillas o aves silvestres presentes en árboles peridomésticos puede ayudar también a disminuir el riesgo de reinfestación de viviendas por R. ecuadoriensis; El manejo de aves de corral, en especial gallinas, puede tener un impacto significativo en la probabilidad de infestación; debería estimularse la sustitución e incineración mensual de nidos de gallina fabricados con materia vegetal; Los programas de mejora de viviendas podrían tener más éxito si incorporasen componentes específicos de sustitución (o revoco) de paredes de barro y de disminución de la complejidad de los tejados, especialmente en los valles interandinos de Loja (techos de teja) y en Manabí (techos de palma); La vigilancia horizontal, descentralizada y basada en la participación de la comunidad será un componente esencial para el control sostenible, a medio y largo plazo, de las poblaciones domésticas y peridomésticas de R. ecuadoriensis. 3.6 Acciones de comunicación y movilización social para fortalecer la vigilancia entomológica de notificación de triatominos, con participación comunitaria (actores sociales y locales) 122 Actividad Metodología Insumos 3.6 Acciones de comunicación y movilización social para fortalecer la vigilancia y control de la enfermedad. Identificar y establecer el rol de los actores locales para la Materiales notificación de didácticos chinchorros por la comunidad. Descripción de requerimiento Rotafolios, libros infantiles, folletos, dípticos, sistemas audiovisuales (películas en formato DVD), tarjetas entomológicas y cajas petri con chinchorros. Metodología Esta actividad se realizara implementando las Unidades Locales de Vigilancia epidemiológica y Entomológica con participación de la comunidad, desarrollando capacidades para respuestas locales y movilización de recursos en el nivel local, provincial y regional en la intervención y control de focos residuales. Diseñando y elaborando un plan de comunicación y capacitación de personal institucional, interinsitucional y comunitario para la vigilancia epidemiológica para la identificación de afiches, dípticos, rotafolios, folletos, tarjetas entomológicas y otros medios audio visuales para la promoción y prevención de la Enfermedad de Chagas. 3.7 Monitoreo y Supervisión de actividades de campo y de vigilancia ento-epidemiológica para Chagas Actividad Metodología 3.7 Monitoreo y Supervisar el Supervisión de cumplimiento de los actividades entoindicadores y metas: epidemiológica para el Encuestas serológicas, control de la encuestas entomológicas, enfermedad diagnóstico y tratamiento Insumos Vehículo Movilización (Terrestre, Fluvial) Descripción de requerimiento Movilización a las areas seleccionadas Viáticos y Subsistencias para aéreo, movilizarse a las areas a supervisar Evaluación entomológica. La información tiene origen: En datos de investigación de rutina en cada ciclo; en datos del Sistema de Vigilancia Entomológica y epidemiológica (registro y denuncia de captura de vectores por la población, casos de transmisión vectorial post intervención). La información debe de ser sistémica, regular y continua. El análisis de estos datos es la base para la toma de decisiones operativas y para la programación de acciones. Debe considerarse que el hallazgo de ejemplares de cada especie tiene significados diferentes en función de las características ecológicas de cada uno. La metodología de control tiene sustentación en un sistema de vigilancia sistémico sustentable y sostenido, que alcance a todas las localidades que en algún momento fueron positivas. Es de vital importancia la participación activa de la comunidad, la coordinación y acciones conjuntas con red de servicios de Salud (Puestos de Vigilancias Comunitarias, Unidades Locales de 123 Vigilancia Entomológica, Laboratorios Distritales y Unidades Operativas del Ministerio de Salud Pública). La decisión de muestreos debe ser tomada por el entomólogo y el epidemiólogo responsables del distrito con apoyo y supervisión del resto de integrantes del equipo de vigilancia vectorial. Se considera que una localidades positiva para cualquier especie de vector cuando en uno o más domicilios se encuentran ejemplares vivos o muertos de triatominos, vestigios de su presencia (heces, exubias) o huevos embrionados después del rociamiento. COMPONENTE 4 Disminuida la incidencia de la Leishmaniasis cutánea mediante promoción y prevención fundamentadas en la vigilancia epidemiológica integral y educación para la salud en áreas endémicas de transmisión del país. 4.1 Vigilancia y monitoreo entomológicos del vector trasmisor de Leishmaniasis en las zonas endémicas del país ACTIVIDADES INSUMOS 4.1 Vigilancia y monitoreo Herramientas de trabajo entomológicos del vector trasmisor de Leishmaniasis en las zonas endémicas del Prendas de protección país Movilización DESCRIPCIÓN DE REQUERIMIENTOS GPS, trampas CDC (luz con aspirador de insectos), trampas Shannon (para colocar en su interior una trampa de luz o cebo), capturadores de insectos, recipientes para muestras de insectos, stikers, marcadores, mochilas, machete, linternas. Uniformes mangas largas, botas de cuero, gorras con orejas, guantes. Vehículo asignado al programa. Metodología de la actividad La investigación entomológica de Leishmaniasis entre sus principales propósitos busca establecer la localización del vector, su dispersión, clasificación de especies y grados de infección, lo que permite diseñar planes operacionales para disminuir riesgos de contraer la enfermedad por parte de las poblaciones que viven en estos sectores. Permite diseñar mapas entomológicos y establecer que especies de lutzomia y especies de parásito vive en el sector investigado, permitiendo esto que los equipos de salud puedan dar un tratamiento selectivo acorde a la especie parasitaria existente. La actividad se realiza en sitios históricos o donde se han reportado casos, los horarios de investigación son en la noche y en sitios con mucha vegetación que por lo general están entre 300 y 1400 metros de altura. El entomólogo que realiza esta actividad selecciona el sitio donde va a realizar las capturas para lo cual utilizan lámparas CDC con aspirador de insectos, también puede realizar esta actividad describiéndose sus piernas (cebo humano) para hacer capturas 124 mediante un aspirador de insectos, una vez que sea capturado los insectos estos se los coloca en un recipiente donde se los etiqueta poniendo sitio de captura, fecha, código y nombre del capturador. 4.2 Diagnóstico oportuno de los pacientes positivos para su tratamiento ACTIVIDADES INSUMOS DESCRIPCIÓN DE REQUERIMIENTOS 5.994 cajas de 10 ampollas de Glucantime de 5ml. Medicamentos: 4.2 Diagnóstico oportuno de los pacientes positivos para su tratamiento Movilización 16.800 unidades de Miltefosina de 50 mg 27.183 unidades de Miltefosina de 10 mg A nivel nacional para distribuir medicamentos a los pacientes positivos a las diferentes direcciones provinciales de salud. La adquisición de medicamentos es para garantizar el tratamiento oportuno de la Leishmaniasis, (Antimoniales pentavalentes, Nitrógeno líquido) utilizando para este fin gastos de movilización para el ciclo de gestión de medicamentos (selección, adquisición, almacenamiento, distribución, uso, dispensación). El principal propósito de tener los stops de medicamentos específicos para la Leishmaniasis cutánea es garantizar que todo paciente diagnosticado con esta enfermedad en el ecuador tenga tratamientos integrales que le permiten su curación y evitar riesgos de reinfección, brindándoles calidad de vida. El tratamiento inicial de la LC y LMC en el Ecuador es en base a antimoniales pentavalentes que es el tratamiento de primera línea a pesar de su toxicidad a nivel cardiaco, renal y hepático. Dentro de este grupo tenemos el antimoniato de meglumina (Glucantime) y el estibo gluconato de sodio (Pentostan). ANTIMONIATO DE MEGLUMINA 1-Deoxi-1-(metilamino)-D-glucitol. Un derivado del sorbitol en el cual el grupo hidroxilo en la posición 1 es sustituído por un grupo metilamino. Se emplea a menudo en conjunto con compuestos orgánicos iodados como medio de contraste.4 Cada ampolla posee 5 ml, conteniendo 81 mg. de antimonio pentavalente (Sb5) para cada ml, conteniendo un total de 405 mg de Sb5 por ampolla. En las formas cutáneas y mucosas, responde bien en dosis de 10 a 15 mg./ Kg./día de Sb5 IM. Durante 20 días o más según la severidad de las lesiones. Los antimoniales pentavalentes presentan una toxicidad potencial cardiaca, hepática, pancreática y renal, debiendo ser utilizados con cautela y ser monitorizados clínica y laboratorialmente, en pacientes con cardiopatías, hepatopatías y neuropatías. De acuerdo a las formas clínicas y a la respuesta terapéutica, el esquema de tratamiento puede ser modificada en lo que respecta a la duración del mismo. 125 Importante. Todas las reacciones adversas graves o potencialmente graves descritas deben ser notificadas a la Jefatura de Área y a los Departamentos de Epidemiología: Arritmias Cardiacas u otras manifestaciones de cardio toxicidad. Insuficiencia renal aguda o elevación de los niveles séricos de urea y creatinina u otras manifestaciones de nefrotoxicidad. Ictericia o elevación de enzimas hepáticas u otras manifestaciones de hepatotoxicidad. Pancreatitis aguda o hiperamilasemia u otras manifestaciones de pancreotoxicidad. No se debe administrar estas drogas en el embarazo, se debe esperar a que termine el período de gestación. La pérdida de la eficacia, las dificultades para su administración y el incremento en la frecuencia y la severidad de los efectos secundarios de las sales de antimonio pentavalente han forzado la búsqueda de medicamentos que pueda remplazarlas en el tratamiento de la Leishmaniasis. En la actualidad, hay una serie de medicamentos que se pueden alternar solo en contados casos debido a la toxicidad manifiesta de los antimoniales o debido a su intolerancia, estos no han demostrado ser 100% eficaces para el tratamiento de la Leishmaniasis en sus distintas formas clínicas, estos son: Sulfato de aminoside, (paramomicina) la misma que se ha utilizado localmente solo y combinado con antimoniato pentavalente en forma intra lesionaliii iv v . Cabe anotar que la experiencia en nuestro país con Antimoniato de Meglumina en forma intra lesional no es abundante, no se ha hecho estudios al respecto, pero nuestra experiencia en la observación es que la lesión cutánea cicatriza más rápidamente que con solo la administración parenteral. Otros estudios con Fluconazol, itraconazol, Dapsone y ketoconazolvi vii viii se han realizado en países endémicos, sobre todo los de Asia, pero no han logrado difundirse para realizar tratamientos en poblaciones grandes afectados por esta patología. Recientemente se ha descrito a la miltefosina como un tratamiento por vía oralix x y como una posibilidad para las personas que no toleran los tratamientos intra musculares, que habitan en regiones alejadas de los servicios de salud o con problemas hepáticos, cardiovasculares y con edades extremas. La miltefosina ha mostrado ser muy eficaz, llegando al 95% de éxito en ensayos clínicos, mientras que sus efectos secundarios se reducirían a vómitos y otros trastornos poco severos. También se debe tener precaución al prescribirles el medicamento a mujeres en edad reproductiva, dada la posibilidad de que ejerza algún efecto adverso sobre el feto. MILTEFOSINA es un derivado de los fosfolípidos de la membrana celular que fue originalmente desarrollado como agente anti neoplásico. Cuando se administra por vía oral, este análogo de la fosfocolina muestra una excelente actividad in vivo contra la Leishmania. 126 La Miltefosina es activa contra la Leishmaniasis extracelular, promastigotes y amastigotes intra celulares, que sobreviven y se multiplican en el compartimiento fagolisosomal de los macrófagos. Cuando se administra por vía oral, este análogo de la fosfocolina muestra una excelente actividad in vivo contra la Leishmania, demuestra ser eficaz y segura para el tratamiento de la Leishmaniasis visceral de la India.xi Tiene una actividad directa marcada contra la Leishmania y que ha sido ya probada en las formas cutáneas en algunos países como Colombia y Guatemala, en los que se han realizado estudios con una tasa de curación mayor al 95%xii. PRESENTACIÓN: La Miltefosina se presenta en cápsulas de 10 y 50 mg. Dosis y administración: La Miltefosina se administra por vía oral, en cápsulas, la dosis diaria depende de la edad y el peso corporal. 2.5 mg/ Kg. /día por 14 a 28 días Si la dosis de 100 mg. Se tolera bien, puede aumentarse la posología a 150 mg. Si la dosis de 150 mg. No se tolera bien, puede disminuirse la posología a 100 mg. Para que haya buena tolerancia a la medicación es necesario que el paciente lo ingiera con “estómago lleno” o sea después de las comidas. Reacciones adversa: Los efectos adversos más frecuentes son: Nauseas, vómitos ocasionales, diarrea transitoria, elevación de las enzimas hepáticas y de la creatinina, que son moderados y transitorios o reversibles al finalizar el tratamiento; por lo tanto, no requieren de la interrupción del tratamiento ni de la reducción de las dosis. Contraindicaciones: No se debe administrar Miltefosina en los pacientes que presenten algunas de las siguientes características: Hipersensibilidad al producto o a alguno de los componentes de la cápsula. Deterioro severo preexistente de la función hepática o renal. Embarazo. Lactancia Criterios de curación: 127 Consiste en la ausencia completa de signos y síntomas de la enfermedad y en la cicatrización de la úlcera cutánea en un término de 60 días posteriores al tratamiento completo. La persistencia de bordes eritematosos, induración posterior al período mencionado, implica persistencia de la infección. La curación parasitológica indica la ausencia del parásito en el cultivo y la negatividad del PCR; la curación clínica no siempre está relacionada con la curación parasitológica. Reactivación: Se define cuando luego de un período de curación clínica, la lesión se presenta nuevamente con formas satélites alrededor de la lesión inicial. Esto se presenta generalmente cuando el paciente no ha recibido el tratamiento adecuado por mala dosificación, abandono del tratamiento, medicamento mal conservado; por lo que, en estos casos se debe repetir un nuevo esquema de tratamiento y esperar un período de 45 a 60 días para observar la evolución de las lesiones. Métodos de control: A más de los métodos epidemiológicos tradicionales, en el control de la Leishmaniasis, uno de los métodos de importancia es la participación comunitaria. Los conceptos y conocimientos de la comunidad son factores que interviene en la permanencia o no de la enfermedad, no tanto por la falta de información o por la persistencia de creencias y costumbres, sino más bien porque la información que llega a través de los diferentes medios no es adecuada y tiene una interpretación particular que puede resultar contradictoria. Los agentes más indicados para el desarrollo de una intervención educativa en la comunidad son los promotores de salud, quienes aunque en muchos casos no saben leer o escribir demuestra en algunas experiencias tener habilidad para comunicarse con la población. 4.3 Evaluación y Capacitación a los profesionales de Salud en diagnóstico, tratamiento, vigilancia y medidas de prevención y control de la Leishmaniasis ACTIVIDADES 4.3 Evaluación y Capacitación a los profesionales de Salud en diagnóstico, tratamiento, vigilancia y medidas de prevención y control de la Leishmaniasis INSUMOS Herramientas de trabajo DESCRIPCIÓN DE REQUERIMIENTOS Proyectores, material de apoyo, cuadernos, plumas, computadoras y material educativo. Profesionales Capacitadores médicos. Movilización Vehículo de la Institución. Metodología de la actividad Se harán visitas a las diferentes areas de Salud, para evaluar al personal médico y afín en sus conocimientos sobre diagnóstico, y manejo del paciente con Leishmaniasis y en actividades de vigilancia y medidas de prevención. Luego se realizara el taller teórico-práctico correspondiente para finalmente proceder a la evaluación final. 128 4.4 Actualización del personal Microscopistas en el diagnóstico de Leishmaniasis cutánea por examen directo de la lesión ACTIVIDADES INSUMOS 4.4 Actualización del personal de Herramientas de trabajo laboratorio en el diagnóstico de Leishmaniasis cutánea por examen directo de Profesionales la lesión Movilización DESCRIPCIÓN DE REQUERIMIENTOS Proyectores, material de apoyo, cuadernos, plumas, computadoras y material educativo. Capacitadores médicos. Vehículo de la Institución. Metodología de la actividad Es de mucha importancia observar que en la Leishmaniasis cutánea el diagnostico Laboratorial que se realiza en el país se basa fundamentalmente en la observación directa del parásito la cual se la logra mediante examen de frotis, biopsias, cultivos. Se harán visitas a las diferentes areas de Salud, para evaluar al personal de laboratorio en sus conocimientos sobre toma de muestra para diagnóstico microscópico del parásito Leishmania. Luego se realizara el taller teórico-práctico correspondiente con capacitación en la toma de muestra, tinción de frotis e identificación parasitológica, para finalmente proceder a la evaluación final. 4.5 Coordinación intra e intersectorial, para ejecutar medidas de prevención y control en base a los datos de la vigilancia ACTIVIDADES DESCRIPCIÓN DE REQUERIMIENTOS INTRA 4.5 Coordinación intra e Coordinación dentro del MSP (nivel central, zonal y distrital, INSPI, intersectorial, para ejecutar Dirección Nacional de Control Vectorial) medidas de prevención y INTER control en base a los datos Organizaciones gubernamentales (educación, gobiernos locales, de la vigilancia agricultura, vivienda, comunidad organizada, promotores de salud). Relaciones intra e inter sectorial El control de las enfermedades vectoriales debe ser siempre integral y sistémica por lo que se requiere la participación activa y coordinada de todas las dependencias del MSP en especial aquellas que están zonas y distritos de riesgos y la acción de socios estratégicos gubernamentales y no gubernamentales como: OPS, Ministerio de educación, gobiernos locales, Ministerio de viviendas, comunidad organizada, etc. 129 4.6 Monitoreo y Supervisión del Componente logístico y técnico ACTIVIDADES INSUMOS Participantes 4.6 Monitoreo y Supervisión del Componente logístico y técnico DESCRIPCIÓN DE REQUERIMIENTOS Equipos del MSP y comunidad organizada en zonas y distritos, participando de manera conjunta y activa en la vigilancia ento-epidemiológica sistémica de la Leishmaniasis cutánea Herramientas de trabajo Implementar un sistema de monitoreo y evaluación de las actividades que se están realizando, formularios y registros. Movilización Vehículo de la Institución. Metodología de la actividad de monitoreo y supervisión Permiten evaluar las actividades que se están realizando y que son productos de la aprobación de un plan operacional, por lo que miden el avance de la ejecución de lo propuesto como meta a cumplirse mes a mes. El monitoreo se lo realiza siempre con la participación de representantes de la Dirección de control vectorial (Programa de Leishmaniasis), representante zonal y del distrito y consiste en el control de calidad de los procedimientos utilizados y de las placas diagnosticadas. Igualmente se encuestará a la población de cada área para evaluar el nivel de información que han recibido y el porcentaje de ejecución de las normas preventivas. Estas actividades permiten establecer los correctivos y garantizan que la consecución de objetivos y metas cumplan con el propósito que tiene el gobierno nacional por intermedio del MSP que es “garantizar calidad de vida a todos los ecuatorianos con énfasis en los sectores más deprimidos” 4.7 Edu-comunicación a la comunidad en areas de riesgo en los métodos de prevención contacto hombre-vector ACTIVIDADES 4.7 Edu-comunicación a la comunidad en areas de riesgo en los métodos de prevención contacto hombre-vector DESCRIPCIÓN DE REQUERIMIENTOS Conocimiento de los modelos de transmisión de cada zona endémica. Recursos humanos (por lo menos 1 epidemiólogo a cargo en cada área). Material para toma de muestras de lesiones de humanos y otros animales. Material para estudios entomológicos. Metodología: La información epidemiológica que orienta la educación para la salud se obtiene a base de vigilancia e investigación, por lo que cada área endémica debe ser investigada y monitoreada para descifrar la dinámica de transmisión en cada una de ellas. La vigilancia consiste en la detección de casos parasitológicamente confirmados, para confirmar la existencia de la enfermedad y la magnitud de la transmisión. Se toma muestra y se hace el diagnostico en cada paciente sospechoso. Igualmente se debe tomar muestras de los animales domésticos y 130 peridomesticos para confirmar o descartar su participación como reservorios. Las muestras son preparadas a partir de frotis teñidos o de biopsias Y/o aspirados para cultivos. Los dípteros del genero Lutzomyia deberán ser capturados en cada área, durante varias noches. Serán disecados y sometidos a PCR para detectar y cuantificar el índice de infección natural con Leishmania. Igualmente se estudiarán su Biología y hábitos de picadura y reposo para establecer las posibles medidas de prevención del contacto con los humanos. Toda esta información se utilizará en las actividades de Educación para la Salud. COMPONENTE 5 Alcanzar la eliminación definitiva de la Oncocercosis en el Ecuador y obtener la Certificación de eliminación de esta enfermedad por parte de la OMS. ACTIVIDADES Visitas Comunitarias Multipropósito a las comunidades bajo Vigilancia Epidemiológica para Oncocercosis DESCRIPCIÓN DE REQUERIMIENTOS Mantener el contacto con las comunidades endémicas es lo que ha dado sostenibilidad al Proyecto y en el 2013 se continuara realizando visitas con actividades multipropósito las comunidades que lo requieran, se espera que el comité de certificación internacional de la OMS visite el país para ingresar a diferentes comunidades de la zona endémica y realizar la evaluación. (Viáticos y subsistencias, otros servicios, combustible). 4.2 VIABILIDAD ECONÓMICA Y FINANCIERA 4.2.1 Metodologías utilizadas para el cálculo de la inversión total, costos de operación y mantenimiento, ingresos y beneficios. Dengue La atención de cada caso de Dengue demanda gastos para el enfermo y para el Estado en días de trabajo perdidos, la OPS/OMS13 realizo estudios sobre el costo de un paciente con dengue en ocho países durante 2005-2006. Como también sean afectados otros miembros de la familia que ayudaban a cuidar al paciente con dengue, un episodio promedio representó 14,8 días perdidos para los pacientes ambulatorios y 18,9 días para los hospitalizados. El costo total promedio de un caso ambulatorio no fatal fue de US$ 514, en tanto que el costo promedio de un caso hospitalizado no fatal fue de US$ 1.491. En promedio, un caso hospitalizado cuesta tres veces más que un caso ambulatorio. Sumando los pacientes ambulatorios y hospitalizados, y contabilizando el riesgo de muerte, el costo total de un caso de dengue es de US$ 828. Este estimativo es muy conservador e ignora los costos sustanciales asociados con los programas de vigilancia y control de los vectores del dengue. 13 Dengue, Guías para el Diagnóstico, Tratamiento, Prevención e Control, OPS/OMS 2010. Pag. #13 131 Este estudio demostró que un episodio de dengue tratado impone costos sustanciales tanto en el sector de la salud como en la economía global. Si una vacuna pudiera prevenir gran parte de esta carga, las ganancias económicas serían significativas. Los niños están en un mayor riesgo de dengue grave. Se requiere cuidado intensivo para los pacientes gravemente enfermos, que incluye líquidos intravenosos, transfusión de sangre o plasma y medicamentos. El dengue afecta a todos los niveles de la sociedad, pero la carga podrá ser mayor entre las poblaciones más pobres que crecen en comunidades con suministro inadecuado de agua y falta de buenas infraestructuras para desechos sólidos, y donde las condiciones son más favorables para la multiplicación del vector principal, Ae. aegypti. Tabla 26: Proyección de Costos de un Paciente con Dengue Periodo 2006-2013 2006* 2007 2008 2009 2010 2011 2012 2013 531 544 589 614 634 663 691 1.542 1.577 1.708 1.782 1.840 1.923 2.003 Inflación Ecuador anual 3,40% 2,30% 8,30% 4,30% 3,30% 4,50% *Dengue, Guías para el Diagnóstico, Tratamiento, Prevención e Control, OPS/OMS 2010. Pag. #13 4,16% Gastos que incurre un paciente con Dengue sin signos de alarma Gastos que incurre un paciente con Dengue con signos de alarma 514 1.491 Tabla 27: Gastos que incurre un paciente con Dengue en Ecuador Gastos que incurre un paciente con Dengue sin signos de alarma Atención Médica profesional Exámenes hemograma y plaquetas Arbovirus (FA, EEV, Dengue) prueba confirmatoria (neutralización) Transporte y alimentación (movilización unidad de salud) Tratamiento Días de trabajo perdidos Total Gastos que incurre un paciente con Dengue con signos de alarma Atención Médica profesional Hospitalización Exámenes hemograma y plaquetas Exámenes ecografía, tomografía, hepáticos Arbovirus (FA, EEV, Dengue) prueba confirmatoria Transporte y alimentación Tratamiento Días de trabajo perdidos Total Valor 691,00 Valor 2.003,00 Fuente: Estadísticas del Proyecto Para evitar o disminuir la transmisión del dengue en el Ecuador es importante adoptar medidas de prevención y control como: eliminación de criaderos del Aedes aegypti en la fase lavaría integrando a la comunidad, disminuir la población adulta del mosquito en las áreas de riesgo, edu-comunicación a nivel intra e intersectorial entre otras, se estima que 132 las medias de prevención demanda gastos para el estado y proporciona bienestar a las personas. En base a estas consideraciones se cuantifica el beneficio neto: el ahorro que implica para el enfermo con Dengue los gastos de (atención médica, exámenes, hospitalización y tratamiento) sean cubiertos por el Estado, considerando una media geométrica de casos con dengue sin signos de alarga y con signos de alarma de los últimos 5 años con una tasa de crecimiento poblacional14 del 1.95% de acuerdo al Censo de Población y Vivienda 2010, para los gastos de atención médica y actividades de control vectorial un incremento anual hasta el 6,12%, en base a la tasa de inflación acumulada de los últimos dos años BCE15 medidas que demandan gasto para el estado y proporciona bienestar a las personas. Tabla 28: Beneficios Neto-Dengue DENGUE Gastos que incurre un paciente con Dengue sin signos de alarma Demanda estimada de casos (media geométrica de los últimos 5 años) SUB-TOTAL DENGUE DENGUE GRAVE Gastos que incurre un paciente con Dengue con signos de alarma Demanda estimada de casos (media geométrica de los últimos 5 años) SUB-TOTAL DENGUE GRAVE Años de vida potencialmente perdidos (A.P.P)*, TASA DE LETALIDAD DE 2% Control Vectorial Beneficio Anual Beneficio Neto 2013 2014 2015 2016 2017 691 733 778 826 876 11.442 11.665 11.888 12.111 12.335 7.906.422 8.550.445 9.248.864 10.003.686 10.805.460 2.003 2.126 2.256 2.394 2.540 194 417 640 863 1.086 388.582 886.542 1.443.840 2.066.022 2.758.440 1.570.601 3.375.983 5.181.364 6.986.746 8.792.127 8.081.071 13.050.793 20.894.041 28.924.861 136.471.496 13.849.501 32.905.955 14.697.091 37.053.118 6.827.917 16.693.522 Fuente: Estadísticas del Proyecto * Los años de vida potencialmente perdidos (A.P.P) se calcula restando la edad máxima para trabajar menos la edad inicial de trabajo (65 - 18 = 47 años de vida productivos) x la tasa de letalidad máxima permisible del 2% de las personas con dengue grave x 12 meses x $ 717.72 ingresos aproximados que generaría una persona (costo de canasta básica familiar mas beneficios de ley). Estos datos pueden aumentar más allá de las proyecciones matemáticas efectuadas, en razón de que la enfermedad puede transformarse en una epidemia. 14 Fuente: Censo de Población y Vivienda 2010 INEC. 15 Fuente: Banco Central del Ecuador 133 Existen otros beneficios que son intangibles como en el ámbito social, económico y político. El impacto en la disminución del vector en el intra y peri domicilio repercute directamente en una mejora de la calidad de vida la población, eso sin contar que la pérdida de una vida no tiene precio ni forma de cuantificar el dolor para una familia Malaria El costo de consulta médica, diagnóstico (hematozoarios en gota gruesa y Pruebas de Diagnóstico Rápido del Plasmodium), tratamiento (Plasmodium vivax y Plasmodium falciparum) y días de trabajo perdidos de una persona con Malaria y otros integrantes de la familia que ayudan a cuidad el enfermo se estima en un promedio de $ 150,13 dólares. Tabla 29: Gastos de paciente con Malaria Gastos de paciente con Malaria Consulta ambulatoria de medicina general 16 Diagnostico Gota Gruesa Hemoparasitos (frotis, gota gruesa) Tarifario MSP (Tarifario MSP) Tratamiento medicamentos P. vivax Días de Trabajo perdidos (717,72/30=23,92) (3 días x 23,92 sueldo diario)* 2 personas TOTAL 1,2 0,43 4,5 144 150,13 Fuente: Estadísticas del Proyecto Ingresos DIRECTOS Tabla 30: Beneficios Neto-Malaria 2013 2014 Consulta ambulatoria de medicina general (Tarifario MSP) 2015 2016 2017 1.20 1.27 1.35 1.43 1.52 0.43 0.46 0.48 0.51 0.55 4.50 4.78 5.07 5.38 5.71 7.5 20 7.96 21.22 8.45 22.52 8.96 23.90 9.51 25.36 144 152.81 162.16 172.09 182.62 177.63 188.5 200.04 212.28 225.27 19,662 19,662 19,662 19,662 19,662 3,492,561 3,706,287 3,933,186 4,173,849 4,429,259 Diagnostico Gota Gruesa Hemoparasitos (frotis, gota gruesa) Tarifario MSP Tratamiento medicamentos P. vivax Indirectos Mosquitero Impregnado Rociado selectivo de viviendas Días de Trabajo perdidos (3 días x 23,92 * 2 personas sueldo diario) TOTAL Demanda estimada de casos (promedio de los últimos 10 años) Beneficio Anual Beneficio Neto 19,735,143 Fuente: Estadísticas del Proyecto Enfermedad de Chagas Se estima que la atención de cada caso de Chagas demanda gastos para el enfermo y para el estado en días de trabajo perdidos, transporte, consulta médica, diagnóstico, 16 Fuente: Tarifario de prestaciones medicas MSP. 134 tratamiento específico y de las complicaciones originadas por la enfermedad de Chagas, $350,58 dólares aproximadamente por paciente. Para el cálculo de los beneficios se consideró: El ahorro del enfermo en: atención médica, diagnostico por método Elisa y HAI, exámenes de (Rx. estándar de tórax, Hemograma completo, Urea, Creatinina, Bilirrubina Total, Bilirrubina Directa, Acido Urico, Transaminasa Pirúvica (ALT), Transaminasa Oxalacética y Fosfatasa Alcalina) y tratamiento sean cubiertos por el Estado. Tabla 31: Gastos que incurre un paciente con Chagas Gastos que incurre un paciente con Chagas Atención Médica profesional 17= 2,1 *6 visitas diaria intrahospitalaria Diagnostico por métodos Elisa y HAI Exámenes Transporte y alimentación (movilización unidad de salud) Tratamiento Días de trabajo perdidos 18 (6 d X $23,92) $12,06 Total 20,00 85,00 60,00 30,00 143,52 $350,58 Fuente: Estadísticas del Proyecto Ingresos COSTOS DIRECTOS Atención Medica Profesional Tabla 32: Beneficios Neto-Chagas 2013 2014 2015 2016 2017 12,06 12,80 13,58 14,41 15,29 20,00 21,22 22,52 23,90 25,36 85,00 60,00 90,20 63,67 95,72 67,57 101,58 71,70 107,80 76,09 30,00 31,84 33,78 35,85 38,05 Días de Trabajo (717,72/30=23,92)*6días $143,52 152,30 161,62 171,52 182,01 Control Vectorial TOTAL $80,00 $430,58 84,90 $456,93 90,09 $484,90 95,61 $514,57 101,46 $546,06 2.721 2.774 2.828 2.883 2.940 $1.171.608,18 $1.267.523,82 $1.371.297,20 $6.899.350,91 $1.483.505,31 $1.605.416,40 Diagnostico por métodos Elisa y HAI Exámenes varios Transporte y alimentación Tratamiento Costos Indirectos Demanda estimada de casos19 Beneficio Anual Beneficio Neto Fuente: Estadísticas del Proyecto L eishmaniasis 17 Fuente: Tarifario de prestaciones medicas MSP. Fuente: Instituto de Estadísticas y Censo-INEC Costo de Canasta Básica Familiar. 19 Corresponde a la demanda insatisfecha x 1.38% Índice Seroprevalencia general de anti cuerpos anti T. cruzi. 18 135 Se considera que la atención de cada caso de Leishmaniasis es de $ 270,66 dólares aproximados por paciente, considerando que los afectados pertenecen sobre todo a poblaciones rurales en donde también impacta la pobreza, este programa debe ser visto como un proyecto de apoyo social en el inmediato, mediano y largo plazo, puesto que la transmisión se produce en todas las áreas tropicales y subtropicales de 23 de las 24 Provincias del País en las que resulta imposible eliminar al vector y reservorios del parásito de la enfermedad. Para el ahorro se consideró el beneficio que tendría de una persona que no se enferme de Leishmaniasis. Tabla 33: Gastos que incurre un paciente si se enferma de Leishmaniasis Gastos que incurre un paciente si se enferma de Leishmaniasis Atención Médica profesional 20= 2,1 *5 visitas Diagnostico Transporte y alimentación (movilización unidad de salud) Tratamiento (30 ampollas x $4=$120) Días de trabajo perdidos (5 d X $23,92) 10,50 0,56 20,00 120,00 119,60 Total 270,66 Fuente: Estadísticas del Proyecto Ingresos Tabla 34: Beneficios Neto-Leishmaniasis COSTOS DIRECTOS Atención Medica Profesional Diagnostico Leishmaniasis, determinación Ac Transporte y alimentación Tratamiento 2013 2014 2015 2016 2017 10,50 11,14 11,82 12,55 13,32 0,56 0,59 0,63 0,67 0,71 20,00 120,00 21,22 127,34 22,52 135,14 23,90 143,41 25,36 152,18 119,6 270.66 1.537 416.004 126,9 287.22 1.567 450.074 134,7 304.80 1.598 487.070 $2.449.859,90 142,9 323.46 1.629 526.916 151,7 343.25 1.660 569.795 Costos Indirectos Días de Trabajo (5 d x $23,92) TOTAL COSTOS Demanda estimada de casos Beneficio Anual Beneficio Neto Fuente: Estadísticas del Proyecto Oncocercosis Esta enfermedad se encuentra en proceso de obtener la certificación de eliminación por parte de la OMS, actualmente se realiza actividades de vigilancia epidemiológica. Este proyecto de vigilancia y control de vectores para prevención de la transmisión de enfermedades metaxénicas, debe considerarse como un conjunto de actividades dirigidas a apoyar el plan social del Buen Vivir en el mediano y largo plazo, puesto que la transmisión se produce en todas las áreas tropicales y subtropicales del país en donde se estima viven alrededor de 8´811.167 habitantes. COSTOS 20 Fuente: Tarifario de prestaciones medicas MSP. 136 Las técnicas que se realizan para el control y prevención de las enfermedades metaxénicas son diferentes, empleando recursos para control vectorial mediante actividades de vigilancia epidemiológica y entomológica e intervenciones con participación intra e intersectorial. Este proyecto desea cubrir las reales necesidades operativas a nivel nacional, sobre todo los relacionados al control y prevención del Dengue, Leishmaniasis, Chagas y Fiebre Amarilla y continuar con actividades para la pre eliminación de la transmisión de la Malaria de casos autóctonos en el país. La inversión que realizaría el estado en este tipo de proyecto social es de $ 97´574.113 dólares que debería ser el presupuesto asignado en los años 2013-2017, este valor es menor al total de beneficios netos proyectado en la población que se encuentra en riesgo de transmisión de contraer estas enfermedades vectoriales en $167.082.566 lo que significa que el proyecto es rentable. La proyección de los costos fijos se realizó de acuerdo a la tasa acumulada de inflación de los últimos dos años del 6.12% del BCE21. 4.2.2. Identificación y valoración de la inversión total, costos de operación y mantenimiento, ingresos y beneficios. Tabla 35: Costos Operativos Periodo 2013-2017 Componentes / Actividades 2013 2014 2015 2016 2017 TOTAL Componente UNO Actividades: 1.1 Visitas domiciliarias para eliminación de criaderos de Aedes aegypti en fase larvaria integrando a la familia 1.2 Fumigación intradomiciliar de viviendas para el control del mosquito Aedes aegypti y otros en fase adulta 1.3 Fumigación de Manzanas con máquinas de ultra bajo volumen para el control del mosquito Aedes aegypti y otros en fase adulta 1.4 Estudios de la eficacia de los plaguicidas utilizados para el control vectorial 1.5 Talleres de capacitación sobre el manejo clínico de pacientes con Dengue dirigido a los equipos de salud a nivel nacional 1.6 Implementar puestos para vigilancia entomológica y monitoreo de vectores de dengue y fiebre amarilla 1.7 Difusión de medidas de prevención y control del dengue 1.8 Edu-comunicación a nivel intra e intersectorial, para ejecutar medidas de prevención y control del dengue 1.9 Talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento en enfermedades metaxénicas al personal del Sector Salud y equipos 6.317.917 6.391.905 10.548.423 11.193.986 11.879.058 46.331.288 393.819 1.902.011 2.677.483 2.841.345 3.015.235 10.829.894 214.686 440.367 550.262 583.938 619.675 2.408.927 55.016 43.694 10.000 10.612 11.261 6.460.585 104.760 101.171 96.730 102.650 108.932 93.079 10.750 11.408 11.978 12.711 13.489 587.990 20.000 60.000 60.000 63.672 67.569 60.337 12.480 13.244 13.906 14.757 15.660 271.241 66.800 114.800 124.800 132.438 140.543 70.047 21 Fuente: Banco Central del Ecuador 137 multidisciplinario 1.10 Sala de entrenamiento de manejo de pacientes con dengue 1.11 Control vectorial de casos de Dengue (control de focos y brotes) 1.12 Monitoreo y Supervisión de actividades de prevención y control del Dengue TOTAL COMPONENTE 1 0 20.000 0 0 0 579.381 0 20.000 21.000 22.285 23.649 20.000 1.149.756 1.190.121 1.294.792 1.374.034 1.458.125 56.934 8.345.984 10.308.721 15.409.374 16.352.428 17.353.196 67.769.703 Componente DOS 2.1 Toma de muestra hemática a febriles sospechosos de paludismo y adopción de esquemas terapéuticos altamente eficaces 2.2 Fortalecimiento del Sistema de Gestión de calidad del diagnóstico microscópico de malaria. 2.3 Monitoreo, Supervisión y Evaluación de actividades de campo en la vigilancia epientomológica para malaria 2.4 Control de brotes de malaria 2.5 Distribución de mosquiteros según requerimiento epidemiológico 2.6 Vigilancia epidemiológica para la eliminación de la malaria 2.7 Rociado de viviendas para control casos de malaria 2.8 Reuniones semestrales de análisis epidemiológico de malaria con los niveles correspondientes 2.9 Caracterización de focos de transmisión: nuevo potencial, nuevo activo, activo residual, residual no activo, endémicos y libres de transmisión 2.10 Vigilancia Entomológica de Malaria TOTAL COMPONENTE 2 270.468 63.500 67.386 71.510 75.887 548.751 12.600 37.500 26.530 19.898 19.898 116.425 17.544 6.960 34.536 7.386 36.649 7.838 38.892 8.318 41.272 8.827 168.894 39.328 13.544 14.373 15.000 15.000 15.000 72.917 200.305 423.164 413.464 438.768 465.621 1.941.322 198.530 155.840 95.377 131.215 109.245 690.207 3.000 5.400 12.000 12.734 13.514 46.648 3.600 12.000 240.305 13.796 255.012 14.640 270.618 15.536 287.180 16.487 1.056.715 72.458 738.551 995.799 943.896 1.022.489 1.052.929 4.753.665 180.366 191.404 203.118 215.549 790.437 8.400 26.700 28.334 30.068 31.908 125.410 0 5.000 5.306 5.631 5.975 21.912 0 0 0 0 0 0 Componente TRES 3.1 Creación a nivel zonal de núcleos de trabajo para priorizar distritos, orientar acciones para la detección y manejo de casos (prioridad niño), aplicación de manuales de normas y procedimientos (protocolos) de diagnóstico, tratamiento etiológico y manejo de las complicaciones cardiacas y/o digestivas además identificar probables brotes de chaguas por vía oral. 3. 2 Fortalecer la capacidad de laboratorio a nivel distrital y/o zonal en métodos parasitológicos para el diagnóstico de Chagas agudo, serológicos y confirmatorios. 3.3 Dar continuidad al tamizaje universal en donantes de sangre optimizando calidad en las acciones y correcta derivación del paciente para confirmación diagnóstica y atención médica. 3.4 Garantizar disponibilidad del medicamento para tratamiento etiológico 138 3.5 Vigilancia entomológica integral funcionando para el fortalecimiento de la capacidad de respuesta local, protocolos de encuestas triatominicas para estandarizar su aplicación y levantamiento de líneas de base. 3.6 Acciones de comunicación y movilización social para fortalecer la vigilancia entomológica de notificación de triatominos, con participación comunitaria (actores sociales y locales) 3.7 Monitoreo y Supervisión de actividades de campo y de vigilancia ento-epidemiológica para Chagas TOTAL COMPONENTE 3 114.111 482.376 511.897 543.226 576.471 2.228.081 0 10.000 10.612 11.261 11.951 43.824 11.790 10.000 10.612 11.262 11.780 55.444 134.301 714.442 758.166 804.566 853.634 3.265.108 6.420 6.813 7.230 7.672 8.142 36.277 0 0 0 0 0 0 13.350 14.167 15.034 15.954 16.931 75.436 7.500 7.959 8.446 8.963 9.512 42.380 3.160 3.353 3.559 3.776 4.008 17.856 5.450 5.784 6.137 6.513 6.912 30.796 0 31.240 33.152 35.181 37.334 136.907 35.880 69.316 73.558 78.060 82.837 339.651 0 0 0 0 89.193 Componente CUATRO 4.1 Vigilancia y monitoreo entomológicos del vector trasmisor de Leishmaniasis en las zonas endémicas del país 4.2 Diagnóstico oportuno de los pacientes positivos para su tratamiento 4.3 Evaluación y Capacitación a los profesionales de Salud en diagnóstico, tratamiento, vigilancia y medidas de prevención y control de la Leishmaniasis. 4.4 Actualización del personal Microscopistas en el diagnóstico de Leishmaniasis cutánea por examen directo de la lesión 4.5 Coordinación intra e intersectorial, para ejecutar medidas de prevención y control en base a los datos de la vigilancia 4.6 Monitoreo y Supervisión del Componente logístico y técnico 4.7 Edu-comunicación a la comunidad en areas de riesgo en los métodos de prevención contacto hombre-vector TOTAL COMPONENTE 4 Componente CINCO 5.1 Visitas Comunitarias Multipropósito a las comunidades bajo Vigilancia Epidemiológica para Oncocercosis TOTAL COMPONENTE 5 89.193 89.193 89.193 TOTAL INVERSION DEL PROYECTO 76.217.320 Fuente: Estadísticas del Proyecto Tabla 36: Costos Inversión Periodo 2013-2017 Costos Inversión Maquinarias y equipos Vehículo Insecticida Equipos informáticos Medicamentos Materiales de laboratorio TOTAL COSTOS DE INVERSION 3.655.522 1.215.000 15.456.476 213.747 968.362 1.047.687 $22.556.794 Fuente: Estadísticas del Proyecto 139 4.2.3. Flujos financieros y Económicos Tabla 37 Matriz de Evaluación Económica de Proyectos de Inversión PROYECTO DE VIGILANCIA Y CONTROL DE VECTORES PARA LA PREVENCION DE LA TRANSMISION DE ENFERMEDAD METAXENICAS EN EL ECUADOR Periodo Inversión Beneficios Reducir el riesgo de adquirir enfermedades metaxénicas, basado en la garantía de los derechos de salud. Total Beneficios 2.013 2.014 2.015 2.016 21.773.696 26.317.925 34.716.415 39.090.226 43 21.773.696 26.317.925 34.716.415 39.090.226 43 8.345.984 10.308.721 15.409.374 16.352.428 17 738.551 995.799 943.896 1.022.489 1 134.301 714.442 758.166 804.566 35.880 69.316 73.558 78.060 9.343.909 12.088.278 17.184.994 18.257.542 Costos Costos de Operación y Mantenimiento Matriz de Marco Lógico Vigilancia epidemiológica y entomológica fortalecida, para controlar y/o disminuir los índices de infestación del mosquito Aedes Aegypti y otros vectores transmisores de Dengue y Fiebre Amarilla. Disminuida la incidencia de Malaria con IPA < 1 x 1000 habitantes en el Ecuador hasta el año 2017 Transmisión vectorial de la Enfermedad de Chagas interrumpida en áreas con vectores domiciliados y mejorando la detección y tratamiento oportuno de casos Disminuida la incidencia de la Leishmaniasis cutánea mediante promoción y prevención fundamentadas en la vigilancia epidemiológica integral y educación para la salud en áreas endémicas de transmisión del país. Eliminación de la Oncocercosis Certificada parte de la OMS año 2013 Total Costos Operación y Mantenimiento. Inversión: componentes de la matriz de Marco Lógico Maquinarias y equipos 3.655.522 Vehiculo 1.215.000 Insecticida 89.193 15.456.476 Equipos informáticos 213.747 Medicamentos 968.362 Materiales de laboratorio 19. 1.047.687 Total Inversión 22.556.794 0 0 0 0 Total Costos 22.556.794 9.343.909 12.088.278 17.184.994 18.257.542 19 -22.556.794 12.429.787 14.229.647 17.531.421 20.832.684 24 FLUJO NETO DE CAJA Fuente: Estadísticas del Proyecto 140 Evaluación costo beneficios La tabla 39 muestra la evaluación económica del Proyecto de Vigilancia y Control de Vectores para la Prevención de la Transmisión de Enfermedades Metaxénicas en el Ecuador, compuesto por cinco estrategias de intervención y el resumen de costos por $ 98.789.113 dólares presupuesto solicitado para el periodo de intervención del proyecto 2013-2017, este valor es menor al total de beneficios proyectado en la población que se encuentra en riesgo de transmisión de contraer estas enfermedades vectoriales en $165.555.850. Beneficio por enfermedad Dengue Malaria Chagas Leishmaniasis Beneficio anual Beneficio Neto 2.013 16.693.522 2.014 20.894.041 2.015 28.924.861 2.016 32.905.955 2.017 37.053.118 3.492.561 3.706.287 3.933.186 4.173.849 4.429.259 1.171.608 1.267.524 1.371.297 1.483.505 1.605.416 416.004 450.074 487.070 526.916 569.795 21.773.696 26.317.925 34.716.415 39.090.226 43.657.588 165.555.850 Fuente: Estadísticas del Proyecto La evolución del beneficio total neto es de $66.781.736 dólares, esto nos demuestra que el proyecto es económicamente factible para el Ministerio de salud. Beneficios totales Netos $ 66.781.736 Se tomó como base la tasa de descuento del Banco Central del Ecuador TMAR 12% para proceder a calcular la tasa de retorno del proyecto (TIR), considerando los flujos de efectivo durante los 5 años, se obtuvo los siguientes resultados. INDICADORES TIR VAN B/C 62% $ 39.400.063 1,52 Como se pude apreciar la tasa interna de retorno es mayor que la tasa de rentabilidad esperada del proyecto del 12%, el valor actual neto del flujo es mayor a cero y la relación costo-beneficio es mayor 1, podemos afirmar que el proyecto es rentable, por cada dólar que invierte es estado, obtiene 0.52 dólares. 4.3. ANÁLISIS DE SOSTENIBILIDAD 4.3.1. Análisis de impacto ambiental y de riesgos En general el proyecto, no generan impacto ambiental y están clasificados en la categoría 2. Las intervenciones que se realizarán para control vectorial con insecticidas son muy 141 puntuales, de poca magnitud y solo se ejecutarían en casos necesarios; además se utilizarían productos biodegradables de poca toxicidad adecuadamente manejados por personal técnico del SNEM y por tanto, no requieren un estudio de impacto ambiental. Los insecticidas utilizados para control de vectores son aprobados y siguen las normas indicadas por la OMS/OPS, son de uso exclusivo para salud pública y su dosificación es la recomendada. 4.3.2.- Sostenibilidad Social: El Proyecto de Vigilancia y Control de enfermedades para la prevención de la transmisión de Enfermedades Metaxénicas, contribuyen al mantenimiento e incremento sostenible en lo social y propende al equilibrio de la sociedad en los aspectos económicos, social y cultural en toda el área de influencia del proyecto, fomentando la equidad e igualdad de género, la equidad étno-cultural e Intergeneracional implementando acciones orientadas a reducir las inequidades y desigualdades en la población. Equidad e igualdad de Género La equidad de género es un concepto que defiende la igualdad entre el hombre y la mujer en el uso y control de los bienes y servicios de una sociedad. Esta consideración lo que propone es que las mujeres deben tener la misma oportunidad y el mismo poder a la hora de la toma de las decisiones. La problemática de las enfermedades transmitidas por vectores es multicausal y entre los factores condicionantes se destacan la presencia de vectores con sus particularidades específicas para cada patología, la falta de educación sumada a una cultura que favorece la proliferación de vectores y el surgimiento de nuevas infecciones debido al alto grado de contacto vector-hombre viviendo en áreas geográficas de difícil acceso. En Ecuador se estima que un alto porcentaje de la población del área rural vive bajo la línea de la pobreza. A su vez la carencia de servicios básicos de saneamiento, agua potable, vivienda digna y la falta de educación sanitaria agudizan la vulnerabilidad de éstos sectores y los convierte en una población susceptible a la transmisión vectorial. El Gobierno nacional a través de la implementación de políticas públicas en la reducción de la pobreza y mejoramiento de las viviendas contribuye a crear un ambiente menos sombrío en relación a la transmisión de enfermedades vectoriales. Equidad étnica cultural Es la igualdad tanto de derechos como de oportunidades y trato entre los individuos de diversos orígenes étnicos, sin discriminarlos en el ámbito social y laboral. Se responsabiliza de orientar la inclusión del enfoque étnico, desde la perspectiva de derechos de los Pueblos Indígenas en los procesos de gestión de políticas públicas. En el proyecto de control de enfermedades transmitidas por 142 vectores se vislumbra que algunas enfermedades metaxénicas se concentran en los grupos étnicos más postergados y más vulnerables en la amazonia ecuatoriana: Shuaras, Ashuaras, Quichuas, Secoyas etc., cuyas costumbres y tipo de viviendas los hace vulnerables a las enfermedades de transmisión vectorial. Se incorporan en el campo de materiales de educación para la salud en relación a las acciones de prevención y control de enfermedades vectoriales en su lenguaje ancestral. Está incorporada en la red de microscopistas y participación comunitaria la población de diversos orígenes étnicos. Equidad Intergeneracional El proyecto atiende a los diferentes grupos etareos en función de la vulnerabilidad. Los grupos etareos de riesgo en las enfermedades transmitidas por vectores son los menores de 5 años, mujeres embarazadas y los ancianos o adultos mayores. La vulnerabilidad en los grupos etareos antes mencionado está dada por la gravedad, complicaciones y muerte que se presentan cuando se hace un diagnóstico y tratamiento tardío, por lo que actualmente se emplea como política publica el diagnostico precoz y tratamiento temprano en éstos grupos poblacionales para evitar mortalidad. 5.- PRESUPUESTO Tabla 38: Fuente de Financiamiento Periodo 2013-2017 Componentes / Rubros Externas FUENTES DE FINANCIAMIENTO (dólares) Internas TOTAL Crédito Cooperación Crédito Fiscales Autogestión A. Comunidad Componente UNO Vigilancia epidemiológica y entomológica fortalecida, para controlar y/o disminuir los índices de infestación del mosquito Aedes Aegypti y otros vectores transmisores de Dengue y Fiebre Amarilla. Actividades: 1.1 Visitas domiciliarias para eliminación de criaderos de Aedes 57.706.372 57.706.372 aegypti en fase larvaria integrando a la familia 1.2 Fumigación intradomiciliar de viviendas para el control del mosquito 17.353.882 17.353.882 Aedes aegypti y otros en fase adulta 1.3 Fumigación de Manzanas con máquinas de ultra bajo volumen para 3.371.747 3.371.747 el control del mosquito Aedes aegypti y otros en fase adulta 1.4 Estudios de la eficacia de los plaguicidas utilizados para el control 6.496.828 6.496.828 vectorial 1.5 Talleres de capacitación sobre el manejo clinico de pacientes con 166.826 166.826 Dengue dirigido a los equipos de salud a nivel nacional 1.6 Implementar puestos para vigilancia entomológica y monitoreo 587.990 587.990 de vectores de dengue y fiebre amarilla 1.7 Difusión de medidas de 60.337 60.337 prevención y control del dengue 143 1.8 Edu-comunicación a nivel intra e intersectorial, para ejecutar medidas de prevención y control del dengue 1.9 Talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento en enfermedades metaxénicas al personal del Sector Salud y equipos multidisciplinario 1.10 Sala de entrenamiento de manejo de pacientes con dengue 271.241 271.241 70.047 70.047 579.381 579.381 1.11 Control vectorial de casos de Dengue (control de focos y brotes) 20.000 20.000 1.12 Monitoreo y Supervisión de actividades de prevención y control del Dengue 86.934 86.934 86.771.584 86.771.584 TOTAL COMPONENTE 1 Componente DOS Disminuida la incidencia de Malaria con IPA < 1 x 1000 habitantes en el Ecuador hasta el año 2017 2.1 Toma de muestra hemática a febriles sospechosos de paludismo y 1.488.602 1.488.602 adopción de esquemas terapéuticos altamente eficaces 2.2 Fortalecimiento del Sistema de Gestión de calidad del diagnóstico 116.425 116.425 microscópico de malaria. 2.3 Monitoreo, Supervisión y Evaluación de actividades de campo 183.894 183.894 en la vigilancia epi-entomológica para malaria 2.4 Control de brotes de malaria 39.328 39.328 2.5 Distribución de mosquiteros según 1.336.630 1.336.630 requerimiento epidemiológico 2.6 Vigilancia epidemiológica para la 1.941.322 1.941.322 eliminación de la malaria 2.7 Rociado de viviendas para control 690.207 690.207 casos de malaria 2.8 Reuniones semestrales de análisis epidemiológico de malaria con los 46.648 46.648 niveles correspondientes 2.9 Caracterización de focos de transmisión: nuevo potencial, nuevo activo, activo residual, residual no 1.056.715 1.056.715 activo, endémicos y libres de transmisión 2.10 Vigilancia Entomológica de 79.109 79.109 Malaria TOTAL COMPONENTE 2 6.978.880 6.978.880 Componente TRES Transmisión vectorial de la Enfermedad de Chagas interrumpida en áreas con vectores domiciliados y mejorando la detección y tratamiento oportuno de casos 3.1 Creación a nivel zonal de núcleos de trabajo para priorizar distritos, orientar acciones para la detección y manejo de casos (prioridad niño), aplicación de manuales de normas y 790.437 790.437 procedimientos (protocolos) de diagnóstico, tratamiento etiológico y manejo de las complicaciones cardiacas y/o digestivas además 144 identificar probables brotes de chaguas por vía oral. 3. 2 Fortalecer la capacidad de laboratorio a nivel distrital y/o zonal en métodos parasitológicos para el diagnóstico de Chagas agudo, serológicos y confirmatorios. 3.3 Dar continuidad al tamizaje universal en donantes de sangre optimizando calidad en las acciones y correcta derivación del paciente para confirmación diagnóstica y atención médica. 3.4 Garantizar disponibilidad del medicamento para tratamiento etiológico 3.5 Vigilancia entomológica integral funcionando para el fortalecimiento de la capacidad de respuesta local, protocolos de encuestas triatominicas para estandarizar su aplicación y levantamiento de líneas de base. 3.6 Acciones de comunicación y movilización social para fortalecer la vigilancia entomológica de notificación de triatominos, con participación comunitaria (actores sociales y locales) 3.7 Monitoreo y Supervisión de actividades de campo y de vigilancia ento-epidemiológica para Chagas TOTAL COMPONENTE 3 248.971 248.971 21.912 21.912 8.000 8.000 2.463.377 2.463.377 43.824 43.824 72.044 72.044 3.648.565 3.648.565 Componente CUATRO Disminuida la incidencia de la Leishmaniasis cutánea mediante promoción y prevención fundamentadas en la vigilancia epidemiológica integral y educación para la salud en áreas endémicas de transmisión del país. 4.1 Vigilancia y monitoreo entomológicos del vector trasmisor de 98.434 Leishmaniasis en las zonas endémicas del país 4.2 Diagnóstico oportuno de los pacientes positivos para su 884.084 tratamiento 4.3 Evaluación y Capacitación a los profesionales de Salud en diagnóstico, tratamiento, vigilancia y medidas de 75.436 prevención y control de la Leishmaniasis. 4.4 Actualización del personal Microscopistas en el diagnóstico de 42.380 Leishmaniasis cutánea por examen directo de la lesión 4.5 Coordinación intra e intersectorial, para ejecutar medidas 17.856 de prevención y control en base a los datos de la vigilancia 145 98.434 884.084 75.436 42.380 17.856 4.6 Monitoreo y Supervisión del Componente logístico y técnico 4.7 Edu-comunicación a la comunidad en areas de riesgo en los métodos de prevención contacto hombre-vector TOTAL COMPONENTE 4 30.796 30.796 136.907 136.907 1.285.891 1.285.891 89.193 89.193 Componente CINCO Eliminación de la Oncocercosis Certificada parte de la OMS año 2013 5.1 Visitas Comunitarias Multipropósito a las comunidades bajo Vigilancia Epidemiológica para Oncocercosis TOTAL COMPONENTE 5 TOTAL INVERSION DEL PROYECTO 89.193 89.193 98.774.113 98.774.113 Fuente: Estadísticas del Proyecto 6. ESTRATEGIA DE EJECUCIÓN 6.1 Estructura Operativa ORGANIGRAMA ESTRUCTURAL DEL SERVICIO NACIONAL DE CONTROL DE ENFERMEDADES TRANSMITIDAS POR VECTORES ARTROPODOS "DR. JUAN ANTONIO MONTALVAN CORNEJO" -SNEM SUBSECRETARIA REGIONAL DE SALUD COMITÉ DE GESTION DIRECCION GENERAL ASESORIA OPS / OMS DEPARTAMENTO ADMINISTRATIVO DEPARTAMENTO ASESORIA JURIDICA SUBDIRECCION TECNICA DEPARTAMENTO CONTROL Y VIGILANCIA EPIDEMIOLÓGICA DEPARTAMENTO DE OPERACIONES DE CAMPO CONTROL DE MALARIA CONTROL DEL DENGUE PROGRAMAS CONTROL DE CHAGAS CONTROL DE LEISHMANIASIS CONTROL ONCOCERCOSIS CONTROL FIEBRE AMARILLA SEDES - ZONAS ZONA I - STO. DOMINGO DE LOS TSACHILAS ZONA II PASTAZA ZONA VII ESMERALDAS ZONA III GUAYAS ZONA IV - LOJA ZONA VIII MACHALA ZONA V LOS RIOS ZONA IX SUCUMBÌOS ZONA VI - MANABI ZONAX - MORONA SANTIAGO ZONA IX METROPOLITANA Fuente: Registro Oficial 1995 vigente Elaborado por: Luisa Tumbaco El SNEM es una institución adscrita al Ministerio de Salud Pública, de acuerdo al Registro Oficial de 1995. La coordinación y seguimiento está a cargo de la Dirección Nacional de Estrategias de Salud Colectiva, de acuerdo a la nueva estructura del Ministerio de Salud Pública. 6.2.- Arreglos institucionales Tabla 39 ARREGLOS INSTITUCIONALES Tipo de ejecución Instituciones Involucradas 146 Directa (D) o Indirecta (I) * INH Áreas y Sub-centros de Salud Escuelas Municipios y Juntas Parroquiales Teniente Político Párroco Comunidad ONGs Seguro Campesino Tipo de arreglo ** Coordinación Coordinación Coordinación Coordinación Coordinación Coordinación Coordinación Coordinación Coordinación MSP MSP MIN. ED. Gobiernos Locales Gobernación Iglesia Comunidad Privados IESS Fuente: Estadísticas del Proyecto 147 6.3.- Cronograma valorado por componentes y actividad Tabla 40 CRONOGRAMA VALORADO POR COMPONENTES Y ACTIVIDADES FLUJO AÑO 2013 SUBTOTAL SUBTOTAL SUBTOTAL SUBTOTAL SUBTOTAL 2.013 2.014 2.015 2.016 2.017 848.194 6.827.917 9.281.071 13.050.793 13.849.501 14.697.091 3.460 1.460 1.532.968 3.972.011 3.717.483 3.944.993 4.186.427 24.868 24.868 13.000 496.646 602.327 713.062 756.701 803.011 4.371 4.941 4.371 7.999 70.016 49.000 15.000 15.918 16.892 8.430 8.430 9.630 8.430 8.430 104.760 111.171 116.730 123.874 131.455 1.150 1.150 1.150 1.150 0 0 10.750 11.408 11.978 12.711 13.489 0 0 0 0 0 0 0 20.000 60.000 60.000 63.672 67.569 2.080 1.040 1.040 1.040 1.040 1.040 1.040 1.040 12.480 13.244 13.906 14.757 15.660 42.680 2.680 2.680 2.680 2.680 2.680 2.680 2.680 2.680 66.800 114.800 124.800 132.438 140.543 0 0 0 0 0 0 0 0 0 0 0 20.000 0 0 0 0 0 0 0 0 0 0 0 0 0 0 20.000 21.000 22.285 23.649 GLOBAL Enero Febrero Marzo Abril Mayo Junio Julio Agosto Sept. Oct. Nov. Dic. 57.706.372 259.156 263.456 388.112 1.329.806 803.374 452.803 463.803 461.803 633.803 461.803 461.803 17.353.882 42.671 44.671 718.072 624.671 65.663 3.460 3.460 18.460 3.460 3.460 3.371.747 13.000 24.868 24.868 186.828 24.868 84.868 24.875 24.868 24.868 166.826 4.371 4.371 4.371 7.167 14.371 4.371 4.941 4.371 587.990 8.430 8.430 8.430 9.630 8.430 8.430 9.630 60.337 0 0 0 5.000 0 1.150 271.241 0 0 0 20.000 0 70.047 0 1.040 1.040 1.040 579.381 0 0 2.680 20.000 0 0 86.934 0 0 Componente UNO 1.1 Visitas domiciliarias para eliminación de criaderos de Aedes aegypti en fase larvaria integrando a la familia 1.2 Fumigación intradomiciliar de viviendas para el control del mosquito Aedes aegypti y otros en fase adulta 1.3 Fumigación de Manzanas con máquinas de ultra bajo volumen para el control del mosquito Aedes aegypti y otros en fase adulta 1.4 Estudios de la eficacia de los plaguicidas utilizados para el control vectorial 1.5 Talleres de capacitación sobre el manejo clinico de pacientes con Dengue dirigido a los equipos de salud a nivel nacional 1.6 Implementar puestos para vigilancia entomológica y monitoreo de vectores de dengue y fiebre amarilla 1.7 Difusión de medidas de prevención y control del dengue 1.8 Edu-comunicación a nivel intra e intersectorial, para ejecutar medidas de prevención y control del dengue 1.9 Talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento en enfermedades metaxénicas al personal del Sector Salud y equipos multidisciplinario 1.10 Sala de entrenamiento de manejo de pacientes con dengue 1.11 Control vectorial de casos de Dengue (control de focos y brotes) 1.12 Monitoreo y Supervisión de actividades de prevención y control del Dengue TOTAL COMPONENTE 1 Componente DOS 6.496.828 65.224 75.674 70.449 125.449 225.099 82.449 70.449 70.449 70.449 70.449 70.449 153.167 1.149.756 1.220.121 1.294.792 1.374.034 1.458.125 86.771.584 392.852 422.510 1.218.022 2.352.271 1.146.565 641.251 582.028 593.251 750.251 580.021 577.101 1.035.970 10.292.093 15.475.153 19.139.544 20.310.884 21.553.910 2.1 Toma de muestra hemática a febriles sospechosos de paludismo y adopción de esquemas terapéuticos altamente eficaces 1.488.602 43.196 43.195 64.500 43.198 186.347 32.901 1.359 1.359 1.359 1.359 1.359 1.359 421.485 243.500 258.402 274.216 290.998 2.2 Fortalecimiento del Sistema de Gestión de calidad del 116.425 0 0 0 0 0 0 0 6.300 0 6.300 0 0 12.600 37.500 26.530 19.898 19.898 148 diagnóstico microscópico de malaria. 2.3 Monitoreo, Supervisión y Evaluación de actividades de campo en la vigilancia epi-entomológica para malaria 2.4 Control de brotes de malaria 2.5 Distribución de mosquiteros según requerimiento epidemiológico 2.6 Vigilancia epidemiológica para la eliminación de la malaria 2.7 Rociado de viviendas para control casos de malaria 2.8 Reuniones semestrales de análisis epidemiológico de malaria con los niveles correspondientes 2.9 Caracterización de focos de transmisión: nuevo potencial, nuevo activo, activo residual, residual no activo, endémicos y libres de transmisión 2.10 Vigilancia Entomológica de Malaria TOTAL COMPONENTE 2 Componente TRES 3.1 Creación a nivel zonal de núcleos de trabajo para priorizar distritos, orientar acciones para la detección y manejo de casos (prioridad niño), aplicación de manuales de normas y procedimientos (protocolos) de diagnóstico, tratamiento etiológico y manejo de las complicaciones cardiacas y/o digestivas además identificar probables brotes de chaguas por vía oral. 3. 2 Fortalecer la capacidad de laboratorio a nivel distrital y/o zonal en métodos parasitológicos para el diagnóstico de Chagas agudo, serológicos y confirmatorios. 3.3 Dar continuidad al tamizaje universal en donantes de sangre optimizando calidad en las acciones y correcta derivación del paciente para confirmación diagnóstica y atención médica. 3.4 Garantizar disponibilidad del medicamento para tratamiento etiológico 3.5 Vigilancia entomológica integral funcionando para el fortalecimiento de la capacidad de respuesta local, protocolos de encuestas triatominicas para estandarizar su aplicación y levantamiento de líneas de base. 3.6 Acciones de comunicación y movilización social para fortalecer la vigilancia entomológica de notificación de triatominos, con participación comunitaria (actores sociales y locales) 3.7 Monitoreo y Supervisión de actividades de campo y de vigilancia ento-epidemiológica para Chagas TOTAL COMPONENTE 3 Componente CUATRO 183.894 0 1.045 1.045 17.090 2.045 5.045 1.045 1.045 1.045 1.045 1.045 1.049 32.544 34.536 36.649 38.892 41.272 39.328 0 0 0 1.740 0 0 0 1.740 0 1.740 1.740 0 6.960 7.386 7.838 8.318 8.827 1.336.630 0 1.128 1.128 191.256 1.128 1.128 1.128 1.128 186.528 1.128 1.128 1.136 387.944 411.686 260.000 179.000 98.000 1.941.322 31.224 31.221 49.621 31.221 54.518 0 0 2.500 0 0 0 0 200.305 423.164 413.464 438.768 465.621 690.207 19.980 19.977 29.835 97.727 26.671 620 620 620 620 620 620 620 198.530 155.840 95.377 131.215 109.245 46.648 0 0 0 0 3.000 0 0 0 0 0 0 3.000 5.400 12.000 12.734 13.514 1.056.715 0 0 0 0 1.200 0 0 1.200 0 0 1.200 0 3.600 240.305 255.012 270.618 287.180 79.109 6.978.880 0 94.400 0 96.566 0 146.129 0 382.232 3.167 278.075 2.167 41.860 2.167 6.318 2.167 18.058 2.167 191.718 2.167 14.358 7.092 0 4.164 14.000 1.280.968 14.857 1.574.173 15.766 1.381.038 16.731 1.390.390 17.755 1.352.309 0 0 0 0 0 0 0 0 0 0 0 180.366 191.404 203.118 215.549 0 14.000 2.100 0 2.100 0 2.100 2.100 0 0 22.400 51.700 54.864 58.222 61.785 21.912 0 0 0 0 0 0 0 0 0 0 0 5.000 5.306 5.631 5.975 8.000 0 0 0 0 0 0 0 0 0 0 0 0 8.000 0 0 14.224 57.694 8.644 4.800 62.300 2.300 2.300 2.300 2.200 2.359 174.111 522.376 554.345 588.271 624.274 0 0 0 0 0 0 0 0 0 0 0 10.000 10.612 11.261 11.951 790.437 248.971 2.463.377 0 6.444 0 8.544 43.824 72.044 0 0 790 0 800 0 9.550 0 820 0 820 0 12.780 13.562 14.392 15.273 16.037 3.648.565 6.444 8.544 15.014 71.694 11.544 4.800 73.950 2.300 5.220 4.400 3.020 2.359 209.291 783.004 838.924 881.776 935.570 149 4.1 Vigilancia y monitoreo entomológicos del vector trasmisor de Leishmaniasis en las zonas endémicas del país 4.2 Diagnóstico oportuno de los pacientes positivos para su tratamiento 4.3 Evaluación y Capacitación a los profesionales de Salud en diagnóstico, tratamiento, vigilancia y medidas de prevención y control de la Leishmaniasis. 4.4 Actualización del personal Microscopistas en el diagnóstico de Leishmaniasis cutánea por examen directo de la lesión 4.5 Coordinación intra e intersectorial, para ejecutar medidas de prevención y control en base a los datos de la vigilancia 4.6 Monitoreo y Supervisión del Componente logístico y técnico 4.7 Edu-comunicación a la comunidad en areas de riesgo en los métodos de prevención contacto hombre-vector TOTAL COMPONENTE 4 Componente CINCO 98.434 0 0 2.140 0 11.000 0 2.140 0 0 2.140 0 0 17.420 18.486 19.617 20.818 22.092 884.084 0 0 0 82.775 0 0 0 73.683 0 0 0 0 156.458 166.033 176.194 186.978 198.421 75.436 0 1.580 790 790 1.580 2.290 1.580 790 1.580 790 790 790 13.350 14.167 15.034 15.954 16.931 42.380 0 0 0 2.500 0 0 2.500 0 0 2.500 0 0 7.500 7.959 8.446 8.963 9.512 17.856 0 0 790 0 790 0 790 0 790 0 0 0 3.160 3.353 3.559 3.776 4.008 30.796 0 0 1.090 0 1.090 0 1.090 0 1.090 0 1.090 0 5.450 5.784 6.137 6.513 6.912 136.907 0 0 0 0 0 0 0 0 0 0 0 0 0 31.240 33.152 35.181 37.334 1.285.891 0 1.580 4.810 86.065 14.460 2.290 8.100 74.473 3.460 5.430 1.880 790 203.338 247.022 262.140 278.183 295.208 5.1 Visitas Comunitarias Multipropósito a las comunidades bajo Vigilancia Epidemiológica para Oncocercosis 89.193 6.135 6.135 7.873 7.316 7.316 6.134 7.316 7.316 7.316 7.316 6.133 12.888 89.193 0 0 0 0 TOTAL COMPONENTE 5 89.193 6.135 6.135 7.873 7.316 7.316 6.134 7.316 7.316 7.316 7.316 6.133 12.888 89.193 0 0 0 0 98.774.113 499.831 535.335 1.391.848 2.899.578 1.457.961 696.335 677.712 695.398 957.965 611.525 595.225 1.056.170 12.074.883 18.079.353 21.621.646 22.861.234 24.136.998 TOTAL INVERSION DEL PROYECTO Fuente: Estadísticas del Proyecto 150 6.4. Origen de los insumos Tabla 41 Origen de insumos Periodo 2013-2017 Componentes / Rubros Tipo de bien ORIGEN DE LOS INSUMOS (USD y %) Nacional Importado TOTAL Componente UNO Adquisición de Temephos Vestuario, Lencería y Prendas de Protección Edición, Impresión, Reproducción y Publicaciones Herramientas Materiales de Construcción, Eléctricos, 1.1 Visitas domiciliarias para eliminación de Plomería y Carpintería criaderos de Aedes aegypti en fase larvaria Combustibles integrando a la familia Mantenimiento de Vehículos Repuestos y Accesorios Aseguramiento del parque automotor del SNEM (incluido SOAT a nivel nacional) Adquisición de 40 vehículos Mantenimiento de edificio Deltametrina liquida al 2.5% 1.2 Fumigación intradomiciliar de viviendas Accesorios (equipos de fumigación) para el control del mosquito Aedes aegypti y Manteniendo y reparación varios otros en fase adulta Maquinas ULV portátil Malathion al 96% g.t. Maquina ULV de arrastre para fumigaciones 1.3 Fumigación de Manzanas con máquinas del SNEM de ultra bajo volumen para el control del Combustibles mosquito Aedes aegypti y otros en fase Materiales de oficina (tizas, lápices, plumas, adulta etc) 1.4 Estudios de la eficacia de los plaguicidas utilizados para el control vectorial Materiales de laboratorio de entomológica 1.5 Talleres de capacitación sobre el manejo clinico de pacientes con Dengue dirigido a Edición, Impresión, Reproducción y los equipos de salud a nivel nacional Publicaciones 1.6 Implementar puestos para vigilancia entomológica y monitoreo de vectores de Materiales de Construcción, Eléctricos, dengue y fiebre amarilla Plomería y Carpintería Contratación de Medios de Comunicación Masivos 1.7 Difusión de medidas de prevención y control del dengue Edición, Impresión, Reproducción y Publicaciones 1.9 Talleres de capacitación en vigilancia, control, prevención, diagnóstico y tratamiento en enfermedades metaxénicas al personal del Sector Salud y equipos multidisciplinario Materiales didácticos 1.10 Sala de entrenamiento de manejo de pacientes con dengue Materiales, equipos e insumos Uniformes personal de oficina 1.12 Monitoreo y Supervisión de actividades Materiales de oficina (cartuchos, tóner) de prevención y control del Dengue Equipos, Sistemas y Paquetes Informáticos TOTAL COMPONENTE 1 Componente DOS Adquisición de Materiales para Laboratorio 2.1 Toma de muestra hemática a febriles y Uso Médico sospechosos de paludismo y adopción de esquemas terapéuticos altamente eficaces Adquisición de Pruebas de Diagnóstico 10.175.084 1.958.472 10.175.084 1.958.472 202.367 202.367 724.988 724.988 53.248 53.248 428.735 1.535.571 1.535.571 428.735 1.535.571 1.535.571 799.469 799.469 1.200.000 202.494 1.892.457 1.200.000 202.494 1.124.963 708.102 119.684 3.506.569 1.892.457 842.820 842.820 1.100.963 1.100.963 807.987 807.987 83.873 83.873 83.747 83.747 26.243 26.243 187.494 187.494 40.000 40.000 291.241 291.241 40.000 40.000 181.862 326.174 213.747 25.762.392 4.631.532 181.862 326.174 213.747 30.393.923 130.560 733.013 130.560 1.124.963 708.102 119.684 3.506.569 733.013 151 Rápido Adquisición de herramientas para mantenimiento de microscopios Medicamentos 2.3 Monitoreo, Supervisión y Evaluación de actividades de campo en la vigilancia epientomológica para malaria 2.5 Distribución de mosquiteros según requerimiento epidemiológico 2.6 Vigilancia epidemiológica para la eliminación de la malaria 2.7 Rociado de viviendas para control casos de malaria 2.10 Vigilancia Entomológica de Malaria TOTAL COMPONENTE 2 Componente TRES 3.1 Creación a nivel zonal de núcleos de trabajo para priorizar distritos, orientar acciones para la detección y manejo de casos (prioridad niño), aplicación de manuales de normas y procedimientos (protocolos) de diagnóstico, tratamiento etiológico y manejo de las complicaciones cardiacas y/o digestivas además identificar probables brotes de chaguas por vía oral. 3. 2 Fortalecer la capacidad de laboratorio a nivel distrital y/o zonal en métodos parasitológicos para el diagnóstico de Chagas agudo, serológicos y confirmatorios. 3.4 Garantizar disponibilidad del medicamento para tratamiento etiológico 3.5 Vigilancia entomológica integral funcionando para el fortalecimiento de la capacidad de respuesta local, protocolos de encuestas triatominicas para estandarizar su aplicación y levantamiento de líneas de base. 3.7 Monitoreo y Supervisión de actividades de campo y de vigilancia entoepidemiológica para Chagas TOTAL COMPONENTE 3 Componente CUATRO 4.1 Vigilancia y monitoreo entomológicos del vector trasmisor de Leishmaniasis en las zonas endémicas del país 4.2 Diagnóstico oportuno de los pacientes positivos para su tratamiento 17.138 17.138 76.278 76.278 15.000 Adquisición de un Bote para Esmeraldas Adquisición de Mosquiteros Impregnados con Insecticida Vestuario, Lencería y Prendas de Protección Prendas de protección Adquisición de Deltametrina 5% Materiales de laboratorio de entomológica 15.000 1.263.713 70.633 384.519 105.000 10.301 2.675.595 Prendas de protección (Mandil, mascarillas, visores plásticos, guantes quirúrgicos, gafas protectoras) 1.263.713 130.560 70.633 384.519 105.000 10.301 2.806.155 21.912 21.912 Adquisición de materiales de laboratorio y kits Elisa Prendas de protección Adquisición de medicamento Nifurtimox Equipos de rociado Uniformes de campo y Prendas de Protección Materiales de aseo Insecticida 123.560 123.560 15.338 15.338 8.000 8.000 10.000 10.000 49.261 30.000 49.261 30.000 235.296 235.296 15.610 Maquinarias y equipos 508.978 Adquisición de microscopio para estudio Materiales de laboratorio de entomológica 5.000 TOTAL INVERSION DEL PROYECTO 5.000 57.157 Adquisición de medicamento para Leishmaniasis TOTAL COMPONENTE 4 0 15.610 508.978 57.157 156.458 62.157 156.458 156.458 218.615 29.009.122 4.918.550 33.927.672 Fuente: Estadísticas del Proyecto 7. ESTRATEGIA DE SEGUIMIENTO Y EVALUACIÓN 7.1.- Monitoreo de la Ejecución Se requiere ejecutar algunas actividades de monitoreo: 152 Estarán vinculadas a los indicadores de GPR y serán medidos a través de indicadores del avance financiero y técnico (cumplimiento de metas y ejecución presupuestaria). 7.2 Evaluación de Resultados e Impactos La estrategia para monitorear la gestión se basa en la información analizada y verificada como recurso principal, vinculado directamente con la toma de decisiones programática, administrativa y financiera. Este sistema está vinculado con los objetivos y metas propuestos. A partir de dichos sistemas de información, se podrán conocer los logros o resultados que se van obteniendo en la gestión institucional, así como la ejecución del proyecto. Los formularios a utilizarse son los siguientes: el registro de fumigación de manzanas y casas, registro para aplicación de larvicidas, el formulario R1 para el rociado de viviendas, el formulario OC-19 para la toma de muestras hemáticas a pacientes febriles, registro de distribución de mosquiteros, registro de investigaciones serológicas para Chagas, información que es recopilada por el departamento de estadísticas del nivel zonal para su posterior envío al nivel central, para que sea consolidada, analizada y validada por la unidad de vigilancia epidemiológica. La evaluación del proyecto se la realizara mediante la medición de indicadores de seguimiento de resultado e impacto como son: DENGUE Índices de casas infestadas con el vector Aedes aegypti Índice de deposito Índice de Breteau MALARIA Índice Parasitario Anual (IPA) Índice de Laminas Positivas (ILP) La frecuencia relativa de infecciones a P. falciparum (F.R.I.F) CHAGAS Índices tripano-triatomino Índice de infestación vectorial Índice de seroprevalencia de Chagas LEISHMANIASIS Índice de infección natural de Lutzomyia Índice de dispersión 153 Número de unidades de salud abastecías con medicamento para tratamiento de Leishmaniasis. ONCOCERCOSIS Índice de Infección de natural por microfilarias Índice Larvas infectivas En función de los compromisos internacionales adquiridos por el país a través de las dos Iniciativas IPA y AMCHA y que Ecuador se ha planteado como meta la eliminación del triatoma dimidiata hasta el año 2014, por lo tanto al ser un vector introducido lograremos un impacto considerable en el primer componente del proyecto: control de la transmisión vectorial. Las acciones de control vectorial para efectos de lograr un impacto y sobre todo que sea sostenible en el mediano y largo plazo es importante montar un sistema de vigilancia epidemiológico-entomológica con participación comunitaria y enfoque de coordinación intra e intersectorial con la finalidad de tener libres de chinchorros y de esta manera eliminando al eslabón más débil de la cadena de transmisión de enfermedades transmitidas por vectores artrópodos vamos a lograr el propósito del proyecto que es la reducción de la morbi-mortalidad en las provincias y cantones endémicos. 154 Bibliografias: iii Asilian A, Jalayer T, Nilforoosshzadeh, Ghassemi RL, Peto R, Wayling S. Treatment of cutaneous leishmaniasis with aminoside (paramomycin) ointment: double- blind, randomized trial in the Islamic Republic of Iran. Bulletin of the World Health Organization 2003; 81:353- 9. iv Faghihi G, Tavakoli- Kia R. Topical Paramomycin vs. Intralesional meglumine antimoniate in cutaneous leishmaniasis. Clinical and Experimental Dermatology 2003; 28: 13- 6. v Moosavi Z, NakhliA, Rassaii S. Comparing the efficiency of topical paramomycin with intralesional meglumine antimoniate for cutaneous leishmaniasis. Internacional Journal Of Dermatology 2005; 44: 1064- 5. vi Dandashi A. Treatment of cutaneous leishmaniasis with fluconazole: a randomized double- blind, placebo- controlled trial. Journal of the European Academy of Dermatology and Venereology: JEADV 2005; 19: 43. vii Dogra J. A. Double- blind study on the efficacy of oral dapsone in cutaneous leishmaniasis. Transactions of the Royal Society of Tropical Medicine and Higiene 1991; 85: 212-3. viii Momeni AZ, Aminjavaheri M, Omidghaemi MR. Treatment of cutaneous leishmaniasis with Ketoconazole cream. The Journal of Dermatological Treatment. 2003; 14: 26- 9. ix Mohebali M, Fotouhi A, Hooshmand B, Zarei Z, Akhoundi B, Rahnema A. Comparison of Miltefosine and meglumine antimoniate for the treatment of zoonotic cutaneous leishmaniasis (ZCL) by a randomized clinical trial in Iran. Acta Tropica 2007; 103: 33- 40. x Sindermann H, Ángel J. Development of miltefosine as an oral treatment fo leishmaniasis. Transactions of the Royal Society of Tropical Medicine and Higiene 2006; 100: S17- 20. xi Sundar S Jha TK, Thakur MD. Oral miltefosine for Indian Visceral Leishmaniasis. N Engl J Med 2002; 347: 17391746. (Datos de archivo: ASTA Medica, Study Nº D18506/ 3154, 2001). xii J. Soto, B.A.Arana, J. Toledo, N.Rizzo, J.C.Vega. Miltefosina for new world cutaneous leishmaniasis. Major Article. Clinica Infectious Diseases Society of America. Maryland. USA. mayo 2003. xii Jackeline Alger. Manual operativo estándar para la gestión del diagnostico microscópico de plasmodium; Organización Panamericana de la Salud- OPS SNEM-RAVREDA - Ecuador 2008. Gydnea Aguirre Dávila; Postura experiencial de los docentes que utilizan la simulación clínica como estrategia didáctica en la carrera de medicina; Tesis de investigación, Universidad Nacional de Colombia, Instituto de Investigación en Educación, Bogotá, Colombia, 2012. 155