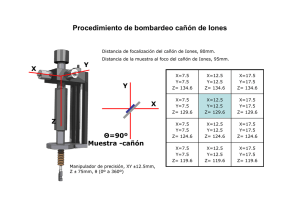
m/z - INTI
Anuncio

SEGUNDAS JORNADAS DE ACTUALIZACIÓN ANALÍTICA INSTITUTO NACIONAL DE TECNOLOGÍA INDUSTRIAL CENTRO DE INVESTIGACIONES TECNOLÓGICAS DE LA INDUSTRIA LÁCTEA INTI Lácteos - Sede Rafaela Análisis de trazas de Somatropina en leche por LC-MS/MS y en modo MRM3 Dr. Fernando A. Iñón Gte. investigación y Desarrollo – Gte. Capacitación y Aplicaciones JENCK S.A. 11 de junio de 2015 Temario • Importancia de la determinación de somatropina en leche • Qué es y cómo funciona un LC-MS/MS y que tipo de espectrómetros existen • Ventajas y aplicaciones de equipos MS/MS híbridos • Determinación de somatropina en leche mediante MRM y MS3 JENCK S.A. • RECURSOS HUMANOS o INFRAESTRUCTURA o JENCK S.A. • Asesoramiento y provisión de Instrumental analítico • Calificación, certificación y mantenimiento de instrumental • Capacitación • Cursos • Seminarios • Desarrollo de aplicaciones Capacitación Jenck S.A. 2015 Cursos teórico-prácticos dictados en JENCK Seminarios de Innovación y Divulgación Tecnológica Seminarios del Departamento de Servicios de Posventa Cursos a medida (dictados en planta o laboratorio del cliente o en JENCK) • Cursos fuera de nuestra sede, en vinculación con universidades y centros de investigación de todo el país • • • • NOTIJENCK.COM.AR GERENCIA DE CAPACITACIÓN Y APLICACIONES [email protected] .:. www.jenck.com TEL: (54) 11-4014-5300 .:. FAX: (54) 11-4014-5353 Somatropina en leche • Tratamiento de vacas con Somatotropina Bobina recombinante(rBST) • aumentar su producción en leche (de 10-15%) • promover su crecimiento, • Favorecer, según ciertos estudios, la fertilidad. Somatropina bovina recombinante en leche • Tratamiento prohibido en muchos países • Comunidad Europea, Japón, Australia, Nueva Zelandia, Canadá, • …Argentina (¿?!) • se utiliza comúnmente en los Estados Unidos, ya que está autorizada por la FDA desde 1994. • La mayoría de los métodos analíticos utilizados para detectar esta hormona implican inmunoensayos, • Incapacidad de diferenciar la hormona natural y la versión recombinante • La rbST en leche se la encuentra presente en baja concentraciones (~ ng/ml, ppb), • La metodología implementada debe poser buena sensibilidad con elevada confianza en su confirmación definitiva. Somatropina bovina recombinante en leche • De todas las matrices, la leche es la matriz más complicada para detectar rBST, ya que: • es una matriz compleja, con alto contenido de proteínas, lípidos y azúcares; • contiene un gran número de proteínas que presentan propiedades fisicoquímicas similares a la rBST • la concentración de rBST muy baja • la caseína puede actuar como secuestrador de rBST • Secuestro de proteína: donde la proteína activa (en este caso la rBST) se un une a un complejo proteico inactivo (en este caso la caseína) • Remoción anticipada de caseínas podría afectar la recuperación de rBST • La cuantificación de proteínas, especialmente en matrices ricas en proteínas, siempre ha sido un desafío • Para resolver estos problemas, se debe utilizar técnicas especializadas • Que pueda validarse y defenderse legalmente Somatropina y somatropina recombinate • La formas natural y recombinante difieren por un aminoácido N-terminal, • rBST, 190 aminoácidos, Peso molecular: 22kDa Alanina Metionina 2 ptes disulfuro 53-164,181- 189 • Ligera diferencia, pero significativa para que un método basado en espectrometría de masas sea una alternativa viable • varias ventajas, incluyendo la especificidad y sensibilidad. Somatropina bovina recombinante en leche • Es necesario contar con una tecnología analítica diferencial capaz de discriminar entre el efecto matriz y el analito en cuestión (rbST); • al intentar eliminar los interferentes de la matriz solamente por métodos físico-químicos (extracción líquido/líquido, evaporaciones, extracción y/o dispersión en fase sólida, cambio de fases, ect.), al fin de obtener un extracto de inyección aceptable, involucra que en cada paso adicional de limpieza disminuye el porcentaje de recuperación del analito. Comparación de metodologías Inmunoensayos Espectrometría de masas Se basa en la detección de la proteína entera a través su unión a anticuerpos específicos + - + - Alta sensibilidad No discrimina entre BST y rBST Discrimina entre BST y rBST Dificulta en la purificación de la matriz Altísima sensibilidad No es fácil detectar la proteína entera, Digestión enzimática previa para enfocarse en el péptido Nterminal Facil de realizar Cuantitativo Principio del espectrómetro de masas (MS) Inyección de muestra Eluido de la columna Separación en la columna < ESI > Introducción al MS fase móvil Protón Eliminación de un protón Adición protónica Ión positivo (molécula protonada ) • • • • イオン化したい化合物の分子 Fuente de iones Unidad de Analizador enfoque Región a presión Región de vacío atmosférica Ión Negativo (molécula desprotonada) Se aplica alto voltaje al eluido de la columna, formando una niebla por adición de nitrógeno (nebulización) Las gotas cargadas disminuyen su tamaño gradualmente hasta provocar la evaporación de iones. Los iones son separados por tamaños dentro del analizador. Al alcanzar el detector, los iones son contados. Detector ¿Cuál es el mayor beneficio de un MS como detector en LC? • El mayor beneficio es: • Adicionalmente al tiempo de retención, puede obtenerse información sobre la masa relacionada con cada compuesto, de forma sencilla y simultánea. • La información de la masa permite reducir el riesgo de; • Identificación errónea del compuesto • Error en la Cuantificación debido a la elución inesperada de interferencias, etc. La posibilidad de separar en función de la masa m/z ↓ Reduce el riesgo de 267 cometer errores de identificación y cuantificación m/z 281 m/z 264 m/z 278 LC-MS: datos analíticos MS (3) (1) (2) cromatograma int. Espectro de masas (4) (1) TIC m/z (2) m/z 582 (3) m/z 193 (4) (5) int. (5) m/z tiempo PDA (dispositivo de fotodiodos) (2) (4) cromatograma (2) 580 nm (3) 210 nm (3) (5) tiempo Espectro UV AU (4) nm AU (5) nm Espectrometría MS/MS • Información estructural • Identificación de compuestos desconocidos • Selectividad adicional a la cromatografía • Análisis de mezclas complejas • No siempre se necesita de un cromatógrafo • Mejor relación señal/ruidos (S/N) • Análisis de trazas • Bajo tiempo de desarrollo de métodos Alta Sensibilidad y Selectividad en Modo MRM Triple Cuadrupolos Ideal para “Targered Analysis” (Análisis de Compuestos Conocidos) que requiere precisión en la cuantificación. Generación de Iones Transporte de Iones Filtro de Iones Fragmentación Filtro de Iones Circuito Iónico Electrónico “Esquiando en Pendiente” Funcioes de la Fuente de Iones API • Nexo de unión entre el HPLC y la primer región de vacío del MS, todo a presión atmosférica. • Generar iones en fase gaseosa • Ionizar el analito (APCI, APPI o AP-MALDI). • Nebulización de los iones en disolución (ESI o NSI). • Desolvatar los cluster (analito(s) más solvente) antes de ingresar al MS. • Eliminar moléculas neutras e iones de carga opuesta a la polaridad de trabajo antes de ingresar al MS. Fuente de Iones API Los “turbo heater” son calentadores cerámicos del aire que promueven la desolvatación de los iones. Se puede programar su temperatura desde Analyst®, permitiendo tener para cada tiempo cromatográfico (δΤ≥1 min.) diferentes temperaturas que optimizan la señal. A su vez reduce el “efecto memoria” y aumenta el rango de flujos de trabajo. API 3200TM, API 4000TM, API 4500TM, API 5000TM, API 5500TM, 3200 Q TRAP®, 4000 QTRAP®, 4500 QTRAP® 5500 QTRAP® poseen la Fuente de Iones API: Turbo VTM ESI - macromoléculas proteinase K thermolysin 29 kDa 34 kDa ESI MS disolución en CH3CN:H2O:ác.acético 50:46:4 temp fuente: 100 oC. Gas Cortina • Interfase ideal para prevenir contaminación • Permite una operación robusta ideal para secuencias largas. Interfase de vacío para el sistema API 5000, 5500, 4500 y 5500 QTrap Orifice plate, Curtain plate Declustering Potential (DP) QJet Orificio de Entrada al MS Presión atmosférica 4-7 mTorr Gas Cortina Región Q1 10 µTorr Q0, Potencial De entrada (EP) Diferencia de presiones debido al vacío aplicado por la bomba mecánica externa Skimmer vs Guías • Guías: • Cuadrupolo solo RF • Enfoca iones en Q0 • Introduce más iones y menos gas en Q0 • Más eficiente que un skimmer QTRAP® 4500 4000 Q TRAP® Incrementa la sensibilidad en todos los modos Nueva guía iónica IonDrive QJet • Permite la entrada de más iones • Guía RF de dos etapas API 6500, 6500 QTRAP • 1ra Etapa: Mejor captura iones entrantes por orificios grandes • 2da Etapa : Mejor transferencia de iones a la región Q0 • Mayor robustez • Mejor barrara contra especies neutras y micro gotas • La eficiencia de transmisión es 2x veces mejor que la guía iónica QJet® original Sciex QTRAP 4500 AcQuRate™ pulse counting detector Highest reproducibility and accuracy Turbo V™ source and Curtain Gas™ interface Unmatched robustness and ruggedness Qurved LINAC® collision cell Shortest MRM cycles and highest scan speed and reduced instrument footprint Linear Accelerator™ Ion trap More efficient and faster Q TRAP® scanning 940 kHz ion path Extended mass range with best low mass ion confinement High pressure Q0 and QJet®2 ion guide Most efficient ion focusing Modos de Barrido Modo de Barrido Q1 Q2 Q3 Propósito Full-Scan Scanning Transmisión Total Trans. Total Info. PM SIM m/z Fijo Transmisión Total Trans. Total Cuantificación Producto m/z Fijo CE + Transmisión Total Scanning Info Estructural MRM m/z Fijo CE + Transmisión Total m/z Fijo Cuantif. Específ. Pérdida neutra Scanning CE + Transmisión Total Scanning Screening Tipo de Compuestos Precursor Scanning CE + Transmisión Total m/z Fijo Screening Tipo de Compuestos MRM Alta Resolución Scaning Alta Resolución CE + Transmisión Total Scaning Alta Resolución Cuantif. Específ. + Cualif. Definitiva. Multi Target Screening m/z Fijo CE + Transmisión Total m/z Fijo + Scanning Cuantif. Específ. + Cualif. Definitiva. Rojo: MS simple, Triple Cuad., QqTOF y Q TRAP® - Verde: Triple Cuad., QqTOF y Q TRAP® - Marrón: solamente QqTOF - Azul: solamente Q TRAP® Selected/Multiple Reaction Monitoring (SRM/MRM) m/z Fijo Q1 • Transmisión Total m/z Fijo Q2 Q3 Ventajas • Monitoreo específico del analito en cuestión. • Altos ciclos de Barrido. • “Simultáneos” Monitoreo de Múltiples Transiciones. • Desventajas • Nula provisión de información estructural. • Las moléculas desconocidas son ignoradas por el MS/MS (Unknowns Screening). Identificación de Compuestos utilizando Relación de Áreas o Alturas en modo MRM Alternativa de Identificación a la Relación de Áreas o Alturas en modo MRM, el modo FullScan MS/MS Q3 en un Sistema Q TRAP® puede funcionar como Cuadrupolo o Trampa Lineal. Atrapamiento de Iones Generación de Iones Transporte de Iones Filtro de Iones Filtro de Iones Fragmentación Ideal para “Targered Analysis” y para GUS (General Unknow Screening) que requiere precisión en la Cuantificación y Confirmación Definitiva. Atrapamiento y Barrido Full-Scan dentro de la Trampa Lineal de Iones Q3 Tecnologías MS/MS Trampa 3D Sensibilidad Full Scan MS3 (o más) QqQ Sensibilidad MRM Pérdida de Neutros Barrido de Precursores Q TRAP Sensibilidad Full Scan MS y MS/MS MS3 Sensibilidad MRM Pérdida de Neutros Barrido de Precursores Ventajas de las trampas lineales de iones • El analizador de masas (corazón del espectrómetro) es mucho más rápido que un triple cuadrupolo convencional. • La tecnología Q TRAP posibilita la utilización de Bibliotecas Espectrales de Compuestos MS/MS • Permite realizar MS3 y así aumentar la especificidad y sensibilidad significativamente. • Q3 puede funcionar como Trampa Lineal y posibilita estudios de elucidación de estructuras (Ej.: Estudios de Impurezas de Plaguicidas y Metabolitos), dado que permite alcanzar una alta resolución en masa (~12 ppm) • Es factible trabajar en modo GUS (General Unknows Screening), para investigar compuestos desconocidos • La tecnología Q TRAP puede funcionar también como un Triple Cuadupolo, manteniendo las ventajas de éste, por ejemplo el amplio rango dinámico (en modo MRM), gran exactitud de cuantificación, etc. Barrido realzado de ion producto (EPI) Q1 Q2 Q3 1) Q1 Selecciona el Ión Precursor. 2) Q2 Genera los Iones Producto. 3) Q3 Atrapa y barre en modo Full-Scan los Iones Producto. s , c p Confirmación con QqLIT o QqQ i t y XIC of +MRM (10 pairs): Exp 1, 216.1/174.0 amu from Sample 7 (10) of Data EPI vs MS2 - EPI dynFT 216.wiff (Turbo Spray) s 1.4e4 (10ng/mL Atrazine) 7.20 n 1.2e4 MRM Max. 1.4e4 cps. t e 1.0e4 8000.0 Is n 6000.0 p 4000.0 c 2000.0 0.0 2 3 4 5 6 7 8 9 Time, min +EPI (216.10) CE (35): Exp 2, 7.028 to 7.344 min from Sample 7 (10) of Data EPI vs MS2 - EPI dynFT 216.wiff (Turbo Spray) 10 11 12 13 14 s i t y , 1 n 4.0e5 x 100 t e 3.0e5 Barrido EPI (Q TRAP) Pureza 95.6% Max. 4.5e5 cps. 174.0 sI n 2.0e5 104.0 132.0 96.0 p 1.0e5 146.0 216.0 79.0 125.9 128.0 138.0 c 110.0 0.0 70 180 190 200 210 220 230 i t y , 80 90 100 110 120 130 140 150 160 170 m/z, amu +MS2 (216.10) CE (35): Exp 2, 7.074 to 7.382 min from Sample 7 (10) of Data EPI vs MS2 - MS2 216.wiff (Turbo Spray) s 3000 n 2500 Barrido PI (QqQ) Pureza 69.5% 96.2 t e 2000 1500 Max. 3136.9 cps. 174.2 104.2 79.2 I n 216.0 1000 132.2 500 0 70 126.8 80 90 100 110 120 130 146.0 138.2 140 150 m/z, amu 160 170 180 190 200 210 220 230 s , c p Confirmación con QqLIT o QqQ i t y XIC of +MRM (10 pairs): Exp 1, 216.1/174.0 amu from Sample 4 (0.5) of Data EPI vs MS2 - EPI dynFT 216.wiff (Turbo Spray) MRM Max. 660.0 cps. (0.5 ng/mL Atrazine) n s 660 600 7.21 t e 500 400 Is n 300 p 200 c 100 0 2 3 4 5 6 7 8 9 Time, min +EPI (216.10) CE (35): Exp 2, 7.121 to 7.301 min from Sample 4 (0.5) of Data EPI vs MS2 - EPI dynFT 216.wiff (Turbo Spray) 10 11 12 13 14 i t y , 1 s 3.5e4 n 3.0e4 t e 2.5e4 Barrido EPI (Q TRAP) Pureza 76.5% Max. 3.5e4 cps. 174.0 sI n 2.0e4 1.5e4 79.0 96.1 216.0 1.0e4 p 104.0 145.9 c 5000.0 180 190 200 210 220 230 i t y , 70 80 90 100 110 120 130 140 150 160 170 m/z, amu +MS2 (216.10) CE (35): Exp 2, 6.628 to 7.861 min from Sample 4 (0.5) of Data EPI vs MS2 - MS2 216.wiff (Turbo Spray) s 89 n 80 t e 60 Barrido PI (QqQ) No hay match Max. 89.2 cps. 174.0 I n 40 20 0 70 80 90 100 110 120 130 140 150 m/z, amu 160 170 180 190 200 210 220 230 Influencia de la concentración en la búscada en bibliotecas 1ng/mL Linear calibration Fit (%) EPI Fit (%) MS2 99.7 100 98.8 4.5E+05 92.3 4.0E+05 Peak Area (counts) MRM QTRAP® 87.1 3.5E+05 95.6 90 QqQ 80 76.5 2 R = 0.9992 69.5 3.0E+05 70 60 2.5E+05 54.6 50 48.2 2.0E+05 40 1.5E+05 30 1.0E+05 20 5.0E+04 10 2.0 0.0 0 0.0 0.0E+00 0 0 5 10 15 20 25 30 Concentration (ng/mL) 35 40 45 50 Cuantificación vía MS3 MS/MS/MS Q1 Q2 1) Q3 3) 2) 1) 2) 3) 4) 5) Selección del Ión Precursor. Fragmentación. Atrapamiento de Ión Producto. Fragmentación del Ión Producto. Escaneo y envío al detector de los Iones Productos Secundarios. 4) 5) MRM & MS/MS/MS MS/MS/MS Aumento de la Selectividad y Sensibilidad Malatión 10 ng/g en Manzana - % CV<5, recuperación entre 90-110 % Interferencias en modo MRM Muestras blanco de orina de 33 sujetos diferentes. Intensidad normalizada a 0.50 pg/uL para MRM 277-168 (transición con mejor LOQ). 10 de 33 sujetos presentan interferencias!!! (flechas indican sujeto con interferencia al TR del clenbuterol Muestras #1, 10 y 11 fortificadas con 0.25 pg/µL Selectividad en modo MS3 Muestras blanco de orina de 33 sujetos diferentes. Intensidad normalizada a 0.05 pg/µL para MS3 277168132 Ninguno presenta interferencias, aún con un umbral 10 veces menor !!! Muestras #1, 10 y 11 fortificadas con 0.25 pg/µL Determinación de rBST • Pasos críticos en la preparación de muestras • Recordar que la rBST está en niveles muy bajos (1-5 ng/mL) • Extracción de grasas de muestras • Precipitación de proteínas • Desnaturalización y optimización de la digestión • Introducción de un estándar interno antes de la preparación de la muestra es esencial para evaluar y compensar perdidas de analito o variabilidad del procedimiento analítico Metodología • Se agrega estándar interno (hormona equina (rEST) ) a 10 mL de muestra • Extracción en fase sólida en cartucho C4 • Se lava cartucho con solución acuosa al 0.1% en ácido trifluoroacetico (TFA), y luego con solución 30:70 (acetonitrilo : sol. aq 0.1% TFA) • Se eluye con 7 mL de solución 80:20 (acetonitrilo : sol. aq 0.1% TFA) • Se evapora hasta 1 mL • Precipitación de proteínas • Se induce con metanol frío, se centrifuga y se seca el sobrenadante • Digestión • El residuo se reconstituye con 120 µL de buffer carbonato de amonio y se digiere a 37°C, con tripsina durante 16 hs • Reconstitución • El digerido se evapora hasta sequedad y se reconstituye con 500 µL de solución 30:70 (acetonitrilo: sol aq. 0.2% ác. fórmico) agregando además antes de la inyección el péptido N-terminal C13 de la de la rBST Metodología LC-MS/MS de BST y rBST Multiple Reaction Monitoring MS/MS/MS Condiciones intrumentales • Shimadzu Nexera XR • Fase móvil A: 90:10 (agua:acetonitrilo), Fase móvil B: 10:90 (agua:acetonitrilo) siempre conteniendo 0.1% ác. fórmico. • Columna150 mm x 2.1 mm x 3 µm C18 Interchrom QS Uptisphere HDO. • Temperatura ambiente, Gradiente 25 min a 300 µL/min. • MS/MS: SCIEX 5500 QTRAP • Equipado con fuente Turbo V™. Ionización electrospay aplicando 3500 V MRM3 MRM Hormona Secuencia péptido N-Terminal Transiciones DP (V) CE (V) Transiciones DP (V) CE (V) AF2 (mv) rBST MFPAMSLSGLFANAVLR 913.2/774.0 913.2/1047.6 35 37 913.2/774.0/791.0 35 37 0.2 rEST MFPAMPLSSLFANAVLR 933.2/794.2 35 38 rBST 13C6 MFP(A13C)MS(L13C)SG(L13C)F (A13C)N(A13C)V(L13C)R 916.2/777.0 35 37 XIC of +MS3 (913.20),(774.00): Exp 2, 790.309 to 790.... 7.0e5 913.2 / 774.0 / 791.0 I n t e n s it y , c p s rBST MRM3 S/N = 74.3 6.0e5 5.0e5 S/N = 74.3 4.0e5 4.0e5 rBST MRM3 3.5e5 913.2 / 774.0 / 961.0 3.0e5 S/N = 60.8 2.5e5 S/N = 60.8 2.0e5 3.0e5 1.5e5 2.0e5 1.0e5 4.71 4.5 5.0 6.69 5.5 6.0 Time, min XIC of +MRM (8 pairs): 913.200/774.000 Da from Sa... 6.5 7.0 0.0 4.0 7.5 rBST MRM 4000 913.2 / 774.0 4.5 4.90 5.75 6.05 6.0 Time, min XIC of +MRM (8 pairs): 913.200/1047.600 Da from S... Max. 4610.0 cps. 5.0 5.5 1000 900 S/N = 68.7 2500 2000 6.5 7.0 7.5 Max. 1085.0 cps. S/N = 32.6 800 3000 6.39 rBST MRM 913.2 / 1047.6 5.60 1085 S/N = 68.7 3500 4.56 7.84 4500 5.58 4.72 5.0e4 6.09 I n t e n s it y , c p s 0.0 4.0 4.62 Max. 4.6e5 cps. 5.67 4.5e5 8.0e5 1.0e5 I n t e n s it y , c p s XIC of +MS3 (913.20),(774.00): Exp 2, 960.349 to 960.... 5.66 9.0e5 I n t e n s it y , c p s Max. 9.1e5 cps. 700 S/N = 32.6 600 500 4.17 4.58 4.83 400 1500 300 5.94 1000 500 0 4.0 4.25 4.34 4.62 4.5 5.00 5.0 200 6.01 5.18 5.5 6.0 Time, min 6.33 6.5 5.74 100 6.60 6.83 7.0 7.397.60 7.68 7.5 0 4.0 6.17 5.13 4.5 5.0 5.5 6.0 Time, min 6.38 6.83 7.09 7.17 6.5 7.0 7.79 7.58 7.5 Cromatograma iónico total rBST 10 ppb rEST MRM 933.2 / 794.2 rBST 13C6 916.2 / 777.0 rBST MRM3 rBST MRM3 913.2 / 774.0 / 960.9 913.2 / 774.0 / 791.0 . . i t y TIC: from Sample 12 (milk, 2 ppb) of rbST 20110512.wiff (Turbo Spray) Max. 3.4e7 cps. s 4.66 3.4e7 4.88 3.0e7 n Cromatograma iónico total t e 2.5e7 4.51 2.0e7 rBST 2 ppb 5.63 I n 1.5e7 5.97 1.0e7 6.67 5.0e6 0.0 0.0 1.0 2.0 3.0 4.0 5.0 6.0 7.0 8.28 8.0 8.89 9.66 9.95 9.0 1.00e5 8.00e4 6.00e4 10.0 11.0 12.0 13.0 14.0 15.0 16.0 17.0 18.0 19.0 20.0 Time, min XIC of +MRM (2 pairs): Exp 1, 916.200/777.000 Da fro... 5.71 rEST MRM 21.0 22.0 23.0 Max. 1.1e5 cps. In te n s ity , c p s In te n s ity , c p s XIC of +MRM (2 pairs): Exp 1, 933.600/794.300 Da fro... 13.85 10.90 933.2 / 794.2 4.00e4 5.63 1.8e5 1.5e5 1.0e5 24.0 Max. 1.8e5 cps. rBST 13C6 916.2 / 777.0 5.0e4 2.00e4 0.00 4.0 4.5 5.0 6.5 7.0 7.5 Max. 1.4e5 cps. 5.64 1.4e5 1.2e5 1.0e5 8.0e4 rBST MRM3 913.2 / 774.0 / 791.0 6.0e4 4.0e4 0.0 3.5 4.0 4.5 5.0 3.5 4.0 4.5 5.0 5.5 6.0 Time, min XIC of +MS3 (913.20),(774.00): Exp 2, 960.469 to 960.... 5.5 Time, min 6.0 6.5 7.0 7.5 8.0e4 rBST MRM3 6.0e4 913.2 / 774.0 / 961.0 7.0 7.5 Max. 9.8e4 cps. 5.60 4.84 4.0e4 0.0 6.5 5.66 9.8e4 4.51 2.0e4 4.68 4.83 2.0e4 0.0 In te n s ity , c p s 5.5 6.0 Time, min XIC of +MS3 (913.20),(774.00): Exp 2, 790.190 to 790.... In te n s ity , c p s 3.5 3.5 4.0 4.5 6.01 5.0 5.5 Time, min 6.0 6.45 6.5 7.0 7.5 Curva de calibración Conclusiones • La espectrometría de masas permite un nuevo enfoque para la detección selectiva de rBST en leche, • A diferencia de los métodos clásicos, permite diferenciar la forma nativa BST de la recombinante rBST • Esto es un paso importantísimo para el control del uso (indebido) de esta hormona en la producción de leche • El método presentado podría mejorarse, especialmente en la preparación de muestra para mejorar el porcentaje de recuperación de la rBST y mejorar aun más los límites de detección. Esto incluye el proceso de digestión con tripsina. • La detección utilizando tecnología MS3 permite reducir significativamente interferencias de matriz, mejorando la relación S/N obtenida. GERENCIA DE CAPACITACIÓN Y APLICACIONES [email protected] .:. www.jenck.com TEL: (54) 11-4014-5300 .:. FAX: (54) 11-4014-5353