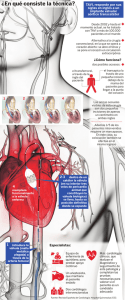
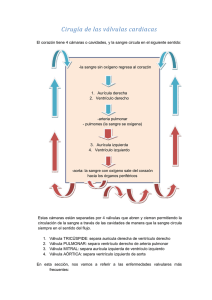
Revisión de las enfermedades coronarias y valvulares
Anuncio

Unidad de Investigación y Desarrollo para los Riesgos Agravados Focus Octubre 2007 Revisión de las enfermedades coronarias y valvulares Índice Introducción 2 Epidemiología y bases fisiopatológicas de la enfermedad coronaria 4 Fisiopatología Epidemiología y nosología Tratamiento de la angina inestable Tratamiento del infarto de miocardio Prevención secundaria Conclusión Impacto de las nuevas técnicas de revascularización miocárdica en el pronóstico de las cardiopatías isquémicas Concepto de revascularización Patologías coronarias La enfermedad coronaria: un nuevo enfoque Disminución de la mortalidad de las enfermedades coronarias Planteamiento de la tarificación de la enfermedad coronaria Principios de tarificación Tarificación de la incapacidad y la invalidez Tarificación de la dependencia Conclusión Valvulopatías cardíacas. Nuestro balance: panorama de los expedientes tratados por SCOR Global Life Valvulopatías nativas Pacientes portadores de prótesis valvular Eco-Doppler cardíaco: examen clave de las enfermedades valvulares Ecocardiografía Efecto Doppler Epidemiología, fisiopatología y factores de morbilidad y mortalidad de las valvulopatías cardíacas Epidemiología de las valvulopatías Fisiopatología de las valvulopatías Aportes de las nuevas técnicas quirúrgicas a la morbilidad y la mortalidad inmediatas y a largo plazo Válvulas mecánicas Válvulas biológicas Comparación de inconvenientes de los dos tipos de prótesis Homoinjertos Autoinjertos Elección del método terapéutico Plastias mitrales Evaluación del riesgo de las enfermedades valvulares cardíacas Consecuencias del enfoque médico más reciente de las valvulopatías cardíacas Esquemas de análisis Ejemplos prácticos de tarificación Conclusión Focus es una publicación del Grupo SCOR. La presente edición es propuesta por el Dr John Evans, Médico-consultante en la Unidad de Investigación y Desarrollo para los Riesgos Agravados de SCOR Global Life. Este folleto ha sido impreso en papel mate, fabricado a partir de un mínimo de 50 % de fibras recicladas combinadas con fibras vírgenes, según certificación del plan de medioambiente ISO 14001 4 8 9 11 12 13 14 14 16 22 22 22 23 24 24 24 25 25 25 27 27 27 29 29 30 36 36 37 37 37 38 39 40 44 44 44 46 49 Focus 3 Introducción La cardiología moderna ha experimentado un desarrollo extraordinario en las últimas décadas del siglo XX, fruto de una estrecha colaboración entre médicos e ingenieros en el diseño, realización y utilización de nuevos métodos de diagnóstico y tratamiento de las enfermedades cardiovasculares. En realidad, las proezas tecnológicas actuales se basan en procedimientos históricos de experimentación y observación, y en siglos de investigación sobre el corazón y la circulación. A principios del siglo XX, los cardiólogos utilizaron por primera vez métodos diagnósticos invasivos por cateterismo cardíaco de los que fue pionero Werner Forssmann en 1929. André Cournand y Dickinson Richards contribuyeron ampliamente a su difusión en los años cincuenta. Esta técnica consiste en la introducción de un tubo fino y flexible (catéter) en el corazón para medir la presión y el flujo sanguíneo, e inyectar una sustancia radiopaca con el fin de visualizar el corazón y sus vasos. Esta valiosa información ha permitido una evaluación mucho más precisa de las enfermedades cardíacas. Poco tiempo después, nació la coronariografía, utilizada por primera vez por Mason Sones en 1958, que permitió la exploración de las arterias coronarias enfermas y abrió el camino a la revascularización del corazón anginoso, técnica perfeccionada por Michael DeBakey en 1964, mediante derivación quirúrgica. Coronariografía: Hubo que esperar los trabajos de Andreas Gruntzig en 1977 para poder abordar estas mismas arterias situadas en la superficie del corazón por vía percutánea, con lo que surgió un nuevo campo de especialización cardiológica, el de la angioplastia coronaria. Esta técnica, cuyo principal defecto estaba relacionado con la restenosis en el sitio dilatado, registró otro progreso importante en los años noventa, gracias a la implantación de endoprótesis comúnmente llamadas «stents». De esta forma, los resultados de los cirujanos angioplásticos pudieron mejorarse y el número de intervenciones se multiplicó. Por otra parte, en los años cincuenta se ideó la primera máquina corazón-pulmón, que dio la posibilidad de operar a los enfermos cardíacos «a corazón abierto». La primera implantación de una prótesis valvular cardíaca mecánica fue practicada por Albert Starr en 1960; hecho que transformó la vida de miles de pacientes afectados por enfermedades valvulares hasta entonces incurables. En 1954, un progreso importante surgió en el campo de los métodos diagnósticos cardiológicos no invasivos con la utilización de los ultrasonidos. Una vez más, fruto de una estrecha colaboración entre un físico, Hertz, y un médico, Edler, la ecocardiografía se desarrolló como un método fiable y no invasivo para obtener datos anatómicos y funcionales cardíacos, que permiten ahora a los cardiólogos seguir mejor a sus pacientes y determinar las intervenciones necesarias. ECOCARDIOGRAFÍA VD VI AO AI Eje longitudinal paraesternal izquierdo: sístole VI = Ventrículo izquierdo AO = Aorta VD = Ventrículo derecho AI = Aurícula izquierda cardíaca o vascular, la llamada prevención «primaria», como después de su aparición, la llamada prevención «secundaria». En la actualidad las técnicas diagnósticas y los medios terapéuticos están ampliamente difundidos. Las mejoras materiales introducidas por los industriales y la experiencia acumulada por los operadores médicos permiten obtener mejores resultados clínicos con el fin de ofrecer una esperanza de vida de duración normal y mejor calidad. Esta publicación brinda la oportunidad de compartir con nuestros colaboradores habituales el resultado de nuestras reflexiones en este campo médico esencial. Nos da la posibilidad de asociar a numerosos profesionales de la selección, en particular durante las presentaciones y los debates organizados en el marco de los Encuentros Médicos de SCOR Global Life. Estos actos tienen como objetivo informar a nuestros clientes sobre los avances médicos y su impacto en nuestro trabajo diario de aseguradores de vida. Los datos recientes facilitados por los médicos especialistas muestran un progreso en el tratamiento de estas patologías cardíacas y deben permitir una mejor selección de los riesgos y una tarificación adecuada. Les deseamos una agradable lectura. Métodos: En la segunda parte del siglo XX también nacieron nuevas familias de fármacos activos en el tratamiento y la prevención de las enfermedades cardiovasculares. Los betabloqueantes y los inhibidores cálcicos previenen la angina de pecho; los fibrinolíticos, los inhibidores plaquetarios y los anticoagulantes orales son importantes para el tratamiento de las enfermedades trombóticas. Asimismo se dispone de tratamientos destinados a la estabilización y hasta la regresión de las placas de ateroma: las estatinas y los inhibidores de la enzima de conversión de la angiotensina. Por otra parte, los resultados de los estudios epidemiológicos han sido fundamentales en la racionalización de la atención médica de los pacientes. Entramos en la era de una medicina «basada en pruebas científicas». La identificación de los factores de riesgo cardiovascular y su corrección forman parte del trabajo diario de los médicos tanto antes de la aparición de una complicación Arteria coronaria derecha Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Derivación aortocoronaria izquierda Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Prótesis mecánica de bola Focus 5 Epidemiología y bases fisiopatológicas de la enfermedad coronaria Luz Las tres túnicas arteriales son la adventicia (pared externa de la arteria), la media y, en contacto con ésta, la íntima o el endotelio (capa de células que separa la sangre del resto de la pared arterial). El endotelio impide la formación del coágulo sanguíneo en una persona normal. En cambio, cuando se produce una rotura en la superficie de la placa, la sangre entra en contacto con el núcleo lipídico y se forma un coágulo. Capa fibrosa Núcleo lipídico Ro t ura Vul ner a Tamaño del corazón de la c bilid ad, e stí mulo s Accidente coronario agudo Varios fenómenos pueden favorecer la rotura de la placa. Tejidos fibrosos Material ateromatoso (núcleo lipídico) Trombo Hemorragia bajo la placa Macrófago Figura 1: Fisiopatología de los síndromes coronarios agudos Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Factores de trombosis - Factores locales - Factores sistémicos Embolización distal s Fenómenos mecánicos Cuando se observan las arterias coronarias, se constata que están en permanente movimiento, puesto que el corazón no deja de latir. Si se sufre de estrés, la presión arterial aumenta, lo que puede favorecer la rotura de las placas. Es el infarto por estrés. Células musculares lisas Octubre 2007 / Revisión de las enfermedades coronarias y valvulares ación /repar Li s i s apa n La rotura de la placa Espesor de la capa i lis La placa crece progresivamente limitando el flujo sanguíneo en el vaso, lo que reduce el aporte de oxígeno al órgano afectado. En lo que se refiere al corazón, cuando Placa vulnerable En varios casos, el proceso de cicatrización supera su objetivo y provoca la oclusión total o parcial del vaso: es el accidente coronario agudo. Se trata de un fenómeno localizado en el vaso. Pero a veces el coágulo se rompe, lo que produce una embolización. Se trata de pequeños fragmentos de coágulo y de placa liberados en la circulación, que obstruyen los pequeños capilares distales al gran vaso. si s bo om Tr Un proceso progresivo La placa se puede representar de forma esquemática como un volcán. El contenido lipídico se puede comparar con la lava. Arriba se encuentra un lago, separado de la lava por la capa fibrosa. Cuando la tapa se rompe, el volcán escupe lava, lo que puede provocar complicaciones. El contenido lipídico es un magma que contiene células, los monocitos macrófagos, así como un material rico en grasas esterificadas y, en especial, el factor tisular, principal activador de la coagulación sanguínea. Si el contenido lipídico entra en contacto con la sangre, se forma inmediatamente una masa y se produce un coágulo. Este fenómeno bó om Tr En algunas familias, el fallecimiento puede ocurrir muy precozmente, a partir de los 30 años. Hoy en día, podemos identificar algunos genes responsables, pero resulta muy largo y difícil establecer una relación de causalidad entre la existencia de un polimorfismo determinado y la expresión clínica de la enfermedad aterotrombótica. Los factores relacionados con la herencia interactúan con el segundo grupo de factores de riesgos cardiovasculares, relacionados con el entorno. Estos factores de riesgos son conocidos: algunos son adquiridos, como el tabaquismo, otros son mixtos, como la hipertensión arterial, las dislipoproteinemias (alteraciones de los lípidos), la diabetes, las alteraciones de la coagulación y la hiperhomocisteinemia. La interacción entre estos factores favorece el desarrollo de las estrías grasas en placas ateroscleróticas y luego, la complicación de estas placas en síndrome coronario agudo. La placa sigue ciclos de crecimiento con fenómenos de rotura (figura 1), que se producen de manera aleatoria. Tras la rotura, el contenido de la placa, el núcleo lipídico, entra en contacto con la circulación sanguínea, lo que crea un fenómeno de coagulación. Se forma entonces un coágulo, que puede ser más o menos obstructivo. Cuando el coágulo es totalmente obstructivo, la circulación sanguínea se interrumpe. La rotura de la placa es clínicamente palpable y se manifiesta por un infarto de miocardio cuando la arteria obstruida es la coronaria, por un accidente vascular cerebral (AVC), cuando es una arteria con destino cerebral, o por una isquemia crítica de miembro, cuando la pierna ya no recibe sangre, con riesgo de evolución hacia la gangrena. Cuando el accidente es grave, puede ocurrir el fallecimiento de origen cardiovascular. ació Los síndromes coronarios agudos son el resultado del llamado proceso de aterogénesis, una transformación progresiva de las estrías grasas en placas, que se observa en todos los individuos, como lo reveló un estudio anatomopatológico llevado a cabo en jóvenes soldados norteamericanos fallecidos durante la guerra de Vietnam. Estas placas son engrosamientos que reducen progresivamente la luz del vaso, sea cual sea su localización anatómica (carótidas, coronarias, miembros inferiores). Esta transformación se acelera bajo el efecto de dos principales factores: el primero de ellos está relacionado con la herencia, que los científicos están intentando desentrañar, y se traduce clínicamente en la aparición de una enfermedad coronaria antes de los 60 años. Fenómenos vasculares La arteria es un tejido vivo. Está alimentada por pequeños vasos situados en la adventicia, los vasa vasorum. Cuando estos capilares se obstruyen, se crea un hematoma a nivel de la placa que, a su vez, puede originar una rotura. Algunas placas son vulnerables porque a nivel de la capa fibrosa, contienen células inflamatorias que, en un momento dado, se activan y digieren la matriz que mantiene la cohesión del conjunto. La digestión de esta matriz pone en contacto el contenido lipídico y la luz vascular que inicia la coagulación. Se forma un coágulo para colmar el vacío que se produce tras la rotura de la capa fibrosa. Más del 99% de los fenómenos de rotura son clínicamente silenciosos debido al carácter armonioso del proceso de cicatrización. em od el Fisiopatología una persona hace un esfuerzo, el flujo aumenta en las arterias coronarias. En caso de disminución del calibre de la arteria, se crea una deuda de oxígeno, puesto que el flujo no puede aumentar suficientemente. Se sabe ahora que cuando el diámetro de la arteria se estrecha en más del 60% debido a la placa, aparece un fenómeno de angina de pecho. Es crónico, al igual que la claudicación intermitente, que se traduce en calambres a nivel de los miembros inferiores tras caminar algunos metros. de coagulación, diseñado por la naturaleza, sirve para cicatrizar las posibles heridas vasculares. Efectivamente, si el endotelio se rompe entonces la sangre en contacto con el endotelio se coagula, lo que permite reparar la lesión vascular. Lis is r El objetivo de esta exposición es aportarles una visión general de los síndromes coronarios agudos. Les propongo empezar con una reseña sobre la fisiopatología, proseguir con un cuadro nosológico y terminar con las estrategias terapéuticas modernas, que Émile Ferrari les detallará. Fenómenos inflamatorios Se trata de una cascada de fenómenos biológicos cuyo resultado es la digestión de la capa fibrosa que separa la sangre del núcleo lipídico. Una vez esta capa digerida, la sangre circulante entra en contacto con el contenido lipídico y provoca la formación del trombo (coágulo sanguíneo). Inflamación / Cicatrización Doctor Jean-Philippe COLLET. Instituto de cardiología - Hospital Pitié-Salpêtrière (París) iz nal Reca ón aci Focus 7 La obstrucción vascular provoca la asfixia progresiva de los tejidos que dependen del vaso ocluido: si no se interviene para abrir el vaso y aportar oxígeno, se irá formando un infarto. Sin intervención, la recanalización vascular se hará espontáneamente, pero a largo plazo, después de producir deterioros irreversibles. En algunos casos, existe un equilibrio entre apertura y cierre del vaso. Desde el punto de vista fisiológico, cada individuo posee un sistema de fibrinolisis, es decir, un mecanismo que evita el crecimiento excesivo del coágulo. Pero cuando se ha superado la etapa de la fibrinolisis fisiológica, el coágulo se desarrolla totalmente y obstruye la luz vascular. A veces se puede establecer una suerte de equilibrio inestable entre el cierre completo y la apertura parcial del vaso. Es el fenómeno de la angina inestable: los deterioros no están demostrados, pero existe un gran riesgo de evolución hacia una oclusión total del vaso. Marcadores biológicos Hoy en día algunas herramientas biológicas permiten afinar el concepto de accidente coronario agudo. En particular existen marcadores biológicos como la troponina, una proteína intracelular que garantiza la contracción del músculo cardíaco. Cuando la célula muscular muere a consecuencia de una obstrucción del vaso, la troponina (figura 3) es liberada en la sangre. Desde hace cinco años, podemos realizar la determinación de esta enzima. Cuando la detectamos en la sangre, sabemos que se ha producido una agresión del miocardio. Trombosis Oclusión Embolización Reperfusión Inestabilidad Infarto T Trombosis Embolia Trombosis Vasoespasmo Obstrucción Afección macrovascular Afección microvascular P O Una vez en contacto con el endotelio roto, las plaquetas sanguíneas se activan y adhieren al subendotelio para reparar la lesión vascular formando un agregado plaquetario. Se aglutinan para sellar la rotura del endotelio (figura 4a), constituyendo un tapiz en el que se activará la coagulación. no Coláge Es posible determinar la troponina en concentraciones muy reducidas que corresponden a microgramos de músculo cardíaco afectado. La utilización de estos marcadores ha permitido detectar un número mucho más importante de accidentes coronarios agudos que antes pasaban desapercibidos. 8 Efectos distales M Plaquetas Esta proteína se ha convertido en una valiosa herramienta para tarificar el riesgo. Existe una correlación directa entre el pronóstico y la concentración medida de esta proteína en la sangre circulante (figura 3b). Mortalidad a los 42 días (%) Efectos locales E Figura 3a: La troponina indica la existencia de una lesión tisular miocárdica que puede estar relacionada con una rotura de placa con trombosis coronaria, y con fenómenos de embolización en el lecho microvascular (capilar). Aterosclerosis Rotura I Trombo Plaquetas que adhieren al espacio subendotelial Mecanismos de obstrucción vascular (+) Troponina La aterotrombosis es una enfermedad bipolar, ya que implica fenómenos locales a nivel del gran vaso, sitio de la oclusión trombótica, y fenómenos distales relacionados con la embolización del material aterotrombótico en la circulación capilar. En algunos pacientes tratados precozmente por un infarto de miocardio mediante una desobstrucción total de la arteria coronaria responsable del infarto, la reperfusión del tejido miocárdico no es eficaz, pues padecen una enfermedad de los capilares asociada a la enfermedad de la gran arteria. Sabemos detectarla y conocemos parcialmente sus mecanismos, pero no contamos con herramientas terapéuticas para intervenir. Éste es uno de los límites actuales más importantes de los tratamientos propuestos. En tres de cada diez pacientes, la reperfusión tisular resulta ineficaz a pesar de la desobstrucción de la arteria coronaria. Valor predictivo TnI = Valor predictivo edad y < Valor predictivo del ST 7,5 7 4 3,4 FT Agregación (plaquetas activadas) TxA2 Serotonina ADP FvW (conformación desplegada) ανβ3 3,7 Fibrinógeno 3 1,7 2 GPllb/llla 1,0 831 0 to < 0,4 174 148 134 50 67 0,4 to < 1,0 1,0 to < 2,0 2,0 to < 5,0 5,0 to < 9,0 Ratio de riesgo 1,0 Intervalo de confianza del 95% 1,8 0,5 - 5,7 3,5 1,2 - 10,6 3,9 1,3 - 11,7 6,2 1,7 - 22,3 Figura 3b: Función pronóstica de la troponina Octubre 2007 / Revisión de las enfermedades coronarias y valvulares nina Adhesión > 9,0 Troponina cardíaca I (ng/ml) Figura 2 roto TxA2 se GPla 5 0 Osteopont ina La coagulación es un proceso que transforma un elemento soluble en la sangre, el fibrinógeno, en un elemento insoluble, la fibrina, que corresponde a la polimerización de las moléculas de fibrinógeno activadas. La fibrina forma una red de fibras que envuelven las plaquetas y refuerzan la estructura del coágulo (figura 4b), permitiendo su crecimiento y la aparición progresiva de una oclusión. 6,0 6 1 Agregación plaquetaria y formación del trombo Figura 4a Lesión miocárdica Una enfermedad bipolar (figura 2) Plaquetas activadas que adhieren al subendotelio lesionado Plaquetas circulantes Células endoteliales Espacio subendotelial LESIÓN TISULAR QUE SE PRODUCE EN UN MOMENTO DADO Rotura ADHESIÓN Y ACTIVACIÓN PLAQUETARIA 7,8 2,6 - 23,0 Figura 4b: La trombosis coronaria Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Va ll Ca++ Vllla lla Focus 9 Desde el punto de vista biológico, el objetivo de la fibrinolisis es la disolución de la trama constituida por la fibrina. En caso de desequilibrio entre la fibrinolisis y la formación del coágulo, la situación evoluciona hacia la obstrucción vascular. Todo empieza pues con la lesión de un vaso y la formación de un coágulo. Sabemos que se produce una cascada biológica: Activación de las plaquetas Agregación de las plaquetas Formación de la fibrina gracias a la activación de la coagulación, favorecida por la trombina Cada una de estas etapas es capital e influye en las demás con fenómenos retroactivos. Para ofrecer una terapia eficaz, hay que utilizar fármacos que bloqueen cada una de las etapas clave de la formación del coágulo (figura 4c). Aspirina Persantina Ticlopidina Clopidogrel Anti-llb/IIIa Heparina LMWH Heparina Antirombina Lesión Activación plaquetaria Agregación plaquetaria Generación de trombina Mecanismos de activación de las plaquetas Varias vías permiten activar las plaquetas: el receptor de ADP, el receptor de la trombina y el receptor del tromboxano. El conjunto provoca una activación de las plaquetas, piedra angular de la formación del coágulo. El objetivo de los tratamientos disponibles es bloquear cada una de estas vías metabólicas: trombina, ADP y tromboxano. Si se activa una de estas vías, se produce la activación de las plaquetas y la exposición a nivel de la plaqueta de receptores membranales en los que se fija una molécula circulante, que provocará la fijación definitiva de las plaquetas. Actualmente disponemos de un fármaco específico para cada una de estas tres vías. Los inhibidores de la ciclooxigenasa provocan un 30% de inhibición de la agregación plaquetaria. El clopidogrel (Plavix), inhibidor de los receptores de ADP, ofrece mayor eficacia. Mediante la combinación de estos dos tratamientos, se consigue bloquear el 60% de las plaquetas. Cada una de estas vías tiene una especificidad diferente (figura 4c). Desde hace algunos años disponemos de moléculas aún más eficaces, las anti-GP IIb/IIIa, que constituyen la denominada vía final común de la agregación plaquetaria. Sin estas moléculas, no hay agregación plaquetaria. Se utilizan en un espacio de tiempo muy corto. Se pueden comparar al air bag de un coche: se usan en los momentos críticos, en caso de accidente coronario agudo. Globalmente permiten reducir en un 50% las complicaciones de estos accidentes. Son moléculas caras y potentes. Aunque tienen una patogenia vecina, estas dos entidades clínicas se tratan de manera distinta: - El IM resulta de una oclusión coronaria total que requiere un tratamiento de reperfusión lo antes posible (trombólisis o angioplastia transluminal). - La AI, más frecuente, es una entidad heterogénea cuya atención diagnóstica es una etapa clave para individualizar a los pacientes con mayor riesgo y, en particular, los pacientes con infarto sin onda Q (IM-no-Q). La AI difiere también del IM por un riesgo de recidiva más alto y por el efecto deletéreo de los trombolíticos. En Francia no se dispone de datos precisos y exactos sobre el número de infartos o anginas inestables, pero se registran cerca de 150 000 ingresos por infartos con elevación del segmento ST. Son pacientes que llegan vivos al hospital, pero sólo uno de cada dos va al hospital. Unos 300 000 pacientes llegan con una angina inestable, la cual representa la patología más frecuente debido a la emergencia de factores de riesgo como la diabetes, el envejecimiento de la población (un 90% de los octogenarios tienen lesiones coronarias) y, por último, la mejor detección de las anginas inestables, posibilitada ahora por la troponina. Tratamiento de la angina inestable - Los marcadores biológicos se han convertido en herramientas indispensables. La troponina puede determinarse en menos de 10 minutos en la cama del paciente. Se trata de una herramienta de selección casi infalible para afirmar la naturaleza isquémica de un dolor torácico con un valor predictivo negativo del 97% y un factor predictivo independiente de la morbimortalidad coronaria. - Estas dos etapas se resumen en una puntuación de riesgo según la escala TIMI (figura 5), que permite evaluar la probabilidad diagnóstica y la morbimortalidad al cabo de un mes. PUNTUACIÓN DE RIESGO TIMI PARA LA ANGINA INESTABLE RIESGO DE EPISODIOS (%) ENTRE D1 Y D15 HISTORIAL edad ≥ 65 años ≥ 3 FRCV Enfermedad coronaria conocida Uso de aspirina PUNTOS PUNTUACIÓN FALLECIMIENTO O IM 1 1 0/1 3 3 3 1 1 2 5 PRESENTACIÓN Angina Reciente y severa enzimas cardíacas ST 3 7 4 12 5 19 1 1 1 1 Puntuación de riesgo: total de puntos (0-7) Figura 5 Actividad de trombina Trombo Figura 4c: Interés de las asociaciones de antitrombóticos para bloquear cada una de las etapas de la trombogénesis Todos estos fármacos están disponibles en el mercado: la aspirina, el principal de ellos; el clopidogrel (Plavix), una nueva molécula; los bloqueadores de la glicoproteína IIb/IIIa; y la heparina. El primer objetivo de la atención de los síndromes coronarios agudos es bloquear la formación del coágulo. Se ha comprobado que la combinación de estos tratamientos permitía evitar más eficazmente la oclusión total del vaso, a pesar de exponer al paciente a un riesgo de hemorragia. Efectivamente, al bloquear la formación del coágulo, estos fármacos favorecen las hemorragias. Un coágulo está formado por fibrina, que constituye una malla con algunos agregados plaquetarios. La alteración de esta trama fibrilar es perturbada a nivel de los agregados plaquetarios. Mediante la utilización de los inhibidores de IIb/IIIa, es posible eliminar los agregados plaquetarios y hacer que los coágulos sean más fácilmente alterables. El principal objetivo es triple: establecer la certidumbre diagnóstica, evaluar el perfil de riesgo de los pacientes e identificar los casos difíciles. Evaluación de la probabilidad diagnóstica y el perfil de riesgo Epidemiología y nosología Clínicamente un síndrome coronario agudo se manifiesta la mayoría de las veces con dolores en el pecho. Se distinguen dos grandes categorías de síndrome coronario agudo. Para ello se utiliza el electrocardiograma, un examen que registra la actividad eléctrica del corazón a nivel de la piel. Se deben diferenciar dos grandes tipos de síndromes coronarios agudos: el infarto de miocardio con elevación del segmento ST (IM) y la angina inestable (Al). - El examen clínico por sí solo permite establecer una probabilidad diagnóstica mediante la enumeración de los factores de riesgo clásicos (un paciente de menos de 40 años ingresado por dolor torácico, no fumador y sin antecedentes genéticos tiene una probabilidad de enfermedad coronaria < 2%); la búsqueda de un antecedente de infarto (interrogatorio, ECG); la búsqueda de una alteración de otro lecho vascular; y la búsqueda de una toma de fármacos con finalidad cardiovascular (aspirina y betabloqueantes). La función ventricular izquierda y la función renal integran el riesgo de episodios isquémicos graves (muerte o infarto), que se deben evaluar mediante la clasificación Killip (figura 6) y el cálculo del aclaramiento de la creatinina. La insuficiencia cardíaca (Killip ≥ 2) y la insuficiencia renal (aclaramiento de la creatinina < 30 ml/ min) multiplican por cuatro la morbimortalidad coronaria al cabo de un mes. CLASIFICACIÓN KILLIP I: Auscultación pulmonar normal II: Estertores hasta campos medios o galope III: Estertores en ambos campos pulmonares IV: Shock cardiogénico Figura 6 Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Focus 11 - Por último, la evaluación del riesgo hemorrágico (figura 7) es capital, ya que los antitrombóticos constituyen la piedra angular del tratamiento de la angina inestable. Estos pacientes presentan el mayor riesgo de episodios isquémicos graves (del 15 al 20% al cabo de un mes), así como el mayor riesgo hemorrágico. OR p <0,0001 Edad >80 2,08 Insuficiencia renal 1,85 0,03 Sexo femenino 1,51 0,018 Uso de anti-GP IIb/IIIa 2,4 <0,0001 Uso de HNF 1,81 0,0096 Uso de diuréticos 2,20 0,0003 Cateterismo cardíaco 2,86 <0,0001 Debido a la alteración permanente o transitoria de las funciones vitales (hígado, riñón y cerebro), estos pacientes presentan altos riesgos isquémicos y hemorrágicos. Prevención de la oclusión coronaria total Se trata de reducir la evolución hacia la trombosis coronaria total y, por lo tanto, la evolución hacia el infarto de miocardio con elevación de ST. Enfoque tradicional Se basa en los ensayos clínicos randomizados de finales de los años noventa, que demuestran la necesidad de un período de estabilización médica mediante la asociación aspirina / heparina / betabloqueantes (figura 8). Identificación de los casos difíciles Se trata de pacientes con alto riesgo y perfil atípico: personas mayores, pacientes diabéticos y contexto perioperatorio. - La heparina no fraccionada (HNF) disminuye en más del 80% el riesgo de evolución de la angina inestable hacia el infarto de miocardio y reduce por tres la incidencia de las anginas inestables refractarias. De manera interesante, las recidivas de IM y las reactivaciones de la AI tras la suspensión del tratamiento han permitido demostrar el interés de combinar la heparina con la aspirina en la fase aguda de la AI. Efectivamente, la HNF se puede suspender después de 4 a 6 días de tratamiento, mientras que la aspirina debe mantenerse a largo plazo en el marco de una prevención secundaria. En las personas mayores, la angina no suele ser típica y puede traducirse en disnea o flujo cerebral reducido, que origina caídas traumáticas o diagnósticos confusos. La angina inestable suele manifestarse con motivo de una enfermedad intercurrente que hay que identificar absolutamente: estado febril, anemia, etc. - Los betabloqueantes reducen la morbimortalidad al prevenir los trastornos graves del ritmo ventricular y la rotura miocárdica. La trombólisis es ineficaz y deletérea en la angina inestable. Los inhibidores cálcicos no ofrecen ningún beneficio demostrado, excepto el verapamil en la fase postinfarto. Figura 7 EFECTO DE LAS TERAPÉUTICAS EN EL DESCENSO DE FALLECIMIENTOS E INFARTOS EN LA FASE AGUDA DE LA ANGINA INESTABLE TRATAMIENTO NÚM DE ENSAYO NÚM DE PACIENTES Aspirina 4 3 114 Heparina 4 1 547 Betabloqueante 5 4 700 12 2 376 Inhibidores cálcicos 5 956 Angioplastia precoz 4 1 473 Trombólisis % de variación del riesgos (con un IC de 95%) de fallecimiento o infarto Enfoque moderno Gracias a una mejor comprensión de la fisiopatología de la angina inestable y de la trombogénesis ha nacido y se ha extendido el concepto de politerapia antitrombótica, que ha permitido en particular el desarrollo de las llamadas estrategias de revascularización precoz mediante angioplastia. El objetivo es asociar las diferentes clases de antitrombóticos para bloquear cada una de las etapas de la trombogénesis, como la activación plaquetaria, la agregación plaquetaria, la generación de trombina y el efecto de la trombina (figura 4c). ¿CUÁLES SON LAS RECOMENDACIONES? Asociar aspirina y clopidogrel en presencia de un anticoagulante (triterapia antitrombótica). Utilizar las Héparinas de bajo peso molecular (HBPM), que aparecen como una mejor opción que la heparina clásica no fraccionada debido a una mejor predictibilidad de la relación dosis-respuesta, una menor incidencia de la activación plaquetaria y una mejor tolerancia. Asociar un inhibidor de la GP IIb/IIIa cuando - se plantea una coronariografía, con el fin de realizar una angioplastia, - o en caso de isquemia refractaria, elevación de la troponina u otros factores de gravedad a falta de estrategia. Aporte de la angioplastia en la fase aguda de la angina inestable Reduce en un 20 a 30% la morbimortalidad coronaria. Este beneficio es tanto más importante cuanto que el perfil de riesgo de los pacientes es alto y la angioplastia va asociada a un inhibidor de la GP IIb/IIIa para limitar las complicaciones agudas precoces. Desafíos futuros -100 -50 < disminución Resultados obtenidos a partir de metaanálisis de ensayos randomizados Fuente: Granger CB. In: Califf RM (Ed) «Acute Coronary Care». Mosby, Philadelphia, PA, 1995; Chap. 42 0 50 aumento > El desarrollo de ensayos randomizados de calidad y la evaluación de numerosas terapéuticas antitrombóticas han hecho avanzar la revascularización por angioplastia, que interesa ahora un 25 a 30% de los pacientes ingresados por angina inestable. Tres principales desafíos permitirán mejorar la atención de nuestros pacientes. Figura 8 Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Octubre 2007 / Revisión de las enfermedades coronarias y valvulares 1. Evaluar estas estrategias agresivas en los pacientes excluidos de los ensayos randomizados por tener una insuficiencia renal grave, una insuficiencia cardíaca, una edad avanzada o un antecedente hemorrágico. Estas personas representan al menos un 40% de los pacientes y presentan una morbimortalidad multiplicada por 4. Por lo tanto, se beneficiarán, a priori, más de este tipo de atención. La evaluación de la tolerancia (riesgo hemorrágico) sigue siendo el mayor escollo. 2. Desarrollar y evaluar una atención expeditiva de la angina inestable mediante una revascularización precoz como en el infarto con elevación de ST. Se prevé que este tipo de enfoque, además de reducir el período de hospitalización y la duración de los tratamientos antitrombóticos agresivos, limite la morbimortalidad en los pacientes con mayor riesgo (angina subintrante, disfunción ventricular izquierda o trastornos graves del ritmo ventricular). 3. Desarrollar herramientas biológicas de seguimiento para adaptar la posología de los tratamientos antitrombóticos. Tratamiento del infarto de miocardio Me limitaré a presentarles algunas nociones básicas. Como ya lo saben, en caso de infarto, la arteria está obstruida. Solemos decir que «el tiempo es miocardio», pues cuanto más temprano intervengamos, más músculo salvaremos y más posibilidades de supervivencia tendrá el paciente. Hay que actuar muy pronto, ya que la desobstrucción de la arteria aumenta la tasa de supervivencia. Para ello, utilizamos la trombólisis o la angioplastia. La trombólisis consiste en desobstruir químicamente el vaso eliminando el coágulo, pero no la placa. La angioplastia consiste en eliminar el coágulo a la vez que la placa. Lamentablemente, la angioplastia sólo se puede practicar en centros especializados, mientras que la trombólisis puede realizarse en el domicilio del paciente. Cuanto más temprano se inicie el tratamiento, mayor será el número de vidas salvadas. Si se puede trombolizar a los pacientes en las tres primeras horas del infarto, se podrán salvar 80 vidas por cada 1 000 pacientes tratados. Pasadas las seis horas, el beneficio del tratamiento será muchísimo menor. Una intervención precoz es pues sumamente importante. Lo mismo rige para la angioplastia: cuanto más temprano se realice, más músculo y, por lo tanto, más vidas salvaremos. Focus Si miramos las condiciones de vida «reales», de cada 100 pacientes que presentan un infarto, 50 se beneficiarán de una trombólisis, 10 se someterán a una angioplastia en la medida en que esta técnica sea accesible, y 40 a 50 no recibirán ningún tratamiento, por lo que sufrirán las complicaciones del infarto que son la insuficiencia cardíaca y la muerte. Éste es uno de los grandes fracasos de los últimos diez años. Hemos progresado considerablemente desde el punto de vista científico en las técnicas de reperfusión. La angioplastia ha avanzado enormemente pero, desde el punto de vista logístico, los resultados son malos. La medicina no ha logrado ir al encuentro de los pacientes. Sólo un 40% es sometido a una revascularización, una tasa que no ha variado en diez años. Éste será nuestro verdadero reto para los años venideros. Prevención secundaria ¿Qué hacer tras un accidente vascular? Ante todo hay que corregir los factores de riesgo y evitar en especial que los episodios coronarios agudos vuelvan a ocurrir. Para ello, hay que pedir al paciente que deje de fumar y adelgace, si es posible, para corregir una diabetes o una hipertensión arterial. Luego utilizaremos varios tipos de fármacos. Estatinas Son agentes hipocolesterolemiantes. Fueron objeto de un premio Nobel de medicina. Actualmente existen 6 ó 7 moléculas disponibles en el mercado. El conjunto de estudios realizados en prevención primaria, es decir en personas que nunca han tenido un accidente vascular, y en prevención secundaria, es decir en personas que han sido víctimas de un accidente, muestra una reducción de la morbimortalidad (muerte/infarto) del 30%. Además se ha comprobado que el beneficio de estos fármacos no estaba totalmente relacionado con la reducción del colesterol, pues se ha observado un efecto propio en la pared del vaso. Estos fármacos son relativamente bien tolerados y su coste corresponde más o menos al consumo de un paquete de cigarrillos al día. Inhibidores de la enzima de conversión Se desarrollaron inicialmente para reducir la presión arterial. La experiencia ha mostrado luego que si se administran después de un infarto, se puede disminuir la Octubre 2007 / Revisión de las enfermedades coronarias y valvulares 13 mortalidad en un 20 a 30% o reducir las complicaciones subsecuentes, especialmente la insuficiencia cardíaca, actuando en la cicatrización del infarto. Aspirina Se utiliza a largo plazo para evitar la recidiva de la formación de coágulos. Previene en especial la muerte súbita y la recidiva de infarto; en contrapartida provoca complicaciones hemorrágicas relativamente moderadas. Reduce en un 30% los riesgos de muerte e infarto. Existe una relación directa entre el beneficio del fármaco y el riesgo del paciente. Las personas con angina inestable son las que presentan mayores riesgos y, por lo tanto, son las que obtienen mayor beneficio del fármaco en términos de reducción de la morbimortalidad. Cuando el riesgo absoluto de episodio coronario supera el umbral del 4%, el beneficio del tratamiento por aspirina aumenta y la relación beneficio/riesgo es favorable al tratamiento. Betabloqueantes Utilizados durante la fase aguda del infarto o a distancia, reducen considerablemente los trastornos del ritmo ventricular y, por lo tanto, las muertes súbitas, así como el riesgo de rotura cardíaca en un corazón debilitado por el infarto. tratamiento de los síndromes coronarios agudos. Actualmente existen marcadores biológicos que permiten evaluar el pronóstico de los pacientes. Se utilizan cada vez más, tanto en la cama del paciente como en urgencias. Uno de estos marcadores es el BNP (brain natriuretic peptide), una hormona liberada por el miocardio. Si su tasa es alta, significa un riesgo de mortalidad muy elevado, sea cual sea el mecanismo de agresión miocárdica. Otros marcadores biológicos permiten evaluar el riesgo de rotura de las placas. Tal es el caso de la proteína C reactiva (CRP): contenida en placas ateroscleróticas, es liberada en la sangre circulante en caso de digestión de una placa. Por lo tanto, es posible detectar a los pacientes que tienen numerosas placas inestables. Empezamos a disponer de marcadores biológicos que ofrecen información para prevenir las complicaciones. Son datos en fase de evaluación, que probablemente les ayuden dentro de algunos años a establecer las calificaciones de seguros. Patrick MALAMUD En lo que se refiere a la prevención primaria, ¿podría especificar los elementos que entran en cuenta para determinar la noción de riesgo cardiovascular absoluto? Por otra parte, ¿podría hablarnos del valor de la medición del espesor íntima/media? Jean-Philippe COLLET El conjunto de estos cuatro medicamentos debería formar parte sistemáticamente de la prescripción en los pacientes que han sufrido un accidente coronario agudo. Conclusión La escala de riesgo absoluto se ha establecido a partir de estudios prospectivos, especialmente el estudio de Framingham, del nombre de una ciudad situada al noreste de Boston, en la que se realiza un seguimiento de los habitantes desde hace casi 50 años. Se trata de una cohorte de 20 000 a 30 000 personas seguidas a largo Globalmente la patología coronaria y su séquito de complicaciones están en vías de regresión gracias esencialmente a los progresos realizados en la prevención primaria y secundaria y la atención de las complicaciones agudas de la enfermedad aterotrombótica coronaria (técnicas de revascularización, en particular). La utilización y la accesibilidad limitadas de estas técnicas constituyen un importante freno al desarrollo del tratamiento de los síndromes coronarios agudos. Se trata ante todo de un reto logístico y educativo. El desarrollo de escalas de riesgo cada vez más fiables representa otro desafío indisociable del progreso en el Octubre 2007 / Revisión de las enfermedades coronarias y valvulares plazo. Se han detectado las características clínicas de estos pacientes (hipertensión arterial, diabetes, etc.) y se les ha seguido a lo largo de los años. A medida que se han ido registrando episodios coronarios, se han podido establecer escalas de riesgos vasculares en función de la existencia de diabetes, hipercolesterolemia o hipertensión arterial. Ha sido posible establecer la llamada escala de Framingham, que tiene en cuenta el peso o el sexo. Son puntuaciones globales que determinan un perfil de riesgo, pero no la probabilidad exacta para cada persona de tener un accidente coronario agudo. Por este motivo, se han desarrollado otras herramientas, como las ecográficas, que permiten una medición del espesor íntima/media: para ello, se coloca un ecógrafo a nivel de las carótidas para medir el espesor entre la íntima, el endotelio vascular, y la media en que está situada la placa. La experiencia ha mostrado que en los pacientes sin accidentes coronarios, este espesor era predictivo del riesgo de accidente coronario, sea cual sea, tanto en las coronarias como en las carótidas. Actualmente numerosos médicos utilizan esta medición como medio de detección. En pacientes que presentan un espesor íntima/media elevado o placas ateroscleróticas detectadas por Doppler con pruebas de esfuerzo dudosas, se tiende a utilizar la coronariografía, pues se sabe que corren mayores riesgos de enfermedad coronaria severa que los demás. Es un indicio de riesgo muy utilizado en los pacientes jóvenes que acaban de tener un infarto, pues las personas que sufren un infarto antes de los 40 años presentan espesores íntima/media muy importantes a nivel de las arterias femorales. Aún no se conocen los mecanismos fisiopatológicos, pero son herramientas que se van introduciendo poco a poco en la práctica diaria. Focus 15 Impacto de las nuevas técnicas de revascularización miocárdica en el pronóstico de cardiopatías isquémicas Profesor Émile FERRARI. Servicio de cardiología - Hospital Pasteur (Niza). Las afecciones coronarias forman parte de las dos o tres primeras causas de mortalidad en las poblaciones ricas, y vivimos en un país rico. En 2020 representarán la primera causa de mortalidad en el planeta, para la totalidad de la población. Son enfermedades graves, ampliamente extendidas, que se convertirán en una de las primeras causas de mortalidad en el futuro. Esta exposición tratará sobre el impacto de las nuevas técnicas de revascularización miocárdica en el pronóstico de las cardiopatías isquémicas. Abordaré sucesivamente el concepto de revascularización, la técnica de la angioplastia, las indicaciones, los resultados respecto a otro método de revascularización como la cirugía, y los resultados respecto al tratamiento médico. El concepto de revascularización Cuando hablamos de infarto de miocardio o cardiopatía isquémica, nos interesamos esencialmente en el ventrículo izquierdo. El corazón consta de cuatro cavidades: las dos aurículas y los dos ventrículos. Su función principal es la de bombear la sangre, especialmente desde los pulmones hacia la circulación general. Cuando hablamos de músculo infartado, nos referimos al músculo del ventrículo izquierdo. La arteria coronaria es como un carburador que alimenta el músculo, sale de la aorta para aportar sangre. El músculo cardíaco es el único que funciona desde antes del nacimiento y hasta la muerte. Lo alimenta la arteria coronaria aportándole sangre, oxígeno y otros nutrimentos durante un promedio de 77 años en el hombre y 83 años en la mujer. Catéter introductor en la aorta Implantación de un «stent coronario» Guía en la arteria coronaria Octubre 2007 / Revisión de las enfermedades coronarias y valvulares La placa de ateroma La placa de ateroma coronario puede romperse y esta rotura de placa es algo muy común. Cada día personas sufren roturas de placas, que se repararon espontáneamente. La placa de ateroma coronario puede ser no obstructiva, obstruir lentamente el vaso o taparlo bruscamente. Si es no obstructiva, el síndrome generado suele ser una angina de pecho de esfuerzo. La angina se detecta clínicamente cuando el paciente describe un dolor colocando el puño en el pecho y explicando que siente como si tuviera el corazón atenazado por una prensa cuando corre para alcanzar el autobús, por ejemplo. Por cierto, lo primero que hay que hacer en esta situación es evitar levantarse tarde por la mañana para no tener que correr detrás del autobús… Cuando un paciente fumador, de 50 años de edad, describe este tipo de dolor opresivo en el pecho, en situación de reposo, que puede irradiarse a la mandíbula o el brazo, significa que padece la llamada angina inestable. Cuando la placa de ateroma no es totalmente obstructiva, la angina también puede provocar una insuficiencia cardíaca isquémica. La reducción del aporte sanguíneo tiene el mismo efecto en el músculo que el riego insuficiente en una planta cuando hace calor. El músculo, al igual que la planta que se marchita, «pierde fuerza». Si la obstrucción es brutal, la arteria se cierra por completo provocando un infarto de miocardio, es decir, la muerte del músculo cardíaco. Los infartos pueden ser silenciosos en los diabéticos, las personas mayores y los hipertensos. En estos casos, los síntomas no incluyen el dolor. Estos pacientes pueden consultar cinco o diez años después del episodio, no por el infarto que pasó desapercibido, sino porque padecen una fuerte insuficiencia cardíaca isquémica. La angina de pecho, que suele servir de alerta, no ha aparecido. Consecuencia de la obstrucción arterial La misma placa de ateroma puede provocar tres procesos distintos dando lugar a tres enfermedades coronarias diferentes: la angina de pecho, el infarto y, en menos ocasiones, una insuficiencia cardíaca isquémica. Me cuesta definir la «cardiopatía isquémica» a pesar de una experiencia de veinte años. ¿Se trata de un síndrome coronario agudo, una arteria que se obstruye bruscamente a pesar de que, dos minutos antes, el paciente se encontraba bien? ¿Se trata del estado de un coronario estable con una placa de ateroma que no obstruye totalmente la arteria, impidiendo el buen funcionamiento del corazón sólo cuando el paciente necesita un flujo cardíaco más importante? ¿O se trata del estado de un coronario demostrado, que ya ha sufrido daños en el ventrículo izquierdo? Me inclino a pensar que la cardiopatía isquémica corresponde a esta última situación. La oclusión repentina de una arteria coronaria se considera raramente como una «cardiopatía isquémica». Incluso en medicina, a pesar de los esfuerzos realizados en términos de nosología, no todo está claro. El infarto de miocardio se debe a la obstrucción total de la arteria que aporta sangre al corazón. Privada de sangre, la parte del músculo que depende de la arteria se necrosa, como cualquier músculo esquelético. Durante mucho tiempo se consideró que para hablar de infarto, había que reunir dos de las tres condiciones siguientes: Dolor típico, constrictivo (presión en el pecho), que dura hasta que la arteria se abre, o que puede durar 24 horas si la arteria no se abre. Algunos signos electrocardiográficos que el médico, y más aún el cardiólogo, debe saber detectar. Presencia de un marcador biológico, la troponina: cuando una célula cardíaca muere, su membrana citoplásmica se abre y «suelta» en la sangre todo su contenido, incluida esta enzima, que indica la existencia de infarto y muerte celular. La troponina es uno de los marcadores biológicos de necrosis miocárdica. Es la enzima cuya tasa sanguínea aumenta más temprano y permanece positiva más tiempo (se normaliza en 2 ó 3 semanas). En algunos pacientes es la única tasa que aumenta. Hace diez años no se podía diagnosticar un infarto cuando los únicos marcadores entonces utilizados, las CPK, no habían aumentado. Esta nueva definición basada en la troponina es más sensible y llevará probablemente a clasificar como «infartos de miocardio» a muchos más coronarios entre los pacientes ingresados en nuestras unidades de cuidados intensivos. Se evalúa en más de un 20% el aumento de la incidencia de infarto por este motivo. Un paciente con dolor en el pecho que ha registrado sólo un aumento de la troponina Octubre 2007 / Revisión de las enfermedades coronarias y valvulares será «clasificado» desde el punto de vista nosológico de la misma manera que un paciente que ha experimentado un aumento de las CPK. En ambos casos el informe de salida del hospital llevará el diagnóstico de «infarto de miocardio», pero el pronóstico será totalmente distinto. Volveremos sobre este punto más adelante. La tasa de troponina aumenta cuando la placa de ateroma se fisura y los «trozos» que se desprenden pueden embolizar, no tanto la arteria principal de 3 milímetros de diámetro, sino una pequeña arteriola periférica, provocando una discreta necrosis, detectable por el aumento de la troponina. ¿Sabemos reconocer con riesgo? las placas de ateroma Todos tenemos placas de ateroma en las paredes arteriales. En algunos, las placas pueden provocar la obstrucción de una arteria. En otros, no acarrean ninguna consecuencia. Al contrario de lo que el aspecto visual puede sugerir, la placa más amenazadora, la que puede agrietarse y tapar la arteria no es la placa más obstructiva. Éste es uno de los temas que plantean dudas en materia de cardiología intervencionista. Tratamos las placas que obstruyen el 75% de la arteria impidiendo la correcta circulación de la sangre, con el fin de limitar las anginas de pecho y las cardiopatías isquémicas. Pero la placa que puede provocar un infarto será probablemente una que sólo obstruye un 25% de la arteria. El caso es que no solemos tratarla porque son demasiadas y es difícil detectarlas. Si bien revascularizamos a los pacientes que presentan una angina de pecho estable, no lo hacemos tanto para evitar el infarto de miocardio, como para evitar la angina y suprimir el dolor de pecho. Cuando tiene una sola arteria afectada por el ateroma, el paciente es monotroncular; cuando tiene dos, es bitroncular; cuando tiene tres, es tritroncular. El riesgo no está estrictamente correlacionado con la importancia de la afectación coronaria. También entra en cuenta la evolutividad, que puede evaluarse mediante varios parámetros, especialmente biológicos. Si los «marcadores sanguíneos» de evolutividad de la enfermedad son bajos, el pronóstico de un paciente tritroncular será menos peyorativo que el de un paciente monotroncular que presente una elevación de los marcadores. Éste es un concepto nuevo en cardiología. En Focus el futuro dispondremos de determinaciones que permitirán ir más allá de lo que el aspecto visual de las arterias pueda sugerir, con lo que podremos tratar prioritariamente a un monotroncular que corre mayores riesgos de agravación que un tritroncular. Métodos de revascularización En algunas situaciones clínicas, es necesario traer «sangre nueva» al corazón realizando una derivación. Para ello, el cirujano puede utilizar las venas de las piernas para conectar «injertos venosos» a nivel de la aorta y «cortocircuitar» la zona anormal, con el fin de traer sangre rica en oxígeno y nutrimentos salvando el estrechamiento coronario y realimentar la parte del corazón en la que la aportación sanguínea está limitada. El cirujano también puede utilizar arterias (mamarias internas) para hacer un puente. Son dos, una a cada lado del esternón. La ventaja es que están conectadas en su parte superior a la arteria subclavia que alimenta el brazo. No tienen ninguna función vital, por lo que es posible seccionarlas y anastomosarlas a una arteria coronaria antes del estrechamiento. Si no se opta por la cirugía, se puede utilizar otra técnica que consiste en colocar un catéter de plástico de 3 milímetros delante de una arteria periférica con el fin de introducir en ella el material necesario para una «dilatación coronaria». De esta forma, se puede empujar dentro de la arteria una guía metálica de 0,4 milímetro de diámetro para que atraviese la lesión obstructiva. A continuación se coloca un balón sobre esta guía-carril, se empuja hasta la altura de la lesión obstructiva y se infla. Por el efecto de la presión, el balón se dilata y empuja la placa de ateroma hacia las paredes de la arteria. Luego se desinfla el balón y se retira. Una vez restablecida la luz en la arteria, es posible colocar una prótesis en forma de malla metálica, denominada «stent», a la altura de la placa. Por último, se quita el catéter dejando la prótesis en el sitio. Patologías coronarias Infarto de miocardio En caso de infarto, la arteria coronaria está totalmente obliterada. Sin aportación de sangre, el músculo Octubre 2007 / Revisión de las enfermedades coronarias y valvulares 17 alimentado por este vaso se vuelve lívido y muere si la oclusión dura entre cuatro y seis horas (ocho horas en algunos casos). La mortalidad de los pacientes que sufren un infarto de miocardio es superior al 40%, a los 30 días. De cada 100 muertes, 50 se producen en las dos primeras horas. Se trata de los pacientes que no han tenido tiempo de llamar al SAMUR y fallecen repentinamente. Si alguien se queja de un dolor en el pecho, hay que llamar al SAMUR. Hay que actuar muy rápido. Un 70 a 80% de los fallecimientos relacionados con un infarto de miocardio ocurre en las primeras 24 horas. Pasado este plazo, se evalúa en un 5 a 10% el porcentaje de fallecimientos anuales tras un infarto. Pocas enfermedades registran una tasa de mortalidad repentina tan alta. Entre los factores pronósticos tras un infarto de miocardio, se considerará el tamaño del infarto. Si la arteria obstruida es de tamaño muy reducido y el infarto afecta un centímetro cuadrado de músculo, el pronóstico no será el mismo que si la porción de músculo afectada es mucho más amplia. Cuanto mayor sea el infarto, más alterada estará la función de bombeo del corazón y mayor será el riesgo de insuficiencia cardíaca. La primera función del ventrículo izquierdo es recibir la sangre de los pulmones para aumentar su flujo y expulsarla hacia la circulación general. La insuficiencia cardíaca corresponde a la disminución del flujo distal. Su pronóstico es malo: la mortalidad es del 50% a los 60 meses. Algunos cánceres tienen un pronóstico mucho mejor. Es evidente que la función ventricular izquierda es un factor pronóstico esencial. Se puede evaluar mediante ecocardiografía y, de manera más precisa, mediante angiografía. Se coloca un catéter en el corazón. Se determinan los contornos del corazón cuando está totalmente lleno y cuando está totalmente vacío. La diferencia entre los dos contornos corresponde al volumen de sangre que el corazón expulsa hacia la circulación general cuando se contrae. Se mide la cavidad ventricular en diástole (debe ser de 130 cc aproximadamente) y en sístole (debe ser de 45 cc). La diferencia representa la fuerza contráctil del corazón, la fracción de eyección, que normalmente es del 60%. Si en un historial figura una fracción de eyección inferior al 40%, el paciente se encuentra en estado serio, por no decir grave. El segundo factor pronóstico ampliamente reconocido en todo el mundo es la isquemia residual, la cual puede afectar al vaso responsable del episodio reciente o a otro vaso. La prueba de esfuerzo permite evaluar la isquemia residual del territorio infartado y comprobar si existe isquemia en otros «territorios». La prueba de esfuerzo consiste en montar al paciente en una bicicleta y pedirle que pedalee con incrementos sucesivos de 30 vatios para que su frecuencia cardíaca aumente como si estuviera realizando un verdadero esfuerzo. Normalmente se lleva al paciente hasta un 75 a 80% de la FMT (frecuencia máxima teórica, equivalente a 220 menos la edad del paciente). Para que la prueba de esfuerzo sea fiable, el paciente tiene que alcanzar una determinada frecuencia cardíaca. Algunos empiezan a presentar, desde los 60 vatios y las 80 pulsaciones por minuto, una isquemia o incluso un trastorno del ritmo. Para estos pacientes, el pronóstico no es bueno. Tratamiento del infarto de miocardio: trombólisis versus angioplastia En caso de infarto de miocardio, lo urgente es abrir la arteria. Cuanto más rápido esté abierta, mayores serán las probabilidades de supervivencia del paciente. La técnica de la angioplastia con balón compite con la trombólisis, que consiste en un simple inyección intravenosa de un fármaco para «disolver» el coágulo que obstruye la arteria. Cuando se interviene en la hora que sigue al infarto, se salvan 80 vidas de cada 1 000 pacientes tratados. Podrán pensar que esta tasa no es alta, sin embargo es uno de los mejores resultados que se registran en cardiología. Cuando se interviene hacia la sexta hora, la tasa baja del 80‰ al 20‰. Cuando se interviene al cabo de doce horas, se expone al paciente a un riesgo hemorrágico relacionado con los fármacos utilizados, mientras que el beneficio esperado es casi nulo. Recuerden que cuanto más temprano se abra la arteria, mayor será el número de vidas salvadas. La trombólisis puede ser practicada por cualquier médico y en cualquier lugar, mientras que la angioplastia requiere el traslado de los pacientes a centros especializados, los cuales no están repartidos igualmente en todo el territorio francés. Estudios recientes realizados en el terreno para comparar los dos métodos de tratamiento arrojan resultados muy similares en términos de mortalidad a los 30 días. Ninguna técnica es significativamente superior a la otra. El medicamento trombolítico utilizado para desobstruir una arteria puede administrarse antes de la llegada al hospital. Ahora bien, los plazos del tratamiento, como acabamos de Octubre 2007 / Revisión de las enfermedades coronarias y valvulares verlo, revisten una importancia crucial; una hora puede ser capital. Por lo tanto, es preferible ofrecer a los pacientes un tratamiento medicamentoso precoz, aunque menos eficaz desde el punto de vista intrínseco que la angioplastia. Este dato es primordial en términos de salud pública. El inconveniente del tratamiento médico es que un 30 a 40% de los pacientes no responden. Además existe un riesgo hemorrágico con los trombolíticos. Por último, es posible que la arteria desobstruida se cierre en las horas que siguen: esto se produce en un 10 a 25% de los casos. La ventaja de la angioplastia en estos casos es que sus resultados son mucho mejores. La tasa de respuesta positiva es del 95% o incluso más con los mejores médicos. El inconveniente es la necesidad de trasladar al paciente a un centro médico especializado que disponga de personal capaz de practicar estas intervenciones. El consenso adoptado es el siguiente. El médico que atiende a un paciente víctima de un infarto de miocardio llama al centro sanitario más cercano. Si se prevé que el traslado va a durar menos de una hora, se lleva al paciente a una sala de cateterismo en la que se practicará la angioplastia. En cambio, si el hospital está saturado o se prevé que el traslado va a durar más de una hora, es preferible que el médico realice una trombólisis. Antes de 1960 la mortalidad del infarto hospitalizado era del 40%. Un paciente ingresado por infarto tenía cuatro probabilidades de diez de morir en el hospital. Más tarde se crearon las unidades de cuidados intensivos coronarios, que permitían colocar electrodos en el paciente para controlar los trastornos del ritmo ventricular, responsables de la mayoría de las muertes precoces. El mero hecho de vigilar a los pacientes durante tres o cuatro días para detectar o tratar las complicaciones rítmicas mortales en un 90% de los casos permitió reducir la mortalidad del 40 al 18%. La trombólisis también contribuyó de manera espectacular a la disminución de la mortalidad. Se recurrió a fármacos como los betabloqueantes y la aspirina, y luego los inhibidores de la enzima de conversión (IEC), para disminuir aún más la mortalidad. La tasa de mortalidad hospitalaria es hoy del orden del 6 al 7%. En los buenos artículos médicos se afirma que no hay rivalidad entre partidarios de la angioplastia y de la trombólisis. En el terreno, eso no es cierto: existe una rivalidad encarnecida entre estos dos tratamientos. En vez de guerrear para saber si más vale dilatar a los pacientes Focus con un método mecánico y eficaz o bien trombolizarlos, lo que resulta un poco más caro pero puede realizarse en un mayor número de personas. Es preferible atenerse a los datos. La proporción de pacientes sometidos a una revascularización, sea cual sea, dentro de la hora y media que sigue al infarto, es decir en el momento en que la intervención tiene más eficacia, es sólo del 8%. En vez de pelearse entre médicos para elegir una técnica de revascularización, sería sin duda preferible procurar que un mayor número de pacientes reciban un tratamiento rápido. En caso de infarto, la angioplastia representa un tratamiento «4 estrellas», pero la trombólisis es más accesible, más simple de realizar y, en términos de salud pública, puede salvar más vidas. 19 Angina estable Tomemos el ejemplo de una persona que va a comprar el pan cada mañana y, al correr detrás del autobús, empieza a sentir dolor en el pecho. En este caso, la «lucha terapéutica» no pone en juego dos técnicas, sino tres: el tratamiento médico, el tratamiento quirúrgico y la angioplastia. Estos tres métodos deben compararse. La supervivencia a más de 18 años de los pacientes sometidos a una derivación coronaria se estudia en el marco del registro CASS, que numerosas aseguradoras utilizan para establecer el pronóstico de estos pacientes. Angina inestable 0,09 Fallecimiento: año La angina inestable se debe a un trombo no totalmente obstructivo. La placa de ateroma reduce el flujo sanguíneo y provoca una isquemia en una parte del corazón. Se puede tratar de una angina en reposo (el paciente sin moverse padece un dolor en el pecho) o una angina al menor esfuerzo. En ambos casos, la angina es reciente y la urgencia es importante. Baja edad en el momento de la cirugía no es un factor favorable, como tampoco lo son el sobrepeso, un historial coronario, la toma de un medicamento diurético (existe una comorbilidad relacionada con la hipertensión o la insuficiencia cardíaca), el tabaquismo o la afectación del tronco común de la arteria coronaria izquierda. El hecho de utilizar sólo derivaciones venosas y no arteriales tampoco es un factor favorable: hoy sabemos que las derivaciones arteriales son más eficaces. Pronóstico de los pacientes sometidos a derivación/controlados 0,1 0,08 Control 0,07 Derivaciones 0,06 0,05 0,04 0,03 0,02 0,01 Desde 1989 el número de anginas inestables es superior al de los infartos de miocardio y esa diferencia irá aumentando. 0 0 2 4 6 8 10 12 14 16 Si la tasa de mortalidad de los pacientes sometidos a derivación es ligeramente más alta que la de la población normal, y si los pacientes de más edad sacan mayor beneficio de esta intervención, es porque existe una subpoblación de pacientes sometidos a derivación con una tasa de mortalidad más alta que la población normal. Resulta que los pacientes coronarios jóvenes suelen padecer una enfermedad evolutiva compleja cuyos factores de riesgo pueden ser numerosos. Es posible que el paciente no haya dejado de fumar o que los fármacos no hayan conseguido normalizar su hipertensión o hipercolesterolemia. 18 Años En algunas formas de angina estable, el tratamiento médico puede ser más eficaz que la revascularización. Nuestros jóvenes médicos tienen a veces la impresión de que prescribir sólo un tratamiento médico a un paciente no es suficiente para tratarlo. No es cierto y en algunos casos, el tratamiento médico es tan eficaz como la cirugía. Registro CASS > 18 años de seguimiento. Desde hace diez o quince años el cuerpo médico se interroga sobre la actitud a adoptar frente a las placas de ateroma coronarias que no son totalmente obstructivas, pero ponen en peligro el músculo cardíaco. ¿Debemos ser muy agresivos y revascularizar con técnicas instrumentales o «sólo» prescribir los medicamentos adecuados? Los numerosos estudios realizados permiten concluir que cuando el vaso es accesible y se administra un tratamiento antitrombótico fuerte, es preferible desobstruir la arteria, no con la misma urgencia que para el infarto de miocardio, pero sí en un plazo de 48 horas. Un estudio comparativo del método no invasivo (trombólisis) y del método invasivo (angioplastia o cirugía) ha demostrado que a los tres meses, el segundo ofrecía un mayor beneficio. Pero hay que pagar un precio. El método invasivo puede originar infartos: a veces, al querer desobstruir una arteria, podemos obstruirla. Pero si protegemos al paciente con los medicamentos mencionados por Jean-Philippe Collet, el precio a pagar (en términos de complicaciones) desaparece. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares En los primeros meses los pacientes sometidos a derivación mueren con mayor frecuencia debido al riesgo operatorio, pero después, su tasa de mortalidad no es catastrófica. No obstante, la diferencia no es considerable. A los cinco años, la tasa de supervivencia es del 90%, una cifra muy satisfactoria respecto a la media de edad, al estado de salud y a la intervención realizada. Aseguramos en el 74% de los casos al menos diez años de supervivencia y, en el 56% de los casos, al menos quince años. La edad del paciente en el momento de la operación es importante. De hecho, observamos que los pacientes operados a los 65 ó 75 años tienen una tasa de supervivencia muy buena, comparable incluso a la de la población testigo. Un paciente mayor, sometido a derivación en el momento oportuno, tiene asegurada una esperanza de vida de diez años en el 74% de los casos y de 15 años en el 54% de los casos. Un septuagenario sometido a derivación tiene una esperanza de vida de diez años en un 60% de los casos. El estudio RITA-2 se llevó a cabo en 1 018 pacientes con angina estable. De forma aleatoria algunos fueron sometidos a una angioplastia y otros a un tratamiento médico solo, y se siguió su estado de salud durante dos años. La tasa de fallecimientos por infarto fue dos veces más importante con la opción instrumental «agresiva». Este estudio fue publicado en 1997 y se refería a técnicas utilizadas entre 1993 y 1994, menos eficaces que las actuales. Pero en mi opinión, los resultados siguen siendo válidos: si bien la angioplastia ha progresado desde entonces, también lo ha hecho el tratamiento médico. Un meta-análisis de la comparación entre tratamiento médico y angioplastia, referente a seis pruebas y 1 000 pacientes, muestra que la angioplastia reduce en un 30% el riesgo relativo de angina de pecho. Este resultado es lógico puesto que la apertura de la arteria permite una revascularización del músculo. También muestra que la angioplastia crea más infartos de miocardio. Con esta técnica se registra un sobrerriesgo de muerte y una mayor necesidad de realizar otra angioplastia o cirugía en el futuro. Cabe Octubre 2007 / Revisión de las enfermedades coronarias y valvulares subrayar que la introducción de un instrumento en una arteria enferma puede crear una patología con consecuencias a largo plazo. El tratamiento médico más importante no es el que elimina los signos de angina de pecho, que pueden ser útiles para dar la alarma, sino el que impide la rotura de la placa. El tratamiento debe evitar que se cree una fisura y el volcán «escupa» su contenido. Si se comparan las técnicas de angioplastia y derivación, como ya lo han hecho numerosos estudios, la primera parece menos compleja que la segunda. Se asocia con menos complicaciones inmediatas: se observan menos accidentes vasculares cerebrales y menos infartos. Sin embargo, el punto débil de la angioplastia radica en la tendencia de la arteria a cicatrizar demasiado cuando se le introduce una prótesis. Esta mala evolución o restenosis, que no depende del operador ni de la técnica, puede afectar al 25 ó 30% de los casos, en los que siempre es posible repetir la intervención para reparar la mala cicatrización. Las ventajas de la derivación son que, a priori, se puede realizar una revascularización más amplia (hasta cinco arterias simultáneamente) y se registran menos recidivas a corto plazo. Los inconvenientes son las complicaciones operatorias. Además, un 10% de las derivaciones se obstruyen desde la salida del quirófano y un 50% en un plazo de diez años, por lo que la tasa de recidiva a los diez o doce años es alta. Existe un gran vacío en el campo de los estudios comparativos entre las diferentes técnicas. Si se comparan la angioplastia y la derivación a los seis meses, la primera es menos eficaz que la segunda con un 70% de buenos resultados frente a un 90%. A los cinco años, la angioplastia sigue teniendo los mismos resultados, mientras que las derivaciones empiezan a obstruirse, por lo que las dos técnicas ofrecen la misma eficacia. A los diez años, la angioplastia sigue registrando un 30% de malos resultados, pero las derivaciones arrojan ya un 50%. En consecuencia, si se quiere comparar las dos técnicas, hay que integrar la dimensión temporal. A los seis meses, la cirugía siempre tiene la ventaja. Por otra parte, las técnicas siguen evolucionando. Cuando se inicia un ensayo, se necesitan entre cinco y ocho años para publicarlo. Si las dos técnicas que se desea comparar han progresado de distintas maneras, el resultado del ensayo sólo tendrá un valor histórico. Es precisamente lo que está pasando con la angioplastia. Focus Su principal inconveniente era la cicatrización después de la colocación de la prótesis. Ahora bien, al parecer habríamos encontrado un remedio contra esta restenosis. En este caso, ¡la angioplastia no presentaría ya ningún inconveniente! El profesor Ferrari muestra un ejemplo de revascularización por angioplastia en una animación vídeo. Se trata de la introducción de una guía hasta el estrechamiento de la arteria para colocar un stent. El segmento patológico queda totalmente reparado. Esta intervención dura unos veinte minutos frente a cuatro o cinco horas para una operación quirúrgica. El paciente puede ingresar por la mañana y salir al día siguiente, mientras que en el caso de la cirugía, necesitaría varios días de reanimación y quince días de convalecencia como mínimo. Preguntas de la sala ¿Se dispone de resultados comparativos entre la angioplastia y las técnicas de derivación coronaria a corazón latiendo? Émile FERRARI Hay que ser justo: ¡los cirujanos también progresan! Intentan encontrar nuevas técnicas. Admitamos sin embargo que mientras la medicina intervencionista progresaba muy rápidamente en los últimos quince años, los cirujanos se han dormido un poco en los laureles debido al número de enfermos que tenían que operar. Cuando vieron que los cardiólogos también podían desarrollar técnicas endovasculares, se dieron cuenta de que tenían que progresar. Actualmente algunos equipos de cirujanos tratan cada vez más de revascularizar a los pacientes sin recurrir a la circulación extracorpórea. Abren el esternón y utilizan la arteria mamaria (esa misma que Dios creó especialmente para los coronarios), para anastomosarla a corazón latiendo, sin derivar la circulación. Esa técnica es mucho menos compleja que la técnica convencional, pero no se puede aplicar a todos los pacientes: no es adecuada para las patologías difusas y las arterias de mala calidad. No obstante, representa un adelanto. Cuando se comparan las técnicas, hay que tener en cuenta los progresos realizados. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares 21 De la sala Desde el punto de vista de la normativa, sólo se puede practicar una angioplastia en un servicio de cirugía cardiovascular con CEC. Émile FERRARI Es una obligación reglamentaria ya anticuada. Es cierto que legalmente, el paciente debe ser trasladable a un centro en menos de una hora. En el sureste de Francia, los centros de cardiología son tan numerosos que el problema no se plantea. En Córcega, sí se plantea y la dilatación sólo puede realizarse en urgencia. Este problema no limita las indicaciones de angioplastia. John EVANS En materia de progresos técnicos, se habla de stents envueltos que resolverían el problema de la restenosis. ¿Cuáles son los avances científicos al respecto? salga bien, y una posibilidad sobre tres o cuatro de que sea necesario proceder, en un plazo de tres a seis meses, a otra dilatación. Seis meses más tarde, le ponemos el contrato en las manos y le preguntamos si prefiere la cirugía o quiere intentar otra angioplastia. Al cabo de tres o cuatro intentos, parece razonable abandonar la angioplastia y confiar el paciente al cirujano. Tratamos de hacer previsiones. Sabemos en particular que un diabético sufre más restenosis que otros pacientes. Si tiene tres lesiones que tratar, le recomendamos de preferencia la cirugía. Michel DUFOUR La duración de la baja laboral constituye para nosotros una preocupación esencial. Imagino que no es la misma en el caso de los tratamientos descritos y en el caso de la cirugía. Émile FERRARI Todo depende de la situación que ha llevado a la angioplastia. En caso de infarto de miocardio, la baja no se Émile FERRARI El principal inconveniente de los stents es la cicatrización proliferativa, la restenosis. Al parecer se habría encontrado el medio de evitar este exceso de cicatrización gracias a un producto inicialmente anticanceroso, que limita la cicatrización. Efectivamente, cuando se opera a un paciente, se le puede formar una cicatriz queloide, es decir, abultada y exuberante. Lo mismo puede ocurrir en los tratamientos contra el estrechamiento de las arterias del corazón. Aparentemente, sería posible impedir la cicatrización proliferativa con este anticanceroso. Los primeros resultados son excelentes. En un artículo del Dr. MC Morice publicado en el New England Journal of Medecine, se indica una tasa de restenosis del 0% al cabo de un año. Hacía casi diez años que se estaban probando todos los medicamentos posibles para acabar con este talón de Aquiles de la angioplastia. Esta familia de medicamentos anticancerosos parece ser la adecuada. Con la respuesta a la restenosis se mejorará necesariamente la técnica y se confiará un menor número de pacientes a los cirujanos. Patrick MALAMUD ¿Cuál es el estado de avance de las angioplastias iterativas? Muchos pacientes se someten a angioplastias iterativas o se benefician de ellas. ¿Hasta dónde podemos llegar en este campo? Émile FERRARI La tasa de restenosis tras una angioplastia es de un 20 a 30%. A cada dilatación es la misma. Cuando se dilata a un paciente, hay siete probabilidades sobre diez de que todo Octubre 2007 / Revisión de las enfermedades coronarias y valvulares justifica por el acto médico sino por la enfermedad, es decir, el infarto. Entre el momento en que el paciente siente un dolor y el momento en que llega al servicio de cardiología, su infarto ha evolucionado. A partir del momento en que se le atiende, se aborta el infarto en curso, pero no se pueden reparar las lesiones ya formadas en el músculo cardíaco. Ahora bien, en caso de infarto, hay que prever uno a varios meses de baja. En cambio, si un paciente consulta un lunes y le «dilatan» al día siguiente por una angina de esfuerzo o incluso de reposo, podría volver al trabajo al cabo de tres días de baja. Puede que intente «tirar de la cuerda», pero no siempre se justifica prescribir tres meses de baja tras una angioplastia, no faltaba más. Focus 23 La enfermedad coronaria: un nuevo enfoque Doctor John EVANS. Médico asesor, SCOR Global Life Disminución de la mortalidad de las enfermedades coronarias Planteamiento de la tarificación de la enfermedad coronaria La disminución observada de la mortalidad de la enfermedad coronaria es el principal aspecto que ha motivado nuestro encuentro. Se constató por primera vez a finales de los años setenta en Estados Unidos. La OMS desarrolló entonces un proyecto internacional, denominado Monica, con el fin de estudiar las tendencias de mortalidad en 21 países. Varios de sus resultados son asombrosos: Nuestra reflexión sobre las enfermedades coronarias no ha desembocado en cambios sustanciales. Hemos comprobado que algunos problemas agudos estaban asociados al infarto de miocardio y al síndrome coronario agudo, y provocaban una mortalidad precoz bastante alta. La piedra angular de la tarificación de las enfermedades coronarias sigue siendo el aplazamiento del riesgo hasta la obtención de una estabilidad clínica. Se destaca la gran variabilidad geográfica de la mortalidad por insuficiencia coronaria. Tras un episodio cardíaco agudo (angina inestable, infarto, angioplastia, derivación coronaria), les aconsejaremos aplazar el riesgo durante seis meses como mínimo. A los seis meses pediremos al médico tratante o al cardiólogo un perfil cardiovascular que demuestre la estabilidad de la enfermedad coronaria, con el fin de descartar el riesgo de muerte precoz y poder seleccionar los mejores riesgos. Puede que algunos de estos consejos parezcan obsoletos, pero la dificultad actual no está relacionada con la enfermedad coronaria aguda, sino con la enfermedad coronaria crónica. En el marco de nuestra evaluación del riesgo, conviene pues identificar los factores que influyen en la mortalidad a largo plazo de un episodio cardíaco agudo. Los países con peores resultados son Checoslovaquia y Rusia. En cambio, el número de fallecimientos por enfermedad coronaria es sumamente reducido en Japón. La tasa de mortalidad siempre es más baja en la mujer que en el hombre. La mayoría de los países industrializados han experimentado desde los años sesenta una disminución significativa de la mortalidad por enfermedad coronaria, mientras que los países del Este han registrado un aumento de esta tasa. Las tasas de mortalidad son más altas en el norte que en el sur de Europa. Este dato ha dado nacimiento al término muy discutible de «paradoja francesa», pues si bien es cierto que la mortalidad es menor en Francia, es más alta en Lille que en Toulouse. Existen factores de prevalencia de la enfermedad coronaria que difieren según las poblaciones, pero también se puede explicar el aumento de la supervivencia por la mayor eficiencia de los médicos. En todo caso, se cuestiona actualmente el modelo clásico de predisposición genética a la arteriosclerosis, agravada por factores ambientales, con complicaciones clínicas que conducen a la muerte. Podemos pensar que los cuidados proporcionados en prevención primaria o secundaria, gracias en parte a la intervención médica, invertirán la tendencia entre el número de complicaciones clínicas y el número de muertes. Los cuidados prodigados en el momento de los síndromes coronarios agudos también contribuirán a la disminución de la mortalidad. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Efectivamente, para los monotronculares, la tasa de supervivencia a los seis años es la misma con angioplastia, derivación o tratamiento médico. Para los tritronculares tratados por cirugía, la tasa de supervivencia a corto y mediano plazo es ligeramente diferente, pero la supervivencia a largo plazo es la misma con derivación o tratamiento médico, debido probablemente a la obstrucción progresiva de las derivaciones. Función ventricular izquierda El segundo dato a tener en cuenta es la función ventricular izquierda. La fracción de eyección es la relación entre el volumen de sangre eyectado y el volumen telediastólico, cuando el ventrículo izquierdo termina de llenarse. Se puede evaluar también mediante coronariografía por ventriculografía. A largo plazo se mide por ventriculografía isotópica o, en la mayoría de los casos, por ecocardiografía. El estudio CASS muestra que la supervivencia a los ocho años es muy diferente entre las personas con fracción de eyección normal y fracción de eyección anormal, sea cual sea el número de troncos coronarios afectados. La supervivencia a los ocho años es claramente inferior cuando la función de eyección está alterada. La tasa de fallecimientos a los doce años aumenta cuando la molestia funcional se agrava. Además, la mortalidad a los cinco años de los insuficientes cardíacos no permite ofrecerles una cobertura de seguro de vida. Gravedad de la afectación coronaria Capacidad funcional El primer dato a tener en cuenta para la evaluación es la gravedad de la afectación coronaria, que se mide mediante coronariografía. Según el estudio CASS, que analiza las supervivencias a los ocho y quince años, existen diferencias significativas en la supervivencia de los pacientes monotronculares y los pacientes tritronculares tanto a los ocho como a los quince años. Nuestra evaluación excluirá la estenosis proximal del tronco coronario izquierdo, que constituye un caso muy particular, una urgencia cardiológica que requiere una revascularización inmediata, ya que amenaza un amplio territorio miocárdico. El estudio CASS, uno de los únicos que propone un seguimiento a largo plazo, muestra una diferencia en la supervivencia de los pacientes según el número de troncos arteriales afectados. El tercer dato es la capacidad funcional y los resultados de los pacientes a largo plazo después del episodio cardíaco agudo, que se pueden evaluar en particular mediante la prueba de esfuerzo. Este factor es mucho más importante en la supervivencia a los seis años que la naturaleza del tratamiento inicial. En un grupo de pacientes cuya capacidad de esfuerzo es normal, sean individuos normales o individuos con enfermedades cardiovasculares, el riesgo relativo de fallecimiento, aun corregido por la edad, es cuatro veces más alto para los pacientes que presentan los peores resultados. Ésa no es una noción nueva: Darwin ya la menciona en su tratado sobre la evolución genética. En este mismo estudio, se ha seguido en el tiempo la supervivencia de los pacientes que consultaron para realizar una prueba de esfuerzo. Los individuos que registraron los peores resultados tienen una curva de supervivencia siempre inferior a los individuos que obtuvieron resultados normales en la prueba de esfuerzo. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Principios de tarificación A partir de la coronariografía, la fracción de eyección ventricular izquierda y la prueba de esfuerzo, se determina una tarificación básica, que varía según los factores pronósticos. El tabaquismo es sin ninguna duda el más importante. Normalmente no lo consideramos como un sobrerriesgo de mortalidad en nuestros expedientes, a no ser que el consumo supere un paquete diario. En cambio, debemos tarifar el tabaquismo persistente en los pacientes que han sufrido un episodio cardiovascular, aunque represente uno o dos cigarrillos diarios. También tarificamos la dislipidemia, la hipertensión y la diabetes. De hecho, el seguro de los diabéticos afectados por una enfermedad coronaria es costoso. Asimismo podemos introducir el factor hereditario si uno de los padres del solicitante de seguro sufrió una enfermedad cardiovascular a una edad inferior a 60 años. Por último, tenemos en cuenta la calidad del tratamiento del solicitante, en particular, con respecto a los cuatro medicamentos principales, la aspirina, los inhibidores de la enzima de conversión, las estatinas y los betabloqueantes. Por consiguiente, el principio esencial de la tarificación será el aplazamiento hasta la «consolidación del estado» y luego una selección médica basada en un cuestionario adaptado a las enfermedades coronarias. También se recomienda obtener el informe hospitalario con los datos de la coronariografía, del tratamiento y de las complicaciones observadas durante la fase aguda, así como el balance de seguimiento con los resultados de una prueba de esfuerzo a los tres o seis meses y una evaluación de la función ventricular izquierda mediante ecocardiografía, realizadas por el cardiólogo tratante. La tarificación del seguro de vida de las estenosis del tronco coronario izquierdo no revascularizadas y de las alteraciones importantes de la función ventricular izquierda ocupa un lugar especial. Se sabe que el capital miocárdico perdido nunca se recupera. La tarificación básica se modula según los factores pronósticos. Los elementos de buen pronóstico son principalmente una afectación coronaria limitada con función ventricular izquierda correcta, la ausencia de isquemia residual en la prueba de esfuerzo, la corrección de los factores de riesgo que han provocado la primera patología y el cumplimiento del tratamiento médico. Cabe recordar que la aterosclerosis no se sitúa sólo en la red coronaria. El estudio BARI, que se refiere a la revascularización por derivación o angioplastia, muestra que la Focus sobremortalidad de los pacientes con afectación carotídea o afectación de las arterias de los miembros inferiores es del 200% respecto a los coronarios sin afectaciones de este tipo. Cuando ambas afectaciones se añaden a la afectación coronaria, la sobremortalidad es del 400%, al límite de la asegurabilidad. Tarificación de la incapacidad y la invalidez Esta cuestión es muy difícil de resolver debido al número de factores que influyen en la duración de la baja laboral o la solicitud de invalidez. Es evidente que una derivación coronaria secundaria a un infarto no tendrá la misma consecuencia en la incapacidad o la invalidez que una angioplastia consecutiva a una angina inestable que ocasionó una baja de tres, cinco o siete días. Durante la evaluación hay que determinar la pérdida funcional, es decir, identificar la naturaleza de la patología. Hay que medir la capacidad de esfuerzo, la existencia o no de una rehabilitación cardíaca. Para averiguar las capacidades funcionales, el médico se remite a la prueba de esfuerzo, que indica si el paciente presenta un riesgo reducido, medio o elevado. El V02max (consumo máximo de oxígeno) ilustra la capacidad de esfuerzo. Es útil comprobar si el paciente padece una isquemia en reposo o de esfuerzo y si tiene trastornos del ritmo durante el esfuerzo. Interactúan pronósticos y factores de riesgos asociados, por lo que se tomarán en cuenta el tipo de trabajo y las condiciones laborales: una persona que trabaja en un ambiente estresante y sufre hipertensión tendrá más riesgos de caer en la incapacidad o la invalidez. También intervienen factores personales como la edad y factores psicológicos o sociales. La depresión es un factor de comorbilidad muy importante. Por otra parte, interviene la motivación de los médicos tratantes: algunos no quieren, erróneamente, que sus pacientes reanuden el trabajo. Por último hay que tener en cuenta la naturaleza del trabajo, en particular si éste es muy físico. Algunos puestos pueden incluso ser perjudiciales. Por ejemplo, el trabajo nocturno provoca alteraciones fisiológicas y dificulta el tratamiento médico. El médico laboral puede facilitar la decisión de vuelta al trabajo contribuyendo a acondicionar el puesto o modular el tiempo de trabajo. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares 25 Valvulopatías cardíacas Nuestro balance: panorama de los expedientes tratados por SCOR Global Life Es difícil proponer una tarificación general debido a la multiplicidad de los factores. Es evidente que el estado clínico se tomará aún más en consideración si el paciente es conductor de camiones o piloto de avión. En caso de anomalía funcional, es más probable que se le declare en incapacidad o invalidez debido a sus responsabilidades profesionales. Desde el punto de vista médico, algunos trastornos del ritmo acarrean un riesgo de síncope que puede ser mortal para los operadores que trabajan en una cadena de producción. No me refiero a problemas con marcapasos, pues los nuevos aparatos resisten a los campos magnéticos. Valvulopatías nativas Las particularidades del contrato de seguro ocasionan a veces bajas laborales prolongadas, especialmente cuando el nivel de indemnización es muy alto, la duración es larga y el período de franquicia es corto. El riesgo de siniestro es mayor con un período de franquicia inferior a 90 días. La edad máxima es de 85 años (sacada probablemente de un expediente de dependencia). El histograma de edades arroja una media de edad de entre 45 y 49 años. La edad de la persona es un factor esencial. Cuánto más cercana esté de la jubilación, menor será la motivación para reanudar la actividad. La evaluación de la enfermedad también es muy importante para saber si el individuo puede, en función de su capacidad ventricular izquierda, realizar o no un esfuerzo físico. La duración de las bajas laborales tomadas a la espera del seguro de garantías complementarias es otro elemento que se debe tener en cuenta. Tarificación de la dependencia Si la persona es autónoma, el antecedente de síndrome coronario agudo sólo ocasionará una sobreprima moderada, relacionada con el riesgo cardiovascular. Aunque caiga en la dependencia, la experiencia nos muestra que la duración del pago de la renta será relativamente corta, al menos en lo que se refiere a la dependencia total. Conclusión SCOR Global Life cuenta con un esquema de tarificación de la enfermedad coronaria que incluye un análisis de la última coronariografía, la función ventricular izquierda, la última prueba de esfuerzo y los factores de riesgo pronósticos. Esperamos que este planteamiento permita llegar a una tarificación más adecuada y cercana al riesgo real que estos pacientes presentan actualmente. Doctor Patrick MALAMUD. Médico asesor, SCOR Global Life Estas patologías representan un número importante de expedientes sobre un período de diez años aproximadamente, con una distribución similar a la que se observa en la clínica. La insuficiencia mitral es la patología que más se observa en materia de riesgo agravado. En esta población, se registran sólo 20 rechazos por 50 aplazamientos (entre los que figuran 3 por razones administrativas). Por tanto, los expedientes que las cedentes nos envían son muy completos. Las patologías asociadas pesan mucho en la tarificación de estas cardiopatías. Al respecto, se observa una predominancia estadística de los trastornos del ritmo y la hipertensión arterial, y se registran relativamente pocas patologías coronarias. Los espesamientos mitrales representan 302 expe-dientes de los que 232 han dado lugar a una tarificación; los rechazos han sido finalmente bastante escasos (un 7% del total). La edad mínima y media es un poco menos alta para esta enfermedad que para el conjunto de las insuficiencias mitrales. Las patologías asociadas son, en principio, poco severas. Se han presentado relativamente pocos expedientes de estenosis mitral (31 en diez años). Es muy difícil sacar información a partir de una población tan reducida. Las enfermedades mitrales (asociaciones de insuficiencia y estenosis) también registran una cifra muy baja (37 expedientes). Esta población limitada no permite obtener datos significativos en lo que se refiere a la edad o a las patologías asociadas. En cambio, la cuestión de las valvulopatías aórticas se plantea en numerosísimos expedientes (560 exactamente). La mayoría de los solicitantes también sufre patologías asociadas, muchos presentan una insuficiencia aórtica. La proporción de aplazamientos es Octubre 2007 / Revisión de las enfermedades coronarias y valvulares muy fuerte (un 23,2% de las solicitudes). Este dato ha llamado nuestra atención. Sólo una parte mínima de estos aplazamientos menciona razones administrativas, es decir, no médicas. La insuficiencia aórtica figura en 333 expedientes entre los cuales se registran 15 rechazos y 61 aplazamientos. El «sex ratio» es característico, teniendo cuenta del sesgo observado en el seguro de vida. Se pueden aislar dos o incluso tres categorías de subpoblaciones. Hay menos personas de edad avanzada. Las patologías asociadas son frecuentes: dislipidemias e hipertensión arterial. Se observan también 15 casos de patologías congénitas asociadas. Los trastornos del ritmo asociados son muy escasos. Por otra parte, la estenosis aórtica figura en los expedientes de 67 solicitantes, que se distribuyen de manera bastante equivalente. Dominan las patologías asociadas de tipo degenerativo, la hipertensión arterial y la dislipidemia. Hay muy pocas patologías congénitas asociadas. Entre las enfermedades aórticas, la insuficiencia y la estenosis aórticas asociadas son raras en el total de solicitudes. Los rechazos son muy frecuentes y la sex ratio sigue siendo muy favorable a los hombres. Las patologías que asocian las afecciones mitrales y aórticas figuran en muy pocos expedientes (75 exactamente) de los cuales 30 dieron lugar a un aplazamiento por un problema de orden médico que explicaremos más adelante. La media de edad es de 48 años; la distribución de las poblaciones no es significativa. Mencionar las patologías asociadas tampoco tiene mucho sentido habida cuenta del número muy reducido de casos. Pacientes portadores de prótesis valvular Entre los expedientes que mencionan la implantación de prótesis valvulares, aparecen dos categorías de población según hayan recibido una prótesis orgánica o sintética. Focus 27 Eco-Doppler cardíaco: examen clave de las enfermedades valvulares De manera algo sorprendente, el grupo de prótesis orgánicas consta de 686 personas. Es el más importante en tamaño, aunque se implantan más prótesis mecánicas que orgánicas. En realidad, desde hace diez años las prótesis sintéticas se han impuesto en la práctica médica. En nuestro caso conciernen a 382 solicitantes y representan 201 prótesis mitrales y 181 prótesis aórticas. La edad mínima y la media de edad de los solicitantes son bastante bajas. También debido al mismo sesgo, el «sex ratio» sigue siendo muy favorable a los hombres. El histograma de distribución de la edades de la población no suscita ningún comentario particular. En cambio, las patologías asociadas son más frecuentes y graves que en el grupo de prótesis orgánicas. Se registran en particular: 21 personas que sufren de hipertensión arterial. 21 personas que presentan trastornos del ritmo. 18 personas que presentan una dislipidemia. 15 diabetes. Por consiguiente, el estado de salud de estos solicitantes es globalmente algo inferior al de las personas que han recibido una prótesis orgánica. Los aplazamientos se deben principalmente a una falta de información médica. ¿Qué datos faltan más en los expedientes de patologías valvulares? La ecografía cardíaca, sin lugar a dudas, que permite comprobar el buen funcionamiento de la prótesis y, de manera más general, seguir la función cardíaca. Fuera de esta causa de aplazamiento, el incremento de los datos disponibles debería permitir tratar más casos en el futuro. Una o dos veces al año, el portador de una prótesis valvular acude al cardiólogo para una consulta de seguimiento. En conclusión, la frecuencia de los aplazamientos puede reducirse. Si, de entrada, un perfil ecográfico figura en el expediente, se puede plantear una tarificación Doctor John EVANS. Médico asesor, SCOR Global Life La ecografía reviste una importancia capital, a veces ignorada, en la evaluación de una valvulopatía y las estrategias de tratamiento. El sonido es un fenómeno vibratorio. Por ejemplo, el mecanismo de producción del sonido de la voz es una vibración de las cuerdas vocales cuyo impulso se transmite a las moléculas del aire por ciclos de compresión y dilatación. Estos ciclos se pueden cuantificar según una frecuencia, medida en hercios (del nombre de un ilustre alemán); un hercio corresponde a un ciclo por segundo. En el campo de los ultrasonidos, la escala abarca millones de ciclos por segundo o megahercios. El límite de audibilidad humana se sitúa alrededor de 16 a 20 miles de ciclos por segundo o kilohercios. La ecografía El sonido de muy alta frecuencia puede ser dirigido hacia un objetivo, al igual que el haz luminoso de una linterna eléctrica. Esta propiedad es muy interesante. Este tipo de sonidos obedecen a las mismas leyes de reflexión y refracción, cuando dan contra un objeto de densidad diferente. Las ondas reflejadas por una interfaz física interesan especialmente al médico. Estos ecos permiten un análisis de la anatomía y del funcionamiento del corazón. Se coloca en el pecho del paciente un sensor transductor dotado de propiedades piezoeléctricas. El ecógrafo envía una señal eléctrica de corta duración a los terminales del sensor, que se pone a vibrar a alta frecuencia. Los ultrasonidos producidos son transmitidos a través del corazón y reflejados por cada interfaz de densidad física diferente. Los ultrasonidos reflejados, «los ecos», hacen vibrar el cristal de modo que crean una corriente eléctrica, transformada finalmente en imagen. Al igual que un sonar sondea los fondos marinos (en cuyo caso el transductor está situado en la quilla del barco), el médico sondea la topografía cardíaca. A partir de la velocidad de propagación de los ultrasonidos, midiendo el tiempo de ida y vuelta entre la emisión y la recepción, es posible calcular la distancia entre el emisor y el reflector. El operador envía un rayo sectorial a través del cuerpo: un corte anatómico del corazón aparece según la incidencia elegida. A partir del corte longitudinal, se pueden distinguir la aorta, la aurícula izquierda, la válvula mitral y el ventrículo izquierdo. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Es posible evaluar la integridad de los velos sigmoideos aórticos, su número, su finura y su movilidad. Lo mismo ocurre con la evaluación de la movilidad de la válvula mitral o la cuantificación de una dimensión del ventrículo izquierdo. En la misma imagen se puede discernir un posible derrame pericárdico. En este corte sectorial, llamado bidimensional o 2D, es posible seleccionar una línea de corte para analizarla. Se trata de una ecografía unidimensional (denominada TM - tiempo movimiento). En este modo, la resolución es mejor y el cálculo de las dimensiones de las cavidades resulta más fácil. La ecografía ofrece pues numerosos datos en los modos TM y 2D: Dimensión de las cavidades en diástole y sístole Índices de función contráctil del ventrículo izquierdo Espesor de las paredes Morfología de las válvulas. Se puede cuantificar la contracción de las paredes del corazón mediante un corte del ventrículo izquierdo. En modo TM, se realizan mediciones en diástole y sístole con objeto de deducir el valor contráctil, un factor determinante en la selección del tratamiento. Efecto Doppler Las ondas sonoras reflejadas desde una interfaz en movimiento hacia una fuente de emisión son comprimidas, lo que aumenta la frecuencia percibida. Si las reflexiones proceden de una interfaz que se aleja de la fuente, las ondas sonoras son más escasas y la frecuencia registrada es menos alta. Es el efecto Doppler, del nombre de un científico austriaco, astromatemático del siglo XIX. Lo utiliza la gendarmería francesa para controlar la velocidad de los vehículos en las carreteras. Del mismo modo, se utiliza en medicina, no para detectar los coches, sino los glóbulos sanguíneos: los que se alejan del sensor inducen frecuencias más bajas; los que se acercan inducen frecuencias más altas. Doppler entendió que la diferencia entre las frecuencias percibidas y emitidas estaba relacionada con la velocidad de desplazamiento del reflector. En la fórmula física que le debemos, la velocidad del flujo sanguíneo examinado Focus está relacionada con la diferencia entre la frecuencia de la onda sonora recibida por el aparato y la frecuencia de emisión del sonido, es decir, la frecuencia Doppler (Fd). La única otra variable (coseno theta) es el ángulo de incidencia entre el eje de desplazamiento de los glóbulos y el eje de examen. El médico puede prescindir de esta variable procurando que el ángulo de incidencia sea de 0° (en el eje de desplazamiento de los glóbulos) o 180° (coseno theta = 1 y por lo tanto, no tiene importancia en la fórmula). Conociendo las velocidades sanguíneas y midiendo superficies de sección en el lugar de la muestra mediante la ecografía bidimensional, se accede físicamente a los flujos sanguíneos, los cuales se deducen de algunas reglas de la hidráulica, leyes que rigen los fluidos. Según la ecuación de continuidad, el flujo debe ser constante en dos lugares distintos. Por lo tanto, si se conocen la superficie y la velocidad sanguínea en un lugar y se mide la velocidad sanguínea en el lugar que se desea explorar, se puede deducir la superficie desconocida: esta aplicación es diaria en la evaluación de las estenosis valvulares, que resulta a veces difícil. Cuanto más cerrada sea la estenosis, más limitada será la superficie. Ésta es una aplicación del efecto Doppler en el análisis de los efectos de las valvulopatías. Otra aplicación se debe a Bernoulli, quien estudió la relación entre la diferencia de presión a cada extremo de un estrechamiento, y la velocidad de un fluido. Esta relación corresponde al cálculo de los gradientes. La velocidad disminuye a la entrada del estrechamiento y aumenta a la salida. A la entrada, la energía cinética del fluido se convierte en energía potencial. La presión por arriba es más alta. Bernoulli relacionó la diferencia de presión a cada extremo de una estenosis con el cuadrado de la velocidad. Midiendo la velocidad máxima de la sangre a la salida de una estenosis, se puede cuantificar el gradiente de presión a cada extremo del estrechamiento. Cuanto más cerrada sea la estenosis, más altos serán la velocidad y el gradiente. Gracias a estas técnicas que recurren al efecto Doppler, el médico dispone de datos muy valiosos sobre las velocidades de los flujos sanguíneos intracardíacos. En caso de estenosis, los valores medidos son anormales. Por consiguiente, la ecografía permite: Facilitar datos sobre la morfología y la anatomía cardíacas. Estimar la superficie valvular (planimetría). Apreciar las dimensiones de las cavidades y las paredes. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares 29 Hemos proyectado una imagen de estenosis mitral. La apertura de las valvas mitrales posterior y anterior es limitada. Se observa también una dilatación de la aurícula izquierda. El efecto Doppler indica el valor de los gradientes de presión y permite calcular las superficies funcionales. Por regla general, cuanto más alto sea el gradiente, más severa será la estenosis. En el caso de las valvulopatías mitrales, la medición de las presiones sanguíneas pulmonares ayuda a evaluar los efectos del gradiente de presión. Una estenosis mitral tiene consecuencias directas en el retorno de la sangre de los pulmones al corazón. Este ejemplo de estenosis mitral evidenciada por el Doppler se caracteriza por una velocidad sanguínea de dos metros por segundo (normalmente, es inferior a un metro por segundo); las velocidades siguen siendo altas durante toda la diástole. Se puede medir el gradiente de presión medio por planimetría de la superficie bajo la curva de velocidad. En nuestro ejemplo, es de doce milímetros de mercurio. En caso de regurgitación valvular, el médico busca la misma información anatómica en TM y 2D. Se interesa más en el ventrículo y la aurícula izquierdos, que sufren la sobrecarga de volumen de las regurgitaciones mitrales y aórticas. Se suele proceder a una evaluación Doppler semicuantitativa. Los cardiólogos clasifican las regurgitaciones en varios grados según su importancia. No existe ningún parámetro suficiente de por sí para evaluar una regurgitación valvular con Doppler, equivalente al gradiente de presión y la superficie valvular obtenidos en la evaluación de las estenosis. Expondré muy brevemente el desarrollo de la ecografía transesofágica, que permite examinar, mediante un fibroscopio equipado con sensor, las estructuras cardíacas por vía posterior. La utilidad de este examen es patente para el estudio de las válvulas a través de la aurícula izquierda, especialmente para los portadores de prótesis mitral. La utilidad futura del ecodoppler cardíaco en la práctica médica es evidente, pues este examen es rápido, no invasivo, reproducible y relativamente económico. No obstante presenta inconvenientes: el procedimiento depende de la experiencia del operador que, sumada a la ecogenicidad del paciente y la calidad del material, condiciona la calidad del resultado. Si el material es vetusto, no se podrán esperar datos importantes. Epidemiología, fisiopatología y factores de morbilidad y mortalidad de las valvulopatías cardíacas Profesor Pierre-Louis MICHEL. Servicio de cardiología - Hospital Tenon (Paris) Epidemiología de las valvulopatías Desde el punto de vista anatómico, el corazón es un conjunto de cavidades. Algunos vasos entran y salen, mientras otros, las arterias coronarias, vascularizan el músculo cardíaco. Las diferentes cavidades son separadas por válvulas. El corazón es una bomba: los momentos en que las cavidades se llenan alternan con los momentos en que se vacían. Para cada una de las válvulas, los períodos de apertura alternan con los períodos de cierre. Se distinguen las valvulopatías estenóticas (estenosis aórticas y mitrales) y las valvulopatías regurgitantes. Estas últimas se caracterizan por un cierre incompleto cuyas consecuencias pueden ser mínimas o muy graves. La válvula mitral separa la aurícula y el ventrículo izquierdo; la válvula aórtica separa el ventrículo izquierdo y la aorta. La epidemiología de las valvulopatías cardíacas se ha modificado. Existen aún pocos estudios con carácter epidemiológico en este ámbito. Cabe mencionar uno de ellos, publicado por la sociedad europea de cardiología (ESC) en el segundo trimestre de 2001. Abarca 5 001 pacientes, repartidos en 25 países de Europa y 92 centros cardiológicos. La distribución es bastante homogénea entre la Europa del Sur y la Europa del Norte. Los pacientes hospitalizados o examinados en el período considerado se incluyen en la encuesta. Entre los pacientes operados del corazón una cuarta parte ha sido seguida en un servicio de cardiología. Un poco menos de las tres cuartas partes presentan valvulopatías nativas. La media de edad es alta. Pero fundamentalmente la media de edad de las personas afectadas por una valvulopatía no deja de aumentar debido a un cambio en las etiologías. En este grupo caracterizado por la presencia de una valvulopatía nativa, se registran sólo un poco más de patologías aórticas que mitrales. La valvulopatía más frecuente es de lejos la estenosis aórtica (una tercera parte de los pacientes). Esto no corresponde con los datos resultantes de la compilación de los expedientes de solicitud de seguros, que se acaba de presentar. El segundo puesto lo ocupa la insuficiencia mitral. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Entre la cuarta parte de los pacientes incluidos en el estudio que ya han sido operados, una quinta parte aproximadamente ha sido sometida a una cirugía conservadora. Ninguna prótesis es mejor que la válvula con la que nos ha dotado la naturaleza. Eso explica que los demás pacientes hayan sido sometidos a una operación de reemplazo valvular. Anteriormente las valvulopatías más frecuentes eran de naturaleza reumática y se debían a una angina estreptocócica ocurrida en la infancia. Esta enfermedad puede causar un reumatismo articular agudo y un deterioro de las válvulas cardíacas. Su gravedad resulta de las lesiones del endocardio y de las válvulas. Un episodio de angina durante la juventud que haya regresado totalmente tras el tratamiento puede provocar secuelas valvulares significativas. El horizonte de aparición es de 10, 20 o incluso 30 años después de la angina inicial. El reumatismo articular agudo casi ha desaparecido en los países desarrollados, pero sigue siendo una plaga en numerosos países en vías de desarrollo. Si bien la proporción de cardiopatías reumáticas se ha reducido considerablemente en Europa –sólo afectan a algunos pacientes de edad muy avanzada, ya operados en la mayoría de los casos–, la incidencia de las valvulopatías degenerativas no deja de aumentar. Los pacientes, cada vez más mayores, tienen tiempo de desarrollar estas patologías con mecanismo degenerativo. ENFERMEDAD CAUSAL en % EA IA EM IM Degenerativa 81,9 50,3 12,5 61,3 Reumática 11,2 15,2 85,4 14,2 3,5 Infecciosa 0,8 7,5 0,6 Inflamatoria 0,1 4,1 0 0,8 Congénita 5,4 15,2 0,6 4,8 Isquémica Otra EA = Estenosis aórtica IA = Insuficiencia aórtica EM = Estenosis mitral IM = Insuficiencia mitral 0 0 0 7,3 0,6 7,7 0,9 8,1 Euro Heart Survey 2001 Focus La estenosis mitral sigue siendo casi siempre de origen reumático. En lo que respecta a la insuficiencia mitral, segunda valvulopatía más frecuente, la etiología predominante es de naturaleza degenerativa. Estos pacientes tienen un promedio de 64 años. Los factores de riesgo cardiovascular corresponden al tabaco en una tercera parte de los casos y a una dislipidemia en la misma proporción. Por otro lado, las personas hipertensas representan casi la mitad de la población. Un antecedente familiar de enfermedad coronaria precoz se observa en una cuarta parte de los pacientes, éste constituye uno de los factores más fuertes de ocurrencia del riesgo vascular. La comorbilidad es relativamente frecuente en estas poblaciones, puesto que se registra un 13% de infartos de miocardio, un 7% de enfermedades neurodegenerativas, un 15% de bronquitis crónicas, etc. A mayor edad de los pacientes, mayor tendencia tendrán a convertirse en polipatológicos. Por tanto, es imperativo tener en cuenta la comorbilidad. En las afectaciones de las válvulas aórticas, el reemplazo valvular es casi siempre inevitable, salvo casos particulares. Aunque muchas veces es necesario reemplazar la válvula, en algunos casos sin embargo la cirugía conservadora sigue siendo posible. En cambio, en las afectaciones de las válvulas mitrales, un gesto conservador suele ser posible. En el tratamiento de la estenosis mitral, una tercera parte de los pacientes han sido tratados por dilatación (antigua comisurotomía quirúrgica). En la insuficiencia mitral, la plastia sigue siendo en muchos casos una opción interesante (promedio europeo del 46%). En buenas manos quirúrgicas, el porcentaje aumenta y la válvula de origen puede conservarse. El pronóstico de evolución difiere totalmente según se conserve o no la válvula de origen y el cirujano tenga o no que reemplazarla. Desde el punto de vista de la mortalidad operatoria, la cirugía cardíaca está en constante progreso. Al principio, en los años sesenta, se registraba un 30 a 40% Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Fisiopatología de las valvulopatías Estenosis aórtica En el caso de las estenosis, a diferencia de las regurgitaciones, el médico se enfrenta a un proceso evolutivo en el que la válvula se espesa y se calcifica progresivamente obstaculizando la eyección del contenido del ventrículo izquierdo. Si no se hace nada, la eyección será cada vez más difícil. Al principio, se nota una ligera esclerosis de la válvula aórtica. Luego se observa un soplo cardíaco sin síntoma asociado. Durante mucho tiempo el paciente no se queja de nada, hasta que la enfermedad valvular tiene repercusiones evidentes en su vida. Existe un período de latencia incluso cuando existe un obstáculo significativo. Los primeros síntomas se objetivan durante un esfuerzo. El paciente percibe por primera vez el fenómeno de origen valvular. Sufre un dolor de tipo angina de pecho, aunque la patología valvular no está necesariamente asociada a una enfermedad coronaria. Entra en una nueva etapa de la enfermedad con la pérdida del conocimiento o el síncope; el proceso conduce finalmente a la insuficiencia cardíaca. Cuando se observan estos signos, el pronóstico vital está en juego. La supervivencia es de tres a cinco años en caso de angina, un poco menos en caso de síncope. Se reduce a algunos meses en el estadio de la insuficiencia cardíaca. Por consiguiente, para determinar la gravedad de una estenosis aórtica, hay que preguntarse en qué medida es sintomática. La presencia de un síntoma justifica la operación cuando ninguna comorbilidad prohíbe el gesto quirúrgico. Según un estudio realizado con personas mayores de 65 años, una cuarta parte de la población presenta una esclerosis aórtica poco significativa; sólo un 2% desarrolla una estenosis, y un 4% después de los 85 años. PROGRESIÓN DE LA ESTENOSIS AÓRTICA Num. Seguimiento Grad / año Faggiano Roger Brener Otto (puntos) (m) (mmHg) 45 112 394 123 18 25 37 30 16 11 12 7 $ de fallecimientos después de una intervención de reemplazo valvular. Actualmente esta cifra se ha reducido al 2 ó 3% para los reemplazos aórticos y al 5 ó 6% para los reemplazos mitrales. Además, los pacientes son en promedio mucho más mayores. Evidentemente la comorbilidad puede aumentar los riesgos de fallecimiento relacionados con la operación. Cada valvulopatía plantea un problema quirúrgico y médico específico. $ De los datos de Europe Heart Survey se desprende que la estenosis aórtica, la valvulopatía más frecuente, tiene ahora una causa esencialmente degenerativa, mucho más común que las etiologías reumáticas. La no consideración de la bicúspide congénita conlleva una infravaloración muy ligera. Las regurgitaciones aórticas tienen en su gran mayoría una causa degenerativa (o distrófica). 31 Superficie (cm2) 0,10 0,10 0,14 0,12 Por lo tanto, las estenosis aórticas no aparecen súbitamente; mediante el ecodoppler cardíaco, un examen poco costoso, es posible seguir su evolución. En promedio, la superficie de la válvula aórtica disminuye anualmente en 0,1 cm2. Las dimensiones del orificio aórtico deben calcularse en función de la superficie corporal media. De modo general, esta superficie representa 3 cm2 en su estado normal. Si se reduce a la mitad, no se registrará ningún síntoma particular. Este estado es el de la esclerosis aórtica. Se caracteriza por un flujo cardíaco normal en reposo, sin generar ningún gradiente. Luego entramos en la zona de la estenosis cerrada cuyo límite alto es de 0,5 cm2 por m2 de superficie corporal. Un orificio aórtico que oscila entre 1,2 y 1,3 cm2 se sitúa en esta zona. Cuando la estenosis aórtica se intensifica, el riesgo de aparición de síntomas aumenta. Según las estadísticas y la distribución gaussiana de la población afectada, el médico puede anticipar la evolución de la patología valvular. Ustedes pueden ver una serie clásica y reciente, descriptiva de la historia natural de la estenosis aórtica, que durante mucho tiempo permanece asintomática. El principal riesgo al que se enfrenta el médico que desea controlar a un paciente es el de la muerte súbita. La preocupación fundamental radica en el hecho de que el primero y último síntoma de la estenosis aórtica puede ser la muerte súbita. Un estudio austríaco ha incluido pacientes que presentaban una estenosis estrecha (velocidad de flujo superior a 5 metros por segundo). Respecto a la esperanza de vida de una población testigo, la existencia de una estenosis aórtica cerrada que requiere un gesto quirúrgico induce una sobremortalidad, demás de conllevar los riesgos relacionados con la operación y la implantación de la prótesis. La operación expone a varios incidentes; los factores que determinan Octubre 2007 / Revisión de las enfermedades coronarias y valvulares la evolución son el grado de calcificación y la velocidad de progresión. Un paciente con una estenosis aórtica que progresa rápidamente tiene un pronóstico mucho menos favorable. Insuficiencia aórtica En el caso de las insuficiencias aórticas, el parámetro fundamental es el volumen regurgitado. Mientras que una estenosis aórtica evoluciona con el tiempo, una regurgitación aórtica es, de entrada, moderada o importante. Si el solicitante declara la existencia de una profilaxis de la endocarditis y no hay motivos por poner en duda esta información, la regurgitación puede tolerarse durante varias decenas de años. No existe razones para aplicar una sobreprima considerable a estas patologías. La regurgitación moderada de la válvula aórtica probablemente seguirá siendo moderada y no evolutiva. En el caso de pacientes que presenten un volumen de regurgitación importante, la apreciación del riesgo adicional requerirá una determinación del volumen. Si es importante (etiología clásica), el pronóstico no será bueno. A un horizonte de 10 años, estos pacientes sufren numerosas complicaciones (aneurismas, insuficiencia cardíaca en casi la mitad de los casos). Cerca de las dos terceras partes son operados y, unos diez años después de la intervención, reaparecen síntomas cardíacos en más del 80% de los casos. Esto sólo es válido para las regurgitaciones importantes y no moderadas. La historia natural de la insuficiencia aórtica crónica importante se caracteriza al principio por el carácter asintomático de la enfermedad, con mantenimiento de la función sistólica. Sólo un 4% de las personas en la primera fase de la patología valvular presentan algún síntoma o una disfunción del ventrículo izquierdo. La muerte súbita es muy rara. No hay motivos para operar a estos pacientes, que presentan un riesgo mínimo de muerte súbita. En cambio, una disfunción del ventrículo izquierdo es una indicación operatoria. Si no se interviene, es probable que pronto aparezcan síntomas. La ecografía permite detectar estas anomalías ventriculares. El factor pronóstico esencial de la insuficiencia aórtica es la contractilidad cardíaca. Focus 33 En términos de frecuencia, la insuficiencia mitral es la segunda patología valvular. Al igual que la regurgitación aórtica, este tipo de insuficiencia presenta una gravedad intrínsecamente relacionada con el volumen. Si la regurgitación es reducida, el paciente puede vivir varias decenas de años, por lo que no hay sobreriesgo adicional. La expresión de «prolapso valvular mitral» es un cajón de sastre que incluye situaciones clínicas muy distintas. Se plantearon diagnósticos de «prolapso» a pacientes que ni siquiera tenían soplo cardíaco. Se les hizo por tanto un diagnóstico de valvulopatía cuando en realidad no presentaban ninguna patología grave. El grado de regurgitación y el mecanismo causal determinan casi toda la evolución de la insuficiencia mitral. Si la regurgitación es importante, existe un argumento de peso a favor de la operación; es preferible intervenir pronto. Además la válvula puede repararse. Después de este tipo de intervención, el paciente recupera una esperanza de vida normal, de modo que se puede hablar con razón de «curación» de la insuficiencia mitral. En una muestra de 216 pacientes seguidos, que presentan una regurgitación importante, el grupo de los que no han sido operados tiene una esperanza de vida media menor. Se han registrado incluso casos de muerte súbita. HISTORIA NATURALDE LA INSUFICIENCIA MITRAL SEVERA Incidencia (%) 100 Cirurgia o fallecimiento (188) 90 ± 3% 80 82 ± 4% 60 63 ± 8% 40 IC (55) Cirurgia (143) 30 ± 12% FA (13) 20 0 0 1 2 3 4 5 6 7 8 9 10 Años después del diagnostico Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Clase funcional (el hecho de ser sintomático) Fracción de eyección ventricular izquierda Presencia de una fibrilación auricular Incluso en los pacientes que no presentan ninguno de estos tres factores y mantienen la función sistólica (personas asintomáticas por antonomasia), la frecuencia de muertes súbitas se acerca al 1%. Este último dato debe integrarse en la atención prestada a estos pacientes. En particular, una cirugía conservadora precoz de la insuficiencia mitral mejora considerablemente la esperanza de vida. La categoría de los enfermos sintomáticos presenta una esperanza de vida inferior a la de del grupo testigo. En cambio, hay que considerar a los enfermos operados precozmente como personas normales. Su esperanza de vida es similar a la de una población testigo. Por tanto, según estos datos es preferible operar las regurgitaciones mitrales lo antes posible. Además, no hay ningún motivo para aplicar sobreprimas a pacientes que precisamente, al haber sido operados del corazón, han recuperado una esperanza de vida normal. No estoy seguro de que una cicatriz de esternotomía no se pague caro a la hora de tomar un seguro. También entra en cuenta la etiología: si la insuficiencia mitral es de origen isquémico, relacionado con una enfermedad coronaria, será relativamente más grave. La etiología reumática también arroja resultados inferiores. Desde el punto de vista estadístico, las insuficiencias mitrales distróficas, las más frecuentes, se tratan por cirugía plástica en más del 85% de los casos. Estenosis mitral Esta valvulopatía es casi siempre de origen reumático. Sólo pueden mencionarse raras etiologías degenerativas a título anecdótico. El reumatismo articular agudo suele remontarse a una edad de entre 5 y 10 años. Un período de latencia prolongada transcurre antes de la aparición de signos evocadores. Esta causa de alteración de las válvulas cardíacas permanece en estado endémico en algunos países en vías de desarrollo (Sudeste asiático, África, Sudamérica…). En estos países el reumatismo articular agudo es una causa importante de muerte en las mujeres jóvenes. Globalmente, la supervivencia depende de los síntomas observados. En los pacientes sintomáticos, los datos de esperanza de vida son bastante catastróficos. Esta enfermedad también es evolutiva, pues la estenosis se agrava progresivamente. El pronóstico de una patología sintomática, sin tratamiento, es malo. La estenosis mitral presenta una particularidad: la evolución tiende hacia la estasis sanguínea, luego la dilatación de la aurícula izquierda y, por último, la formación de coágulos. Existe una complicación grave, los efectos de los accidentes tromboembólicos, que pueden causar hemiplejías, siempre dramáticas, especialmente en una mujer de 25 años. Estos accidentes tienen un origen cardíaco, por lo que el síntoma inicial es un accidente vascular cerebral en un 25% de los casos. Este riesgo justifica un gesto terapéutico en los pacientes con estenosis cerradas aún asintomáticas. La administración de un tratamiento anticoagulante a estos pacientes los expone a complicaciones hemorrágicas. Reduce efectivamente la tasa de accidentes tromboembólicos, pero no los suprime. El tratamiento moderno es percutáneo: consiste en introducir por una vena un dispositivo de dilatación de la válvula. Para ello, se realiza una punción del septo auriculoventricular, pasando el catéter por una vía que sólo existió durante la vida fetal. Se coloca un balón, que el operador luego podrá inflar, en el lugar adecuado: a través de la válvula mitral. Una vez amarrado e inflado el balón en la válvula mitral, se consigue abrir las comisuras, con lo que se ensancha el orificio mitral. El gradiente de presión que existía entre la aurícula y el ventrículo disminuye: el ecodoppler permite objetivar la apertura comisural. Los enfermos en los que se practica esta dilatación en un estadio precoz registran excelentes resultados. Este gesto quirúrgico es eficaz y transforma, en cierta medida, el pronóstico. En conclusión, se observa un importante retroceso del reumatismo articular agudo en las etiologías de las cardiopatías valvulares en Europa. En cambio, el fenómeno es exactamente inverso en las etiologías degenerativas. Las valvulopatías más frecuentes son las estenosis aórticas (esencialmente en los pacientes muy mayores, que no suelen solicitar seguros) y la insuficiencia mitral. Esta última cardiopatía concierne probablemente más a las aseguradoras. Las estenosis valvulares son evolutivas, una DILATACIÓN PERCUTÁNEA DE UNA ESTENOSIS MITRAL Aspecto ecográfico de la estenosis antes y después de la dilatación Después Insuficiencia mitral A partir de otra serie de pacientes seguidos en el transcurso de los años ochenta, se pueden deducir otros datos. Si la etiología de la insuficiencia mitral es una ruptura de las cuerdas de la válvula, el pronóstico espontáneo no es bueno. Este tipo de paciente, sobre todo en ritmo sinusal, tiende a desarrollar una fibrilación auricular. Las consecuencias terapéuticas y pronósticas son bien conocidas. Cabe destacar el riesgo de muerte súbita y algunos factores que la favorecen: Antes La supervivencia de los pacientes operados, incluso sin complicaciones operatorias, es inferior a la de una población apareada de la misma edad, no operada. Es idéntica en los primeros años y se deteriora más tarde. Si además el paciente presenta una alteración de la función sistólica izquierda, la supervivencia a largo plazo es cada año menor respecto a la del grupo testigo. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Inflación del balón a través de la estenosis Focus estenosis moderada se irá cerrando. En cambio, las regurgitaciones valvulares presentan pocas probabilidades de evolución; una regurgitación reducida no suele aumentar. En la respuesta médica a los problemas planteados por las regurgitaciones valvulares, la cardiología ha realizado progresos considerables. La detección y los tratamientos recurren ampliamente al ecodoppler cardíaco. La cirugía no ha dejado de avanzar, reduciendo en diez veces la mortalidad inicial relacionada con la operación de reemplazo valvular. Evidentemente, los riesgos no son nulos –como aseguradores, ustedes lo saben mejor que nadie–, pero no son nada comparables a los riesgos de una cirugía valvular en los inicios de la práctica de estas intervenciones. Esto debería tenerse en cuenta en las primas y las tarificaciones. John EVANS Por mi parte, noto que los pacientes a veces restan importancia a sus síntomas. El ecodoppler es indispensable como complemento para proporcionar datos objetivos. Si el paciente es sintomático, la intervención quirúrgica debe realizarse sin lugar a dudas. Pero si es asintomático, ¿existen medios para tomar una decisión, cuando aún no se determinado con precisión la gravedad de los síntomas? Pierre-Louis MICHEL En este caso conviene apreciar el modo de vida. Una persona mayor que permanece en casa no se puede comparar con una persona deportista. Además de esta evaluación de la actividad del paciente, se debe realizar, en caso de duda, una prueba de esfuerzo para cuantificar un poco los efectos de la patología vascular del interesado. Algunas personas están acostumbrados al esfuerzo físico, especialmente las que practican deportes de resistencia (maratón, ciclismo). Sus capacidades son a veces considerables. Los síntomas de las valvulopatías sólo aparecen cuando el nivel de gasto de energía es alto, mucho más alto que en las personas sin actividad física notable. Si su actividad física diaria es nula, el paciente se quedará sin aliento en una bicicleta haciendo un esfuerzo del orden de 60 vatios. Esto no significa que su corazón esté deteriorado; apunta más bien a una desadaptación cardiovascular al esfuerzo. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares 35 Las solicitaciones al corazón dependen de la actividad física básica y del entrenamiento. Esto puede constituir un argumento a favor del mantenimiento de una actividad física regular. Tras una intervención por vía percutánea en una valvulopatía mitral, ¿la válvula sigue evolucionando con el tiempo, como en caso de estenosis mitral? De la sala Pierre-Louis MICHEL En caso de insuficiencia aórtica, conviene determinar el volumen de regurgitación. ¿En qué criterios se basa la investigación por ecodoppler? Ocurre lo que ocurría antes, cuando se practicaba una comisurotomía quirúrgica. Una patología reumática afectó a la válvula hace 15 ó 20 años. No podemos plantearnos que esta válvula salga indemne. La estenosis evoluciona más o menos rápido según la edad. Está claro que el paciente no recuperará una válvula nueva. En todo caso, una estenosis mitral, patología poco frecuente, no tendrá buen pronóstico. Una vez operada, la válvula seguirá sometida a factores de cambio y alteración. En el ámbito de las cardiopatías reumáticas, el médico se enfrenta con frecuencia a estenosis mitrales ya operadas, a recidivas, etc. La válvula está alterada por un proceso reumático evolutivo, no puede considerarse como nueva. Simplemente se gana tiempo. Estas enfermedades cardíacas requieren una atención a largo plazo. Piensen en el estado del arte en materia de tratamiento de la insuficiencia cardíaca. Se acaban de registrar progresos considerables con las endoprótesis. Sin embargo, no significan la curación, debido al potencial de desarrollo del ateroma en la Pierre-Louis MICHEL Los ecografistas me parecen muy simpáticos. Cada año, alguno piensa haber resuelto la cuestión y determinado un nuevo índice definitivo, que supera a los demás. Año tras año, un «mejor» índice sucede a otro. En consecuencia, no faltan los índices de cálculo en la literatura. Ninguno es perfecto ni está exento de aproximaciones. Por tanto, un buen ecografista debe ser ante todo un buen cardiólogo. Los parámetros de análisis son múltiples y sólo una síntesis fundada conduce a un diagnóstico fiable. A veces comparo a los ecografistas a un Santo Tomás pervertido. Santo Tomás decía: «Ver para creer». El ecografista ve, luego cree. A veces algunas imágenes difíciles de interpretar pueden inducirle en error. Este examen depende mucho, por tanto, de la habilidad del operador que lo realiza. John EVANS De la sala ¿Cuáles son las características de una buena cirugía de la insuficiencia mitral? Pierre-Louis MICHEL Tras la intervención, no se debe registrar ninguna regurgitación residual ni ninguna estenosis residual, ni siquiera mínimas. Un paciente con regurgitación mitral operado por un buen cirujano, como Christophe Acar, sale del hospital sin regurgitación ni estenosis valvulares residuales en un 95% de los casos. Hoy en día, a treinta años de distancia, podemos apreciar los resultados de la cirugía desde las primeras operaciones del Profesor Carpentier. Son fiables y se mantienen para todas las patologías valvulares. El éxito de este tipo de intervenciones se evalúa a largo plazo, por lo que podemos hablar legítimamente de curación de la patología valvular. Es cierto que el paciente lleva una cicatriz de esternotomía, pero su corazón debe considerarse como normal. Este punto debe tenerse en cuenta. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares coronaria. Por tanto, la mayor probabilidad de presentar una patología coronaria está relacionada con el hecho de ser ya coronario. De la sala Soy reumatólogo y me gustaría saber si la espondiloartritis anquilosante agrava el pronóstico de la insuficiencia aórtica. Pierre-Louis MICHEL La espondiloartritis anquilosante no deja de ser una etiología poco frecuente. En realidad, todo depende de la naturaleza de la regurgitación y de los problemas asociados. Los trastornos de la conducción pueden requerir la implantación de un aparato. Una persona puede necesitar una prótesis valvular y un marcapasos. De la sala ¿Cuál debe ser la frecuencia de seguimiento de una persona con valvulopatía? Pierre-Louis MICHEL Si la afectación es mínima, un balance anual o bianual será suficiente. Si es muy significativa, convendrá estrechar la vigilancia (cada año y luego cada semestre). Focus 37 Aportes de las nuevas técnicas quirúrgicas a la morbilidad y la mortalidad inmediatas y a largo plazo Profesor Christophe ACAR. Servicio de cirugía cardiotorácica, Instituto de cardiología Pitié-Salpêtrière La cirugía cardíaca es una especialidad joven, que nació en los años sesenta. Se desarrolló recientemente con respecto a otras especialidades. En Francia se realizan anualmente 38 000 intervenciones de cirugía a corazón abierto, lo que corresponde a la media de los países industrializados. Sólo en Ile-de-France, se llevan a cabo 11 000 operaciones, lo que representa casi una tercera parte del total. Desde hace unos diez años, el número de gestos quirúrgicos tiende a estabilizarse alrededor de la cifra antes mencionada. Anualmente se practican 291 000 intervenciones quirúrgicas, lo que sitúa el país en la media europea. ¿Qué patologías se observan en nuestros servicios de cirugía cardíaca? Aproximadamente una mitad corresponde a intervenciones de cirugía coronaria y la otra a intervenciones de cirugía valvular. Cierto número de pacientes son sometidos a una doble cirugía, a la vez en las coronarias y las válvulas. El cirujano tiene que intervenir a veces en patologías congénitas. Los injertos cardíacos sólo representan un aspecto marginal de la cirugía: sólo se realizan 136 anualmente en la región parisina. Existen dos categorías de prótesis para reemplazar las válvulas : válvulas mecánicas y válvulas biológicas. Las válvulas mecánicas tienen la considerable ventaja de la durabilidad: son fáciles de insertar, pues su fabricación industrial no ha dejado de progresar. Las válvulas de origen natural no requieren ningún mantenimiento particular, al contrario de las válvulas mecánicas. Poseen excelentes características de seguridad, pues son perfectamente compatibles con la sangre y no ocasionan la formación de coágulos. No presentan los diferentes defectos resultantes de la producción industrial. ¿Qué prótesis valvulares se implantan en Francia? Según una encuesta realizada en la industria, se registran un 38% de prótesis mecánicas y un 39% de bioprótesis. De las 38 000 intervenciones practicadas en Francia, 17 000 son valvulares. Globalmente, una mitad de las válvulas implantadas son mecánicas y la otra mitad son prótesis de origen biológico. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Además cabe mencionar la reparación quirúrgica de las válvulas mitrales. Para evaluar estadísticamente la importancia de esta reconstrucción, se considerará que la plastia representa un 21% de las operaciones valvulares. Nos basamos para ello en la cantidad de anillos protéticos producidos por la industria. Sólo una ínfima minoría de los pacientes reciben un homoinjerto valvular (un 2%). Válvulas mecánicas ¿Cuáles son las diferentes categorías de válvulas artificiales? La mecánica de la válvula ha evolucionado considerablemente, aunque el principio de una válvula entre dos cavidades es muy sencillo. La cantidad de modelos disponibles no ha dejado de aumentar. Aquí pueden ver una válvula de bola con excelentes prestaciones. Este modelo es muy sólido. No presenta casi ningún riesgo de desgaste o alteración estructural. Es ligeramente obstructivo, pues el flujo sanguíneo debe rodear el obstáculo que representa la bola. Veamos ahora las prótesis de disco: aquí tenéis un disco oscilante, fabricado en carbono pirolítico. Sujetado con bisagra, el dispositivo se abre prácticamente a 90°. Estas válvulas siguen siendo un poco obstructivas y voluminosas pues la apertura del disco requiere bastante espacio. Por ello, los ingenieros han elaborado la válvula moderna: la prótesis bivalva. Ustedes pueden observar aquí un disco separado en dos, fijado a una armazón por una bisagra. El dispositivo entero también es de carbono pirolítico. El principal inconveniente de las prótesis mecánicas es su compatibilidad imperfecta con la sangre. Se corre el riesgo de tener que tratar al paciente con anticoagulantes de por vida. El tratamiento se ajusta seleccionando un INR comprendido entre 2 y 3 para las prótesis aórticas. Se refuerza seleccionando un INR comprendido entre 3 y 5 para las prótesis mitrales, valores recomendados para esta clase terapéutica delicada. Válvulas biológicas Las válvulas orgánicas proceden de tejidos animales fijados con glutaraldehído, lo que induce una excelente tolerancia de los mismos, una vez tratados. No se observa casi ninguna reacción de rechazo. El único inconveniente de las prótesis orgánicas es el desgaste y el deterioro progresivos, que requieren a largo plazo una reintervención en la válvula sustituida. Se distinguen esencialmente dos tipos de bioprótesis: Las prótesis porcinas (a base de válvulas aórticas de cerdo), insertadas en un anillo para favorecer su implantación Las otras prótesis (a base de pericardio de ternera), montadas industrialmente en un soporte de implantación. Comparación de inconvenientes de los dos tipos de prótesis En definitiva, la complicación esencial de las válvulas mecánicas es el riesgo de formación de un coágulo o trombo. Una trombosis extensiva, en la que la válvula se encuentra totalmente bloqueada, impide el buen funcionamiento de la prótesis y obstaculiza el movimiento de las valvas. El cuadro clínico, de estenosis aguda, justifica una reintervención. A veces la trombosis es más discreta, en forma de pequeños coágulos. Si están situados en un lugar inadecuado, pueden bloquear la apertura de las dos valvas. Este fenómeno es terrible por sus consecuencias hemodinámicas muy deletéreas. Impide el restablecimiento de un flujo sanguíneo normal. En raras ocasiones pueden aparecer con el tiempo encapsulaciones fibrosas y la cicatriz puede obstaculizar la acción de la prótesis. La alteración estructural también es poco frecuente. Ustedes pueden ver aquí una fractura de la bola de la prótesis sintética. Las prótesis biológicas exponen a reintervenciones debido a su desgaste con el tiempo, aunque no presentan el riesgo de formación de coágulos. Se pueden observar desgarros y calcificaciones de la válvula que obstaculizan la apertura de la prótesis y obligan a una nueva operación en la válvula. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Desde el punto de vista estadístico puede ser interesante comparar los dos tipos de prótesis con el uso. Me he basado en grandes series para obtener un consenso. La media de edad de implantación es de 62 años para las prótesis mecánicas y de 75 años para las prótesis biológicas. La primera complicación es la trombosis, que origina embolias, para las dos categorías de dispositivos implantables. En esta serie estadística muy amplia, el riesgo de trombosis es idéntico (un 22% de pacientes afectados) para las prótesis mecánicas y biológicas. Este resultado es bastante sorprendente. Cabe temer las hemiplejías y las discapacidades importantes que esta complicación puede ocasionar. Sin embargo, estas cifras no se pueden comparar totalmente debido a la diferencia de media de edad que acabo de mencionar. La complicación tromboembólica evidenciada en el grupo de las prótesis biológicas no estaba relacionada con la prótesis, sino con la edad de los pacientes afectados, más propensos a enfermedades vasculares. Finalmente, el problema a considerar no se refiere a la prótesis, sino a la edad del paciente. Esta serie se ha extraído de una población operada de la válvula aórtica; ahora bien, sabemos que las trombosis son más frecuentes tras la implantación de una prótesis en posición mitral. Está claro que el riesgo de trombosis es más alto después de implantar una válvula sintética que una válvula biológica. Las complicaciones hemorrágicas son más frecuentes en las válvulas mecánicas que en las bioprótesis, para las que no es necesario un tratamiento con anticoagulantes. Los pacientes con complicaciones hemorrágicas representan un 13% en el grupo de las prótesis sintéticas frente a sólo un 5% en el otro grupo. En cambio, el riesgo de reintervención por deterioro de la válvula es mucho más alto con las bioprótesis, pues es del 11% a los 10 años frente a sólo el 4% con las prótesis mecánicas, para las que el reemplazo resulta necesario en muy pocos casos. Homoinjertos Este tema interesa a pacientes en los que se procede al cambio homoinjerto. Desde el punto de vista injerto fue realizado por Donald algo particulares, de la válvula por histórico, el primer Ross en Londres, Focus en 1962. Más de 25 000 intervenciones de esta naturaleza se han practicado desde entonces, esencialmente entre 1962 y 1974. Su número se ha reducido con el desarrollo de las prótesis mecánicas y los progresos de la industria de las válvulas. El nuevo interés por esta técnica se debe en gran parte a la constatación de una degeneración de las bioprótesis. Los homoinjertos valvulares son posibles gracias a ablaciones realizadas en pacientes fallecidos por razones extracardíacas. Esas válvulas se pueden utilizar si se extraen muy pronto. Este modo de obtención es muy importante en Estados Unidos, Canadá y Reino Unido. Desde 1994, con la aprobación de las leyes francesas de bioética, no se pueden extraer válvulas de cadáveres a no ser de pacientes en estado de muerte cerebral. Si el corazón no se puede utilizar para un injerto, la extracción se puede limitar a las válvulas. Se conserva en un banco de tejidos. En muchos casos, las válvulas cardíacas son funcionales y se pueden emplear para reemplazos valvulares. Los trasplantes cardíacos también pueden utilizarse con estos fines. El miocardio no se puede utilizar, pero a veces las válvulas siguen siendo funcionales. Una vez recuperadas las válvulas, se sigue un protocolo de descontaminación a base de antibióticos. A continuación se criopreservan en un banco de tejidos, sometiéndolas a una disminución progresiva de la temperatura hasta 60° bajo cero. De esta forma se pueden preservar hasta su implantación. Las condiciones de extracción están bien definidas: El donante debe tener menos de 60 años El donante no debe tener enfermedades generales como cáncer o enfermedades infecciosas El donante no debe haber recibido tratamientos con hormonas hipofisarias. Se recurre al homoinjerto sobre todo para tratar las afecciones de la válvula aórtica (regurgitación relacionada con una bicúspide, estenosis aórtica en bicúspide, reumatismo articular agudo). El resultado a largo plazo de los homoinjertos varía según la franja de edad de los pacientes operados. Veinte años después de la operación, el 42% sigue en vida. El homoinjerto está contraindicado para los menores de 20 años, habida cuenta de los datos de seguimiento a largo plazo. La endocarditis infecciosa (infección de las válvulas) es una de las patologías para Octubre 2007 / Revisión de las enfermedades coronarias y valvulares 39 las que el homoinjerto es especialmente interesante. Puede aparecer en una prótesis, al desarrollarse formaciones infecciosas en contacto con la válvula implantada. El homoinjerto no se realiza con material sintético, permite reemplazar la válvula sin aportación de material extraño y sin riesgo de contaminación adicional en caso de endocarditis. Cabe recordar que la endocarditis constituye una complicación temible, que origina embolias (embolias renales, embolias del bazo y embolias cerebrales muchas veces gravísimas, pues el infarto generado es muy extenso). Existe, como se lo hemos señalado, un riesgo de endocarditis en las prótesis. Los homoinjertos ofrecen la inmensa ventaja de proteger contra una nueva infección. Autoinjertos Las otras intervenciones que quedan por describir son marginales en cuanto a su número. El autoinjerto o la intervención de Ross consiste en reemplazar la válvula enferma usando la válvula vecina. Por ejemplo, el cirujano diseca una parte de la válvula pulmonar para integrarla en la válvula aórtica. Finalmente, la válvula pulmonar es sustituida por homoinjerto (válvula humana procedente de un donante). Si la válvula pulmonar (gemela anatómica de la válvula aórtica) está colocada en posición aórtica, hablamos de «autoinjerto». Esta intervención presenta un interés evidente para los atletas jóvenes, pues las características de la válvula de origen son excelentes. No hay casi ningún gradiente de obstrucción que temer tras la implantación. El atleta operado podrá realizar los mismos esfuerzos que un individuo normal. Las cifras de esperanza de vida son muy buenas, pues se registra un 72% de ausencia de fallecimientos a un horizonte de veinte años. Sin embargo, se señalan algunas reintervenciones. La intervención de Ross es especialmente interesante en los niños: ofrece la esperanza de un crecimiento normal, sin obstrucción ni alteración de la válvula. Por esta razón es la técnica preferencial para reemplazar la válvula aórtica en un niño. Elección del método terapéutico Según las circunstancias y el contexto clínico, ¿qué válvula elegir para los pacientes mayores? ¿Cabe seleccionar una prótesis mecánica o de origen biológico? La selección consiste en cotejar la esperanza de vida del paciente y el resultado esperado con la implantación de la válvula. Una prótesis biológica se alterará necesariamente con el tiempo, pero más lentamente en los pacientes muy mayores (de más de 70 años). Los primeros signos de deterioro empiezan a aparecer pasados los diez años de esperanza de vida residual. Antes, no hay nada que temer. Hay pocas probabilidades de tener que realizar una reintervención en un paciente mayor de 70 años que recibe una bioprótesis. Está claro que la edad es un factor de riesgo decisivo. Según el instituto francés de estadísticas, a los 70 años un hombre tiene una esperanza de vida de 13 años, y una mujer, de 16 años. La implantación de una bioprótesis expone a un hombre y más aún a una mujer a un riesgo de reintervención en la válvula. A los 75 años, la esperanza de vida de un hombre es de 9 años y la de una mujer, de 13 años. Por consiguiente, la práctica actual consiste en implantar una bioprótesis en el hombre a partir de los 70 años y en la mujer a partir de los 75 años. Sin embargo, para seleccionar una prótesis, entran en cuenta otros factores además de la edad, relacionados en particular con la enfermedad cardíaca. Si el paciente presenta una estenosis aórtica, no tendrá exactamente la misma esperanza de vida que la población normal. Es aún más el caso cuando la patología valvular está asociada a afectaciones de las arterias coronarias. He insistido en el hecho de que la esperanza de vida depende del sexo: cuando el paciente sufre una patología de las arterias coronarias, hay que tener presente que las mujeres tienen un pronóstico peyorativo respecto a los hombres. Sus arterias coronarias tienen dimensiones reducidas y las patologías evolucionan más rápidamente. Sin embargo, en la categoría de personas con coronarias normales, las mujeres tienen una esperanza de vida mejor que los hombres. Por otra parte, cuanto más acentuada esté la cardiopatía, más avanzado será el estadio y mayor el riesgo de muerte a largo plazo. De ahí que en los pacientes con esperanza de vida limitada se tienda a utilizar bioprótesis. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Por último, intervienen consideraciones socioeconómicas. Un paciente de 80 años tiene una esperanza de vida de 7 años. Si presenta una estenosis aórtica, su esperanza de vida se reduce a 2 años. Por consiguiente, se trataría de alargar esta última en 5 años. Para este beneficio, se le expondrá a una mortalidad operatoria (un 10%) y a varias complicaciones entre las cuales graves morbilidades neurológicas con secuelas. El coste de la operación valvular asciende a 23 000 euros. La opción médica también implica una opción de sociedad. Abordemos ahora el reemplazo de una válvula mitral en un paciente joven. En principio, se procede a este tipo de operación con una prótesis mecánica. Esta válvula no es tan ventajosa en posición mitral como aórtica debido a la multiplicación por cinco del riesgo de trombosis. Los riesgos inherentes al tratamiento anticoagulante también tienen que mencionarse. A un horizonte de 10 años, un 83% de los pacientes aún en vida no han sufrido ningún accidente particular. Un 71% de los pacientes con una media de edad de 51 años en el momento de la operación siguen en vida diez años más tarde. Las prótesis mecánicas no representan la solución ideal en los pacientes jóvenes, pero tampoco las prótesis biológicas, ya que un 52% de las personas de menos de 60 años deben volver a operarse en un plazo de 10 años. El riesgo de degeneración de la bioprótesis es más alto en posición mitral que aórtica, si se observan los resultados obtenidos en una serie de 232 mujeres jóvenes (con una media de edad de 24 años). La supervivencia a los 10 años sólo es del 84%, para una franja de edad tan joven. Se han desarrollado soluciones de sustitución; nuestro servicio ha propuesto un método de autoinjerto de la válvula mitral. Para las válvulas mitrales, los homoinjertos presentan resultados comparables a las bioprótesis, tras el análisis de una muestra de 104 pacientes. Sus tasas de reintervención también son comparables. Sin embargo, este método expone a un riesgo de deterioro precoz de la válvula y su tasa de intervención es más alta durante el primer año. Por tanto, este modo de reemplazo de la válvula mitral no se considera óptimo; no ofrece mejores resultados que el reemplazo valvular mitral. Por consiguiente, la decisión se toma esencialmente en función de la franja de edad. En principio, los pacientes mayores de 70 años reciben una bioprótesis. En el caso particular de una mujer con patología poco avanzada, que no presenta ninguna afectación coronaria, se utiliza más bien una válvula mecánica. Focus En los pacientes con edades comprendidas entre los 40 y los 70 años, los cirujanos acostumbran a implantar una prótesis mecánica. Una contraindicación al tratamiento anticoagulante constituye un factor de excepción. En este caso, se recurrirá a la bioprótesis o al homoinjerto para la válvula aórtica. Si el paciente presenta una endocarditis infecciosa, el homoinjerto será el método preferencial para corregir su patología valvular. Si la edad del paciente es inferior a 20 años, se empleará preferentemente el método de Ross o se procederá, llegado el caso, a la implantación de una prótesis mecánica. Por último, abordaremos la alternativa entre reemplazo valvular y plastia. Se deberá optar por este método siempre que sea posible. Pienso en particular a la cirugía plástica de la válvula mitral. Plastias mitrales Este método que permite evitar un reemplazo fue elaborado por Alain Carpentier a finales de los años sesenta. Consiste en implantar un anillo protético en el lugar de la válvula afectada. Existen diferentes tipos de insuficiencia mitral, según la anormalidad de los movimientos de la válvula: aumento (prolapso) o disminución (restricción de la válvula). Una clasificación funcional en tres tipos orienta al cirujano a lo largo de la operación: es imperativo que éste pueda identificar el tipo funcional que tiene delante. La ecografía sigue siendo el mejor examen para objetivar el tipo funcional mitral alterado. Aquí podemos observar un prolapso: requiere una transposición corregida de cuerdas para evitar el desplazamiento de la válvula hacia la aurícula izquierda. ¿Qué representa una plastia mitral con respecto a las demás intervenciones? La respuesta depende esencialmente de las situaciones clínicas y la experiencia. En nuestro caso, recurrimos muy a menudo a una plastia mitral. Entre dos tercios y tres cuartos de los enfermos que recibimos para una cirugía mitral son sometidos a una operación de plastia mitral. Este dato es destacable aún más cuando una cuarta parte de estos pacientes acuden por un reemplazo valvular. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares 41 La mortalidad operatoria depende mucho de la etiología de la valvulopatía mitral. Es muy baja para las causas degenerativas (las más frecuentes) y el reumatismo articular agudo. Es significativamente más alta cuando existe una patología coronaria o una endocarditis infecciosa, en cuyos casos las tasas de mortalidad alcanzan un 9%. Comparemos ahora los resultados entre plastia y reemplazo de la válvula mitral. Indudablemente la supervivencia a largo plazo es más alta en caso de plastia que de reemplazo de la válvula. La plastia mitral representa la mejor respuesta quirúrgica cuando es realizable, en los pacientes con valvulopatía mitral. La etiología de la patología valvular influye mucho en las respuestas a largo plazo. Al comparar las etiologías, observamos que la mortalidad es superior para un reumatismo articular agudo que para una afección degenerativa. Las personas que no necesitan una reintervención a los quince años representan un 93% de los pacientes con etiologías degenerativas frente a sólo un 75% de los pacientes con válvulas reumáticas. El uso de los métodos modernos de investigación ha permitido mejorar los resultados de los gestos quirúrgicos. La ecografía se utiliza ampliamente en los quirófanos, que ahora deben estar equipados con aparatos de ecografía y sondas para realizar investigaciones por vía transesofágica. Fundamentalmente, las posibilidades de realizar una plastia en la válvula aórtica son mucho menores que en la válvula mitral. En realidad se limitan a algunos casos. En la válvula aórtica se acostumbra pues a realizar un reemplazo. Cabe mencionar, sin embargo, el síndrome de Marfan, que asocia una afectación de la válvula aórtica con aneurismas, especialmente de la aorta ascendente. Aquí una RMN muestra una ectasia de la raíz aórtica, se puede ver una dilatación de la aorta. El mecanismo de la insuficiencia aórtica se explica en estos pacientes por un aneurisma, que ejerce una tracción sobre la válvula. Si se afloja la tracción devolviendo a la válvula aórtica su diámetro normal, se restablece la contracción. Con la distancia, contamos con resultados interpretables. En 158 pacientes estudiados, la supervivencia a los quince años se acerca a un 60%. Finalmente, en este grupo especial la tasa de reintervención es reducida. Globalmente, para disponer de datos comparativos en toda Europa, es posible consultar el registro Euroscore, a partir del cual se puede comparar la Europa del Sur (incluida Francia) y la Europa del Norte. En la Europa del Sur, un 65% de los pacientes han sido operados por una valvulopatía aórtica y un 35% por una patología mitral. En la Europa del Norte, estas cifras son del 73% y del 27%, respectivamente. Esto se explica por la rareza relativa del reumatismo articular agudo en esta región. Es interesante comparar la relación entre plastia y reemplazo valvular. Se registra un 25% de plastias en la Europa del Sur frente a un 19% en la Europa del Norte (con un 81% de reemplazos valvulares). La asociación de una prótesis de válvula y una derivación coronaria representa un 16% en la Europa del Sur frente a un 31% en la Europa del Norte (donde los pacientes suelen ser un poco más mayores). La mortalidad global de los pacientes operados por derivación es del 3,4%. Esta cifra se duplica en caso de cirugía de la válvula aórtica (un 6%). Es un poco más alta aún en caso de intervención en la válvula mitral. Si no se sobreañade ningún otro factor de riesgo, la mortalidad operatoria de una cirugía valvular es mucho más reducida, por lo que el contexto clínico debe apreciarse cuidadosamente. A cada factor de gravedad se asocia un factor de ponderación para predecir el riesgo operatorio. Para ello se utilizan unos quince factores de mortalidad hospitalaria. Como último recurso se puede plantear un injerto cardíaco en los raros casos en que la patología valvular llega a la fase terminal. Se coloca al paciente bajo circulación extracorpórea mientras se le implanta un nuevo corazón. Al final de la intervención se pueden ver líneas de sutura en la aurícula y los grandes vasos. Pero el pronóstico de los pacientes trasplantados por valvulopatía no es tan bueno como el de los pacientes trasplantados por otra causa: cabe temer la aparición de cardiopatías isquémicas y cardiopatías dilatadas. La supervivencia de pacientes trasplantados por enfermedades valvulares es menor que la de los pacientes trasplantados debido a otras etiologías. Para terminar presentaré el caso de un paciente sometido a una plastia mitral. Era paucisintomático, como es el caso a veces de las personas que acuden al cirujano. Presentaba una regurgitación importante, caracterizada por una falta de aliento moderada. La ecografía había detectado una insuficiencia mitral considerable. La lesión estaba relacionada con una ruptura de cuerda de la válvula mitral. Se realizó una resección de la parte enferma de la válvula y se envió la muestra para su estudio anatomopatológico. La intervención en sí consistió en reparar el defecto creado por la resección valvular. Al final de la operación se tuvo que completar la plastia con la implantación de un anillo protético calibrado para el orificio valvular, a fin de devolver a la válvula una forma y dimensiones normales. CIRUGÍA VALVULAR AÓRTICA Tipo de válvula Número Edad Supervivencia Sin reintervención a los 10 años Mecánica St Jude Baudet JTCVS 1995 773 57 74% > 94% Bioprótesis porcina Hancock Logeais JHVD 1995 1 108 74 46% 89% 589 67 71% 97% 1 022 49 77% 85% Bioprótesis pericardio bovino Carpentier Edwards Aupart Annais TS 1996 Homoinjerto O'Brien JHVD 2001 Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Focus 43 CIRUGÍA VALVULAR MITRAL Tipo de válvula Número Edad Supervivencia Sin reintervención a los 10 años Mecánica St Jude Baudet JTCVS 1995 207 53 71% > 96% Bioprótesis porcina Hancock Legarra JHVD 1999 122 61 65% 77% Bioprótesis pericardio bovino Carpentier Edwards Aupart JTCVS 1997 150 62 71% 90% Plastia Técnica de Carpentier Deloche JTCVS 1990 206 49 90% 92% John EVANS De la sala En la prensa médica se menciona un reemplazo de válvula aórtica mediante endoprótesis. ¿Esta práctica sólo se encuentra por el momento en fase de investigación? ¿En qué medida los pacientes reanudan una vida normal tras una operación de cirugía? ¿Algunos sufren discapacidades importantes? Christophe ACAR Christophe ACAR Efectivamente, se trata de un procedimiento que materializa una vía de investigación apasionante. Alain CRIBIER, del hospital de Rouen, es el impulsor de este método, que consiste en colocar una válvula por vía percutánea. Se ha probado en cuatro o cinco pacientes, con resultados más o menos buenos. El objetivo es reemplazar la válvula aórtica sin tener que abrir el tórax y, por lo tanto, sin exponer al paciente a los riesgos de la circulación extracorpórea. Desde el punto de vista técnico, no se puede afirmar que el procedimiento sea perfecto y pueda competir con el gesto de referencia: la operación con esternotomía y el reemplazo de la membrana. En principio, los pacientes llevan una vida normal, pero todo depende de las condiciones en que se ha practicado la operación. Si el paciente estaba en buena forma en ese momento y el gesto se estudió bien, no se debe temer ninguna complicación significativa en la vida de todos los días. Se puede imponer un período de rehabilitación a una paciente sin aliento, que camina con la ayuda de muletas. En cambio, un paciente de 30 años sometido a una plastia no lo necesita. ¿Cuál es el interés del homoinjerto en la endocarditis de Libman-Sachs? Christophe ACAR Christophe ACAR La endocarditis de Libman-Sachs no deja de ser excepcional, por no decir rarísima. Se ha realizado este tipo de operación, pero ha necesitado nuevas intervenciones. En este caso particular, la mejor técnica es la plastia, cuando es posible. El período siguiente a la operación es el que presenta más riesgos. Ninguna operación de este tipo está exenta de riesgos; las complicaciones son más frecuentes en los seis meses siguientes (coágulos, trombosis...). Octubre 2007 / Revisión de las enfermedades coronarias y valvulares El ejercicio profesional del paciente es totalmente determinante. Si requiere un esfuerzo físico importante, el paciente deberá reconvertirse debido a su cardiopatía. John EVANS John EVANS ¿Qué pasa con una persona joven, sometida a un reemplazo valvular sin complicaciones? ¿Cuáles son los índices de reanudación del trabajo y de invalidez? Agradecemos encarecidamente al Doctor Acar su exposición exhaustiva y las respuestas que ha dado a nuestras preguntas. John EVANS Según las curvas de mortalidad, el riesgo fatal parece existir sólo durante el primer año siguiente a la implantación de la prótesis. La curva de supervivencia es prácticamente paralela a la curva de referencia. De la sala A largo plazo, todo depende de la condición preoperatoria del paciente. Si éste no presentaba falta de aliento ni cardiopatía avanzada, debe recuperar una esperanza de vida normal. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Christophe ACAR Focus 45 Evaluación del riesgo de las enfermedades valvulares cardíacas Doctor Dominique LANNES. Médico asesor, SCOR Global Life Consecuencias del enfoque médico más reciente Entraremos ahora en el campo específico de la medicina de seguros para realizar la síntesis de los datos muy útiles que han sido comunicados a nuestra asamblea de aseguradores. El objetivo es contar con reglas fiables para la tarificación de los reemplazos valvulares y las valvulopatías. Nos situamos en el campo del riesgo agravado, puesto que las patologías consideradas son serias. Sin embargo, la medicina ha evolucionado y el diagnóstico se ha afinado considerablemente gracias a la ecocardiografía cardíaca. Esta técnica ha permitido ganar en precisión para la vigilancia de los pacientes sometidos a la implantación de una prótesis valvular. Asimismo ha abierto el camino hacia una prevención sistemática de la endocarditis, cuando se observa un soplo anormal. Una patología valvular no debe operarse ni demasiado temprano, ni demasiado tarde. Los expedientes de los pacientes que presentan un corazón en mejor estado en el momento de la intervención son más fáciles de evaluar. Desde el punto de vista técnico, las prótesis bivalva fabricadas en carbono han sustituido a los modelos antiguos. Las plastias representan aún un progreso considerable, especialmente en la cirugía de la válvula mitral. Aquí también la ecocardiografía facilita la vigilancia de los pacientes. En materia de seguros, se debe tener en cuenta la capacidad analítica del examen. El ecodoppler interviene en el diagnóstico como en el seguimiento de la valvulopatía (en principio, cada seis meses). El momento óptimo para realizar la intervención quirúrgica se determina cada vez mejor. Como aseguradores y reaseguradores, podemos hoy revisar nuestro planteamiento del riesgo en las personas con una enfermedad valvular que justifica la implantación de una prótesis. Podemos reducir el riesgo asumido realizando una selección adecuada. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Esquemas de análisis La selección médica se basa en el cuestionario. Un soplo cardíaco puede ser el signo de una valvulopatía. Si una persona padece una insuficiencia cardíaca que requiere un tratamiento fuerte a base de diuréticos e IEC, nos enfrentamos a una valvulopatía severa que motiva un rechazo. La referencia a una disnea es un signo de alarma fundamental que justifica como mínimo unos exámenes complementarios. En todo caso, ante una patología valvular, hay que pedir el último balance de seguimiento y la última ecografía. Un cuestionario específico de las valvulopatías permitirá afinar el análisis y la tarificación. ¿Cómo proceder para la tarificación? Hay que apoyarse en la clínica y la ecografía. La disnea de esfuerzo es capital para la evaluación clínica. La llamada clasificación NYHA define: Una clase I correspondiente a una capacidad de esfuerzo normal. Una clase II correspondiente a una falta de aliento durante un esfuerzo importante. El profesor Michel ha insistido en el carácter relativo de este esfuerzo, según la actividad física a la que está acostumbrada la persona. Una clase III correspondiente a una falta de aliento al menor esfuerzo (para intentar subir una escalera, por ejemplo). Una clase IV correspondiente al edema pulmonar. Las dos últimas clases motivan un aplazamiento o un rechazo. En materia de ecografía, cada dos años los cardiólogos plantean nuevos criterios para clasificar a los enfermos y definir mejor las valvulopatías. No se han puesto de acuerdo aún en un modo de clasificación común. Por el momento, según las anomalías detectadas, se distinguen los siguientes grados: Grado I o mínimo. Grado II o moderado. Grado III o medio. Grado IV o grave. Se tratará de determinar a qué clase pertenece un solicitante. Generalmente las dos últimas justifican un aplazamiento o un rechazo. Se prestará una atención especial a las dilataciones de las cavidades cardíacas, las hipertrofias y las anomalías de la función de eyección. Habrá que apoyarse en los datos clínicos y los informes de ecografía. Los solicitudes que se pueden tarifar son las de pacientes asintomáticos, que no presentan ninguna falta de aliento o síncope. No se prevé ninguna operación en esta categoría, que corresponde a los grados I o II del análisis por ecocardiografía. Trastornos del ritmo Muerte súbita Angina Efectivamente, este último riesgo se explica por el hecho de que algunos pacientes, muchas veces mayores, asocian una patología valvular a una patología coronaria. La mortalidad de la cirugía valvular, según los datos presentados por los profesores Michel y Acar, se sitúa entre un 3 y un 5%. Después de la cirugía, es posible volver a calcular y determinar los principales riesgos, que corresponden a: Los rechazos o aplazamientos son motivados por: La pertenencia a la categoría de los enfermos muy sintomáticos de grado III o IV en el esquema de evaluación de la molestia durante el esfuerzo. La pertenencia a los grados III o IV en el esquema de análisis por ecocardiografía. La programación de una cirugía valvular en un futuro próximo. En una persona con valvulopatía, se distinguen el período anterior a la operación, el período perioperatorio y el período postoperatorio, en el que la válvula se estabiliza. El principal período de riesgo es el de la cirugía valvular. La desinserción o la trombosis de la prótesis. Los accidentes debidos al tratamiento anticoagulante. En definitiva, el período circundante a la cirugía justifica un aplazamiento o rechazo. Pasa lo mismo si: Se observan síntomas de las clases III o IV o signos de insuficiencia cardíaca. La ecografía objetiva una situación correspondiente a los grados III o IV. En estos casos hay que pedir al solicitante que vuelva después de la operación de cirugía valvular. Globalmente, un paciente puede presentar durante varios años las siguientes características clínicas: «soplo cardíaco, ausencia de disnea, ecocardiografía correcta». Cuanto más nos acerquemos a la operación quirúrgica, más patentes serán los síntomas y más clara será la ecografía. Habrá pues que determinar el momento adecuado para iniciar la operación, que representa un período clave en la evaluación de los riesgos. Un tercer período sigue a esta etapa decisiva: es el período posterior a la intervención. Por tanto, la antiselección es máxima en el período preoperatorio inmediato. No se recomienda contratar un seguro justo antes de una operación, como lo indica el sentido común. Antes de la cirugía valvular, los principales riesgos notables son los siguientes: Endocarditis Insuficiencia cardíaca Octubre 2007 / Revisión de las enfermedades coronarias y valvulares TARIFICACIÓN Aplazamiento o rechazo 6 meses Sobremortalidad Sobremortalidad +50… a… +250 +50… a… +250 Período inasegurable Focus Ejemplos prácticos de tarificación Abordaremos ahora los aspectos específicos de la tarificación a partir de casos concretos. 47 A una mujer de 35 años afectada por una estenosis mitral y disnea al hacer esfuerzos importantes (footing), cuya ecocardiografía objetive una estenosis mitral moderada (superficie valvular de dos centímetros cuadrados), se le aplicará la siguiente tarificación: En el caso de una tarificación solicitada mucho antes de que una operación se haga inevitable, si la persona es asintomática de clase I o II y los datos de la ecografía corresponden a los grados I o II, se aplicará una sobremortalidad que oscile entre el 50 y el 250%. 200% por sobremortalidad (se tendrán en cuenta los riesgos de trastornos del ritmo, embolia de los vasos supraaórticos y probable operación futura) 250% por incapacidad e invalidez 100% por dependencia Tras una cirugía valvular, si el paciente es asintomático o muy poco sintomático, y presenta su última ecocardiografía de seguimiento así como un balance de buen funcionamiento de la prótesis y del ventrículo izquierdo, la sobremortalidad se situará en una horquilla de entre el 25% y el 150%. En el caso de un hombre de 65 años, afectado por una estenosis aórtica tratada mediante la implantación de una prótesis mecánica, asintomático, que presente un ecodoppler normal y cuya prótesis funcione normalmente, se seguirán los siguientes criterios: Este nuevo ejemplo traduce una pequeña revolución en los esquemas de tarificación, que tienen en cuenta los progresos de las plastias mitrales: un prolapso aislado de válvula mitral, sin complicaciones, se considerará como un riesgo normal. En caso de prolapso de la válvula mitral con soplo y regurgitación, se aplicará la tarifa de la insuficiencia mitral. En caso de doble valvulopatía (estenosis aórtica e insuficiencia mitral, por ejemplo), se evaluará el riesgo según cada caso y no se recomendará de entrada ningún rechazo sistemático. Veamos ahora una serie de casos clínicos. Para un hombre de 50 años que presente una insuficiencia mitral asintomática, moderada según el ecodoppler, con ventrículo izquierdo funcional y de tamaño normal, la tarificación será la siguiente: 75% por sobremortalidad 125% por incapacidad e invalidez 25% por dependencia (el riesgo es menor) A un hombre de 50 años afectado por una insuficiencia aórtica y disnea al subir las escaleras, tratado con diuréticos e IEC, que no presente los resultados de un ecodoppler cardíaco, se le rechazará la solicitud. En todo caso, no servirá para nada pedir un ecodoppler ya que el paciente tiene que ser operado. Si éste se opone a la decisión, cabrá obtener la última ecocardiografía y pedir más datos. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Además la endocarditis infecciosa sigue dando miedo en el mundo médico. ¿Cuáles son los riesgos reales de exposición? Pierre-Louis MICHEL El riesgo no disminuye: la incidencia sigue siendo baja pero estable en los países desarrollados (con 25 nuevos casos anuales por cada millón de habitantes). Se registra aproximadamente el mismo porcentaje en Francia, con 1 500 casos anuales de endocarditis. La mortalidad permanece en torno al 15 ó 20%. El riesgo de intervención precoz se sitúa alrededor del 50%. Esta enfermedad 50% por sobremortalidad Rechazo por incapacidad e invalidez, dada su edad (sin embargo, todo depende del perfil del paciente y no conviene aplicar ningún razonamiento mecánico) 100% por dependencia A una mujer de 50 años, sometida a una plastia de la válvula mitral hace tres años, asintomática, que presente un ecodoppler sin anomalía, se le ofrecerá una tarifa que tenga en cuenta los datos expuestos por el profesor Michel ante esta asamblea: 25% por sobremortalidad (porcentaje casi idéntico al de la población normal) 50% por incapacidad e invalidez (sólo examinamos expedientes, cabe ser prudentes) 25% por dependencia Por consiguiente, el hecho de llevar una cicatriz en el esternón, a consecuencia de una plastia destinada a corregir una insuficiencia mitral, no conduce a un rechazo sistemático por parte de la aseguradora. John EVANS Nuestros esquemas de tarificación siguen la evolución de la clínica y las prácticas hospitalarias. Si nuestras decisiones parecen a veces algo severas a la vista de lo que se ha expuesto, cabe recordar que no todas las operaciones se practican en la región parisina y no todos los médicos son tan experimentados y eficaces como nuestros interlocutores. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares da miedo y sus consecuencias siguen siendo severas. Se puede observar un cambio en la epidemiología, así como una disminución de las endocarditis relacionadas con estreptococos presentes en la boca. La profilaxis antibiótica ha dado sus frutos. En cambio, se nota un aumento de las endocarditis de estreptococos digestivos, especialmente en las personas mayores, afectadas por patologías degenerativas. Los riesgos son importantes para los que poseen una prótesis valvular y presentan una insuficiencia aórtica. Pero teóricamente no existen motivos para aplicar un recargo por endocarditis a las personas con estenosis mitral. Focus 49 Conclusión L La mortalidad relacionada con las enfermedades cardiovasculares está en continua disminución en el llamado mundo industrializado. Desgraciadamente no es el caso en otras partes, especialmente en los países del tercer mundo donde quedan muchos progresos por realizar en la atención a estas patologías. Sin embargo, con las exposiciones de nuestros invitados acabamos de ver que gracias a los adelantos en los campos del diagnóstico, el tratamiento y la prevención de las enfermedades coronarias, las personas que tienen acceso a los cuidados pueden esperar una mayor longevidad y una mejor calidad de vida. Por consiguiente, hay que traducir estos progresos médicos en términos concretos para las personas afectadas por estas enfermedades que deseen un seguro de personas con cobertura de los riesgos de fallecimiento e incapacidad. En SCOR Global Life, creemos que es posible ofrecer condiciones de seguro más favorables, siempre que obtengamos los datos necesarios para una apreciación objetiva de los riesgos. Nuestras políticas de selección y tarificación deben evolucionar paralelamente a los avances médicos para que una amplia mayoría de las personas afectadas por estas enfermedades puedan realizar su proyecto de vida social y profesional. Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Octubre 2007 / Revisión de las enfermedades coronarias y valvulares Collección SCOR Global Life Newsletters 28 27 26 25 24 23 22 21 20 19 18 17 16 15 14 13 12 11 10 09 08 07 06 Edición Especial 05 04 03 02 01 Un año en Vida: Cronología 2006 del Seguro de Vida Asegurar a los solicitantes transplantados renales Un año en Vida: Cronología 2005 del Seguro de Vida Obesidad mórbida y banda gástrica Los productos de vidas preferentes en Seguros de Vida La fibromialgia El reaseguro al servicio de la selección de riesgos Un año en Vida: Cronología 2004 del Seguro de Vida Fondos de pensiones: panorama europeo Proyecciones de mortalidad y rentas vitalicias El seguro de incapacidad o invalidez Tarifas diferenciadas Hombres / Mujeres: el debate europeo El seguro privado de dependencia Las aseguradoras contra el fraude al seguro La selección financiera Cobertura de las enfermedades graves Contratos de seguro en unidades de cuenta Deportistas profesionales El sector bancaseguros en el mundo El seguro privado de dependencia - Comparaciones internacionales Fondos de pensiones alemanes Control de las exposiciones: Un principio de buena gestión Incidencias de los atentados del 11 de septiembre de 2001 en las prácticas de los seguros de personas Reform of the German old-age security system Fumadores / No fumadores: Construcción de una tarifa segmentada El Reaseguro Herramienta de refuerzo del patrimonio propio no comprometido Alcoholismo y seguro de personas Marcadores clásicos y marcador actual: la CDT Las compañias de seguros y la lucha contra el blanqueo VIH y cobertura de seguro Focus Seguro de los tumores genitales en los hombres jovenes La Bancaseguros Diabetes and its complications Hepatitis virales B y C balance de la situación Concepción y realización: Franklin Partners Revisión de las enfermedades coronarias y valvulares Autor Dr John Evans [email protected] Responsable de Publicación Bérangère Mainguy tél. + 33(0)1 46 98 84 73 [email protected] 1, avenue du Général de Gaulle 92074 Paris la Défense cedex France www.scor.com N° ISSN: en curso.