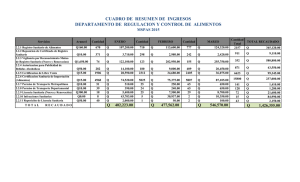
Informe Colectivo ensayo 24 de 2014
Anuncio

9(1) 2014 COMPLEMENTARIEDAD ENTRE HEMATOLOGÍA Y CITOGENETICA EN CASOS DE LEUCEMIA INFANTIL Y VIGILANCIA EPIDEMIOLOGICA Crane C1, Bermúdez A1 1.- Grupo Genetica Cronicas. Instituto Nacional de Salud Introducción: El cáncer en los niños es una enfermedad que constituye un importante problema de salud pública, por la alta letalidad y por el costo social. Según el análisis de mortalidad de las leucemias realizado en el Instituto Nacional de Cancerología (1), las leucemias son la principal causa de cáncer pediátrico y corresponden al 30 % de las neoplasias malignas en menores de 15 años. Aproximadamente, el 75 % son leucemia linfoide aguda y del 15 al 20 % son leucemia mieloide aguda. De acuerdo con esto, ocurren 497 casos nuevos de leucemia cada año en Colombia, lo que representa el 42,5 % de todos los tipos de cáncer en la niñez y para el año 2008, el 48,2 % de las defunciones por cáncer en menores de 15 años correspondió a leucemias de cualquier tipo. Es importante que la letalidad medida como la razón incidencia/mortalidad, en el año 2002 fue de 1,3 en Colombia, mientras que para Estados Unidos fue de 5,1. La razón por la cual fallecen más niños proporcionalmente, se puede encontrar en las diferencias socioeconómicas aunque también pueden haber factores biológicos y genéticos que sean desfavorables, sin embargo la dificultad en la accesibilidad a exámenes de citogenética para el diagnóstico preciso y para el seguimiento pueden estar contribuyendo al fracaso del tratamiento. En este mismo sentido la calidad de las pruebas de hematología debe garantizarse. Otros autores (2), informan que en Colombia 1 se presentan altas tasas de incidencia por leucemias en niños. El diagnóstico definitivo y la aplicación de los tratamientos presentan demoras y tasas de abandono que contribuyen a una alta mortalidad; además, no se cuenta con los beneficios de los adelantos terapéuticos de otros países, a lo cual se puede agregar que también se carece de adelantos diagnósticos logrados en Europa y Norte América principalmente en las aplicaciones moleculares de la Citogentica así como en el diagnóstico automatizado en hematología. Ante esta situación con las leucemias del país, es necesario revisar la participación del laboratorio en la Vigilancia de las leucemias pediátricas, con el fin de identificar si es necesario proponer algún cambio en este sentido. Metodología Se revisó el protocolo actual para la vigilancia en Salud Pública de las leucemias (3), se analizó el aporte del Laboratorio de acuerdo con el flujograma de información, también se analizó la información que el laboratorio aporta en la definición de caso y la forma en que se evidencia en la ficha de notificación del SIVIGILA. Resultados El protocolo vigente para la vigilancia en Salud Pública está dirigido al Cáncer Infantil como evento a vigilar, que contempla en el primer grupo de patologías a las Leucemias y enfermedades mieloproliferativas y mielodisplásicas. En cuanto a los objetivos, se FOR-R01.5040-021 V00 propone: Determinar la oportunidad de atención de los menores de 18 años con cáncer notificados a través del Sistema de Vigilancia en Salud Pública, Generar espacios de análisis de la información resultado de la vigilancia en salud pública a nivel territorial e interinstitucional, para mejorar la oportunidad de atención de los menores de 18 años con cáncer, Estimar la sobrevida global, libre de evento, mortalidad atribuible al tratamiento y frecuencia de abandono del tratamiento de los menores de 18 años con cáncer tratados en centros de oncología y/o hematología pediátrica en Colombia y Divulgar de forma periódica la información producto de la vigilancia en salud pública a los diferentes actores del sistema de salud, involucrados en el proceso de atención de los menores de 18 años con cáncer, como insumo para la toma de decisiones a nivel local, regional y nacional. La amplitud de estos objetivos permite la aplicación a las diferentes situaciones de cáncer incluidas las leucemias. En la definición operativa de caso, se estableció específicamente el Caso probable de Leucemia Aguda Pediátrica en población menor de 18 años, y se incluye como criterio obligatorio la presencia de al menos un blasto, con lo cual el involucramiento del laboratorio es esencial y obligatorio. En la definición operativa de los desenlaces, el recuento de blastos sigue siendo el criterio para la recaída hematológica. Por otra parte, en cuanto a la notificación, las fuentes de los datos son Las Unidades Primarias Generadoras de Datos (UPGD), definidas como las Instituciones Prestadoras de Servicios de Salud que estén en capacidad de establecer diagnóstico probable de cáncer en menores de 18 años. En este caso el laboratorio clínico no cumple con la definición de UPGD. El protocolo establece el papel del laboratorio en la vigilancia del cáncer infantil, en dos aspectos específicos, la determinación de blastos en las leucemias y la determinación de marcadores tumorales en otros tipos de cáncer. Hemograma o extendido de sangre periférica fue el criterio de diagnóstico probable. Discusión La participación del laboratorio en el protocolo del SIVIGILA es esencial para la definición de caso probable, en la medida en que acompaña la confirmación del hallazgo clínico, puesto que la definición de caso es esencialmente clínica y se inicia por la presencia de al menos un síntoma, al cual se tiene que sumar el hallazgo del laboratorio. Sin embargo, un hecho que limita la oportunidad de la notificación, es que no está definido que a partir del dato de laboratorio se pueda iniciar el proceso de caso probable, para confirmar por clínica. Esto es coherente con el hecho de que el laboratorio clínico no está contemplado como UPGD, porque no puede hacer la configuración de caso. El papel asignado al laboratorio es puntual y tiene una delimitación de uso, en la etapa de definición de caso probable y en la confirmación posterior al diagnóstico clínico. Sin embargo limita la especificidad de la vigilancia, si se considera que el diagnóstico diferencial es importante y este se logra mediante la aplicación de técnicas de Citogenética molecular, para definir rearreglos estructurales y presencia de clones para el seguimiento del tratamiento. Para lograr un apoyo diagnóstico adecuado de las enfermedades hematolinfoides, se cuenta con la Citogenética estructural y con la técnica de Hibridación in situ con sondas fluorescentes (FISH), utilizando las sondas adecuadas en cada situación clínica (4), por ejemplo en Leucemia Linfoblastica Aguda (ALL) con la alteración estructural por translocación t(9;22) (q34;q11), la detección se hace mediante sonda de color dual LSI ETV6(TEL)/RUNX1(AML1), con la cual se mejora la oportunidad en la identificación de clones. El laboratorio puede ser una fuente importante de información para la vigilancia de las leucemias, tanto en la etapa inicial de diagnóstico por hematología, como en la En cuanto a la ficha de notificación, Cáncer en menores de 18 años código INS 115, la opción que le corresponde de información en el módulo de datos de laboratorio es señalar si el 2 FOR-R01.5040-021 V00 CITOGENETICA CLÍNICA Círculo de calidad Esta publicación se distribuirá con cada entrega del informe de resultados para los participantes en el programa de Evaluación Externa del Desempeño del Instituto Nacional de Salud, para citogenética clínica Correspondencia: AJ Bermúdez Genética Salud Pública Instituto Nacional de Salud Avenida El dorado N° 51-20 Bogotá Colombia Fax. 2207700 – 1265 Bogotá [email protected] Editor Antonio José Bermúdez Comité Editorial Cecilia Crane Dora Robayo Asistencia Maria Leonor Sanchez En el año 2006 el gobierno de Colombia por medio del decreto 2323 establece la estructura de la Red Nacional de Laboratorios. El Instituto Nacional de Salud tiene la responsabilidad de velar por la organización de la red, decreto 272 de 2004 y los laboratorios de citogenética hacen parte de la misma, por su importancia en el diagnostico especializado, aplicado a la asistencia, a la investigación y a la salud pública. Con la filosofía de los “Circulos de calidad”, esta publicación tiene como fin proveer información sobre citogenética clínica y socializar los resultados del programa de evaluación externa del desempeño. CONTENIDO 1. Complementariedad entre hematología y citogenetica para la vigilancia por laboratorio de las leucemias en población infantil 4. Resultados del ejercicio de evaluación externa del desempeño, primer ensayo ciclo 2014 - 2015 11. Nota técnica 12. Información de interés en salud pública 14.Cronograma: 3 etapa de confirmación y seguimiento a través del diagnóstico Citogenético o por FISH. Sin embargo, esta posibilidad no está contemplada en el protocolo de vigilancia en salud pública actualmente en aplicación, razón por la cual sería conveniente implementar la vigilancia por laboratorio, que tendría como objetivo informar los casos inmediatamente sean captados, con el fin de complementar la vigilancia por el SIVIGILA. Conclusión La vigilancia epidemiológica de las leucemias en niños es muy importante por la alta letalidad que tiene en Colombia, para lo cual está en uso el protocolo del SIVIGILA, sin embargo se puede mejorar la oportunidad en la captación de casos y la especificidad en el diagnóstico, mediante la vigilancia por laboratorio, complementaria con el SIVIGILA. Para eso es necesario dirigir los laboratorios clínicos hacia la automatización en hematología, independiente de su nivel de complejidad y así mismo incentivar a los laboratorios de citogenética para el diagnóstico de leucemias, por cariotipo y por FISH. Referencias 1.- Vera AM, Pardo C, Duarte MC, Suárez A. Análisis de la mortalidad por leucemia aguda pediátrica en el Instituto Nacional de Cancerología. BIOMEDICA. 2012;32(3). doi: http://dx.doi.org/10.7705/biomedica.v32i3.691 2.- Piñeros M, Pardo C, Otero J, Suárez A, Vizcaíno M, Álvarez VH, Castiblanco C, Trejo R. Rev Colomb Protocolo de vigilancia en salud pública de las leucemias agudas pediátricas. Guidelines for Epidemiologic Surveillance of Acute Pediatric Leukemias in Colombia. Cancerol 2007;11(4):219-227 3.- Ministerio de Salud y Protección Social. Protocolo de Vigilancia en Salud Pública. Cáncer Infantil. PRO-R02.051 Versión 00 2014 – Jun – 11. Pp: 28 4.- Hastings R, Howell R, Betts D, Porter S et al. E.C.A. Permanent working group for Cytogenetic and Society. Guidelines and Quality assurance for Acquired Cytogenetics. 2013 . No. 31 Reporte e información de casos de leucemias El Ministerio de Salud y Protección, El Instituto Nacional de Salud y SIVIGILA, solicitan a los laboratorios de citogenetica que informen cuando tengan un diagnostico citogenético de anomalía cromosómica en leucemias al correo [email protected] Se necesita informar la anomalía encontrada y el diagnostico de ingreso de la muestra al laboratorio, el nombre o identificación del paciente y el nombre de la EPS. Su colaboración es muy importante para contribuir a reducir la mortalidad infantil por esta causa. FOR-R01.5040-021 V00 Citogenética Clínica Programa de Evaluación Externa del Desempeño Evaluación externa de desempeño Citogenética clínica Informe del primer ensayo ciclo 2014 - 2015 INTRODUCCIÓN Informe correspondiente al ensayo Número 24, primero de 2014 - 2015, realizado con muestra compartida para analizar según la rutina diaria del laboratorio. Contiene el análisis de resultados de 20 laboratorios que cumplieron con el procedimiento solicitado. MATERIALES DE CONTROL DE CALIDAD La muestra para análisis en este caso fue producto intermedio. Se envíaron dos laminas bandeadas (Nos 1 y 2) correspondientes a una muestra procesada de un niño de 18 meses de edad, hijo de padres no consanguíneos de 26 y 23 años, a quien se solicitó el cariotipo por presentar criptorquidia bilateral. Al examen físico se encontró peso de 9820 g, talla de 80 cm, envergadura de 79 cm, perímetro cefálico de 47 cm y el único hallazgo fenotípico es la criptorquidia. Tiene una prima, hija de tía materna con polidactilia preaxial. No hay más antecedentes relevantes. Se solicitó hacer la lectura de las laminas como un caso rutinario del laboratorio. La muestra se circuló entre los diferentes laboratorios participantes, en forma secuencial coordinada de acuerdo con lo establecido en la Guia Técnica Colombiana, GTC 55-1, por lo tanto el valor asignado está dado por el laboratorio administrador de EEDDCARIO, sin embargo el ítem de ensayo se verificó al final del proceso de circulación, para garantizar que no hubo cambios significativos durante el desarrollo del ensayo de aptitud. El resultado enviado por cada laboratorio fue revisado por una citogenetista de EEDDCARIO, para revisión del cumplimento de estándares de calidad, de acuerdo con las recomendaciones que se han aceptado por el Programa de Evaluación del Desempeño. Esta evaluación se verificó por el mismo observador en lecturas independientes. Los resultados fueron presentados al panel de expertos. A partir de esta información se evaluó el componente técnico, analítico e interpretativo para cada caso. De acuerdo con las observaciones del grupo de expertos, se hizo la calificación final porcentual promediando la obtenida en cada uno de los tres componentes. RESULTADO ESPERADO Se definió de acuerdo con el consenso avalado por el grupo experto, que se puden dar dos posibles resultados, ambos correctos de acuerdo con la nomenclatura ISCN: Opción 1: 45,XY,rob(13;14)(q10;q10) Opción 2: 45,XY,der(13;14)(q10;q10) Además se evalua el cumplimiento de los mínimos de calidad en cada área de desempeño, los cuales están descritos en la tabla 2, junto con el puntaje y la respectiva ponderación. 4 FOR-R01.5040-021 V00 El desempeño técnico óptimo debe alcanzar un 100%, definido por la calidad en el material mostrado en el informe, el cual debe tener una resolución y ordenamiento, que reflejan el desempeño técnico. El desempeño analítico y el interpretativo, se califican por el incumplimiento en algunos de los requerimientos de calidad, por lo tanto el resultado esperado en estas áreas es cero fallas. RESULTADOS DEL EJERCICIO Los resultados se presentan según código en la tabla 1. El componente técnico representa el 40% de la calificación final, está constituido por el logro de seis puntos según se cumpla con los requisitos solicitados. El desempeño analítico esperado es de 18 puntos. De este valor se resta el puntaje asignado cuando se evidencia algún error y el puntaje obtenido se expresa en porcentaje. Igualmente se maneja el desempeño interpretativo, que corresponde a un esperado de 15 puntos, valor del cuál se resta un puntaje cuando se evidencia error y se expresa en porcentaje. Cada uno representa el 30% de la calificación final (Tabla 2). Para obtener la calificación, frente a cada parámetro se estableció un puntaje único, que se obtiene cuando se cumple la condición especificada, sin valores intermedios. El puntaje esperado se encuentra en la primera columna de la tabla dos y el valor obtenido para cada laboratorio participante en la columna correspondiente a su código. Para el porcentaje final se aplica la siguiente ecuación: % Final = Desempeño Técnico % x0.4 + Desempeño Analítico% x0.3 + Desempeño Interpretativo % x 0.3 Por ejemplo: • • • Un laboratorio obtiene 100% en el desempeño técnico por cumplir con todos los requisitos de calidad Obtiene 4 puntos en el desempeño analítico por tener un error en la nomenclatura ISCN y un error en la identificación de cromosomas normales. Esto representa que perdió el 22%, por eso el puntaje logrado es 78%. Obtiene 100% en el desempeño interpretativo porque no tuvo errores. 93 = 100x0.4 + 78x0.3 +100x0.3 La escala de interpretación se estableció por el grupo de expertos, con base en la gravedad del problema. Solamente se pueden aceptar errores que no afecten la interpretación clínica del resultado, pero de ninguna manera errores con equivocación grave. Rango 100% =90, <100 >70, <90 =70 o menos 0 Valoración Excelencia Aceptable Aceptable para revisión No aceptable No participa En la tabla uno se presentan los resultados de todos los participantes por códigos. En la tabla dos, se muestran los resultados según cada una de las áreas de desempeño, y el indicador de porcentaje final obtenido. En la tabla tres se establece un ordenamiento del primer lugar hacia abajo, independientemente de que se logre una calificación final aceptable. 5 FOR-R01.5040-021 V00 En la gráfica uno se presenta por medio de dispersión de puntos para cada laboratorio, el % logrado en cada área de desempeño. A cada laboratorio se le envía un informe individual con la secuencia temporal de desempeño en los ensayos a la fecha y en el recuadro la calificación actual. También se adjuntan las observaciones para seguimiento y para la construcción del plan de mejora cuando el resultado sea no aceptable, el cuál debe ir acompañado de un cronograma para seguimiento. Se pueden hacer las reclamaciones que se considere pertinente, dentro del plazo de una semana después de recibido el informe. Tabla 1. Resultados por laboratorio según código Código Laboratorio 2230609 2430905 Resultado Laboratorios (observación) 45,XY,rob(13;14)(q10;q10)[25] 45,XY,rob(13;14)(q10;q10)[25] 2570604 2581340 2860806 2880714 3240603 45,XY,der(13;14)(q10;q10) 45,XY,rob(13;14)(q10;q10) 45,XY,rob(13;14)(q10;q10) 45,XY,rob(13;14)(q10;q10) 45,XY,rob(13;14)(q10;q10) 3261339 4241238 45,XY,rob(13;14)(q10;q10)[60] 45,XY,rob(13;14)[30] 4521235 45,XY,rob(13;14)(q10;q10)[50] 4580602 4621236 45,XY,der(13;14)(q10;q10)[100] 45,XY,rob(13;14)(q10;q10)[30] 4890610 45,XY,rob(13;14)(q10;q10)[25] 5420617 45,XY,rob(13;14)(q10;q10)[25] 7460611 7850715 8320601 45,XY,rob(13;14)(q10;q10) 45,XY,rob(13;14)(q10;q10) 45,XY,rob(13;14)(q10;q10)[25] 8470613 8620608 8720612 45,XY,der(13;14)(q11.1;q11.1) 45,XY,rob(13;14)(q10;q10) 45,XY,rob(13;14)(q10;q10) Otros Análisis de 42 cels Análisis de 60 cels No envían laminas en tiempo establecido Análisis de 50 cels No envían laminas en tiempo establecido Resultado de consenso avalado por el grupo experto: Opción 1: 45,XY,rob(13;14)(q10;q10) Opción 2: 45,XY,der(13;14)(q10;q10) 6 FOR-R01.5040-021 V00 Tabla 2.- Indicadores por área de desempeño, según código del laboratorio participante 8470613 8720612 2860806 2880714 7850715 2430905 4521235 4621236 4241238 3261339 2581340 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 0 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 0 1 1 1 Número mínimo de células examinadas según el caso 1 0 1 1 1 1 1 1 1 1 1 0 1 0 1 1 1 0 1 1 0 1 1 0 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 0 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Suma % 5 83 6 100 6 100 6 100 6 100 6,0 100 6 100 6 100 6 100 4 67 5 83 6 100 6 100 6 100 5 83 6 100 6 100 4 67 6 100 0 0 0 0 0 0 0 0 0 0 0 No cumple Puntaje asignado 0 Sin error Carece de alguno de los elementos establecidos en la norma técnica Colombiana[1], sin afectar la interpretación. Carece de evidencia documental del cariotipo Falla para proveer una correcta interpretación clínica del hallazgo citogenético. 0 0 0 0 0 0 0 6 100 0 0 0 0 0 0 0 0 0 0 0 0 1 1 2 3 3 3 4 4 5 Puntaje asignado 0 0 100 0 0 0 100 0 100 0 1 1 1 0 100 0 100 0,0 100 0 100 0 0 0 0 0 100 0 0 0 100 4 0 100 0 0 0 1 0,0 100 0 0 0 100 0 100 0 0 0 0 100 0 100 0 0 0 0 0 1 1 1 0 100 0 100 0 0 0 100 0 100 0 100 1 1 1 0 1 1 4 3 Falla en la inclusión de recomendaciones apropiadas con base al resultado, como requerimiento de otra muestra, muestra de confirmación, muestras de parientes y otras pertinentes. 2 Falla en la interpretación correcta del cariotipo 5 7 0 0 1 Suma % DESEMPEÑO INTERPRETATIVO 7691234 8620608 1 1 1 Nomenclatura ISCN con errores que afectan la interpretación clínica Asignación errónea de puntos de ruptura Falla en la obtención del cariotipo correcto 2461237 7460611 1 1 1 Identificación incorrecta de los cromosomas normales 3441016 3240603 1 0 1 DESEMPEÑO ANALÍTICO 3460707 2230609 1 0 0 Sin error Nomenclatura ISCN con errores menores que no afecten la interpretación Nomenclatura ISCN con error significativo, como orden incorrecto de descripción de anomalías 4670632 4890610 1 1 1 Tinciones o bandeamientos aplicados según indicación. Oportunidad de entrega de resultados en el plazo establecido 4580602 5420617 0 Número de solapamientos máximo de uno. Calidad de las bandas en definición. Cumple 2870631 2570604 1 DESEMPEÑO TÉCNICO 8370630 8320601 Número de bandas mínimo para el tipo de muestra. 24 4320633 Código Ensayo Suma % 0 100 0 0 1 93 1 93 0 100 0 100 0 100 0 100 1 93 0 0 1 93 0 100 0 0 0 100 0 0 1 93 1 93 0 0 0 100 1 93 0 0 0 0 0 100 1 93 0 0 1 93 1 93 1 93 % final 93 0 98 98 100 100 100 100 98 0 98 87 0 100 0 91 98 0 100 98 0 0 93 98 0 98 85 98 FOR-R01.5040-021 V00 Tabla 3. – Indicadores en (%) por área de desempeño en el ensayo Desempeño Código Desempeño Técnico Desempeño Analítico Desempeño Interpretativo % final Excelente Excelente Excelente Excelente Excelente Excelente aceptable aceptable aceptable aceptable aceptable aceptable aceptable aceptable aceptable aceptable aceptable aceptable aceptable aceptable 4890610 2230609 3240603 7460611 4580602 7850715 2570604 5420617 8620608 8470613 2880714 2430905 4621236 4241238 2581340 8320601 4521235 2860806 8720612 3261339 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 83 83 83 67 67 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 100 93 93 93 93 93 93 93 93 93 100 100 93 100 93 100 100 100 100 100 100 98 98 98 98 98 98 98 98 98 93 93 91 87 85 No participa 4320633 No participa 8370630 0 0 0 0 0 0 0 0 No participa 2870631 0 0 0 0 No participa 4670632 0 0 0 0 No participa 3460707 No participa 3441016 0 0 0 0 0 0 0 0 No participa 2461237 0 0 0 0 8 FOR-R01.5040-021 V00 Grafica 1. – Resultados del desempeño en el ensayo Gráfica comparativa entre los laboratorios, por código, según los indicadores por área de desempeño. Para cada laboratorio se ubica en su línea de abscisa cada uno de los cuatro indicadores. La situación ideal es lograr 100 % en el desempeño final. 9 FOR-R01.5040-021 V00 Grafica 2. – Resultados del desempeño histórico en los ensayos 10 a 24 La gráfica muestra los resultados por ensayo y la línea de tendencia, con pendiente positiva que indica mejora continua en los últimos ensayos. 10 FOR-R01.5040-021 V00 NOTA TECNICA UTILIZACION DE MEDIO AMNIOMAXTM – II EN CULTIVOS DE CELULAS DE LIQUIDO AMNIOTICO El medio Gibco® AmnioMAX™-II, Referencia 11269-016 es un medio completo y suplementado, contiene Suero fetal de Bovino, Gentamicina y L-glutamina para maximizar la adhesión y crecimiento celular, también tiene un sistema de buffers que proporciona gran estabilidad durante la manipulación de los cultivos. Desarrollado para cultivos a corto termino de células de liquido amniótico humanas para diagnostico citogenético y procedimientos in vitro de diagnostico. Entre sus principales características se encuentra listo para su uso, certificados en calidad y funcionalidad, formulación optimizada y certificado de cada lote para esterilidad, pH y osmolaridad. Debe mantenerse almacenado congelado de -5 a -20°C protegido de la luz, pero una vez descongelado para su uso se debe almacenar de 2 a 8°C por aproximadamente 10 días. Los cultivos primarios de células de líquido amniótico son cultivadas por aproximadamente 6 días en medio completo antes de medir el número de colonias y el número total de colonias mitóticas. Referencia: Gibco- Life Technologies, Publication Number MAN 0007371. Gibco® AmnioMAX™-II Complete Medium (1X) liquid. 11 FOR-R01.5040-021 V00 INFORMACIÓN DE INTERÉS EN SALUD PÚBLICA Se presentan las tablas con la información consolidada que proveen los laboratorios de citogenética, durante el ejercicio 2013-2014. Tabla 4. – Cariotipos en sangre periférica según el resultado obtenido, por departamento, de acuerdo con información suministrada por los laboratorios. Sangre periférica Cariotipo normal Cariotipo anormal Síndrome de Down Otras anomalías ANTIOQUIA 1135 186 84 112 ATLANTICO 294 69 20 49 DISTRITO CAPITAL 5660 824 607 519 HUILA 138 27 22 5 VALLE 346 7573 73 1179 50 783 23 708 Total Esta información está actualizada a Diciembre de 2014, sujeta a cambio por revisión final en 2015. Tabla 5. – Cariotipos en líquido amniótico según el resultado obtenido, por departamento, de acuerdo con información suministrada por los laboratorios. Líquido amniótico Cariotipo normal cariotipo anormal Síndrome de Down Otras anomalías ANTIOQUIA 66 29 0 0 ATLANTICO - - - - DISTRITO CAPITAL 524 156 0 0 HUILA - - - - VALLE 341 590 59 185 0 0 Total Esta información está actualizada a Diciembre de 2014, sujeta a cambio por revisión final en 2015. Tabla 6. – Cariotipos en estados leucémicos según el resultado obtenido, por departamento, de acuerdo con información suministrada por los laboratorios. Estados leucémicos Cariotipo normal cariotipo anormal Cromosoma filadelfia Otras anomalías ANTIOQUIA 795 348 0 0 ATLANTICO DISTRITOCAPITAL 2998 1044 0 87 HUILA VALLE 238 19 Total 3793 1392 0 87 Esta información está actualizada a Diciembre de 2014, sujeta a cambio por revisión final en 2015. 12 FOR-R01.5040-021 V00 Grupo asesor de expertos de EEDDCARIO - Primer ejercicio 2014 - 2015 NOMBRES Y APELLIDOS OLGA MARIA MORENO JAVIER LÓPEZ R MONICA ZAPATA CECILIA CRANE CORREO ELECTRONICO Universidad Javeriana Asociación Colombiana de Genética Colsanitas Instuituto Nacional de Salud [email protected] [email protected] [email protected] [email protected] Haga sus comentarios sobre la información suministrada en este boletín a EEDDCARIO [email protected] 13 FOR-R01.5040-021 V00 Instituto Nacional de Salud ACTIVIDAD A DESARROLLAR 2012 -Jun-13 FOR-D01.0000-001 ENERO RESPONSABLE Inscripciones año 2015 nuevos inscritos, hay 20 Laboratorios participantes laboratorios participando Envio informe analisis de resultados 1o ensayo 2014-2015 Genetica-Cronicas Recepcion resultados 2o. Ensayo 201 4-15 Genetica-Cronicas Envio informe de analisis de resultados 2o. Ensayo 2014-15 Genetica-Cronicas Envio tercer ensayo 2014 Genetica-Cronicas Recepcion de resultados terecer ensayo 201415 Envio informe de analisis de resultados 3o. Ensayo 2014-15 Versión: 02 CRONOGRAMA DE ACTIVIDADES PROGRAMA EEDDCARIO AÑO 2015 PROCESO PLANEACIÓN INSTITUCIONAL Genetica-Cronicas Genetica-Cronicas Envio cuarto ensayo 2014-15 Genetica-Cronicas Recepción resultados cuarto ensayo 2014-15 Genetica-Cronicas TALLER ANUAL PROGRAMA EEDDCARIO Genetica-Cronicas Envio informe de analisis de resultados cuarto ensayo 2014-15 Genetica-Cronicas Envio primer ensayo 2015-16 Genetica-Cronicas Recepción resultados primer ensayo 2015-16 Genetica-Cronicas Envio informe de analisis de resultados primer ensayo 2015-16 Genetica-Cronicas Envio segundo ensayo 2015-16 Genetica-Cronicas 14 x x x x FEBRERO x x x x x MARZO x x x MAYO ABRIL x x x x x x x x x 1 de 1 JUNIO x x x x x JULIO x x x AGOSTO x x x x x SEPTIEMBRE x x x x x OCTUBRE x x x x NOVIEMBRE x x x x DICIEMBRE x x x x 15 9 21 1 19 16 10 22 10 21 9 20 30 14 FOR-R01.5040-021 V00 x