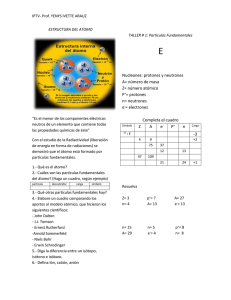
El Núcleo Atómico
Anuncio

EL NÚCLEO ATÓMICO El Núcleo Atómico Japón vuelve a la energía nuclear tras el desastre de Fukushima El país nipón reabre este martes uno de los 48 reactores paralizados desde 2011 MACARENA VIDAL LIY Tomioka (Fukushima) 10 AGO 2015 00:28 CEST88 Japón se prepara para un proceso sin precedentes: la vuelta al uso de la energía nuclear tras el parón absoluto consecuencia de la tragedia de Fukushima hace cuatro años. Aunque otros países han vivido ya la experiencia de reiniciar un reactor apagado, en ninguna parte el proceso ha alcanzado las dimensiones de Japón. Mañana, el país tiene previsto encender el primer reactor de la central de Sendai, en Kyushu, al sur del país. El primer ministro, Shinzo Abe, planea que le sigan muchos más. Su objetivo es que en 2030 la nuclear represente entre el 22% y el 24% de la cesta energética nipona. Sin embargo, la mayoría de los ciudadanos está en contra. Y ninguno más que los que dejaron sus hogares precipitadamente aquel fatídico 11 de marzo. “Es como quemarse y, pese a eso, volver a poner la mano en el fuego. Ya saben que es peligroso. Este primer ministro no piensa en las próximas generaciones, solo quiere el beneficio a corto plazo”, opina Kazawa Makoto, de 69 años. Antes del terremoto y tsunami que precipitaron el accidente de la central nuclear de Fukushima Daiichi, tenía una planta para secar pescado que empleaba a 18 personas. Gracias a un préstamo oficial ha vuelto a empezar de manera mucho más modesta en Yotsukura, a unos 40 kilómetros de la central y unos 200 al norte de Tokio, pero no consigue cubrir gastos. “Apenas vienen dos o tres personas diarias a la tienda. Y vender fuera es imposible, nadie quiere ni oír hablar de productos que vengan de Fukushima”. Makii Sugahara, de 76 años, está entre los 120.000 desplazados que aún viven en alojamientos provisionales. Realojada tras el accidente en Antonio Zaragoza López Página 1 EL NÚCLEO ATÓMICO Hisanohama, a 35 kilómetros de la central, está de acuerdo con Makoto. “Por mucho que se diga que económicamente es necesario, prefiero que no se vuelva a la energía nuclear. Si se repite un incidente, el precio es muy alto”, indica en la tienda de su amiga Erui Sato, en una calle comercial de módulos prefabricados, la primera de la zona y que se ha convertido en el centro de reuniones de los evacuados. “Era necesario crear un área de intercambio social. Antes no había otra cosa que hacer y la gente se quedaba en casa a llorar”, explica. El precio al que alude Sugahara es visible apenas a una treintena de kilómetros. En la zona de exclusión en torno a la central accidentada, de 20 kilómetros a la redonda, Tomioka fue entonces uno de los lugares más afectados y hoy es una de las localidades más retrasadas en la reconstrucción. Aún pueden verse en algunas de sus calles —coches volcados, casas destrozadas— las cicatrices del tsunami, que llegó aquí con olas de 6 metros. En todo el pueblo, donde antes habitaban 16.000 personas, solo los grillos interrumpen un silencio de tumba. Y la maleza es la solitaria habitante de unas casas donde unas bicicletas infantiles en un jardín, unos cacharros de cocina en una ventana son los únicos indicios de que hubo una vida corriente. Miles de enormes bolsas negras se acumulan en los espacios públicos. Guardan el humus, ramaje y otros residuos radiactivos que empleados del Gobierno local, en uniforme antiradiación, van apilando cuidadosamente en descampados, a la espera de que se terminen de construir los basureros radiactivos que planea el Gobierno para la zona. La Autoridad Reguladora de lo Nuclear (NRA) japonesa asegura que se tomarán todas las precauciones con la vuelta al uso de la energía atómica. “Un desastre como el que ocurrió en Fukushima no se repetirá”, ha asegurado su director, Shunichi Tanaka, al diarioNikkei Shimbun. El organismo, establecido en 2012, ha impuesto nuevos estándares de seguridad mucho más rígidos, que incluyen el establecimiento de una serie de fuentes de energía alternativas y provisiones contra los casos más extremos de terremoto o tsunami. Antonio Zaragoza López Página 2 EL NÚCLEO ATÓMICO Si todo transcurre según lo previsto, el primer reactor de Sendai, de 890 megavatios, reanudará las operaciones comerciales en septiembre. El proceso se repetirá en octubre con el segundo. De los 48 reactores nucleares que había en Japón, y que cerraron gradualmente tras el peor incidente nuclear desde el de Chernóbil en 1986, 25 en 15 plantas han solicitado reabrir. Otros cinco se han declarado obsoletas. Tan solo cinco han recibido el visto bueno de la NRA por el momento, aunque los tribunales han paralizado la puesta en marcha de uno de ellos. El Gobierno japonés alega que la energía nuclear es imprescindible para la economía del país. Importa el 90% del petróleo que consume y, aunque paliado por los bajos precios del crudo, desde el desastre nuclear el gasto en energía ha creado un fuerte déficit en la balanza comercial, que en julio se situaba en los 1,73 billones de yenes. Su plan a largo plazo prevé que para 2030 esta energía cubra casi una cuarta parte de las necesidades del país. En 2011 representaba el 39%. “Somos un país con pocos recursos energéticos. Necesitamos alcanzar un equilibrio entre el coste, la seguridad y el respeto al medio ambiente”, apunta Masakazu Toyoda, presidente del Instituto de Economía de la Energía y partidario del reencendido. El sector nuclear, asegura, ahorró cerca de 33 billones de yenes a Japón en importación de energía, un ahorro que se está dilapidando al ritmo de 3,6 billones de yenes anuales en compras de petróleo en el exterior por año de parón. Su uso también contribuirá a que Japón pueda cumplir sus objetivos de reducción de emisiones, alega. Las voces en contra alegan que los ciudadanos y las empresas ya se han acostumbrado a usar menos electricidad. “Se ha demostrado que ahorrar energía no equivale a perder calidad de vida”, sostiene Tetsunari Iida, del Instituto para Políticas Sostenibles de Energía. Aunque la gran preocupación de los ciudadanos es la seguridad. En el caso de Sendai, alegan falta de claridad en los planes de evacuación o sobre la actividad volcánica en la zona. Es una incógnita también cómo responderán los reactores tras una inactividad prolongada. Según la Antonio Zaragoza López Página 3 EL NÚCLEO ATÓMICO Asociación Nuclear Mundial, de 14 reactores que volvieron a funcionar tras cuatro años de paro en algún lugar del mundo, todos padecieron fallos técnicos o apagados de emergencia. Contenido Temático 1.- Repaso a la estructura Atómica (pág. 5) 1.1.- Modelo Atómico de Thonsom (pág. 10) 1.2.- Modelo Atómico de Rutherford (pág. 11) 2.- Estudio del Núcleo Atómico (pág. 15) 2.1.- Forma y tamaño del Núcleo (pág. 15) 2.2.- Componentes del Núcleo Atómico (pág. 16) 2.3.- Partículas y Antipartículas (pág. 27) 2.4.- Antimateria (pág. 32) 2.5.- Fuerzas de Interacción Nuclear (pág. 36) 2.5.1.- Fuerza Nuclear Fuerte (pág. 38) 2.5.2.- Fuerza Nuclear Débil (pág. 42) 2.6.- Energía del Núcleo Atómico (pág. 45) 2.7.- Reacciones Nucleares. Radiactividad (pág. 47) 2.7.1.- Radiactividad Natural (pág. 50) 2.7.1.1.- Radiación alfa (pág. 50) 2.7.1.2.- Radiación beta (pág. 51) 2.7.1.3.- Radiación gamma (pág. 52) 2.7.1.4.- Series Radiactivas (pág. 52) 2.7.1.5.- Datación. Prueba del Carbono-14 (54) 2.7.2.- Radiactividad Artificial (pág. 55) 2.8.- Reacciones Nucleares (pág. 60) 2.8.1.- Reacciones Nucleares de Fisión (pág.61) 2.8.2.- Reacciones Nucleares de Fusión (pág. 68) 2.9.- Estructura del Núcleo Atómico (pág. 74) 2.9.1.- Modelo de Capas (pág. 74) 2.9.2.- Modelo de la Gota Líquida (pág. 75) Antonio Zaragoza López Página 4 EL NÚCLEO ATÓMICO 1.- Repaso a la Estructura Atómica Si miramos a nuestro alrededor lo que vemos es Materia. La Materia está constituida por compuestos químicos, los compuestos químicos por moléculas (unidad más simple del compuesto químico en cuestión que goza de las propiedades físicas y químicas de ese compuesto) y las moléculas por ATOMOS. ¿Qué son los átomos? La Teoría Atómica de Dalton pudo explicar las leyes Ponderales (cantidades en masa de los componentes de una reacción química) de las reacciones químicas. Fue publicada en 1803 y establece los siguientes postulados: 1.- Todos los elementos químicos están constituidos por partículas discretas, invisibles e indivisibles llamadas átomos.. 2) Los átomos de un mismo elemento son idénticos en todas sus propiedades, especialmente en tamaño y masa. 3) Los átomos de elementos diferentes son totalmente diferentes en todas sus propiedades. 4) Durante las reacciones químicas, existe un reordenamiento de átomos, sin que el átomo se divida o destruya. La molécula del compuesto resulta entonces de la superposición de átomos de elementos diferentes. 5. Los átomos de dos elementos pueden combinarse en mas de una relación entera y sencilla para formar más de un compuesto. El primer y segundo postulado de la teoría de Dalton no son totalmente correctos, no porque se equivocará en sus investigaciones sino por la razón de que en 1803 no eran conocidos los electrones y protones. Antonio Zaragoza López Página 5 EL NÚCLEO ATÓMICO Sin embargo fue el primero en utilizar, sin saberlo, el concepto de Partícula Elemental al considerar que el átomo era indivisible: Las partículas elementales son los constituyentes elementales de la materia, más precisamente son partículas que no están constituidas por partículas más pequeñas ni se conoce que tengan estructura interna.. Posteriores investigaciones dieron luz a las partículas elementales: CIENTÍFICO AÑO NOMBRE MASA(Kg) C. ELÉCTRICA THOMSON 1897 Electrón (e-) 9,1 . 10-31 1,602 . 10-19 C (-) RUTHERFORD 1909 Protón (p+) 1,67 . 10-27 1,602 . 10-19 C (+) CHADWICK Neutrón (no) 1,675 . 10-27 1932 0,00 La primera evidencia de la existencia de las partículas elementales como constitutivas de los átomos y por tanto de que los átomos no eran indivisibles como postulaba la teoría atómica de Dalton, se obtuvo de los estudios de la conductividad eléctrica de gases a bajas presiones. Los gases son aislantes para voltajes bajos, sin embargo, frente a voltajes elevados se vuelven conductores. Cuando en un tubo de vidrio que contiene un gas se hace parcialmente el vacío y se aplica un voltaje de varios miles de voltios, fluye una corriente eléctrica a través de él. Asociado a este flujo eléctrico, el gas encerrado en el tubo emite unos rayos de luz de colores, denominados "rayos catódicos", que son desviados por la acción de los campos eléctricos y magnéticos. Para estudiar las propiedades de los rayos catódicos, el científico inglés Joseph John Thomson (1856-1940) diseñó un dispositivo formado por un tubo de vacío en cuyos extremos se situaban dos electrodos metálicos a los que se aplicaba una diferencia de potencial elevada. Los rayos catódicos emergentes del cátodo se hacían pasar por un colimador para limitar la anchura del haz y, después, por unas placas metálicas en las que se aplicaba un campo eléctrico. Finalmente, los rayos se proyectaban sobre una pantalla fluorescente: Antonio Zaragoza López Página 6 EL NÚCLEO ATÓMICO Con este esquema, Thomson observó que el campo eléctrico desviaba los rayos catódicos en sentido vertical hacia la placa positiva. Ello demostraba la carga eléctrica negativa inherente a estos rayos y la existencia de una masa y de la consiguiente inercia, que impedía que fueran absorbidos por la placa. Por tanto, debía existir una partícula elemental constituyente de los rayos catódicos, a la que se llamó "electrón"(e). Thomson determinó el valor de la relación entre la carga "e" y la masa "m " del electrón, que hoy día se acepta como: e / m = 1,758796 . 1011 C . Kg-1 C = Culombios (Unidad de carga elécrica) Experiencia de Millikan Después del descubrimiento de Thomson sobre la relación carga-masa del electrón, sólo restaba determinar el valor de una de estas magnitudes para conocer las propiedades básicas de esta partícula elemental. De ello se encargó, tras varios intentos aproximativos de otros investigadores, el estadounidense Robert A. Millikan (18681953). Entre 1909 y 1913, Millikan perfeccionó un complejo montaje experimental, basado en esencia en el uso de un modelo en el que la aplicación de un campo eléctrico intenso entre las placas de un condensador permite mantener inmóvil y suspendida una gotita de Antonio Zaragoza López Página 7 EL NÚCLEO ATÓMICO aceite por equilibrio de las fuerzas gravitatoria y electrostática que actúan sobre ella. Tras arduas pruebas experimentales, Millikan logró determinar la carga del electrón conociendo la masa de la gota y la intensidad del campo eléctrico aplicado. Hoy día, el valor admitido de esta carga es -19 igual a qe = - 1,60210 · 10 C (valor negativo debido a la desviación de los rayos Canales dentro de un campo magnético y hacia el polo positivo). A raíz de ello y de la relación de Thomson puede deducirse la masa del -31 electrón, que resulta m e = 9,1091 · 10 kg. El descubrimiento del protón El físico alemán E. Goldstein en 1886 realizó algunos experimentos con un tubo de rayos catódicos con el cátodo perforado. Observó unos rayos que atravesaban al cátodo en sentido contrario a los rayos catódicos. Recibieron el nombre de "Rayos Canales". El estudio de estos rayos determinó que estaban formados por partículas de carga positiva. Esto aclaró que las partículas salían del seno del gas y no del electrodo positivo. En el año 1918 Rutherford descubrió que cuando se disparan partículas alfa (He+2) contra un gas de nitrógeno, sus detectores de centelleo muestran los signos de núcleos de hidrógeno. Rutherford Antonio Zaragoza López Página 8 EL NÚCLEO ATÓMICO determinó que el único sitio del cual podían provenir estos núcleos era del nitrógeno y que por tanto el nitrógeno debía contener núcleos de hidrógeno. Por estas razones Rutherford sugirió que el núcleo de hidrógeno, que en la época se sabía que su número atómico (Z) era 1, debía ser una partícula elemental. Se consiguió aislar la partícula elemental positiva o "protón", cuya carga es la misma que la del -19 electrón pero positiva (qp = 1,60210 · 10 C ) y su masa es 1837 veces mayor a la me- (me- = 9,1 . 10-31 Kg). Enlazar online para visualizar los videos Descubrimiento del electrón http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_mate ria/curso/materiales/atomo/catodicos.htm El descubrimiento del electrón http://www.hiru.com/fisica/el-descubrimiento-del-electron Descubrimiento del protón http://bibliotecadigital.ilce.edu.mx/sites/ciencia/volumen2/ciencia3/068/ htm/sec_8.htm Descubrimiento del protón http://recursostic.educacion.es/secundaria/edad/3esofisicaquimica/3qui ncena5/3q5_contenidos_2d.htm Descubrimiento del Neutrón Se sabía que el átomo de hidrógeno contenía solamente un protón, y que el átomo de helio contenía dos protones. Por tanto, la relación entre la masa de un átomo de helio y un átomo de hidrógeno debería ser 2:1. Sin embargo, en realidad la relación es 4:1. Rutherford y otros investigadores habían propuesto que debería existir otro tipo de partícula elemental, hecho que el físico inglés James Chadwick probó en 1932. Antonio Zaragoza López Página 9 EL NÚCLEO ATÓMICO Cuando Chadwick bombardeó una delgada lámina de berilio con partículas alfa (He+2), el metal emitió una radiación de muy alta energía, similar a los rayos Gamma (γ) Experimentos posteriores demostraron que esos rayos realmente constan de un tercer tipo de partículas, que Chadwick llamó "neutrones" debido a que se demostró que eran partículas eléctricamente neutras con una masa ligeramente mayor que la masa de los protones ( mp+ = 1,67 . 10-27 Kg) . El misterio de la relación de las masas ahora podía explicarse. En el núcleo de helio existen dos protones y dos neutrones, mientras que en el núcleo de hidrógeno hay sólo un protón y no hay neutrones (isótopo Protio del Hidrógeno, 1H); por tanto, la relación es 4:1. Enlazar online para visualizar los videos Descubrimiento el neutrón http://quimica.laguia2000.com/general/descubrimiento-del-neutron Descubrimiento del neutrón http://www.nocturnar.com/forum/ciencia/439082-descubrimiento-delneutron.html El electrón, el protón y el neutrón son los componentes fundamentales del átomo. Veremos a continuación la distribución de estas partículas en el átomo, es decir, estudiaremos los diferentes Modelos Atómicos. 1.1.- Modelo Atómico de Thomson En 1904 Joseph John Tomson dio a conocer su modelo atómico también llamado como "pastel de pasas". En dicho modelo, el átomo está compuesto por electrones, de carga negativa, en un átomo positivo, como pasas en un pastel. Las pasas son los electrones y el bizcocho los protones. Se pensaba que los electrones se distribuían Antonio Zaragoza López Página 10 EL NÚCLEO ATÓMICO uniformemente alrededor del átomo. Los protones se consideraban como una sopa de carga positiva o como una nube de carga positiva. El modelo atómico de Thomson tiene el inconveniente de no incorporar al neutrón ( no se había descubierto todavía) en la estructura del átomo. Enlaces Modelo atómico de Thomson http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_mate ria/curso/materiales/atomo/mod_thom.htm http://www.deciencias.net/simulaciones/quimica/atomo/rutherford.htm Antonio Zaragoza López Página 11 EL NÚCLEO ATÓMICO 1.2.- El Experimento de Ernest Rutherford . Modelo Atómico de Rutherford Desde principios de 1900 ya se conocían las siguientes características de los átomos: a) Contienen electrones b) Contienen protones c) Contienen neutrones d) Son eléctricamente neutros En 1910 Rutherford, utilizó partículas alfa (He+2) para demostrar la estructura de los átomos. Rutherford efectuó una serie de experimentos utilizando láminas muy delgadas de oro y de otros metales, como blanco de partículas "α" provenientes de una fuente radiactiva. Antonio Zaragoza López Página 12 EL NÚCLEO ATÓMICO Ellos observaron que la mayoría de las partículas "α" atravesaban la lámina sin desviarse, o bien con una ligera desviación. De vez en cuando, algunas partículas alfa eran desviadas de su trayectoria con un gran ángulo. En algunos casos, las partículas alfa regresaban con la misma dirección pero sentido contrario hacia la fuente radiactiva. Tiempo después, Rutherford pudo explicar los resultados del experimento de la dispersión de partículas "α" utilizando un nuevo modelo de átomo. De acuerdo con Rutherford, la mayor parte de los átomos debe ser espacio vacío. Esto explica por qué la mayoría de las partículas "α" atravesaron la lámina de oro sufriendo poca o ninguna desviación. Rutherford propuso que las cargas positivas de los átomos estaban concentradas en un denso conglomerado central dentro del átomo, que llamó "núcleo". Cuando una partícula “α" (positiva) pasaba cerca del núcleo, actuaba sobre ella una gran fuerza de repulsión, lo que originaba una gran desviación de la partícula "α". Una gran desviación también podría ser producida por la atracción ente las partículas "α" (positivas) y los electrones (negativos) de la Corteza Electrónica. Más aún, cuando una partícula “α” incidía directamente sobre el núcleo, experimentaba una repulsión tan grande que su trayectoria se invertía por completo. Antonio Zaragoza López Página 13 EL NÚCLEO ATÓMICO Las desviaciones de las partículas "α" eran debidas, según Rutherford, a que el núcleo estaba cargado eléctricamente con carga positiva. Por lo tanto en el núcleo se situaban los protones. También se podía dar la circunstancia de que las partículas "α" no atravesaran el núcleo por posibles choques inelásticos quedando incrustadas en el núcleo. Esta situación requería que el núcleo contuviera una gran cantidad de masa con respecto al resto del átomo, lo que incluía en el "Nucleo" los protones y neutrones. Sabemos pues que las partículas del "núcleo" tienen: a) Carga positiva proporcionada por los protones b) Otros experimentos determinaron que los protones tienen la misma cantidad de carga eléctrica que los electrones, pero de signo contrario, y que su masa es de 1,67262 × 10-27 Kg. Aproximadamente 1840 veces la masa de los electrones. Hasta este punto, los científicos visualizaban el átomo de la siguiente manera: a) La masa del núcleo constituye la mayor parte de la masa total del átomo. En esta masa intervienen la masa del protón y del neutrón b) El núcleo ocupa solamente 1/1013 del volumen total del átomo c) El radio de un átomo es aproximadamente de 100 pm (picómetro = 1pm = 1 . 10-12 m), mientras que el radio del núcleo atómico es solamente de 0,005 pm. d) Los protones están confinados en el núcleo del átomo e) Los neutrones se encuentran en el núcleo del átomo Antonio Zaragoza López Página 14 EL NÚCLEO ATÓMICO f) Los electrones giran alrededor del núcleo describiendo órbitas circulares y a cierta distancia de él constituyendo la Corteza Electrónica. Modelo atómico de Rutherford: Enlazar online para visualizar los videos Video: Modelo Atómico de Rutherford:Video: Experiencia de https://www.youtube.com/watch?v=Pc0LWkUWPI8 Video: Experiencia de Rutherford https://www.youtube.com/watch?v=i3-qchO5RbM Video: Modelo atómico de Rutherford https://www.youtube.com/watch?v=QEGOI3k0VV4 Enlaces https://www.tplaboratorioquimico.com/quimica-general/teoriaatomica/el-experimento-de-ernest-rutherford-el-proton-y-elnucleo.html http://www.bioygeo.info/pdf/Experimento_Rutherford.pdf Antonio Zaragoza López Página 15 EL NÚCLEO ATÓMICO http://www.fullquimica.com/2011/03/teoria-atomica-molecular-dedalton-1808.html Bueno ya estamos donde queremos estar. El átomo consta de dopartes: Todo lo que se ha estudiado a lo largo de la E.S.O. y del Bachillerato sobre Química se ha basado en el estudio de los electrones, es decir, de la Corteza Electrónica. Pero ¿que sabemos del Núcleo? ¿Como es posible que en el núcleo existan los protones con la misma carga eléctrica positiva y no se repelan saliendo del núcleo ?. Hemos llegado al objetivo de este trabajo. El Estudio del Núcleo Atómico.. 2.- Estudio del Núcleo Atómico 2.1.- Forma y Tamaño del Núcleo Rutherford mediante el experimento que lleva su nombre determinó en el átomo: a) La Corteza Electrónica en la que se distribuían los electrones describiendo orbitas circulares alrededor del Núcleo. b) El Núcleo que estaba cargado eléctricamente de forma positiva y contenía prácticamente la totalidad de la masa del átomo. La carga positiva la aportaba los protones (p+). La masa la determinaba la masa de los protones y de los neutrones(no) cuya suma recibe el nombre de Número Másico (A). La masa del átomo viene determinada por la suma de las masas de las tres partículas elementales (mp+, mno y me-) pero la masa de los electrones la podemos considerar despreciable frente a la masa de los protones y de los neutrones. La masa de los protones y neutrones es prácticamente la misma y 1835 veces mayor que la masa del electrón. La Forma del Núcleo de un átomo depende de las fuerzas electrostáticas atractivas entre los protones del núcleo (+) y los electrones (-) de la corteza electrónica. Antonio Zaragoza López Página 16 EL NÚCLEO ATÓMICO a) Si la fuerza atractiva cumple la ley de Coulomb (dos cargas eléctricas se atraen con una fuerza que es directamente proporcional al producto de las cargas e inversamente proporcional al cuadrado de la distancia que las separa): F = K . qe- . qp+ / R2 los protones se reparten en el núcleo de forma uniforme haciendo que dicho núcleo tenga forma esférica.. En el caso de los elementos químicos 1H, 8O, 20Ca, 28Ni, 50Sn y 82Pb tienen un núcleo esférico y los cercanos a ellos en su números atómicos tienen un núcleo que podemos considerar Esféricos o CASI Esféricos. b) Si la distribución de los protones no es uniforme, además de las fuerzas electrostáticas aparecen otras de efectos débiles pero lo suficiente para distorsionar la forma esférica favoreciendo la forma de Esferoides ligeramente alargados. Se han determinado un gran número de radios nucleares mediante la dispersión de las partículas "α" al incidir en núcleos de átomos metálicos obteniéndose un valor del mismo del orden de 10-14 m. Se ha llegado a la conclusión: el radio del núcleo es directamente proporcional a la raíz cúbica del número másico (A): R = R0 (A)1/3 A = Número másico Ro = Constante de proporcionalidad de valor 1,25 . 10-15 metros. Esta aproximación es válida sólo para los núcleos particularmente esféricos con un bajo A. Si el núcleo lo consideramos esférico, el volumen de la esfera viene determinado por la ecuación: V = 4/3 . π . R3 Antonio Zaragoza López Página 17 EL NÚCLEO ATÓMICO Si a esta ecuación llevamos el valor de R de la ecuación anterior tenemos que: V = 4/3 . π . ( Ro . A1/3)3 V = 4/3 . π . Ro3 . A En donde podemos apreciar que el volumen del núcleo es directamente proporcional al número másico (A) del elemento químico. La densidad nuclear (m/V) en núcleos esféricos es proporcional al número de nucleones (protones + neutrones) y tiene un valor constante 1015 veces mayor que la densidad de la materia macroscópica. Esta densidad nuclear nos aporta dos datos: a) Gran compacidad de los nucleones dentro de un núcleo. b) La materia macroscópica está esencialmente vacía, ya que la mayor parte de la masa está concentrada en los núcleos atómicos. Recordemos: El radio de un átomo es aproximadamente de 100 pm ( 1pm = 1 . 10-12 m), mientras que el radio del núcleo atómico es solamente de 0,005 pm. Enlaces https://tuylaquimica.files.wordpress.com/2011/03/nc3bacleoat.pdf http://www.biologia.edu.ar/botanica/tema9/9-1nucleo.htm http://web.educastur.princast.es/proyectos/jimena/pj_franciscga/Ruthe rford2.htm Antonio Zaragoza López Página 18 EL NÚCLEO ATÓMICO 2.2.- Componentes del Núcleo Atómico Actualmente, se sabe que las partículas elementales de los átomos: electrones, protones y neutrones son divisibles ( no son partículas elementales[1]). La duda está en identificar cuáles son las verdaderas partículas elementales. Dado que la longitud de onda de la luz es mucho mayor que el tamaño de un átomo, no es posible emplear la luz como instrumento para ver las partes que lo constituyen. [1] Las partículas elementales son los objetos más simples que se pueden concebir. En general no tienen partes ni se pueden dividir en componentes más sencillas, sin embargo los experimentos de colisiones entre partículas a muy altas energías han revelado que algunas partículas que se creían simples en realidad son compuestas y que estaban formadas por partículas más simples. Para estudiar las fuerzas nucleares, los físicos tienen que perturbar los neutrones y protones del núcleo bombardeándolo con partículas extremadamente energéticas. Estos bombardeos han revelado más de 200 partículas elementales, no todas ellas son constituyentes de los átomos, muchas de ellas proceden del choque entre partículas elementales. La mayoría de estas partículas elementales sólo existe durante un tiempo mucho menor a una cienmillonésima de segundo. Tal cantidad de entidades elementales sorprendió a los físicos, hasta que fueron capaces de comprender que muchas de esas partículas realmente no eran elementales sino compuestas constituyendo las subpartículas. Antonio Zaragoza López Página 19 EL NÚCLEO ATÓMICO Las partículas más pesadas (hadrones) y las de masa intermedia (mesones) fueron consideradas, en principio, elementales. Actualmente se sabe que son partículas compuestas. Sólo las partículas más ligeras resultaron ser elementales. Este mundo subnuclear salió a la luz por primera vez en los rayos cósmicos. Estos rayos están constituidos por partículas de muy alta energía que bombardean constantemente la Tierra desde el espacio exterior; muchas de ellas atraviesan la atmósfera y llegan incluso a penetrar en la Corteza Terrestre. La radiación cósmica incluye muchos tipos de partículas, de las que algunas tienen energías que superan con mucho a las logradas en los aceleradores de partículas. Cuando estas partículas altamente energéticas chocan contra los núcleos, pueden crearse nuevas partículas.. En el "modelo estándar", que refleja nuestro estado de conocimiento sobre los constituyentes últimos de la materia establece dos series de partículas elementales: a) Los Fermiones o "particulas de materia". b) Los Bosones, "partículas mediadoras de fuerza" o "partículas portadoras de las interacciónes fundamentales". Los Fermiones y Bosones tienen una propiedad llamada "spin" (momento angular intrínseco de rotación). Los fermiones tienen spin semi-entero y los bosones tienen un spin entero. Los Fermiones se clasifican en dos grandes grupos: a) Los Leptones b) Los Quarks Cada uno de estos dos grupos está compuesto por seis partículas elementales constituyendo 12 partículas de "materia". Los Leptones Antonio Zaragoza López Página 20 EL NÚCLEO ATÓMICO Los leptones son partículas muy ligeras que siempre interactúan por medio de la Fuerza Nuclear Débil (se verá) y si tienen carga también están bajo la acción de la interacción electromagnética, pero nunca bajo la acción de la Interacción Nuclear Fuerte (se verá). Entre los leptones nos encontramos las partículas: a) El Electrón (e-) b) El Muón (µ) c) La partícula tau (T ) (T) d) Neutrino electrónico (Ve) (Ve) e) Neutrino muónico (Vµ)(Vµ) f) Neutrino tau (VT)(VT) Enlazar vía online para visualizar los videos Video: Quarks y Leptones (Inglés subtitulado) https://www.youtube.com/watch?v=I3jtzXr69GY Video: El Electrón https://www.youtube.com/watch?v=6feftMHfPII Video: El Electrón https://www.youtube.com/watch?v=zspxN62jlvo Video: El Muón (Inglés) https://www.youtube.com/watch?v=ejcaz7wXawY&list=PLkoDUZZt7 2sSxmf1vhj-fsZdePR61ONYS Antonio Zaragoza López Página 21 EL NÚCLEO ATÓMICO Video: Los Neutrinos https://www.youtube.com/watch?v=eXDLkNL9wuw Video: Los Neutrinos https://www.youtube.com/watch?v=FO-mJHPIFdw Video: Los Neutrinos y la velocidad de la luz https://www.youtube.com/watch?v=JetgzFhQKG0 Los Quarks Los Quarks están bajo la acción de la Fuerza Nuclear Fuerte, pero no se encuentran libres en la naturaleza. Siempre están ligados con otros quarks ya sea en un barión o en un mesón. Entre los Quarks tenemos: a) Quarks up (arriba), (u) b) " down (abajo), (d) c) " charm (encantado), (c) d) " strange (estraño), (s) e) " f) " top ((cima), (t) bottom (fondo), (b) Enlazar online para visualizar el video Video: Los Quarks http://www.youtube.com/watch?v=3udGCbEfsfg&feature=results_vid eo&playnext=1&list=PLDD991B445A6FCEC8 Antonio Zaragoza López Página 22 EL NÚCLEO ATÓMICO Partículas fundamentales del Modelo Estándar LEPTONES FAMILIAS NOMBRE QUARKS SIMB. electrón e neutrinoe NOMBRE SIMB. up u ᵧ down d muon µ charm c neutrinoµ γµ estrange s 1ª e 2ª tau l top t neutrinol γe bottom b 3ª Los quarks y leptones que interaccionan entre ellos mediante el Salvo los tres neutrinos, que tienen carga eléctrica nula, las restantes 9 partículas tienen carga eléctrica. El electrón, muón y partícula tau tienen la misma carga eléctrica. Tomando como carga patrón la del electrón, la carga eléctrica de los quarks: up, charm y top es positiva e igual a 2/3 de la carga del electrón, mientras que los quarks: dow, strange y bottom tienen carga eléctrica negativa e igual a 1/3 de la carga electrónica patrón. Sólo las partículas con carga eléctrica no nula son sensibles a las fuerzas de origen electromagnético. Antonio Zaragoza López Página 23 EL NÚCLEO ATÓMICO Las partículas elementales poseen diferentes masas. Tomaremos como referencia la masa del electrón, me = 9,109 . 10-31 Kg. PARTÍCULA Muón MASA 206 > me Partícula Tau Neutrinos 3477 > me Masas NO NULAS pero desconocidas Los quarks no han sido detectados en forma libre, por el denominado efecto de confinamiento (se las observa únicamente con otras partículas) por lo que la noción de masa para los quarks es en consecuencia más compleja. Los valores que se aportan son valores aproximados: Quarks "u" 6 > me Quarks "c" 2500 > me Quarks "t" 334000 > me Quarks "d" 12 > me Quarks "s" 200 > me Quarks "b" 8400 > me Si consideramos como base el módulo de la carga eléctrica del electrón: qe = | - 1,6 . 10-19 C | = 1,6 . 10-19 C y a este valor le damos simbólicamente el valor de la unidad: | qe | = 1 podemos establecer las cargas eléctricas de los diferentes Quarks: QUARKS up (u) charm (c) top ( t) dow (d) strange (s) botton (b) Antonio Zaragoza López CARGA ELÉCTRICA + 2/3 + 2/3 + 2/3 - 1/3 - 1/3 - 1/3 Página 24 EL NÚCLEO ATÓMICO Combinaciones de tres quarks forman los Bariones (como el protón) y combinaciones de un quark y un anti-quark (se verá) forman la famila de los Mesones. Video: Quarsk y Leptones. Carga de color https://www.youtube.com/watch?v=29x-36OsUDg Video: Quarsk y Leptones https://www.youtube.com/watch?v=6TQxZ3bYxBo Los quarks se unen mediante partículas llamadas gluones. El gluón es un bosón ( incluye partículas fundamentales como fotones, gluones, bosones W y Z el bosón de Higgs), portador de la interacción nuclear fuerte. No posee masa ni carga eléctrica, pero sí carga de color ( estado cuántico). Un protón está formado por dos quarks up y un quark down. Un neutrón está formado por dos quarks down y un quark up. En las partículas compuestas de quarks, como el "protón" y el "neutrón", podemos determinar su carga eléctrica en función de la carga eléctrica de las subpartículas que las forman. Ejemplo: Protón → p+ → + 1 Protón (p+)= 2 quarks u + 1 quarks d = 2 . (+ 2/3) + (- 1/3) = = + 4/3 - 1/3 = + 3/3 = + 1 Antonio Zaragoza López Página 25 EL NÚCLEO ATÓMICO Neutrón → n0 Neutrón (no)= 2 quarks d + 1 quarks u = 2 ( - 1/3) + (+ 2/3) = = - 2/3 + 2/3 = 0 Los protones se mantienen unidos a los neutrones por el efecto de los piones ( los veremos más adelante), que son mesones compuestos, formados por parejas de quark y antiquark. El muón (µ) es esencialmente un electrón pesado, y puede tener carga positiva o negativa. Es aproximadamente 200 veces más pesado que un electrón. La partícula tau es una partícula elemental masiva que pertenece a la tercera generación de leptones ( Neutrino Tau y partícula Tau) . Su carga es negativa (T-) y su masa es de 1800 MeV/C2. El hadrón es una partícula compuesta por la unión de quarks y/o antiquarks o bien gluones como los protones y neutrones. Se encuentran afectadas por la fuerza nuclear fuerte. Los neutrinos nacen de la radiación "β". Esta radiación consiste en la liberalización de electrones procedentes del núcleo. En el núcleo NO EXISTEN ELECTORES. Cuando un neutrón se desintegra se produce un protón que queda en el núcleo y un electrón que se libera. Pero la suma de las masas del electrón y el protón resultante no es igual a la masa del neutrón. Como la masa no puede desaparecer en el universo, tiene que haber algo más que sale del neutrón cuando éste se desintegra. Ese algo más es el neutrino. Antonio Zaragoza López Página 26 EL NÚCLEO ATÓMICO Existen tres tipos de neutrinos asociados a cada una de las familias : a) Neutrino electrónico (Ve) b) Neutrino muónico (Vµ) c) Neutrino tauónico (VT) Un neutrino es una partícula de masa prácticamente nula que no tiene carga y no siente la fuerza nuclear fuerte. Debido a no sentir la fuerza nuclear fuerte ni la fuerza electrostática, es muy difícil detectarlos. Como ya se comentó los Quarks no se han podido aislar. Siempre se encuentran en grupos de a tres formando los protones y neutrones, en donde están unidos por el intercambio de gluones) o en grupos de a dos formando los mesones π y mesones K. Esta capacidad para unirse, se debe a que experimentan la acción de la Fuerza Nuclear Fuerte. Los quarks presentan las fuerzas de interacción fuerte teniendo "cargas de color" (estados cuánticos) no nulas (roja, verde o azul). Los leptones son insensibles a este tipo de fuerzas y tienen cargas de color nulas. Antonio Zaragoza López Página 27 EL NÚCLEO ATÓMICO Tanto los leptones como los quarks son además sensibles a las fuerzas derivadas de la denominada Interacción Débil. La existencia del pión fue predicha en 1935 por el físico japonés Yukawa Hideki y fue descubierto en 1947. Según la teoría más aceptada, las partículas nucleares se mantienen unidas por “fuerzas de intercambio” en las que constantemente se intercambian piones comunes a los neutrones y los protones. El pión, unas 200 veces más pesado que el electrón, puede tener carga positiva,, negativa o nula. . El pión es el nombre común que reciben tres partículas subatómicas: π0, π+ y π−. Un pión está formado por un quark y un antiquark. Hay varios piones, dependiendo de qué combinación quark/antiquark se tiene. Por ejemplo: a) Un quark up y uno antidown producen un pión de carga positiva, denotado como π+. b) Un quark down y uno antiup componen el pión de carga negativa, π-. c) Un quark up y uno antiup, o unodown , producen el pión neutro, π0. PIÓN u dd P El π0 es un poco más ligero y su desintegración produce dos fotones. Antonio Zaragoza López Página 28 EL NÚCLEO ATÓMICO El Kaón o mesón - K es una partícula subatómica compuesta por un par quark - antiquark. Pertenece a la familia de los mesones junto con el pión. Los kaones cargados tienen una composición de quarks: a) Quars up-antistrange en el kaón positivo (K+) b) Quarks antiup-strange en el kaón negativo (K-). MESON K+ U S Son realmente importantes porque introducen un nuevo número cuántico que se denomina "Extrañeza". Relacionada con el quark strange. Además del K+ y K- también existe el Ko. En total tenemos cuatro Kaones: 1 K+, 1 K- y 2 Ko. Se producen kaones cuando un pión choca con un protón en el núcleo de un átomo. La interacción nuclear fuerte entre el pión y el protón produce, en un tiempo cortísimo (unos 10-23 segundos) un par de kaones, que salen despedidos en diferentes direcciones.Fueron descubiertos experimentalmente en Manchester en 1947 al analizar La masa de los kaones (positivos y negativos) es de 493,67 MeV/c2. El Kaón neutro tiene una masa de 497,72 MeV/ C2. A partir de 1953 se pudieron producir artificialmente (los kaones), en reacciones originada en aceleradores de partículas. Antonio Zaragoza López Página 29 EL NÚCLEO ATÓMICO En Abril de 2009 descubren un quark top solitario. Los quarks top siempre se habían observado de dos en dos. La existencia de este quark confirma parámetros de gran importancia de la física de partículas, como el número total de quarks. Este hallazgo es también trascendente en la búsqueda de la partícula de Higgs,"El bosón de Higgs" o "Partícula de Dios".". Esta partícula, el bosón, explicaría como de una gran explosión (Big - Bang), con muchísima liberación de energía se podía obtener materia. Los físicos, para poder explicar los resultados de ciertas experiencias postulan la hipótesis de que los quarks podrían ser partículas compuestas formadas por una partículas elementales llamadas "preones". De los preones nada se sabe y de momento los quarks siguen siendo partículas elementales. Enlaces http://particleadventure.org/spanish/quark_funs.html http://es.wikipedia.org/wiki/Quark#Descubrimiento_experimental http://historiaybiografias.com/el_atomo1/ http://www.monografias.com/trabajos52/particulassubatomicas/particulas-subatomicas.shtml http://educativa.catedu.es/44700165/aula/archivos/repositorio/1000/1162/html/ 21_partculas_subatmicas.html http://es.gizmodo.com/el-lhc-descubre-un-nuevo-tipo-de-particulasubatomica-1717685013 http://es.slideshare.net/Rickandroller/particulas-subatmicas?related=1 2.3.- Partículas y Antipartículas Paul Dirac formuló la ecuación relativista que lleva hoy su nombre. Cuando resolvió su ecuación, Dirac se encontró con que además de describir el electrón tenía soluciones adicionales que describían otra partícula con una carga eléctrica opuesta a la del electrón. Dirac decidió que las soluciones adicionales de su ecuación describían el protón. Pero, tras un análisis más meticuloso, se hizo evidente que las Antonio Zaragoza López Página 30 EL NÚCLEO ATÓMICO partículas que describían las soluciones adicionales tenían que tener exactamente la misma masa que el electrón, circunstancia que no se cumple ( mp+ > 1800 me-). Las soluciones adicionales tenían que corresponder a una partícula completamente nueva de la misma masa que el electrón, pero de carga opuesta. Esta partícula fue descubierta en 1932 por Carl Anderson. La nueva partícula es la antipartícula del electrón que se conoce con el nombre de "positrón" (e+). La primera antipartícula compuesta, el "antiprotón" (p-), fue descubierta por Emilio Segré y Owen Chamberlain, en 1955. Ambos ganaron por ello el premio Nobel de Física, en 1959. Conocemos que toda la materia está formada por unas “pocas” partículas, fundamentalmente: protones, neutrones y electrones (hay muchas otras, pero atengámonos a las básicas). Cada una de ellas tiene una masa, carga (positiva, negativa o neutra) y spin (algo así como un “giro” de la partícula) propio, y diferente de el de otra partícula. Las antipartículas tienen la misma masa y el mismo spin que sus compañeras, las partículas ordinarias, pero cargas inversas. Cuando una estrella es muy masiva, su núcleo puede producir tanta luz de rayos gamma (radiación electromagnética) que parte de la energía de la radiación es convertida en pares de partículas y antipartículas. Todos los quark posee una antipartícula denominada antiquark. Lo mismo sucede con los leptones. La existencia de antipartículas parece ser un capricho de la naturaleza. Para las antipartículas muchas cosas suceden al contrario de sus opuestas. ¿Todo tiene un opuesto? ¿Para cada partícula existe una opuesta?. No todas las partículas tienen sus opuestas. El fotón no tiene un antifotón. Antonio Zaragoza López Página 31 EL NÚCLEO ATÓMICO Todos los fermiones tienen antipartículas, pero no todos los bosones tienen antipartículas. No existe una regla lógica que explique esto. Son pocas las partículas que no tienen su opuesto como una posibilidad de suceder. ¿Cómo podemos explicar que una partícula que no tiene carga pueda tener antipartícula?. Este es el caso del neutrón, no tiene carga eléctrica pero si tiene antipartícula, el antineutrón. Podemos explicarlo por dos mecanismos distintos: a) El neutrón tiene carga cero. Se trata de una partícula compuesta de tres quarks, su antipartícula se constituiría por la unión de los antikuarks correspondientes. El neutrón y antineutron se diferencias en sus quarks b) El neutrón no tiene carga eléctrica, pero en cambio posee un campo magnético que apunta en una determinada dirección. Y existe el "antineutrón", que tampoco tiene carga eléctrica pero cuyo campo magnético apunta en la dirección opuesta. Considero que la primera explicación es la correcta porque la partícula y antipartícula no se diferencian en el spin.. Antonio Zaragoza López Página 32 EL NÚCLEO ATÓMICO Partículas y Antipartículas: PARTICULA C. ELÉCTRICA MASA(MeV) ᵧ FOTÓN ( ) NUCLEONES PROTÓN (p+) NEUTRÓN(nO) LEPTONES ELECTRÓN (e-) MUÓN (µ-) MUÓN (µ+) TAU (T-) TAU (T+) NEUTRINO (Ve) NEUTRINO (Vµ) NEUTRINO (VT) QUARKS up (u) charm (c) top (t) dow (d) strange (s) botton (b) MESONES PIÓN (π+) PIÓN (µ-) PIÓN (π0) KAÓN (K+) KAÓN (K0) KAÓN (kO) KAÓN (K-) ANTIPARTÍCULA C. ELÉC. MASA(MeV) 0 ᵧ +1 0 938,26 939,55 ANTIPROTÓN ( p ) ANTINEUTRÓN ( n ) -1 -1 +1 -1 +1 0 0 0 0,511 105,659 105,659 1800 1800 < 2 . 10-4 < 2 . 10-4 < 2 . 10-4 0 + 2/3 + 2/3 + 2/3 - 1/3 - 1/3 - 1/3 +1 -1 0 +1 0 0 -1 6 > me 2500 > me 334000 > me 12 > me 200 > me 8400 > me 139,58 139,58 134,97 493,82 497,76 497,76 493,76 POSITRÓN (e+) MUÓN (µ+) MUÓN (µ-) TAU (T+) TAU (T-) NEUTRINO (Ve) NEUTRINO (Vµ) NEUTRINO (VԎ) -1 0 +1 +1 -1 +1 -1 0 0 0 938,26 939,55 0,511 105,659 105,659 1800 1800 < 2 . 10-4 < 2 . 10-4 < 2 . 10-4 up ( u ) charm ( c ) top ( t ) dow ( d ) strange ( s ) botton ( b ) - 2/3 - 2/3 - 2/3 + 1/3 + 1/3 + 1/3 6 > me 2500 > me 334000 > me 12 > me 200 > me 8400 > me PIÓN (π-) PIÓN (µ+) PIÓN (π0) KAÓN (K-) KAÓN (KO) KAÓN (kO) KAÓN (k+) -1 +1 0 -1 0 0 +1 139,58 139,58 139,58 493,82 497,76 497,76 493,82 La forma más fácil de separar partículas opuestas es a través del uso de campos electromagnéticos. Bajo la acción del campo electromagnético una determinada variedad se desvía hacia la izquierda en tanto que la otra se desvía hacia la derecha. Video: Antipartícula https://www.youtube.com/watch?v=QEIxWhH2n1Y ¿Qué ocurriría si tenemos juntas partículas y antipartículas? Si electrones y positrones chocan entre sí se aniquilan emitiendo energía en forma de radiación en el proceso. Esta energía proviene de la masa de las partículas y antipartículas. Como sabemos, la masa es una Antonio Zaragoza López Página 33 EL NÚCLEO ATÓMICO forma de energía, lo que fue señalado por Albert Einstein en su teoría especial de la relatividad hace poco más de cien años ( E = m . c2). Transformaciones de las partículas Una partícula puede convertirse en otra, pero siempre que se forma una partícula sin la existencia previa de otra, es decir, tiene que formarse simultáneamente una antipartícula. He aquí un ejemplo. Un neutrón puede convertirse en un protón, lo cual es perfectamente admisible, porque lo único que ha sucedido es que una partícula se ha convertido en otra. Pero en esa conversión se forma también un electrón. Es decir, una partícula se ha convertido en dos. Para contrarrestar esa segunda partícula se forma una diminuta antipartícula llamada «antineutrino». n0 → p+ + e- + antineutrino Una partícula (el neutrón) se ha convertido en otra (el protón) más un par partícula / antipartícula (el electrón y el antineutrino). A partir de energía se pueden formar pares partícula / antipartícula, que a su vez pueden volver a convertirse en energía. De energía no podemos sacar una partícula sola, ni una única antipartícula, pero sí un par. Como la propia energía está formada de fotones, se plantea entonces el problema de si el fotón es una partícula o una antipartícula. No parece que haya ningún modo de convertir un fotón en un electrón, por lo cual no puede ser una partícula; ni tampoco de convertirlo en un antielectrón, por lo cual tampoco puede ser una antipartícula. Sin embargo, un fotón de rayos gamma suficientemente energético, sí puede convertirse en un par electrón / antielectrón. Parece, pues, que el fotón no es ni una partícula ni una antipartícula, sino un par partícula / antipartícula. Este par se anula convirtiéndose en energía (fotón). Todo fotón es a la vez un antifotón, o digámoslo así, un fotón es su propio opuesto. Antonio Zaragoza López Página 34 EL NÚCLEO ATÓMICO Enlaces http://www.sabermas.umich.mx/archivo/seccionesanteriores/articulos/75-numero-10/154-el-mundo-de-laantimateria.html http://www.academico.cecyt7.ipn.mx/FisicaIV/unidad3/particulas.htm http://www.fisicanet.com.ar/monografias/monograficos5/es099_las_ant iparticulas.php https://universocuantico.wordpress.com/2009/04/18/antiparticulasesas-cosas-raras-i/ http://www.quantum-rd.com/2009/12/uno-de-los-primeros-exitos-dela-teoria.html http://quimica.laguia2000.com/elementos-quimicos/antiparticulas 2.4.- Antimateria En 1928, el físico inglés Paul Dirac fue el primero en combinar la relatividad y la mecánica cuántica ( visto en el apartado anterior) , y así llegó a una ecuación que describe con precisión al electrón. Pero la ecuación de Dirac también predice la existencia de una partícula con las mismas propiedades que el electrón, pero con carga positiva: una antipartícula. Y no sólo debía existir una antipartícula para el electrón, sino también para el resto de partículas conocidas. El descubrimiento en 1932 del positrón, la antipartícula del electrón, confirmó la teoría de Dirac. Podemos decir que las partículas ordinarias forman la materia que nos rodea, también sus correspondientes antipartículas podrían formar átomos de antimateria; es decir, positrones que dan vueltas alrededor de un núcleo compuesto por antiprotones y antineutrones. Antonio Zaragoza López Página 35 EL NÚCLEO ATÓMICO Enlazar online para visualizar los videos Video: Antimateria https://www.youtube.com/watch?v=6uFBDotF7IM Video: Antimateria https://www.youtube.com/watch?v=sYYN57kegXU Sabemos que el sistema partícula - antipartícula no existe puesto que al chocar entre ellas se destruyen y se genera energía. ¿ Si todas las partículas tienen una antipartícula, como es posible que exista el Universo? Según la teoría, el Big Bang debió haber creado igual cantidad de materia y antimateria, las cuales, en cuanto se encontraran, se aniquilarían mutuamente y produciendo gran cantidad de energía. Nada más que energía. No existiría la materia. Para poder salir de la ambigüedad recurrimos al hecho de que los cálculos indican que desde el principio existió una partícula extra de materia por cada mil millones de pares de materia y antimateria. Con esta partícula extra de materia empezó a formarse el Universo tal y como lo conocemos hoy. Estas partículas supervivientes se unieron luego para formar los primeros átomos, que más tarde constituirían las primeras estrellas y galaxias. Según estos cálculos la antimateria no existe en el Universo, NO existen las antipartículas y esto no es así actualmente. Conocemos partículas y antipartículas. Debe existir alguna fuente de antipartículas. Las fuentes de la antipartículas son: a) Las antipartículas caen constantemente a la Tierra en forma de rayos cósmicos. Parece haber evidencia de producción de antimateria en las tormentas eléctricas. b) La desintegración radiactiva de algún elemento químico puede producir antipartículas. El isótopo del potasio 40K produce en su desintegración positrones (e+). Antonio Zaragoza López Página 36 EL NÚCLEO ATÓMICO c) En los en los aceleradores de partículas se puede generar antimateria. Los primeros intentos se remontan a principios de la década de 1990 en el CERN ( Organización Europea de Investigaciones nucleares). El método consistía en hacer pasar un antiprotón muy veloz cerca de un núcleo atómico pesado lo que de producía un par electrón-positrón. En este hipotético caso, el antiprotón podía unirse con el positrón y formar un átomo de antihidrógeno. Después de muchos intentos e introducción de trampas para guardar las antipartículas los investigadores han logrado aislar la antimateria en dispositivos llamados trampas de Penning, que son trampas iónicas parecidas a pequeños aceleradores, dentro de los cuales las partículas pueden permanecer en movimiento mientras los campos eléctricos impiden que choquen contra las paredes. Los antiprotones que quedan presos llegan a zonas conocidas como cinturones de radiación de Van Allen. Los científicos en CERN utilizan un desacelerador de partículas para disminuir la velocidad de antiprotones y posicionarlos junto con positrones. Desde 2009, el equipo ha sido capaz de crear átomos de antihidrógeno y mantenerlos por 17 minutos. Incluso, en enero de 2014, crearon un rayo de antihidrógeno en el que se identificaron 80 átomos de antimateria. Aplicaciones de la Antimateria Dado que una pequeña cantidad de antimateria es capaz de producir grandes cantidades de energía, la propulsión de vehículos impulsados por ella es hipotéticamente posible. La limitación, como hemos visto, es encontrar o disponer de suficiente antimateria. Existen experimentos que simulan propulsión y almacenamiento, pero están en una fase sumamente temprana de desarrollo. Al ser la antimateria existente en el universo muy escasa para poder utilizarla como fuente de energía tenemos que fabricarla. La energía de fabricación de una antipartícula es muy superior a la que se libera en el choque entre partícula y antipartícula. Sería un proceso económicamente no factible. Antonio Zaragoza López Página 37 EL NÚCLEO ATÓMICO En medicina se utiliza la antimateria en la topografía de emisión de positrones (PET). Se utilizan los positrones para producir imágenes de alta resolución del cuerpo. Los positrones que emiten isotopos radioactivos se alían con sustancias químicas como la glucosa, las cuales son inyectadas en el torrente sanguíneo, donde los isotopos son liberados al ser procesados por el cuerpo. Al liberarse son aniquilados, lo que produce rayos gama, utilizados para construir las imágenes. Enlazar online para visualizar los videos Video: Antimateria y su fabricación https://www.youtube.com/watch?v=6uFBDotF7IM Video: Antimateria https://www.youtube.com/watch?v=dkY8tXQPxAM Video: Antimateria https://www.youtube.com/watch?v=sYYN57kegXU Video: Cinco características de la Antimateria https://www.youtube.com/watch?v=1XHJIYkcnZ8 Enlaces http://www.comoves.unam.mx/numeros/articulo/157/antimateria-elotro-lado-del-espejo http://pijamasurf.com/2015/05/10-cosas-que-tal-vez-no-sabes-sobre-laantimateria/ http://www.batanga.com/curiosidades/5957/es-posible-crearantimateria http://www.oei.es/divulgacioncientifica/noticias_548.ht http://hipertextual.com/2015/11/antimateria-antiprotones-interaccion http://www.cienciakanija.com/2015/11/08/se-mide-la-fuerza-quemantiene-unida-a-la-antimateria/ Antonio Zaragoza López Página 38 EL NÚCLEO ATÓMICO 2.5.- Fuerzas de Interacción Nuclear En el campo de la Física se estudian CUATRO tipos de Interacción o Fuerzas existentes en la Naturaleza: La mayoría de los fenómenos que ocurren en la naturaleza: a) El movimiento de los planetas, cometas y otros astros en torno al Sol b) El movimiento de las cargas eléctricas en un conductor que inducen a un campo magnético c) Las fuerzas de atracción que experimentan los electrones en torno al núcleo Pueden ser explicados por estos tipos de Fuerzas. Estas fuerzas se clasifican en: a) Fuerza de Gravedad b) Fuerza Electrostática o Electromagnética c) Fuerza Nuclear Fuerte d) Fuerza Nuclear Débil En el mundo del átomo “las partículas elementales se clasifican de acuerdo con sus interacciones”. por lo tanto existen para cada interacción, un tipo de partícula específica (Young y Freedman) Fuerza de la Gravedad Todos los cuerpos son atraídos por una fuerza que es directamente proporcional a sus masas, e inversamente proporcional al cuadrado de la distancia que los separa. La Antonio Zaragoza López Página 39 EL NÚCLEO ATÓMICO fuerza gravitacional es la causante de que los cuerpos caigan y del movimiento de los cuerpos celestes que se encuentran en el universo. F = G . M . m / R2 La fuerza gravitacional tiene radio de acción infinito. Fuerza electrostática o Electromagnética Este tipo de fuerza explica las fuerzas de atracción y de repulsión que existen entre cuerpos cargados eléctricamente. Si dichos cuerpos o partículas tienen el mismo signo de las cargas (positivas o negativas) existirá una fuerza de repulsión. Si las cargas son de distinta naturaleza aparecen la fuerza de atracción. Fuerza Nuclear Fuerte Es la interacción que permite mantener los nucleones (protones y neutrones) unidos. Mantiene unidos a los quarks para formar hadrones, (protones, neutrones y mesones) dando estabilidad al núcleo atómico y como consecuencia hace posible la existencia de la materia. Fuerza Nuclear Débil Este tipo de fuerza es responsable de la desintegración "β" de los núcleos de los átomos, es decir, de que un quark de un tipo se transforme en un quark de otro tipo. Es una fuerza más débil que las tres anteriores lo que permite las emisiones radiactivas. La desintegración "β" libera electrones del núcleo atómico. Enlazar online para visualizar los videos Video: Fuerzas Fundamentales de la Naturaleza https://www.youtube.com/watch?v=xBFxNWq8vZE Dentro del Tema estudiaremos las que actúan a nivel nuclear. Antonio Zaragoza López Página 40 EL NÚCLEO ATÓMICO Enlaces http://www.batanga.com/curiosidades/2011/06/07/las-4-fuerzasfundamentales-de-la-fisica-actual http://fuerzasfundamentales.blogspot.com.es/2011/10/introduccionfuerzas-fundamentales-de.html http://fm-fuerzas.blogspot.com.es/p/conclusion.html 2.5.1.- Fuerza Nuclear Fuerte El modelo atómico propuesto por Ernest Rutherford predecía que los protones y neutrones estaban agrupados en el núcleo atómico. Los protones tienen carga eléctrica positiva. Los protones generarían entre ellos una fuerza electrostática de REPULSIÓN. Estas fuerzas de repulsión no permitirían la formación de núcleos de átomos de elementos químicos y por lo tanto la existencia de la materia. Sin embargo los protones no se repelen entre sí desobedeciendo la ley de Coulomb. Sabemos a ciencia cierta que los núcleos atómicos existen, luego debe de existir algún tipo de fuerza que anule o equilibre las fuerzas de repulsión. La respuesta llegó con la aparición de la Fuerza Nuclear Fuerte., la cual predomina sobre la anterior y hace posible que se mantengan unidos los componentes nucleares. Esta fuerza actúa indistintamente entre dos nucleones cualesquiera, protones o neutrones (protón - protón; protón - neutrón; neutrón - neutrón)). Su alcance es del orden de las dimensiones nucleares. Recordemos que los protones y neutrones están constituidos por los quarks, por lo tanto las Fuerzas de Interacción Fuerte mantienen unidos a los quarks. La teoría de la Cromodinámica Cuántica establece que las fuerzas de Interacción Nuclear Fuerte están constituidas por Cargas de Color ( las cargas de color no tienen nada que ver con el concepto que tenemos de color, se trata de estados cuánticos). Antonio Zaragoza López Página 41 EL NÚCLEO ATÓMICO En los años 30 (1930) el científico Yukawa publicó un artículo en el que planteó la hipótesis que explicara la Fuerza Nuclear Fuerte. Este tipo de fuerza se transmitía a través de partículas. El transmisor de la Fuerza Nuclear Fuerte debía ser una verdadera partícula. La idea se basa en que si tenemos un protón y otro cerca de él, para que el primero atraiga al segundo el primer protón debe crear una partícula lanzarla hacia el segundo y este recogerla. Estas partículas son los gluones, que también tienen carga de color y por lo tanto pueden interactuar entre ellos. La unión de partículas en el núcleo atómico se produce mediante las cargas de color de los quaks y antiquarks. Cuando un quark lanza un gluón a otro quark se tranforma en su antiquarks. La fuerza entre partículas con carga de color es la más intensa de la cuatro fuerzas elementales de la Naturaleza (gravitatoria, electrostática y Fuerza de Interacción Débil), llegando a crear lo que se conoce como " confinamiento de color". Los gluones son las partículas portadoras de la Fuerza Nuclear Fuerte: Enlazar online para visualizar los videos Video: Fuerza Nuclear Fuerte. Los gluones https://www.youtube.com/watch?v=g-ZHRzC_l7M Video: Intercambio de gluones entre quarks https://www.youtube.com/watch?v=cvTIqHdTQhg Los quarks pueden presentar seis tipos de carga de color: rojo, azul, verde, antirojo, antiazul y antiverde. Las cargas antiroja, antiazul y Antonio Zaragoza López Página 42 EL NÚCLEO ATÓMICO antiverde están relacionadas con las correspondientes roja, azul y verde. Unas serían las cargas positivas clásicas y las otras las negativas. Los gluones tienen una carga de color resultante de la combinación color - anticolor, por ejemplo, se puede tener un gluón rojo-antiazul o un gluón verde-antirojo. La fuerza repulsiva entre dos protones (la misma carga eléctrica) que debería existir desaparece al trabajar con fuerzas de Interacción Fuerte en donde las únicas cargas que existen son las de Color. La Fuerza Nuclear Fuerte entre nucleones (protones y neutrones) se realiza mediante piones. Esta fuerza mediante la transferencia de piones es de poco alcance, a niveles de radios nucleares. Cada neutrón o protón puede "emitir" y "absorber" piones cargados o neutros. Esta transferencia implica la transformación de un protón en un neutron y viceversa. Nos encontramos con la siguiente situación: un protón emite inicialmente un pión positivo convirtiéndose en un neutrón, el pión positivo es reabsorbido por un neutrón convirtiéndose en un protón: p+ → no + π+ no + π+ → p+ El efecto neto de ese intercambio es una fuerza atractiva entre protones: p+ → no + π+ no + π+ → p+ ---------------------------------------------------------------- p+ → p+ Antonio Zaragoza López Página 43 EL NÚCLEO ATÓMICO Otra posibilidad sería: Un neutrón emite un pión negativo y se convierte en un protón, el pión negativo al ser reabsorbido por otro protón da lugar a un neutrón: no → p+ + πp+ +→ π- + no El efecto resultante sería una fuerza atractiva entre neutrones. no → p+ + πp+ → π- + no ------------------------------------------------------------------- n0 → n0 Como conclusión podemos establecer: a) En la Fuerzas de Interacción Fuerte no existen cargas eléctricas b) Los quarks (dentro del nucleón correspondiente) se unen mediante la fuerza de Interacción Nuclear Fuerte por el intercambio de "gluones" c) La unión entre: Protón - Protón Protón - Neutrón Neutrón - Neutrón se produce por el intercambio entre partículas compuestas de "piones" Enlazar online ara visualizar los videos Video: Fuerza Nuclear Fuerte https://www.youtube.com/watch?v=AtAFdxlJ1m4 Antonio Zaragoza López Página 44 EL NÚCLEO ATÓMICO Video: Fuerza Nuclear Fuerte https://www.youtube.com/watch?v=x6Vbb6MRLts Video: Los Gluones https://www.youtube.com/watch?v=g-ZHRzC_l7M Video: Los Kuarks y los Gluones https://www.youtube.com/watch?v=cvTIqHdTQhg Enlaces http://www.batanga.com/curiosidades/4259/propiedades-de-la-fuerzanuclear-fuerte-confinamiento-y-libertad-asintotica http://www.particleadventure.org/spanish/strongs.html http://hyperphysics.phy-astr.gsu.edu/hbasees/astro/stem.html http://astroverada.com/_/Main/T_strong.html http://www.windows2universe.org/sun/Solar_interior/Nuclear_Reactio ns/Nuclear_forces/strong.html&lang=sp http://www.alt64.org/wiki/index.php?title=Interacciones_nucleares 2.5.2.- Fuerza Nuclear Débil La Fuerza Nuclear Débil es una interacción que forma parte de las cuatro fuerzas fundamentales de la Naturaleza. El proceso de Interacción Débil se lleva a cabo por la combinación de partículas elementales para lograr que los neutrones se conviertan en protones. Las partículas portadoras de la Interacción Débil se clasifican según el spin cuántico[1]: a) Bosones.- Los bosones W y Z son las partículas mediadoras de la Iinteracción Nuclear Débil. Poseen un spin entero y tienen mucha masa. b) Fermiones.- Se caracterizan por tener espín semi-entero (1/2, 3/2,). Antonio Zaragoza López Página 45 EL NÚCLEO ATÓMICO [1] El espín o momento angular intrínseco se refiere a una propiedad física de las partículas subatómicas, por la cual toda partícula elemental tiene un momento angular intrínseco de valor fijo. Son dos tipos de partículas fundamentales ( Bosones y Fermiones), se encargan en general de cambiar el Sabor de la partícula (Cada tipo de quark se denomina sabor. Hay pues seis "sabores" de quarks. Al estar presente tanta partícula en este proceso cabe recordar que los protones y los neutrones son partículas que están formadas por la combinación de tres quarks cada uno de ellos. Al ser solo combinaciones de quarks es fácil pasar de un neutrón a un protón. Este tipo de interacción de quarks causa una forma de radiactividad llamada decaimiento beta, en este proceso el neutrón se transforma en protón y se eliminan un electrón y una partícula casi sin masa llamada antineutrino. Esquema del decaimiento beta: Observar que el decaimiento Beta consiste en transformar un quark "d" en un quark "u". El Decaimiento Beta se produce de forma natural en los elementos químicos radiactivos. Este decaimiento es por lo tanto un fenómeno de radiactividad, concretamente en la "radiación β" que consiste en lo mismo que el "decaimiento Beta". El átomo libera electrones del núcleo. Antonio Zaragoza López Página 46 EL NÚCLEO ATÓMICO Esta misma Interacción Débil es la responsable de la conversión no solo de neutrones en protones, sino también de la desintegración de muchas partículas inestables como: a) piones en muones b) muones en electrones La Interacción Débil es más fuerte que la gravitación a cortas distancias. Después de lo escrito y leído podemos concluir que la Fuerza de Interacción Débil Nuclear se caracteriza por: a) Es la única fuerza que afecta a los neutrinos. b) Es la única interacción capaz de cambiar los números cuánticos categorizados como sabor (no se refiere al sentido del gusto) característica propia de los leptones y quarks en la interacción débil. c) La partícula mediadora son los bosones. d)La fuerza débil es la encargada de transformar automáticamente masa en temperatura y velocidad de reacción de algunas reacciones nucleares que ocurren en estrellas como el sol. Es por efecto de esta interacción la producción del brillo y la energía en interior del Sol y las estrellas. Esto ocurre “cuando dos protones (núcleos de hidrógeno) están muy próximos, gracias a la fuerza nuclear débil, tenga lugar la transformación de un protón (p) en un neutrón (n), un electrón positivo (e+) y un neutrino (νe).” Enlazar online para visualizar los videos Video: Fuerza Nuclear Fuerte y Débil https://www.youtube.com/watch?v=GiQGugIoSm8 Video: Fuerza Nuclear Fuerte y Débil https://www.youtube.com/watch?v=DVfWu-wu_nM Antonio Zaragoza López Página 47 EL NÚCLEO ATÓMICO Video: Los Kuarks. Fuerza Nuclear Fuerte y Débil https://www.youtube.com/watch?v=GiQGugIoSm8 Enlaces http://www.particleadventure.org/spanish/npes.html http://fm-fuerzas.blogspot.com.es/p/fuerza-nuclear-debil.html http://astroverada.com/_/Main/T_weak.html http://fuerzasfundamentales.blogspot.com.es/2011/11/fuerzainteraccion-nuclear-debil.html http://cienciaetecnologias.com/interacao-nuclear-fraca/?lang=es 2.6.- Energía del Núcleo Atómico Los esposos Curie habían observado que cada átomo de una sustancia radiactiva funciona como una fuente constante de energía. Más tarde Rutherford y Soddy habían hecho ver que esa energía salía del interior del átomo y que debía de ser enorme comparada con la producida por cambios químicos. Hoy día se sabe que esa energía proviene del NUCLEO de los átomos. Se define la Energía Nuclear como la energía necesaria para separar los nucleones (protones y neutrones) de un núcleo, o bien como la energía que se libera cuando se unen los nucleones para formar el núcleo.. Como los núcleos de los átomos están formados de protones y neutrones, es de esperarse que la masa del núcleo pudiera determinarse sumando la masa de ellos. Sin embargo, se demostró, con gran sorpresa de los científicos, que la masa total de un núcleo es diferente de la suma de la masa de los protones y neutrones. Todos los núcleos de los elementos ligeros, excepto el del hidrógeno, pesan menos que la suma de las masas de sus neutrones y protones. Antonio Zaragoza López Página 48 EL NÚCLEO ATÓMICO Esta diferencia se conoce como Defecto Másico. Al fusionarse los nucleones para formar un núcleo se desprende una enorme cantidad de energía, conocida como energía de fusión. La energía asociada al Defecto Másico se puede calcular por la ecuación de Einstein: E = m . c2 En donde "m" es el defecto másico y "c" la velocidad de la luz. Esta ecuación indica que la masa se puede transformar en energía y la energía en masa y, además, que una pequeña cantidad de masa se transforma en una cantidad de energía verdaderamente asombrosa, pues el valor de c = 300.000 Km/s = 3 . 108 m/s, es una cantidad muy grande, y al elevarla al cuadrado se vuelve enorme. La energía nuclear sería la equivalente a la destrucción de todas las fuerzas de unión entre partículas dentro del núcleo atómico. En los núcleos livianos se observa un aumento abrupto de la energía de enlace por nucleón frente al número másico A. El máximo de energía corresponde a núcleos semipesados como los correspondientes al Fe, Co, Ni con un valor del número másico de A = 62, donde las fuerzas de atracción serán máximas. El decrecimiento de la energía para A > 60 se debe a la repulsión eléctrica entre los protones cuyo número va aumentando y reduce por tanto la estabilidad de los núcleos. En general, la energía nuclear es millones de veces más eficiente que la energía obtenida por la combustión al carbón (combustibles fósiles). La energía nuclear se puede liberar en forma muy rápida mediante reacciones nucleares: a) La reacción de fisión nuclear del 235U b) La reacción de fusión de los núcleos ligeros, como los núcleos de hidrógeno para formar núcleos de helio. Antonio Zaragoza López Página 49 EL NÚCLEO ATÓMICO La energía nuclear también puede ser liberada mediante la desintegración radiactiva de núcleos de átomos inestables. Para obtener una mejor estabilidad, el átomo inestable se transforma en otro tipo de átomo más estable, mediante la emisión de energía en forma de radiación. Este fenómeno se conoce como Radiactividad. En la naturaleza, la mayoría de los elementos son estables. Pero, también existen algunos inestables, y para lograr la estabilidad, se desintegran gradualmente emitiendo una o varias partículas y allí aparece la energía en forma de radiación. Este fenómeno se produce de modo natural. Vivimos desde siempre en un medio ambiente naturalmente radiactivo, estamos hablando de la Radioactividad Natural. Enlazar online para visualizar los videos Video: Energía del Átomo https://www.youtube.com/watch?v=x2KaWHlbiNM Enlaces http://bibliotecadigital.ilce.edu.mx/sites/ciencia/volumen1/ciencia2/42/h tm/sec_11.html http://www.educarchile.cl/ech/pro/app/detalle?ID=133193 http://erenovable.com/energia-atomica/ http://www.ecured.cu/N%C3%BAcleo_At%C3%B3mico http://www.escritoscientificos.es/trab1a20/carpetas/nuclear/nu02.htm http://assets.mheducation.es/bcv/guide/capitulo/8448169549.pdf Antonio Zaragoza López Página 50 EL NÚCLEO ATÓMICO 2.7.- Reacciones Nucleares. Radiactividad En los núcleos más ligeros, con un valor de Z aproximado a 20 (20 protones y 20 neutrones), los núcleos son estables. Encontramos pues que la relación entre el número de protones y neutrones son los determinantes de la estabilidad de los núcleos atómicos.. En los núcleos de elementos químicos pesados contienen más neutrones que protones. Pero al ir añadiendo protones y neutrones llega un momento que el diámetro nuclear es mayor que la distancia de acción de la fuerza nuclear fuerte. Cuando el tamaño nuclear supera los 60 protones y neutrones se hace inestable. Los protones más alejados solamente notan la fuerza de repulsión electrostática, la fuerza nuclear fuerte no los alcanza, y salen despedidos del núcleo en direcciones opuestas. Se produce el Decaimiento Beta estudiado en el apartado anterior y en donde se manifestaba que un neutrón se transformaba en un protón y se liberaba un electrones y un antineutrino. De esta forma el núcleo se hacía más estable porque ese decaimiento implicaba que el núcleo inicial se transformara en el núcleo de un nuevo elemento químico más ligero y liberación de energía en forma de radiación. Un núcleo inestable se vale de la radiactividad para liberarse de todas aquellas partículas que le confieren una mayor energía, para alcanzar un estado de mayor estabilidad y mínima energía. Con esto, el núcleo inestable disminuye su relación neutrón/protón. El Decaimiento Beta es una radiación tipo β (emisión de electrones procedentes del núcleo atómico): W- no → p+ + 1 e- + V La estabilidad nuclear se consigue mediante las reacciones nucleares que son las que dan origen a la Radiactividad. Antonio Zaragoza López Página 51 EL NÚCLEO ATÓMICO Una reacción nuclear es un proceso de combinación y transformación de las partículas y núcleos atómicos. Una reacción nuclear se representa mediante una ecuación que muestra el proceso en el que intervienen núcleos atómicos, estamos hablando de la "Radiactividad Natural". Existen otro tipo de reacciones nucleares consistentes en el bombardeo de un núcleo con otros núcleos de menor tamaño o, incluso, con partículas subatómicas. En esto consistiría la Radiactividad Artificial. Como ejemplos de reacciones nucleares tenemos: 27 Al13 + 4He2 → 30P15 + 1no 14 N7 + 4He2 → 17O8 + 1p1 7 Li3 + 1P1 → 4He2 + 4He2 27 Al13 + 1no → 27Mg12 + 1p1 En todas estas reacciones se debe conservar la masa (la suma de los números másicos de los productos y reactivos es la misma) y la carga (la suma de los números atómicos, en productos y reactivos es la misma), dicho de otra manera, la suma de los exponentes y de subíndices debe permanecer constante en los dos miembros de la reacción nuclear. El origen de la radiactividad tiene lugar en 1869 por los experimentos realizados por Becquerel al descubrir que un compuesto natural del uranio emitía radiaciones. El matrimonio Pierre y Marie Curie encontraron otro elemento, el Torio, que emitía el mismo tipo de radiación que el Uranio. Las radiaciones producidas por el uranio y el torio reciben el nombre de "Ionizantes" porque poseen un nivel de energía, que al interaccionar con la materia, producen ionización en ésta. Es decir, son capaces de modificarla a nivel atómico y molecular. Antonio Zaragoza López Página 52 EL NÚCLEO ATÓMICO Las emisiones emitidas en el fenómeno de la Radiactividad pueden ser. a) Electromagnéticas b) Rayos X o rayos gamma c) Corpusculares 1.- Núcleos de helio 2.- Electrones 3.- Positrones 4.- Protones En resumen, es un fenómeno que ocurre en los núcleos de ciertos elementos inestables, que son capaces de transformarse o decaer, espontáneamente, en núcleos atómicos de otros elementos más estables. Enlazar online para visualizar los videos Video: La Radiactividad. Esposos Curie y Becquerel https://www.youtube.com/watch?v=Y15JROM48yI La Radiactividad se clasifica en: a) Radiactividad Natural b) Radiactividad Artificial 2.7.1.-Radiactividad Natural Existen tres tipos de radiaciones emitidas por compuesto radiactivos: a) Radiación "α" b) Radiación "β" ᵧ c) Radiación " " Enlazar online para visualizar los videos Antonio Zaragoza López Página 53 EL NÚCLEO ATÓMICO Video: Reacciones Nucleares https://www.youtube.com/watch?v=VodUVQWcnUU 2.7.1.1.- Radiación "α" Consiste en la emisión de núcleos de átomos de Helio, 4He2, la llamada partícula "α". La partícula "α" son átomos de He ionizados (He+2). Representaremos dicha partícula en las reacciones nucleares como 4 He2. Cuando un núcleo inestable emite una partícula "α" se crea otro átomo de un elemento químico distinto en donde su número másico (A) se reduce en 4 unidades y su número atómico (Z) en 2 ( 1ª Ley de Fajan y Soddy sobre la Desintegración Nuclear): A XZ → A-4YZ-2 + 4He2 Esta radiación es típica de elementos químicos de núcleos atómicos muy pesados. Como ejemplo: 210 Po84 → 206Pb82 + 4He2 Con esta radiación el Po que es inestable se transforma en átomos de plomo que son estables. 2.7.1.2.- Radiación "β" Son electrones emitidos por el núcleo con gran velocidad y energía. Sabemos que los electrones se encuentran orbitando alrededor del núcleo en la corteza electrónica. ¿Cómo es posible la emisión de electrones por parte del núcleo del átomo cuando en este no existen electrones?. El Decaimiento Beta da respuesta a esta cuestión. El Decaimiento Beta consiste en la transformación de un neutrón en un protón liberándose un electrón. Antonio Zaragoza López Página 54 EL NÚCLEO ATÓMICO 1 n0 → p+ + e- + 1 neutrino Como resultado de una radiación "β" es un nuevo átomo cuyo número másico (A) permanece constante pero su número atómico (Z) aumenta en una unidad (2ª Ley de Fajan y Soddy sobre la Desintegración Radiactiva): A XZ → AYZ+1 + oe-1 Como ejemplo veamos la desintegración del Bismuto - 210 (otra forma de representar los isótopos de un elemento químico): 210 Bi83 → 210Po84 + 0e-1 2.7.1.3.- Radiación "ᵧ" Son radiaciones electromagnéticas o fotones que son emitidas junto a las partículas "α" y "β". ᵧ La radiación " " no modifica el número másico ni el número atómico del núcleo emisor de la radiación. No se crea un átomo nuevo. Ejemplo: 125 ᵧ Te52 → 125Te52 + " " El poder de penetración en nuestro organismo (riesgo de cáncer) es: ᵧ " " > "β" > "α" Los isótopos naturales, unos cuarenta, terminan transformándose en otros isótopos hasta llegar a convertirse en uno estable del plomo. Todas la transmutaciones atómicas ocurren por emisiones alfa y beta. Antonio Zaragoza López Página 55 EL NÚCLEO ATÓMICO Cuando un núcleo se va desintegrando, emite radiación "α" o "β" y da lugar a otro núcleo distinto también radiactivo, que emite nuevas radiaciones. El proceso continuará hasta que aparezca un núcleo estable, no radiactivo. Todos los núcleos que proceden del inicial (núcleo padre) forman una serie radiactiva o Reacciones en cadena radiactiva. 2.7.1.4.- Series Radiactivas o Reacciones Nucleares en Cadena Se conocen tres series radiactivas de los isótopos naturales: la del Torio, la del Actinio y la del Uranio. Serie del Torio: Para simplificación de la serie radiactiva estableceremos un código de color para las flechas que nos indican el sentido de la desintegración emitiendo una radiación: Emisión de radiación "α" Emisión de radiación "β" 232 Th → 228Ra → 228Ac → 228Th → 224Ra → 220Rn → 216Po → 212P b → 212Bi → 212Po → 208 Tl → Antonio Zaragoza López 208 Pb ( Estable) 208 Pb ( Estable) Página 56 EL NÚCLEO ATÓMICO Serie del Actinio o del 235 U: 235 U → 231Th → 231Pa → 227Ac → 227Th → 223Ra → 219Rn → 215Po → 223 Fr → 211Pb → 211Bi → 207Tl → 207Pb (Estable) 215 At 211 Po Serie del Uranio-238: 238 U → 234Th → 234Pa → 234U → 230Th → 226Ra → 222Rn → 218Po → → 214Pb → 214Bi → 214Po → 210Pb → 210Bi → 216Po → 206Pb (Estable) Enlazar online para visualizar los videos Video: Radiactividad Natural https://www.youtube.com/watch?v=AhdRBpTI1wU Video: Radiactividad Natural y Artificial https://www.youtube.com/watch?v=V5gS5RfyQNw Video: Radiación Natural y Artificial https://www.youtube.com/watch?v=V5gS5RfyQNw 2.7.1.5.- Datación mediante la prueba del Carbono - 14 14 El isótopo del carbono C6 ( En el núcleo: 6 p+ y 8 n0) se desintegra con la emisión de un electrón (-10e) transformándose en 14N7 (En el núcleo: 7 p+ y 7 n0), lo que se representa mediante la ecuación nuclear siguiente: 14 C6 → Antonio Zaragoza López 14 N7 + 0 -1 e Página 57 EL NÚCLEO ATÓMICO El carbono 14 tiene su origen principalmente en la atmósfera debido a la acción de los rayos cósmicos sobre los átomos de nitrógeno: 14 N7 + 1no → 14C6 + 1H1 La vida media del radioisótopo 14C6 es de 5580 años (tiempo que tarda en desintegrarse la mitad de la muestra inicial de radioisótopo). El 14C6 es incorporado al dióxido de carbono de la atmosfera, CO2 ( carbono radiactivo). Ese dióxido de carbono es absorbido por las plantas durante la fotosíntesis, de esta forma todas las plantas tienen carbono - 14. Si los animales toman plantas, también tendrán carbono - 14. Las plantas al asimilar el dióxido de carbono lo pueden hacer mediante la forma radiactiva como la normal, 12C6. Estableciéndose una proporción 14C6 / 12C6 que permanece prácticamente constante mientras la planta esté viva. Los animales y el hombre mediante la alimentación guardan la misma relación entre los dos tipos de carbono. Cuando la planta o el animal muere, deja de ingerir 14C6 pero el que existía en sus tejidos sigue desintegrándose por lo que la proporción 14 C / 12C disminuirá con el tiempo con una velocidad que depende de su periodo de semidesintegración. La medición de la radiactividad de un objeto permite determinar la edad de la muerte de la planta o del animal a partir de la cual se había fabricado. Dicha medición se utiliza para la datación de fósiles animales y vegetales. La prueba carbono 14 se utiliza para determinar la edad de artefactos arqueológicos y material biológico hasta 50.000 años atrás tomando como base la vida media de dicho átomo, 14C. Se utiliza en huesos, tela, madera y fibras de plantas creadas por la actividad humana. Enlazar online para visualizar los videos Video: Prueba del Carbono - 14 https://www.youtube.com/watch?v=YQB-GlspNA8 Video: Prueba Carbono - 14 en la Sábana Santa https://www.youtube.com/watch?v=ledjYkyUaG0 Antonio Zaragoza López Página 58 EL NÚCLEO ATÓMICO Video: Prueba Carbono - 14 (1) https://www.youtube.com/watch?v=dumlw3m8KM8 Video: Prueba Carbono - 14 (2) https://www.youtube.com/watch?v=YRZ5UjFAYtY Enlaces http://www.batanga.com/curiosidades/4547/como-funciona-ladatacion-por-carbono-14 http://ytusabes.blogspot.com.es/2011/01/en-que-consiste-la-prueba-decarbono-14.html http://www.swagger.mx/natural/101-como-funciona-la-pruebacarbono-14 2.7.2.- Radiactividad Artificial Cuando aparece "Artificial" el hombre, a nivel científico, está creando radiactividad y esperemos que con un fin que sea beneficioso para la humanidad. Los esposos Curie bombardearon núcleos de Boro y Aluminio (ambos elementos con núcleos estables) con partículas "α". Observaron que tanto el Boro como el Aluminio emitían radiaciones después de retirar el compuesto químico radiactivo que emitía las partículas "α". Los esposos Curie consiguieron convertir dos átomos con núcleos estables en elementos radiactivos (sus átomos ya no tienen núcleos estables). En la experiencia de los Curie se basa la Radiactividad Artificial o Radiactividad Inducida. Se produce cuando se bombardean ciertos núcleos estables con partículas apropiadas. Si la energía de estas partículas tiene un valor adecuado, penetran en el núcleo bombardeado y forman un nuevo núcleo que, en caso de ser inestable, se desintegra después radiactivamente. Antonio Zaragoza López Página 59 EL NÚCLEO ATÓMICO En los últimos 50 años se han obtenido en el laboratorio más de 1200 isótopos radiactivos. El número de isótopos por elemento químico varía desde uno (hidrógeno y boro) hasta 34 (indio). Todos ellos se obtienen por reacciones de bombardeo, en las que un núcleo estable se transforma en radiactivo. Una reacción típica de bombardeo se produce, por ejemplo, cuando se bombardea el isótopo estable del aluminio 27Al13 con neutrones: 27 Al13 + 1n0 → 28Al13 Al absorber un neutrón se transforma en el isótopo 28Al13 que es inestable y se desintegra con emisión de un electrón formando un isótopo estable de silicio, 28Si14: 28 Al13 → 28Si14 + 0e-1 Los primeros isótopos radiactivos artificiales fueron elaborados por Irene Curie y Fréderic Joliot, bombardeando isótopos estables con partículas "α" de elevado contenido energético. Un ejemplo es la siguiente reacción: 27 Al13 + 4He2 → 30P15 + 1n0 El 30P15 es radiactivo y se desintegra según la reacción: 30 P15 → 30Si14 + 0e1 (Positrón, antipartícula del electrón e-) Si bombardeamos el 238U92 con neutrones se pueden producir las siguientes reacciones nucleares: Simbología: AXZ 238 U92 + → 239 1 n0 → U92 → 239 Np93 + 0e-1 → 239 Np93 → 239Pu94 + 0e-1 Pu94 + 2 1n0 → Antonio Zaragoza López 239 241 Pu94 → 241 Am95 + 0 e-1 Página 60 EL NÚCLEO ATÓMICO Si el bombardeo se realiza mediante iones (partículas "α", He+2): 239 Pu94 + 242 Cm96 + 4 He2+2 → 4 He2+2 → 242 Cm96 + 245 Cf98 + 1 n0 1 n0 Si bombardeamos con el isótopo 12C6: 238 U92 + 12 Cf98 + 12 249 C6 → 246 Cf98 + 4 1n0 C6 → 257Unq104 + 4 1n0 Con el isótopo 15N7: 249 15 249 18 Cf98 + N7 → 260Unp105 + 4 1n0 Con 18O8: Cf98 + O8 → 263Unh106 + 4 1n0 Enlazar online para visualizar los videos Video: Radiactividad Natural y Artificial https://www.youtube.com/watch?v=V5gS5RfyQNw Aplicaciones de la Radiactividad Artificial Las radiaciones ionizantes pueden ser útiles para: a) Producción de energía b) Esterilización de alimentos c) Conocer la composición interna de diversos materiales d) Detectar errores de fabricación y ensamblaje e) En el campo de la medicina: Antonio Zaragoza López Página 61 EL NÚCLEO ATÓMICO 1.- Estudios diagnósticos (Medicina Nuclear y Radiología) y tratamientos (Medicina Nuclear y Radioterapia) 2.- Análisis de elementos que se encuentran en concentraciones muy bajas f) Trazadores en estudios de procesos físicos, químicos, biológicos y médicos g) Control del espesor de hojas y láminas en las industrias del papel, del hule y en general en espesores de láminas de plásticos h) Control del llenado de líquidos en frascos y latas en industrias como la cervecera y la de envasado de alimentos i) Fuentes intensas de radiación en radiografías industriales y de la medicina nuclear j) Esterilización de material quirúrgico desechable k) Esterilización de productos químicos y biológicos l) Identificación del cabello humano, también puede utilizarse para comparar manchas de grasa muy pequeñas, partículas de polvo invisibles a simple vista y partículas de pintura de automóvil, también casi invisibles, en casos de accidente. Otra ventaja de este análisis es que las muestras sometidas a examen no sufren daño alguno y pueden, por lo tanto, admitirse como prueba en los tribunales. En TV podemos ver muchas series policiacas en donde el mejor instrumento para la identificación del asesino consiste en pruebas científicas. Los isótopos radiactivos (trazadores) han hecho posible grandes avances en el conocimiento médico: a) Han ayudado a realizar estudios sobre el cáncer b) Sistemas que forman la sangre c) Metabolismo del hierro d) Actividad de las hormonas e) Conocer el funcionamiento del hígado y riñón f) La formación de vitaminas g) Drogas Antonio Zaragoza López Página 62 EL NÚCLEO ATÓMICO h) Leche Se han realizado gran número de investigaciones en procesos bioquímicos; por ejemplo: a) El estudio del metabolismo de las grasas y formación del colesterol b) La biosíntesis de aminoácidos en el interior de las células c) Estudios de genética La exposición rápida a grandes dosis de radiaciones ionizantes y a cuerpo entero en los accidentes radiológicos puede provocar un síndrome hiperagudo en el que la muerte puede presentarse muy rápidamente (minutos a horas). El sujeto presentará: a) Nerviosismo extremo b) Confusión c) Náuseas d) Vómito e) Pérdida del conocimiento Poco tiempo después aparecen: a) Convulsiones y diarrea b) Alteraciones de la bomba sodio-potasio c) Edema cerebral d) Meningitis e) y muerte Los efectos que la radiación produce en los organismos se han clasificado en cuatro grupos: a) Los que producen cáncer b) Las mutaciones genéticas Antonio Zaragoza López Página 63 EL NÚCLEO ATÓMICO c) Los efectos en los embriones durante el embarazo d) Quemaduras por exposiciones excesivas Enlazar online para visualizar los videos Video: Radiactividad Natural y Artificial https://www.youtube.com/watch?v=V5gS5RfyQNw Video: Aplicaciones de las radiaciones en Medicina https://www.youtube.com/watch?v=W_yj78z9bjo Enlaces http://www.taringa.net/posts/cienciaeducacion/9807404/Radiactividad-y-sus-aplicaciones-en-la-vidadiaria.html http://www.escolar.com/lecturas/preguntas-y-respuestas/por-que5/por-que-es-util.html http://radioactividadartificialoinducida.blogspot.com.es/ http://www.escuelapedia.com/radioactividad-natural-y-radioactividadartificial/ http://www.sociedadelainformacion.com/departfqtobarra/nuclear/radi actividad/radioactividad.htmhttp://www.construmatica.com/construpe dia/Radiactividad_Natural http://www.educarchile.cl/ech/pro/app/detalle?ID=136399 http://unidadderadiactividad.blogspot.com.es/p/particulas.html http://www.detectivedonradon.com/2012/03/14/origen-de-laradiactividad-natural/ http://blogdequimica4.blogspot.com.es/2011/09/el-nucleo-inestabilidadnuclear.html 2.8.- Reacciones Nucleares La energía nuclear es aquella que se libera como resultado de una reacción nuclear, dicho de otra forma, el fenómeno radiactivo Antonio Zaragoza López Página 64 EL NÚCLEO ATÓMICO lleva como consecuencia de liberalización de energía, por dos razones: a) El fenómeno de la radiactividad es un proceso exotérmico b) La existencia del "Defecto Másico" ( E = m . c2) Si nuestro objetivo es obtener energía podemos seguir dos procesos: a) Reacción Nuclear de Fisión.- División de núcleos atómicos pesados b) Reacción Nuclear de Fusión.- Unión de núcleos atómicos muy livianos Como dato: Una reacción nuclear es un millar de veces más energética que una reacción química normal, por ejemplo, la generada por la combustión del combustible fósil del metano. 2.8.1.- Reacciones de Fisión Nuclear En las reacciones nucleares un núcleo, de un elemento químico pesado, es desintegrado en otro núcleo o núcleos más ligeros. La desintegración tiene lugar mediante el bombardeo de un núcleo inicial por una partícula subatómica que nosotros consideraremos que es el "neutrón". En este proceso se libera gran cantidad de energía debido a que el núcleo pesado es menos estable que sus productos. Además de los núcleos más ligeros también se liberan " neutrones". No es un error lo escrito (bombardeo con neutrones y liberación de uno o varios neutrones). La Fisión Nuclear es producida por "neutrones" y además se crean más "neutrones". Veamos un ejemplo de fisión nuclear: 235 U92 + 1n0 → Antonio Zaragoza López 134 Xe54 + 100Sr38 + 2 1n0 Página 65 EL NÚCLEO ATÓMICO neutrón 100 Sr38 neutrón neutrón 235 U92 neutrón 134 Xe54 neutrón Los núcleos resultantes (100Sr38 y 134Xe54) son inestables y por tanto podrán desintegrarse emitiendo electrones o positrones mediante la Desintegración Beta. La fisión del uranio-235 se caracteriza por: a) No se produce una gran liberación de energía b) Se producen más neutrones que los utilizados en el bombardeo inicial Por esta propiedad es posible obtener una "reacción nuclear en cadena", es decir, una secuencia de reacciones de fisión nuclear autosuficientes. Los neutrones generados en las etapas iniciales de la fisión pueden inducir fisión en otros núcleos de uranio-235, que a su vez producen más neutrones, y así sucesivamente. En menos de un segundo, la reacción se vuelve incontrolable, liberando una gran cantidad de calor a los alrededores. Antonio Zaragoza López Página 66 EL NÚCLEO ATÓMICO U U U U neutrón U U U La reacción en cadena debe ser controlada. Para ello los neutrones son frenados, para que no explote el reactor, mediante unas barras de control (generalmente, de Carburo de Boro). Estas barras absorben neutrones disminuyendo el número de fisiones. Dependiendo del número de barras que se introduzcan se generará mayor o menor energía calorífica. Si el números de barras de absorción de neutrones es muy elevado las fisiones se reducirían al máximo llegándose Antonio Zaragoza López Página 67 EL NÚCLEO ATÓMICO inclusive a la parada del reactor de la central nuclear. En el reactor existen las barras de absorción en un número determinado y estudiado para que en caso de accidente todas las barras entrarían en funcionamiento y el reactor se pararía. Este calor, calienta unas tuberías de agua, y esta se convierte en vapor, que pasa por unas turbinas, haciéndolas girar. Estas a su vez, hacen girar un generador eléctrico, produciendo así electricidad. El reactor se refrigera, para que no se caliente demasiado, y funda las protecciones, incluso cuando este esté parado, ya que la radiación hace que el reactor permanezca caliente. Como combustible se utilizan barras de Uranio enriquecido al 4% con Uranio-235. El Uranio natural es mayoritariamente U-238, el que es fisionable es el U-235, que es un 0,71% del Uranio que se encuentra en la naturaleza, de ahí que solo un pequeño porcentaje del Uranio se aproveche y se requieran grandes cantidades de este para obtener una cantidad significativa de U-235. Enlazar online para visualizar los videos Video: Fisión Nuclear https://www.youtube.com/watch?v=AOwe5WrruY0 Video: Energía Nuclear https://www.youtube.com/watch?v=kS5ads9zEdc Video: Reactor nuclear https://www.youtube.com/watch?v=TCYPafKI1Jk Antonio Zaragoza López Página 68 EL NÚCLEO ATÓMICO Energía de la Fisión Nuclear El Uranio fisionable es el Uranio - 235 (235U). En este fenómeno de fisión se liberan 200 MeV de energía. El U-235 se encuentra de forma natural en un mineral llamado Pechblenda que contiene un gramo de Uranio por cada kilogramo de mineral. En este mineral el contenido de Uranio - 235 es del 0,7 %. Si suponemos un Kilogramo de dicho mineral: 1000 g Pechblenda . 0,7 g 235U / 100 g Pechblenda = 7 g 235U Ma 235U = 235 u (unidades de masa atómica) 1 mol 235U = 235 g 1 mol 235 - U = 6,023 . 1023 núcleos de 235U Podemos establecer que: 235 g de 235U / 6,023 . 1023 núcleos de 235U Nuestra muestra supuesta contiene 7 g de 235U: 7 g 235U . 6,023 . 1023 núcleo de 235U / 235 g de 235U = 0,18 . 1023 núcleos Recordemos que: 1 núcleo 235U / 200 MeV (Dato) 0,18 . 1023 núcleo de 235U . 200 MeV/ 1 núcleo de 235U = 36 . 1023 MeV = = 36 . 1029 eV Antonio Zaragoza López Página 69 EL NÚCLEO ATÓMICO 1 eV = 1,6 . 10-19 J 36 . 1029 eV . 1,6 . 10-19 J / 1 eV = 57,6 . 1010 J . 1 Kj / 1000 J = = 57,6 . 107 Kj Conclusión: 1 Kg de Pechblenda → 7 g de 235U → Se libera una energía calorífica de 57,6 . 107 Kj Si el Uranio - 235 está enriquecido partimos de una concentración de este isótopo del 3 - 5 % con lo que la energía liberada será muchísimo mayor (el enriquecimiento del Uranio - 235 se verá más adelante). Es importante poner de manifiesto que todos los núcleo no son fisionables. Solo lo hacen de forma espontanea los núcleos pesados con valores de Z muy grandes (Uranio, Torio). El Uranio tiene Z = 92. Los elementos de Z > 92 no existen en la naturaleza, deben fabricarse artificialmente. Esta es la razón de que en las centrales nucleares se utilice el Uranio como combustible. El Uranio - 235, el utilizado en las centrales nucleares, no es el Uranio 235 que existe en la naturaleza formando parte de de la Pechblenda. Este mineral contiene únicamente el 0,7 % de este isótopo del Uranio. Para poder ser utilizado se debe proceder al enriquecimiento del mismo para conseguir una cantidad comprendida entre un 3 - 5 %. El enriquecimiento del Uranio - 235 requiere que el mineral sea transformado en gas a baja temperatura. Se procede a bombear gas de flúor hacia una planta de conversión de minerales, el gas de óxido de uranio reaccionará con el gas de flúor y con esto se producirá hexafluoruro de uranio (UF6). Se deja que el gas actúe para separar y reunir los isótopos de Uranio - 235. El Uranio - 235 también tiene aplicación en otros campos con objetivos muy distinto al de las centrales nucleares. Hablamos de BOMBAS (PUM), como las arrojadas sobre Hiroshima y Nagasaki. Antonio Zaragoza López Página 70 EL NÚCLEO ATÓMICO Para poder eliminar la contaminación ambiental y por tanto el Calentamiento Global debemos abandonar los combustibles fósiles y utilizar la energía eléctrica. Hoy día (2016) ya van apareciendo los vehículos que utilizan la electricidad para sus desplazamientos. La cantidad de energía eléctrica necesaria para eliminar los fenómenos anteriores no pueden ser proporcionadas por las energías renovables (eólica, geotérmica, etc). Le tenemos mucho miedo a la energía nuclear pero, en mi opinión, es la única que puede resolver los problemas medioambientales. Enlazar online para visualizar los videos Video: Fisión y Fusión https://www.youtube.com/watch?v=JXiGB__Ov7w Video: Energía atómica. Fusión y Fisión https://www.youtube.com/watch?v=vyF_WNlRndY Video: Funcionamiento de una Central Nuclear https://www.youtube.com/watch?v=AOwe5WrruY0 Video: Funcionamiento de una Central Nuclear https://www.youtube.com/watch?v=_SDaXT5TLfM Video: Funcionamiento de una Central Nuclear https://www.youtube.com/watch?v=kS5ads9zEdc Video: Energía Nuclear (Inglés) Video: Energía Nuclear https://www.youtube.com/watch?v=4_Jd4l0ptYA Video: Central Nuclear Video: Energía Nuclear https://www.youtube.com/watch?v=pXUXIHtfXgA Video: Central Nuclear Video: Energía Nuclear https://www.youtube.com/watch?v=UdHRcQwGn2k Antonio Zaragoza López Página 71 EL NÚCLEO ATÓMICO Enlaces http://www.escritoscientificos.es/trab1a20/carpetas/nuclear/nu04.htm http://www.gobiernodecanarias.org/educacion/3/usrn/lentiscal/2-CDFiisca-TIC/2-9Nuclear/Nuclear-TeoriarWeb/ELEMENTOS%20BASICOS%20DE%20FISICA%20NUCLE AR.htm http://www.fisicanet.com.ar/quimica/estructura_atomica/ap10_nucleo_ atomico.php http://www.monografias.com/trabajos82/estructura-del-nucleoatomico/estructura-del-nucleo-atomico.shtml https://es.answers.yahoo.com/question/index?qid=20080328103902AA Cfj6z http://energia-nuclear.net/que-es-la-energia-nuclear/fision-nuclear http://web.educastur.princast.es/proyectos/jimena/pj_franciscga/fusion yfision.htm http://www.fisicahoy.com/talleres/fision_nuclear_reacciones_en_caden a https://www.tplaboratorioquimico.com/quimica-general/quimicanuclear/fision-nuclear.html 2.8.2.- Fusión Nuclear La fusión nuclear constituye un proceso de tipo inverso al de la fisión en el cual dos núcleos ligeros se reúnen para formar uno más pesado. A medida que los núcleos (dos, por ejemplo) se acercan aparecen fuerzas de repulsión electrostática. Estas fuerzas se deben vencer para que se produzca la fusión de los dos núcleos y esto lo conseguiremos con energías cinéticas adecuadas de los núcleos. Las fuerzas de repulsión electrostática aumentan al aumentar el número atómico (Z) lo que nos indica que la fusión será posible para núcleos ligeros. El hidrógeno, en condiciones normales de temperatura, se repele entre sí cuando intentas unirlo (fusionarlo) a otro átomo de hidrógeno. Para vencer esta repulsión electrostática, el átomo de hidrógeno debe chocar Antonio Zaragoza López Página 72 EL NÚCLEO ATÓMICO violentamente contra otro átomo de hidrógeno, fusionándose, y dando lugar a Helio, que no es fusionable. La diferencia de masa entre productos y reactivos es mayor que en la fisión, liberándose así una gran cantidad de energía (muchísimo mayor que en la fisión). Estos choques violentos, se consiguen con una temperatura del orden de los 109 K, , que hace aumentar la velocidad de los átomos. Las reacciones de fusión reciben el nombre de Reacciones Termonucleares por las altas temperaturas que requieren para su producción. En la Fusión también existen reacciones en cadena. Como ejemplo de estas reacciones en cadena tenemos el denominado ciclo de Critchfield o ciclo protón-protón , cuyas etapas son: 1 H¹ + 1 H¹ → 1 H² + e+ + υ 1 2 H¹ + 1 H² → 2 He³ + γ He³ + 2 He³ → 2 He4 + 21 H¹ donde e+ y υ (positrón y neutrino). La cantidad de energía liberada en un ciclo completo es, en este caso, de 26,2 MeV. Otras reacciones de fusión: 2 D1 + 2D1 → 3T1 + 1H1 + 4.03 MeV 2 D1 + 2D1 → 3 He2 +1n0 + 3.27 MeV 2 D1 + 3T1 → 4He2 + 1n0 + 17.6 MeV donde: 1 H1 = Isótopo del Hidrógeno (Protio) 2 D1 = Isótopo del Hidrógeno (Deuterio) 3 T1 = Isótopo del Hidrógeno (Tritio) Antonio Zaragoza López Página 73 EL NÚCLEO ATÓMICO Enlazar online para visualizar los videos Video: Fisión y Fusión https://www.youtube.com/watch?v=JXiGB__Ov7w Video: Energía atómica. Fusión y Fisión https://www.youtube.com/watch?v=vyF_WNlRndY Se está investigando sobre las reacciones de fusión en cadena pero lo conocido no es lo suficientemente importante como para llevar la teoría a la práctica y poder crear las centrales nucleares de fusión. Enlazar online para visualizar los videos Video: Posible planta nuclear de fusión en 30 años https://www.youtube.com/watch?v=gT7LRj3BRKw Sin embargo lo conocido sobre la fusión nuclear ha sido suficiente para crear artilugios mortíferos para todos los seres vivos del planeta. Estamos hablando de la bomba de Hidrógeno.: Bomba de Hidrógeno es el nombre popular: a) Bomba Termonuclear.- Por las elevadas temperaturas que produce b) Bomba de fusión .- En una de sus etapas utiliza reacciones de Fusión En este tipo de bomba se utilizan: a) Reacciones de Fisión b) Reacciones de Fusión La bomba de Hidrógeno se basa inicialmente en un proceso de fisión y posteriormente realizar la fusión de átomos de Hidrógeno consiguiéndose una bomba Termonuclear. El proceso de fisión consiste en la división de átomos Uranio - 235 o Plutonio - 239 para posteriormente dar paso la fusión de átomos de hidrógeno. Se consigue de esta forma una doble función mortífera: Antonio Zaragoza López Página 74 EL NÚCLEO ATÓMICO a) La emisión de radiaciones.- Problemas de Cáncer b) Muy elevada temperatura.- Por la liberación de radiación electromagnética. Problemas de los diferentes niveles de quemaduras en los cuerpos humanos. Una bomba Atómica de Fisión (Hiroshima y Nagasaki) al estallar libera una energía que se mide en kilotones, las bombas Termonucleares se miden en megatones (un megatón son 1.000 kilotones): 1 Megatón = 1000 Kilotones 1 Kilotón = 1000 Kg de T.N.T (Trinitrotolueno) La bomba Termonuclear lanzada por Rusia en 1961 tenía una potencia de 50 megatones. Enlazar online para visualizar los videos Video: Bomba de Hidrógeno https://www.youtube.com/watch?v=wFAcNqlQSPc Video: Bomba de Hidrógeno https://www.youtube.com/watch?v=hm8gOl1g5ZU Video: Bomba de Hidrógeno https://www.youtube.com/watch?v=FPCgptskoho La Bomba de neutrones o Bomba - N Me interesa comentar este tipo de bomba para demostrar el gran poder mortífero de los humanos. Tras la Segunda Guerra Mundial y los estudios de los efectos producidos, los americanos llegaron a la conclusión de que las bombas tradicionales utilizadas producían los efectos para lo que fueron creadas: Antonio Zaragoza López Página 75 EL NÚCLEO ATÓMICO a) Destrucción de infraestructuras (edificios, puentes, centrales eléctricas, pantanos, puentes, etc) b) Gran cantidad de muertes entre el personal militar y civil Pero dichas bombas podían ser negativas en determinadas situaciones. Supongamos que queremos tomar una ciudad. El Centro de Operaciones mandaría primeramente a la aviación con las citadas bombas. Más tarde la infantería, apoyada por los tanques, entraban en la ciudad para rematar la acción de la aviación. Se encontraban con un panorama de destrucción de edificios (muchos escombros) y gran cantidad de cadáveres. Pero el avance era muy lento. Si no existieran escombros por las calles los tanques avanzarían más rápidamente y la toma de la ciudad duraría mucho menos tiempo. Cómo se podría conseguir que no existieran escombros? Los americanos, muy listos ellos en este campo, pensaron que se podrían lanzar bombas que mataran a todo vicho viviente pero los edificios y otras infraestructuras quedaran indemnes. Se pusieron a pensar y nació la bomba deNeutrones o Bomba - N. Dicha bomba es una pequeña arma termonucleares basada en un proceso de radiación directa incrementada o bomba de radiación forzada. En las bombas H normalmente el 50% de la energía liberada se obtiene por fisión nuclear y el otro 50% por fusión. En la bomba de neutrones se consigue hacer bajar el porcentaje de energía obtenida por fisión a menos del 50%, e incluso se ha llegado a hacerlo de cerca del 5%. La perdida de energía se amortiza por una gran radiación ionizante (radiactividad), hasta 7 veces mayor que las de una bomba H. Las radiaciones emitidas son fundamentalmente rayos X y gamma de alta penetración. En segundo lugar, buena parte de esta radiactividad es de mucha menor duración (menos de 48 horas) de la que se puede esperar de una bomba de fisión. Las consecuencias prácticas son que al detonar una bomba - N se produce poca destrucción de estructuras y edificios, pero mucha muerte de seres vivos (tanto personas como animales), incluso aunque estos se encuentren dentro de vehículos o instalaciones blindadas o acorazadas. Antonio Zaragoza López Página 76 EL NÚCLEO ATÓMICO Estas bombas permiten la continuación de operaciones militares en el área por parte de unidades al no existir escombros que impidan el avance. Implican un efecto colateral llamado Activación neutrónica de materiales que estén en las cercanías ampliando los efectos de la radiación, haciendo que átomos estables se convirtieran en inestables por el ataque de los neutrones. Las personas o animales perderían la vida a las pocas horas del estallido de la bomba. Enlazar online para visualizar los videos Video: Bomba de neutrones sobre Yemen https://www.youtube.com/watch?v=7bujDevJ18o Video: Israel lanza bomba de neutrones contra Yemen https://www.youtube.com/watch?v=sUfudG95_qw Enlaces http://www.educarchile.cl/ech/pro/app/detalle?ID=133193 http://www.educarchile.cl/ech/pro/app/detalle?ID=133193 http://www.solociencia.com/fisica/particulas-elementales-particulaselementales.htm http://encina.pntic.mec.es/jsaf0002/p32.htm http://es.gizmodo.com/como-funciona-una-bomba-de-hidrogeno-y-porque-es-tan-p-1751325417 https://www.youtube.com/watch?v=hm8gOl1g5ZU http://internacional.elpais.com/internacional/2016/01/07/actualidad/14 52193525_759126.html http://muyinteresantespain.blogspot.com.es/2012/11/la-bomba-quedestruye-al-hombre-sin.html#.VpitCfnhDIU http://www.siglo21info.com/1945-1989/militaris/armas/neutrones.html Antonio Zaragoza López Página 77 EL NÚCLEO ATÓMICO 2.9.-Estructura del Núcleo Atómico Si queremos dar explicaciones sobre las propiedades del Núcleo Atómico así como de su comportamiento debemos distribuir los nucleones dentro del mismo, es decir, establecer una estructura nuclear. Existen dos modelos teóricos que intentan establecer el ordenamiento interior del Núcleo: a) El modelo de Capas b) El modelo de la Gota Líquida 2.9.1.- Modelo de Capas Distribuye los nucleones de una forma parecida a como están distribuidos los electrones en la Corteza Electrónica. Se trata de un modelo "cuántico" (como los números cuánticos semejantes a los conocidos) en donde los nucleones se situarían en niveles energéticos. En las capas inferiores se encontrarían los nucleones con menor contenido energético, los correspondientes a los que establecen Interacciones Débiles. En las capas superiores los causantes de las interacciones Fuertes. La observación experimental de espectros nucleares de rayos γ semejantes a los espectros de líneas atómicos, así como la existencia de núcleos estables cuyo número de nucleones correspondería a una estructura de capas completas, constituyen los principales argumentos en favor de este modelo de la arquitectura interna del núcleo. Por analogía con la situación en las capas electrónicas del átomo se supone que los núcleos con capas exteriores nucleónicas llenas deberían ser más estables que los que no tienen ocupadas las capas exteriores. La teoría más sencilla indica que los núcleos con 2, 8, 20, Antonio Zaragoza López Página 78 EL NÚCLEO ATÓMICO 40, 70 o 112 protones o neutrones serían estables (Números mágicos). Sin embargo, ello no encajaba con la observación. La física Maria Goeppert Mayer tuvo en cuenta el espín de protones y neutrones y encontró que los núcleos con 2, 8, 20, 28, 50, 82 o 126 protones o neutrones serían particularmente estables. Para casi todos los núcleos con A (Número Másico) impar en estado fundamental (estado de energía más bajo) el modelo proporciona resultados que concuerdan con los valores experimentales para propiedades como, por ejemplo, el espín, y resultados aproximados para otras propiedades como el momento dipolar magnético. 2.9.2.- Modelo de la Gota Líquida Las fuerzas nucleares darían lugar a una configuración semejante a la gota de un líquido que en su estado de más baja energía adopta una geometría esférica. Es el modelo más simple y describe el núcleo como una colección fuertemente empaquetada y en donde las partículas apenas tienen espacio entre ellas. Donde la densidad es igual en todas partes del núcleo y existe una superficie que actúa como frontera. Es decir, el modelo supone que el núcleo tiene un comportamiento similar al de una gota de líquido incompresible. Los nucleones en el núcleo jugarían el mismo papel que las moléculas de la gota. Funciona con propiedades características del tamaño nuclear y predice la estabilidad de los núcleos. Esta gota de líquido puede oscilar cambiando su forma si recibe una cantidad de energía adicional. Los estados excitados de los núcleos se corresponderían con estas configuraciones deformadas respecto de la fundamental. Para excitaciones suficientemente grandes, la oscilación de la gota podría dar lugar a su fragmentación en dos, lo que explicaría el mecanismo de la fisión nuclear. Antonio Zaragoza López Página 79 EL NÚCLEO ATÓMICO Este modelo nace como consecuencias de datos experimentales que necesitan complicados cálculos matemáticos (ecuaciones matemáticas) para su explicación. Enlaces http://www.fisicanet.com.ar/quimica/estructura_atomica/ap10_nucleo_ atomico.php http://cuentos-cuanticos.com/2014/05/04/el-nucleo-atomico-y-susmodelos/ --------------------------------- O ---------------------------------Antonio Zaragoza López Antonio Zaragoza López Página 80