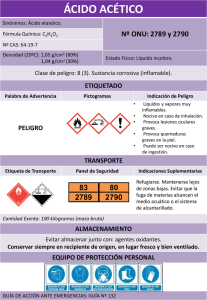
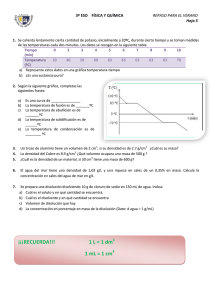
NTE INEN 2141: Conservas vegetales. Determinación
Anuncio

Re p u b l i co fEc u a d o r ≠ EDI CTOFGOVERNMENT± I no r d e rt op r o mo t ep u b l i ce d u c a t i o na n dp u b l i cs a f e t y ,e q u a lj u s t i c ef o ra l l , ab e t t e ri n f o r me dc i t i z e n r y ,t h er u l eo fl a w,wo r l dt r a d ea n dwo r l dp e a c e , t h i sl e g a ld o c u me n ti sh e r e b yma d ea v a i l a b l eo nan o n c o mme r c i a lb a s i s ,a si t i st h er i g h to fa l lh u ma n st ok n o wa n ds p e a kt h el a wst h a tg o v e r nt h e m. NTE INEN 2141 (1998) (Spanish): Conservas vegetales. Determinación cualitativa y cuantitativa del ácido benzóico y benzoatos alcalinos INSTITUTO ECUATORIANO DE NORMALIZACIÓN Quito - Ecuador NORMA TÉCNICA ECUATORIANA NTE INEN 2 141:98 CONSERVAS VEGETALES. DETERMINACIÓN CUALITATIVA Y CUANTITATIVA DEL ÁCIDO BENZÓICO Y BENZOATOS ALCALINOS. Primera Edición CANNED VEGETABLES. BENZOATES. QUALITATIVE AND QUANTITATIVE DETERMINATION OF BENZOIC ACID AND ALKALI First Edition DESCRIPTORES: Productos agroindustriales, conservas vegetales, análisis químico, determinación del contenido de ácido benzóico, método cualitativo, análisis por volumetría, absorción espectrométrica molecular. AL 02.01-329 CDU: 664.1.635:547.581.2:543.42 CIIU:3113 ICS: 67.080.20 CDU: 664.1.635:547.581.2:543.42 ICS: 67.080.20 CIIU: 3113 AL 02.01-329 Norma Técnica Ecuatoriana Voluntaria NTE INEN 2 141:98 CONSERVAS VEGETALES. DETERMINACIÓN CUALITATIVA Y CUANTITATIVA DEL ÁCIDO BENZÓICO Y BENZOATOS ALCALINOS 1998-07 1. OBJETO 1.1 Esta norma establece los métodos de ensayo para determinar cualitativa y cuantitativamente el ácido benzóico y benzoatos alcalinos de los productos elaborados a partir de frutas y vegetales. 2. ALCANCE 2.1 Los métodos son aplicables a productos elaborados de frutas y vegetales que contienen ácido benzóico y benzoatos alcalinos, especialmente a jugos de frutas, salsa y concentrado de tomate, jaleas y mermeladas, que contengan o no sal, y a productos preservados con ácido láctico y vinagre. 3. MÉTODO CUALITATIVO 3.1 Fundamento y resumen a) Fundamento. El método se basa en la reacción del ácido benzóico con el cloruro férrico, dando un precipitado de color rojizo que indica la presencia de ácido benzóico. b) Resumen. El método consiste en la homogeneización del producto, seguido de una dilución y acidificación de la porción de ensayo; extracción del ácido benzóico mediante éter etílico y posterior evaporación de la capa etérea; se alcaliniza con amoníaco, se elimina el exceso de amoníaco y se agrega cloruro férrico. 3.2 Reactivos o materiales 3.2.1 Solución (1 + 3) de ácido clorhídrico. 3.2.2 Éter etílico, grado reactivo. 3.2.3 Éter de petróleo, fracción que destila abajo de 60°C. 3.2.4 Solución acuosa neutra al 0,5 % de cloruro férrico. 3.2.5 Solución (1 + 9) de hidróxido de amonio. Para la prueba de Mohler: 3.2.6 Solución aproximadamente al 10% de NaOH. 3.2.7 Ácido sulfúrico concentrado, obtenida por dilución de 2 volúmenes de ácido sulfúrico concentrado, ρ20 = 1,84 g/cm3, con un volumen de agua. 3.2.8 Nitrato de potasio cristalizado. 3.2.9 Todos los reactivos deben ser de pureza analítica reconocida, y el agua usada debe ser destilada. (Continúa) _________________________________________________________________________________________________________ DESCRIPTORES: Productos agroindustriales, conservas vegetales, análisis químico, determinación del contenido de ácido benzóico, método cualitativo, análisis por volumetría, absorción espectrométrica molecular. -1- 1997-035 NTE INEN 2 141 1998-07 3.3 Equipo 3 3.3.1 Embudo de decantación, de 250 cm , 3 3.3.2 Probeta, de 50 cm , 3.3.3 Cápsula de porcelana, 3.3.4 Baño María, 3.3.5 Centrífuga, 3.3.6 Instrumental de laboratorio, Para la prueba de Mohler: 3.3.7 Baño de glicerina. 3.4 Procedimiento 3.4.1 Preparación de la muestra. 3.4.1.1 Líquidos no alcohólicos. Muchos líquidos pueden ser sometidos directamente a la extracción según 3.4.2, sin ningún tratamiento adicional. Si durante la extracción se forman emulsiones difíciles de separar, transferir con una pipeta volumétrica 100 cm3 de la muestra a un matraz volumétrico de 250 cm3, agregar aproximadamente 5 g de cloruro de sodio, agitar hasta dilución completa de la sal, ajustar el volumen con alcohol etílico de 95% (v/v), volver a agitar vigorosamente, dejar reposar durante 10 minutos, agitando ocasionalmente, filtrar y luego tratar una alícuota del filtrado de acuerdo a lo indicado en 3.4.1.2. 3.4.1.2 Líquidos alcohólicos. A un volumen de 200 cm3 de la muestra alcalinizar en presencia de papel indicador, mediante la adición de una solución aproximadamente al 10% de hidróxido de sodio; luego evaporar en baño de María hasta que el volumen se reduzca aproximadamente a 1/3 del volumen original y volver con agua destilada al volumen original de 200 cm3, filtrar si es necesario. 3.4.1.3 Sustancias sólidas y semisólidas. Moler y homogeneizar bien la muestra, transferir una cantidad conveniente de 50 a 200 g de acuerdo a la consistencia de la muestra a un matraz volumétrico de 500 cm3, agregar agua destilada hasta un volumen aproximadamente de 400 cm3 y agitar hasta lograr una mezcla homogénea. Agregar de 2 a 5 g de CaCl2 y agitar hasta que se disuelva. Alcalinizar en presencia de papel indicar con una solución aproximadamente al 10% de hidróxido de sodio; diluir con agua hasta la marca, agitar vigorosamente, dejar en reposo durante no menos de 2 h agitando ocasionalmente y luego filtrar. 3.4.2 Procedimiento analítico 3 3.4.2.1 Colocar en el embudo de decantación 50 cm de la muestra original o un volumen equivalente del extracto acuoso preparado como se indicó en 3.4, agregar 1/10 de dicho volumen de la solución (1 + 3) de ácido clorhídrico y extraer con 50 cm3 de éter etílico, agitar nuevamente y luego dejar decantar hasta separación en dos capas. 3.4.2.2 Si la mezcla se emulsifica, agregar de 10 a 15 cm3 de éter de petróleo y agitar. Si este tratamiento no rompe la emulsión, centrifugar o dejar reposar hasta que una porción considerable de la capa acuosa se separe; se elimina esta última, agitar vigorosamente y dejar separar otra vez. 3 3.4.2.3 Lavar dos veces la capa de éter con porciones de 5 cm de agua, cada vez, eliminando ésta después de cada lavado; luego transferir la fase etérea a la cápsula de porcelana, la cual se coloca en baño de María, cuando se haya separado la mayor parte del éter, retirar y dejar evaporar el resto a temperatura ambiente. (Continúa) -2- 1997-035 NTE INEN 2 141 1998-07 3.4.2.4 Si hay cantidades apreciables de ácido benzóico, éste se cristaliza en forma de hojitas las cuales producen un olor característico con el calentamiento. El residuo cristalino disolver en agua caliente y dividir en dos porciones, en las que se realizan las pruebas siguientes: 1. Prueba con cloruro férrico. Una de las porciones de 3.4.2.4 alcalinizar con pocas gotas de hidróxido de amonio, expeler el exceso de amonio por evaporación y luego disolver el residuo en pocos centímetros cúbicos de agua caliente, filtrar si es necesario y agregar pocas gotas de la solución al 0,5% de cloruro férrico. Un precipitado color rojizo de benzoato férrico indica la presencia de ácido benzóico. 2. Prueba modificada de Mohler. Esta prueba se realiza cuando la muestra contiene fenolftaleina, la cual interfiere en la prueba con cloruro férrico. En este caso se procede de la siguiente manera: a) A la otra porción de 3.4.2.4 agregar de 1 a 2 gotas de una solución aproximadamente al 10% de NaOH y evaporar hasta sequedad. b) Al residuo agregar 5 a 10 gotas de H2SO4, un pequeño cristal de KNO3 y calentar durante 10 minutos en un baño de glicerina a una temperatura de 120 a 130°C; cuidar que el baño no sobrepase la temperatura de 130°C. 3 c) Dejar enfriar, agregar 1 cm de agua caliente, añadir amoníaco hasta completa alcalinidad y hervir la solución para descomponer el NH4NO2 que puede formarse. d) Enfriar y agregar unas gotas de solución incolora, recién preparada de (NH4)2S, teniendo cuidado de que no se mezclen las dos capas de líquido, la formación de un anillo café rojizo entre las dos capas líquidas indica la presencia de ácido benzóico. NOTA. Al mezclar las dos capas el color se difunde a través de la solución y al calentar cambia a un color amarillo verdoso; éste cambio de coloración, debido a la presencia de ácido benzóico no se produce cuando se trata de ácido salicílico o de ácido cinámico, ya que estos dos ácidos forman compuestos coloreados que no se destruyen por el calentamiento. 4. MÉTODO CUANTITATIVO POR VOLUMETRÍA 4.1 Fundamento y resumen a) Fundamento. El método se basa en la dosificación del ácido benzóico por alcalimetría. b) Resumen. Consiste en extraer el ácido benzóico en medio ácido con cloroformo, eliminación del solvente por calentamiento, disolución del residuo en alcohol neutro y titulación del mismo con solución normalizada de hidróxido de sodio. NOTA. La presencia de vainillina interfiere con éste método, dando resultados erróneos. 4.2 Reactivos y materiales 4.2.1 Cloruro de sodio pulverizado 4.2.2 Lechada de cal, suspención acuosa de hidróxido da calcio, preparada con óxido de calcio recientemente apagado, suspención 1 en 3. 4.2.3 Solución al 10% de hidróxido de sodio 4.2.4 Solución saturada de cloruro de sodio 4.2.5 Solución (1 + 3) de ácido clorhídrico 4.2.6 Cloroformo (Continúa) -3- 1997-035 NTE INEN 2 141 1998-07 4.2.7 Alcohol neutralizado a la fenolftaleina 4.2.8 Solución alcohólica al 0,1 % de fenolftaleina 4.2.9 Solución 0,05 N de hidróxido de sodio 4.3 Equipo 4.3.1 Balanza analítica, con sensibilidad 0.1 mg 4.3.2 Pipetas volumétricas de 100 cm3 4.3.3 Matraz volumétrico, de 500 cm3 4.3.4 Varillas de vidrio 4.3.5 Cápsulas de porcelana 4.3.6 Erlenmeyer de 300 cm3 4.3.7 Desecador, con ácido sulfúrico concentrado 4.4 Procedimiento 4.4.1 Preparación de la muestra 4.4.1.1 Método general a) Mezclar perfectamente la muestra, moler si es sólida o semisólida y transferir 150 cm3 o 150 g al matraz volumétrico de 500 cm3. b) Agregar suficiente cloruro de sodio pulverizado para saturar el agua presente en la muestra. c) Alcalinizar al papel tornasol con la solución al 10% de hidróxido de sodio o con la lechada de cal y diluir a 500 cm3 con la solución saturada de cloruro de sodio. d) Agitar perfectamente y dejar en reposo por lo menos durante 2 horas agitando periódicamente y luego filtrar. NOTA 1. Si la muestra contiene grandes cantidades de grasa que puede contaminar el filtrado, agregar a éste una pequeña cantidad de la solución al 10% de NaOH y extraer con éter etílico antes de proceder como se indica en 4.4.2. NOTA 2. Si la muestra contiene alcohol, proceder como se indica en 4.4.1.4. 4.4.1.2 Salsa de tomate a) A 150 g de la muestra agregar 15 g de cloruro de sodio pulverizado y transferir la mezcla al matraz 3 volumétrico de 500 cm enjuagando el recipiente donde se hizo la pesada con aproximadamente 150 3 cm de la solución saturada de cloruro de sodio. b) Alcalinizar ligeramente al papel tornasol con la solución al 10% de hidróxido de sodio y completar al volumen con la solución saturada de cloruro de sodio. c) Dejar en reposo por lo menos 2 horas, agitando frecuentemente, luego pasar a través de una bolsa de muselina gruesa ejerciendo cierta presión, el líquido escurrido filtrar a través de papel filtro. (Continúa) -4- 1997-035 NTE INEN 2 141 1998-07 4.4.1.3 Jaleas y mermeladas a) Digerir 150 g de muestra en aproximadamente 300 cm3 de solución saturada de cloruro de sodio. b) Agregar 15 g de cloruro de sodio pulverizado y luego alcalinizar al papel tornasol con lechada de cal. 3 c) Transferir al matraz volumétrico de 500 cm y completar el volumen con la solución saturada de cloruro de sodio. d) Dejar en reposo durante no menos de 2 horas, agitando frecuentemente, luego centrifugar si es necesario y filtrar por papel filtro. 4.4.1.4 Productos conteniendo alcohol, tales como sidra, vinos y similares 3 a) A 250 cm de muestra alcalinizar al papel tornasol con la solución al 10% de NaOH y evaporar en un baño de María hasta aproximadamente un volumen de 100 cm3. b) Transferir a un matraz volumétrico de 250 cm3, agregar 30 g de cloruro de sodio pulverizado, agitar 3 hasta que se disuelva y diluir al volumen de 250 cm con la solución saturada de NaCl. c) Dejar en reposo durante no menos de 2 horas agitando frecuentemente y luego filtra en papel filtro. 4.4.2 Procedimiento analítico 4.4.2.1 Transferir por medio de una pipeta, una alícuota de 100 a 200 cm3 del filtrado preparado de acuerdo a lo indicado en 4.4 al embudo de decantación y neutralizar al papel tornasol con la solución (1 + 3) de ácido clorhídrico, agregando 5 cm3 de exceso. 4.4.2.2 Extraer cuidadosamente con cloroformo, usando porciones sucesivas de 70, 50, 40 y 30 cm3. Para evitar la formación de una emulsión agitar cuidadosamente después de cada adición, aplicándole un movimiento rotativo; por lo general, la capa de cloroformo se separa rápidamente después de dejarlo reposar unos pocos minutos. NOTA. Si se forma emulsión, se puede romper ésta mediante una de las siguientes maneras: a) Por agitación de la capa de cloroformo con una varilla de vidrio. b) Pasando la emulsión a un segundo embudo de decantación y dándole a éste 1 ó 2 movimientos bruscos de uno a otro extremo del embudo; o bien, c) Por centrifugación durante unos pocos minutos. 4.4.2.3 Debe tenerse cuidado al drenar la solución de cloroformo que esté lo más clara posible después de cada extracción sucesiva; es decir, no debe drenarse ninguna porción de emulsión con la capa de cloroformo. Si se toma esta precaución el extracto de cloroformo no necesita ser lavado. 4.4.2.4 Transferir los extractos combinados a una cápsula de porcelana, lavar el embudo de decantación varias veces con una pequeña cantidad de cloroformo, y evaporar a sequedad a la temperatura ambiente en una corriente de aire seco. 3 NOTA. El extracto también puede transferirse del embudo de dacantación a un Erlenmeyer de 300 cm , lavando el embudo con 3 porciones de 5 3 a 10 cm cada una de cloroformo, luego destilar muy lentamente a baja temperatura hasta un volumen aproximado a 1/4 del volumen original, 3 transferir el residuo a la cápsula de porcelana, lavando el matraz con 3 porciones de 5 a 10 cm de cloroformo, y finalmente evaporar a sequedad a la temperatura ambiente en una corriente de aire seco. 4.4.2.5 Secar el residuo durante la noche o hasta que ningún olor de ácido acético se pueda detectar cuando se trate de una muestra de salsa de tomate, colocando la cápsula en un desecador que contenga ácido sulfúrico. (Continúa) -5- 1997-035 NTE INEN 2 141 1998-07 4.4.2.6 Disolver el residuo de ácido benzóico en 30 a 50 cm3 de alcohol neutralizado a la fenolftaleina, agregar aproximadamente 1/4 de su volumen de agua destilada, una o dos gotas de la solución indicadora de fenolftaleina y titular con la solución 0,05 N de NaOH. 4.4.2.7 Esta determinación efectuar por duplicado. 5. CÁLCULOS 5.1 El contenido de ácido benzóico y benzoatos alcalinos en la muestra se expresa como benzoato de sodio anhidro, en porcentaje en masa, y se obtiene de acuerdo a la siguiente fórmula: 0,144 x V x N V1 Ab = ⎯⎯⎯⎯⎯⎯⎯ x ⎯⎯⎯⎯⎯⎯⎯- x 100 m V2 En donde: Ab = Porcentaje en masa de ácido benzóico y benzoatos alcalinos, expresado como benzoato de sodio anhidro. V = Volumen de la solución de NaOH, gastado en la titulación, en cm3 V1 = Volumen del filtrado final en la preparación de la muestra, en cm3, ver 4.4. Los valores son los siguientes: - método general, (ver 4.4.1.1), V1 = 500 - salsa de tomate, (ver 4.4.1.2), V1 = 500 - jaleas y mermeladas, (ver 4.4.1.3), V1 = 500 - sidra, vinos y similares, (ver 4.4.1.4), V1 = 250 V2 = Alícuota tomada para el ensayo, en cm3, ver 4.4.2.1 N = Normalidad de la solución de NaOH m = Masa de la muestra original, en gramos NOTA 1. En el caso de líquidos alcohólicos, numeral 4.4.1.4, este factor en vez de ser la masa de la muestra original, es el volumen de la 3 muestra original, en cm . En este caso, Ab es porcentaje en masa sobre volumen. 3 NOTA 2. 1 cm de solución 0,05 N de hidróxido de sodio equivale a 0,0072 g de benzoato anhidro. 5.2 Repetibilidad 5.2.1 La diferencia entre los resultados de dos determinaciones realizadas simultáneamente o en rápida sucesión por el mismo analista, no deberá se mayor del 5% del valor medio. 5.2.2 El resultado final será la media aritmética de las dos determinaciones, siempre que el requisito de repetibilidad se haya cumplido. (Continúa) -6- 1997-035 NTE INEN 2 141 1998-07 6. MÉTODO DE ABSORCIÓN ESPECTROMÉTRICA MOLECULAR 6.1 Alcance. Este método es aplicable con un contenido de ácido benzóico superior a 200 mg por litro o kilogramo de producto, y en particular, a jugos de frutas, puré o pasta de tomate, salados o no y a productos preservados con vinagre o ácido láctico. 6.2 Resumen. El método consiste en la extracción del ácido benzóico de una muestra de ensayo acidificada usando éter dietílico, nitración seguida de reducción, y reacción de Moholer modificada con hidrocloruro de hidroxilamina. Medida espectrométrica de la absorbancia del complejo rojo obtenido. 6.3 Reactivos. Todos los reactivos deben ser de calidad analítica reconocida y el agua a usarse debe ser destilada. 6.3.1 Ácido benzóico, solución estándar que corresponde a 1 g de ácido benzóico por litro. 3 Pesar, con aproximación de 0,0001 g, 100 mg de ácido benzóico. Disolver en 25 cm de una solución de 3 hidróxido de sodio 0,1 mol/l y diluir a 100 cm con agua. 1 cm3 de ésta solución estándar contiene 1 mg de ácido benzóico. 6.3.2 Solución de nitración. Disolver 23 g de nitrato de potasio en 250 cm3 de ácido sulfúrico concentrado (ρ20 = 1,84 g/cm3). 6.3.3 Hidrocloruro de hidroxilamina, 20 g/l de solución. 6.3.4 Solución de amoníaco, concentrado (ρ20 = 0,910 g/cm3). 6.3.5 Solución de fenolftaleína. Disolver 1 g de fenolftaleína en 100 cm3 de alcohol al 60 % (v/v). 6.3.6 Hidróxido de sodio, 1 mol/l de solución. 6.3.7 Hidróxido de sodio, 0,1 mol/l de solución. 6.3.8 Ácido sulfúrico, solución al 25 % (m/m). 6.3.9 Solución Carrez I. Disolver 150 g de ferrohexacianuro II potásico trihidratado [K4Fe(CN)6.3H2O] en agua y diluir a 1000 cm3. 6.3.10 Solución Carrez II. Disolver 300 g de sulfato de zinc heptahidratado (ZnSO4.7H2O) en agua y diluir a 1000 cm3. 6.3.11 Éter dietílico, recientemente destilado. 6.4 Equipo Equipo usual de laboratorio, y en particular 6.4.1 Embudos de separación, de 200 cm3 de capacidad, ajustado con tapones. 3 6.4.2 Pipetas, de 1,2,5,10,25 y 50 cm de capacidad. 3 3 6.4.3 Pipeta, de 2 cm de capacidad, graduada en divisiones de 0,1 cm . 6.4.4 Matraces volumétricos, de 10 y 100 cm3 de capacidad, ajustado con un tapón de vidrio. 6.4.5 Baño de agua caliente. (Continúa) -7- 1997-035 NTE INEN 2 141 1998-07 6.4.6 Tubos de ensayo, de 1,5 o 2,0 cm de diámetro. 6.4.7 Estufa, capaz de ser controlada 103 ± 2 oC. 6.4.8 Baño de agua, capaz de ser controlado a 20 ± 2 oC. 6.4.9 Baño de agua, capaz de ser controlado a 60 ± 2 oC. 6.4.10 Espectrómetro, adecuado para efectuar medidas a una longitud de onda de 533 nm, con celdas de trayectoria óptica de 10 mm de longitud. 6.5 Procedimiento 6.5.1 Preparación de la muestra de ensayo 6.5.1.1 Productos líquidos, mezclar completamente la muestra de laboratorio. 6.5.1.2 Productos semi-densos (puré, etc), mezclar completamente la muestra de ensayo. Prensar una parte de la muestra a través de cuatro capas finas de gasa, rechazar las primeras gotas de líquido y usar el remanente para la determinación. (Seguir las instrucciones dadas para productos líquidos). 6.5.1.3 Productos espesos, mezclar completamente la muestra de laboratorio. 6.5.2 Porción de ensayo 6.5.2.1 Productos líquidos, tomar, con una pipeta (6.4.2), 10 cm3 de la muestra de ensayo y transferir a un embudo de separación de 200 cm3 (6.4.1). 6.5.2.2 Productos espesos a) Pesar, con aproximación de 0,01 g, 10 g de la muestra de ensayo. b) Clarificación de la porción de ensayo, añadir una pequeña cantidad de agua a la porción de ensayo y alcalinizar añadiendo la solución de hidróxido de sodio (6.3.6) en presencia de la solución de fenolftaleína (6.3.5); colocar por 30 min en el baño de agua caliente (6.4.5); después de enfriar, transferir a un matraz volumétrico de 100 cm3 , añadir 2 cm3 de la solución Carrez I (6.3.9) y 2 cm3 de la solución Carrez II (6.3.10) y diluir hasta la marca con agua. Dejar en reposo por 30 min y luego centrifugar o filtrar. Usar esta solución clarificada para la extracción (6.5.3). 6.5.3 Extracción y purificación de ácido benzóico 3 6.5.3.1 Productos líquidos. Añadir 2 cm de la solución de ácido sulfúrico (6.3.8) a la porción de ensayo en el embudo de separación. Añadir 25 cm3 de éter dietílico (6.3.11), agitar y dejar en reposo hasta separación de la fase etérea. Repetir esta extracción agitando una vez mas con 25 cm3 de éter dietílico. combinar las dos fases etéreas. Extraer el ácido benzóico de la fase etérea sin lavar con agua, añadiendo 2 cm3 de la solución de hidróxido de sodio (6.3.6) en presencia de una gota de solución de fenolftaleína (6.3.5) y agitando por 5 min. Separar la fase alcalina. Luego extraer dos veces agitando con 2 cm3 de la solución de hidróxido de sodio (6.3.7). 3 Recolectar los extractos alcalinos en un matraz volumétrico de 10 cm (6.4.4) y diluir hasta la marca con agua. 6.5.3.2 Productos espesos. Añadir 50 cm3 de la solución de ácido sulfúrico (6.3.8) a 50 cm3 de la solución obtenida después de la clarificación (b). Añadir 50 cm3 de éter dietílico (6.3.11), agitar y dejar en reposo 3 hasta separación de la fase etérea. Repetir esta extracción dos veces más agitando con 50 cm de éter 3 dietílico. Combinar las fases etéreas en un embudo de separación de 200 cm (6.4.1). (Continúa) -8- 1997-035 NTE INEN 2 141 1998-07 3 3 Añadir 5 cm de agua, agitar y rechazar la fase acuosa. Añadir 2 cm de la solución de hidróxido de sodio (6.3.6) a la fase etérea y agitar (hasta aquí se habrá formado benzoato de sodio). Separar la fase alcalina. Luego extraer dos veces agitando con 2 cm3 de la solución de hidróxido de sodio (6.3.7). Recolectar los extractos alcalinos en un matraz volumétrico de 10 cm3 (6.4.4) y diluir hasta la marca con agua. 6.5.4 Determinación 6.5.4.1 Desarrollo del color 3 De acuerdo con el contenido de ácido benzóico esperado, transferir 0,5 a 1,0 cm del extracto alcalino a un tubo de ensayo (6.4.6) y evaporar hasta sequedad en el baño de agua caliente (6.4.5). Transferir a la estufa (6.4.7) y deshidratar por 15 min a 103 ± 2 oC. Dejar enfriar, añadir 1 cm3 de la solución de nitración (6.3.2) y colocar en el baño de agua caliente por 20 min, (es recomendable agitar al tubo de ensayo durante los primeros minutos). Transferir al baño de agua (6.4.8), manteniendo a 20 ± 2 oC por el tiempo de 15 min. Cuidadosamente añadir 2 cm3 de agua y dejar 15 min adicionales. Añadir 10 cm3 de la solución de amoníaco (6.3.4), añadiendo los primeros 5 cm3 en fracciones de 0,5 cm3 y el resto en fracciones de 1 cm3. Dejar en el baño de agua por 15 min, tener cuidado que la temperatura del baño de agua no exceda de 20 ± 2 oC. Añadir 2 3 cm de la solución de hidrocloruro de hidroxilamina (6.3.3) y colocar en el baño de agua (6.4.9), mantener la temperatura a 60 ± 2 oC por 5 min. 6.5.4.2 Medición espectrométrica Enfriar el tubo de ensayo, llenar una celda espectrométrica con la solución y medir la absorbancia a 533 nm en los siguientes 30 min por medio del espectrómetro (6.4.10). 6.5.5 Preparación de la curva de calibración 6.5.5.1 Preparación de los juegos de soluciones estándar En una serie de cinco tubos de ensayo, transferir por medio de la pipeta (6.4.3), los volúmenes de la solución estándar de ácido benzóico (6.3.1) indicados en la tabla. TABLA Volumen de la solución estándar de ácido benzóico 3 cm Correspondencia en masa de ácido benzóico mg 0,6 0,8 1,0 1,2 1,4 0,6 0,8 1,0 1,2 1,4 6.5.5.2 Desarrollo del color Transferir los tubos al baño de agua caliente (6.4.5) y evaporar hasta sequedad. Transferir los tubos a la estufa (6.4.7) y deshidratar por 15 min a 103 ± 2 oC. Continuar conforme a lo descrito en 6.5.4.1, desde el segundo párrafo que empieza con las palabras "[Dejar enfriar, añadir 1 cm3 de la solución de nitración (6.3.2)..."]. (Continúa) -9- 1997-035 NTE INEN 2 141 1998-07 6.5.5.3 Mediciones espectrométricas. Proceder conforme a lo explicado en 6.5.4.2. 6.5.5.4 Trazado de la curva. Trazar la curva teniendo, por ejemplo, en las abcisas los juegos de soluciones estándar de ácido benzóico, en microgramos, y en las ordenadas los valores correspondientes de la absorbancia. 6.5.6 Número de determinaciones Efectuar dos determinaciones en porciones de ensayo tomadas de la misma muestra de ensayo (6.5.1). 6.6 Expresión de los resultados 6.6.1 Método de cálculo y fórmula 6.6.1.1 Productos líquidos El contenido de ácido benzóico, expresado en miligramos por litro, se calcula mediante la expresión: m x V2 C = ⎯⎯⎯⎯⎯ x 1000 V1 x V3 En donde: C = contenido de ácido benzóico, en mg/l; m = masa del ácido benzóico, leída desde la curva de calibración, en mg; V1= volumen de la porción de ensayo, en cm3, es decir 10 cm3 (ver 6.5.2.1); V2= volumen del extracto alcalino, en cm3, es decir 10 cm3 (ver 6.5.3); V3= volumen del extracto alcalino tomado para el desarrollo del color, en cm3 (ver 6.5.4.1). 6.6.1.2 Productos espesos El contenido de ácido benzóico, expresado en miligramos por kilogramo, se calcula mediante la expresión: m2 x V1 x V3 C = ⎯⎯⎯⎯⎯⎯⎯⎯ x 1 000 m1 x V2 x V4 En donde: C = contenido de ácido benzóico, en mg/kg; m1= masa de la porción de ensayo, en g; m2= masa del ácido benzóico, leída desde la curva de calibración, en mg; V1= volumen de la solución clarificada preparada, en cm3, (ver 6.5.2.2); V2= volumen de la solución clarificada tomada para la extracción, en cm3, es decir 50 cm3 (ver 6.5.3.2); (Continúa) -10- 1997-035 NTE INEN 2 141 1998-07 V3= volumen del extracto alcalino, en cm3, es decir 10 cm3 (ver 6.5.3); 3 V4= volumen del extracto alcalino tomado para el desarrollo del color, en cm (ver 6.5.4.1). 6.6.2 Repetibilidad 6.6.2.1 La diferencia entre los resultados de dos determinaciones (6.5.6), realizadas simultáneamente o en rápida sucesión por el mismo analista, no deberá exceder 10 mg de ácido benzóico por litro o por kilogramo de producto. 6.7 Nota del procedimiento 6.7.1 La presencia de ácido fórmico y ácido sórbico no interfiere con la determinación de ácido benzóico. 6.8 Reporte del ensayo 6.8.1 El reporte del ensayo debe mostrar el método usado y los resultados obtenidos, además debe mencionar cualquier condición de operación no especificada en la presente norma, así como cualquier circunstancia que pueda haber influido en los resultados. 6.8.2 El reporte del ensayo debe incluir todos los detalles necesarios que permitan la completa identificación de la muestra. (Continúa) -11- 1997-035 NTE INEN 2 141 1998-07 APÉNDICE Z Z.1 DOCUMENTOS NORMATIVOS A CONSULTAR Esta norma no requiere de otras para su aplicación. Z.2 BASES DE ESTUDIO Norma ICAITI 34 003 h26 Productos elaborados a partir de frutas y hortalizas. Determinación cualitativa y cuantitativa del ácido benzoico y benzoatos alcalinos. Instituto Centroamericano de Investigación y Tecnología Industrial ICAITI, Guatemala 1975. International Standard ISO 6560. Fruit and vegetable products. Determination of benzoic acid content (benzoic acid contents greater than 200 mg per litre or per kilogram). Molecular absorption spectrometric method. Geneva 1983 -12- 1997-035 INFORMACIÓN COMPLEMENTARIA Documento: NTE INEN 2 141 TITULO: CONSERVAS VEGETALES. DETERMINACIÓN Código: CUALITATIVA Y CUANTITATIVA DEL ÁCIDO BENZÓICO Y AL 02.01-329 BENZOATOS ALCALINOS. ORIGINAL: REVISIÓN: Fecha de iniciación del estudio: Fecha de aprobación anterior por Consejo Directivo 1996-07-18 Oficialización por Acuerdo No. de publicado en el Registro Oficial No. de Fecha de iniciación del estudio: Fechas de consulta pública: de a Subcomité Técnico: Salsa de tomate Fecha de iniciación: 1997-01-10 Integrantes del Subcomité Técnico: Fecha de aprobación: 1997-06-13 NOMBRES: INSTITUCIÓN REPRESENTADA: Dra. Armanda Coronel Rivera (Presidente) INSTITUTO DE HIGIENE Y MEDICINA TROPICAL-GUAYAQUIL INSTITUTO DE INVESTIGACIONES TECNOLÓGICAS DE LA E.P.N. LA PORTUGUESA S.A. COMNACA TRIBUNA ECUATORIANA DE CONSUMIDORES Y USUARIOS INSTITUTO NACIONAL DE HIGIENE - QUITO DIRECCIÓN MUNICIPAL DE HIGIENE NESTLE ECUADOR S.A. ALISA ECUAVEGETAL S.A. DACA NESTLE ECUADOR S.A. INEN Dra. Rosario Barrera F. Ing. Helmut Nickel Garaicoa Ing. Juan Miniguano Michelle O. Fried Dra. Lucia Navas Dr. Hernan Riofrío Ing, Ramiro Valarezo Sr. Rodolfo Philco Dra. Susana Sánchez de Rojas Dr. Guido Martínez Ing. Jorge Arturo Gómez Ing. Bolívar Cano (Secretario Técnico) P.V.P. S/. 4 500,oo Otros trámites: CARÁCTER: Se recomienda su aprobación como: OPCIONAL Aprobación por Consejo Directivo en sesión de 1998-05-28 como: Voluntaria Oficializada como: VOLUNTARIA Por Acuerdo Ministerial No. 290 de 1998-06-23 Registro Oficial No. 363 de 1998-07-17 Instituto E c u a toria no d e N orma liz a c ión, IN E N - B a q u e rizo Mor e no E 8-29 y A v. 6 d e Dic ie mb r e C a silla 17-01-3999 - T e lfs: (593 2)2 501885 a l 2 501891 - F ax: (593 2) 2 567815 Dir e c c ión G e n e r a l: E-Ma il:furr e st a @ in e n.g ov.e c Á r e a T é c nic a d e N orma liz a c ión: E-Ma il:norma liz a c ion @ in e n.g ov.e c Á r e a T é c nic a d e C e rtific a c ión: E-Ma il:c e rtific a c ion @ in e n.g ov.e c Á r e a T é c nic a d e V e rific a c ión: E-Ma il:v e rific a c ion @ in e n.g ov.e c Á r e a T é c nic a d e S e rvic ios T e c noló gic os: E-Ma il:in e n c a ti @ in e n.g ov.e c R e gion a l G u a y a s: E-Ma il:in e n g u a y a s @ in e n.g ov.e c R e gion a l A zu a y: E-Ma il:in e n c u e n c a @ in e n.g ov.e c R e gion a l C himb or a zo: E-Ma il:in e nrio b a mb a @ in e n.g ov.e c U RL:w w w.in e n.g ov.e c