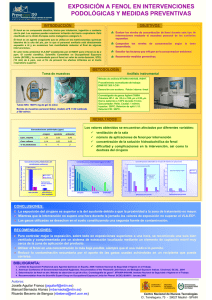
Estudio de la Oxidación Avanzada de Fenol en combinación con
Anuncio

UNIVERSIDAD SIMÓN BOLÍVAR DECANATO DE ESTUDIOS PROFESIONALES COORDINACIÓN DE INGENIERÍA QUÍMICA ESTUDIO DE LA OXIDACIÓN AVANZADA DE FENOL EN COMBINACIÓN CON CATALIZADORES DE ÓXIDOS DE HIERRO Por: ANGEL JAVIER SÁNCHEZ ROJAS INFORME DE PASANTÍA Presentado ante la Ilustre Universidad Simón Bolívar como requisito parcial para optar al título de Ingeniero Químico Sartenejas, Abril 2011 UNIVERSIDAD SIMÓN BOLÍVAR DECANATO DE ESTUDIOS PROFESIONALES COORDINACIÓN DE INGENIERÍA QUÍMICA ESTUDIO DE LA OXIDACIÓN AVANZADA DE FENOL EN COMBINACIÓN CON CATALIZADORES DE ÓXIDOS DE HIERRO Por: ANGEL JAVIER SÁNCHEZ ROJAS Realizado con la asesoría de: Tutor Académico: Prof. Oswaldo Núñez Tutor Industrial: Fernando Liendo INFORME DE PASANTÍA Presentado ante la Ilustre Universidad Simón Bolívar como requisito parcial para optar al título de Ingeniero Químico Sartenejas, Abril 2011 RESUMEN En el presente trabajo se estudió la degradación del compuesto orgánico Fenol, en presencia de luz UV (Ultravioleta), el oxidante peróxido de hidrógeno y el uso del catalizador sintetizado en Intevep. Para ello, se combinaron todos los efectos de reactivos antes mencionados y se logró establecer dosis óptimas para H2O2 y catalizador Intevep que aseguran una completa degradación del contaminante. Se variaron los parámetros de temperatura y pH de la reacción y se comprobó que el aumento del primero favorece la velocidad de reacción del proceso así como también la disminución del segundo; estas tendencias son similares al proceso fotofenton que posee un esquema auto catalítico, a pH menores de 3 por la generación de hierro (II) y (III) en solución, que se traducen en producción de radicales hidroxilos altamente oxidantes. Se comprobó que la cinética de reacción del proceso fotocatalítico sigue un modelo de primer orden y se ajustó al modelo propuesto por Langmuir-Hinshelwood. Se encontró que la constante de velocidad de pseudo-primer orden disminuyó con el aumento de la concentración inicial del compuesto orgánico. A su vez, se validó la eficiencia del proceso de fotocatálisis heterogénea evaluando el efecto de la introducción de otros catalizadores al proceso, así como también la introducción de ozono en presencia del catalizador de óxidos de hierro sintetizado en Intevep. Todos ellos como alternativas viables para el tratamiento de efluentes contaminados de la industria petrolera. iv Dedicado a: Dios, mi Madre, mi Padre y mi Hermana v AGRADECIMIENTOS Primeramente a Dios por darme la fuerza y confianza necesaria en mis estudios, por guiarme en mi vida, por acompañarme en los momentos más difíciles y llenarme de bendiciones hasta que sobre abunde, por ser siempre mi proveedor. A mis padres por apoyarme y guiarme en todos éstos años, por creer en mí siempre y sustentarme en todo momento. Por ser un ejemplo a seguir. A mi hermana por brindarme su apoyo, sus consejos, su disposición y animarme a seguir adelante. A mi familia: Henry, Eli, sobrinos, Abuelo Majin, abuela Herminia, primos y primas, tías y tíos. Por ser parte de mi vida, por llenarme de momentos de alegría y regocijo, por brindarme su amor y llenarme de consejos. A mis amigas Laurita, Olga, Katherine, Mary y Daniela por ser tan especiales conmigo, por compartir tantos momentos de alegría juntos, por apoyarnos en las largas noches de estudio, por su completa disposición a ayudarme y por cultivar tan apreciada amistad. A mis amigos de vivenciales: Raúl, Esteban, Reinaldo, Violette, Gabriel. Por acompañarme en estos años en la USB, por brindarme su amistad y compartir gratos momentos. A mi tutor Académico, Oswaldo Núñez por su completa disposición y ayuda en este trabajo. A mi tutor Industrial Fernando Liendo, por su apoyo en circunstancias críticas, por permitirme trabajar junto con él y aprender cosas interesantes. A la gente de la gerencia de Ambiente de Intevep: Aniuska, Carmen, Ricardo Lozada, Ricardo Harner, José, Armando, Francisco, por hacerme sentir bien en el trabajo, por estar pendiente de mis avances y ser grandes personas. A mis compañeros de pasantías en Intevep: Mariana, Carlos, Lisbeth, Perozo y Joel por ser tan panas y compartir momentos de angustia, distracción vi y alegría en ese tiempo. ÍNDICE GENERAL INTRODUCCIÓN………….……………………………………..……………………………….1 CAPÍTULO 1. DESCRIPCIÓN DE LA EMPRESA………………………………………..…3 1.1 Nombre de la empresa……………………………………………………………………...3 1.2 Ubicación de la empresa………………………………………………………………...……..3 1.3 Antecedentes de la empresa……………………………………………………………………3 1.4 Misión de la empresa………………..…………………………………………........................7 1.5 Visión de la empresa…………………………………………………………………………...7 1.6 Objetivos de la Empresa……………………………………………………………………….7 1.6.1 Objetivo general de la empresa…………………………………………………...................7 1.6.2 Objetivos específicos de la empresa……………………………………………………...........7 CAPÍTULO 2. FUNDAMENTOS TEÓRICOS…………………………………………………...9 2.1 Contaminación del Agua…………………………………………………………………........9 2.1.1 Impacto ambiental de la Industria petrolera……………………………………………........9 2.1.2 El Fenol como contaminante orgánico del petróleo……………………………………......10 2.1.2.1 Propiedades del Fenol…………………………………………………………………….10 2.2 Espectroscopia………………………………………………………………………………..11 2.3 Espectroscopia UV – Vis……………………………………………………………………..12 2.4 Cinética química……………………………………………………………………………...12 2.4.1 Catálisis en reacciones químicas…………………………………………………………...13 2.4.2 Concentración de las especies reactivas. Ley de Lambert Beer………………………........13 2.5 Tratamiento del agua……………………………………………………………………........14 2.5.1 Tratamiento Primario………………………………………………………………….........14 2.5.2 Tratamiento secundario…………………………………………………………………….14 2.5.3 Tratamiento Terciario………………………………………………………………………15 2.5.4 Oxidación Avanzada………………………………………………………………………..15 2.6 Clasificación de los Procesos de Oxidación Avanzada………………………………………16 2.7 Tecnologías avanzadas de oxidación fotoquímicas…………………………………………..17 2.7.1 Fotólisis directa……………………………………………………………………………..17 2.7.2 Fotólisis del agua en el ultravioleta de vacío (UVV)…………………………………........18 vii 2.7.3 UV/H2O2 …………………………………………………………………………………...18 2.7.4 UV/O3 ……………………………………………………………………………………...19 2.7.5 Foto – Fenton………………………………………………………………………….........20 2.7.6 Ventajas de las Tecnologías de Oxidación Avanzada……………………………………...21 2.8 Semiconductores con actividad fotocatalítica………………………………………………..22 2.9 Fotocatálisis Heterogénea……..……………...…………………………………………...........23 CAPÍTULO 3. MARCO METODOLÓGICO……………………………………………………25 3.1 Fase de inicio…………………………………………………………………………………25 3.1.1 Reactivos Químicos, Equipos e instrumentos de análisis…………………………………..25 3.1.2 Métodos de análisis………………………………………………………………………...28 3.1.2.1 Caracterización de Fenol……………………………………………………………........28 3.1.2.2 Método colorimétrico 4-amino antipirina. Standard Methods 5530D (Modificada)……..……………………………………………………………………………….29 3.1.2.3 Curva de calibración de Fenol……………………………………………………………30 3.1.2.4 Determinación de la concentración de Peróxido de Hidrógeno……………………... ….30 3.2 Fase de Ejecución…………………………………………………………………………….31 3.2.1 Esquema de montaje Experimental………………………………………………………...32 3.2.2 Toma de muestras para cada experiencia………………………………………………….33 3.2.3 Fotólisis de la solución……………………………………………………………………..33 3.2.4 H2O2 en solución…………………………………………………………………………...34 3.2.5 H2O2 + catalizador…………………………………………………………………….........34 3.2.6 H2O2+ UV…………………………………………………………………………………..34 3.2.7 H2O2+ UV + Catalizador…………………………………………………………………...34 3.2.8 Síntesis de catalizador TiO2-Fe…………………………………………………………….35 3.3 Fase de Análisis de resultados………………………………………………………………..35 3.4 Fase de cierre…………………………………………………………………………………35 CAPÍTULO 4. RESULTADOS Y DISCUSIÓN………………………………………………...36 4.1 Curva de Calibración de Fenol……………………………………………………………….36 4.2 Balance de masa. …………………………………………………………………………….37 4.3 Fotólisis de solución acuosa………………………………………………………………….37 viii 4.4 Peróxido de Hidrógeno en solución…………………………………………………………..38 4.5 Peróxido de Hidrógeno + Catalizador Intevep……………………………………………….39 4.6 Peróxido de Hidrógeno + UV………………………………………………………………...40 4.7 Determinación de dosis óptimas de H2O2 y Catalizador Intevep…………………………….41 4.8 Peróxido de Hidrógeno + UV + Catalizador Intevep………………………………………...42 4.8.1 Variación de pH……………………………………………………………………….........45 4.8.2 Variación de la concentración de Fenol……………………………………………….........46 4.8.3 Variación de temperatura de reacción……………………………………………………50 4.8.4 Variación de Catalizadores…………………………………………………………………51 4.9 Efecto de Ozono en solución……………………………………………………………...........53 4.10 Mecanismo de reacción……………………………………………………………………..54 CONCLUSIONES………………………………………………………………………………..56 RECOMENDACIONES……………………………………………………………………........57 REFERENCIAS BIBLIOGRAFICAS…………………………………………………………...58 BIBLIOGRAFÍA…………………………………………………………………………………59 ix ÍNDICE DE TABLAS Tabla 2.1 Propiedades fisicoquímicas del Fenol…………………………….…………………...10 Tabla 2.2 Potenciales redox de algunos agentes oxidantes………………………….…………...16 Tabla 4.1 Constantes de velocidad de pseudo-primer orden determinadas para la fotocatálisis heterogénea del Fenol………………………...………………………………………….……….47 Tabla 4.2 Velocidad inicial de reacción para la fotocatálisis del Fenol….………………………49 Tabla 4.3 Constantes de velocidad y equilibrio de adsorción para el modelo de Langmuir Hinshelwood…………………………………………………………………...............................50 Tabla 4.4 Constantes de velocidad de pseudo-primer orden para proceso fotocatálisis heterogéneo………….………………..…………………………………………………………..51 Tabla 4.5 Constantes de velocidad de pseudo-primer orden para cada catalizador...…….……...52 Tabla 4.6 Constantes de velocidad de pseudo-primer orden para degradaciones con Ozono…....54 x ÍNDICE DE FIGURAS Figura 2.1 Estructura molecular del Fenol……………………………….………………………10 Figura 2.2 Espectro Electromagnético………………………………………..…………………..11 Figura 2.3 Transiciones electrónicas de compuestos orgánicos en la región UV – Vis………….12 Figura 2.4 Estructuras de bandas y distribución de electrones para un metal y semiconductor intrínseco…………………………………………………………………………………………22 Figura 2.5 Procesos que ocurren en la interfase Semiconductor – electrolito bajo irradiación......24 Figura 3.1 Espectrofotómetro……………………………………………………………….........26 Figura 3.2 Lámpara UV………………………………………………………………………..…26 Figura 3.3 Bomba peristáltica…………………………………………………..………………...26 Figura 3.4 Tanque reservorio………………………………………………………..……………27 Figura 3.5 pH metro digital…………………………………………………………….………...27 Figura 3.6 Balanza digital…………………………………………………………………..…….27 Figura 3.7 Motor de vacio monofásico…………………………………………………………...28 Figura 3.8 Ozonador de descarga eléctrica…..…………………………………………………...28 Figura 3.9 Preparación de soluciones de Fenol para curva de calibración………………….........30 Figura 3.10 Montaje experimental……………………………………………………..................32 xi Figura 3.11 Montaje del laboratorio………………………………………………………...........32 Figura 4.1 Curva de calibración para el Fenol. A una longitud de onda λ= 500 nm……………..36 Figura 4.2 Balance de masa del sistema para 5 ppm de Fenol…………………………………...37 Figura 4.3 Efecto de luz UV en solución de 5 ppm Fenol…………..……………………………38 Figura 4.4 Efecto de la introducción de H2O2 en solución de 5 ppm de Fenol…….…………….39 Figura 4.5 H2O2 + Catalizador de óxido de hierro en solución de 5 ppm de Fenol…….………..39 Figura 4.6 Degradación de Fenol en presencia de Peróxido de hidrógeno y luz UV………..…...40 Figura 4.7 Variación de dosis de catalizador en función del porcentaje de degradación de Fenol a 5 ppm para soluciones de 200 mL…………………………………………………......................41 Figura 4.8 Degradación de Fenol a 5 ppm variando dosis de H2O2 en solución…………………42 Figura 4.9 Degradación de 5 ppm de Fenol utilizando UV,H2O2 y catalizador de óxidos de hierro……………………………………………………………………………………………...43 Figura 4.10 Mecanismo de degradación Fotocatálisis Heterogénea……………………………..44 Figura 4.11 Efectos combinados de reactivos en la degradación de Fenol…………………........45 Figura 4.12 Variación de pH para ensayos de H2O2 + UV + Catalizador………………………..45 Figura 4.13 Degradación de Fenol variando su concentración…………………………………...46 Figura 4.14 Degradación de Fenol a diferentes concentraciones………………………………...47 xii Figura 4.15 Determinación de la velocidad inicial de reacción para la degradación de Fenol. [Fenol]0= 10 ppm, [Catalizador]= 1,4 g; pH= 3,0; T=50°C……………………………………...48 Figura 4.16 Linealización del modelo cinético de Langmuir-Hinshelwood para la fotocatálisis heterogénea de Fenol……………………………………………………………………………..49 Figura 4.17 Degradación de Fenol utilizando H2O2, UV y catalizador de hierro a diferentes temperatura de reacción…………………………………………………………………………..50 Figura 4.18 Degradación de 5 ppm de Fenol en presencia de varios catalizadores……………...52 Figura 4.19 Degradación de 5 ppm Fenol utilizando Ozono [5ppm]……………………….........53 Figura 4.20 Mecanismo de oxidación fotocatalítica del Fenol…………………………………...55 xiii LISTA DE SÍMBOLOS Y NOMENCLATURA Ai: Absorbancia de la especie i b: Longitud de camino óptimo C: Concentración de Fenol Co: Concentración inicial de Fenol Ci: Concentración de la especie i εi: Coeficiente de absortividad molar de la especie i hv: Luz ultravioleta kobs: Constante de velocidad observada de pseudo-primer orden Ki: Constante de equilibrio de adsorción del modelo Langmuir Hinshelwood de la especie i ki: Constante de velocidad del modelo de Langmuir Hinshelwood de la especie i Q: Caudal de flujo ra: Velocidad de reacción de la especie A ro: Velocidad de reacción inicial UV: Ultra violeta UVV: Ultravioleta de vacío t: Tiempo xiv 1 INTRODUCCIÓN La preocupación del hombre por el medio ambiente se limitó, hasta la revolución industrial, a su adaptabilidad al medio y a su protección contra fenómenos naturales. Los grandes y acelerados cambios tecnológicos e industriales han traído consigo nuevas amenazas al medio ambiente, motivadas por las modernas actividades humanas. Por tal razón, la conciencia ambientalista nace del reconocimiento por parte de la sociedad civil y demás entes gubernamentales del impacto ambiental que generan dichas actividades industriales, además de reconocer que su impacto va más allá de la esfera nacional y se convierte en un problema con influencia a escala planetaria. Dentro de las actividades modernas que se llevan a cabo a nivel mundial, se encuentra la industria petrolera. La cual genera contaminación de los cuerpos de agua por efluentes provenientes de la industria de los hidrocarburos. Dicha contaminación suele suceder en las diferentes etapas necesarias para la industria. Desde la etapa inicial de exploración, que involucra materiales potencialmente contaminantes del entorno geográfico (ácidos, formulaciones de lodo base agua y base aceite) necesarios para la estimulación y perforación exitosa de los pozos productores, los cuales contaminan suelos superficiales y subterráneos, aguas superficiales y subterráneas y el aire. Seguidamente la etapa de transporte del crudo a los sistemas de almacenamiento para su posterior refinación, en ésta etapa está latente la posibilidad de derrames de crudo debido a la fatiga de tuberías, bombas, tanques de almacenamiento. Luego una vez que el crudo llega a la refinería se inicia una de las fases más críticas para la generación de una matriz de contaminación. Dado que se maneja un alto volumen de crudo y se inicia una serie de procesos y operaciones para la transformación del mismo, dichas operaciones involucran corrientes de materiales necesarios para la obtención de los productos refinados, consecuentemente se generan aguas residuales de la refinería con altos contenidos en compuestos orgánicos e inorgánicos que deben ser tratados eficazmente antes de su deposición al ambiente. Finalmente en la etapa de comercialización y transporte de productos está latente la posibilidad de derrames por tuberías y tanques. Como remediación para agua contaminadas se dispone de tratamientos biológicos o tratamientos químicos convencionales, sin embargo, la generación de compuestos más tóxicos y complejos en la industria han provocado que el tratamiento biológico y otras técnicas suelan ser 2 lentas o insuficientes para la descontaminación de las aguas, es por ello, que se busca emplear procesos alternativos para el tratamiento de efluentes contaminados que complementen los procesos existentes y contribuyan a realizar cambios profundos en la estructura de los contaminantes para su limpieza. Los procesos de oxidación avanzada son una herramienta eficaz que contribuye como atractiva solución para tratamiento de agua. Entre los procesos de oxidación avanzada se encuentra el uso de catalizadores de óxidos de hierro en presencia de peróxido de hidrógeno y UV, el cual contribuye a degradar la materia orgánica mediante la generación de radiales libres OH· que atacan los sustratos orgánicos y logran en muchos casos 100 % desaparición del contaminante. El presente estudio consistió en degradar el Fenol que es un típico compuesto orgánico presente en las aguas provenientes de la industria petrolera, se verificó la eficiencia del proceso de oxidación avanzada utilizando hierro en solución que constituye un metal que se encuentra en grandes cantidades en minerales en Venezuela, en presencia de peróxido de hidrógeno que es fácil de manejar y ambientalmente benigno y luz UV. Adicionalmente se evaluó la eficiencia de la introducción del oxidante ozono en presencia del catalizador de óxidos de hierro, como posible tecnología a utilizar para el tratamiento de efluentes contaminados. Los objetivos del trabajo consideran los siguientes aspectos: 1. Estudiar la degradación fotocatalítica del Fenol en función del pH, la concentración inicial del sustrato orgánico y la masa del catalizador. 2. Obtener los parámetros cinéticos del modelo de Langmuir–Hinshelwood como posible modelo cinético para explicar la fotocatálisis. 3. Evaluar la influencia de la temperatura en la degradación de Fenol. 4. Estudiar el efecto de la introducción de diferentes catalizadores (Magnetita, TiO2-Fe) en la degradación del Fenol CAPÍTULO 1 DESCRIPCIÓN DE LA EMPRESA 1.1 Nombre de la empresa INTEVEP, S.A., Centro de Investigación y apoyo Tecnológico. Filial de PDVSA 1.2 Ubicación de la empresa La empresa se encuentra ubicada en los Altos Mirandinos. Urbanización Santa Rosa. Sector el Tambor. Ciudad de Los Teques. Estado Miranda. Caracas. Venezuela. 1.3 Antecedentes de la empresa Período 1973-78: A través de la promulgación del Decreto Presidencial No. 1385, se creó la Fundación para la Investigación de Hidrocarburos y Petroquímica lo que abrió el camino a lo que hoy constituye el centro de investigación científica y apoyo tecnológico de la Industria petrolera nacional. En febrero de 1974, se instaló la Fundación para la Investigación en Hidrocarburos y Petroquímica, Invepet. En 1976, aún manteniendo la figura jurídica de Fundación, se cambió su denominación a la actualmente conocida: Intevep. PDVSA se convirtió en su patrocinante. Igualmente en 1976, se iniciaron los primeros proyectos de investigación y desarrollo (IyD) definidos como prioritarios para la Industria. En este sentido, el Consejo de Administración aprobó la constitución de seis gerencias técnicas: Ciencias de la Tierra, 4 Ingeniería General, Ingeniería de Petróleo, Ciencias Básicas, Ingeniería de Procesos, y Computación y Sistemas. En 1977, se incorporó un grupo de 75 profesionales y técnicos del Centro de Petróleo y Química del IVIC, para establecer una estructura organizativa que comprende tres divisiones: Exploración y Producción, Refinación y Petroquímica, y Administración y Servicios. Entre julio y agosto de 1978, se efectuó la mudanza a su actual sede, lo que permitió dotar y poner en marcha un significativo número de laboratorios. Período 1979-1984 En junio de 1979, Intevep se constituyó como empresa mercantil, filial de Petróleos de Venezuela, lo cual permitió adoptar políticas y actividades administrativas alineadas con la Corporación. En 1980, Intevep se enfrentó a dos retos fundamentales: ejecutar los programas de Ingeniería y Diseño ya establecidos, y continuar la formación del equipo humano y la infraestructura requerida para los mismos. Los esfuerzos tecno - científicos se concentraron en las áreas de mayor importancia para la Industria. En 1983, se diseñó el Modelo Geológico de la Faja del Orinoco, se seleccionó el proceso propio de mejoramiento de crudos pesados y se realizó el estudio de las refinerías del Caribe. Adicionalmente, se creó la Unidad de Petroquímica y se estableció un programa definido de asistencia a Pequiven. El programa de Control de Calidad fue uno de los logros resaltantes, así como la creación de la Red de Información Petrolera y Petroquímica, RIPPET. En 1984, Intevep mostró un notable avance en el desarrollo de una tecnología propia para el mejoramiento de crudos pesados: HDH®, y en el desarrollo y optimización de métodos para el transporte superficial de crudos pesados y extrapesados, actividades que situaron a la Industria en una posición de liderazgo en cuanto a este tipo de investigaciones en el ámbito mundial. 5 Periodo 1985-1989 Durante 1985, se mantuvo el énfasis en áreas de transporte y mejoramiento de crudos pesados y extrapesados, recuperación adicional de crudos livianos y medianos, utilización de materiales residuales, apoyo a procesos de refinación y asesoría en control de calidad. En 1986, la tecnología de emulsiones para la producción y manejo de crudos pesados fue integrada efectivamente a las operaciones de la Industria. El proceso de mejoramiento HDH® fue validado en su fase de planta piloto lo cual permitió adelantar el desarrollo de la ingeniería básica de un módulo comercial. En 1987, PDVSA decidió ampliar la misión de Intevep, asignándole la responsabilidad de centralizar las actividades de ingeniería básica y la prestación de servicios técnicos operacionales avanzados a la Corporación. En 1998, se registraron avances fundamentales en áreas estratégicas de la Industria. En efecto, productos y procesos generados en Intevep entran en fase de implantación operacional: el producto Orimulsión entró a su fase de comercialización, se completaron con éxito las pruebas piloto de transporte mediante Flujo Anular®, finaliza el desarrollo tecnológico de coque y aleaciones con alto contenido de vanadio, así como las pruebas del proceso HHC™ y de los catalizadores requeridos. Adicionalmente, se introdujo en el mercado nacional un aceite lubricante formulado en Intevep y se cumplieron las pruebas de demostración del proceso de mejoramiento HDH®. Durante el año de 1989, en respuesta al cambio de alcance en las actividades de Intevep, se dio a la Empresa una nueva denominación: Intevep, S.A., Centro de Investigación y Apoyo Tecnológico. Período 1990-1995 En 1990, se adquirieron los derechos de uso de la tecnología Etherol, de la British Petroleum, para la producción de éteres a ser utilizados en el mejoramiento de octanaje de las gasolinas y reemplazar el tetra etilo de plomo. Intevep recibe el primer premio en Tecnología, de la Academia de Ciencias del Tercer Mundo (TWAS), por el desarrollo de la tecnología Imulsión, además de otros prestigiosos galardones. 6 Se completaron importantes convenios de cooperación con diversas universidades venezolanas (UCV, ULA, USB y UCAB), tanto para el trabajo conjunto en actividades de Investigación y Desarrollo, como para el fortalecimiento de especialidades académicas afines al campo científico -técnico. En 1991, el desarrollo del proceso HDH® fue merecedor del Premio de Ciencias de la UNESCO y recibió la aprobación, por parte de PDVSA, para construir la planta pionera en la Refinería Cardón, con una capacidad de 15 mil barriles diarios. Período 1995-1999 Durante estos años, Intevep se mantuvo estable en cuanto a la crearon nuevos proyectos de apoyo a la industria petroleras venezolana. Igualmente, Intevep afianzó sus relaciones con el sector de ciencia y tecnología, a través de convenios para el desarrollo de trabajos conjuntos con las universidades nacionales, el Ministerio de Ciencia y Tecnología, Instituto Venezolano de Investigaciones Científicas (IVIC), Funvisis, Fundación Instituto Ingeniería, IUT Región Capital, entre otros. Período 2000-Actualidad: Intevep jugó un papel significativo durante la contingencia de finales de 2002 y comienzos de 2003, cuando numerosos técnicos, especialistas y gerentes de la Empresa asumieron voluntariamente la enorme responsabilidad de apoyar directamente las diferentes áreas afectadas por la acción del paro petrolero. Gracias a este apoyo, refinerías, plantas, campos e instalaciones en general, se mantuvieron operativas durante la crisis más dura que vivió la Corporación durante su historia. Juegan papel importante acciones como la certificación de combustibles, los equipos de respuesta rápida, los entrenamientos in situ a las personas que recién ingresaban, instrumentación de refinerías y atención a daños ambientales entre varias actividades. Actualmente, Intevep continúa su importante labor como centro de soporte técnico y científico de la industria petrolera, bajo el lema de “Soberanía Tecnológica”, sin olvidar el 7 papel de gran relevancia que le corresponde en el plano al respaldar y ejecutar cada uno de los programas que desarrolla el Gobierno Bolivariano. 1.4 Misión de la empresa Preservar el patrimonio de PDVSA y sus empresas filiales, mediante la ejecución de acciones preventivas y correctivas, enmarcadas en el principio de corresponsabilidad, contribuyendo así a la continuidad del negocio y al desarrollo integral de la nación. 1.5 Visión de la empresa Ser la Organización líder en materia de seguridad, capaz de adaptarse a las exigencias que presente PDVSA y sus nuevos negocios. 1.6 Objetivos de la Empresa 1.6.1 Objetivo general de la empresa Proporcionar soluciones en materia de seguridad de manera oportuna y confiable que satisfagan las necesidades de nuestros clientes a través de una gestión fundamentada en el desarrollo armónico e integral de nuestro personal, la implantación de tecnología de vanguardia y en la mejora continua de nuestros procesos. 1.6.2 Objetivos específicos de la empresa Desarrollar tecnologías que permitan incrementar el factor de recobro. Generar soluciones tecnológicas integrales a la medida de los negocios, con especial énfasis en crudos pesados y extrapesados. Apoyar el desarrollo de Gas Costa Afuera en el país. Impulsar y garantizar la correcta gestión ambiental de las operaciones de PDVSA. Desarrollar tecnologías de refinación dirigidas a procesar dietas de crudos pesados. 8 Fortalecer las relaciones de cooperación en las áreas de ciencia y tecnología entre PDVSA, las universidades y otras instituciones, para elaborar propuestas de valor. Establecer nuevos esquemas para adoptar tecnologías de punta. Fortalecer la explotación en áreas cercanas a desarrollos actuales. Apalancar el desarrollo endógeno sostenible. Cerrar brechas para garantizar el logro de objetivos. Mantener una permanente comunicación con los clientes y proveedores internos y establecer los acuerdos de niveles de servicios. Incorporar y operar soluciones de seguridad con tecnología de punta y bajo standards abiertos. Reducir sistemáticamente el riesgo en las instalaciones y los procesos de la corporación. CAPÍTULO 2 FUNDAMENTOS TEÓRICOS En el presente trabajo se establecen las bases principales que apoyan y fundamentan la investigación científica llevada a cabo, por lo que se presentan los conceptos mínimos necesarios para el entendimiento y justificación de la misma. 2.1 Contaminación del Agua El agua es un recurso vital para los seres vivos, su influencia en el desarrollo, sostenimiento y calidad de vida en los seres humanos es indiscutible. Se considera que el agua se encuentra contaminada cuando se ven alteradas sus propiedades físico–químicas, biológicas y composición debido a la intervención de materias extrañas como: microorganismos, productos químicos, residuos industriales, materia orgánica, sustancias radioactivas y calor, entre otras. Dichos contaminantes pueden traer efectos nocivos para la salud de las personas y comprometen el desarrollo de ecosistemas naturales. 2.1.1 Impacto ambiental de la Industria petrolera La industria petrolera tiene una importante incidencia en la contaminación del medio ambiente, las actividades de exploración, extracción, refinación y transporte del petróleo involucra una serie de procesos con gran impacto ambiental que se traduce en la contaminación de aguas de producción asociadas a las distintas actividades. Trayendo consecuencias a las comunidades cercanas y en general a los ecosistemas y medio ambiente. En Venezuela el crudo se caracteriza por poseer alta viscosidad, alto contenido de metales pesados, alto contenido de metales de azufre y de nitrógeno, y en general altos contenidos de compuestos saturados, aromáticos, poliaromáticos, resinas y asfaltenos. Algunos de los cuales son altamente tóxicos. 10 2.1.2 El Fenol como contaminante orgánico del petróleo El Fenol es un hidrocarburo aromático cuya base es el benceno y posee un grupo hidroxilo como sustituyente, su estructura se representa en la Figura 2.1 como sigue: Figura 2.1 Estructura molecular del Fenol [1] Es un poderoso bactericida, es tóxico en concentraciones de (1- 10) ppm en aguas. Su toxicidad, depende de la tolerancia natural que posean los organismos expuestos, de sus características ecofisiológicas y de los grupos funcionales que se enlazan al anillo lo cual le puede proporcionar un mayor o menor grado de toxicidad y biodegradabilidad. Los fenoles están presentes en los desechos industriales de: químicos orgánicos, plásticos y sintéticos, refinerías petroleras, plantas de coke (hierro y acero), jabones y detergentes, textiles oxidado por el ozono. 2.1.2.1 Propiedades del Fenol Las propiedades del fenol se resumen a continuación (Tabla 2.1): Tabla 2.1 Propiedades fisicoquímicas del Fenol [1] Constantes Peso Molecular Punto de Fusión (a 760 mmHg) Punto de Ebullición (a 760 mmHg) Gravedad Específica (a 25 °C) Punto de Ignición Punto de Inflamación Temperatura crítica Presión crítica Densidad del vapor (aire = 1) Valores 94,11 40,9 °C 181,9 1078 715 °C 79,4 °C 419 °C 60,5 atm 3,24 11 El Fenol representa el contaminante en estudio realizado en esta investigación, de allí la importancia de conocerlo y saber sus características, así como impacto al ambiente y seres humanos. 2.2 Espectroscopia La espectroscopia molecular se define como el estudio de la interacción entre la luz y la materia. La luz puede considerarse como una onda en movimiento producida por la oscilación de campos eléctricos y magnéticos. Además de la naturaleza ondulatoria, la luz está formada por un conjunto de partículas denominadas fotones. Si una muestra es sometida a radiación electromagnética, se pueden producir cambios en los estados energéticos de los átomos o moléculas que conforman el material. Estos cambios energéticos están asociados a procesos de absorción o emisión de radiación electromagnética. El espectro electromagnético se divide en varias zonas de acuerdo a la longitud de onda (Figura 2.2). Figura 2.2 Espectro Electromagnético [2] Las regiones de mayor interés del espectro electromagnético para el tratamiento de agua son UV – Vis. La radiación UV se divide en tres categorías: UV – A, entre 320 nm y 400 nm UV – B, entre 280 nm y 320 nm UV – C, entre 200 nm y 280 nm VUV: “Vacum” UV: UVV: UV Vacío: entre 40 nm y 200 nm La región Visible va desde 400 nm hasta 800 nm 12 2.3 Espectroscopia UV – Vis La energía absorbida en la región UV – Vis produce cambios en la energía electrónica de la molécula producto de las transacciones de los electrones de valencia en la molécula. Estas transacciones consisten en la excitación de un electrón desde un orbital molecular al siguiente orbital de mayor energía. Estos compuestos se conocen como cromóforos. Las transiciones observadas frecuentemente en la región UV – Visible corresponden a electrones implicados en enlaces σ o π y en pares no enlazantes n de átomos de hidrógeno, carbono, nitrógeno y oxígeno. Las transiciones de menor energía, π π* y n en un espectrofotómetro común, mientras que la de mayor energía σ n*, se observan σ* y n σ* suelen aparecer en el ultravioleta lejano. La Figura 2.3 muestra el requerimiento energético de estas transiciones y su zona de absorción típica. Figura 2.3 Transiciones electrónicas de compuestos orgánicos en la región UV – Vis 2.4 Cinética química La cinética química permite conocer la variación de la velocidad con la que ocurre una reacción química, en base a esto, se puede conocer la rapidez con que se transforman ciertos reactivos químicos en productos (Ecuación 2.1). Dicha estimación se evalúa mediante una ley de velocidad que permite relacionar la velocidad de una reacción química en función de las concentraciones de las especies involucradas en un tiempo dado. El modelo matemático que permite simular el efecto deseado considera volumen de reacción constante y se define como (Ecuación 2.2): 13 (2.1) (2.2) Con el fin de encontrar la ley de velocidad que define una reacción química, se determina de forma continua la concentración de un reactivo o un producto en función del tiempo y se realiza un análisis de regresión para ajustar los datos a una ecuación de velocidad adecuada. Si la concentración de uno de los reactivos es mucho menor que la de las otras especies químicas se puede considerar el ajuste de la ley de velocidad a una ecuación de pseudo-primer orden. Si existe una reacción con catálisis heterogénea se puede usar el modelo Langmuir Hinshelwood. De igual manera, se puede obtener información de la rapidez de una reacción a través del cálculo de la pendiente de la curva concentración vs tiempo, por el método de las concentraciones iniciales, es decir, midiendo la pendiente a los inicios de la reacción. 2.4.1 Catálisis en reacciones químicas Un catalizador es una especie química que dentro de un proceso catalítico reacciona con las sustancias reactivas promoviendo un mecanismo alterno de reacción que favorece la transformación de los reactivos a productos, mediante la disminución de la barrera energética que permite la formación de los mismos. Existen dos tipos importantes de catálisis, la homogénea y la heterogénea, en la catálisis homogénea el catalizador se encuentra en la misma fase que las especies reactantes; y en la catálisis heterogénea el catalizador se encuentra en una fase diferente a la mezcla reactiva. 2.4.2 Concentración de las especies reactivas. Ley de Lambert Beer Si la reacción es llevada a cabo en disolución se puede utilizar Espectroscopia UV-Vis para determinar la concentración de las moléculas que absorban radiación en esa región del espectro electromagnético. 14 La ley que describe cuantitativamente el fenómeno de absorción de luz, se conoce como Ley de Lambert Beer, la misma establece que la fracción de radiación absorbida por un compuesto es proporcional al número de moléculas encontradas en un determinado recorrido, es decir, en solución la absorción del soluto será proporcional a su concentración para el caso en que el disolvente no absorba en el rango de longitudes de onda considerado. En base a esto la absorbancia se puede expresar (Ecuación 2.3): (2.3) La validez del uso de la ley de Lambert Beer para hallar la concentración de un soluto se restringe para el caso en que la relación entre la absorbancia y la concentración es una línea recta. 2.5 Tratamiento del agua Para la purificación y mejora del agua en el consumo humano e industrial se utilizan diversos tipos de tratamientos, los cuales se clasifican en: Tratamientos Primarios, Secundarios, Terciarios y los Tratamientos Alternativos de Oxidación Avanzada. 2.5.1 Tratamiento Primario Consiste en la separación de contaminantes por vías mecánicas y de aprovechamiento de diferencias en la densidad de las partículas. Se destacan en éste tipo de tratamiento: la filtración, sedimentación, la flotación, la separación de aceites y la neutralización. Para el tratamiento de efluentes por éste método se separan mecánicamente los desechos de mayor tamaño como palos, piedras, trapos. Posteriormente se llevan al tanque de sedimentación, el efluente separado se lleva a un tanque de desinfección con cloro que elimina las bacterias y es arrojado a un lago, río o mar cuando cumple con las restricciones ambientales. A su vez, los sedimentos pasan a un tanque digestor, luego al lecho secador y son llevados a un relleno sanitario o utilizados como abono para las tierras. 2.5.2 Tratamiento secundario 15 El tratamiento secundario es un proceso biológico que utiliza bacterias aerobias como un primer paso para remover hasta cerca del 90 % de los desechos biodegradables que requieren oxígeno. Después de la sedimentación, el agua pasa a un tanque de aireación en donde se lleva a cabo el proceso de degradación de la materia orgánica y posteriormente pasa a un segundo tanque de sedimentación, de ahí al tanque de desinfección por cloro y después se descarga para su reutilización. 2.5.3 Tratamiento Terciario Son utilizados cuando se desea eliminar de los efluentes algunas sustancias o compuestos en particular. Por lo tanto, estos tratamientos dependerán del tipo de contaminante a eliminar, y se consideran como procesos complementarios del tratamiento secundario ya que se logra mejorar la calidad del agua usada al estándar requerido para su posterior descargue al ambiente receptor (mar, río, lago, campo, etc). Entre los cuales se tiene: procesos de desalinización, extracción por solventes, intercambio de iones, etc. Dentro de las operaciones que se utilizan en el tratamiento terciario de aguas contaminadas están: la micro filtración, la coagulación y precipitación, la adsorción por carbón activado, el intercambio iónico, la ósmosis inversa, la electrodiálisis, la remoción de nutrientes, la cloración y la ozonización. 2.5.4 Oxidación Avanzada Los procesos de oxidación avanzada o también conocidos como TAO’s o PAO’s son procesos químicos alternativos para el tratamiento de aguas, los cuales se fundamentan principalmente en la generación del radical Hidroxilo OH·, el cual posee un alto potencial Redox, que ataca eficazmente moléculas orgánicas promoviendo la descomposición de las mismas en moléculas de menor peso molecular gracias a la generación de reacciones en cadena que pueden terminar o no en mineralización (producción de CO2 + H2O). Dentro de los posibles agentes reductores se encuentran (Tabla 2.2): 16 Tabla 2.2 Potenciales redox de algunos agentes oxidantes [3] En éste tipo de tratamiento, no se obtienen lodos que requieran a su vez una posterior disposición, y son útiles como complemento de tratamientos biológicos que no logran eliminar eficazmente contaminantes en bajas concentraciones. Y sirven para la eliminación de compuestos formados por pretratamientos alternativos, como la desinfección. Dentro de las tecnologías existentes de oxidación avanzada se encuentran dos grandes grupos: Procesos Foto químicos y los Procesos no Foto químicos. 2.6 Clasificación de los Procesos de Oxidación Avanzada Procesos no Foto químicos: Ozonización en medio alcalino (O3/OH-) Ozonización con peróxido de hidrógeno (O3/H2O2) Peróxido de hidrógeno y catalizador (H2O2/Fe2+) Procesos Fenton (Fe+2/H2O2) Procesos Foto químicos: 17 Fotólisis directa Fotólisis del agua en el ultravioleta de vacío (UVV) UV/peróxido de hidrógeno UV/O3 Foto- Fenton Fotocatálisis Heterogénea En general, las tecnologías que usan luz ultravioleta (proceso fotoquímico) se ven favorecidas por la presencia de la misma en comparación con aquellas que no poseen iluminación. 2.7 Tecnologías avanzadas de oxidación fotoquímicas La energía absorbida en la región UV – Visible produce cambios fotoquímicos en una molécula, producto de las transiciones de los electrones de valencia, las cuales cubre longitudes de onda entre (200 – 800) nm. El uso de la luz solar asegura un considerable ahorro de energía e instalaciones industriales más seguras, sin embargo, debe tenerse en cuenta que en el espectro solar sólo está presente un 3- 5 % de luz UV. 2.7.1 Fotólisis directa En este proceso no se adiciona reactivos químicos para el tratamiento de agua. Se basa en que un fotón de 254 nm equivale a 4,89 eV, energía suficiente para producir rupturas homolíticas y heterolíticas en moléculas. En la mayoría de los casos la ruptura homolítica produce radicales de acuerdo a (Ecuación 2.4): (2.4) Los radicales libres producen reacciones en cadena, que generan productos finales de menor peso molecular. En presencia de oxígeno es posible reacciones adicionales que producen el radical superóxido que a su vez contribuye en la degradación de compuestos (Ecuación 2.5): (2.5) 18 Esta tecnología tiene como limitante el tratamiento de aguas turbias o con sólidos suspendidos, ya que compromete la absorción de irradiación de las moléculas contaminantes, a su vez, la efectividad vendrá acompañada con la intensidad de la lámpara utilizada y el tiempo de exposición. 2.7.2 Fotólisis del agua en el ultravioleta de vacío (UVV) Este proceso aprovecha la irradiación a longitudes de ondas menores que la región UV-C, es decir, más bajas que 190 nm, y usa generalmente lámparas de excímeros de Xe (λ = 172 nm). En el tratamiento del agua produce radicales hidroxilos, átomos de hidrógeno y electrones acuosos de acuerdo a (Ecuación 2.6): (2.6) Generándose en presencia de oxígeno los radicales conforme a Ecuaciones 2.7 y 2.8: (2.7) (2.8) Los radicales generados pueden llevar a cabo simultáneamente oxidaciones y reducciones. El proceso requiere el suministro de oxígeno, el uso de material de cuarzo y la provisión de alta potencia. 2.7.3 UV/H2O2 Esta tecnología genera casi cuantitativamente dos ·OH por cada molécula de H2O2 irradiada (Ecuación 2.9). (2.9) 19 Si además del H2O2, los contaminantes se fotolizan directamente, mejora la eficiencia del proceso de destrucción oxidativa. El proceso foto químico es más eficiente en medio alcalino. En exceso de peróxido y con altas concentraciones de ·OH, tienen lugar reacciones competitivas que producen un efecto inhibitorio para la degradación. Los ·OH son susceptibles de recombinarse o de reaccionar de acuerdo con el siguiente esquema [3] (Ecuaciones 2.10 –13): (2.10) (2.11) (2.12) (2.13) Se puede notar que se consume ·OH en las Ecuaciones 2.10 y 2.13 disminuyendo la probabilidad de oxidación. Se debe determinar en cada caso la cantidad óptima de H2O2, para evitar un exceso que podría retardar la degradación. 2.7.4 UV/O3 Cuando se tiene ozono disuelto en agua y se irradia la mezcla se obtiene radicales hidroxilos a partir de la previa formación de peróxido de hidrógeno de acuerdo a (ecuación 2.14-15): (2.14) (2.15) A su vez, se forma radicales hidroxilos a partir de la irradiación directa del ozono que se descompone en medio acuoso (Ecuación 2.16) y se producen los radicales libres por la reacción del oxígeno atómico con el agua del medio (Ecuación 2.17). 20 (2.16) (2.17) El ozono puede producirse en situ por descarga eléctrica en corriente de aire, y no deja olores ni gustos residuales. En contraposición, el ozono no es tan miscible en agua como el H2O2, y su uso involucra transferencia de masa de la fase gaseosa a la fase acuosa, existiendo limitaciones de disolución [3]. 2.7.5 Foto – Fenton A finales del siglo XIX diferentes ensayos de Fenton demostraron que eran capaces de oxidar ciertos compuestos orgánicos mediante soluciones de peróxido de hidrógeno y sales ferrosas. El mecanismo de reacción propuesto se basa en la generación del radical hidroxilo ·OH gracias a la reacción entre el ión Fe+2 y el peróxido de hidrógeno (Ecuación 2.18), luego los radicales formados reaccionan mediante la oxidación del Fe(II) (Ecuación 2.19), y también mediante la oxidación de la materia orgánica. (Ecuación 2.20). (2.18) (2.19) (2.20) En condiciones ácidas (pH<3) la reacción es autocatalítica y sigue el siguiente esquema de reacción: (Ecuaciones 2.21 – 26). (2.21) (2.22) 21 (2.23) (2.24) (2.25) (2.26) El proceso Fenton no conduce a la mineralización y por eso se emplea el uso de luz UV para mejorar la degradación de los sustratos orgánicos. (Ecuaciones 2.27 y 2.28): (2.27) (2.28) 2.7.6 Ventajas de las Tecnologías de Oxidación Avanzada Estas tecnologías presentan las siguientes ventajas: Transformar químicamente al contaminante. Generalmente se consigue la mineralización completa (destrucción) del contaminante. No suele generar barros. Son muy útiles para contaminantes refractarios a otros métodos. Sirven para tratar contaminantes a muy baja concentración. No se forman productos de reacción, o se forman en baja concentración. Eliminan compuestos formados por pre-tratamientos alternativos. Consumen menos energías que los demás métodos. Sirven de pre-tratamiento para un método biológico. Mejoran las propiedades organolépticas de aguas tratadas. 22 2.8 Semiconductores con actividad fotocatalítica El proceso de fotocatálisis se basa en la transferencia de carga a través de la interfaz formada entre un semiconductor iluminado y una solución acuosa. En esta interfaz hay una densidad local de carga diferente a la del seno de ambas fases, produciéndose un campo eléctrico que actúa como fuerza impulsora en el proceso de transferencia de carga. [4] El solapamiento de los orbitales atómicos de los electrones de valencia en el semiconductor forman bandas de estados electrónicos permitidos que se separan por una banda de energía prohibida o gap, la cual limita la banda de valencia (BV), de menor energía, y la banda de conducción (BC), de mayor energía. La Figura 2.4 muestra tal efecto Figura 2.4 Estructuras de bandas y distribución de electrones para un metal y semiconductor intrínseco [4] La posición de la energía de fermi con respecto a las bandas de conducción y valencia distingue a los metales de los semiconductores y aislantes. Para los metales Ef cae sobre la banda de conducción, mientras que para los semiconductores y aislantes en la zona de energía prohibida o gap. Para los semiconductores Eg es suficientemente pequeño como para que sea posible excitar electrones de la banda de valencia a la de conducción (ebc-), dejando espacios vacíos o huecos en la banda de valencia, los cuales se comportan frente a un campo eléctrico como una partícula con carga positiva del mismo modulo que la carga del electrón. Dichos huecos se denotan hbv+. 23 2.9 Fotocatálisis Heterogénea Los semiconductores de interés en fotocatálisis son sólidos (generalmente óxidos o calcogenuros). Al ser éstos irradiados con fotones cuya energía es igual o superior a la energía del bandgap Eg se promueve la movilización de electrones de la banda de valencia a la de conducción (ebc-) y quedan huecos en la banda de valencia (hbv+) los cuales junto con los electrones son los portadores de carga. La ecuación 2.29 denota tal efecto (2.29) Las especies fotogeneradas se consideran dinámicamente activas puesto que migran rápidamente a la superficie y participan en diferentes reacciones químicas. Los huecos pueden reaccionar con sustratos orgánicos para formar radiales libres (ecuación 2.30). A su vez, pueden reaccionar con moléculas de agua o grupos hidroxilos absorbidos en la superficie del catalizador formando radicales libres hidroxilos de acuerdo a las reacciones siguientes (ecuaciones 2.31 y 2.32). (2.30) (2.31) (2.32) Los electrones de la banda de conducción suelen reaccionar con el oxígeno disuelto para formar el radical superóxido (ecuación 3.33) (2.33) Finalmente los radicales libres formados por los huecos o vacantes son altamente reactivos y promueven la oxidación de sustratos orgánicos por medio de reacciones de abstracción de 24 hidrógeno, adición a dobles enlaces o anillos aromáticos; el sistema redox es completado con la reducción del oxígeno disuelto. En la figura 2.5 se esquematiza las reacciones de las especies fotogeneradas con los sustratos orgánicos y especies absorbidas. Figura 2.5 Procesos que ocurren en la interfase Semiconductor – electrolito bajo irradiación [5] CAPÍTULO 3 MARCO METODOLÓGICO El desarrollo de los experimentos llevados a cabo para la presente investigación, se realizó en el laboratorio de Tratamiento de efluentes de PDVSA INTEVEP. Para lo cual se siguió la presente metodología desarrollada en 4 fases: Inicio, Ejecución, Análisis de resultados, Cierre. 3.1 Fase de inicio Se contempló el estudio y revisión de tópicos relacionados con catálisis heterogénea, procesos de oxidación avanzada, efluentes y tratamientos de efluentes de la industria petrolera. A su vez, la revisión y puesta a punto de métodos analíticos para la determinación de parámetros del tipo: Fenol, pH, Ozono, Peróxido de hidrógeno. 3.1.1 Reactivos Químicos, Equipos e instrumentos de análisis A continuación se describen los reactivos químicos utilizados en los diferentes ensayos: Fenol, C6H12OH, grado analítico, puro, MERCK Ácido Sulfúrico, H2SO4, 95%, RIEDEL DE HAEN 4-Amino antipirina, puro, RIEDEL DE HAEN Ferrocianuro de Potasio, Baker analyzed, J.T BAKER INC. Fosfato dihidrógeno de Potasio, K2HPO4, RIEDEL DE HAEN Fosfato de Hidrógeno de Potasio, KH2PO4, RIEDEL DE HAEN Peróxido de Hidrógeno, H2O2, Superoxigen, 40 Volumen, LOREAL Agua destilada desionizada, H2O Hidróxido de Sodio, NaOH, 99%, MALLINCKRODT Sulfato de hierro, FeSO4, RIEDEL DE HAEN 26 Ácido Clorhídrico, HCl Bisulfito de Sodio, NaHSO3 Ozono, O3 A continuación se presenta una lista de los instrumentos y equipos de análisis utilizados en el trabajo experimental: Espectrofotómetro portátil, HACH Figura 3.1 Espectrofotómetro Lámpara germicida, 254 nm, Atlantic Ultraviolet, Corporation Hauppauge Figura 3.2 Lámpara UV Bomba peristáltica, 600 rpm, MASTERFLEX Figura 3.3 Bomba peristáltica 27 Beaker de 3000 mL de capacidad, PIREX Figura 3.4 Tanque reservorio pH metro digital, Orion 330, THERMO Figura 3.5 pH metro digital Balanza analítica digital, HA – 200 A, AND Figura 3.6 Balanza digital 28 Equipo de microfiltración al vacío: Kitazato 250 mL, papel filtro MILLIPORE de 0,8 µm, motor de vacío 1760 rpm, SIEMENS. Figura 3.7 Motor de vacio monofásico Ozonador de descarga eléctrica, entrada de aire, WELBACH T 408 Figura 3.8 Ozonador de descarga eléctrica Reactor cilíndrico de cuarzo, PIREX 3.1.2 Métodos de análisis A continuación se presenta el procedimiento empleado para los diferentes análisis realizados en la investigación: 3.1.2.1 Caracterización de Fenol A fin de hallar la concentración de Fenol presente en solución se aplicó el método colorimétrico de la 4-amino antipirina. El cual permite relacionar la absorbancia de las muestras en estudio con la concentración de Fenol, teniendo previamente la curva de calibración de Fenol. 29 3.1.2.2 Método colorimétrico 4-amino antipirina. Standard Methods 5530D (Modificada) Este método establece la determinación de compuestos fenólicos que reaccionan con 4aminoantipirina formando un complejo acuoso coloreado. Una cantidad determinada de muestra se hace reaccionar con 4-aminoantipirina a pH 7,9 en presencia de ferrocianuro de potasio formando un complejo coloreado. La absorbancia de este complejo se mide a 500 nm. Equipo Utilizado: - Espectrofotómetro equipado con celdas de absorción de 1 a 5 cm para uso a 500 nm. - Medidor de pH. - Material de vidrio, limpio y seco. Reactivos Utilizados: - Hidróxido de amonio NH4OH (0,5 N): Medir 6,4 ml de NH4OH concentrado en 200 ml - Buffer de Fosfato: Pesar 20,9 g de K2HPO4 y 14,46 g de KH2PO4 en 200 ml - Sol de 4-aminoantipirina: Pesar 0,5 g del reactivo puro en 25 ml - Sol de Ferrocianuro de potasio K3Fe(CN)6 : Pesar 2,0 g del reactivo puro en 25 ml Procedimiento: - Medir 100 ml de la muestra o completar a 100 mL (filtrar si es necesario) - Las muestras se colocan en beakers de 250 ml y se les añade 2,5 ml de NH4OH 0,5 N y se ajusta inmediatamente a pH 7,9 ± 0,1 con el buffer de fosfato. - Se adiciona 1,0 ml de la solución 4 aminoantipirina, se mezcla bien y se agrega 1,0 ml de la solución de K3Fe(CN)6. Agitar bien. - Luego de 15 minutos, transferir a las celdas y leer la absorbancia a 500 nm. 30 3.1.2.3 Curva de calibración de Fenol Se prepararon soluciones de 100 mL que contenían Fenol en las siguientes concentraciones: (0,5, 1, 2, 4, 5, 6, 8 y 10) ppm. A las mismas se le aplicó el método colorimétrico de 4aminoantipirina. Luego se les halló su absorbancia a cada una y se graficó Absorbancia vs Concentración. Colorimétricamente, las muestras tomaron las siguientes características (figura 3.1): Figura 3.9 Preparación de soluciones de Fenol para curva de calibración Con la curva de calibración obtenida, se obtuvo la concentración de Fenol en función de la absorbancia mediante una línea recta, permitiendo así hallar la concentración de las mismas. 3.1.2.4 Determinación de la concentración de Peróxido de Hidrógeno Cuando se agrega una solución de permanganato de potasio a una solución de peróxido de hidrógeno acidificada con ácido sulfúrico, se produce la siguiente reacción: (3.1) Esta reacción constituye la base del método de análisis siguiente: Técnica: 31 En un matraz aforado de 250 mL de pone 25 mL de peróxido de hidrógeno, mediante una bureta, se lleva a volumen con agua y se homogeniza. Se toma 25 mL de esta solución y se pasa a un frasco cónico. Se diluye con 200 mL de agua y se agrega 20 mL de ácido sulfúrico (1+5) y se titula con permanganato de potasio hasta color rosa pálido permanente. Se repite la titulación, debiendo concordar en 0,1 mililitro. Luego, el peso de peróxido de hidrógeno por litro de solución original está dado por: (3.2) Preparación de permanganato de potasio 0,1 N Se pesa 3,5 g de permanganato de potasio sobre un vidrio reloj, se pasa a una vaso de precipitados de 1500 mL, se agrega un 1 L de agua, se cubre con un vidrio reloj, se calienta la solución a ebullición, se hierve suavemente durante 15–30 minutos y se deja enfriar a temperatura ambiente. Se filtra mediante un crisol filtrante de porcelana porosa, a un crisol o embudo filtrante de vidrio poroso. Se recoge el filtrado en un recipiente, previamente lavado con mezcla sulfocrómica, y luego, repetidas veces con agua destilada. La solución filtrada debe conservarse en frasco limpio, con tapa esmerilada, y mantenerla en la oscuridad o en luz difusa, e conservarla en frasco de vidrio de color caramelo oscuro. 3.2 Fase de Ejecución Durante esta etapa se planteó la revisión de funcionamiento y operación de reactor por lotes donde: se estableció el caudal de operación del proceso, se realizaron las líneas bases del proceso sin tratamiento químico, luego aplicando luz UV y peróxido de hidrógeno. Se determinó la eficiencia del proceso de remoción de fenol mediante catálisis heterogénea empleando diferentes catalizadores de óxidos de hierro en presencia de peróxido de hidrógeno. A su vez, se determinó el pH ideal de reacción, dosis de catalizador y tiempo óptimo del proceso, así como la influencia de la temperatura. Se comparó el estudio anterior con la eficiencia de remoción de fenol empleando proceso de ozonólisis. 32 3.2.1 Esquema de montaje Experimental Para la realización de los experimentos a escala laboratorio se contó con el montaje dado por la Figura 3.10. El mismo consiste en un tanque reservorio de capacidad 2,5 L. El cual contiene la solución a degradar y ésta es impulsada a través de una bomba peristáltica hacia el reactor que contiene la lámpara UV de 254 nm que promueve la fotocatálisis. Figura 3.10 Montaje experimental En el tanque reservorio se garantizó la homogeneidad de la solución en el proceso, mediante un magneto y plancha agitadora, que a su vez proveía de temperatura para la solución. El reactor posee una entrada de ozono para los casos en que se aplicó el mismo. La figura 3.11 muestra el sistema real Figura 3.11 Montaje del laboratorio 33 3.2.2 Toma de muestras para cada experiencia La manera en que se tomaron las muestras de Fenol en solución dependió de la presencia o ausencia de catalizador en solución, por lo que en cada caso se procedió de la siguiente manera: Solución sin catalizador: Se tomaron muestras de 10 mL de la solución principal en estudio utilizando una pipeta, se enrazó dicho volumen hasta 100 mL con agua destilada en beakers de 250 mL. Solución con catalizador: Para cada muestra se tomó 15 mL de solución principal utilizando una pipeta, posteriormente se vació el contenido en un beaker de 100 mL y se le aplicó filtración al vacío utilizando el equipo de microfiltración. La solución filtrada se le añadió 5 mL de Bisulfito de sodio que asegura contrarrestar el peróxido que haya quedado presente en solución. Finalmente se enrazó hasta 100 mL con agua destilada la solución resultante. Por último a cada muestra tomada se le aplicó el método colorimétrico a fin de hallar la concentración de Fenol presente en las mismas. 3.2.3 Fotólisis de la solución En ésta experiencia se prepararon 2 L de solución de Fenol a 5 ppm. La misma fue recirculada en el sistema reactor – tanque reservorio a un caudal de 500 (mL/min). Se tomó la primera muestra de solución para el tiempo inicial. Inmediatamente se encendió la lámpara UV y se tomaron muestras para tiempos determinados, para cada muestra tomada se apagaba la lámpara UV y se encendía nuevamente una vez tomada la misma para que continuara la reacción. A las muestras obtenidas se le hallaron las absorbancias asociadas de acuerdo al método colorimétrico, luego se determinó su concentración en función del tiempo utilizando la curva de calibración de Fenol. 34 3.2.4 H2O2 en solución En ésta experiencia se diluyó una cantidad conocida de peróxido de hidrógeno en 2 L de solución de Fenol a 5 ppm, se dejó recircular en el sistema (Q = 500 mL/min) y se tomaron muestras para tiempos determinados a las cuales se les aplicó el método colorimétrico de caracterización de Fenol. Se halló las concentraciones de Fenol en función del tiempo de estudio. 3.2.5 H2O2 + Catalizador Intevep Se estudió el efecto de la introducción del catalizador de óxidos de hierro en solución (intevep), para ello se agregó una dosis conocida del catalizador y del peróxido de hidrógeno en 1 L de agua destilada y se procedió a recircular la misma en el sistema reactor–tanque reservorio durante 15 min (Q=500 mL/min). A fin de que el catalizador estuviese diluido en solución, seguidamente se agregó 1 L de solución que contenía una dosis conocida de Fenol, se procedió a tomar alícuotas de solución para tiempos determinados y se halló la concentración de Fenol de la misma manera que en las experiencias anteriores. 3.2.6 H2O2+ UV En éste caso se diluyó una cantidad conocida de peróxido de hidrógeno en 2 L de solución de Fenol a 5 ppm, se siguió el mismo procedimiento del punto 3.2.4 con la premisa de encender la lámpara UV y apagarla cuando se tomaban las muestras en los tiempos determinados. Finalmente se halló la concentración de Fenol a través del tiempo. 3.2.7 H2O2+ UV + Catalizador Para la presente experiencia se combinó los efectos de cada reactivo. Se agregó una dosis conocida del catalizador y peróxido de hidrógeno en 1 L de agua destilada, la solución se puso a recircular en el equipo durante 15 min (Q= 500 mL/min). Inmediatamente se añadió 1 L de solución que contenía Fenol en proporción conocida. Se tomó la muestra para el tiempo 0, luego se encendió la lámpara UV y se tomaron muestras de solución para tiempos determinados. A cada muestra se le hallo la concentración de Fenol de acuerdo al método colorimétrico. 35 3.2.8 Síntesis de catalizador TiO2-Fe Se impregnó con hierro (III) la superficie del catalizador dióxido de titanio, de acuerdo al siguiente procedimiento: Se pesaron 15 g de TiO2 y se añadieron a un vaso de precipitado de 100 mL, luego se añadió 7,5 mL de ácido nítrico HNO3 concentrado y se agitó fuertemente durante 30 min. Se lavó el TiO2 con agua deionizada utilizando filtración al vacío. Se secó a 105 °C en baño de maría para evaporar el agua, luego se pesó 5 g TiO2 lavado y se le añadió 200 mL de solución 6,2 nM de Fe(NO3)3 . 9 H2O y se mezcló por 30 min. Se introdujo en un horno a 180 °C para secarlo por 24 horas. Posteriormente se calcinó a 500 °C por 7 horas. Se lavó con agua deionizada y se secó nuevamente a 105 °C en un baño de maría. Luego se realizó pruebas en sistema reactor – tanque reservorio a fin de evaluar la incidencia de hierro en la superficie del catalizador para la degradación de Fenol. Siguiendo los pasos mencionados en el apartado 3.2.7 3.3 Fase de Análisis de resultados Esta fase contempló el estudio e interpretación de gráficas y efectos obtenidos para cada experiencia realizada, luego en base a dicho estudio se propuso escalamiento y recomendaciones de tecnologías a aplicar de acuerdo a los resultados obtenidos, finalmente se empezó la redacción del presente trabajo de investigación. 3.4 Fase de cierre Esta fase contempló la elaboración de la presentación del proyecto de investigación, afinación de detalles del trabajo de investigación y conclusiones de los resultados obtenidos. CAPÍTULO 4 RESULTADOS Y DISCUSION Los resultados obtenidos para la degradación del Fenol se presentan a continuación de forma consecutiva, donde se muestra el efecto de la introducción de reactivos químicos como los son: Peróxido de hidrógeno, UV, Catalizadores de óxidos de hierro, ozono, etc. Y se pone de manifiesto la eficiencia de las tecnologías implementadas. 4.1 Curva de Calibración de Fenol Como primera experiencia, se obtuvo la curva de calibración del Fenol, aplicando el mencionado método colorimétrico, se comprobó la linealidad para las concentraciones de Fenol en estudio, demostrándose la validez de la Ley de Lambert-Beer que permite relacionar la absorbancia con la concentración de manera proporcional. La figura 4.1 muestra tal efecto: Figura 4.1 Curva de calibración para el Fenol. A una longitud de onda λ= 500 nm 37 Para la obtención de dicha curva se midió la Absorbancia de las muestras tratadas para 500 nm de acuerdo al método de caracterización de Fenol y a su vez se muestra el coeficiente de correlación de ajuste que asegura una buena aproximación. 4.2 Balance de masa. En ésta experiencia se colocó a recircular en el sistema reactor-tanque reservorio, una solución que contenía 5 ppm de Fenol, con el objetivo de tomar muestras cada 10 min a fin de comprobar que no existen fugas en el sistema que pudieran ocasionar errores más adelante en las experiencias. A su vez, se comprobó la eficiencia del método de caracterización de Fenol para las muestras seleccionadas. La figura 4.2 muestra tal efecto, en donde el tiempo de estudio fue de 1 hora y todas las medidas estuvieron cercanas al valor inicial. En base a esto se escogió la dosis de estudio para Fenol de 5 ppm, ya que la misma presentó menores variaciones de la concentración con el paso del tiempo. Figura 4.2 Balance de masa del sistema para 5 ppm de Fenol 4.3 Fotólisis de solución acuosa. Se estableció las condiciones necesarias para observar la degradación del contaminante en estudio (Fenol), el cual estuvo bajo irradiación de la lámpara UV que emite una longitud de onda 38 λ= 254 nm. Que asegura rupturas homolíticas y heterolíticas en las moléculas formando reacciones en cadena por medio de radicales libres. En la figura 4.3 notamos tal efecto al observar la disminución de la concentración del Fenol a través del tiempo debido a la exposición UV, nótese que para un tiempo de exposición de 1 hora se logra degradar en un 43% el Fenol, sin embargo, ésta tecnología está condicionada por el tiempo de exposición y como es evidente no asegura una completa desaparición del contaminante en estudio, debido principalmente a la poca reactividad de los radicales libres producidos para atacar moléculas de Fenol presentes en solución. Figura 4.3 Efecto de luz UV en solución de 5 ppm Fenol 4.4 Peróxido de Hidrógeno en solución. En éste caso se estudió el efecto de introducir una cantidad conocida de peróxido de hidrógeno al sistema, a fin de evaluar su aporte de forma individual y compararlo luego al introducir otros reactivos químicos. La cantidad introducida fue de 10 mL de H2O2 de 14000 ppm. Lo cual equivale aproximadamente a 70 ppm en los 2 L de solución. El pH del medio se ajustó con ácido sulfúrico y se colocó en un valor de pH= 3. La Figura 4.4 muestra tal efecto, en donde se observa una leve disminución de la concentración de Fenol, tan sólo 9,3% de degradación. Debido a que la temperatura del medio estuvo a 50°C y se sabe que el peróxido de hidrógeno se descompone fácilmente por calentamiento, a su vez, no se forman radicales libres que ataquen a la molécula de Fenol eficazmente. 39 Figura 4.4 Efecto de la introducción de H2O2 en solución de 5 ppm de Fenol. 4.5 Peróxido de Hidrógeno + Catalizador Intevep. Se introdujo al caso anterior el catalizador principal sintetizado en Intevep para evaluar el efecto que éste posee en la degradación del contaminante. El catalizador de óxidos de hierro proporciona Fe (III) y Fe (II) en solución, lo cual permite relacionar el efecto que se obtiene por la tecnología Fenton, sólo que en éste caso se trata de un proceso heterogéneo. La figura 4.5 nos muestra la disminución de la concentración de Fenol para el tiempo en estudio. Figura 4.5 H2O2 + Catalizador de óxido de hierro en solución de 5 ppm de Fenol 40 En base a éste resultado se puede observar que el Fenol tuvo un porcentaje de degradación de 30% en el tiempo observado, motivado al hecho de que se promueven en solución radicales hidroxilos altamente oxidantes de acuerdo al esquema de reacción previamente mencionado (Ecuaciones 2.18 – 2.20). No obstante, se logra aumentar el porcentaje de degradación de Fenol al introducir dicho catalizador en 21% con respecto al caso en que sólo se tenía H2O2 en solución. Lo que nos habla de que el catalizador en estudio posee una contribución importante a la hora de degradar el compuesto. 4.6 Peróxido de Hidrógeno + UV. Se estudió el efecto de la introducción de H2O2 en solución en presencia de luz UV. Con el fin de observar la contribución de cada uno en la degradación de Fenol. En la figura 4.6 se observa el efecto, obteniéndose un alto porcentaje de degradación de 94%. Figura 4.6 Degradación de Fenol en presencia de Peróxido de hidrógeno y luz UV Dicho porcentaje tan elevado se debe a que al ser irradiada una molécula de H2O2 por fotones con energía superior a la de la unión O-O se tiene un rendimiento cuántico casi unitario y se producen casi cuantitativamente dos radicales hidroxilos por cada molécula de peróxido de hidrógeno. De acuerdo a la ecuación 2.9. 41 Luego la presencia de radiales hidroxilos en solución promueve la degradación del contaminante. 4.7 Determinación de dosis óptimas de H2O2 y Catalizador Intevep. Se estableció una serie de experimentos a pequeña escala (200 mL) con el fin de determinar la dosis óptima de catalizador a utilizar en los experimentos de 2 L de solución que se usaron en el montaje experimental reactor–tanque reservorio. Para ello se fue variando la concentración de catalizador utilizada en presencia de 5 ppm de Fenol + H2O2 y se tomó una muestra inicial en el tiempo 0 y luego a los 30 min. Finalmente se comparó las concentraciones finales obtenidas, y para la dosis de catalizador que obtuviera un porcentaje de degradación mayor, se estableció como la óptima. La figura 4.7 muestra lo indicado. Figura 4.7 Variación de dosis de catalizador en función del porcentaje de degradación de Fenol a 5 ppm para soluciones de 200 mL La dosis implementada de peróxido de hidrógeno se mantuvo fija en 70 ppm a fin de observar el efecto de variar la concentración de catalizador. Luego se tomó como dosis óptima 70 mg para 200 mL, lo que equivale a 1,4 g de catalizador para los 2000 mL que se usaron. Luego de aumentar más de 70 mg de acuerdo a la figura 4.7 se observa un efecto inhibitorio que se atribuye al hecho de sobresaturar la solución con Fe (II) que en presencia de radicales hidroxilos es 42 oxidado de acuerdo a ecuación 2.19 atrapando a los OH· susceptibles de degradar la materia orgánica. Posteriormente con el fin de hallar la mínima concentración de peróxido de hidrógeno necesaria para efectuar una correcta degradación de Fenol que asegura que el reactivo no estuviese en exceso, se varió la concentración de H2O2 para diferentes ensayos de degradación en condiciones similares. Los efectos los tenemos en la figura 4.8 y los experimentos se realizaron para condiciones de pH=3, temperatura T= 50°C, en presencia de UV y peróxido de hidrógeno. Tal como sigue: Figura 4.8 Degradación de Fenol a 5 ppm variando dosis de H2O2 en solución. Como se puede observar, el efecto de disminuir la concentración de peróxido de hidrógeno presente en solución disminuye el porcentaje de degradación del Fenol y desfavorece la velocidad de reacción, sin embargo, para el caso estudiado se tomó como la dosis óptima de reactivo 17,5 ppm ya que ésta asegura un elevado porcentaje de degradación y no sugiere un significativo efecto en la degradación del contaminante cuando la misma es aumentada. 4.8 Peróxido de Hidrógeno + UV + Catalizador Intevep La base del estudio propuesto en esta investigación es proveer las condiciones óptimas para la aplicación de las tecnologías en conjunto previamente estudiadas, para ello en base a las dosis 43 óptimas halladas para el catalizador de óxidos de hierro y de peróxido de hidrógeno en solución se introdujo el efecto de la luz UV, obteniéndose el efecto que se muestra a continuación (figura 4.9): Figura 4.9 Degradación de 5 ppm de Fenol utilizando UV,H2O2 y catalizador de óxidos de hierro De acuerdo a la figura 4.9 se verifica la eficiencia que existe entre la combinación de los diferentes efectos que se tienen por cada reactivo, dado que a los 6 minutos de reacción se tiene casi un 100% de degradación del contaminante. Las condiciones a la cual se llevó a cabo la degradación fueron las siguientes: pH=3, T=50°C, dosis utilizada [1:7:1,4g] donde se representa la relación de [Fenol, H2O2, Catalizador]. Debido a que en éste caso se trata de una fotocatálisis heterogénea se explica el mecanismo mediante el cual se promueve la degradación por ésta vía conforme a las referencias mencionadas en el marco teórico. Mecanismo de degradación: 44 Figura 4.10 Mecanismo de degradación Fotocatálisis Heterogénea Además del efecto antes mencionado en la Figura 4.10 se tienen efectos combinados de los ensayos previamente estudiados. A saber, para el caso de peróxido y catalizador, se sabe que la proporción de hierro en solución promueve la formación de radicales libres y degradación de compuestos orgánicos (Ecuaciones 2.18 – 2.20), por otra parte tenemos la contribución de radicales libres por la vía de UV + H2O2 que como se observa en la Figura 4.11 tiene un efecto determinante a la hora de degradar el fenol, en efecto la degradación por vía H2O2 + UV es la que posee una mayor contribución para la eliminación del Fenol. Por último la completa disminución del contaminante se logra gracias a la introducción del catalizador de hierro en presencia de luz UV y peróxido de hidrógeno. 45 Figura 4.11 Efectos combinados de reactivos en la degradación de Fenol La figura 4.11 demuestra el efecto de la combinación de las diferentes tecnologías para la degradación del Fenol, el resultado óptimo se tiene al combinar peróxido de hidrógeno en presencia de luz UV y catalizador Intevep. 4.8.1 Variación de pH A continuación se presenta la variación del parámetro pH en solución, el mismo se varió introduciendo base (NaOH) en el proceso. El resultado obtenido es el siguiente (Figura 4.12) Figura 4.12 Variación de pH para ensayos de H2O2 + UV + Catalizador 46 De acuerdo a la Figura 4.12 se demuestra que el proceso de degradación está favorecido a pH ácido. Debido a la similitud que se tiene con el proceso fotofenton anteriormente explicado, ya que se tiene en condiciones ácidas un esquema de reacción autocatalitico que genera hierro (II) y (III) en solución, a su vez que contribuye a la generación del radical hidroxilo principal agente oxidante. Conforme al esquema de reacciones (2.21 – 2.26). 4.8.2 Variación de la concentración de Fenol Con la finalidad de observar el efecto de variar la concentración del contaminante en estudio se aumentó su concentración en solución, manteniendo los valores óptimos encontrados de reactivos químicos. Es decir, H2O2= 17,5 ppm; Catalizador = 1,4 g. la Figura 4.13 muestra las diferencias Figura 4.13 Degradación de Fenol variando su concentración. Se asume un modelo de primer orden que describe la reacción ya que se complementó adecuadamente al hacer un ajuste de mínimos cuadrados de los datos experimentales y la constante de pseudo-primer orden asociada se halló al graficar Ln([Fenol]) vs t. tal como se muestra en la Figura 4.14. 47 Figura 4.14 Degradación de Fenol a diferentes concentraciones De la figura anterior se pueden resumir los efectos en la tabla 4.1 tal como sigue: Tabla 4.1 Constantes de pseudo-primer orden determinadas para la fotocatálisis heterogénea del Fenol Concentración Fenol (mg/L) pH±0,1 kobs (min-1) R2 5 3,0 0,5758 0,9829 10 3,0 0,2676 0,9928 La disminución de la velocidad de reacción al aumentar la concentración del contaminante sugiere que la constante de velocidad asociada al modelo cinético que describe la reacción, depende inversamente de la concentración del sustrato. Se puede asociar el mecanismo de reacción de la fotocatálisis heterogénea al modelo propuesto por Langmuir-Hinshelwood (ecuación 4.1), en el cual se supone que el sustrato participa en un equilibrio de adsorción – desorción en la superficie del catalizador para ser oxidado por el o los radicales OH· 48 Se puede entender el modelo cinético propuesto de primer orden de Langmuir-Hinshelwood como un modelo que posee una constante observada de velocidad que depende inversamente de la concentración del sustrato (ecuación 4.3) (4.2) Para la determinación de los parámetros del modelo propuesto se linealizó el mismo y se ajustaron los datos experimentales como el inverso de la velocidad en función del inverso de la concentración inicial (ecuación 4.4) La realización de éste ajuste implicó la determinación de la velocidad inicial de reacción la cual fue hallada como la pendiente en los primeros minutos de reacción de un gráfico [Fenol] vs t. La figura 4.15 muestra el ejemplo para una fotodegradación realizada. Figura 4.15 Determinación de la velocidad inicial de reacción para la degradación de Fenol. [Fenol]0= 10 ppm, [Catalizador]= 1,4 g; pH= 3,0; T=50°C 49 La tabla 4.2 presenta los valores de velocidad obtenidos para la foto degradaciones realizadas, junto con el coeficiente de correlación del ajuste. Tabla 4.2 Velocidad inicial de reacción para la fotocatálisis del Fenol Concentración Fenol (mg.L-1) pH±0,1 -r0 (mg. L-1 .min-1) R2 5 3,0 1,09 0,9985 10 3,0 1,59 0,9796 En la figura 4.16 se muestra la linealización de los datos experimentales de acuerdo al modelo de Langmuir-Hinshelwood. Figura 4.16 Linealización del modelo cinético de Langmuir-Hinshelwood para la fotocatálisis heterogénea de Fenol La tabla 4.3 resume el valor de las constantes k y K del modelo de Langmuir-Hinshelwood. Las cuales se obtuvieron del intercepto y pendiente del ajuste lineal realizado, dicho ajuste se consideró correcto a pesar de no contar con varios puntos que permitan validar que los datos experimentales se ajustan a una tendencia lineal, apoyado en la experiencia que poseen los autores en fotocatálisis heterogénea que sugieren este modelo como válido en la amplia bibliografía que existe [1, 4, 10, 11, 12]. Sin embargo, se hace necesario validar la suposición con nuevos puntos sobre la gráfica en experiencias futuras. 50 Tabla 4.3 Constantes de velocidad y equilibrio de adsorción para el modelo de Langmuir Hinshelwood K (L.mg-1) k (mg.L-1. min-1) 0,20 kK(min-1) 2,43 0,49 De acuerdo a los valores obtenidos de la tabla 4.3 se tiene que la constante de velocidad del proceso (k) supera en doce veces el valor de la constante de equilibrio de adsorción (K), por lo que se infiere que el proceso degradativo en ésta tecnología está principalmente dominado por efectos no asociados a la adsorción en el catalizador, sino por el contrario asociado a la producción de radicales libres OH· por efecto de hierro en solución y peróxido de hidrógeno, a su vez que el efecto UV + H2O2 tiene una gran contribución como anteriormente se ha mencionado (figura 4.11). 4.8.3 Variación de temperatura de reacción Se estudió el efecto de disminuir la temperatura en la reacción, tomando en cuenta que todas las experiencias se realizaron a T=50°C, en éste caso se trabajó con las mismas condiciones de los experimentos anteriores pero a temperatura ambiente T=22°C. El efecto se observa en la figura 4.17 junto con una degradación a las mimas condiciones pero T=50°C. Figura 4.17 Degradación de Fenol utilizando H2O2, UV y catalizador de hierro a diferentes temperatura de reacción. 51 Resulta evidente de acuerdo a la figura 4.17 que la velocidad de reacción aumenta conforme aumenta la temperatura de reacción, en efecto la constante de velocidad de reacción asociada al proceso se muestra en la tabla 4.4 Tabla 4.4 Constante de pseudo-primer orden para proceso fotocatálisis heterogéneo Temperatura de reacción( °C ± 1) pH±0,1 kobs (min-1) R2 22 3,0 0,2933 0,9372 50 3,0 0,5758 0,9829 De acuerdo a éste resultado se puede mencionar que el proceso fotocatalítico no sigue la degradación del contaminante por vía de interacción entre la superficie del catalizador, a pesar de que es ampliamente mencionado que en el proceso de fotocatálisis heterogénea la influencia de la temperatura no posee un efecto determinante, en éste caso si, por lo que se puede inferir que la principal fuente de generación de radicales hidroxilos susceptibles a degradar la materia orgánica se forman por la ruptura del enlace oxígeno–oxígeno del H2O2 en presencia de UV, además de la oxidación de hierro (II) en solución por vía fotofenton. 4.8.4 Variación de Catalizadores En ésta experiencia se comprobó la efectividad que presenta el Catalizador Intevep con respecto a dos catalizadores diferentes. El primero de ellos es el Fe3O4 que se conoce como mineral magnetita y está constituido por óxido ferroso–férrico, el cual provee cationes Fe(II) y Fe(III) en solución. Por otro lado, se preparó un catalizador modificado de dióxido de titanio (TiO2-Fe), el cual se impregnó con hierro (III) sobre su superficie a fin de observar diferencias. La Figura 4.18 resume el efecto de los diferentes catalizadores, todos ellos bajo las mismas condiciones de reacción. pH=3, T=50°C, UV, Catalizadores= 1,4 g; H2O2= 17,5 ppm. 52 Figura 4.18 Degradación de 5 ppm de Fenol en presencia de varios catalizadores. De acuerdo a la figura 4.18 se nota que el catalizador intevep posee cierta eficiencia con respecto al de magnetita Fe3O4, que se traduce en un ligero aumento en la velocidad de reacción, sin embargo, es comparable el efecto pues ambos proveen hierro en solución que permiten la formación de radicales libres OH· siguiendo el esquema de reacción fotofenton en fase heterogénea. Por otro lado el catalizador TiO2-Fe no presentó una eficiencia comparable, quizás debido a que el hierro minó la superficie del catalizador quitando sitios activos que promueven la oxo-reducción de sustratos orgánicos, aunado al hecho de que se haya cometido errores a la hora de prepararlo que inhabilitaron su efecto. La tabla 4.5 presenta las constantes de velocidad asociadas a cada catalizador. Tabla 4.5 Constantes de pseudo-primer orden para cada catalizador Catalizadores pH±0,1 kobs (min-1) R2 TiO2-Fe 3,0 0,2468 0,9812 Fe3O4 3,0 0,4325 0,9905 Catalizador Intevep 3,0 0,5758 0,9829 Finalmente se pone de manifiesto que el catalizador intevep presenta una eficiencia marcada, en donde la principal ruta de degradación está determinada por la irradación de moléculas de peróxido de hidrógeno, luego sigue la presencia de Hierro (II) y (III) en solución y por último la 53 adsorción–desorción de sustratos orgánicos en la superficie del catalizador, que al combinar los efectos permiten degradar adecuadamente soluciones de Fenol. 4.9 Efecto de Ozono en solución Como última experiencia se estudió el efecto que posee la introducción del oxidante Ozono en solución, luego se observó el efecto en presencia del catalizador intevep. En la figura 4.19 notamos el comportamiento del ozono en ausencia y presencia de catalizador. Las condiciones de reacción para ésta experiencia fueron: [Fenol]= 5 ppm, [Ozono]= 5 ppm, T= 22°C, pH=4,5. Figura 4.19 Degradación de 5 ppm Fenol utilizando Ozono [5ppm] De acuerdo a la figura 4.19 notamos que la cinética de reacción sigue una ley de velocidad de primer orden. Donde se alcanza un 92% de degradación del contaminante para el caso de ozono sin catalizador. El mecanismo de reacción asociado a ésta tecnología sigue el siguiente esquema de reacción (ecuaciones 4.5 – 11). (4.5) (4.6) 54 (4.7) (4.8) (4.9) (4.10) (4.11) La producción de radicales libres como ya sabemos es la responsable de la oxidación del sustrato en estudio. Por otro lado, se tiene también, la mejora de dicho efecto una vez introducido el catalizador (100 % degradación), dado que éste provee Fe+2 en solución que resulta como iniciador dentro del esquema de reacciones (4.5 – 11) y no se limita a asegurar valores de pH básicos solamente. La tabla 4.6 resume las constantes de velocidad de primer orden halladas para ambos casos. Tabla 4.6 Constantes de pseudo-primer orden para degradaciones con Ozono Ozono pH±0,1 kobs (min-1) R2 Sin catalizador 4,5 0,1921 0,9285 Con catalizador intevep 3,5 0,2358 0,9998 Las soluciones analizadas se estudiaron a pH natural (4,5); sin embargo, la presencia del catalizador intevep en la experiencia en la que se introdujo el mismo bajó el pH de la solución, lo que implica que el efecto de hierro (II) en solución fue el iniciador para la producción de radicales libres y su posterior degradación del contaminante en dicha experiencia. 4.10 Mecanismo de reacción Finalmente se propone el siguiente mecanismo de reacción de degradación del Fenol, de acuerdo a la formación del intermediario radical dihidroxi ciclohexadieno fundamentado en la 55 referencia [6], el cual mayoritariamente está presente en las posiciones orto y para del anillo bencénico. En medio ácido y básico el radical dihidroxilo ciclo hexadieno rápidamente elimina agua, generando los radicales fenoxilicos que conducen a la formación de los productos principales de la oxidación del fenol que son la hidroquinona y el catecol y que son aún más tóxicos que el propio Fenol. Luego, los consecuentes ataques del radical hidroxilo, sobre estos productos conllevan a la formación de compuestos del tipo benzoquinona y de los ácidos mucónico y maléico, que posteriormente pasan a ácido oxálico para ser posteriormente mineralizados en CO2 y agua. La figura 4.20 muestra lo explicado y complementa el estudio realizado. Figura 4.20 Mecanismo de oxidación fotocatalítica del Fenol 56 CONCLUSIONES El estudio de las diferentes tecnologías utilizadas a lo largo de ésta investigación, sus efectos individuales y combinados para la degradación del compuesto orgánico Fenol permiten concluir lo siguiente: El proceso de degradación de Fenol utilizando luz UV a una longitud de onda de λ= 254 nm en presencia de H2O2 posee una alta eficiencia gracias a los radicales OH· generados. La introducción del catalizador Intevep sintetizado en la empresa provee una mejora sustancial al proceso degradativo del Fenol. El efecto principal en la degradación del Fenol por parte del catalizador se debe a la inclusión de Fe+2 en solución y el aporte del par electrón – hueco en su superficie no es determinante. La degradación fotocatalítica del Fenol sigue un modelo cinético de primer orden a pH ácido y puede modelarse por Langmuir-Hinshelwood. La constante cinética de pseudo-primer orden para la degradación del Fenol disminuye en función de aumento de la concentración inicial del sustrato orgánico. A pH básico se desfavorece el proceso fotocatalítico heterogéneo para la destrucción del Fenol. El aumento de la temperatura de reacción favorece el aumento en la velocidad de degradación de Fenol para el proceso fotocatalítico heterogéneo. La constante cinética de pseudo-primer orden es mayor para el catalizador Intevep, seguidamente para el magnetita (Fe3O4) y por último para el dióxido de titanio impregnado con hierro (III) (TiO2-Fe). El efecto ozono-catalizador en solución presenta alta eficiencia y es también susceptible de aplicar para tratamiento de efluentes. 57 RECOMENDACIONES Se recomienda realizar cromatografía de masas al agua, antes y después del tratamiento, para identificar intermediarios y proponer mecanismo de reacción y validar el propuesto. Ampliar el estudio para diferentes concentraciones iniciales de Fenol a fin de hallar sus modelos cinéticos y verificar si cumplen con el modelo Langmuir-Hinshelwood. Se sugiere realizar el estudio de fotocatálisis heterogénea empleando diferentes compuestos orgánicos y también en aguas de producción de la industria petrolera. Se recomienda tener una abertura con una válvula en el tanque reservorio que permita obtener solución al abrirla, sin la necesidad de recurrir a pipetas para la toma de muestras. 58 REFERENCIAS BIBLIOGRAFICAS [1] Vergara, N, “Proceso de oxidación avanzada para la eliminación de fenoles en aguas de producción de la estación de flujo sinco d”, Tesis ULA, 2007. [2] Lenntech, Water treatment Solutions, Disponible en internet: http://www.lenntech.com/library/uv/will1.htm, consultado el 25 de Agosto de 2010. [3] Litter, M, “Tecnologías avanzadas de oxidación: tecnologías solares”, UNSAM, Argentina, 2005, Cap 5, pp 67 -82. [4] Candal, R; Bilmes, S; Blesa, M “Semiconductores con actividad fotocatalítica”, Ciemat, Madrid, 2004, Cap 4. Pp 97 – 123. [5] Vargas, R, “Estudio cinético de la degradación fotocatalítica de dibenzotiofeno y triton x-100 usando simulación solar y TiO2 como catalizador”, Tesis USB, 2007. [6] Kasprzyk, B; Ziólek, M; Nawrocki, J. “Catalytic Ozonation and methods of enhancing molecular ozone reactions in water treatment”. Applied Catalysis B: Environmental 46, pp 639669, 2003. 59 BIBLIOGRAFÍA [1] Vargas, R; Núñez, O “Photocatalytic degradation of oil industry hydrocarbons models at laboratory and at pilot-plant scale”. Solar Energy, 84, 345-351, 2010. [2] Herrmann, J,M, “Destrucción de contaminantes orgánicos por catálisis heterogénea”. Unión Europea, 2005, Cap 10, pp 147 – 163. [3] Zambrano, C, “Estudio de la oxidación de fenoles mediante ozono generado en plasmas de alto voltaje”, Tesis UCV, 1993. [4] Vargas, R; Núñez, O “Hydrogen bond Interactions at the TiO2 Surface: their contribution to the pH dependent photocatalytic degradation of p-nitrophenol”. Journal of Molecular Catalysis A: Chemical , 300, 65-7, 2009. [5] Shawaeh, R; Khashman, O; Bisharat, G, “Photocatalytic degradation of phenol using Fe-TiO2 by different illumination sources”. International Jorunal of Chemistry, Vol 2, No 2, Agosto 2010. Pp 10 -14 [6] López, R; Núñez, O; Morales, F; Calderón, C y Liewald, W, “Aplicación de sistemas oxidantes avanzados en el tratamiento de aguas residuales de la industria petrolera (sistema fenton)”. Acta científica Venezolana, Vol 50, No1, 1999, pp 75 – 80. [7] Alegría, Y; Liendo, F; Núñez, O, “On the fenton degradation mechanism. The role of oxalic acid”. ARKIVOC (X), 538-549, 2003 [8] Pardo ,G., Vargas, R; Núñez, O “Photocatalytic TiO2-assisted Decomposition of Triton X100: Inhibition of p-nitrophenol Degradation”. J.Phys.Org.Chem. 21, 12, 1072-1078, 2008. [9] Wu, Q; Hu, X y Yue, P, “Mechanism and kinetic studies of heterogeneous UV/Fenton process for the oxidation of aqueous organic pollutants: electron transfer at catalyst surface to initiate the redox process”. Hong Kong, China. Pp 1-10 60 [10] Hidalgo, K; Lovera, M, Sánchez, A “Tratamiento con luz solar y TiO2 de efluentes contaminados”. Miniproyecto de Ingeniería Química, USB. 2009. [11] Vargas, R; Núñez O “The Photocatalytic Oxidation of Dibenzothiophene (DBT)”. Journal of Molecular Catalysis A: Chemical, 294, 74-81, 2008. [12] Kuehr, I; Núñez O “Titanium dioxide photoinduced degradation of some pesticide/fungicide precursors”. Pest. Manag.Sc. 63,5,491-494, 2007. [13] Barrios, N; Sivov, P; D’Andrea, D; Núñez, O “Conditions for Selective Photocatalytic Degradation of Naphthalene in Triton X-100 Water Solutions”. Int. J.Chem.Kinetics 7, 37, 414419, 2005.