1 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD
Anuncio

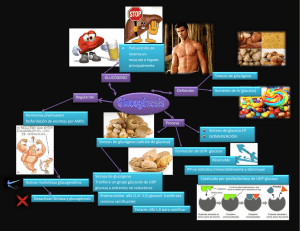
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. Integración de las Vías Anabólicas y catabólicas de carbohidratos. Incluye el metabolismo de los glúcidos varios aspectos de especial importancia para el organismo animal, entre otros: todo lo relacionado con el metabolismo del glucógeno, su síntesis (glucogenogénesis), su degradación (glucogenólisis), y la regulación hormonal y enzimática de este proceso. Además tenemos la glucólisis y asociada a ella, el ciclo de Krebs. Por último, gluconeogénesis y la vía oxidativa colateral de la glucosa. Debemos también referir aquí algunas consideraciones sobre un proceso de especial significación en el campo de la biología, nos referimos a la fotosíntesis. La fotosíntesis es un proceso metabólico de primer orden en el caso de los vegetales y de gran repercusión para los animales y para la vida en general. Mediante la fotosíntesis, realizada por las plantas verdes, se fija en compuestos orgánicos la energía solar y el CO2 atmosférico liberándose al mismo tiempo 02 con lo que se establece un ciclo biológico entre animales y plantas que es la base de todos los procesos biológicos en nuestro planeta. Los compuestos orgánicos formados principalmente glúcidos que son usados como fuente de energía química por los animales o como sillares constitutivos de las cadenas carbonadas presentes en los aminoácidos, lípidos, vitaminas y demás compuestos orgánicos. La energía lumínica emitida por el sol es captada por las plantas, pues ellas poseen un pigmento muy similar a la hemoglobina, llamado clorofila, presente en los cloroplastos. La planta utiliza esta energía y la transforma en energía química. Digestión y Absorción de los carbohidratos En la dieta normal de la mayoría de los animales y el hombre aparecen varios polisacáridos, entre otros la celulosa, el almidón, el glucógeno, así como otros polímeros de la glucosa, hexosas, pentosas, etc. También algunos disacáridos (lactosa, sacarosa, maltosa y otros compuestos relacionados con los carbohidratos. Todos ellos son fuente de glucosa para las células, para ello, 1 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. primero deben ser digeridos (hidrolizados) y después absorbidos.La digestión de los glúcidos se realiza a todo lo largo del tubo digestivo por medio de un grupo importante de enzimas hidrolíticas que en su conjunto reciben el nombre de carbohidrasas.En la boca, aunque con acción muy limitada por el poco tiempo que los alimentos permanecen en ella, actúa una amilasa, conocida como amilasa salival o ptialina capaz de hidrolizar los almidones hasta maltosa. Esta enzima que es activada por iones de cloruro, trabaja a un pH de 6,6 a 6,8 por lo que al llegar los alimentos al estómago se inactiva. En este lugar debemos considerar el efecto hidrolítico realizado por el ácido clorhídrico del jugo gástrico, el cual es capaz de hidrolizar un porcentaje considerable de los almidones y otros polisacáridos presentes en la dieta. Sin embargo, es en el intestino delgado donde ocurre la hidrólisis fundamental de los carbohidratos ingeridos, debido a la presencia de la amilasa pancreática, la cual es capaz de hidrolizar el almidón y otros polisacáridos de estructura semejante a la maltosa. La amilasa pancreática es una alfa-amilasa por lo que no actúa sobre las cadenas beta de los glúcidos, tales como la celulosa y otras estructuras. Su pH óptimo de acción es de 7,1, y actúa hidrolizando indistintamente los enlaces alfa 14 a lo largo de la cadena de amilasa de modo que produce finalmente una mezcla de glucosa y maltosa. La alfa amilasa puede actuar también sobre las cadenas de amilopectina, sin embargo, su acción se limita a los enlaces 1-4, no teniendo capacidad para actuar sobre las ramificaciones 1-6. Una enzima desramificadora (alfa 1-6), hidroliza los enlaces 1-6 en los puntos de ramificación liberando glucosa. Por la acción conjunta de estas amilasas se produce la hidrólisis del almidón. De esta manera se liberan en el intestino delgado grandes cantidades de glucosa y algunos disacáridos representados por la maltosa, así como otros tales como la sacarosa y la lactosa que pueden existir en dependencia de la dieta. Estos no pasan directamente a la sangre, sino que por acción de las enzimas específicas (maltosa, sacarasa, etc.), son desdoblados en el mismo epitelio intestinal, 2 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. producto de la acción del jugo intestinal que poseen las mencionadas enzimas. Al final, producto de la digestión, se liberan a partir de los glúcidos ingeridos grandes cantidades de glucosa, galactosa, fructosa, pentosas y otros monosacáridos, los que deben ser absorbidos. Por otra parte, la celulosa, que constituye una fracción importante en la dieta de los herbívoros, no es modificada por enzimas propias del tubo digestivo, sino que a nivel del intestino grueso (colon y ciego) es degradada por acción bacteriana con producción de ácidos grasos inferiores, los cuales se absorben y son usados por el animal. Es de destacar el hecho de que parte de los carbohidratos ingeridos no se digieren y son eliminados con las heces, contibuyendo de forma destacada al normal funcionamiento del tubo digestivo. Los monosacáridos se absorben en el intestino delgado y pasan a la sangre por el sistema porta que los conduce al hígado. La absorción de estos puede realizarse por dos mecanismos: por difusión (pasiva) y por transporte activo. La posibilidad de la absorción pasiva (difusión) de algunos monosacáridos es, aunque no improbable, muy limitada y no fundamental. Es por ello que se debe considerar el mecanismo de transporte activo como el fundamental para la absorción de las hexosas y en especial para la glucosa. El paso de las hexosas a través de la barrera intestinal tienen lugar a una tasa fija e independientemente de su concentración en la luz del epitelio, así como en contra de un gradiente osmótico. Son también absorbidas más rápidamente las hexosas que las pentosas; todo ello hace concluir, que el transporte activo es el fundamental proceso de absorción de la glucosa. Es de destacar también que el transporte activo de la glucosa a nivel intestinal se puede bloquear por factores que inhiben el proceso de fosforilación y la síntesis de ATP, así como cuando disminuye el aporte de oxígeno todo lo hace concluir en un mecanimos activo con gasto de energía. 3 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. Glucogenogénesis Con el nombre de glucogenogénesis o glucogénesis se designa el proceso metabólico mediante el cual la glucosa es convertida en glucógeno, polímero de reserva de los glúcidos en las células animales. Mediante este mecanismo se almacenan grandes cantidades de glucosa cuando el aporte de la misma lo permite, utilizándose más tarde en dependencia de las necesidades del organismo. La glucogenogénesis es, la principal vía anabólica del metabolismo de los glúcidos.Prácticamente todas las células del organismo tienen la capacidad de almacenar la glucosa en forma de glucógeno, destacándose dentro de ellas las células hepáticas y las musculares. Las células del riñón, epitelio intestinal, del útero y otras más, presentan también niveles de glucógeno que deben ser tomados en consideración. Por el contrario, la neurona prácticamente contiene muy poco glucógeno, lo que determina la dependencia de las mismas del aporte directo de glucosa. El hígado, después de una comida rica en carbohidratos puede contener hasta el 1% de su masa de glucógeno. El sistema muscular, por su dimensión, es sin duda la mayor reserva de glucógeno del organismo. Cabe destacar, sin embargo, que las reservas de glucógeno del organismo en general son reservas para corto plazo. Es decir, utilizando sólo sus reservas de glucógeno un animal sólo tiene energía para unas 16 a 18 horas. Las reservas a largo plazo como veremos más adelante están representadas por los lípidos. La biosíntesis del glucógeno se realiza por un complejo enzimático, donde debe destacarse la acción de la glucógeno-sintetasa, enzima responsable de la incorporación de la forma activa de la glucosa a las cadenas preexistentes que forman el glucógeno. Es necesario precisar que el glucógeno no se forma de nuevo enteramente, sino que siempre existe una pequeña cantidad de glucógeno en la célula, lo que recibe el nombre de "semilla", el cual incrementa su volumen en dependencia del aporte de glucosa o decrece si es necesario, en caso contrario es necesario suministrar glucosa ala célula. Este último proceso recibe el nombre 4 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. de glucogenólisis y será estudiado a continuación de este tema. Por ello debe considerarse siempre la presencia de cierta cantidad de glucógeno formando gránulos presentes en el citoplasma, que incluso presentan enzimas asociadas a ellos, que se encuentran en constante metabolismo según las condiciones celulares. La formación de glucógeno se realiza a expensas de la glucosa, sin embargo, todos los glúcidos pueden ser convertidos en glucosa en las células, por ello todos pueden, en la práctica, formar glucógeno. En el tema correspondiente a la vía colateral de oxidación de la glucosa veremos como las triosas, tetrosas y pentosas pueden ser convertidas en hexosas. Por otra parte, entre la fructosa y la glucosa existe un equilibrio regular catalizado por una isomerasa, al igual que entre la galactosa y la glucosa en este caso por una epimerasa. El glucógeno hepático constituye una buena reserva de glúcidos para las necesidades de las células del organismo en general. Es responsable, entre otras cosas, de mantener la glicemia normal que aporta la glucosa libre a todo el organismo, principalmente al tejido muscular que requiere constantemente de ella para formal sus propias reservas y, en especial, para mantener el aporte de glucosa ala neurona:, Por otra parte, niveles adecuados de glucógeno en el hígado hacen a este órgano más preparado para responder a los efectos tóxicos u otros productos nocivos. Es necesario señalar que en el hígado a expensas del glucógeno se forma el ácido glucorónico de gran importancia en los mecanismos normales de detoxicación hepática. Al mismo tiempo niveles inadecuados de glucógeno impedirían el uso de la glucosa por los tejidos con la consecuente movilización de las grasas, las cuales en su oxidación tienden a incrementar los niveles de cuerpos cetónicos. Por ello la existencia de adecuados niveles hepáticos de glucógeno son sinónimos de un buen funcionamiento del metabolismo en general. 5 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. Glucogenólisis Por glucogenólisis se entiende el proceso mediante el cual a partir del glucógeno se obtiene glucosa. Es por tanto la degradación del glucógeno a glucosa el cual ocurre como tal en el hígado pues en otros tejidos el producto final es la glucosa 6fosfato que se incorpora a la vía de la glucólisis. La glucogenólisis pudiera considerarse el proceso inverso de la glucogenogénesis aunque los pasos no son los mismos a la inversa, Es necesario señalar aquí en este caso, de manera similar a la glucogenogénesis, el glucógeno no se transforma totalmente en glucosa, sino que, en dependencia de las necesidades de las células el mismo se degrada parcialmente quedando siempre un resto que, cuando el aporte de glucosa se restituye, es capaz de formar glucógeno otra vez. A nivel celular, tanto en el hígado como en el músculo, el metabolismo del glucógeno, que incluye su síntesis y su degradación tiene que estar perfectamente controlado. Se comprende, por ejemplo, que si una molécula de glucógeno estuviese por un momento sometida a la acción de la fosforilasa activa, estaría degradándose y si en otra, por el contrario, el efecto lo estuviese realizando la glucógeno sintetasa activa se estaría sintetizando. El efecto para la célula en cuestión sería en la práctica nulo. Por eso ambas enzimas están sometidas a un mismo control que depende a su vez de los niveles de AMP cíclico y de la acción hormonal y en muy estrecha relación con los mecanismos reguladores de la glucólisis y del ciclo de Krebs. Se comprende que un exceso de glucosa, abundante suministro de ácidos grasos, reflejado en niveles altos de ATP estimularía la acción de la glucógeno sintetasa e inactivaría la glucógeno fosforilasa con lo que se almacena glucógeno. Por el contrario, niveles bajos de glucosa por un intenso trabajo muscular u otra causa, con bajos niveles de ATP (con el consecuente aumento del AMP y el ADP) producirían un efecto estimulador sobre la fosforilasa e inhibirían la sintetasa. Analizando el proceso integralmente, el mecanismo de la regulación de la glucogenogénesis y la glucogenólisis depende en primer lugar de la activación e 6 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. inactivación de las enzimas glucógeno sintetasa y la glucógeno fosforilasa, enzimas claves de ambos procesos por incorporación de ácido fosfórico a partir del ATP. La incorporación depende a su vez de dos quinasas o cinasas inespecíficas, las cuales podemos llamar glucógeno sintetasa quinasa y glucógeno fosforilasa quinasa y que llamaremos simplemente cinasa. La acción de esta cinasa es incorporar fósforo a la glucógeno sintetasa la cual se inactiva por este medio y a la glucógeno fosforilasa que por ello es activada, quiere decir que el efecto es contrario para ambas enzimas. Cuando cesa la acción de las cinasas se produce por la acción de las fosfatasas la eliminación del fósforo de la glucógeno sintetasa, con lo cual se activa y de la glucógeno fosforilasa inactivándola. Glucólisis Glucólisis se entiende la degradación de la glucosa. La glucólisis como tal está constituida por una serie de reacciones mediante la cual la glucosa se convierte en ácido pirúvico. Este proceso, hasta aquí es universal y se desarrolla de forma similar en todos los organismos vivos, desde una bacteria hasta el hombre. La degradación de la glucosa hasta ácido pirúvico se conoce como la vía de EmbdenMeyerhof. A partir de este punto, ácido pirúvico, se produce en dependencia de las transformaciones que le ocurran a dicho ácido, diferentes modalidades que varían según los organismos y tejidos analizados y que par ello dan un carácter particular a cada glucólisis en cuestión y que en muchos casos señalan la obligación de aplicar un apellido a la glucólisis que se trate. En las células de los animales superiores el ácido pirúvico presenta dos destinos principales. El primero y más fundamental es su descarboxilación a acetil CoA con la incorporación de este compuesto al ciclo de Krebs o ciclo tricarboxilico donde es oxidado por completo a CO2. Esta glucólisis, que en verdad está formada por tres procesos bien identificados; vía de Embden-Meyerhof, descarboxilación del pirúvico y ciclo de Krebs se acostumbra a llamar glucólisis aerobia y es clásica su reacción global.Esta secuencia se desarrolla, corno es lógico, en tejidos que 7 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. tengan un aporte adecuado de oxígeno, pues requiere de la cadena respiratoria para aceptar los equivalentes de reducción que se producen. La segunda posibilidad del ácido pirúvico en los animales superiores es su reducción a ácido láctico la cual es típica en el tejido muscular en contracción, los eritrocitos y las células del cristalino del ojo. Esta reacción, la cual se desarrolla en un medio carente de oxígeno, es conocida como glucólisis anaerobia Otros organismos, sobre todo las bacterias, presentan distintas variantes en cuanto al metabolismo posterior del ácido pirúvico que caracteriza la forma propia de la utilización de la glucosa. Muchas levaduras, por ejemplo, convierten el ácido pirúvico en alcohol etílico, recibiendo este proceso el nombre genérico de fermentación alcohólica o fermentación etílica. Algunas bacterias producen ácido acético, láctico, propiónico, etcétera, por lo que el proceso recibe entonces el nombre de fermentación acética, fermentación láctica, propiónica.como se presenta en la siguiente figura. Figura 5 : Rutas metabólicas del ácido pirúvico 8 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. Vía de Embden-Meyerhof La vía de Embden-Meyerhof como tal está constituida por una serie de 10 reacciones, que se desarrollan en el citoplasma de la célula, al final de la cual la glucosa queda convertida en dos moléculas de ácido pirúvico. Para su estudio, dada la amplitud de la misma, es conveniente dividirla, de manera didáctica, dos etapas; una primera etapa que podemos llamar transformación de la glucosa en triosas mediante la cual la glucosa se prepara para su catabolismo transformándose en 3 fosfogliceraldehido y una segunda etapa donde se producen las reacciones de óxido-÷reducción y el 3 fosfogliceraldehído se convierte en ácido pirúvico y que llamaremos transformación de las triosas en ácido pirúvico. Pasemos a considerar la primera etapa de la glucólisis donde las hexosas (glucosa) quedan convertidas en triosas. Esta etapa de la glucólisis se inicia en verdad en la mayoría de las células a partir de esta etapa de la glucólisis se inicia en verdad en la mayoría de las células a partir de la glucosa 6 fosfato liberada en la glucogenólisis, sin embargo, para establecer un balance más adecuado la hemos iniciado a partir de la glucosa. En esta primera reacción la glucosa es fosforilada a glucosa 6 fosfato por acción de las hexoquinas que requiere la presencia de iones de Mg y el ATP como donador de radicales de fosfato macroenergético. Se puede considerar una reacción activadora que permite a la glucosa entrar en la secuencia de reacciones de la glucólisis. La hexoquinasa cataliza la reacción de fosforilación de la glucosa y de muchas más hexosas. Es una enzima reguladora pues puede ser inhibida por su propio producto de acción ya que cantidades apreciables de glucosa 6 fosfato en la célula inhibirían su activador alostérico de la glucógeno sintetasa (D). En el hígado la fosforilación de la glucosa puede realizarse por medio de la glucocinasa que no es inhibida por la glucosa 6 fosfato. Esta reacción e irreversible. 9 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. En el siguiente paso la glucosa 6 fosfato es convertida en fructosa 6 fosfato por medio de la fosfohexosa isomerasa (fosfoglucoisomerasa). Es una reacción francamente reversible en ambas direcciones. Continúa la glucólisis con la fosforilación de la fructosa 6 fosfato a fructos 1-6 difosfato. Reacción catalizada por lo fosfofructo cinasa que requiere la colaboración de los iones de magnesio y el ATP como fuente de fosfatos macroenergéticos. Esta reacción es sumamente importante pues la fosfofructo cinasa es una enzima clave que regula toda la glucólisis por varios mecanismos. Esta enzima posee múltiples moduladores alostéricos positivos y negativos que son los responsables de regular su actividad que varían de una célula a otra. Concentraciones elevadas de ácido cítrico, ATP o de ácidos grasos de cadena larga la inhiben, mientras el ADP o el AMP la estimulan. Como es lógico suponer concentraciones elevadas de ATP crearían la posibilidad de su utilización por la célula de forma directa cuando sea necesario, por ello no haría falta seguir oxidando la glucosa. Por otra parte los excesos de glucosa, una vez cubiertos los niveles de glucógeno y de ATP, son convertidos en ácidos grasos a partir del acetil CoA o proveniente de la glucólisis. Para ello la vía de degradación de la glucosa debe ser mantenida, lo cual es realizado por un metabolito intermedio de esta vía, la fructosa 2-6 difosfato, que actúa estimulando la enzima fosfofructocinasa, independiente del nivel inhibitorio del ATP. Con ello la vía continúa hasta el acetil CoA que pasa a formar parte del Ciclo de Krebs. El siguiente esquema resume las vías anabólicas y catabólicas de la glucosa en los animales, teniendo como eje central la glucosa-6-fosfato en la función celular hepática 10 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. GLUCÓGENO 1 2 GLUCOSA -6FOSFATO HEPÀTICA TG ÀCIDOS GRASOS GLUCOSA SANGUÌNEA NADPH 3 5 Àcido pirùvico 7 COLESTEROL 4 RIBOSA-5FOSFATO NUCLEÒTIDOS 6 ACETIL-CoA ATP ADP+Pi 8 e- 9 CO2 O2 10 H2O Figura 6. Rutas metabólicas de la glucosa. Ciclo de Krebs En los animales superiores la única vía degradativa para el acetil CoA es su incorporación al ciclo de Krebs donde es oxidado totalmente a CO 2. Este ciclo, de enorme significación dentro del metabolismo intermediario de los aminoácidos, glúcidos y lípidos, constituye de hecho la etapa final del metabolismo oxidativo de estos tres grupos de compuestos. Conocido inicialmente como ciclo del ácido cítrico y también como ciclo tricarboxílico, por las características de este ácido de poseer tres grupos carboxílicos, hoy se acostumbra a usar el nombre de ciclo de Krebs en homenaje al bioquímico alemán H. A. Krebs quien en 1937, a partir de una serie de experimentos realizados en suspensiones de músculos de paloma, integró y 11 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. postuló la secuencia fundamental de la serie de reacciones cíclicas de esta vía metabólica, a la que él denominó ciclo del ácido cítrico , sentando las bases para un estudio más profundo sobre el tema. El ciclo de Krebs no es una vía metabólica particular de los glúcidos, sino que en sí constituye la vía oxidativa final común para los productos de la oxidación de los aminoácidos, los glúcidos y los ácidos grasos. Los glúcidos, lípidos y aminoácidos en sus vías catabólicas oxidativas, sufren primero una oxidación parcial en procesos metabólicos propios y los productos de esto pasan al ciclo de Krebs, donde son oxidados totalmente hasta CO2. Los aminoácidos originan por desaminación oxidativa determinados cetoácidos; la degradación de la glucosa por la glucólisis conduce a la producción del ácido pirúvico y acetil CoA, mientras que las grasas en su vía oxidativa,conocida como beta oxidación, producen también acetil CoA. Todos estos productos confluyen en el ciclo de Krebs, el cual es posible por la existencia de un juego completo de enzimas ubicadas en la fracción mitocondrial de las células del metabolismo aerobio, muy en relación con las enzimas de la cadena respiratoria, a la que aportan material reductor para la síntesis del ATP, lo cual es su principal objetivo. Por otra parte, aunque el ciclo como tal debe considerarse una vía catabólica, pues su función principal es la degradación del acetil CoA a CO2 , muchas de sus reacciones se encuentran en relación con otras vías del metabolismo. El ciclo, en su conjunto, se desarrolla en las mitocondrias de todas las células del metabolismo aerobio, que poseen las enzimas requeridas para catalizar las 10 reacciones principales de este ciclo, muy en relación con la cadena de respiración a la que aportan equivalentes de reducción (NADH) y (FADH) para la síntesis del ATP. El primer hecho importante de señalar la propia existencia del ciclo, donde al conjugarse los productos finales de los glúcidos, lípidos y aminoácidos, se produce un mayor aprovechamiento de los mismos. La existencia de vías distintas para 12 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. cada uno de estos provocaría una mayor complejidad y menor eficiencia del organismo. Igualmente, es de mencionar la gran cantidad de energía que aporta el ciclo; el sistema del ciclo tricarboxílico es uno de los principales suministradores de material reducido a la cadena respiratoria para la síntesis del ATP. También, varios compuestos del ciclo se utilizan como material para la síntesis de nuevas sustancias. Por ejemplo, a partir de los ácidos axaloacéticos y cetoglutárico se originan por transaminación, los aminoácidos, el ácido aspártico y el ácido glutámico respectivamente, que están muy relacionados tonel ciclo de la úrea. Así mismo, para la síntesis del anillo porfirínico hace falta el succinil CoA. La utilización de los componentes del ciclo para estas reacciones permite sintetizar muchos productos de gran utilidad para el animal. De especial significación es la utilización del oxaloacético para la síntesis de la glucosa (gluconeogénesis), la cual se realiza a partir del ácido láctico, el ácido pirúvico y varios aminoácidos que deben originar como etapa intermedia ácido oxaloacético de forma que el componente central del ciclo se ve muy relacionado con la formación de glucosa en el organismo, por lo cual es posible señalar que todos los compuestos que originan oxaloacético pueden finalmente originar glucosa y glucógeno; por eso se designan con el nombre de glucogenéticos. Es de destacar tambiién la relaciión del ciclo con el nivel de cuerpos cetónicos. Producto de la oxidación de los ácidos grasos se producen residuos de ácido beta hidroxibutírico y beta cetobutírico. Estos compuestos tienen carácter cetónico y pueden oiginar acetona. Normalmente estos compuestos presentan un nivel fisiológico producto del equilibrio que mantienen con el acetil CoA que es oxidado en el ciclo, cuando el aporte de glúcidos es deficiente, no existen los niveles adecuados de oxaloacético para mantener el correcto funcionamiento del ciclo, por tanto, no se oxida el acetil CoA, lo cual provoca aumento en la sangre de los cuerpos cetónicos y se produce la cetosis. Tal es el caso que se produce en la cetosis bovina y en la diabetes mellitus, aunque por causa diferente.El esquema 13 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. que se muestra a continuación,permite observar la integración del ciclo con las demás rutas metabólicas del animal. 14 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. 15 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Escuela de Ciencias Agrícolas, Pecuarias y del Medio Ambiente., ECAPMA. Contenido didáctico del curso Bioquímica Metabólica Elaboró: Jairo Granados., MSc. Figura 7. Integración de las vías metabólicas, a partir del consumo 16