SmPC_Esplenol comp eferv Final
Anuncio

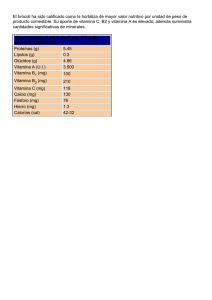
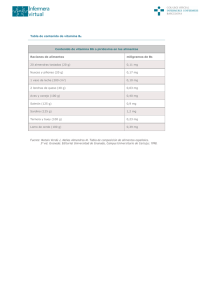
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO ESPLENOL comprimidos efervescentes 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por comprimido efervescente: Extracto etanólico seco estandarizado de raíz de Panax Ginseng G115 (5:1) …………………………... (equivalente a 1,6 mg de ginsenósidos) Retinol (palmitato) (vitamina A)……………………… Tiamina (mononitrato) (vitamina B1)………………… Riboflavina (vitamina B2)……………………..……… Piridoxina (hidrocloruro) (vitamina B6)……………… Cianocobalamina (vitamina B12)…………………...... Acido ascórbico (vitamina C)………………………… Colecalciferol (vitamina D3) ……………………..….. DL- Alfa-Tocoferol acetato (vitamina E)…………...... Nicotinamida …………………………………………. Pantotenato de calcio ………………………………… Deanol (bitartrato) …………………………………… Rutósido (como sulfato de sodio de rutina) .………… Hierro (sulfato de hierro II) …….……………………. Calcio (carbonato, glicerofosfato, fluoruro y pantotenato) Fósforo (glicerofosfato de calcio y de magnesio) ……. Flúor (fluoruro de calcio) ……………………………. Cobre (sulfato de cobre II) …………………………… Potasio (cloruro y acesulfamo de potasio) …………… Manganeso (sulfato de manganeso II) ……….………… Magnesio (glicerofosfato) …………………..………… Zinc (sulfato) …………………………………………… 40 mg 1.500 UI 2 mg 2 mg 1 mg 1 microgramo 60 mg 200 UI 10 mg 15 mg 10 mg 26 mg 20 mg 10 mg 90,6 mg 70 mg 0,2 mg 1 mg 8 mg 1 mg 10 mg 1 mg Eliminado: ¶ Excipientes con efecto conocido: Aceite de soja parcialmente hidrogenado, 0,15 mg; aspartamo (E951), 18 mg (equivalente a 0,010 g de fenilalanina); sacarosa, 221,8 mg; sodio, 235,5 mg (10 mmol); sorbitol (E-420) 190,43 mg; almidón de maíz. Para consultar la lista completa de excipientes, ver sección 6.1. 3. FORMA FARMACÉUTICA Comprimido efervescente. Los comprimidos son redondos de color amarillo claro. 4. DATOS CLÍNICOS 4.1 Indicaciones terapéuticas Estados carenciales de vitaminas y minerales, como en caso de dietas inadecuadas, cuando el aporte de Ginseng además se considere adecuado. Estados pasajeros de agotamiento y decaimiento. Convalecencias. Esplenol comprimidos efervescentes está indicado en mayores de 15 años. 4.2 Posología y forma de administración Posología - Adultos y adolescentes mayores de 15 años: La dosis habitual recomendada es de 1 comprimido efervescente al día, administrado preferiblemente por la mañana, con el desayuno. En caso necesario, por indicación médica, puede aumentarse la dosis a 2 comprimidos, uno por la mañana con el desayuno y otro al mediodía con la comida. Población pediátrica Esplenol no debe administrarse a niños menores de 15 años (ver sección 4.4). Forma de administración Vía oral. El comprimido debe disolverse en una cantidad suficiente de agua y esperar a que cese completamente el burbujeo antes de su ingestión. No debe tomarse de forma continuada durante más de 30 días. Si los síntomas no mejoran o empeoran después de 15-30 días de tratamiento, se debe reevaluar el estado clínico. 4.3 Contraindicaciones - Hipersensibilidad a los principios activos, a análogos o metabolitos de la vitamina D o a alguno de los excipientes incluidos en la sección 6.1. - Insuficiencia renal. - Enfermedades hepáticas o del tracto biliar. - Hipertensión. - Hipercalcemia. - Estados de ansiedad o excitabilidad. - Hipervitaminosis A o D, o exceso de minerales u oligoelementos en sangre u orina. - Este medicamento contiene aceite de soja. No debe utilizarse en caso de alergia a la soja. - Osteodistrofia renal con hiperfosfatemia. - Litiasis cálcica. 4.4 Advertencias y precauciones especiales de empleo - No exceder la dosis recomendada (ver secciones 4.2 y 4.9) - No deberá utilizarse como sustitutivo de una dieta equilibrada y deberán tenerse en cuenta otros aportes de vitaminas y minerales. - Insuficiencia cardiaca: debe considerarse el balance riesgo- beneficio antes de la administración de este medicamento. - Debe considerarse el balance riesgo- beneficio antes de la administración, en los siguientes casos: hiperfosfatemia, arterioesclerosis, sarcoidosis y otras enfermedades granulomatosas, trastornos intestinales graves (como obstrucción), enfermedad de Leber (atrofia hereditaria del nervio óptico). - Se debe tener en cuenta el contenido en flúor de este medicamento cuando se ingieran otros productos o alimentos que lo contengan o si el agua de abastecimiento local contiene una cantidad superior a 0,7 mg/l o ppm. - Se debe administrar con precaución en caso de historia de formación de cálculos renales, ya que el ácido ascórbico, el calcio y los fosfatos pueden potenciar su formación. - Deberán tener precaución los pacientes en tratamiento con: anticoagulantes orales, diuréticos tiazídicos, glucósidos digitálicos, otros productos que contengan vitamina A o análogos, antiácidos que contienen aluminio o magnesio, indinavir, preparados conteniendo vitamina D o análogos, (ver sección 4.5). Población pediátrica Esplenol no debe utiliza en niños menores de 15 años por la presencia de algunos de sus componentes, como el Ginseng. Interferencias con pruebas analíticas Este medicamento contiene principios activos que pueden producir alteraciones en los resultados de pruebas analíticas. - Determinación de bilirrubina: posible aparición de resultados falsamente elevados por el contenido en vitamina A, con el reactivo de Ehrlich. - Determinación de colesterol: posible aparición de concentraciones séricas falsamente elevadas por interferencia de la vitamina A y la D con la reacción de Zlatkis- Zak. - Determinaciones fluorimétricas y tests de laboratorio basados en espectrofotometría o reacciones con color: grandes dosis de riboflavina y nicotinamida pueden producir coloración o sustancias fluorescentes en orina o plasma con posible aparición de resultados falsos. - Tests de laboratorio basados en reacciones de oxidación-reducción: el ácido ascórbico podría interferir con dichos tests. - Determinación de glucosa en orina: pueden aparecer resultados erróneos, por ejemplo con el método de glucosa oxidasa, por la presencia de ácido ascórbico. - Glucosa en sangre: se ha observado una disminución de los niveles de glucosa en sangre tras la administración de Panax ginseng. Esto deberá ser tenido en cuenta especialmente en pacientes diabéticos. - Tests químicos para detectar sangre oculta en heces: probable aparición de falsos negativos, en el test con guayacol, a causa del ácido ascórbico. Advertencias sobre excipientes Este medicamento puede ser perjudicial para personas con fenilcetonuria porque contiene aspartamo que es una fuente de fenilalanina. Este medicamento contiene 10 mmol (235,5 mg) de sodio por comprimido, lo que deberá tenerse en cuenta en el tratamiento de pacientes con dietas pobres en sodio. Este medicamento contiene sacarosa. Los pacientes con intolerancia hereditaria a la fructosa, malabsorción a la glucosa o galactosa, o insuficiencia de sacarasa-isomaltasa, no deben tomar este medicamento. Este medicamento contiene sorbitol. Los pacientes con intolerancia hereditaria a la fructosa no deben tomar este medicamento. Este medicamento contiene aceite de soja. No debe utilizarse en caso de alergia la soja. 4.5 Interacción con otros medicamentos y otras formas de interacción Interacciones debidas al retinol: - Anticoagulantes orales como warfarina y dicumarol: con grandes dosis de vitamina A, probable aumento del efecto anticoagulante y riesgo de hemorragia; se debería monitorizar por posibles signos. - Colestiramina, colestipol, aceite mineral: posible reducción de la absorción de la vitamina A; se deberán separar las dosis lo más posible (al menos 2 horas). - Medicamentos análogos a vitamina A como retinoides: posible aumento de riesgo de toxicidad por vitamina A; se debe evitar su uso concomitante con este medicamento. - Minociclina: posible toxicidad aditiva con vitamina A con probable incremento de riesgo de hipertensión intracraneal benigna (efectos adversos asociados son: dolor de cabeza, trastornos visuales, nauseas, etc.). Interacciones debidas al colecalciferol: - Antiácidos que contengan aluminio o magnesio: no se recomienda su administración conjunta con colecalciferol porque pueden aumentar los niveles séricos de aluminio y su toxicidad, y causar hipermagnesemia, respectivamente, especialmente en pacientes con insuficiencia renal crónica; las tomas se espaciarán al menos 2-3 horas. - Antiepilépticos como hidantoínas (como fenitoína), barbitúricos, primidona o ácido valproico: pueden reducir los efectos de la vitamina D por acelerar su metabolismo; los pacientes tratados durante largo tiempo con anticonvulsivantes pueden requerir suplementos de vitamina D. - Calcitonina y algunos bisfosfonatos: pueden ser antagonizados en el tratamiento de hipercalcemia, con el uso conjunto de vitamina D. - Cimetidina: posible reducción de las concentraciones sistémicas de colecalciferol, debido a aumento del aclaramiento de éste. - Colestiramina, colestipol, aceite mineral, orlistat: probable reducción de las concentraciones sistémicas de colecalciferol, por reducir la absorción intestinal de vitaminas liposolubles como la D; las tomas se espaciarán al menos 2-3 horas. - Diuréticos tiazídicos: puede aumentar el riesgo de hipercalcemia en administración conjunta con vitamina D. - Glucósidos cardiacos: la hipercalcemia que puede causar la vitamina D puede potenciar la toxicidad de los glucósidos digitálicos causando arritmias cardiacas. - Otros análogos de vitamina D: puede producirse efecto aditivo. - Preparados que contienen calcio en altas dosis: posible incremento del riesgo de hipercalcemia. Interacciones debidas al alfa- tocoferol: - Colestiramina, colestipol, aceite mineral, orlistat: probable interferencia con la absorción de vitaminas liposolubles como la E, pudiendo disminuirla; se debería espaciar la toma al menos 2 horas. Interacciones debidas al ácido ascórbico: - Antiácidos que contengan aluminio: no se recomienda su administración conjunta con grandes dosis de ácido ascórbico, especialmente en pacientes con insuficiencia renal, por posible aumento de la absorción de aluminio. - Deferoxamina: el ácido ascórbico en grandes dosis no debería administrarse durante el primer mes de un tratamiento con deferoxamina ya que podría agravar la toxicidad por hierro. - Hierro: el ácido ascórbico puede incrementar la absorción gastrointestinal de hierro. - Indinavir: el ácido ascórbico puede disminuir su concentración plasmática, con probable reducción de su eficacia. Interacciones debidas a la piridoxina: - Altretamina: posible reducción de la respuesta a altretamina. - Amiodarona: posible aumento de fotosensibilidad. - Algunos medicamentos como antituberculosos (isoniazida, cicloserina, etionamida), hidralazina, penicilamina o anticonceptivos orales pueden incrementar los requerimientos de piridoxina. Interacciones debidas a los minerales: - Altas dosis de un mineral pueden reducir la biodisponibilidad de otros minerales y vitaminas: por ejemplo con medicamentos conteniendo calcio, magnesio y otros minerales podrían reducir los niveles de otros minerales como fosfato, hierro, calcio, fluoruro; con la administración de medicamentos conteniendo hierro, zinc, fluoruro y otros minerales puede haber una inhibición de su absorción y eficacia de este medicamento; se debe separar la administración al menos 2 horas de medicamentos como antiácidos u otros con minerales. - Antibióticos como tetraciclinas (por ej. doxiciclina), fluoroquinolonas y similares (norfloxacino, pefloxacino, etc): posible disminución de su absorción y eficacia; la dosis de este medicamento se deben separar varias horas de la administración del antibiótico. - Bisfosfonatos: posible reducción de su absorción por el contenido de minerales como calcio, magnesio, hierro, zinc, etc.; se debe separar la administración de este medicamento un tiempo (aproximadamente 2 horas). - Corticosteroides: posible inhibición de la absorción intestinal de calcio. - Diuréticos tiazídicos: posible aparición de hipercalcemia, en ingestión conjunta con sales de calcio en grandes dosis. Interacciones debidas al ginseng: - Fármacos anticoagulantes como warfarina o acenocumarol: el ginseng podría reducir su eficacia, aumentando el riesgo de coágulo, por lo que no deberían usarse en combinación sin supervisión médica. - Inhibidores de la monoaminoxidasa (IMAO) como tranilcipromina: el ginseng podría potenciar sus efectos con aparición de crisis hipertensivas, con ansiedad, temblores, insomnio, cefaleas, manía. - Digoxina: se ha descrito aumento de sus niveles en sangre. - Fármacos para la diabetes: los pacientes diabéticos podrían tener que ajustar las dosis, ya que el ginseng puede reducir levemente los niveles de glucosa en sangre. - Cafeína: con cantidades excesivas se requiere precaución con la toma de ginseng o evitar su uso conjunto pues se podrían potenciar los efectos estimulantes sobre el sistema nervioso. - Zidovudina: se ha informado de un posible efecto sinérgico del ginseng. 4.6 Fertilidad, embarazo y lactancia Embarazo La experiencia en humanos sugiere que el retinol (vitamina A) produce malformaciones congénitas cuando se administra durante el embarazo. Los estudios realizados en animales han mostrado toxicidad para la reproducción para algunos principios activos (ver sección 5.3). Las dosis de vitamina A que exceden de las dosis diarias recomendadas (2.500 UI/día en U.S.) se deben evitar en mujeres embarazadas o susceptibles de quedarse embarazadas. Se ha observado en un número limitado de informes, la aparición de malformaciones fetales en humanos tras la ingesta por la madre de grandes dosis de vitamina A (10.000 U.I. o más diarias) durante o antes del embarazo. Se ha observado que existe riesgo de aborto espontáneo o malformaciones congénitas en mujeres que han tomado vitamina A en dosis terapéuticas durante el segundo mes de gestación. No debe utilizarse Esplenol comprimidos efervescentes durante el embarazo. Lactancia Algunas vitaminas de este medicamento (D, A, etc.) se excretan en la leche materna en cantidades que pueden tener efectos en el lactante, si se administran dosis terapéuticas en mujeres en período de lactancia. Esplenol comprimidos efervescentes no debe utilizarse durante la lactancia. 4.7 Efectos sobre la capacidad para conducir y utilizar máquinas La influencia de Esplenol comprimidos efervescentes sobre la capacidad para conducir y utilizar máquinas es insignificante pero si el paciente padece algún síntoma de malestar, no debe conducir ni utilizar máquinas peligrosas. 4.8 Reacciones adversas La frecuencia de las reacciones adversas se ha descrito utilizando el convenio de frecuencias MedDRA. Muy frecuentes (≥ 1/10) Frecuentes (≥ 1/100 a < 1/10) Poco frecuentes (≥ 1/1.000 a < 1/100) Raras (≥ 1/10.000 a < 1/1.000) Muy raras (< 1/10.000, incluyendo notificaciones aisladas) Frecuencia no conocida (no puede estimarse a partir de los datos disponibles). Otras reacciones adversas se han notificado durante el periodo de utilización de las vitaminas y minerales que contiene este medicamento; su frecuencia no se ha podido establecer con exactitud. - Trastornos del sistema inmunológico: Frecuencia no conocida: hipersensibilidad a alguno de sus componentes, con erupción cutánea con prurito y urticaria o reacciones más importantes en raras ocasiones (opresión en la garganta, dolor en el pecho…). - Trastornos del sistema nervioso: Frecuencia no conocida: nerviosismo, insomnio, euforia, dolor de cabeza. - Trastornos vasculares: Hipertensión arterial, edema. - Trastornos gastrointestinales: Frecuentes: náuseas, vómitos. Frecuencia no conocida: dolor de estómago, calambres o diarrea, principalmente con grandes dosis. - Trastornos de la piel y el tejido subcutáneo: Frecuencia no conocida: prurito e irritación, eritema facial. - Trastornos renales y urinarios: Coloración amarillo brillante de la orina a causa de la riboflavina, que no interfiere con ninguna función del organismo pero puede interferir con ciertos tests de laboratorio; asimismo, existe el riesgo de formación de cálculos y de precipitar ataques agudos de gota en individuos predispuestos. - Trastornos del aparato reproductor y de la mama: En raros casos se han notificado metrorragia y mastalgia. Notificación de sospechas de reacciones adversas Es importante notificar las sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano. Website: www.notificaRAM.es 4.9 Sobredosis Se describen a continuación algunos de los síntomas de sobredosis de cada principio activo de este medicamento: -Síntomas de toxicidad por Vitamina A: pocas horas después de la administración de una sobredosis de vitamina A se pueden producir: irritabilidad, vértigo, somnolencia, delirio, pseudotumor cerebral, dolor de cabeza y trastornos visuales; pocos días después de una intoxicación puede producirse eritema y descamación de la piel generalizada. Los síntomas generalmente desaparecen en pocos días tras la interrupción del tratamiento. En administración crónica, la cantidad necesaria para producir hipervitaminosis de vitamina A varía considerablemente entre los individuos; el riesgo de toxicidad puede aumentar en caso de enfermedad renal o hepática, hiperlipoproteinemia, etc.; entre las primeras manifestaciones de sobredosis crónica están: fatiga, malestar, letargo, irritabilidad, fiebre leve y sudoración excesiva; los niños pueden dejar de aumentar de peso de forma normal, dolor de huesos largos, mialgia, hipercalcemia e hipercalciuria, osteoporosis y osteosclerosis (con calcificación ectópica de tendones, músculos y tejido subcutáneo); cambios dérmicos como alopecia, dermatitis, cambios en la coloración de la piel, etc. Puede también producirse flujo vascular anormal en el hígado, síntomas de hepatotoxicidad con test anormales de laboratorio; el consumo crónico de vitamina A puede causar daño hepático crónico. - Toxicidad por Vitamina D: la administración de altas dosis de vitamina D y/o durante largos períodos de tiempo puede producir hipercalcemia, hipercalciuria e hiperfosfatemia. Síntomas iniciales de la intoxicación son: debilidad, fatiga, somnolencia, cefalea, anorexia, sequedad de boca, sabor metálico, náuseas, vómitos, espasmos abdominales, poliuria, polidipsia, nicturia, estreñimiento o diarrea, tinnitus, hipotonía (en niños sobre todo), dolor muscular u óseo; síntomas más tardíos de hipercalcemia son: rinorrea, prurito, disminución de la líbido, nefrocalcinosis, insuficiencia renal, osteoporosis en adultos, retardo del crecimiento en niños, anemia, conjuntivitis con calcificación, fotofobia, pancreatitis, calcificación vascular generalizada, convulsiones, calcificación de tejidos blandos; los desequilibrios hidroelectrolíticos junto con moderada acidosis puede dar lugar a arritmias cardiacas. Aunque los síntomas de la sobredosis suelen ser reversibles, se pueden producir calcificaciones en los tejidos blandos, que pueden provocar fallo renal o cardíaco. -Dosis excesivas de Ácido Ascórbico: diarrea o estreñimiento, calambres abdominales, cálculos renales, elevación de la glucosa plasmática, irritación en el epitelio urinario por acción acidificante de la orina; grandes dosis de ácido ascórbico pueden provocar hemólisis en pacientes con deficiencia de Glucosa 6-fosfato deshidrogenasa. -En caso de toxicidad por Nicotinamida se pueden producir trastornos gastrointestinales. -Dosis excesivas de Piridoxina pueden causar neuropatía periférica acompañada de fotosensibilidad. -Dosis excesivas de Vitamina E podrían agravar defectos de coagulación. - Es poco probable que, debido a sus dosis, los minerales produzcan toxicidad en caso de sobredosis de Esplenol comprimidos efervescentes, sin embargo se indican a continuación síntomas característicos de sobredosis. Dosis excesivas de calcio pueden producir niveles altos del mismo en orina y cálculos renales; también es posible hipercalcemia, principalmente en pacientes que reciban grandes dosis de preparados de vitamina D. El fósforo está en relación recíproca con el calcio. Sobredosis de magnesio puede producir hipermagnesemia. Síntomas de intoxicación aguda por hierro, cobre, zinc o fluoruro producen en principio trastornos gastrointestinales; la toxicidad aguda por fluoruro afecta al sistema nervioso central y la crónica se manifiesta en los huesos y los dientes. Dosis elevadas de Ginseng pueden provocar un cuadro de sobrestimulación con hipertensión, nerviosismo, insomnio, aumento de la irritabilidad, erupciones en la piel, dolor de cabeza, mareo, edema, alteraciones digestivas como diarrea matinal, alteraciones menstruales y sensación dolorosa en las mamas. Se ha descrito el llamado “síndrome de abuso de ginseng”, en consumidores habituales de cantidades importantes de raíz de ginseng (3 g diarios) y consumos de hasta dos años de duración, con agravamiento de las reacciones adversas descritas y con síntomas como hipertensión, debilidad y temblores en caso de interrupción brusca del consumo. Las hipervitaminosis A y D son reversibles, desapareciendo normalmente los síntomas a los pocos días de interrumpirse en tratamiento, a no ser que el deterioro renal causado por vitamina D sea grave. En caso de sobredosis se deberá interrumpir el tratamiento con este medicamento y se procederá a la instauración de tratamiento sintomático. 5. PROPIEDADES FARMACOLÓGICAS 5.1 Propiedades farmacodinámicas Grupo farmacoterapéutico: Multivitamínicos con minerales, incluyendo combinaciones. Código ATC: A11AA03. Esplenol contiene una asociación de vitaminas liposolubles, hidrosolubles, minerales y oligoelementos. Estos componentes intervienen en su mayor parte como constituyentes de enzimas o coenzimas en numerosas funciones del organismo, tales como el metabolismo de hidratos de carbono, grasas, aminoácidos, ácidos nucleicos, formación de huesos, transmisión nerviosa y mantenimiento del equilibrio ácido-base. Además, contiene extracto estandarizado de ginseng G115 y deanol, que ejercen un efecto tónico general y rutósido. Las vitaminas liposolubles, retinol, colecalciferol y alfa tocoferol, son almacenadas en los tejidos. Su deficiencia se puede producir, entre otras causas, cuando la ingesta de lípidos está limitada o en caso de problemas de absorción. El retinol es una forma de vitamina A para uso clínico. La vitamina A es esencial para el crecimiento, la reproducción y el funcionamiento de la mayoría de los órganos, destacando sus funciones especializadas en el ojo. El colecalciferol (vitamina D3) es sintetizado en la piel a partir de colesterol en la exposición a la radiación ultravioleta; esta vitamina es necesaria para la formación normal del hueso y la homeostasis mineral; regula las concentraciones séricas de calcio; un metabolito (calcifediol) se forma en el hígado y después es hidroxilado en el riñón a su forma activa (calcitriol); aumenta la eficacia de la absorción intestinal de calcio y fósforo. El tocoferol acetato es una forma de la vitamina E cuya principal función es antioxidante, protegiendo a las membranas celulares. Las vitaminas hidrosolubles (vitaminas del complejo B y vitamina C) actúan principalmente como cofactores de enzimas. La tiamina se combina con adenosín trifosfato (ATP) para formar pirofosfato de tiamina (cocarboxilasa); la tiamina es necesaria para la función del miocardio, células nerviosas y metabolismo de carbohidratos. La riboflavina es un constituyente de dos coenzimas, flavin mononucleótido (FMN) y flavin adenina dinucleótido (FAD), formas activas que participan en numerosas reacciones de oxidación y reducción. La piridoxina existe en tres formas, además como piridoxal y piridoxamina; se conocen como vitamina B6, que sirve como cofactor para muchos enzimas; un efecto de deficiencia seria de piridoxina es neuritis periférica. La cianocobalamina es una forma de la vitamina B12; ésta es activa en todas las células, especialmente en la médula ósea, sistema nervioso central y tracto gastrointestinal; deficiencia de vitamina B12 puede producirse en vegetarianos estrictos, en caso de malabsorción, etc. El ácido ascórbico es un poderoso agente reductor que sirve para proteger el lecho de la membrana capilar; es necesario para la biosíntesis de un precursor de colágeno y dentina; favorece la absorción de hierro desde los alimentos. La nicotinamida es la amida del ácido nicotínico y la forma fisiológicamente activa; son constituyentes de los coenzimas, nicotinamida adenina dinucleótido (NAD) y nicotinamida adenina dinucleótido fosfato (NADP), agentes de transferencia de electrones. La deficiencia de ácido nicotínico puede dar lugar a un síndrome conocido como pelagra, con síntomas como dermatitis, diarrea y demencia (3 Ds). El pantotenato de calcio es la sal cálcica del ácido pantoténico, precursor del coenzima A, que es activo en muchas reacciones biológicas y juega un papel fundamental en la síntesis de ácidos grasos. El deanol (bitartrato) es un precursor de la colina que puede favorecer la formación de acetilcolina. Se ha usado como estimulante y en astenia psíquica. El rutósido es un flavonoide con propiedades que favorecen la circulación de retorno. Los minerales son micronutrientes que están presentes en el organismo en diversos compuestos orgánicos, con funciones como constituyentes de muchas enzimas, hormonas, vitaminas y compuestos inorgánicos; diferentes tejidos del cuerpo contienen cantidades de distintos minerales, como el hueso, con un elevado contenido de calcio, fósforo y magnesio; el fósforo (el 85% de sus reservas están en el hueso) interviene como componente funcional de fosfolípidos, carbohidratos y nucleoproteínas; el calcio, que es el catión más abundante, en un 99% aproximadamente está en el esqueleto, el resto en el fluido extracelular y otras estructuras, y está en relación recíproca con el fósforo; el magnesio participa en la formación del hueso. El hierro se distribuye en los compartimentos metabólicos activo y de depósito, y el funcional se encuentra sobre todo en la hemoglobina. Se almacena en los tejidos como ferritina y hemosiderina. Los minerales también están implicados en la permeabilidad de la membrana celular, la presión osmótica y el equilibrio ácido-básico e hídrico, y algunos actúan en la neurotransmisión; el manganeso es necesario para la síntesis de mucopolisacáridos. Además, el medicamento contiene extracto de raiz Panax Ginseng que ejerce un efecto tónico general. El ginseng contiene mezclas complejas de saponinas denominadas ginsenósidos o panaxósidos. 5.2 Propiedades farmacocinéticas Debido a que el extracto estandarizado de ginseng G115 es un extracto complejo, que contiene más de 200 sustancias identificadas, la realización de estudios farmacocinéticos es muy compleja. Sin embargo, se han realizado estudios farmacocinéticos de los ginsenósidos individuales purificados en diversas especies animales. La biodisponibilidad determinada en ratones, utilizando Ginsenósido Rg1 marcado radiactivamente (C14), originado a partir de extracto estandarizado de ginseng G115, resultó ser del 30 %. Tras la administración intraperitoneal, dependiendo de la especie animal y del tipo de ginsenósido, se determinaron las vidas medias de Ginsenósido Rg1 y Rb1 siendo éstas de 27 minutos y 14.5 horas, respectivamente. Las vitaminas se absorben fácilmente en el tracto gastrointestinal. Su metabolismo es hepático y la eliminación es renal (en el caso de las hidrosolubles) y fecal (en el caso de las liposolubles). Las sales minerales se absorben en el intestino, eliminándose por orina y heces. El deanol muestra una buena absorción por vía oral y se elimina por vía urinaria. Atraviesa la barrera hematoencefálica cuando se administra por vía oral o intraperitoneal. 5.3 Datos preclínicos sobre seguridad Ginseng La DL50 del extracto estandarizado de ginseng G115 por vía oral es superior a 5g/kg en rata y ratón y superior a 2g/kg en cerdo miniatura. La influencia del extracto estandarizado de ginseng G115 en la reproducción, fue estudiada en 2 generaciones de ratas Sprague-Dawley. Se alimentaron a animales de ambos sexos con una dieta control o con una dieta complementada con extracto estandarizado de ginseng G115, a dosis de 1,5, 5 o 15 mg/kg de peso corporal al día. Los parámetros de la reproducción y la lactancia en los grupos tratados fueron comparables para las dos generaciones de madres y crías. No se observaron variaciones relacionadas con el tratamiento en el peso corporal semanal de los animales, consumo de alimentos, parámetros hematológicos y exámenes oftalmológico, histopatológico y macroscópico. La administración de extracto estandarizado de ginseng G115 a ratas Wistar y conejos hembra de Nueva Zelanda embarazadas no causó anormalidades en el desarrollo fetal. Las ratas fueron tratadas con 40 mg/kg/día durante los primeros 15 días tras el apareamiento y los conejos hembra fueron tratados con 20 mg/kg/día del 7º al 16º día tras el apareamiento. La obtención de los fetos fue por cesárea el día 21 en ratas y el 27 en conejos hembras. No se observaron anormalidades en los fetos de ambas especies. Deanol La DL50 del deanol administrado por vía oral fue de 3,1 g/kg en ratones y de 2,6 g/kg en ratas. En estudios de toxicidad subaguda y crónica llevados a cabo en diversas especies animales, se concluyó que el deanol mostraba una buena tolerancia, teniendo en cuenta las dosis mucho más elevadas utilizadas en los estudios con respecto a la dosis terapéutica. Vitaminas La dosis causante de toxicidad aguda en humanos adultos es para la vitamina D y la vitamina A, de 25.000-50.000 U.I y 300.000-900.000 U.I., respectivamente. La dosis causante de toxicidad crónica es de 2.000 U.I. para la vitamina D y de 100.000 U.I. para la vitamina A. Estudios en animales han mostrado toxicidad reproductiva de la sobredosis de vitamina D que se ha asociado a anomalías fetales. La vitamina A en altas dosis es teratogénica en animales. En estudios de reproducción en animales se ha informado de anomalías fetales en el SNC, ojo, paladar y tracto urogenital, asociados con sobredosis de vitamina A. En animales, se produjo síndrome de ácido retinoico con la administración de altas dosis de vitamina A, caracterizado por malformaciones en el SNC, craneofaciales, cardiovaculares y en el timo; en humanos se observaron anomalías similares en pacientes en tratamiento con ácido retinoico que se quedaron embarazadas. La vitamina E en dosis muy altas en animales puede causar hemorragias, incremento del tiempo de protrombina y trastornos de la coagulación. Se ha visto que la vitamina E inhibe la producción de prostaglandina E2 y mejora la respuesta inmune en ratones viejos. Existe una sospecha de posible teratogenicidad por hierro en un estudio retrospectivo en el que se observó que la incidencia de anomalías congénitas fue mayor en mujeres que habían tomado suplementos de hierro durante el primer trimestre del embarazo, comparado con las que no lo habían tomado durante ese período. Estudios in vitro indican que cuando se exponen concentraciones de 45 a 135 ppm de fluoruro sódico a queratinocitos orales humanos durante 4 horas pueden causar síntesis anormal de DNA. No se han realizado estudios in vivo utilizando concentraciones de fluoruro (12.000 a 14.000 ppm) mucho mayores que las dosis de los estudios in vitro. 6. DATOS FARMACÉUTICOS 6.1 Lista de excipientes Gelatina Sacarosa Almidón de maíz (sin gluten) DL-alfa-tocoferol Aceite de soja parcialmente hidrogenado Citrato de sodio Ácido cítrico Maltodextrina Hidrógenocarbonato de sodio Aspartamo (E-951) Acesulfamo de potasio Sorbitol (E-420) Povidona Macrogol 6000 Estearato de magnesio Aromas de naranja, mandarina y limón. 6.2 Incompatibilidades No procede. 6.3 Periodo de validez 2 años 6.4 Precauciones especiales de conservación No conservar a temperatura superior a 30ºC. Mantener el envase perfectamente cerrado. 6.5 Naturaleza y contenido del envase Frasco de polipropileno con tapón de polietileno y agente desecante. Envases conteniendo 15 comprimidos efervescentes. 6.6 Precauciones especiales de eliminación La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con las normativas locales. 7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN BOEHRINGER INGELHEIM ESPAÑA, S.A Prat de la Riba, 50 08174 Sant Cugat del Vallès (Barcelona). 8. NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN 65.378 9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN Fecha de la primera autorización: 21/05/2003. Fecha de la última renovación: 21/05/2008. 10. FECHA DE LA REVISIÓN DEL TEXTO Julio/2013