Equilibrio Iónico
Anuncio
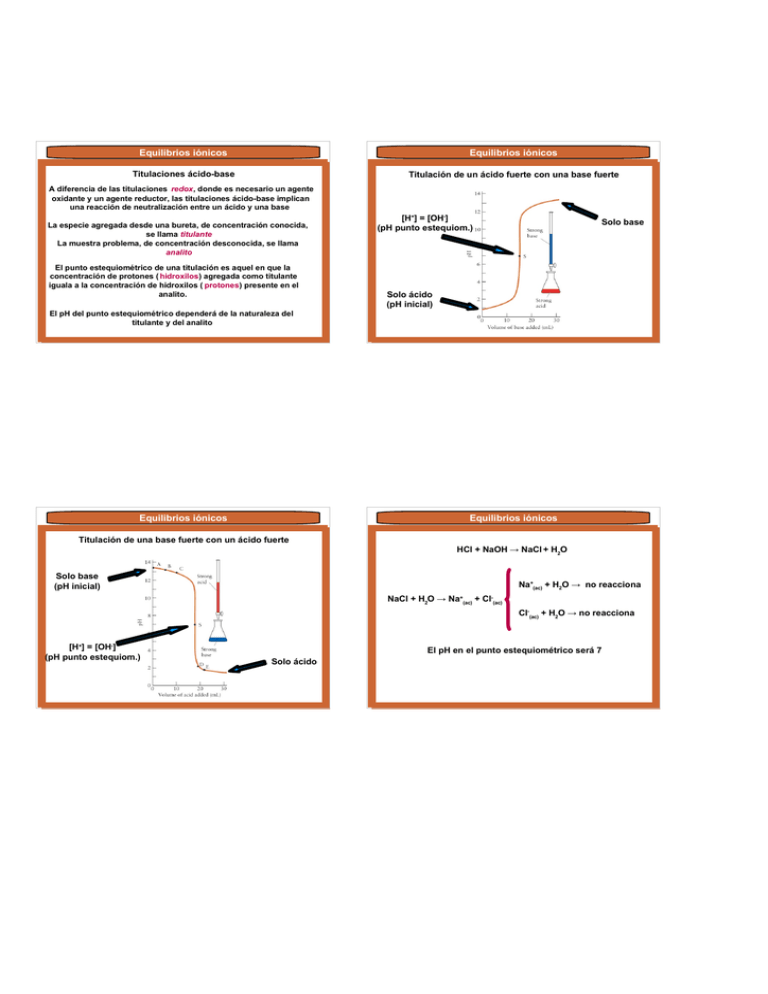
Equilibrios iónicos Equilibrios iónicos Titulaciones ácido-base Titulación de un ácido fuerte con una base fuerte A diferencia de las titulaciones redox, donde es necesario un agente oxidante y un agente reductor, las titulaciones ácido-base implican una reacción de neutralización entre un ácido y una base La especie agregada desde una bureta, de concentración conocida, se llama titulante La muestra problema, de concentración desconocida, se llama analito El punto estequiométrico de una titulación es aquel en que la concentración de protones ( hidroxilos) agregada como titulante iguala a la concentración de hidroxilos ( protones) presente en el analito. [H+] = [OH-] (pH punto estequiom.) Solo base Solo ácido (pH inicial) El pH del punto estequiométrico dependerá de la naturaleza del titulante y del analito Equilibrios iónicos Equilibrios iónicos Titulación de una base fuerte con un ácido fuerte HCl + NaOH → NaCl + H2O Solo base (pH inicial) Na+(ac) + H2O → no reacciona NaCl + H2O → Na+(ac) + Cl-(ac) Cl-(ac) + H2O → no reacciona [H+] = [OH-] (pH punto estequiom.) El pH en el punto estequiométrico será 7 Solo ácido Equilibrios iónicos Equilibrios iónicos Titulación de 25 mL de HCl 0.1 M con NaOH 0.1 M Titulación de un ácido débil con una base fuerte VH C l VNa O H Vt o t a l Moles H+ Moles OH- Exceso (M) pH 25.00 0.0 25.00 0.0025 0.00 0.1 (H+) 1.0 25.00 10.00 35.00 0.0025 0.0010 0.043 (H+) 1.4 25.00 24.99 49.99 0.0025 0.002499 0.00002 (H +) 4.7 25.00 25.00 50.00 0.0025 0.0025 0 7.0 25.00 25.01 50.01 0.0025 0.002501 0.00002 (OH-) 25.00 26.00 51.00 0.0025 0.0026 0.002 (OH ) 11.3 25.00 50.00 75.00 0.0025 0.0050 0.033 (OH-) 12.5 9.3 - [H+] = [OH-] (pH punto estequiom.) Solo ácido (pH inicial) Equilibrios iónicos Equilibrios iónicos CH3COOH + NaOH → NaCH3COO + H2O Titulación de una base débil con un ácido fuerte Na+(ac) + H2O → no reacciona NaCH 3COO + H2O → Na + + Ac (ac) - (ac) Ac-(ac) + H2O HAc (ac) + OH - Solo base (pH inicial) El pH en el punto estequiométrico será mayor que 7 [H+] = [OH-] (pH punto estequiom.) Equilibrios iónicos Equilibrios iónicos HCl + NH4OH → NH4Cl + H2O NH4+(ac) + H2O NH3 + H3O+ NH4Cl + H2O → NH4+(ac) + Cl-(ac) Cl-(ac) + H2O → no reacciona El pH en el punto estequiométrico será menor que 7 Equilibrios iónicos Equilibrios iónicos Calculo del pH durante una titulación de un ácido o base débil con una base o ácido fuerte Cada agregado de NaOH lleva a una neutralización total de los OH- Se titulan 25 mL de HAc 0.1 M (0.0025 moles) con NaOH 0.1 M HAc + H2O −5 H3O+( a c ) + Ac-( a c ) K a =1.8×10 - = + [ Ac ][ H ] [ HAc] + El pH inicial será [ H ]= [ HAc] K a pH =2.9 HAc + OHC0 x C0 – x H2O + Ac0 0 - x y el pH se calcula según - pH = pK a log [ Ac ] [ HAc ] Ejemplo: al agregar 10 mL de NaOH 0.1 M (0.0010 moles) se tiene HAc + OHH2O + Ac0.0025 0.0010 0 Equilibrios iónicos HAc + OH0.0025 0.0010 0.0015 Equilibrios iónicos Al agregar 25 mL de NaOH 0.1 M (0.0025 moles) la neutralización es total H2O + Ac0 0 - HAc + OH0.0025 0.0025 0.0010 [HAc] = 0.0015 moles x 1000 mL / 35 mL = 0.043 M [Ac-] = 0.0010 moles x 1000 mL / 35 mL = 0.029 M - pH = pK a log [ Ac ] =4.57 [ HAc ] 0 0 H2O + Ac0 - 0.0025 y el pH corresponde a una solución de NaAc de la concentración correspondiente [Ac-] = 0.0025 moles x 1000 mL / 50 mL = 0.050 M El anión Ac- hidróliza por ser base conjugada de un ácido débil Ac- + H2O 0.050 0.050 - x - Equilibrios iónicos K h= Equilibrios iónicos Uso de indicadores ácido-base para determinar el pH del punto estequiométrico de una titulación 2 Kw [ HAc ][OH ] x −10 =5.6×10 = = Ka 0.050−x [ Ac ] Condición: el rango de pH en que el indicador cambia de color debe encontrarse en la zona vertical de la curva de pH vs volumen de titulante [OH-] = 5.3x10- 6 M → pOH = 5.28 → pH = 8.72 Al agregar 30 mL de NaOH, el exceso de OH- inhibe la hidrólisis del ion AcHAc + OH 0.0025 0.0030 0 Ac- + H 2O 0.045 0.045 - x - Como tenemos un rango de pH en que el indicador cambia de color, el punto estequiométrico es determinado de forma aproximada. Por tal razón, hablamos de punto final de una titulación H2O + Ac 0 0.0005 - 0.0025 HAc + OH 0 0.009 x 0.009 + x HAc + OH0 0 x x pH = 11.9 Equilibrios iónicos Equilibrios iónicos rango de pH en que debe actuar un indicador para poder ser usado en esta titulación rango de pH en que debe actuar un indicador para poder ser usado en esta titulación Equilibrios iónicos Problema 11. ¿Qué indicador de los dados anteriormente utilizaría para una titulación de 25 mL de HAc 0.1 M con NaOH 0.1 M? Problema 12. Si un ácido débil HX tiene una Ka desconocida, ¿Cómo aprovecharía una curva de titulación para determinar la constante? Equilibrios iónicos Equilibrios de solubilidad Una solución saturada de una especie sólida en agua contiene la máxima cantidad de la misma disuelta en una cantidad determinada del solvente a una temperatura dada Si la especie se agrega en exceso, algo de la misma permanecerá precipitada, de forma que podemos pensar en un equilibrio CA( s ) C+( a c ) + A-( a c ) La constante de equilibrio para este proceso se denomina producto de solubilidad y se escribe Kp s Kp s = [C+] [A-] Equilibrios iónicos La solubilidad molar de una sustancia, S, es la cantidad máxima de la misma, medida en moles, que puede disolverse en un litro de solución. Sus unidades son mol L-1 o M. CA( s ) CA( a c ) S 0 CA( a c ) S C + (ac) 0 S +A 0 S (ac) Kp s = S2 Equilibrios iónicos Y de forma más general, CxAy ( s ) CxAy ( a c ) S 0 CxAy ( a c ) S x C+( a c ) + y A-( a c ) 0 0 xS yS Kp s = (x S)x (y S)y Si conocemos la solubilidad molar de una sustancia podemos conocer su producto de solubilidad Si conocemos el producto de solubilidad de una sustancia podemos conocer su solubilidad molar Equilibrios iónicos Equilibrios iónicos Problema 13. Si la solubilidad molar del Ag2CrO4 es 6.5x10- 5 M, calcular el valor de Kp s para esa sal. Factores que afectan la solubilidad Ag2CrO4 (s) Ag2CrO4 ( a c ) S 0 Kp s = (2S)2 S Ag2CrO4 ( a c ) S 2 Ag+( a c ) + CrO42 - ( a c ) 0 0 2S S Kp s = 4 S3 Kp s = 1.1x10- 1 2 Efecto del ion común: el agregado de una sal o hidróxido conteniendo un ion en común con la especie que forma la solución saturada de interés, disminuye la solubilidad de la misma. Equilibrios iónicos CaF2 S 0 (a c ) Ca2 +( a c ) + 2 F- ( a c ) 0 0 S 2S Equilibrios iónicos Efecto del pH ¿pH de una solución saturada de Mg(OH)2? Mg(OH)2 Kp s = 1.7x10- 1 0 = S (2S)2 (s) Mg2 +( a c ) + 2 OH- ( a c ) S = (1.7x10- 1 0 / 4)1 / 3 = 3.5x10- 4 M Kps = [Mg2 +] [OH-]2 CaF2 S 0 1.8x10- 1 1 = S (2S)2 (a c ) Ca2 +( a c ) + 2 F- ( a c ) 0 0.10 M S 2 S + 0.10 Kps = 1.7x10- 1 0 = S (2S + 0.10)2 ≈ S (0.10)2 S = 1.7x10- 1 0 / 0.010 = 1.7x10- 8 M S = 1.7x10- 4 M [OH-] = 2 S = 3.4x10- 4 M → pOH = 3.48 → pH = 10.52 Una solución saturada de Mg(OH)2 tendrá un pH de 10.52 Equilibrios iónicos Mg(OH)2 (s) Equilibrios iónicos Mg2 +( a c ) + 2 OH- ( a c ) CaF2 En presencia de una solución amortiguadora de pH = 9 pH = 9 → pOH = 5 → [OH-] = 1.0x10- 5 M [OH-] permanece constante Kps = [Mg2 +] [OH-]2 1.8x10- 1 1 = S (1.0x10- 5)2 S = 0.18 M La solubilidad del hidróxido aumentó por el aumento de la acidez del medio (s) F- ( a c ) + H2O CaF2 (s) + 2 H2O Ca2 +( a c ) + 2 F- ( a c ) HF ( a c ) + OH- ( a c ) Ca2 +( a c ) + 2 HF ( a c ) + 2 OH- ( a c ) Equilibrios iónicos Equilibrios iónicos Problema 14. Indique si la solubilidad de las siguientes sustancias se ve influenciada por el pH: a) Ni(OH)2; b) CaCO3; c) BaSO4. a) Ni(OH)2 ( s ) Ni(OH)2 +2H + (s) CaCO3 (ac) 2 H2O Ni 2+ (ac) (s) + H2O HCO3- ( a c ) + OH- ( a c ) Ca2 +( a c ) + HCO3- ( a c ) + OH- ( a c ) Un aumento de la acidez favorece la solubilidad (recordar el CaF2) + 2 H2O Un aumento de la acidez favorece la solubilidad (recordar el Mg(OH)2) Ca2 +( a c ) + CO32 - ( a c ) CO32 - ( a c ) + H2O Ni2 +( a c ) + 2 OH- ( a c ) 2 OH- ( a c ) + 2 H+ ( a c ) CaCO3 ( s ) b) BaSO4 c) (s) Ba2 +( a c ) + SO42 - ( a c ) SO42 - ( a c ) + H2O BaSO4 (s) + H2O HSO4- ( a c ) + OH- ( a c ) Ba2 +( a c ) + HSO4- ( a c ) + OH- ( a c ) Equilibrios iónicos Equilibrios iónicos Precipitación selectiva Q = [Pb2 +] [SO42 -] Las sales Pb(NO3)2 y Na2SO4 son extremadamente solubles en agua y están completamente disociadas Si Q > Kp s precipitará PbSO4 hasta que Q = Kp s Una mezcla de ambas formará también PbSO4 y NaNO3 Si Q < Kp s no precipita PbSO4 y se puede disolver más hasta que Q = Kp s El NaNO3 es muy soluble, pero el PbSO4 tiene un Kp s de 1.6x10- 8 Dependiendo de las concentraciones iniciales de Pb(NO3)2 y Na2SO4 puede haber precipitación de PbSO4 o no Si Q = Kp s no precipita PbSO4 y no se disolverá sólido ya que tenemos una solución saturada Equilibrios iónicos Problema 15. Determinar si se formará precipitado al mezclar 100 mL de Pb(NO3)2 3.0x10- 3 M y 400 mL de Na2SO4 5.0x10- 3 M. Kp s(PbSO4) = 1.6x10- 8 [Pb2 +] = 3.0x10- 3 M x 100 mL / 500 mL = 6.0x10- 4 M [SO42 -] = 5.0x10- 3 M x 400 mL / 500 mL = 4.0x10- 3 M Q = [Pb2 +] [SO42 -] = 2.4x10- 6 Como Q > Kp s tendremos precipitado de PbSO4 Equilibrios iónicos Problema 16. Una solución contiene los iones Mg2 + (0.050 M) y Cu2 + (0.020 M). ¿Qué ion precipitará primero al agregar OH-? ¿Qué concentración de OH- es necesaria para iniciar cada precipitación? Kp s(Mg(OH)2) = 1.8x10- 1 1, Kp s(Cu(OH)2) = 2.2x10- 2 0 Cuanto menor es el valor del Kp s, más insoluble es la especie Para el Mg(OH)2 Kp s = [Mg2 +] [OH-]2 - [OH ]= K ps + [ Mg ] = 1.8×10−11 −5 =1.9×10 M 0.05 Para el Cu(OH)2 Kp s = [Cu2 +] [OH-]2 - [OH ]= K ps [ Cu+ ] = 2.2×10−20 −9 =1.0×10 M 0.02 Equilibrios iónicos Es posible separar iones presentes en solución por el agregado de otro ion que forme sales insolubles con ellos. La clave de la separación son los distintos valores de los Kp s, cuanto más diferentes sean esos valores más fácil será la separación