Ponencia
Anuncio

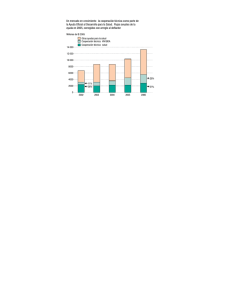
las variaciones en números Variaciones (por procedimiento nacional) Solicitudes 12000 10000 8767 7588 8000 7769 7386 6601 5804 6000 4984 4950 4193 4000 Diferencia entre solicitado y autorizado 3018 2719 2395 12000 2000 10000 Tipo I 0 2005 2006 2007 2008 2009 2010* Autorizaciones 12000 9799 9419 10000 8000 6000 9807 8610 8000 5658 6000 5758 5379 4000 5374 Tipo II 4355 4000 2000 3313 1718 2000 2008 0 0 2005 2006 2007 tipo I 2008 tipo II 2009 2010* 2005 2006 2007 2008 2009 2010* Variaciones (solicitudes por procedimiento nacional y MRP/DCP) Solicitudes variaciones tipo I 12000 10000 8767 7588 8000 7769 7386 6679 6601 6254 5804 6000 Diferencia entre solicitudes tipo I 10000 4000 3865 3645 3313 9000 2033 2000 8000 nacionales 0 2005 2006 2007 2008 2009 2010 7000 6000 Solicitudes variaciones tipo II 12000 5000 10000 4000 8000 3000 6000 4193 4000 2395 2000 2719 1718 1909 2407 3112 3018 RMP/DCP 4984 4950 3690 2000 1000 1331 0 0 2005 2006 2007 Nacional 2008 MRP/DCP 2009 2010 2005 2006 2007 2008 2009 2010 Variaciones (solicitudes por procedimiento nacional y MRP/DCP) Solicitudes variaciones tipo I 12000 10000 8767 7588 8000 7769 7386 6679 6601 6254 5804 6000 Diferencia entre solicitudes tipo II 6000 4000 3865 3645 3313 2033 2000 5000 nacionales 0 2005 2006 2007 2008 2009 2010 Solicitudes variaciones tipo II 12000 4000 3000 10000 8000 2000 6000 4000 2395 2000 2719 1718 1909 2407 3112 3018 RMP/DCP 4984 4950 4193 3690 1000 1331 0 0 2005 2006 2007 Nacional 2008 MRP/DCP 2009 2010 2005 2006 2007 2008 2009 2010 • Entrada en vigor del RD 1091/2010 • Presentación de traducciones de prospectos y fichas técnicas a la AEMPS • Directrices para la resolución de variaciones de adecuación al RD 1345/2007 y otras variaciones coexistentes en el tiempo • Aplicación de la Cláusula “Sunset” • Proyecto “Medicamento accesible” • Entrada en vigor del RD 1091/2010 • Aplicar las ventajas del nuevo marco normativo a todos nuestros procedimientos texto después de alegaciones Disposición adicional única. Modificación de las autorizaciones de comercialización de medicamentos de uso humano autorizados con anterioridad al 1 de enero de 1998. A la entrada en vigor del Reglamento que dicte la Comisión Europea, en cumplimiento de la previsión establecida en el apartado 4 del artículo 23 ter de la Directiva 2001/83/CE, el capítulo VI del Real Decreto 1345/2007, de 11 de octubre, continuará resultando de aplicación a las modificaciones de las autorizaciones de comercialización de los medicamentos de uso humano autorizados con anterioridad al 1 de enero de 1998, siempre que en dicha fecha el medicamento no se encontrase autorizado en otro Estado miembro. texto final del RD 1091/2010 Disposición adicional única. Modificación de las autorizaciones de comercialización de medicamentos de uso humano autorizados con anterioridad al 1 de enero de 1998. Hasta la entrada en vigor del reglamento de aplicación a las autorizaciones de comercialización que dicte la Comisión Europea, en cumplimiento de la previsión establecida en el apartado 4 del artículo 23 ter de la Directiva 2001/83/CE, el capítulo VI del Real Decreto 1345/2007, de 11 de octubre, en su redacción anterior a la vigente, continuará resultando de aplicación a las modificaciones de las autorizaciones de comercialización de los medicamentos de uso humano autorizados con anterioridad al 1 de enero de 1998, siempre que en dicha fecha el medicamento no se encontrase autorizado en otro Estado miembro. texto después de alegaciones Disposición adicional única. Modificación de las autorizaciones de comercialización de medicamentos de uso humano autorizados con anterioridad al 1 de enero de 1998. A la entrada en vigor del Reglamento que dicte la Comisión Europea, en cumplimiento de la previsión establecida en el apartado 4 del artículo 23 ter de la Directiva 2001/83/CE, el capítulo VI del Real Decreto 1345/2007, de 11 de octubre, continuará resultando de aplicación a las modificaciones de las autorizaciones de comercialización de los medicamentos de uso humano autorizados con anterioridad al 1 de enero de 1998, siempre que en dicha fecha el medicamento no se encontrase autorizado en otro Estado miembro. texto final del RD 1091/2010 Disposición adicional única. Modificación de las autorizaciones de comercialización de medicamentos de uso humano autorizados con anterioridad al 1 de enero de 1998. Hasta la entrada en vigor del reglamento de aplicación a las autorizaciones de comercialización que dicte la Comisión Europea, en cumplimiento de la previsión establecida en el apartado 4 del artículo 23 ter de la Directiva 2001/83/CE, el capítulo VI del Real Decreto 1345/2007, de 11 de octubre, en su redacción anterior a la vigente, continuará resultando de aplicación a las modificaciones de las autorizaciones de comercialización de los medicamentos de uso humano autorizados con anterioridad al 1 de enero de 1998, siempre que en dicha fecha el medicamento no se encontrase autorizado en otro Estado miembro. • Entrada en vigor del RD 1091/2010 • Aplicar las ventajas del nuevo marco normativo a • • • • todos nuestros procedimientos Clasificación de las variaciones Asunción de las directrices y de su actualización Presentación de las variaciones Resolución de las variaciones • Entrada en vigor del RD 1091/2010 • Aplicar las ventajas del nuevo marco normativo a • • • • todos nuestros procedimientos Clasificación de las variaciones Asunción de las directrices y de su actualización Presentación de las variaciones Resolución de las variaciones Simplificación Transparencia y previsibilidad Eficiencia (evaluación adaptada al riesgo) Flexibilidad ¿Cómo 3 …hacer operativa la adopción del Reglamento (CE) 1234/2008? • Modificación del RD 1345/2007 • Adaptación a las “Guidelines” • Consenso de procedimientos • Modificación de RAEFAR • Convivencia de ambas clasificaciones (a extinguir) Octubre 2009 División de Gestión División de Clínica División de Química División de Biológicos División de Farmacovigilancia División de Sistemas de la Información Área Jurídica