introducción a los metabolismos - U
Anuncio

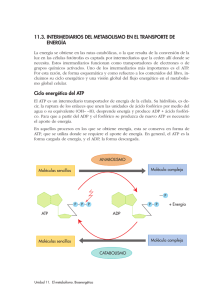
Universidad de Chile Programas de Magíster en Nutrición y Alimentos REGULACIÓN DE LA ABSORCIÓN Y METABOLISMO DE LOS NUTRIENTES INTRODUCCIÓN A LOS METABOLISMOS Dra. Catalina Carrasco 05 de abril de 2012 50 MACRONUTRIENTES MATERIA PRIMA COMBUSTIBLE RESPIRACIÓN CELULAR SÍNTESIS ENERGÍA Trabajo celular Impulso nervioso Contracción muscular Movimiento organelos ENERGÍA CAPACIDAD DE REALIZAR UN TRABAJO Contenida en los enlaces químicos entre los átomos que forman las moléculas que constituyen de los alimentos CAPACIDAD PARA REALIZAR UNA ACCIÓN QUÍMICA METABOLISMO (del griego “metabole”, cambio) El metabolismo es “el mapa de rutas” de miles de reacciones químicas que ocurren en la célula. Las enzimas dirigen dichas rutas metabólicas, acelerando diferencialmente reacciones determinadas. Es el proceso por el cual los sistemas vivos adquieren y usan la energía para llevar adelante las funciones vitales. Comprende los procesos físicos y químicos involucrados en el mantenimiento y reproducción de la vida. OBJETIVOS DEL METABOLISMO Obtención de energía útil (ATP) para la célula, a partir de moléculas orgánicas. Convertir nutrientes macromoléculas. exógenos en precursores de Construcción de macromoléculas propias a partir de dichos precursores. Formación y degradación de las macromoléculas, como: hormonas, neurotransmisores, proteínas, lípidos de membrana, etc. CARACTERÍSTICAS DEL METABOLISMO 1. El producto de una reacción metabólica puede ser el sustrato de otra. Muchas reacciones se encadenan y forman una secuencia ordenada, que se denomina vía o ruta metabólica, como por ejemplo la glucólisis, oxidación, ciclo de la ornitina, etc. A B C D CARACTERÍSTICAS DEL METABOLISMO 2. Cada vía metabólica tiene una finalidad, por ejemplo, la glucólisis es la ruta de degradación de la glucosa para obtener energía, el ciclo de Calvin sintetizar monosacáridos en la fase oscura de la fotosíntesis, etc. Las rutas metabólicas pueden ser: -Lineales, en las que se parte de un metabolito inicial que se va transformando y origina otro distinto, (A B C D) como la glucólisis - Circulares, como el Ciclo de Krebs, el de la ornitina o el de Calvin, en las que se parte de un metabolito que sufre distintas transformaciones para originar distintos productos y regenerar el metabolito inicial. CARACTERÍSTICAS DEL METABOLISMO 3. Muchas reacciones (vías o rutas) tienen lugar simultáneamente, y para evitar interferencias entre ellas cada una ocurre en un compartimiento celular específico, las rutas están compartimentalizadas y con ello la eficacia enzimática aumenta. Por ejemplo: Citoplasma: Glucólisis, gluconeogénesis, síntesis de triglicéridos y de proteínas (traducción). Mitocondria: Ciclo de krebs, -oxidación, fosforilación oxidativa. Retículo endoplasmático: síntesis de lípidos y de proteínas. Núcleo: duplicación y transcripción. CARACTERÍSTICAS DEL METABOLISMO Piruvato deshidrogenasa 24 cadenas polipeptídicas, contiene TPP (pirofosfato de tiamina, vitamina B1). Decarboxilación. Dihidrolipoamida transacetilasa 24 cadenas polipeptídicas, contiene 2 moléculas de ácido lipoico. Acetilación. Dihidrolipoamida deshidogenasa 12 cadenas polipeptídicas, contiene FAD (Flavin adenin dinucleótido). Oxido-reducción 4. El metabolismo está regulado por enzimas, que son específicas de cada metabolito o sustrato y actúan sobre cada ruta metabólica. A veces varias enzimas se asocian para aumentar su eficacia y constituyen complejos multienzimáticos como el de la piruvato deshidrogenasa, que actúa sobre el piruvato al entrar en la mitocondria. OXIDACIÓN DEL PIRUVATO La reacción es aparentemente sencilla, Piruvato + NAD+ + CoA → acetil-CoA + NADH + H+ + CO2 ΔG´º = - 33.5 KJ/mol CARACTERÍSTICAS DEL METABOLISMO 5. La energía desprendida en las reacciones exotérmicas o exergónicas (liberan energía) se utiliza en las endergónicas (consumen energía). Moléculas especializadas, como el ATP. RESUMEN CARACTERÍSTICAS DEL METABOLISMO 1.- Vía o Ruta metabólica 2.- Finalidad 3.- Compartimentalizadas 4.- Regulado por enzimas 5.- Exergónicas o endergónicas METABOLISMO CATABOLISMO • ANABOLISMO Los tres componentes solidos principales (98%) de los alimentos son los carbohidratos, los lípidos y las proteínas responsables de proveer la casi totalidad de la energia requerida para todas las funciones celulares. • Los carbohidratos representan cerca del 50-60% de los alimentos sólidos del ser humano y químicamente se les identifica como polisacáridos. • El 20% de los alimentos sólidos en el hombre son las proteínas. • El 20-30% restante son los lípidos, componentes primordiales de los aceites y las grasas, cuyo representante más común son los triacilglicéridos. METABOLISMO CATABOLISMO ANABOLISMO ANFIBOLISMO: Reacciones que permiten almacenar la energía. CATABOLISMO Liberan energía por ruptura de enlaces químicos de moléculas complejas a otra más simple. La energía liberada es almacenada en los enlaces fosfato de alta energía del ATP. Pasa de moléculas con alto contenido energético (muy reducidas) a otras con escaso contenido (muy oxidadas). •Reacciones de degradación o destrucción •Reacciones de oxidación •Desprenden energía •A partir de muchos sustratos distintos, se originan los mismos productos (rutas convergentes) ANABOLISMO Consumen energía para construir moléculas de mayor tamaño a partir de moléculas más simples. Se crean nuevos enlaces, para ello es necesario un aporte de energía, el ATP. Las nuevas moléculas son almacenadas para luego ser utilizadas o formar parte de la célula. •Reacciones de síntesis o construcción •Reacciones de reducción •Consumen energía •A partir de pocos sustratos distintos, se originan muchos productos distintos (rutas divergentes) CATABOLISMO reacciones exergónicas ANABOLISMO reacciones endergónicas FASES DEL CATABOLISMO Y ANABOLISMO FASE I “fase inicial o preparatoria” Las grandes macromoléculas se degradan en sus monómeros con enzimas específicas. Ocurre fuera de la célula, como en la digestión. No se libera energia utilizable durante esta primera etapa. Fase I C A T A B O L I S M O FASES DEL CATABOLISMO Y ANABOLISMO FASE I “fase inicial o preparatoria” Las grandes macromoléculas se degradan en sus monómeros con enzimas específicas. Ocurre fuera de la célula, como en la digestión. FASE II “fase intermedia”: Los monómeros son degradados por procesos específicos hasta Acetil-CoA. Glucólisis, -oxidación, transaminación. Se genera una pequena cantidad de ATP Fase I C A T A B O L I S M O Fase II FASES DEL CATABOLISMO Y ANABOLISMO FASE I “fase inicial o preparatoria” Las grandes macromoléculas se degradan en sus monómeros con enzimas específicas. Ocurre fuera de la célula, como en la digestión. FASE II “fase intermedia”: Los monómeros son degradados por procesos específicos hasta Acetil-CoA. Glucólisis, b-oxidación, transaminación. Se genera una pequena cantidad de ATP FASE III “fase final”: El Acetil-CoA es oxidado hasta CO2 y H2O, originando gran cantidad de NADH (poder reductor) y ATP. Ocurre en la mitocondria. El catabolismo y anabolismo son simultáneos y son interdependientes, pero NO SON exactamente las mismas reacciones en sentido contrario: •Muchas reacciones catabólicas son irreversibles. •Las rutas catabólicas y anabólicas pueden localizarse en distintos compartimentos •La regulación enzimática es distinta en casi todas los procesos. Fase I C A T A B O L I S M O Fase II Fase III A N A B O L I S M O ATP ADENOSIN TRIFOSFATO •El ATP no se almacena. •Continuo consumo y producción. •Se consumen 45 kg de ATP al día, pero la cantidad presente es menor de 1 g. Adenina es una de las cinco bases nitrogenadas. derivada de las purinas, que forman parte del ADN y ARN Ribosa, es una pentosa Trifosfato PAPEL DEL ATP EN EL METABOLISMO La célula puede realizar tres clases principales de trabajo donde se requiere energía: Bombeo sustancias e iones a través de la membrana en contra de la dirección del movimiento espontáneo. ATP Batido de cilias y flagelos, contracción células musculares, fluir del citoplasma dentro de la célula o movimiento cromosomas en la división celular. Impulso de reacciones endergónicas, que no ocurrirían espontáneamente PAPEL DEL ATP EN EL METABOLISMO El ATP participa en la activación de un metabolito para que pueda reaccionar en una vía metabólica, se hace con la fosforilación de dicha molécula. En el paso de la glucosa a glucosa-6fosfato para iniciar la glucólisis. SÍNTESIS DE ATP ADP + Pi ATP Fosforilación del ADP Acumula energía formando enlaces de alta energía. Acoplado a reacciones exergónicas (fosforilación oxidativa) Proceso no espontáneo Glucólisis SÍNTESIS DE ATP Directa: fosforilación a nivel de sustrato: cuando un sustrato (X~p) dona su p al ADP para hacer ATP Un sustrato rompe algún enlace rico en energía, ésta se libera y se aprovecha para fosforilar el ADP. SÍNTESIS DE ATP Indirecta: fosforilación oxidativa: Acoplada al transporte electrónico en la membrana interna de la mitocondria. REACCIONES DE ÓXIDO-REDUCCIÓN En las reacciones químicas la energía se “conduce” a través de los enlaces químicos, por medio de los electrones, pasando por distintos niveles de energía. Reacciones de oxidación-reducción (REDOX). OXIDACIÓN: pérdida de un electrón (o un átomo de H). El átomo o molécula que pierde el electrón se ha oxidado. REDUCCIÓN: ganancia de electrones (o un átomo de H). El átomo o molécula que pierde el electrón se ha reducido. La oxidación y la reducción siempre ocurren simultáneamente, porque el electrón que pierde un átomo es aceptado por otro. Cuanto mayor sea el contenido en H de un compuesto (cuánto más reducido esté) mayor es su contenido energético y más energía se puede sacar de él. Cuanto más oxidada esté una sustancia menos energía contiene. Los ácidos grasos (CH3-(CH2)14-COOH suministran mucho más energía que la glucosa (C6H12O6) y ésta mucho más que el CO2 (sin hidrógenos, es la forma más oxidada del carbono). Nicotinamida adenina dinucleótido (NAD+), Nicotinamida adenina dinucleótido fosfato (NADP+) Flavina adenina dinucleótido (FAD). Son nucleótidos que actúan como coenzimas de enzimas deshidrogenasas u oxidasas y participan en el metabolismo como moléculas transportadoras de electrones en reacciones de oxido-reducción. Forma oxidada: Forma reducida: NAD+ NADH + H+ NADPH + H+ FADH2 NADP+ FAD EJEMPLO DE REACCIÓN DE OXIDACIÓN Succinato es convertido a fumarato por la pérdidad de dos electrones y dos protones. Reacción de oxidación, ocurre en la mitocondria, en el ciclo del ácido cítrico, acoplada a la reducción de FAD a FADH2 Electrones viajan acompañados de un H+: transferencias de H Glucosa 2ATP 4 ATP GLUCOLISIS 2 H2O 2 NADH OXIDACIÓN DEL PIRUVATO 2 NADH 2 CO2 4 ATP 10 NADH 2 FADH2 2 FADH2 2 H2O CICLO DE KREBS (Ciclo del citrato) 6 NADH 4 CO2 2 ATP ¿Para qué sirve la generación de NADH en el metabolismo de la glucosa? Membrana Interna TERMODINÁMICA ESTUDIO DE LA ENERGÍA Primera Ley La energía puede convertirse de una forma en otra, pero no se puede crear ni destruir. Al variar la energía interna en un sistema cerrado, se produce calor y un trabajo. “La energía no se pierde, sino que se transforma”. Segunda Ley TERMODINÁMICA ESTUDIO DE LA ENERGÍA La Segunda Ley de la Termodinámica energía potencial del estado inicial > ENTROPÍA (S) magnitud física energía que no puede utilizarse para producir un trabajo. energía potencial del estado final energía cinética grado de desorden de un sistema TRABAJO En la naturaleza, el desorden es un estado más probable que el orden Entropía (S) tiende a crecer constantemente. ENLACE QUÍMICO ENERGÍA POTENCIAL REACCIÓN QUÍMICA CALOR Capacidad del sistema para realizar trabajo útil. Energía libre TRABAJO Energía disponible para el trabajo se denomina ENERGÍA LIBRE O ENTALPÍA (G) No toda la energía almacenada en un sistema (H) está disponible para el trabajo. Energía total del sist. El desorden del sistema, se resta a la energía total. Entropía G = H - TS Temperatura, en grados Kelvin ENERGÍA LIBRE (G) ¿Puede un proceso puede ocurrir espontáneamente? El sistema debe ceder energía Perder orden, ganar desorden PROCESO ESPONTÁNEO G = H - T S Valor negativo Cuando los cambios en H o en S son grandes, G tiene un valor negativo ENERGÍA LIBRE (G) La energía desprendida en una reacción se utiliza en otra. (1) Glucosa + Pi → glucosa 6-fosfato + H2O ΔG´º = 3 Kcal / mol (2) ATP + H2O → ADP + Pi ΔG´º = - 7,3 Kcal / mol ATP + glucosa → ADP + glucosa 6-fosfato ΔG = - 4,3 Kcal / mol ENERGÍA LIBRE (G) G negativo G positivo - Reacción exergónica - Reacción endergónica - Liberación neta de energía libre. - Los reactantes pierden G - Espontáneas - Toman energía de su entorno - Almacenan más G en las moléculas - No son espontáneas Si un proceso químico es exergónico en una dirección, entonces el proceso inverso debe ser endergónico. ACOPLAMIENTO ENERGÉTICO Las enzimas acoplan la combustión espontánea de los alimentos a reacciones que producen ATP El ATP transfiere la energía liberada por la ruptura de las uniones químicas en los procesos exergónicos hacia las reacciones endergónicas. Modelo mecánico que ilustra el principio de acoplamiento de reacciones A) Oxidación directa de glucosa a CO2 y H2O, que produce sólo calor B) En la misma reacción está acoplada a una segunda reacción como producción de ATP (balde de agua), C) El ATP producido puede servir para otro proceso celular. Los procesos metabólicos se organizan en: Vías Metabólicas Transformación de un sustrato inicial en un producto final a través de reacciones intermediarias. Cada una de las reacciones está catalizada por una enzima diferente http://highered.mcgraw-hill.com/sites/0072437316/student_view0/chapter8/animations.html# ENZIMAS Todas las reacciones que se efectúan en los seres vivos son catalizadas por enzimas. Perfil de una reacción exergónica - Acelera el transcurso de una reacción química, sin intervenir en ella ni como reactivo ni como producto. - No provoca la reacción sólo afecta la velocidad con que ocurre la misma. - Los catalizadores disminuyen la energía de activación Con enzima CLASIFICACIÓN DE LAS ENZIMAS (FAD+) FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 1.- Suministro de Nutrientes (sustratos) La velocidad de la reacción Vía muy activa FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 1.- Suministro de Nutrientes (sustratos) Vmax es constante, independiente de la cantidad de sustrato (zona de saturación). La velocidad aumenta en forma no lineal (zona mixta). La velocidad aumenta en forma lineal (zona proporcional). Esto ocurre debido a que los sitios activos de las enzimas se encuentran todos interactuando con las moléculas de sustrato, por lo tanto hasta que no finalice la reacción la enzima no puede unirse a otro sustrato. ¿Qué ocurriría con la Vmax si se aumenta la concentración de enzima? FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 2.- Regulación de la actividad enzimática 2.1. Temperatura Óptima CALOR Desnaturalización Energía cinética de las moléculas Velocidad de las reacciones FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 2.- Regulación de la actividad enzimática 2.2. Inhibición por producto final Cuando el producto final Z se acumula, inhibe alguno de los primeros pasos de la ruta. Retroalimentación negativa (feedback negativo) en una ruta metabólica. FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 2.- Regulación de la actividad enzimática 2.3. Alostérica capaz de reconocer efectores MODULAR LA ACTIVIDAD DE LAS ENZIMAS Efectores positivos – Actividad enzimática controlada por el enlace de pequeñas moléculas a la enzima en un sitio diferente al sitio activo (Activador o Inhibidor) – No alteran químicamente a la enzima que regulan – Pueden modificar el km o la Vmax de la reacción Efectores negativos FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 2.- Regulación de la actividad enzimática 2.3. Alostérica Inhibidor Activador FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 2.- Regulación de la actividad enzimática 2.4. Modificación covalente – Esta modificación puede ser reversible o irreversible – Es siempre mediada por otra enzima – Puede resultar en un incremento o disminución de la actividad de la enzima – Pueden modificar el km o la Vmax de la reacción ATP Enzima (Inactiva) ADP Kinasa Enzima (Activa) P FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 2.- Regulación de la actividad enzimática 2.4. Modificación covalente – Esta modificación puede ser reversible o irreversible – Es siempre mediada por otra enzima – Puede resultar en un incremento o disminución de la actividad de la enzima – Pueden modificar el km o la Vmax de la reacción Enzima Enzima (Inactiva) (Activa) Fosfatasa ATP ADP P FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 2.- Regulación de la actividad enzimática 2.4. Modificación covalente FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 3.- Regulación de la cantidad enzimática -La actividad enzimática está regulada por la concentración de enzima en la célula - Las enzimas pueden ser constitutivas o inducibles (su concentración incrementa dependiendo de las necesidades metabólicas) Involucra el control a nivel del ADN. El ADN es la molécula que almacena la información para la síntesis de proteínas de acuerdo al siguiente flujo de información: FACTORES QUE MODIFICAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS ¿Cómo se regula una vía metabólica? 4.- Carga energética El contenido de la célula de compuestos adenilados como AMP, ADP son constantes. La cantidad de energía presente en la célula está en relación con ATP y ADP. El ATP es el doble de ADP. La carga energética tiene efecto sobre algunas enzimas y éste proviene de la función enzimática en el uso o generación del ATP. A fin de proteger su priv acidad, PowerPoint bloqueó la descarga automática de esta imagen. GLUCÓLISIS •Etapa esencialmente irreversible •Estimulada por ADP y AMP. •Inhibida por ATP •Controla el flujo de carbono a través de la glucólisis •Etapa esencialmente irreversible •Estimulada por ADP y AMP •Es inhibida por acetil CoA, NADH y ATP •Controla la rapidez con la que funciona el ciclo de Krebs Acetil CoA RESUMEN Regulación de las vías metabólicas 1.- Suministro de nutrientes (sustratos) 2.- Regulación de la actividad enzimática (rápido) 2.1. Temperatura 2.2. Inhibición por producto final 2.3. Alostérica 2.4. Modificación covalente (fosforilación y desfosforilación) 3.- Regulación de la cantidad enzimática (lento) 4.- Carga energética