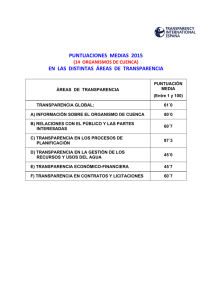
1 - Universidad de Cuenca
Anuncio

UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA RESUMEN En los últimos años, procesos como la globalización, avances tecnológicos, llegada de multinacionales, y la migración, han conllevado a que la población adopte un estilo de vida semejante al de las grandes ciudades. Cada vez se dispone de menos tiempo para actividades fuera del trabajo, la población se vuelve más “cómoda”, sedentaria, e ingiere “comidas rápidas”, sin considerar su efecto dañino para el organismo. Este estudio pretende verificar, que el incremento en el peso corporal, modifica no solo el aspecto físico, sino también la homeostasis del organismo, alterando la secreción de insulina y trayendo consigo graves consecuencias para la salud. Palabras clave: Endocrinología Glicemia Insulina Sobrepeso PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 1 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA ÍNDICE Página número INTRODUCCIÓN……………………………………………………………………12 CAPITULO I Generalidades de Endocrinología……..………….…...………………………………………………...14 Endocrinología Y Metabolismo……………………………………………………..17 Sistema endocrino………..………………………………………………………….18 Coordinación de las funciones corporales por los mensajeros químicos……………………………………………………………………..……….20 Hormonas……………………………………………………………………………..23 Principales glándulas endocrinas y sus hormonas……………………….27 Clasificación de las hormonas………..…………………………………….29 Almacenamiento y secreción de las hormonas…………..……………….32 Control de la secreción hormonal…………………………………………..34 Hormonas y proteínas ligadoras……………………………………………38 Receptores hormonales y su activación………….………………………..40 Regulación del número de receptores…………………..…………………44 Mecanismos de acción hormonal………...………………………………...45 Apoptosis hormonal…… ………………...………………………………….59 Trastornos de la función endocrina……….…………………….………………….61 Determinación de concentraciones hormonales en sangre……………………..63 CAPITULO II Carbohidratos………………………………….……………………………………..64 Estructura química…………………………………………………………………...66 Función de los hidratos de carbono…..……………………………………………67 Metabolismo de carbohidratos………..…………………………………………….68 Glucosa………………………………………………………………………………..71 Metabolismo de la glucosa……..……………………………….…………………..72 Glucólisis……………….….…………………………………………….……………78 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 2 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Regulación de la glucólisis…………………………………….………………………………………..82 Gluconeogénesis…………………………………………………………………….83 Balance energético de la gluconeogénesis……………………………………….85 Regulación de la gluconeogénesis…………………………………………………85 Interrelaciones de los órganos en la gluconeogénesis………….…………….....86 Ruta de las pentosas fosfato……………………….……………………………….89 Uso del hidrógeno para sintetizar grasas, función del dinucleótido de nicotinamida y adenina fosfato……………….…………………………………91 Glucogénesis…………………………………………………………………………92 Glucogenólisis………………….……………….……………………………………94 Ciclo de KREBS……..……………………………………………………………….95 Alteraciones del metabolismo de la glucosa…………………………….………..98 Diabetes…………………………………………………………………….............100 Hipoglicemia………….……………………………………………………………..108 CAPITULO III El páncreas…………………...………………...…………………………………..117 Insulina…………………………………………..…………………………………..122 Química y síntesis de la insulina…..……….……………………………..124 Mecanismo de acción……………………….……………………………...130 La insulina y sus efectos metabólicos……………….……………………137 Efecto de la insulina sobre el metabolismo de los hidratos de carbono en otras células……………………………………………….152 Efecto de la insulina sobre el metabolismo de las proteínas y sobre el crecimiento……………………………………………………..162 Regulación de la secreción de insulina…………………………..….…...168 Factores estimuladores de la biosíntesis y secreción de la insulina………………………………………………………………..169 Otros factores que estimulan la secreción de insulina…………………174 Alteraciones del metabolismo de la insulina…………………………………….179 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 3 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Hipoinsulinismo………….………………………………………………….182 Hiperinsulinismo (hipoglucemia)…………………………………………..189 CAPITULO IV Balance energético y nutricional……..……………………….…………………..191 Metabolismo energético………..………………………………………………..…191 Valor calórico de los alimentos……………………………………………………193 Valores de los nutrientes…………………………………………………………..195 Necesidades diarias de proteínas……………………….………………..195 Medición de la energía producida por el cuerpo (gasto calórico)……….…….197 Metabolismo total….………………………………………………………..197 Metabolismo basal……………………...…………………………………..198 Efecto térmico de la comida……………………………………………….203 Actividad física………………...…………………………………………….203 Balance calórico……………….…………………………………………………....204 Tipos de balance calórico (o energético)………………..……………………….204 Métodos clínicos y experimentales para determinar la utilización metabólica de las proteínas, los hidratos de carbono y grasas……………….206 Regulación de la ingesta alimenticia……………………………………………..210 Centros neuronales de regulación de la ingesta alimenticia…..………212 Factores que regulan la cantidad de alimento ingerido…..…………….212 Control de peso……………………………………………………………………..218 Componentes estructurales principales del ser humano…………..…………..219 Sobrepeso………………………………………………………...…………………226 La dinámica del equilibrio energético…………………..…………………226 Obesidad………………………………….…………………………………………229 Causas de la obesidad………..……….…………………………………..230 Susceptibilidad a desarrollar obesidad……..…………………………….232 Clasificación de la obesidad……………….………………………………233 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 4 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Los peligros de la obesidad………………..…………………………..236 Falta de peso…………………..……………………………………………………246 CAPITULO V ANÁLISIS PRÁCTICO Muestreo……………………………………………………………………………..247 Métodos………………………….…………………………………………………..249 Técnicas: Determinación cuantitativa de Insulina…….…………..…………………253 Determinación cuantitativa de glucosa…….….……….……………………...256 Formas de Control……………………..…………………………………………..257 Datos obtenidos en la práctica ……………………………….…………………..259 Análisis estadístico descriptivo…………………….……………………….……..261 Interpretación de resultados…………...…………………………………..262 Análisis gráfico de los resultados Interpretación de resultados……………………………………………….267 Análisis estadístico Interpretación de resultados…………………...…………………………..274 CAPITULO VI Conclusiones………………………………………………………………………..297 Recomendaciones………………………………………………………………….301 Bibliografía……………………………………….………………………………….303 Anexos……………………………………………………………………………….311 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 5 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUÍMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA ESTUDIO COMPARATIVO DE NIVELES DE INSULINA Y GLUCOSA EN PERSONAS CON SOBREPESO Y PERSONAS CON PESO NORMAL EN LA CIUDAD DE CUENCA TESIS DE GRADO PREVIO A LA OBTENCIÓN DEL TÍTULO DE BIOQUÍMICO FARMACEUTICO DIRECTOR DE TESIS: Dra. Graciela Chérrez Verdugo AUTORES: Lorena Bravo Medina Patricia Delgado Torres Cuenca – Ecuador 2006 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 6 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Agradecemos en primer lugar a Dios por habernos permitido realizar todos nuestros sueños y lograr alcanzar las metas que hasta ahora nos hemos propuesto. A la Escuela de Bioquímica y Farmacia y a todas las personas que de una u otra manera han colaborado tanto en nuestra formación profesional como en la realización de la presente tesis. Particular y especialmente a la Dra. Graciela Chérrez Verdugo, Directora de Tesis; a las Dras. Lurdes Jerves, Luz María Samaniego, y al Dr. Fausto Zaruma, quienes con sus conocimientos y dedicación contribuyeron a que el presente trabajo llegue a una feliz realización. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 7 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA DEDICATORIA A mis queridos padres Jorge y Diocelina a mis hermanos María, Jorge, Rubén, David, y Pablo, por creer en mi, y apoyarme y hacer posible que mis estudios culminaran con éxito. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 8 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA DEDICATORIA El presente trabajo va dedicado a mis padres, Patricio y Malena; y a mis hermanos Vero y Paúl por su apoyo y comprensión durante toda mi carrera y por ayudarme a alcanzar mis metas. A mis abuelitos por siempre estar allí dándome animo, sobre todo a mi querido abuelito Jorge, porque se que desde donde estas siempre me has cuidado y apoyado en todo. A todas esas personitas especiales, Diego, Lore, Vane, Fernánda, y Verito, por estar siempre a mi lado compartiendo los momentos difíciles y alegres de mi vida y por ayudarme a seguir adelante cuando sentía que ya no tenía fuerzas. Patricia PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 9 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA INTRODUCCIÓN En los últimos años, el ritmo de desarrollo de la Ciudad de Cuenca se ha incrementado considerablemente. Procesos tales como la globalización, avances tecnológicos, la llegada de multinacionales, y sobre todo el fenómeno migratorio, ha conllevado a que la población en general adopte un estilo de vida semejante al presentado en las grandes ciudades. Dicho cambio se refleja sobre todo en la actividad física y en las costumbres alimenticias adoptadas en la actualidad. Cada vez es menor el tiempo del que se dispone para desarrollar actividades fuera del trabajo, lo que hace que la población tienda a volverse más “cómoda”, es decir, emplea más medios de transporte, tornándose sedentarios y prefieren ingerir las denominas “comidas rápidas” , sin PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 10 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA considerar el efecto dañino que pueda desarrollar en su organismo. La adopción de dichos hábitos se ve reflejada en el incremento cada vez mayor de personas que presentan sobrepeso, e incluso en algunos de los casos obesidad, sin tomar en cuenta la edad o el sexo de las personas que lo padecen. Se sabe que el problema del sobrepeso esta directamente relacionado con incremento de la tendencia a desarrollar enfermedades crónicas y ha disminuir el tiempo de vida de dichas personas. Es importante comprobar, que un incremento en el peso corporal, va ha modificar no solo su aspecto físico, sino también la homeostasis de su organismo. De tal manera que este estudio se enfoca hacia verificar si el sobrepeso influye o no en la secreción de insulina por las células B PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 11 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA pancreáticas, y como se presentan los niveles de glicemia en dichos casos. CAPITULO I Generalidades de Endocrinología Las funciones del organismo están reguladas por dos sistemas de control principales: el sistema nervioso y el sistema hormonal o endocrino. El sistema endocrino, junto con el nervioso, constituyen dos de los más importantes sistemas que permiten mantener la homeostasis ó medio interno del organismo, participan de manera coordinada en todas las funciones generales de regulación del cuerpo humano, como mantener la temperatura, la presión sanguínea, la cantidad de glucosa en sangre, etc. (3) Para poder comprender los cambios o las alteraciones que se presenten en nuestro organismo, es fundamental conocer la composición y el funcionamiento de dichos sistemas, en este caso nos enfocaremos específicamente PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 12 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA al sistema endocrino, el cual esta relacionado directamente con nuestro estudio. La endocrinología es la especialidad médica que se encarga del estudio de la síntesis, secreción, función hormonal, y de los mecanismos de regulación de estas, además de los efectos normales de sus secreciones, y los trastornos derivados del mal funcionamiento de las mismas. Etimológicamente endocrino proviene de dos vocablos griegos, Endon: dentro y Krinein: secretar o separar; es decir, secretar al interior. (72) La endocrinología puede ser dividida en dos grandes áreas de estudio: A. Endocrinología y Metabolismo: El sistema endocrino regula el metabolismo hidroelectrolítico, del calcio y fósforo (sistema óseo), de los carbohidratos, de los lípidos y de las proteínas. B. La regulación del anabolismo y catabolismo de estos compuestos, está orientada a regular la energía necesaria PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 13 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA para las actividades celulares, el crecimiento y el desarrollo. En situaciones negativas como por ejemplo desnutrición, el organismo deja de crecer y desarrollarse para mantener las actividades celulares. Como ejemplos de hormonas que participan en el metabolismo tenemos: HORMONAS REGULAN… Antidiurética, atrial natriurética, aldosterona, angiotensina, y la prolactina el equilibrio hidrosalino Paratohormona, tirocalcitonina, vitamina D, estradiol, dehidroepiandrosterona glucocorticoides, insulina, hormona del crecimiento, hormonas tiroideas, somatostatina, y el glucagón el sistema esquelético, y el metabolismo del calcio y fósforo del organismo hormona del crecimiento, leptina, estrógenos, hormonas tiroideas, insulina el metabolismo de los lípidos andrógenos, insulina, glucocorticoides, hormonas tiroideas, hormona del crecimiento PATRICIA DELGADO TORRES LORENA BRAVO MEDINA el metabolismo de los carbohidratos el metabolismo de las proteínas 14 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA C. Endocrinología y Reproducción: El sistema endocrino participa de manera fundamental en la regulación de los procesos que permiten el crecimiento y desarrollo de los gametos masculino y femenino. Esto basado a la integración del sistema de regulación: Sistema Nervioso Central - Hipotálamo - Hipófiso - Gonadal. Una alteración en cualquiera de estos niveles de regulación alterará la reproducción y conducirá a la infertilidad. Existen hormonas que tienen tanto función metabólica como reproductiva. Entre ellas tenemos a la testosterona, el estradiol y la leptina. D. Otras funciones del sistema endocrino son aquellas referidas a los procesos de diferenciación celular, y en el control del sistema inmunológico. En el primer caso tenemos como ejemplo el rol de las hormonas tiroideas en el proceso de la mielinización de las fibras nerviosas; así, su deficiencia congénita resulta en cretinismo, una patología donde se observa retardo mental. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 15 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Igualmente los andrógenos gonadales son importantes para la diferenciación de los genitales externos, los conductos reproductivos internos, y del cerebro masculino. En el segundo caso existe un sistema de regulación a través de los glucocorticoides que modulan la respuesta inmune; en éste sistema también participa el sistema nervioso, por lo que podemos calificarlo como sistema neuro-inmuno-endocrino. (8;72) SISTEMA ENDOCRINO El cuerpo realiza funciones muy específicas que deben ser controladas como reguladas," el sistema endocrino es el sistema que logra que estos cambios se puedan dar a simple vista cuando son muy externos, aunque normalmente suelen ser internos". (44) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 16 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA El sistema endocrino consiste en varias glándulas que segregan sustancias químicas llamadas hormonas en el flujo sanguíneo. Los órganos endocrinos también se denominan glándulas sin conducto o glándulas endocrinas, debido a que sus secreciones se liberan directamente en el torrente sanguíneo, mientras que las glándulas exocrinas liberan sus secreciones sobre la superficie interna o externa de los tejidos cutáneos, la mucosa del estómago o el revestimiento de los conductos pancreáticos. Este sistema está relacionado con el control de las diferentes funciones metabólicas del organismo tales como la velocidad de las reacciones químicas en las células y el transporte de sustancias a través de las membranas celulares; además se encuentra involucrado en otros aspectos del metabolismo celular, tales como el crecimiento y la secreción. (72) Los tejidos que producen hormonas se pueden clasificar en tres grupos: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 17 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Glándulas endocrinas: producción exclusiva de hormonas. Ejm: tiroides Glándulas endo-exocrinas: producen también otro tipo de secreciones además de hormonas. Ejm: el páncreas Tejidos no glandulares: produce sustancias parecidas a las hormonas. Ejm: tejido nervioso del sistema nervioso autónomo. Algunos de los efectos hormonales ocurren en segundos, mientras que otros requieren de varios días para comenzar, y posteriormente continúan durante semanas o incluso meses. (3;8) COORDINACIÓN DE LAS FUNCIONES CORPORALES POR LOS MENSAJEROS QUÍMICOS PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 18 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Las células interactúan unas con otras y modifican su actividad metabólica por acción de sustancias químicas denominadas transmisores. Existen diferentes tipos de transmisión química: Transmisión Neurocrina: ocurre en el sistema nervioso a través de la liberación de sustancias químicas denominadas neurotransmisores al espacio intersináptico, luego se une a un receptor post-sináptico modificando la actividad metabólica de la célula post-sináptica. Transmisión Endocrina: ocurre en el sistema endocrino a través de la liberación de sustancias químicas denominadas hormonas, que actúan a distancia sobre una célula efectora. Transmisión Neuroendocrina: ocurre por la liberación de sustancias químicas (neurohormonas) en los terminales nerviosos hacia la circulación, y actúan a PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 19 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA distancia sobre una célula efectora. Como ejemplo tenemos la secreción de las neurohormonas (hormonas liberadoras e inhibidoras) del hipotálamo a la eminencia media y que a través de la vía sanguínea porta-hipofisiaria se van a trasladar a la hipófisis anterior donde van a actuar. Transmisión paracrina: ocurre entre dos células adyacentes, donde una de las células secreta la sustancia (parahormona), que actúa por difusión en la célula vecina modificando su función. No hay participación de la vía sanguínea. Transmisión autocrina: Es cuando una sustancia química actúa sobre la misma célula que la produce para regular su secreción. (72) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 20 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA HORMONAS La comunicación entre las distintas células y glándulas del sistema endocrino se lleva a cabo mediante un tipo especial de biomoléculas, unos mensajeros químicos que se denominan hormonas. En 1902, Bayliss y Starling definieron por primera vez el concepto de hormona, al descubrir la secretina, liberada a la circulación por la mucosa duodenal, y que estimula el flujo pancreático. Estos autores definieron a la hormona como cualquier sustancia producida normalmente en las células de una región del organismo y llevada por el torrente sanguíneo a otras partes, sobre las cuales actúa con efecto favorable para el organismo en conjunto. (58; 69) Actualmente se definen a las hormonas como compuestos químicos secretados en mínimas concentraciones al torrente sanguíneo por células o grupos de células PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 21 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA específicas, y que actúan en células distantes al lugar de origen, donde se unen a receptores específicos produciendo una respuesta biológica. Existen sustancias que simulan el efecto de una hormona pero no son hormonas; éstas son la glucosa, los ácidos grasos no esterificados, y las prostaglandinas. La glucosa actúa sobre el páncreas y libera insulina, pero no es hormona porque actúa en altas concentraciones (miligramos), en tanto que las hormonas actúan a mínimas concentraciones: pico gramos (10-12 g) y nanogramos (10-9 g). Muchas de las hormonas secretadas por las células endocrinas son inactivas (precursoras) y requieren transformarse en otra molécula para tener actividad biológica. Por ejemplo, la tiroxina (T4) secretada por la glándula tiroides requiere perder un iodo y transformarse en tri-iodotironina (T3) para ser biológicamente activa. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 22 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Algunas hormonas son locales, mientras que otras son generales; las primeras poseen efectos locales específicos, por ello su nombre, como por ejemplo la acetilcolina liberada en las terminaciones nerviosas parasimpáticas y esqueléticas. (58) Las hormonas generales son secretadas en su mayoría por glándulas endocrinas específicas; como ejemplo de estas encontramos a la adrenalina y la noradrenalina, secretadas por la médula suprarrenal en respuesta a la estimulación simpática. Algunas hormonas generales afectan a casi todas las células del organismo, tal como la hormona del crecimiento de la hipófisis anterior, y la hormona tiroidea del tiroides. Otras hormonas solo afectan a tejidos específicos “tejidos diana”, porque solo ellos poseen receptores celulares diana específicos a los que se unirán las hormonas para iniciar sus acciones. (69;72) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 23 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Principales Glándulas Endocrinas Figura 1.1 (www.ADAM.org.com) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 24 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA PRINCIPALES GLÁNDULAS ENDOCRINAS Y SUS HORMONAS Glándula Hipófisis anterior (base del cerebro) Hormona Función Hormona del crecimiento Induce el crecimiento de casi todas las célula y tejidos del organismo Adrenocorticotropina Hace que la corteza suprarrenal secrete hormonas corticosuprarrenales Tirotropina Hace que la glándula tiroides secrete tiroxina y triyodotironina Hormona folículo estimulante Induce el crecimiento de folículos ováricos antes de la ovulación, promueve la formación de esperma en los testículos Hormona luteinizante Prolactina Promueve el desarrollo de las mamas y la secreción de leche Hormona antidiurética (vasopresina) Hace que los riñones retengan agua; en concentraciones elevadas producen vaso constricción y eleva la tensión arterial Hipófisis posterior (base del cerebro) Glándulas suprarrenales (sobre los riñones) Papel importante en la producción de la ovulación, produce la secreción de hormonas sexuales en ovarios y testículos Oxitocina Contrae el útero durante el parto, además contrae las células mioepiteliales de las mamas ayudando a expulsar la leche Cortisol Posee múltiples funciones en el control del metabolismo de proteínas, carbohidratos y grasas Aldosterona Tiroxina y Triyodotironina Glándula tiroides PATRICIA DELGADO TORRES LORENA BRAVO MEDINA Reduce la excreción de sodio en los riñones y aumenta la excreción de potasio Aumenta la velocidad de las reacciones químicas en casi todas las células, aumentando así el nivel del metabolismo 25 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA (cuello) Calcitonina Favorece el depósito de calcio en los huesos y reduce la concentración del mismo en el líquido extracelular Insulina Favorece la entrada de glucosa en las células del organismo controlando así la velocidad del metabolismo de los hidratos de carbono Glucagón Aumenta la síntesis y liberación de glucosa procedente del hígado hacia los líquidos corporales Estrógenos Estimulan el desarrollo de los órganos sexuales femeninos, de las mamas y de caracteres sexuales secundarios Islotes de Langerhans (Páncreas) Ovarios Progesterona Testículos Testosterona Glándula paratiroides (cuello) Parathormona Estimula la secreción de “leche uterina” por las glándulas endometriales uterinas. Ayuda a promover el desarrollo del aparato secretor de las mamas Estimula el crecimiento de los órganos sexuales masculinos y de caracteres sexuales secundarios Controla la concentración de Ca en el líquido extracelular mediante: a) absorción de Ca en el intestino, b) excreción de Ca por los riñones, c) liberación Ca de los huesos. Gonadotropina coriónica humana Favorece el crecimiento del cuerpo lúteo y la secreción de estrógenos y progesterona por este. Estrógenos Favorece el crecimiento de órganos sexuales de la madre y de algunos tejidos del feto. Placenta Progesterona Somatomamotropina humana PATRICIA DELGADO TORRES LORENA BRAVO MEDINA Promueve el desarrollo del endometrio antes de la implantación del huevo fecundado, favorece el desarrollo de algunos tejidos y órganos fetales, promueve el desarrollo del aparato secretor mamario de la madre. Probablemente favorezca el crecimiento de algunos tejidos fetales, ayuda al desarrollo mamario de la madre. 26 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA CLASIFICACION DE LAS HORMONAS: Desde el punto de vista químico, las hormonas son de tres tipos: 1. Hormonas esteroideas: poseen una estructura química basada en el núcleo esteroideo, similar al colesterol, en la mayoría de los casos derivan del propio colesterol. Las hormonas esteroidales son lipofílicas y se producen en glándulas cuyo origen embriológico es mesodérmico, tales como la corteza adrenal, el ovario y el testículo. El núcleo fundamental de estas hormonas es el ciclopentano-perhidrofenantreno. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 27 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Figura 1.2: (http://www.uv.es/garoa2/estresyadiccion/psicoendocrinolog ia.htm) Las hormonas esteroidales según el número de átomos de carbono pueden dividirse en pregnanos (21 carbonos), androstanos (19 carbonos) y estranos (18 carbonos). Los ejemplos típicos de estos grupos son la progesterona, la testosterona y el estradiol, respectivamente. 2. Derivadas del aminoácido tirosina: existen dos grupos, el primero representado por las dos hormonas tiroideas metabólicas (tiroxina y triyodotironina), son PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 28 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA formas yodadas de derivados de la tirosina. El segundo representado por las dos hormonas principales de la médula suprarrenal (adrenalina y noradrenalina), que son catecolaminas, también derivadas de la tirosina. Tirosina Figura 1.3: (Laguna José, Piña Enrique, Bioquímica de Laguna) 3. Proteínas o péptidos: todas las restantes hormonas endocrinas importantes son proteínas, péptidos o derivados inmediatos de estos. Las hormonas de la hipófisis anterior son proteínas o grandes polipéptidos, las hormonas de la hipófisis posterior, hormona antidiurética y oxitocina, son péptidos, cada uno con tan sólo nueve aminoácidos. La insulina, el glucagón y la parathormona son grandes polipéptidos. (43;72) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 29 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA ALMACENAMIENTO Y SECRECIÓN DE LAS HORMONAS: Las glándulas endocrinas no emplean una forma única de almacenamiento y secreción de sus hormonas, sin embargo la mayoría sigue ciertos patrones generales. Todas las hormonas proteicas están formadas por el retículo endoplasmático granuloso de las células glandulares, de la misma manera que se forman otras proteínas secretoras. No obstante la proteína inicial formada por el retículo endoplasmico casi nunca es la propia hormona final, sino que es mayor que la hormona activa y se denomina preprohormona. (3;58) Posteriormente esta gran proteína se desdobla, por lo general cuando aún se encuentra en el retículo endoplásmico, y forma una proteína más pequeña denominada prohormona; esta es transportada por las vesículas transportadoras del retículo endoplásmico hasta PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 30 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA el aparato de Golgi, donde se va ha dar lugar a la separación de otra porción de la proteína. El aparato de Golgi suele condensar las moléculas de hormona en pequeñas vesículas encapsuladas por una membrana, denominadas vesículas secretoras o gránulos secretores. Estas vesículas permanecen almacenadas en el compartimiento citoplásmico de la célula endocrina hasta que aparece una señal específica (señales nerviosas, hormonales, química, física) para producir la secreción. El comienzo de la secreción hormonal después de un estímulo, y la duración de la acción de las mismas, varía considerablemente entre las diferentes hormonas, así por ejemplo algunas hormonas como la adrenalina y la noradrenalina son secretadas en cuestión de segundos una vez estimulada la glándula, y puede desarrollar su acción completa en otros pocos segundos o minutos. Otras PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 31 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA hormonas como la tiroxina o la horma del crecimiento, pueden tardar meses en producir su efecto completo. La cantidad de hormonas necesarias para controlar la mayor parte de las funciones metabólicas y endocrinas son increíblemente pequeñas. Sus concentraciones en la sangre oscilan entre 1 picogramo (una billonésima de gramo) por cada mililitro de sangre hasta un máximo de algunos microgramos (unas millonésimas de gramo) por mililitro de sangre. (3;58;72) Del mismo modo, las tasas de secreción de las diversas hormonas son extremadamente pequeñas, por lo general en el orden de los microgramos o miligramos por día. CONTROL DE LA SECRECIÓN HORMONAL: La secreción hormonal es regulada por estímulos directos y por mecanismos de retroalimentación. Los sistemas PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 32 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA hormonales se integran en ejes donde hay un sistema de regulación superior, conformado por el sistema nervioso central (SNC), que a través de una regulación neurocrina actúa sobre el hipotálamo. El SNC, el hipotálamo y la hipófisis son comunes para todos los ejes de regulación hormonal; a partir de la hipófisis se diversifican las funciones. Así tenemos, el eje SNC-hipotálamo-hipófiso-gonadal; eje SNC-hipotálamo-hipófiso-tiroideo; hipófiso-córtico adrenal; eje eje SNC-hipotálamo- SNC-hipotálamo-hipófiso- pancreático entre otros. Los principales mecanismos de control de la secreción hormonal son: Regulación directa: ocurre de un nivel superior a otra de nivel inferior. Por ejemplo, la hipófisis que secreta la hormona luteinizante (LH) estimula la secreción de la testosterona por las células de Leydig en el testículo. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 33 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Retroalimentación: es la regulación a partir de una glándula del nivel inferior hacia la glándula que la estimula y que está en un nivel superior. Este sistema permite mantener el equilibrio en la secreción hormonal para evitar que una glándula de nivel inferior se mantenga sobreestimulada por una glándula de nivel superior. Por ejemplo, la hipófisis (nivel superior) secreta hormona del crecimiento (GH), y ésta actúa sobre el hígado produciendo, el factor de crecimiento similar a insulina-I ó IGF-I (nivel inferior), crecimiento de los que a su vez actúa sobre el huesos. Si no ocurriera retroalimentación, la GH seguiría actuando y se produciría crecimiento desmesurado del hueso (gigantismo). La IGF-I por retroalimentación inhibe la secreción de GH. (3;58) Se pueden distinguir dos mecanismos de retroalimentación, estos son: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 34 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA a) Retroalimentación negativa: se genera cuando el producto final inhibe la secreción de la glándula. Por ejemplo, la hormona luteinizante (LH) estimula en las células de Leydig del testículo la producción de testosterona, la cual al circular por la sangre llega a la hipófisis donde va a inhibir la secreción de LH. b) Retroalimentación positiva: se genera cuando la secreción de una célula efectora incrementa la secreción de la hormona que la estimula; éste mecanismo de regulación es el que ocurre menos frecuentemente en el organismo. Un ejemplo es la liberación cíclica de gonadotropinas en la fase pre-ovulatoria de la mujer. Evoluciones realizadas a los mecanismos de retroalimentación demuestra que el factor importante que se debe controlar no suele ser la tasa de secreción de la propia hormona, sino el grado de actividad del órgano diana. Tan solo cuando la actividad del órgano diana se PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 35 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA eleva hasta un nivel apropiado, la retroalimentación hacia la glándula adquiere el poder suficiente para frenar la secreción posterior de la hormona. (43;72) Si el órgano diana responde escasamente a la hormona, la glándula endocrina secreta cada vez más hormona, hasta que el órgano diana alcanza el nivel de actividad apropiado, pero a expensas de una secreción excesiva de la hormona de control. HORMONAS Y PROTEINAS LIGADORAS: Las hormonas esteroidales y las tiroideas circulan en la sangre tanto ligada a una proteína como en forma libre, siendo ésta última la biológicamente activa. Generalmente las determinaciones hormonales se refieren a la concentración total (hormona libre + hormona ligada a la proteína), y no siempre una alteración en los niveles de la hormona total refleja una alteración de la fracción libre, PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 36 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA puesto que existen muchas situaciones en que se afecta el contenido de la proteína ligadora sin que necesariamente ocurra una disfunción hormonal. (43;58;72) Existen hormonas proteicas como la hormona de crecimiento que se unen a proteínas ligadoras circulantes en sangre como paso necesario para su acción hormonal. Se considera a esta proteína ligadora como el receptor extracelular, pues su ausencia resulta en falla de la acción de la hormona del crecimiento. Para su acción hormonal, la hormona de Crecimiento (GH) se une al receptor celular, y este complejo hormonareceptor extracelular (proteína ligadora) se une a un receptor de membrana, y a partir de allí se produce la cascada que determina finalmente la acción de la hormona, en este caso la hormona de crecimiento. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 37 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA RECEPTORES HORMONALES Y SU ACTIVACIÓN: Muchas células son expuestas a las hormonas, sin embargo, sólo algunas responden debido a la especificidad de la acción hormonal. Las hormonas endocrinas casi nunca actúan directamente sobre la maquinaria intracelular para controlar las reacciones químicas celulares finales, en su lugar, casi siempre se combinan primero con receptores hormonales situados en la superficie de las células o en el interior de las mismas. Después de la unión a los receptores, se inicia una cascada de reacciones en la célula, en la que cada fase es más poderosa que la anterior. Los receptores están compuestos principalmente por proteínas, pero tienen modificaciones secundarias de carbohidratos y pueden estar selectivamente inmersos en la membrana lipídica, también pueden estar fosforilados, o PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 38 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA formar oligómeros por puentes de disulfuro o interacciones covalentes. (3;72) El número y afinidad de los receptores pueden modificarse de acuerdo a las circunstancias. Casi todos los receptores hormonales son proteínas grandes, cada célula a estimular posee por lo general entre 2000 y 100000 receptores. Cada receptor suele ser muy específico para una única hormona, ello determina el tipo de hormona a actuar sobre un tejido en particular. La localización general de los receptores para los diferentes tipos de hormonas son: a) En o sobre la superficie de la membrana celular: Por lo general tienen receptores de membrana aquellas hormonas que por su tamaño no pueden entrar a la célula o aquellas que por su poca liposolubilidad tampoco lo pueden hacer, estos son generalmente PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 39 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA específicos peptídicas y para hormonas catecolamínicas proteicas, (adrenalina y noradrenalina). En algunos casos es necesario que la hormona se una previamente a una proteína ligadora que circula en sangre y sólo después de esta unión se puede activar el receptor de membrana b) En el citoplasma celular: casi todos los receptores para las diferentes hormonas esteroideas se encuentran en el citoplasma. c) En el núcleo celular: los receptores de las hormonas metabólicas tiroides se encuentran en el núcleo, se cree que por estar situados en asociación directa con uno o más cromosomas. (43;72) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 40 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Las hormonas amínicas, peptídicas y las proteicas se unen a receptores de membrana, y las hormonas esteroidales lo hacen a receptores intracelulares. Recientemente se ha demostrado que algunos sistemas celulares tienen receptores de membrana para los esteroides; por ejemplo el espermatozoide tiene receptores de membrana para progesterona. Los receptores de los andrógenos pertenecen a una superfamilia de receptores mecanismos genéticos nucleares complejos para que emplean controlar el desarrollo y las funciones de los tejidos “blanco”, activando o reprimiendo la transcripción de genes a través de su asociación a segmentos específicos del DNA y/o proteínas. Las hormonas que actúan a través de receptores de membrana activan la formación de un segundo mensajero, que lleva el mensaje de la hormona al interior de la célula para la elaboración de la respuesta biológica o acción hormonal. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 41 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA En la membrana plasmática existe también un tipo de receptores que son tirosinas kinasas. En este tipo de receptores se unen la insulina, el factor de crecimiento similar a insulina (IGF), y el factor de crecimiento epidermal (EGF), por ende, la hormona se constituye en el primer mensajero. (3;58;72) Regulación del número de receptores: El número de receptores en una célula diana no suele permanecer constante de un día para otro, ni siquiera de minuto a minuto, debido a que las propias proteínas del receptor a menudo resultan inactivadas o destruidas durante la realización de su función, y pueden ser reactivadas en otro momento o obtenerse nuevas mediante el mecanismo de fabricación de proteínas de la célula. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 42 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La unión de una hormona con los receptores de la célula diana produce una reducción del número de receptores activos, ya sea por inactivación de las moléculas receptoras o por una disminución en la producción de estas. Esto recibe el nombre de “regulación a la baja” de los receptores, disminuyendo la respuesta del tejido diana a la hormona. En ocasiones las hormonas estimulantes inducen la formación de más moléculas receptoras de lo normal, de tal manera que el tejido diana se hace cada vez más sensible a los efectos estimulantes de la hormona, generando así una “regulación al alza” de los receptores. (3;58) MECANISMOS DE ACCIÓN HORMONAL La respuesta de un organismo a la administración de una hormona puede ser considerada bajo tres modalidades: función, mecanismo de acción, y el efecto biológico. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 43 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La función se refiere al propósito o utilidad de la hormona respecto a la regulación metabólica o a los cambios metabólicos que produce. El mecanismo de acción se refiere a como una hormona interactúa con un receptor específico y todos los eventos intracelulares subsiguientes que conllevarán al efecto biológico, el cual es la respuesta medible que produce la hormona sobre un órgano o acción enzimática. (43) Las hormonas influencian los estados funcionales y morfogenéticos de tejidos que se encuentran distantes de las glándulas endocrinas que las producen. Otras, como los andrógenos participan en la diferenciación celular, la proliferación, así como en la carcinogénesis. El sistema endocrino también regula el sistema inmunológico. Por ejemplo, los cambios cíclicos en la respuesta inmune tienen implicancia fisiológica, tal como la disminución o supresión de la inmunidad mediada por células, para evitar que los espermatozoides, y el embrión pre-implantacional sean PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 44 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA reconocidos como extraños, y de esta manera favorecer la fertilización y la implantación respectivamente. Las hormonas afectan a sus tejidos diana activando en primer lugar los receptores diana situados en las células del tejido, alterando la función del propio receptor, y este receptor es entonces la causa directa de los efectos hormonales. (43;69;72) Mecanismo de acción para hormonas con receptores de membrana: Las hormonas con receptores de membrana actúan produciendo a nivel intracelular sustancias denominadas “segundo mensajeros”. Un segundo mensajero es una sustancia cuya concentración aumenta intracelularmente en respuesta a la hormona primaria (primer mensajero). Su función es la de llevar la señal hormonal al interior de la célula, con la finalidad de traducirla en acción biológica. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 45 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Los segundos mensajeros actúan fosforilando proteínas que a su vez van a actuar sobre porciones específicas del DNA denominadas elementos de respuesta, y a partir de allí ejercer la acción hormonal. Entre los segundos mensajeros tenemos: el AMP cíclico, el GMP cíclico, el ión calcio, el ión calcio unido a la calmodulina, el ácido araquidónico y sus metabolitos, el inositol trifosfato, y el diacilglicerol. 1. AMP cíclico: es el segundo mensajero para muchas hormonas y media sus efectos metabólicos dentro de las células. Es producido por la adenil ciclasa que es una enzima unida al lado interno de la membrana citoplasmática. Esta enzima convierte ATP en AMP cíclico en presencia de iones Mg2+. La concentración de AMPc en el citoplasma es a su vez controlada por una segunda enzima, la fosfodiesterasa que cataliza la hidrólisis de AMPc en 5’-AMP. (43;58) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 46 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA El AMPc activa una proteína kinasa. La proteína kinasa nativa está compuesta de dos subunidades: catalítica y regulatoria. La subunidad regulatoria suprime la actividad de la proteína kinasa nativa mediante su asociación con la subunidad catalítica. La activación de la proteína kinasa ocurre después de que se ha liberado la subunidad catalítica de la subunidad regulatoria, por la unión del AMPc a la subunidad regulatoria de la proteína kinasa. La proteína kinasa activa (subunidad catalítica) fosforila proteínas específicas denominadas: - Proteína ligadora del elemento de respuesta al AMPc (CREB) - Modulador del elemento de respuesta al AMPc (CREM) La fosforilación de estas proteínas produce cambios en sus actividades lo que les permiten interactuar con secuencias específicas del DNA denominadas elementos de respuesta PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 47 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA al AMPc (CRE) para modular la transcripción del gen. Tanto la CREB como el CREM pertenecen a una familia de proteínas ligadoras que tienen alguna homología entre sí. Esta familia de proteínas ligadoras incluye tanto inhibidores como activadores de la transcripción de los genes. En los efectos tróficos de respuesta prolongada, el sistema regula la síntesis proteica a nivel de la transcripción y la translación de los ácidos nucleicos. Las gonadotropinas en las gónadas son buen ejemplo de la activación del AMPc. (58;69) 2. GMP cíclico: es producido por acción de la enzima guanidil ciclasa, la cual se encuentra en forma soluble y unida a la membrana, que convierte GTP a GMPc. La GMPc es posteriormente inactivada por acción de una fosfosdiesterasa. La GMPc activa la proteína kinasa G que a su vez fosforila proteínas. La hormona atrial natriurética y el óxido nítrico actúan a través de la activación del GMPc. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 48 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Fosfodiesterasas: regulación de la son enzimas que permiten la concentración intracelular de AMPc y GMPc. En el organismo se encuentran 5 tipos de fosfodiesterasas: - Fosfodiesterasa I: Estimulada por el complejo calcio-calmodulina - Fosfodiesterasa II: Estimulada por GMPc - Fosfodiesterasa III: Inhibida por GMPc - Fosfodiesterasa IV: Específico para AMPc - Fosfodiesterasa V: Específico para GMPc. 3. Calcio: actúa como segundo mensajero al incrementarse como fracción libre intracitoplasmática o al unirse a la calmodulina. En este, la hormona específica se une a un receptor en el lado externo de la membrana; esto conduce a un cambio conformacional en la membrana que directamente estimulará la apertura o la constitución de los PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 49 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA canales de calcio que favorecerán el influjo de calcio. (3;69;72) Los iones de calcio pueden afectar los procesos celulares directamente o pueden ligarse a la calmodulina. El complejo calcio-calmodulina puede ligarse a ciertas enzimas con la finalidad de activarlos. Este complejo activa una proteína kinasa en el núcleo, fosforilándolo y activando a la proteína ligadora dependiente de AMPc y el elemento de respuesta dependiente de AMPc. La proteína kinasa nuclear dependiente de calcio-calmodulina puede funcionar como un mediador de la transcripción inducida por calcio en sistemas endocrinos y neuroendocrinos como el hipocampo, hipotálamo y pituitaria. El calcio intracelular puede activar los sistemas de secreción formando un puente de los gránulos de secreción con la membrana plasmática desarrollando el acoplamiento estímulo-secreción. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 50 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Otra forma de aumentar el calcio intracelular es a través de su liberación de los compartimentos celulares, tales como el retículo endoplásmico y la mitocondria. Este proceso puede ser desarrollado por acción de un segundo mensajero, el inositol trifosfato (ITP), que a su vez procede de la hidrólisis del fosfatidil-inositol-4,5-bifosfato. El calcio intracelular puede participar en los procesos de exocitosis para la secreción hormonal, o activar sistemas enzimáticos que participan en la formación de otros mensajeros. (3;72) 4. Fosfoinositoles: Los fosfoinositoles (fosfatidilinositol, fosfatidil inositol monofosfato, y fosfatidil inositol bifosfato) se encuentran en la cara interna de la membrana citoplasmática. De todos estos, el fosfatidilinositol-4,5bifosfato es el que interviene después que la hormona se une a su receptor. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 51 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA R1 R2 P P OH OH Fosfolipasa C R1 OH R2 OH 1.2 diacilglicerol (DAG) P P Fosfoinositol 4,5- bifosfato (PIP2) P OH OH OH P Inositol 1,4,5 – trifosfato (IP3) Figura 1.4: (Laguna José, Piña Enrique, Bioquímica de Laguna) Según el modelo, la hidrólisis de este fosfolípido por acción de una fosfodiesterasa produce diacilglicerol (DAG) e inositol-1,4,5-trifosfato (ITP). El diacilglicerol siempre tiene en el carbono 1 el ácido graso: Ácido araquidónico. El ITP actúa movilizando calcio intracelular, mientras que el diacilglicerol puede activar una proteína kinasa C (PKC) o liberar ácido araquidónico. (5;69;78) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 52 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La activación de una proteína kinasa C por acción de la DAG, induce la fosforilación de proteínas que favorecen la respuesta biológica u hormonal. El DAG por acción de una lipasa dependiente de calcio puede liberar ácido araquidónico de la posición 1 del DAG. El ácido araquidónico puede activar la formación de GTP a GMP cíclico, o ser metabolizada por la enzima lipooxigenasa para producir hidroxiperóxidos y leucotrienos, o por la enzima ciclo-oxigenasa para producir prostaglandinas, tromboxano, y prostaciclina. Varios de estos metabolitos actúan como segundo mensajeros. Las hormonas pueden actuar en cualquiera de estas vías; así, la insulina, la angiotensina II y las hormonas hipotalámicas actúan a través de la proteína kinasa C, el EGF a través de la vía de la lipo-oxigenasa, la serotonina a través de la vía de la ciclo-oxigenasa; la hormona atrial natriurética activa el sistema guanilato ciclasa-GMPc. (3;5) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 53 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Mecanismo de acción para hormonas con receptores intracelulares: A diferencia de las hormonas peptídicas, que debido a su peso molecular no pueden penetrar a la célula, los esteroides y las hormonas tiroideas, por su bajo peso molecular y por su naturaleza lipofílica atraviesan con facilidad la membrana citoplasmática. Aunque los esteroides y las hormonas tiroideas penetran a todas las células del organismo, sólo aquellas células que contienen receptores específicos para ellas responderán al estímulo hormonal. Los esteroides son transportados en el torrente sanguíneo en forma libre o ligados a proteínas séricas, como la globulina ligadora de hormonas sexuales (SHBG), la globulina ligadora de corticosteroides (CBG), y la albúmina. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 54 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA En las células de los órganos blanco, los esteroides ingresan por difusión, aunque se puede unir a la SHBG en el suero y unirse a un receptor de membrana y activar la formación de AMPc. Si el esteroide difunde dentro de la célula por difusión, permanece dentro de ella por un tiempo largo, por lo que puede mantenerse una concentración intracelular aumentada. En el núcleo se encuentran células efectoras de una proteína de alto peso molecular y con una alta afinidad para ligar selectivamente un esteroide dado, y que es conocido como receptor. (58;69;72) El receptor se ubica dentro del núcleo, y la unión del esteroide al receptor induce a un cambio conformacional del receptor que mejora su afinidad para secuencias específicas en el DNA denominadas Elementos de Respuesta a los Esteroides (ERE). Esta reacción, a su vez induce cambios en la expresión de los genes que finalmente genera la síntesis de proteína y la respuesta celular. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 55 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La asociación de esteroide al receptor precede cualquier efecto fisiológico, más aún, los tejidos que carecen del receptor, no responderán al estímulo hormonal. Este es el caso del testículo femenizante donde el testículo fetal produce testosterona pero al no haber receptores para testosterona, no se produce la acción de esta hormona. La mayoría de interacciones esteroide-receptor ocurre dentro del núcleo, excepto el receptor de los glucocorticoides, que parece translocarse del citoplasma al núcleo después de haberse ligado a la hormona. (3;72) La activación de los elementos de respuesta induce que la enzima RNA polimerasa ocupe el sitio de iniciación para que sintetice el RNAm. El RNA mensajero migra hacia los ribosomas del citoplasma donde se sintetiza la proteína cuya codificación ha sido desreprimida. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 56 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA En conclusión, los esteroides modulan la transcripción de genes por su interacción con secuencias específicas de genes en el DNA. Estas secuencias son conocidas como elementos de respuesta, y facilitan que sintetice RNA mensajero durante la transcripción, seguido por la síntesis proteica durante la translación, y en esta forma producir los efectos fisiológicos. APOPTOSIS HORMONAL: La proliferación de las células y la muerte celular participan de manera armónica en el mantenimiento de la homeostasis celular. La apoptosis es la muerte celular programada que ocurre normalmente en diferentes estadios de la morfogénesis, crecimiento y desarrollo de los metazoarios, y en el recambio normal del tejido adulto. Durante la apoptosis, una célula a través de un proceso dependiente de energía ingresa a un suicidio PATRICIA DELGADO TORRES LORENA BRAVO MEDINA celular iniciado por señales 57 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA específicas en un microambiente aparentemente normal. La apoptosis se inicia en células específicas por agentes endógenos (hormonas) y exógenos (radiación, químicos, virus). Las hormonas pueden participar estimulando la apoptosis o previniéndola. Los glucocorticoides estimulan la apoptosis induciendo la muerte de timocitos inmaduros. La melatonina tiene un efecto preventivo de la apoptosis en las células neuronales inducidas por 6-hidroxidopamina. (3;58;68) La Bcl-2 es una proteína que inhibe la apoptosis. El estradiol regula la producción de Bcl-2 en varios tejidos, entre ellas, las neuronas del hipotálamo. Una vez iniciada la apoptosis ocurre una cascada de eventos bioquímicos y morfológicos que resultan en una degradación irreversible del DNA genómico y la fragmentación de la célula. La secuencia de eventos de la apoptosis son: agregación de la cromatina, condensación PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 58 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA nuclear y citoplasmática, y una eventual fragmentación de la célula en un conglomerado de segmentos con membranas (cuerpos apoptóticos) que a menudo contienen organelas intactas. Estos cuerpos apoptóticos son fagocitadas por los macrófagos. La fragmentación del DNA ocurre antes de que haya cambios en la permeabilidad de la membrana plasmática y de las intracitoplasmáticas. (69;72) TRASTORNOS DE LA FUNCIÓN ENDOCRINA Hiperfunción: El exceso de actividad y aumento de producción hormonal es debido a la hiperfunción de una glándula, puede estar causada por un tumor productor de hormonas que es benigno o, con menos frecuencia, maligno. Las enfermedades más frecuentes con hiperfunción son: Hiperparatiroidismo primario Hiperparatiroidismo nutricional secundario PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 59 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Hipertiroidismo Hiperadrenocorticismo (síndrome de Cushing) Insulinoma (hiperinsulinismo) Hipofunción: La actividad insuficiente puede deberse a defectos congénitos, cáncer, lesiones inflamatorias, degeneración, trastornos de la hipófisis que afectan a los órganos, traumatismos, o, en el caso de enfermedad tiroidea, déficit de yodo. Las más frecuentes son: Hipopituitarismo Hipotiroidismo Hipoparatiroidismo primario Hipoadrenocorticismo (síndrome de Adisson) Diabetes mellitus (Hipoinsulinismo) Diabetes Insípida (43;52) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 60 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA DETERMINACION DE CONCENTRACIONES HORMONALES EN SANGRE Casi todas las hormonas se encuentran presentes en la sangre en cantidades extremadamente pequeñas, algunas en concentraciones de hasta picogramos por mililitro, por ello, resulta casi imposible determinar estas concentraciones por métodos químicos habituales. Se han desarrollado métodos extremadamente sensibles para la determinación de hormonas, de sus precursores y de sus productos metabólicos, entre estos métodos tenemos el Radioinmunoanálisis y la Quimioluminicencia (se tratará en detalle en el Capítulo V). (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 61 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA CAPITULO II CARBOHIDRATOS Introducción: Los hidratos de carbono son una clase básica de compuestos químicos, son la forma biológica primaria de almacén o consumo de energía. (11) Están constituidos por carbono hidrógeno y oxígeno; pueden presentarse bajo la forma de polisacáridos (almidones) disacáridos o monosacáridos, que se desdoblan en el tracto digestivo hasta formar glucosa que es la fuente de energía por excelencia. Los carbohidratos proporcionan el calor y energía necesarios para realizar las actividades corporales. (32) Cuando se ingieren en exceso se almacenan en forma de glucógeno, en el hígado y en los músculos, aunque si los depósitos están llenos se transforman en lípidos que se almacenan en el tejido adiposo. (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 62 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA El término hidrato de carbono es poco apropiado, ya que estas moléculas no son átomos de carbono hidratados, es decir, enlazados a moléculas de agua, sino de átomos de carbono unidos a otros grupos funcionales químicos. Este nombre proviene de la nomenclatura química del siglo XIX, ya que las primeras sustancias aisladas respondían a la formula elemental Cn(H2O)n (donde "n" es un entero según el número de átomos). De aquí el término "carbonohidratado" se haya mantenido, si bien posteriormente se vio que otras moléculas con las mismas características químicas no se corresponden con esta fórmula. (18) Sinónimos: Hidratos de carbono: aunque ha habido intentos para sustituir los términos de hidratos de carbono y carbohidratos, desde 1996 el Comité Conjunto de la Unión Internacional de Química Pura y Aplicada y de la Unión PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 63 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Internacional de Bioquímica y Biología Molecular recomienda el término carbohidrato y desaconseja el de hidratos de carbono.(11) Glúcido: este nombre proviene de que, pueden considerarse derivados de la glucosa por polimerización y pérdida de agua. El vocablo procede del griego "glycýs", que significa dulce. (11) Azúcares: este término sólo puede usarse para los monosacáridos (aldosas y cetosas) y los oligosacáridos inferiores (disacáridos).(11) Estructura química: Los carbohidratos son moléculas compuestas en su mayor parte por átomos de carbono, hidrógeno y oxígeno; la unidad fundamental básica es un monosacárido, el más PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 64 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA común es la glucosa; otros dos monosacáridos importantes son la fructosa y la galactosa. (5) Los carbohidratos no son moléculas cuyos carbonos están hidratados, sino enlazados a grupos alcohólicos o hidroxilos (-OH), y a radicales hidrógeno (-H). Además siempre hay un grupo funcional como una grupo cetónico (-C=O-) o un grupo aldheído (-CH=O), por lo que los glúcidos podrían llamarse polihidroxicetonas (cetosas) o polihidroxialdheídos (aldosas). (7) En la naturaleza se encuentran en los seres vivos, formando parte de biomoléculas aisladas o asociadas a otras como las proteínas y los lípidos. (18) Función de los hidratos de carbono: Los carbohidratos desempeñan diversas funciones, siendo las de reserva energética y formación de estructuras las dos más importantes. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 65 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Pero la función de estos "hidratos de carbono" es mantener la actividad muscular, la temperatura corporal, la tensión arterial, el correcto funcionamiento del intestino y la actividad neuronal. (13) METABOLISMO DE CARBOHIDRATOS Las principales rutas del metabolismo de los carbohidratos o bien comienzan o bien terminan con la glucosa. La comprensión de las rutas metabólicas relacionadas con la glucosa, así como su regulación es necesaria, debido a la importancia del papel jugado por la glucosa en el organismo. (71) Se inicia con la digestión y absorción de los mismos: Digestión: La digestión de los carbohidratos desdobla los almidones y otros polímeros en monosacáridos componentes, agregando una molécula de agua al compuesto en cada punto donde se encuentran unidos dos monosacáridos PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 66 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA sucesivos, así en el tubo digestivo hay enzimas que catalizan este proceso de hidrólisis. (18) Los almidones y otros grandes carbohidratos se digieren por acción de la ptialina de la saliva, amilasa de jugo pancreático, ácido clorhídrico del estómago y amilasa del intestino delgado produciendo disacáridos (maltosa e isomaltosa). (19) Los productos finales de la digestión de los carbohidratos son: glucosa, galactosa y fructosa, el producto final más abundante es la glucosa. (5) En la degradación de los carbohidratos el 80% es glucosa, el 10 % es galactosa y el resto es fructosa. (18) Asimilación: Abarca varias funciones: 1. Absorción de los productos digestivos terminales hacia los líquidos corporales. 2. Transporte de estos hacia células en las que se emplearán. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 67 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 3. Cambios químicos de algunos en otras sustancias requeridas con diferentes finalidades. (3) Absorción: Las sustancias son absorbidas por medio de pliegues mucosos, vellosidades y microvellosidades dirigiéndose hacia los capilares sanguíneos y el vaso quilífero central. (3) Este proceso se realiza por dos mecanismos: la absorción activa y cotransporte de sodio. (5) Los monosacáridos junto con sustancia portadora de células epiteliales y sodio producen desplazamiento de sodio tirando del monosacárido junto a el, por lo tanto las células epiteliales consumen energía. El sodio es posteriormente expulsado de la célula intestinal a cambio de potasio que penetra en un proceso que requiere de ATP, la glucosa en parte se difunde hacia la sangre y en parte es fosforilada. Este mecanismo es PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 68 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA importante porque permite que ocurra la absorción en el intestino cuando existen concentraciones bajas. (3) Las principales rutas metabólicas de los glúcidos son: Glicólisis. Neoglucogénesis. Glucogénesis. Ciclo de las pentosas. En el metabolismo oxidativo encontramos rutas comunes con los lípidos como son el ciclo de Krebs y la cadena respiratoria. (19) GLUCOSA Es el compuesto orgánico más abundante de la naturaleza. Es la fuente principal de energía de las células, mediante la degradación catabólica y es el componente principal de polímeros de importancia estructural como la celulosa, y de polímeros de almacenamiento energético como el almidón.(11) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 69 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Es la forma más importante por la cual los carbohidratos son absorbidos desde el tracto intestinal. Es la única molécula energética utilizada por una serie de células especializadas y casi la única por las células del cerebro. Es tan importante para estas células y para el conjunto del organismo que existen diferentes órganos casi especializados en su utilización, de tal manera que aseguran un suministro continuo de la misma en todo momento. (18) El metabolismo de la glucosa está relacionado con dos enfermedades metabólicas bastante comunes, como son la diabetes y la obesidad, contribuyendo a una serie de problemas muy importantes como la ateroesclerosis, la hipertensión, ceguera, etc. (30) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 70 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA METABOLISMO DE LA GLUCOSA La glucosa se metaboliza de manera diferente en diferentes células: Eritrocitos. Después de penetrar la membrana plasmática mediante la proteína de transporte de glucosa GLUT-1, la glucosa se metaboliza principalmente por la glicólisis. Estas carecen de mitocondrias y el producto final es el lactato, que se libera en la sangre. La glucosa utilizada en los eritrocitos por la ruta de la pentosas fosfato provee de NADPH para mantener reducido el glutatión, que tiene un papel fundamental en la destrucción de peróxidos orgánicos y el H2O2, que causan daños muy importantes en las membranas, el DNA, y otros componentes celulares, lo que provocaría la muerte de muchas células. (3) Cerebro. El cerebro toma glucosa de la sangre mediante la proteína transportadora de glucosa GLUT-3, independiente de insulina. La glicólisis da lugar a piruvato, que se oxida a CO2 y H2O. También tiene lugar en estas células la ruta de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 71 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA las pentosas fosfato para proveer de NADPH para las rutas de síntesis y el mantenimiento del glutatión en la forma reducida. (9) Células del músculo y del corazón. Estas células utilizan rápidamente la glucosa. La insulina estimula el transporte de la glucosa hacia estas células mediante la proteína transportadora de glucosa GLUT-4. Dentro de estas células, la glucosa se utiliza para dar lugar al piruvato, y posteriormente oxidarse completamente. Al contrario que los tejidos mencionados anteriormente, el músculo y el corazón pueden sintetizar cantidades significativas de glucógeno, proceso muy importante en estas células. (3) Tejido adiposo. En el tejido adiposo también se transporta la glucosa mediante la proteína GLUT-4, dependiente de la insulina. El piruvato se genera por la glicólisis y se oxida por la piruvato deshidrogenasa para dar acetil-CoA, en este caso utilizado para la síntesis de ácidos grasos. La generación del NADPH, necesario para la síntesis de los PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 72 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA ácidos grasos, se realiza por la ruta de las pentosas fosfato. El tejido adiposo puede realizar glucogenosíntesis y glucogenolisis, pero en mucha menor medida que en el músculo y corazón. (3) Hígado. El hígado tiene el número mayor de rutas para la utilización de la glucosa. La toma de glucosa se realiza por una proteína transportadora de glucosa, GLUT-2, de alta capacidad y baja afinidad. La glucosa se utiliza por la ruta de las pentosas fosfato en gran medida, ya que produce NADPH para la síntesis, mantenimiento del glutatión reducido, y numerosas reacciones enzimáticas localizadas en el retículo endoplásmico. También provee de ribosa fosfato, necesario para la síntesis de nucleótidos. (3) El hígado también realiza la glicólisis, siendo el piruvato producido, utilizado para la formación de acetil-CoA, para el ciclo de Krebs o ciclo de los ácidos tricarboxílicos. El hígado, en contraste con otros tejidos, tiene la capacidad de producir glucosa a partir de compuestos de tres PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 73 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA carbonos, como el lactato, el piruvato, el glicerol o la alanina, por el proceso denominado de la luconeogénesis, para poder proporcionar glucosa a otras células. (6) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 74 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Figura 2.3 (www. gluco_983/cm34.PDF) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 75 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA GLUCÓLISIS La glucólisis , glicólisis o ruta de EMBDEN-MEYERHOF es la secuencia metabólica que consistente en una serie de reacciones enzimáticas, en las que se oxida la glucosa produciendo dos moléculas de piruvato y dos equivalentes reducidos de NADH los que al introducirse en la cadena respiratoria, producirán tres moléculas de ATP. (19) Es la única vía en los animales que produce ATP en ausencia de oxígeno. Los organismos primitivos se originaron en un mundo cuya atmósfera carecía de 02 por esto, la glucólisis se considera como la vía metabólica más primitiva y por lo tanto, está presente en todas las formas de vida actuales. Es la primera parte del metabolismo energético y en las células eucariotas ocurre en el citoplasma.(18) Se caracteriza por una serie de reacciones que se llevan a cabo en el citoplasma de la célula y permiten la conversión PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 76 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA de glucosa a 2 moléculas de piruvato, 2 moléculas de ATP y 2 NADH+H. (5) La reacción global de la glucólisis es: Glucosa + 2 NAD+ + ADP + 2 Pi → 2 NADH + 2 piruvato + 2 ATP + 2 H2O + 4 H+ Sustratos alternos para la glucólisis: Si bien es cierto que la glucosa representa el sustrato mas importante para la fermentación y la respiración en un gran número de organismos y tejidos, no quiere decir que sea el único, además de que para algunos tejidos, en ciertas circunstancias, tiene poco significado desde el punto de vista metabólico. Por esto es necesario preguntar cuáles son las principales moléculas alternativas para la glucólisis y cómo las maneja la célula. (5) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 77 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA De inicio se debe establecer un principio: sin importar la naturaleza química de los sustratos, éstos deben ser rápidamente transformados en una molécula que pueda ser incorporada a alguno de los intermediarios en la vía de la glucólisis.(5) Entrada de la fructosa y de la galactosa: La hidrólisis de la sacarosa produce glucosa y fructosa mientras que la hidrólisis de la lactosa produce glucosa y galactosa. Todas estas hexosas se convierten en intermediarios de la glicólisis. (5) Existen dos vías principales para la fructosa: una en el hígado y otra en el músculo. La entrada de la fructosa en la glicólisis tiene varios pasos. (7) En el hígado, se convierte en fructosa 1-fosfato (F1P) por la fructoquinasa, para posteriormente escindirse en gliceraldehido y dihidroxiacetona fosfato (DHAP) por la fructosa 1-fosfato aldolasa. El gliceraldehido se convierte PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 78 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA en gliceraldehido 3 fosfato (G3P) por la triosa quinasa con gasto de ATP. (5) Otra posibilidad es que se convierta en fructosa-6-fosfato por la hexoquinasa, pero esta enzima es unas 20 veces más activa con la Glucosa que con la Fructosa, salvo en el tejido adiposo o en el músculo, donde la concentración de Fructosa es bastante grande. La galactosa se convierte en glucosa 6P en cuatro etapas. En primer lugar se convierte en galactosa-1-fosfato, por una galactoquinasa. La Galactosa 1P se une a un resto uridilo procedente de la UDP-glucosa, catalizado por la galactosa-1-fosfato uridiltransferasa, formando UDP- galactosa y Glucosa 1P. Posteriormente la UDP-galactosa4-epimerasa invierte la configuración del OH en C4 formando UDP-glucosa. La Glucosa 1P se isomeriza en Glucosa 6P por la fosfoglucomutasa. (5) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 79 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Regulación de la glucólisis: Uno de los propósitos de la vía glucolítica es la producción de ATP, lo que hace necesario que la vía sea continua y regulada para mantener en equilibrio el metabolismo energético celular. (7) Esta regulación se realiza de dos maneras, controlando la velocidad de conversión de la glucosa a lactato y regulando la cantidad de glucógeno que es transformado a glucosa libre. La principal reacción que controla el flujo de glucosa por la glucólisis es la reacción catalizada por la fosfofructocinasa, enzima alostérica que es inhibida (moduladores negativos) por el ATP y el citrato, sustrato del ciclo de Krebs y activada (moduladores positivos) por el AMP y el ADP y la fructosa 2,6 bifosfato, lo que da lugar a un punto delicadamente sensible al estado de balance energético de la célula, definido como el cociente del par ATP/ADP. (5) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 80 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Además de su sensibilidad a ATP, ADP y AMP, la fosfofructocinasa es alostéricamente inhibida por el citrato y por los ácidos, grasos. El modulador alostérico positivo más potente de la fosfofructoquinasa y con más influencia sobre la velocidad de flujo de monosacáridos a través de la glucólisis, es la fructosa 2,6-bifosfato, la cual revierte la inhibición producida por el ATP, aumenta la afinidad de la enzima por su sustrato y así activa la glucólisis. (5) GLUCONEOGÉNESIS Gluconeogénesis es la síntesis de una nueva glucosa, se refiere a que la glucosa puede ser formada en el hígado y en los riñones a partir de moléculas que no son carbohidratos: como lactato, glicerol y aminoácidos. (10) El piruvato es la molécula inicial de esta vía. (5) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 81 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La producción de glucosa a partir de otros metabolitos es necesaria para su uso como una fuente de energía para el cerebro, testículos, eritrocitos, riñón, entre otros. (9) La glucólisis y la gluconeogénesis son rutas metabólicas estrechamente relacionadas y si bien comparten 7 reacciones son diferentes en cuanto a sustratos, productos, energía, regulación, etc. (5) En condiciones fisiológicas solo opera una de las dos vías. Las reservas de carbohidratos satisfacen las necesidades fisiológicas por unas 24 horas, en caso de ayuno prolongado, a través de la gluconeogénesis se forma la glucosa para proveer de energía a las células se libera glicerol del tejido adiposo y a partir de la poza de aminoácidos se suministran los intermediarios del ciclo de los ácidos tricarboxílicos. (7) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 82 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Balance energético de la gluconeogénesis: La gluconeogénesis requiere energía, en resumen, se necesitan dos moléculas de lactato para formar una de glucosa; la suma global de las reacciones de la gluconeogénesis es: 2 lactato + 4 ATP + 2 GTP + 4 NADH + 4 H+ + 4 H2O -> glucosa + 4 ADP + 2 GDP + 2 NAD+ + 6 Pi + 2 NADH + 2 H+ Se gastan 4 moléculas de ATP y 2 de GTP al convertir dos lactatos en una glucosa. (5) Otros sustratos gluconeogénicos: La conversión de lactato en glucosa es el camino clave de la gluconeogénesis sin embargo, no es el único sustrato de la vía. Se consideran sustratos de la gluconeogénesis los metabolitos que se convierten en lactato o en cualquiera de los intermediarios de la vía: (7) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 83 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Fosfoenolpiruvato. Alanina Acetato. Glutamato. Acetil Co A. Aspartato. Regulación de la gluconeogénesis: La enzima clave de la regulación de la gluconeogénesis es la piruvato descarboxilasa, cuyo activador alostérico es la acetilcoenzima A. (19) La reacción inicial de la gluconeogénesis es el primer sitio de su regulación. El segundo sitio de control es el paso de la fructosa 1.6bifosfato a la fructosa 6-fosfato. (5) La fructosa 1,6-bifosfatasa, es inhibida por el AMP y la fructosa 2.6-bifosfato y ambos, a su vez, estimulan el paso opuesto, es decir la síntesis de la fructuosa 1,6-bifosfato. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 84 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Es una regulación recíproca y coordinada: un aumento de ATP disminuye la glucólisis al inhibir el paso de la fructuosa 6-fosfato a fructosa 1,6-bifosfato, como esto coincide con bajos niveles de AMP, se favorece la reacción inversa propia de la gluconeogénesis. (5) La insulina deprime la gluconeogénesis al reprimir la formación de las enzimas del proceso (piruvato carboxilasa, fosfoenolpiruvato carboxiquinasa, fructosa 1-6 bifosfatasa y glucosa 6-fosfatasa) y facilita la glucólisis. Por el contrario, los glucocorticoides, el glucagón y la epinefrina inducen la síntesis de dichas enzimas y activan la gluconeogénesis. (13) Interrelaciones de los órganos en la gluconeogénesis: En los mamíferos, el hígado, y de manera secundaria, el riñón, son los órganos donde se realiza la gluconeogénesis. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 85 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Otros tejidos, como el muscular y el adiposo intervienen enviando, a través de la sangre, sustratos apropiados para ser convertidos por el hígado en glucosa. El primer proceso identificado fue el ciclo de Cori, y comprende la serie de reacciones para regenerar la glucosa en el hígado a partir del lactato muscular, la glucólisis anaerobia en el músculo convierte el glucógeno en lactato. (5) La anaerobiosis en el músculo, el exceso de lactato y la ausencia de la piruvato carboxilasa favorecen el paso de lactato a la sangre para ser captado por el hígado, donde se convierte en glucosa o glucógeno. (3) El glucógeno hepático puede generar glucosa sanguínea, pero el glucógeno muscular no libera glucosa por carecer el músculo de la glucosa 6-fosfatasa. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 86 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Esta situación metabólica del músculo facilita que el piruvato capte un grupo amino, por transaminación, para convertirse en alanina. (5) En condiciones fisiológicas existe un flujo continuo y neto de alanina del músculo al hígado, donde es desaminada y parcialmente transformada en glucosa. (3) El tejido adiposo libera continuamente glicerol, formado por la degradación continua de los triacilglicéridos almacenados en los adipositos, este sale a la circulación y es captado por el hígado para su posible conversión a glucosa.(3) RUTA DE LAS PENTOSAS FOSFATO Se lleva a cabo en el citoplasma de las células, tiene 2 propósitos fundamentales: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 87 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La generación de NADPH + H, coenzima que se utiliza en la biosíntesis de ácidos grasos y esteroides. La formación de ribosa 5 fosfato, carbohidrato necesario para la síntesis de nucleótidos.(3) Resumen de la ruta de las pentosas fosfato: La glucosa libera durante varias fases de la conversión una molécula de dióxido de carbono y cuatro átomos de hidrógeno, con la formación de un azúcar de cinco carbonos, la D-ribulosa. Esta sustancia, a su vez, puede transformarse de manera progresiva en otros azúcares de cinco, cuatro, siete y tres carbonos. Finalmente, diversas combinaciones de estos azúcares pueden volver a sintetizar glucosa. (76) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 88 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Uso del hidrógeno para sintetizar grasas, función del dinucleótido de nicotinamida y adenina fosfato: El hidrógeno liberado durante el ciclo de las pentosas fosfato no se combina con el NAD+ como en la glucólisis, sino con el dinucleótido de nicotinamida y adenina fosfato (NADP+), casi idéntico al NAD+ con excepción del radical fosfato extra. (5) Esta diferencia es extremadamente significativa, porque sólo el hidrógeno unido al NADP+ en forma de NADPH se puede utilizar para la síntesis de grasas a partir de los hidratos de carbono, así como para la síntesis de algunas otras sustancias. (5) El NADPH abundante ayuda a convertir la acetil-CoA, también derivada de la glucosa, en ácidos grasos dé cadena larga. Ésta es otra ruta en la que la energía de la PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 89 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA molécula de glucosa no se utiliza para la síntesis de ATP sino en este caso para almacenamiento de grasa en el cuerpo. (7) GLUCOGÉNESIS La glucosa que entra continuamente en las células cuando no se necesita de inmediato para energía se almacena como glucógeno. Cuando las células hepáticas y musculares están saturadas de glucógeno, la glucosa entonces se convierte en grasa en el hígado. (76) La glucogénesis es el proceso de formación de glucógeno cuyas reacciones químicas se ilustran a continuación: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 90 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Reacciones químicas de la glucogénesis y la glucogenolisis que además muestran las conversiones entre la glucosa sanguínea y el glucógeno hepático. Puede observarse que la glucosa 6- fosfato se puede convertir primero en glucosa 1 fosfato, después esta se transforma en uridina difosfato glucosa que finalmente se convierte en glucógeno. (3) Se necesitan varias enzimas concretas para estas conversiones y cualquier monosacárido que pueda convertirse en glucosa puede participar en las reacciones. Determinados compuestos más pequeños, entre ellos el ácido láctico, el glicerol, el ácido pirúvico y algunos aminoácidos desaminados, se pueden transformar también en glucosa o compuestos muy afines y después convertirse también en glucógeno. (5) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 91 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA GLUCOGENÓLISIS Glucogenólisis significa descomposición del glucógeno almacenado por la célula para formar de nuevo glucosa, que se utiliza entonces para proporcionar energía. (3) Es la vía mediante la cual el glucógeno almacenado en el hígado y en el tejido muscular, es fosforilado, para formar finalmente la molécula de glucosa 6 fosfato, la cual tiene varias posibilidades metabólicas. La glucogenólisis no se produce por inversión de las mismas reacciones químicas que sirven para sintetizar glucógeno; en su lugar, cada molécula de glucosa sucesiva de cada rama del polímero de glucógeno es escindida mediante una fosforilación, catalizada por la enzima fosforilasa. En condiciones de reposo, la fosforilasa se encuentra en una forma inactiva, de modo que se almacena glucógeno. Cuando se necesita volver a formar glucosa a partir de glucógeno, hay que activar primero la fosforilasa. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 92 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Activación de la fosforilasa por la adrenalina y el glucagón: Dos hormonas, la adrenalina y el glucagón, activan en concreto la fosforilasa y, por tanto, producen una glucogenólisis rápida. El efecto inicial de cada una de estas hormonas es la síntesis de AMP cíclico en las células. Esta sustancia inicia entonces una cascada de reacciones químicas que activan la fosforilasa. El glucagón estimula la formación de AMP cíclico principalmente en las células hepáticas, con lo que a su vez el glucógeno hepático se transforma en glucosa y ésta se libera a la sangre, elevando así la concentración de glucosa en sangre. (3;5) CICLO DE KREBS Se trata de una serie de reacciones químicas cuyo resultado es la transformación del grupo acetilo de la acetil CoA en dióxido de carbono y átomos de hidrógeno, todas PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 93 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA estas reacciones se llevan a cabo en la mitocondria. Los átomos posteriormente de hidrógeno produciendo liberados enormes se oxidan cantidades de energía para formar ATP. (70) Al inicio del ciclo de la Acetil CoA es combinada con el ácido oxaloacetico para formar ácido cítrico, liberándose la acetil coenzima A para luego ser usadas nuevamente. El ácido oxaloacético a su vez es el producto final de la cadena de reacciones, por lo que interviene nuevamente al inicio del ciclo conforme se forma; repitiéndose así el ciclo una y otra vez. (18) El ATP obtenido en la glucólisis y el ciclo del ácido cítrico es poco por lo que se dice que el 90% del ATP final se obtendrá durante la oxidación ulterior de los átomos de hidrógeno liberados en las primeras fases del desdoblamiento de la glucosa. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 94 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Para esto hay una serie de reacciones que se llevan a cabo, transformándose: 1. Los átomos de hidrógeno en hidrogeniones. 2. El oxígeno disuelto en iones hidroxilo. Luego estos iones se unen y forman agua. Durante el desarrollo de las reacciones de oxidación se liberaran grandes cantidades con lo que elaborara ATP (proceso llamado Fosforilación Oxidativa). (19) Los átomos de hidrógeno se eliminan por pares; uno inmediatamente constituye un ion hidrógeno y el otro se combina con NAD, para formar NADH, que luego liberara el otro átomo de hidrógeno y reconstituirá el NAD para ser usado una y otra vez. (18) Los electrones eliminados de los átomos de hidrógeno entran en una cadena de transporte de electrones, cuyos miembros incluyen una flavoproteína, citocrómos, etc. (19) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 95 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Al final de la cadena el oxigeno se combina con iones de hidrógeno para formar agua, y durante el transporte de electrones por la cadena se liberara energía para la formación de ATP. (5) ALTERACIONES DEL METABOLISMO DE LA GLUCOSA En una persona normal que no ha ingerido alimentos durante tres o cuatro horas, la cantidad de glucosa en sangre oscila alrededor de 80mg/100 ml. Rara vez pasa de 120 mg /100ml ni después de una comida que contenga grandes cantidades de carbohidratos o no ser que existan alteraciones en el organismo. (3) Glucemia basal alterada: Existe un grupo de sujetos con niveles de glucosa en sangre que, aunque no cumplen con los criterios diagnósticos de la diabetes, son demasiado altos para ser considerados normales. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 96 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Este grupo se define por Glucemia basal alterada (9) Glucosa plasmática en ayunas mayor a 110 mg/dl, pero inferior a 126 mg/dl. (3) Tolerancia anormal a la glucosa (TAG): Mal denominada "intolerancia a la glucosa", la TAG es una situación intermedia entre la normalidad y la diabetes. Los pacientes con TAG (sobrecarga de glucosa patológica pero sin alcanzar los valores diagnósticos de diabetes) presentan con mayor frecuencia que la población general enfermedad vascular, hipertensión, alteraciones electrocardiográficas y dislipemias. (12) Entre el 10 y el 70% de estos pacientes evolucionan hacia una diabetes clínica en los 10-15 años siguientes, de modo que una proporción importante no progresan hacia la diabetes o incluso revierten a la normalidad, especialmente si adelgazan. (9) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 97 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Con estos datos, y para evitar el estigma psicológico y sociológico del término "diabetes", se optó por la expresión diagnóstica "tolerancia anormal a la glucosa" en sustitución de antiguas denominaciones como diabetes latente o prediabetes. (9) La diabetes mellitus no es en una afección única, sino un síndrome dentro del cual deben individualizarse diferentes entidades nosológicas. (33) El nexo común de todas ellas es la hiperglucemia y sus consecuencias, es decir, las complicaciones específicas, las cuales son comunes a todas las formas de diabetes. (12) DIABETES La diabetes es un trastorno crónico de base genética caracterizado por tres tipos de manifestaciones:(33) a) un síndrome metabólico consistente en hiperglucemia, glucosuria, polifagia, polidipsia, poliuria y alteraciones en el PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 98 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA metabolismo de los lípidos y de las proteínas como consecuencia de un déficit absoluto o relativo en la acción de la insulina. (33) b) un síndrome vascular que puede ser macroangiopático y microangiopático y que afecta todos los órganos, pero especialmente el corazón, la circulación cerebral y periférica, los riñones y la retina.(33) c) un síndrome neuropático que puede ser a su vez autónomo y periférico. (33) CLASIFICACION DE LA DIABETES: Diabetes Mellitus Tipo 1 Inmuno mediada Idiopática. Diabetes Mellitus Tipo 2 Diabetes gestacional Otros tipos específicos de Diabetes Mellitus PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 99 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Defectos genéticos Enfermedades del páncreas exócrino Endocrinopatías Inducida por drogas o medicamentos Infecciones Formas poco comunes inmuno-mediadas Síndromes genéticos asociados a diabetes (3) Diabetes Mellitus tipo 1: Llamada diabetes insulino-dependiente, se diagnostica generalmente durante la infancia. En la diabetes tipo 1, el páncreas produce poca insulina, o no la produce en absoluto, así que inyecciones diarias de insulina son necesarias. Entre 5 y 10% de todos los casos conocidos de diabetes son del tipo 1. El proceso de desarrollo de la diabetes tipo 1 es gradual, pudiendo ser necesarios varios años antes de que se manifieste clínicamente. (12) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 100 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La enfermedad se desarrolla por el ataque del sistema inmune contra las propias células beta del páncreas. Este proceso parece tener varias etapas: • Hay, primero, una susceptibilidad o predisposición genética, en la que parece haber implicados varios genes. • Además, parece necesario que ocurra un factor desencadenante ambiental (infección viral, estrés, toxinas, etc.), tras el cual, aparece el proceso inmunológico frente a las propias células beta, que son destruidas. (9) La reacción inmunológica está mediada por anticuerpos y células, habiéndose detectado autoanticuerpos frente a proteínas presentes en la superficie de las células beta, como la descarboxilasa del ácido glutámico (GAD), los IA2, dirigidos contra una fosfatasa presente en el interior de las células beta; y anticuerpos contra la propia insulina. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 101 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Estos anticuerpos pueden ser detectados en el suero de los pacientes meses y años antes del desarrollo de la enfermedad, y se han convertido en marcadores de un estado conocido como prediabetes. (13) Diabetes mellitus tipo 2: También se llama diabetes no dependiente de insulina. Aunque ésta generalmente se presenta en los adultos de edad mediana, los adolescentes y los adultos jóvenes están desarrollando diabetes tipo 2. (13) Entre 90 y 95 por ciento de los casos de diabetes son del tipo 2. Este padecimiento se desarrolla cuando el cuerpo no produce suficiente insulina y además, no utiliza la cantidad de insulina disponible con eficiencia (resistencia a la insulina).(12;33) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 102 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La diabetes tipo 2 se puede controlar mediante la dieta y el ejercicio; sin embargo, algunas personas también necesitan medicamentos orales o insulina para ayudar a controlar el azúcar en sangre.(13) Factores de riesgo de diabetes. • El exceso de peso/ la obesidad • La edad avanzada • Antecedentes familiares de diabetes • Diabetes durante el embarazo • Falta de actividad física • Raza (afroamericano, latino/hispano o nativo americano).(64) Diabetes gestacional: El embarazo normal produce varios cambios homeostáticos en la mujer. En ayunas la mujer embarazada es hipoglicémica, hipoaminoacidémica (alanina), hipoinsulinémica, hiperlipidémica e hipercetonémica. (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 103 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Desde el principio del embarazo, el ayuno incide en una severa disminución de la glucosa materna circulante del orden de 15 mg a 20 mg, en relación con la mujer no embarazada; este fenómeno es más acentuado en el segundo y tercer trimestre. (12) La insulina materna no atraviesa la membrana placentaria por lo cual el feto secreta su propia insulina a partir de la semana 10 del embarazo actuando como hormona de crecimiento fetal. (9) La respuesta metabólica después de la ingesta en la mujer embarazada, se caracteriza por hiperglicemia, hipertrigliceridemia, hiperinsulinemia y resistencia periférica a la insulina, lo cual convierte al embarazo como un evento diabetogénico pudiendo desenmascarar un estado de diabetes latente, porque ante el aumento en las necesidades de insulina, el embarazo actúa como una prueba funcional de reserva. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 104 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Es por esta razón que toda gestante debe tener durante su control prenatal pruebas de diagnóstico temprano para la diabetes gestacional tales como la prueba de O’Sullivan con 50 g de glucosa y la carga de tolerancia oral como prueba confirmatoria de diabetes gestacional en caso de sospecha o riesgo de diabetes gestacional.(12) Las gestantes que tengan alto riesgo biopsicosocial se consideran de alto gestacional porque riesgo el para estrés presentar aumenta diabetes los niveles circulantes de glucosa por tres mecanismos básicos: 1. Las catecolaminas liberadas por el estrés tienen un efecto glucogenolítico indirecto. 2. Los estímulos corticales del estrés llevan finalmente a un estímulo de secreción de ACTH y cortisol con efecto hiperglicemiante. 3. El estrés aumenta aún más la resistencia periférica a la insulina. (12) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 105 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA HIPOGLICEMIA En individuos normales la concentración plasmática de glucosa permanece entre unos estrechos límites (70-100 mg/dL) durante las 24 h del día merced a la eficacia de diversos mecanismos homeostáticos, hormonalmente controlados, que mantienen un adecuado balance entre la producción y el consumo de glucosa. (9) Durante el período posprandial, la producción endógena de glucosa se encuentra suprimida y el metabolismo y almacenamiento incrementados. En esta fase anabólica del metabolismo la insulina, segregada por las células beta pancreáticas, es la hormona responsable del cese de la producción hepática de glucosa a la vez que estimula su utilización por los tejidos insulínsensibles. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 106 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Por el contrario, en el período de ayuno o postabsortivo se intensifica la producción de glucosa y disminuye sensiblemente su consumo. (6) Esta fase catabólica del metabolismo se caracteriza por el estímulo en la producción hepática de glucosa, a través de la glucogenólisis y gluconeogénesis, mediada por la secreción de glucagón por las células alfa pancreáticas, y la participación en distinto grado de catecolaminas, cortisol y hormona del crecimiento. En circunstancias normales los sistemas señalados son efectivos para mantener un adecuado equilibrio entre la producción y el consumo de glucosa. (6) Cuando la glucosa plasmática desciende a valores inferiores a los normales (alrededor de 55 mg/dL) se pone en marcha un mecanismo representado por la disminución o supresión de la secreción insulínica y la elevación de las hormonas contrarreguladoras, en especial glucagón y adrenalina. Pero cuando el sistema homeostático se rompe PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 107 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA o resulta insuficiente aparece el cuadro clínico de la hipoglucemia que se acompaña de manifestaciones variables de disfunción del SNC debido a que estas estructuras, a diferencia de otras del organismo, sólo pueden utilizar la glucosa como principal fuente de energía. (3) Así pues, la hipoglucemia debe ser contemplada como un síndrome plurietiológico caracterizado por la disminución en la concentración de la glucosa plasmática y la aparición de una serie de signos y síntomas como consecuencia de aquella disminución y de la activación hormonal contrarreguladora. (12) Clasificación de la hipoglucemia: Tradicionalmente la hipoglucemia se ha clasificado en dos grandes grupos: de ayuno o postabsortiva y posprandial o reactiva, caracterizándose el primero por la aparición del cuadro clínico después de 5-6 h de la última ingesta, por lo general tras el ayuno nocturno, y el segundo por el PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 108 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA desarrollo de la sintomatología entre pocos minutos y 2-4 h después del consumo de alimentos. Sin embargo, hipoglucemias se debe graves tener reconocen en cuenta casi que siempre las una enfermedad o trastorno subyacente de los que se consideran dentro de las causas de hipoglucemia de ayuno y que en ocasiones la sintomatología puede aparecer en el período posprandial. (12) Asimismo, entre las causas más frecuentes de hipoglucemia se encuentran las relacionadas con el tratamiento insulínico o con sulfonilureas de la diabetes mellitus, y entre las menos habituales las que se encuentran ligadas a algunos trastornos congénitos o hereditarios del metabolismo hidrocarbonado. (9) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 109 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Hipoglucemia de ayuno o postabsortiva: El cuadro clínico se desarrolla en situaciones que existe un consumo excesivo de glucosa, que puede cursar con hiperinsulinismo o con niveles adecuados de insulina, y en otras en que la alteración consiste en la producción insuficiente de glucosa. (12) Hipoglucemia posprandial o reactiva: La causa más frecuente de hipoglucemia posprandial está representada por el hiperinsulinismo alimentario en pacientes sometidos a cirugía digestiva (gastrectomía, gastroyeyunostomía, piloroplastia, vagotomía). La absorción rápida de los hidratos de carbono ingeridos, junto a estímulos intestinales que potencian la secreción de insulina, determinan una marcada hiperinsulinemia que se sigue de un descenso acelerado de los valores plasmáticos de glucosa. (12) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 110 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La hipoglucemia reactiva idiopática, considerada durante mucho tiempo como un síndrome hipoglucémico de aparición frecuente, consta en realidad de dos síndromes: Uno, raro, de verdadera hipoglucemia que se acompaña de manifestaciones clínicas neurogénicas, disminución posprandial de la glucemia y recuperación de las alteraciones tras la ingesta hidrocarbonada, y otro, más común, de seudohipoglucemia en el que la aparición de los síntomas adrenérgicos no se acompaña del descenso de la glucosa plasmática. (3) El mecanismo implicado en el síndrome hipoglucémico verdadero es desconocido, mientras que en la seudohipoglucemia podría existir una liberación aumentada de catecolaminas como respuesta a la ingesta o una sensibilidad exagerada a estas hormonas tras su liberación posprandial normal.(3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 111 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA No se puede descartar que factores como el estrés o la ansiedad actúen de alguna forma en el desencadenamiento de la seudohipoglucemia. (6) Manifestaciones clínicas Las manifestaciones de la hipoglucemia se pueden agrupar en dos tipos de síntomas: 1) neurogénicos o autonómicos inducidos por la secreción excesiva de catecolaminas y 2) neuroglucopénicos en relación con la disfunción cerebral secundaria a la deprivación de glucosa. (12) Entre los signos y síntomas neurogénicos o autonómicos se encuentran la taquicardia, palpitaciones, ansiedad, temblor, sudoración y la sensación de hambre. (3) La magnitud de estas manifestaciones se encuentra inversamente relacionada con la disminución en la concentración de la glucosa plasmática, de tal forma que a PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 112 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA menor concentración de glucosa más intensos son los síntomas neurogénicos. (9) Los signos y síntomas neuroglucopénicos consisten en cefalea, fatiga o laxitud, trastornos de la conducta, torpor mental, cambios de la personalidad, visión borrosa, diplopía, incoordinación, alucinaciones, amnesia, convulsiones y pérdida de la conciencia, que puede abocar al coma y a la muerte si no se corrige el déficit del aporte de glucosa. Se ha documentado el desarrollo de hipotermia y de fiebre posthipoglucémica tras la instauración de un cuadro neuroglucopénico. (3) Aunque la expresividad clínica de los cuadros hipoglucémicos es muy variable de un sujeto a otro y en ocasiones es difícil adscribir una manifestación determinada a la producción excesiva de catecolaminas o al cuadro neuroglucopénico (pacientes diabéticos tratados o no con insulina, diferentes percepciones de los síntomas), PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 113 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA el patrón sintomático que se desarrolla en un paciente concreto es siempre el mismo. Se ha señalado por algunos autores la falta de un orden cronológico en la evolución de los signos y síntomas hipoglucémicos, pero en individuos normales cuando la concentración plasmática de glucosa alcanza los 50-55 mg/dL se produce la inhibición de la secreción de insulina y se activan las hormonas de contrarregulación, y con cifras de glucosa plasmática de 45 mg/dL se evidencia un trastorno cognitivo como expresión de la disfunción cerebral. (12) Por tanto, puede aceptarse que la secuencia normal como respuesta al descenso de la glucemia está representada por: 1) disminución de la secreción de insulina. 2) incremento en la secreción de las hormonas de la contrarregulación. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 114 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 3) aparición de manifestaciones clínicas. 4) alteración del conocimiento. (12) CAPITULO III EL PÁNCREAS Constituye una glándula de secreción mixta, situada detrás del estómago, por delante de las primeras vértebras lumbares. (8) Posee una doble función, por una parte, existe una porción pancreática con función de glándula exocrina, la cual secreta jugo pancreático y por la otra una porción endocrina que secreta una serie de hormonas peptídicas, como insulina, glucagón, somatostatina y polipéptido pancreático. (9) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 115 /2006 Anatomía y UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Fisiología del páncreas: Figura 3.1 (Robbins Stanley L., Cotran Ramzi S., Kumar Vinay, M.D., Patología Estructural y Funcional El páncreas se encuentra en la parte superior derecha de la cavidad abdominal, en asociación estrecha con el duodeno (Figura3.1). Se compone de dos grandes tipos de tejido, como lo ilustra la Figura 3.2: 1) Los acinos, que secretan jugo digestivo al duodeno, y 2) los islotes de Langerhans, que secretan insulina y glucagón de forma directa a la sangre. (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 116 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Célula beta Figura 3.2 Anatomía fisiológica de un islote pancreático de Langerhans (Guyton Hall, Tratado de Fisiología Médica) Islotes de Langerhans. Figura 3.3 (http://www.monografias.com/trabajos14/insulina/insulina.shtml) El páncreas cuenta con 1 a 2 millones de islotes de Langerhans, cada uno de unos O,3 mm de diámetro; los PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 117 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA islotes se organizan en torno a pequeños capilares, hacía los que vierten sus hormonas. (71) Las masas celulares redondeadas que producen las secreciones endocrinas y que constituyen los islotes de Langerhans, se sitúan entre las masas glandulares exocrinas del páncreas. Las células de los islotes de Langerhans son inervadas por fibras simpáticas y parasimpáticas que influyen en la secreción hormonal. (3) Los islotes contienen tres tipos fundamentales de células, alfa, beta y delta, que se diferencian entre sí por sus características morfológicas y de tinción. Las células beta representan casi el 60 % de la totalidad, se encuentran sobre todo en el centro de cada islote y secretan insulina y amilina, hormona que suele liberarse paralelamente a la insulina, pese a que no se conoce bien su función, contienen gránulos alcohol-solubles. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 118 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Las células alfa, localizadas en la periferia del islote, contienen gránulos alcohol-insolubles y producen glucagón, componen casi un 25 % del total. Y las células delta, que representan un 10%, están situadas entre las alfa y beta, siendo las responsables de la síntesis y secreción de la somatostatina. Además, existe por lo menos otro tipo de célula, la célula PP en cantidad reducida, que produce una hormona de función incierta, denominada polipéptido pancreático. (3-18) Los islotes no tienen conductos, de manera que las hormonas se difunden en los capilares y son transportadas a todas las partes del organismo. (3) La estrecha relación entre estos distintos tipos celulares de los islotes de Langerhans, permiten la regulación directa de la secreción de algunas hormonas por otras. La insulina inhibe la secreción de glucagón, la somatostatina inhibe la secreción tanto de insulina como de glucagón. (6) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 119 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA El páncreas, además de sus funciones digestivas, secreta dos hormonas, la insulina y el glucagón, para la regulación del metabolismo de la glucosa los lípidos y las proteínas. (18) El objetivo principal de este capítulo consiste en exponer las funciones fisiológicas de la insulina y la fisiopatología de algunas enfermedades, causadas por una secreción o actividad anómalas de estas hormonas. INSULINA Frederick Grant Banting, Charles Best, James Collip, y J.J.R. Macleod de la Universidad de Toronto, Canadá, descubrieron la insulina en 1922. El Doctor Banting recibió el Premio Nobel de Fisiología o Medicina por descubrir esta hormona. (59) La insulina (Latín insula, "isla") es una hormona polipeptídica formada por 51 aminoácidos. Es segregada PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 120 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA por las células beta de los islotes de Langerhans del páncreas, en forma de precursor inactivo (proinsulina), el cual pasa al aparato de Golgi, donde se modifica, eliminando una parte y uniendo los dos fragmentos restantes mediante puentes disulfuro. (3) Interviene en el aprovechamiento metabólico de los nutrientes, sobre todo con el anabolismo de los hidratos de carbono. Su déficit provoca la diabetes mellitus y su exceso provoca hiperinsulinismo con hipoglucemia. (71) Ejerce tres efectos básicos en el metabolismo de los carbohidratos: • Aumenta el metabolismo de la glucosa • Disminuye la cantidad de glucosa en la sangre • Aumenta la cantidad de glucógeno almacenado en los tejidos (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 121 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA QUÍMICA Y SÍNTESIS DE LA INSULINA: La insulina es una proteína pequeña; la humana tiene un peso molecular de 5,808. El gen de la insulina humana se localiza en el brazo corto del cromosoma 11. Se compone de dos cadenas de aminoácidos A y B, como muestra la Figura3.5 unidas entre sí por 2 puentes disulfuro entre las cadenas, que conectan A7 con B7, y A20 con B19. Un tercer puente disulfuro que conecta los residuos 6 y 11 de la cadena A. (5) En la mayor parte de las especies no varia la localización de estos puentes disulfuro ni el número de aminoácidos, puede presentarse sustitución de aminoácidos que ocurren en muchas cadenas sin afectar la bioactividad. Cuando se separan las dos cadenas de aminoácidos desaparece la actividad funcional de la molécula de insulina. (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 122 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Figura 3,5 Se sintetiza en las células beta con la maquinaria celular habitual para la síntesis de proteínas. (3) Primero, los ribosomas acoplados al retículo endoplasmico traducen el ARN de la insulina y forman una preprohormona insulínica. Esta preprohormona posee un peso molecular aproximado de 11500 y luego se desdobla en el retículo endoplasmico para formar la proinsulina, con un peso molecular cercano a 9000. (Figura 3,5). (71) Figura 3.5 (http://www.uned.es/pea-nutricion-y-dietetica-I/guia/diabetes/prodinsu.htm) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 123 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Proinsulina: La proinsulina es una molécula formada por una cadena proteínica de 81 aminoácidos, que es precursora de la insulina. Las células Beta del páncreas procesan la proinsulina convirtiéndola en insulina por la sustracción enzimática del péptido C, que es una estructura de 30 aminoácidos que conecta las cadenas A y B (de 21 y 30 aminoácidos, respectivamente). (71) La proinsulina es sintetizada por los ribosomas sobre el retículo endoplasmico rugoso, y la remoción enzimática del segmento líder (pre) del péptido con la formación del enlace disulfuro y el doblez, tienen lugar en la cisterna de este organelo. (19) La molécula de proinsulina es transportada hacia el aparato de Golgi, en donde se inicia la proteolisis (insulina y fragmentos peptídicos) que son empaquetados en los gránulos secretores. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 124 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Figura 3.6 ((http://www.uned.es/pea-nutricion-y-dietetica-I/guia/diabetes/prodinsu.htm) La pro-insulina se rompe por acción de enzimas tipo tripsina dentro del aparato de Golgi, formándose una parte en insulina y la otra queda como pro-insulina. En los gránulos de las células beta se forma un complejo insoluble insulina-cinc que es la forma como se almacena. (71) En los gránulos continua la maduración, conforme atraviesan el citoplasma hacia la membrana plasmática. No obstante, casi una sexta parte del producto final secretado continúa en forma de proinsulina. La proinsulina apenas posee actividad insulinica. (18) Debido a una estimulación apropiada los gránulos maduros se fusionan con la membrana plasmática y descargan su PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 125 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA contenido hacia el líquido extracelular mediante un proceso de exocitosis. (5) La molécula elemental de insulina, contiene dos cadenas polipeptídicas formadas por 51 aminoácidos, unidas entre si por dos puentes disulfuro, presentando la cadena A un anillo disulfuro. El péptido C no tiene ninguna función conocida. Sin embargo, se segrega en las mismas cantidades que la insulina y, de hecho, circula en la sangre más tiempo que la insulina, por lo que es un preciso marcador cuantitativo del funcionamiento de las células Beta. Así, unos niveles normales de péptido C indican una secreción relativamente normal del páncreas. Cuando se secreta insulina a la sangre, circula casi siempre en forma no ligada; su semivida plasmática es de 6 minutos por termino medio y desaparece de la circulación en unos 10 a 15 minutos. Si se exceptúa la parte de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 126 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA insulina que se une a los receptores de las células efectoras, el resto se descompone por la enzima insulinasa, sobre todo en el hígado y en menor medida en los riñones y en los músculos y de forma muy discreta en casi todos los demás tejidos. (3) Su desaparición inmediata del plasma tiene interés porque, a veces, es tan importante desactivar rápidamente el efecto de la insulina como activar las funciones reguladoras de la misma. (6) 1. Preproinsulina (L guía, B cadena, C cadena, A cadena); proinsulina consiste BCA, sin L 2. plegamiento espontáneo 3. Cadenas A y B unidas por puentes sulfuros 4. Guía y la cadena C son cortadas 5. Restos de insulina Figura 3.7 ( www. ADAM.org.com) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 127 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Mecanismo de acción: La acción de la insulina empieza cuando la hormona se une a su receptor glucoproteico específico sobre la superficie de la células blanco. Estas acciones pueden ocurrir en un lapso de segundos o minutos (transporte, fosforilación de la proteína, activación de la enzima e inhibición de la síntesis de RNA) o después de algunas horas (síntesis de proteínas y DNA, así como crecimiento celular). (3) El receptor de la insulina es un heterodímero que consiste en dos subunidades designadas como alfa y beta en la configuración a2b2 unidas por enlaces disulfuro. Ambas subunidades están fosforiladas, cada una con una estructura y función única. La subunidad alfa es completamente extracelular y une a la insulina, la subunidad beta es una proteína transmembranal PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 128 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA que desarrolla la segunda función principal de un receptor la transducción de la señal. La porción citoplasmática de la subunidad beta tiene actividad de tirosina cinasa y un sitio de autofosforilación. (5) El receptor de la insulina es sintetizado y degradado de manera constante y su vida media es de 7 a 12 horas.Se sintetiza en el retículo endoplasmico como un péptido de cadena sencilla y rápidamente se fosforila en el aparato de Golgi. En el ser humano este receptor se localiza en el cromosoma 19. (3) Cuando la insulina se une con el receptor ocurren algunos eventos: • Existe un cambio conformacional del receptor. • Hay un entrecruzamiento de los receptores y forma PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 129 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA microagregados. • El receptor se interioriza. • Se genera una o mas señales. (3) En condiciones en las que los niveles de insulina plasmática son altos por ejemplo en obesidad o acromegalia el número de receptores de insulina se encuentra disminuido y los tejidos blanco se vuelven menos sensibles a la insulina (resistencia a la insulina en la obesidad y en la diabetes mellitus tipo II). (13) Activación de los receptores de las células efectoras por la insulina y efectos celulares resultantes: Para que la insulina inicie sus efectos en las células efectoras, ha de unirse primero y activar una proteína receptora de la membrana, cuyo peso molecular se aproxima a 300 000. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 130 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Este receptor activado y no la insulina es el que desencadena los efectos posteriores. (3) El receptor insulinico (Figura3.8), es una combinación de cuatro subunidades enlazadas a través de puentes disulfuro : dos subunidades alfa que se encuentran totalmente fuera de la membrana, celular, y dos beta, que atraviesan la membrana y sobresalen en el interior del citoplasma. La insulina se une a las subunidades alfa del exterior de la célula pero, debido a su unión con las subunidades beta, las porciones de las subunidades beta que se introducen en el interior de la célula se autofosforilan. (5) De esta manera, se tornan en una enzima activada, una tirocina cinasa local que, a su vez, fosforila muchas otras enzimas intracelulares. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 131 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Figura 3.8. (Guyton Hall, Tratado de Fisiología Médica) El efecto neto es una activación de algunas de estas enzimas y una inactivación de otras. (5) Por este mecanismo, la insulina dirige la maquinaria metabólica intracelular para provocar los efectos deseados sobre metabolismo de los glucidos, lípidos y proteínas. A partir de ése momento, se desconocen los mecanismos moleculares. (5) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 132 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Los efectos finales de la estimulación insulínica son los siguientes: • Pocos segundos después de la unión de la insulina con sus receptores de membrana, las membranas de casi el 80% de las células orgánicas aumentan considerablemente la captación de glucosa en particular las de las células musculares y adiposas, pero no así las de la mayoría de las neuronas encefálicas. La glucosa, que se transporta en mayor cantidad a la célula, se fosforila de inmediato y sirve de sustrato para todas las funciones metabólicas habituales de los hidratos de carbono. Se cree que la aceleración del transporte de glucosa es consecuencia de una translocación de numerosas vesículas intracelulares, a las membranas de la célula; estas vesículas portan, dentro de sus propias membranas, varías moléculas de proteínas transportadoras de glucosa, que se unen a la membrana PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 133 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA celular y facilitan el paso (captación) de glucosa al interior de la célula. Cuando deja de haber insulina, las vesículas se desprenden de la membrana celular en unos 3 a 5 minutos y regresan al interior de las células; este ciclo se repite tantas veces como sea necesario.(3;5;7) • La membrana celular se vuelve más permeable para muchos aminoácidos, los iones potasio y los iones fosfato, cuyo transporte al interior de la célula se incrementa. (3) • En los 10 a 15, minutos siguientes, se observan efectos más lentos que cambian la actividad de muchas más enzimas metabólicas intracelulares. Estos efectos se deben, sobre todo a una variación en la fosforilación enzimática. (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 134 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA • Durante algunas horas e incluso días tienen lugar efectos aún más tardíos. Estos obedecen a los cambios, en la velocidad, de traducción de los ARN mensajeros dentro de los ribosomas para dar nuevas proteínas, e incluso, (los efectos más tardíos) a un cambio de las velocidades de transcripción del ADN del núcleo celular. A través de estas acciones, la insulina modela de nuevo gran parte de la maquinaria enzimática celular hasta conseguir sus objetivos metabólicos. (3) LA INSULINA Y SUS EFECTOS METABÓLICOS PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 135 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Figura3.9 (http://www.uned.es/pea-nutricion-y-dietetica-I/guia/diabetes/prodinsu.htm) Cada uno de estos tipos de células del cuerpo, utilizan la glucosa de una manera diferente. Este uso está determinado por el sistema enzimático específico de cada una. (71) Históricamente, la insulina se ha asociado con el azúcar en la sangre y, ciertamente, esta hormona ejerce efectos profundos sobre el metabolismo de los hidratos de carbono. Sin embargo, las causas habituales de muerte entre los enfermos diabéticos metabolismo lipídico, se deben por a alteraciones ejemplo acidosis del y arteriosclerosis. Además, la menor capacidad de síntesis de proteínas de los pacientes con una diabetes prolongada determina una atrofia de tejidos y múltiples alteraciones funcionales. (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 136 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Por tanto, es evidente que la insulina, influye en el metabolismo de los lípidos de las proteínas casi tanto como en el de los glúcidos. La secreción de insulina se asocia con la abundancia energética. En otras palabras, cuando el régimen de alimentación dispone de alimentos energéticos suficientes, en particular de un exceso de hidratos de carbono y de proteínas, se secreta mucha insulina. Así sucede, sobre todo, en el caso del exceso de hidratos de carbono. A su vez, la insulina desempeña una función primordial para almacenar la energía sobrante. (71) Si se consumen hidratos de carbono en exceso, se almacenan principalmente como glucógeno en el hígado y en los músculos. También determina un depósito de grasa en el tejido- adiposo. Además, el exceso de hidratos de carbono, que no se almacena como glucógeno, se transforma por estímulo de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 137 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA la insulina en grasas que se depositan en el tejido adiposo. Si el exceso es de proteínas, la insulina ejerce un efecto directo para que las células absorban más aminoácidos y los transformen en proteínas. Por último, inhibe la descomposición de las proteínas intracelulares. Efectos de la insulina sobre el metabolismo de los hidratos de carbono. La insulina es la principal hormona que regula los niveles de glucosa en sangre. Su función es controlar la velocidad a la que la glucosa se consume en las células del músculo, tejido graso e hígado. (71) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 138 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Fuente http://www.uned.es/pea-nutricion-y-dieteticaI/guia/diabetes/prodinsu.htm Inmediatamente después de consumir una comida rica en hidratos de carbono, la glucosa que se absorbe en la sangre induce una secreción rápida de insulina. Por su parte, la insulina provoca una captación rápida, almacenamiento y aprovechamiento de la glucosa por casi PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 139 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA todos los tejidos del organismo, pero sobre todo por los músculos, tejido adiposo e hígado. La insulina favorece la captación y el metabolismo musculares de la glucosa. Durante gran parte del día, la energía para el tejido muscular no depende de la glucosa sino de los ácidos grasos. La principal razón es que la membrana muscular en reposo es muy poco permeable a la glucosa, salvo que se estimule la fibramuscular por la insulina; la cantidad de insulina secretada entre las comidas es muy reducida para propiciar una entrada importante de glucosa dentro de las células musculares (miocitos). (59;71) Sin embargo, existen dos situaciones en las que el músculo consume mucha glucosa. Una de ellas es el ejercicio moderado e intenso. Para esta utilización de la glucosa no se necesitan grandes cantidades de insulina porque las fibras musculares que se ejercitan se tornan permeables a la glucosa. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 140 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA El segundo estado en el que el músculo consume mucha glucosa son las horas siguientes a las comidas, en esta fase, la concentración sanguínea de la glucosa se eleva y el páncreas secreta mucha insulina. La insulina «extra» induce un transporte rápido de la glucosa al miocito. Por eso, el míocito utiliza glucosa en lugar de ácidos grasos en este periodo. Efecto facilitador cuantitativo de la insulina del transporte de glucosa por la membrana de la célula muscular. (59) La Figura 3.10 muestra el efecto cuantitativo de la insulina, que facilita el transporte de glucosa por la membrana del miocito. En la parte curva inferior rotulada como «control» se presenta la concentración de glucosa libre medida dentro de la célula y se comprueba que es prácticamente de cero, pese a que la concentración extracelular se eleva hasta casi 750 mg/100 mL. En cambio, la curva rotulada PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 141 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA como «insulina» revela que la concentración intracelular de glucosa aumenta hasta 400 mg/100 mL cuando se añade insulina. Así pues, está claro que la insulina puede acelerar el transporte de glucosa al interior de la célula muscular en reposo, por lo menos, 15 veces. (3;59) FIGURA 3.10 Efecto favorecedor de la insulina de la entrado de glucosa en la célula muscular. Nótese que, cuando falta insulina (control), la concentración intracelular de glucosa se mantiene casi en cero, a pesor de la elevada glucosa extracelular (Tomado de Park. Morgón, Koji, Smith: enEisenstein (ed): The Biochemical Aspects of Hormone Action;Bostón, Littie, Brown.) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 142 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La insulina facilita la captación, el almacenamiento y la utilización de glucosa por el hígado: El glucógeno del hígado es otra forma de almacenamiento de glucosa. Es mucho más fácil disponer del glucógeno para obtener energía que de los triglicéridos, que primero tienen que ser convertidos en ácidos grasos y, posteriormente, en cuerpos cetónicos. El hígado controla estas conversiones y también convierte los aminoácidos en glucosa si es necesario. Aunque la insulina no sea necesaria para el transporte de la glucosa al hígado, afecta directamente la capacidad del hígado para aumentar la captación de la glucosa al reducir el valor de glucogenólisis (la conversión de glucógeno en glucosa), aumentando la síntesis de glucógeno, y disminuyendo el valor de gluconeogénesis. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 143 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Uno de los efectos más importantes de la insulina es el depósito casi inmediato de glucógeno en el hígado a partir de casi toda la glucosa absorbida después de una comida. Luego entre las comidas cuando ya no se dispone de alimento y la glucemia empieza a descender, la secreción de insulina disminuye con rapidez y el glucógeno hepático se transforma de nuevo en glucosa, que se libera otra vez a la sangre para evitar que la glucemia baje demasiado. (18;71) El mecanismo por el cual la insulina facilita la captación y depósito de glucosa en el hígado comprende varias etapas casi simultáneas: 1. La insulina inactiva la fosforilasa hepática, enzima encargada de descomponer el glucógeno hepático en PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 144 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA glucosa. Con ello, impide la descomposición del glucógeno ya almacenado por los hepatocitos. 2. Aumenta la captación de la glucosa sanguínea por el hepatocito, para ello aumenta la actividad de la enzima glucocinasa una de las que provoca la fosforilación inicial de la glucosa tras su difusión al hepatocito. La glucosa una vez fosforilada queda, atrapada de forma pasajera dentro del hepatocito, porque no puede difundir de nuevo fuera la membrana celular. 3. La insulina aumenta, la actividad de las enzimas favorecedoras de la síntesis de glucógeno en particular de la glucógeno sintasa, responsable de la polimerización de los monosacáridos para formar las moléculas de glucógeno. El efecto neto de todas estas acciones es un incremento del glucógeno hepático. El glucógeno puede aumentar hasta un total aproximado de 5-6% de la masa hepática, PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 145 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA que equivale prácticamente a 100 gramos de glucógeno almacenado en todo el hígado.(59;71) Cuando termina una comida y la glucemia empieza a descender hasta unas cifras bajas, suceden varios acontecimientos por los que el hígado vuelve a liberar glucosa a la sangre circulante: El descenso de la glucemia hace que el páncreas reduzca la secreción de insulina. La falta de enumerados insulina revierte anteriormente todos para el los efectos depósito de glucógeno; en particular, cesa la nueva síntesis de glucógeno en el hígado y se evita la captación de más glucosa de la sangre por el hígado. La falta de insulina junto con el incremento del glucagón, activa la enzima fosforilasa, que determina la descomposición del glucógeno en glucosa-fosfato. La enzima glucosa fosfatasa, inhibida previamente por PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 146 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA la insulina, se activa ahora por la falta de la hormona y provoca la liberación de la glucosa de su radical fosfato, con lo que la glucosa libre difunde de nuevo a la sangre. (3;5;71) Así pues, el hígado elimina la glucosa de la sangre cuando ésta se acumula en exceso después de una comida y la devuelve cuando la concentración de glucosa en sangre se reduce entre las comidas. De ordinario, casi el 60% de la glucosa de las comidas se deposita, como se ha indicado, en el hígado y luego se devuelve. La insulina propicia la conversión del exceso de glucosa en ácidos grasos e inhibe la gluconeogénesis hepática: Si la cantidad de glucosa que entra en el hepatocito es superior a la que se puede depositar como glucógeno o utilizar para el metabolismo hepatocítico local, la insulina PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 147 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA fomenta la conversión de todo este exceso de glucosa en ácidos grasos. Luego, estos ácidos grasos se empaquetan como triglicéridos dentro de lipoproteínas de muy baja densidad, que son transportadas por la sangre al tejido adiposo para depositarse como grasa. (3;5) La insulina inhibe la neoglucogénesis. Para ello, reduce la cantidad y la actividad de las enzimas hepáticas necesarias para este proceso. Sin embargo, parte del efecto está mediado por una acción de la insulina que reduce la liberación de aminoácidos del músculo y de otros tejidos extrahepáticos y a su vez, la disponibilidad de los precursores necesarios para la gluconeogénesis.(3) Falta de efecto de la insulina sobre la captación y utilización de glucosa por el encéfalo: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 148 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA El encéfalo se diferencia mucho de casi todos los demás tejidos del organismo, puesto que la insulina posee un efecto mínimo sobre la captación o utilización de la glucosa. En cambio, las células encefálicas son permeables a la glucosa y pueden aprovecharla sin intermediación de la insulina. Las células encefálicas también se diferencian bastante del resto en que normalmente sólo consumen glucosa para la energía y en que pueden aprovechar los demás sustratos energéticos como las grasas, pero con dificultades. Por tanto resulta esencial mantener la glucemia por encima de determinados valores críticos, y ésta es una de las funciones principales del sistema regulador de la glucemia. Si la glucemia es baja en exceso, hasta el intervalo de 20 a 50 mg/100ml aparecen síntomas de shock hipoglicemico PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 149 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA que se caracterizan por irritabilidad nerviosa progresiva con sincope, crisis convulsivas e incluso coma. (5;59) Efecto de la insulina sobre el metabolismo de los hidratos de carbono en otras células: La insulina aumenta el transporte de glucosa y su utilización por casi todas, las demás células del organismo (con excepción de las encefálicas), de manera análoga a como altera el transporte y el uso de glucosa por las células musculares. Con respecto al metabolismo de la insulina, las células del músculo tienen dos funciones primarias: • Convertir la glucosa en la energía que necesita el músculo para funcionar. • Servir como un depósito de proteína y glucógeno. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 150 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Como el tejido graso, el músculo necesita que la insulina facilite el transporte de la glucosa a través de la membrana de la célula. La célula del músculo tiene sus enzimas propias para controlar los dos caminos metabólicos hasta la glucosa: su conversión en energía contráctil y su conversión en glucógeno. Cuando el nivel de glucosa en sangre es normal, la insulina también influye sobre las enzimas de las células del músculo al favorecer la captación de aminoácidos e impedir la utilización de la proteína propia. Efecto de la insulina sobre el metabolismo lipídico: La función primaria de la célula del tejido adiposo es almacenar energía en forma de grasa. Estas células contienen enzimas únicas que convierten la glucosa en triglicéridos y posteriormente los triglicéridos en PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 151 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA ácidos grasos, que son liberados y convertidos en cuerpos cetónicos según el hígado los va necesitando. Tanto la conversión de glucosa a triglicéridos como la ruptura de los triglicéridos a ácidos grasos son regulados por la insulina. La insulina también inhibe la lipasa, un enzima que descompone la grasa almacenada en glicerol y ácido grasos. (59;71) Por lo tanto, regulando la captación de glucosa en las células grasas, la insulina influye en el metabolismo de las grasas. En ausencia de insulina, las células grasas segregan de forma pasiva la grasa almacenada en grandes cantidades, por lo que no se metabolizan completamente y conducen al diabético a la cetoacidosis. Pese a no resultar tan visibles como los efectos sobre el metabolismo de los hidratos de carbono, las acciones de la insulina sobre el metabolismo lipídico resultan igual de importantes a largo plazo. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 152 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Llama la atención el efecto a largo plazo de la falta de insulina, que produce una aterosclerosis marcada a menudo con infartos de miocardio, ictus cerebrales y otros accidentes cerebrovasculares. (3;5;59) La insulina favorece la síntesis y el depósito de lípidos: La insulina ejerce diversos efectos que determinan el depósito de lípidos en el tejido adiposo. En primer lugar, aumenta la utilización de la glucosa por casi todos tejidos orgánicos y reduce automáticamente la utilización de la grasa, es decir, ahorra lípidos. No obstante, la insulina fomenta la síntesis de ácidos grasos sobre todo cuanto mas hidratos de carbono se ingieran; estos se emplean de inmediato para la energía y aportan el sustrato para la síntesis de grasas. (59) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 153 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Casi toda la síntesis tiene lugar en los hepatocitos; luego los ácidos grasos son transportados desde el hígado por las lipoproteínas de la sangre a las células adiposas, donde se almacenan. Los factores que incrementan la síntesis de ácidos grasos en el hígado son: 1. La insulina acelera el transporte de glucosa a los hepatocitos. Una vez que la concentración hepática de glucógeno alcanza un 5 a 6%, ésta se inhibe y previene la síntesis continuada de glucógeno. A continuación toda la glucosa adicional que ingrese en el hepatocito es la disponible para la síntesis de grasas. Primero, la glucosa se descompone hacía piruvato por la vía glicolítica y el piruvato se convierte después en acetil Coenzima A el sustrato para la síntesis de ácidos grasos. 2. Con el ciclo del ácido cítrico se forma un exceso de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 154 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA iones citrato e isocitrato, cuando se utilizan cantidades exageradas glucosa con fines energéticos. Estos iones ejercen después un efecto directo dé activación de la Acetil Co A carboxilasa enzima necesaria para carboxilar la acetil-CoA y formar maloniÍ-CoA, como en la primera etapa de la síntesis de ácidos grasos. 3. Casi todos los ácidos grasos se sintetizan, después dentro del propio hepatocito y se emplean para formar triglicéridos, la forma habitual en que se deposita la grasa. Estos se liberan desde los hepatocitos a la sangre con las lipoproteínas La insulina activa liproteina lipasa de las paredes capilares del tejido adiposo que desdobla de nuevo los triglicéridos hacia los ácidos grasos requisito para su absorción en las células adiposas donde se transformas de nuevo en triglicéridos y se almacenan. (3;71) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 155 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La insulina cumple otros dos efectos importantes necesarios para que se deposite la grasa en las células adiposas. • Inhibe la acción de la lipasa, sensible a esta hormona. Esta es la enzima que hidroliza los triglicéridos ya depositados en las células adiposas. Así pues, inhibe la liberación de ácidos grasos del tejido adiposo hacia la sangre circulante. • Fomenta el transporte de glucosa a las células adiposas a través de la membrana celular de la misma forma que el transporte hacía los miocitos. Parte de la glucosa se emplea luego para la síntesis de diminutas cantidades de ácidos grasos, pero lo que es más importante, también se forman grandes cantidades de alfa-glicerol fosfato. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 156 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Esta sustancia suministra glicerol que se une con los ácidos grasos para dar los triglicéridos, forma en que se deposita la grasa en las células adiposas. Así pues, cuando falta insulina, se bloquea incluso el depósito de grandes cantidades de los ácidos grasos transportados desde el hígado con las lipoproteínas. El déficit de insulina aumenta el uso metabólico de la grasa: Todos los aspectos sobre la descomposición de los lípidos y su uso con fines energéticos se estimulan mucho cuando falta insulina. (5;59) Este hecho sucede de forma normal entre las comidas, porque la secreción de insulina es mínima, pero puede agravarse en la diabetes mellitus, dado que la secreción de insulina es casi nula. Los efectos resultantes son éstos: • El déficit de insulina provoca una lipólisis de la grasa almacenada, con liberación de los ácidos grasos PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 157 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA libres. Cuando falta insulina, se invierten todos los efectos de la insulina que promueven el depósito de la grasa. El más importante es que la enzima lipasa sensible a la insulina de las células adiposas se activa de manera intensa. Con ello se hidrolizan los triglicéridos almacenados y se liberan enormes cantidades de ácidos grasos de glicerol a la sangre circulante. (59;71) La consecuencia es que las concentraciones plasmáticas de los ácidos grasos libres empiezan a aumentar a los pocos minutos. Estos ácidos grasos libres se transforman luego en el sustrato energético principal de casi todos los tejidos orgánicos, además del encéfalo. • El déficit de insulina aumenta las concentraciones plasmáticas de colesterol y de fosfolípidos: El exceso de ácidos grasos del plasma, junto con la falta de insulina, PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 158 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA favorece también la conversión hepática de algunos de los ácidos grasos en fosfolípidos y colesterol, dos de los principales productos del metabolismo lipídico. (28) Estas dos sustancias junto con el exceso de triglicéridos que se crea en ese momento en el hígado, son descargadas a la sangre con las lipoproteínas. A veces, las lípoproteínas del plasma se triplican cuándo falta insulina con lo que la concentración total de lípidos plasmáticos alcanza varias unidades porcentuales en lugar de la cifra habitual de 0,6%. • El consumo exagerado de grasas durante la falta de insulina provoca cétosis y acidosis. La falta de insulina también causa una síntesis exagerada de ácido acetoacético en los hepatocitos, con el efecto siguiente: en ausencia de insulina, pero en presencia de un exceso de ácidos grasos en los hepatocitos, se activa el PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 159 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA mecanismo de la carnitina para el transporte de los ácidos grasos a las mitocondrias. (28;59) Dentro de las mitocondrias, la oxidación beta de los ácidos grasos tiene lugar con gran rapidez y se liberan enormes cantidades de acetil CoA, gran parte de este exceso de acetil Co A se condensa después para formar ácido acetoacético que a su vez se libera a la sangre circulante. Casi todo este ácido pasa a las células periféricas convirtiéndose de nuevo en acetilCoA y utilizándose con fines energéticos de la manera habitual. Al mismo tiempo, la falta de insulina reduce la utilización de ácido acetoacético por los tejidos periféricos. Así pues, el hígado libera tanto ácido acetoacético que los tejidos no llegan a metabolizarlo, a veces alcanza cifras de 10 mEq/L o más, que representan un grave estado de acidosis orgánica. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 160 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Parte del ácido acetoacético también se convierte en ácido beta hidroxibutirico y acetona. Estas dos sustancias, junto con el ácido acetoacético pueden producir cetoacidosis. (3;5;7) El ácido acetoacético y el ácido hidroxibutírico pueden ocasionar acidosis grave y coma, con el resultado frecuente de muerte, en la diabetes grave. Efecto de la insulina sobre el metabolismo de las proteínas y sobre el crecimiento: La insulina facilita la síntesis y el depósito de proteínas, en las horas siguen a una comida, si la sangre circulante que tiene un exceso de nutrientes, no sólo se depositan hidratos de carbono y grasas en los tejidos sino también proteínas; para ello se precisa la insulina. (3) El modo en que la insulina facilita el depósito de proteínas no se conoce tan bien como los mecanismos de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 161 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA almacenamiento de la glucosa y de los lípidos. A continuación, se exponen algunos hechos conocidos: • La insulina estimula el transporte de muchos aminoácidos al interior de las células. Entre estos aminoácidos, cabe destacar la valina, la leucina, la isoleucina, la tirosina y la fenilalanina. Así pues, la insulina comparte con la hormona de crecimiento la capacidad de aumentar la entrada de aminoácidos en la célula. Sin embargo, los aminoácidos sobre los que opera no son necesariamente los mismos. • La insulina aumenta la traducción del RNA mensajero, es decir, la síntesis de nuevas proteínas. Por vías desconocidas, la insulina activa la maquinaria ribosómica. Cuando falta insulina los ribosomas dejan de trabajar; la insulina actúa casi como un mecanismo de encendido-apagado. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 162 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA • Durante un periodo aún mas largo la insulina aumenta, aun mas la velocidad de transcripción de determinadas secuencias del ADN de los núcleos celulares, con lo que se forman mayores cantidades de ÁRN y prosigue la síntesis de proteínas en particular, se favorece la formación de una vasta red de enzimas para el almacenamiento de los hidratos de carbono, lípidos y proteínas. • La insulina inhibe, el catabolismo de las proteínas con lo que reduce la velocidad de liberación de los aminoácidos de las células, sobre todo de las células musculares. capacidad Posiblemente de la esto insulina se para debe a reducir la la descomposición habitual de las proteínas por los lisosomas celulares. • Dentro del hígado, la insulina deprime la tasa de gluconeogénesis de esta manera, reduce la actividad PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 163 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA de las enzimas gluconeogenéticas, los sustratos más utilizados para la síntesis de glucosa mediante gluconeogénesis son los aminoácidos del plasma, con esta supresión de la gluconeogénesis se conservan los aminoácidos para su depósito corporal en forma de proteínas. En resumen, la insulina facilita la síntesis de proteínas y evita su descomposición. (3;7;9) La carencia de insulina determina un descenso de las proteínas y un aumento de los aminoácidos en el plasma: Casi todo el deposito de proteínas se detiene cuando falta insulina. El catabolismo de las proteínas aumenta, la síntesis de proteínas cesa y se vierten enormes cantidades de aminoácidos al plasma. La concentración plasmática de aminoácidos aumenta mucho y casi todo el exceso de aminoácidos se emplea bien directamente como fuente energética o bien como PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 164 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA sustrato de la gluconeogénesis. Esta descomposición de los aminoácidos da lugar, por último, a una mayor eliminación de urea en la orina. La disminución resultante de las proteínas (caquexia) es una de las secuelas más graves de la diabetes mellitus intensa. Puede determinar una debilidad extrema, así como alteración de numerosas funciones orgánicas. (3) La insulina y la hormona del crecimiento interactúan de manera sinérgica para propiciar el crecimiento. La insulina se necesita para la síntesis de las proteínas y por tanto, resulta tan esencial para el crecimiento de los animales como la propia hormona de crecimiento. En definitiva, parece que ambas hormonas operan de manera sinérgica estimulando el crecimiento y que cada una cumple una función especial diferente de la otra. Quizá, parte de estos hechos (la necesidad de ambas PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 165 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA hormonas) se deba a que cada hormona propicia la entrada de distintos aminoácidos en la célula, si bien todos se necesitan para crecer. (71) Regulación de la secreción de insulina: Un páncreas funcionando normalmente puede fabricar y liberar diariamente de 40 a 50 unidades de insulina. Además, tiene varios cientos de unidades almacenadas y disponibles para ser segregadas cuando se necesitan. El cerebro usa en torno al 25% de la glucosa total de cuerpo. Sin embargo, debido a que el cerebro almacena muy poca glucosa, abastecimiento siempre constante y tiene que controlado haber de un glucosa disponible en la corriente sanguínea. El objetivo es mantener al cerebro funcionando adecuadamente. En este sentido, es de vital importancia que el nivel de glucosa en sangre se mantenga en un rango PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 166 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA de 60 a 120 mg/dl, con el fin de prevenir una falta de suministro al sistema nervioso.(3;9) Factores estimuladores de la biosíntesis y secreción de la insulina: Antes se creía que la concentración sanguínea de la glucosa controlaba casi por completo la secreción de insulina. Sin embargo, a medida que se han conocido mejor las funciones metabólicas de la insulina sobre el metabolismo de las proteínas y de los lípidos, se ha comprobado que los aminoácidos de la sangre y otros factores también desempeñan importantes funciones reguladoras de la secreción hormonal. (3;5) El aumento de la glucemia estimula la secreción de insulina: En el hombre y en muchas otras especies, el estimulo más importante de la síntesis y secreción de insulina es la glucemia. Las células beta se comportan como unos PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 167 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA verdaderos glucostatos, siendo sensibles a pequeñas variaciones en la concentración de glucosa en sangre. La insulina estimula el almacenamiento de glucógeno hepático y la utilización de glucosa en los tejidos extrahepáticos, o en ambos. (3;59) Cuando la glucemia en ayunas es normal, de 80 a 90 mg/100 ml, la tasa de secreción de insulina es mínima, del orden de 25ng/min/kg de peso corporal, cifra con una actividad fisiológica muy discreta. Sin embargo, si la glucemia aumenta de forma repentina hasta dos o tres veces el valor normal y se mantiene así, la secreción de insulina se eleva de forma llamativa en dos etapas, como lo reflejan las variaciones de la insulina plasmática de la Figura 3.11. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 168 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Figura 3.11 aumento de la concentración plasmática de insulina tras la elevación brusca de la glucosa sanguínea hasta 2 o 3 veces su valor normal. Obsérvese el pico inicial rápido de insulina y el incremento tardío pero más acusado y mantenido que tiene lugar de 15 o 20 minutos después. ( Tomado de Park. Morgón, Koji, Smith: enEisenstein (ed): The Biochemical Aspects of Hormone Action;Bostón, Littie, Brown.) • La concentración plasmática de insulina se eleva casi 10 veces en los 3 a 5 minutos siguientes al incremento brusco de la glucemia; esto se debe a un vertido inmediato de la insulina preformada desde las células beta de los islotes de Langerhans. • Sin embargo, esta tasa inicial elevada de secreción no se mantiene, puesto que la concentración de insulina desciende hasta valores intermedios en un plazo de 5 a 10 minutos. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 169 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA • Aproximadamente 15 minutos después del estímulo, la secreción de insulina aumenta por segunda vez y alcanza una meseta en las 2 a 3 horas siguientes, en esta ocasión con una tasa secretora aún mayor que la de la fase inicial. Esta secreción se debe tanto a la liberación añadida de la insulina previamente formada como a la activación del sistema enzimático que sintetiza y libera nueva insulina a partir de estas células. Además de la glucosa, hay otros azúcares que pueden estimular la secreción de insulina, incluyendo la fructosa, ribosa y manosa.(3;7;9;59) Retroacción entre la concentración sanguínea de la glucosa y la tasa secretora de insulina: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 170 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Conforme aumenta la concentración sanguínea de glucosa por encima de 100 mg/100 ml de sangre, la tasa de secreción insulínica se eleva de inmediato y alcanza un máximo del orden de 10 a 25 veces los valores basales para glucemias de 400 a 600 mg/100 mL, como muestra la Figura 3.12. Así pues el incremento de la secreción insulínica tras un estímulo de glucosa es espectacular, tanto por su rapidez como por la elevadísima secreción alcanzada. Además, la secreción de insulina se inactiva casi con la misma celeridad, a los 3-5 minutos del regreso de la glucemia a los valores del ayuno. Figura 3.12 (Tomado de Park. Morgón, Koji, Smith: enEisenstein (ed): The Biochemical Aspects of Hormone Action;Bostón, Littie, Brown.) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 171 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Esta respuesta de la secreción de insulina al aumento de la glucemia constituye un mecanismo retroactivo sumamente importante para regular la glucemia. En otras palabras, todo aumento de la glucemia eleva la secreción de insulina y ésta, a su vez aumenta el transporte de glucosa a las células del hígado, músculo y otros tejidos, reduciendo y normalizando la concentración sanguínea de glucosa. (3) Otros factores que estimulan la secreción de insulina Las células beta se pueden ver estimuladas por otros factores como: • La presencia de aminoácidos, concretamente arginina o leucina entre otros. • Algunas hormonas gastrointestinales importantes como la gastrina, la secretina, la colecistocinina y el PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 172 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA péptido inhibidor gástrico (que parece el más potente de todos) aumentan la secreción de insulina de forma moderada. • Las Catecolaminas son potentes inhibidores de la secreción. • El sistema parasimpático es estimulador y el simpático es inhibidor • El glucagón pancreático es un potente estimulador de la liberación, pero una pequeña parte se debe a los niveles de glucosa. • Los antagonistas hormonales de la insulina incluyen hormona del crecimiento, prolactina, corticotrofina, glucocorticoides, lactógeno placentario, adrenalina y hormona tiroidea. (59;71) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 173 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Papel de la insulina y de otras hormonas en el “cambio” entre el metabolismo de los hidratos de carbono y de los lípidos. De la exposición anterior queda claro que la insulina fomenta la utilización de los hidratos de carbono con fines energéticos y reduce el uso de los lípidos. A la inversa, la falta de insulina lleva a la utilización de los lípidos y a la exclusión de la glucosa, salvo por el tejido encefálico. Más aún, la señal que controla este mecanismo de cambio es en esencia, la concentración sanguínea de glucosa. Si la glucemia se reduce, se suprime la secreción de insulina y los tejidos utilizan la grasa con fines energéticos, con excepción del encéfalo. Si aumenta la glucemia, se estimula la secreción de insulina y se utilizan los hidratos de carbono en lugar de los lípidos; el exceso de la glucosa sanguínea se deposita en PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 174 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA forma de glucógeno hepático, grasa hepática y glucógeno muscular. (3;30) Por lo tanto, una de las funciones más importantes de la insulina corporal consiste en controlar cuál de estos dos alimentos será utilizado, de un momento a otro, por las células con fines energéticos. Se conocen, como mínimo, otras cuatro hormonas que también influyen en este mecanismo de cambio: la hormona de crecimiento de la adenohipofisis, el cortisol de la corteza suprarrenal, la adrenalina de la médula suprarrenal, y el glucagón de las células alfa de los islotes pancreáticos de Langerhans. Tanto la hormona de crecimiento como el cortisol se liberan en respuesta a la hipoglucemia, y ambos inhiben la utilización celular de la glucosa, mientras que fomentan el uso de los lípidos. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 175 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Sin embargo, los efectos de estas dos hormonas se instauran lentamente y suelen tardar varias horas en alcanzar su expresión máxima. (3) La adrenalina resulta muy necesaria para elevar la glucosa plasmática en los períodos de estrés, cuando se excita el sistema nervioso simpático. Sin embargo, la adrenalina opera de forma distinta a otras hormonas, puesto que aumenta al mismo tiempo la concentración plasmática de los ácidos grasos. Las causas de estos efectos son: 1) la adrenalina ejerce un efecto glucogenolítico muy potente en el hígado y a los pocos minutos libera grandes cantidades de glucosa a la sangre. 2) además, posee un efecto lipolítico directo sobre las células adiposas, porque activa la lipasa sensible a la PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 176 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA insulina de los tejidos adiposos y aumenta también mucho la concentración sanguínea de ácidos grasos. Desde el punto de vista cuantitativo, el estímulo de los ácidos grados es mucho mayor que el de la glucemia. Así pues, la adrenalina estimula en particular la utilización de los lípidos en situaciones tan estresantes como el ejercicio, el shock circulatorio y la ansiedad. (3;5;71) ALTERACIONES DEL METABOLISMO DE LA INSULINA Hipoinsulinismo. El Hipoinsulinismo origina el padecimiento conocido como diabetes sacarina, que es el más común en las enfermedades endocrinas, una enfermedad metabólica que afecta a muchas funciones corporales. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 177 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Un signo de diabetes sacarina es la concentración anormalmente elevada de glucosa en la sangre o hiperglucemia; ésta, a su vez, provoca que la glucosa sea eliminada por la orina, circunstancia llamada glucosuria. Debido a que es incapaz de satisfacer sus necesidades energéticas, el cuerpo empieza a consumir grasas y proteínas. (3;9;12) Síntomas: Hiperglucemia, glucosuria, diuresis Utilización disminuida de los carbohidratos Catabólia y cetogénesis aumentada de las grasas Metabolismo de las proteínas y pérdida de nitrógeno aumentadas Gluconeogénesis Pérdida de peso corporal Polifagia Coma y muerte (9;17) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 178 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Hiperglucemia, glucosuria y diuresis: Incapacidad de las células para utilizar la glucosa disponible Molécula de azúcar no atraviesa la membrana en ausencia de insulina. Disminución de la utilización de glucosa, aumenta los valores de glucemia. Aparece glucosa en la orina. Aumento de la excreción de orina (Poliuria). Sed intensa (Polidipsia). (12;17) Utilización disminuida de los carbohidratos: La mayoría de los tejidos de la economía pierden la capacidad de metabolizar la glucosa. El tejido nervioso y los eritrocitos no necesitan insulina. Obliga al organismo a utilizar como fuente de energía a las proteínas y las grasas. (3) Catabólia aumentada de las grasas y proteínas: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 179 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Al aumentar la catabólia de las grasas se incrementa la concentración de cuerpos cetónicos como cetoacético y betahidroxibutírico en la sangre. Olor característico de la orina y respiración del animal diabético. Pérdida de Na y K. (3) Pérdida de peso, polifagia: Pérdida de peso porque muchas de las sustancias productoras de energía se pierden en la orina. (12) Coma y muerte: Deshidratación, acidosis, cetonemia. (6) Hiperglucemia sintomática. Se produce poliuria seguida de polidipsia y pérdida de peso cuando los niveles elevados de glucosa plasmática causan una glucosuria intensa y una diuresis osmótica que conduce a deshidratación. La hiperglucemia puede causar también visión borrosa, fatiga y náuseas y llevar a diversas infecciones fúngicas y PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 180 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA bacterianas. En la DM tipo II, la hiperglucemia sintomática puede persistir días o semanas antes de que se busque atención médica; en las mujeres, la DM tipo II con hiperglucemia sintomática suele asociarse con prurito debido a candidiasis vaginal. (12) Complicaciones tardías. Las complicaciones tardías aparecen tras varios años de hiperglucemia mal controlada. Los niveles de glucosa están aumentados en todas las células, a excepción de donde existe una captación de glucosa mediada por la insulina (sobre todo en el músculo), produciéndose un aumento de la glicosilación y de la actividad de otras vías metabólicas, que puede ser causada por las complicaciones. La mayoría de las complicaciones microvasculares pueden retrasarse, prevenirse o incluso invertirse mediante un control estricto de la glucemia, es decir, consiguiendo niveles de glucosa en ayunas y posprandiales próximos a la normalidad, que se reflejan en concentraciones casi normales de hemoglobina glucosilada PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 181 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA (Hb A1C). Una enfermedad microvascular como la aterosclerosis puede producir síntomas de arteriopatía coronaria, claudicación, erosión de la piel e infecciones. Aunque la hiperglucemia puede acelerar la aterosclerosis, los muchos años de hiperinsulinemia que preceden a la aparición de la diabetes (con resistencia a la insulina) pueden representar el principal papel iniciador. Sigue siendo frecuente la amputación de un miembro inferior por vasculopatía periférica grave, claudicación intermitente y gangrena. (6;12;13) El antecedente de una retinopatía simple (las alteraciones iniciales de la retina que se observan en la exploración oftalmoscópica o en fotografías de la retina) no altera la visión de manera importante, pero puede evolucionar a edema macular o a una retinopatía proliferativa con desprendimiento o hemorragia de la retina, que pueden causar ceguera. Alrededor de un 85% del total de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 182 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA diabéticos desarrollan con el tiempo algún grado de retinopatía. La nefropatía diabética aparece aproximadamente en 1/3 de los pacientes con DM tipo I y en un porcentaje menor de pacientes con DM tipo II. En los primeros, la TFG puede aumentar inicialmente con la hiperglucemia. Tras unos 5 años de padecer una DM tipo I puede presentarse una albuminuria clínicamente detectable (300 mg/l) que no tiene explicación por otra enfermedad del tracto urinario. La albúmina anuncia una disminución progresiva de la TFG con una alta probabilidad de desarrollar una nefropatía de fase terminal en 3 a 20 años (mediana, 10 años). La albuminuria es casi 2,5 veces más alta en los pacientes con DM tipo I con PA diastólica >90 mm Hg que en los que tienen PA diastólica <70 mm Hg. Por consiguiente, tanto la hiperglucemia como la hipertensión aceleran la evolución a la nefropatía en fase terminal. La nefropatía diabética suele ser asintomática hasta que se desarrolla la nefropatía en PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 183 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA fase terminal, pero puede originar un síndrome nefrótico. La albuminuria y la nefropatía pueden prevenirse o retrasarse con el captopril, un inhibidor de la ECA. A la vez que un tratamiento enérgico de la hipertensión evita el deterioro de la función renal, los inhibidores de la ECA han demostrado sumar beneficios sobre otras clases de antihipertensivos. De hecho, los inhibidores de la ECA evitan la proteinuria en diabéticos hipertensos y no hipertensos. Datos recientes indican que esos fármacos también previenen la retinopatía. (6;12;13) La neuropatía diabética se presenta frecuentemente como una polineuropatía distal, simétrica, de predominio sensitivo que causa déficit sensitivos que se inician y suelen caracterizarse por una distribución en "calcetines y guantes". La entumecimiento, polineuropatía hormigueos diabética y puede parestesias causar en las extremidades y, con menor frecuencia, dolor e hiperestesia PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 184 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA intensa y debilitante de localización profunda. Los reflejos aquíleos suelen estar disminuidos o abolidos. Las mononeuropatías dolorosas y agudas que afectan a los pares craneales III, IV y VI, así como a otros nervios, como el femoral, pueden aumentar en semanas o meses, se presentan con mayor frecuencia en los diabéticos de edad avanzada y se atribuyen a infartos nerviosos. La neuropatía del sistema autónomo se presenta principalmente en diabéticos con polineuropatía y puede causar hipotensión postural, trastornos de la sudación, impotencia y eyaculación retrógrada en los varones, deterioro de la función vesical, retardo del vaciamiento gástrico (a veces con un síndrome posgastrectomía), disfunción esofágica, estreñimiento o diarrea y diarrea nocturna. La disminución de la frecuencia cardiaca en respuesta a la maniobra de Valsalva, o al pasar a la bipedestación, y la ausencia de variación de la frecuencia PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 185 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA cardiaca durante la ventilación profunda son signos de neuropatía autonómica en los diabéticos. (12;13) Las úlceras de los pies y los problemas articulares son causas importantes de patología en la DM. La principal causa predisponente es la polineuropatía diabética; la denervación sensitiva dificulta la percepción de los traumatismos por causas tan comunes como los zapatos mal ajustados o las piedrecillas. Las alteraciones de la sensibilidad propioceptiva conducen a un modo anormal de soportar el peso y a veces al desarrollo de articulaciones de Charcot. El riesgo de infección por hongos y bacterias aumenta debido a la disminución de la inmunidad celular causada por la hiperglucemia y los déficit circulatorios originados por la hiperglucemia crónica. Son muy frecuentes las infecciones cutáneas periféricas y las aftas orales y vaginales. El proceso inicial puede ser una infección micótica que lleva a lesiones interdigitales, grietas, fisuras y PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 186 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA ulceraciones exudativas que facilitan una invasión bacteriana secundaria. (12) Hiperinsulinismo (Hipoglucemia)* Nivel de glucosa plasmática anormalmente bajo que conduce a síntomas de estimulación del sistema nervioso simpático o de disfunción del SNC. El hiperinsulinismo, o secreción de insulina en exceso por las células beta, es causado generalmente por un tumor de las células de los islotes. En tales casos, la glucosa sanguínea disminuye y puede bajar lo suficiente para causar desmayo, coma y convulsiones.(6;9;12) Efectos: Oxidación Eliminación de glucosa Depósito de glucógeno Lipogénesis Vértigo PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 187 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Incoordinación Debilidad muscular Sistema nervioso Temblores Pérdida del conocimiento Convulsiones Disminución moderada de glucosa --- Activa sistema nervioso simpático ----- Liberación de Adrenalina ---Glucogenólisis hepática. Liberación de ACTH ----- Aumenta los valores de glucemia. (12;17) * Tema se trato en detalle en el capitulo anterior PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 188 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA CAPITULO IV BALANCE ENERGÉTICO Y NUTRICIONAL Al hablar de metabolismo energético nos estamos refiriendo al estudio del aporte y gasto de energía indispensable para la realización de todas las funciones de los seres vivos. Metabolismo energético: Para que un organismo vivo cumpla con todas sus funciones básicas tales como la respiración, crecimiento, movimiento, etc.; requiere de una fuente de energía dependiendo de: a. La liberación de energía de los compuestos que la contienen. b. Mecanismos de transducción de la energía PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 189 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Gran parte del metabolismo aprovecha la energía proveniente de los alimentos, esta energía al ser liberada puede transformarse en diversas formas de trabajo mecánico, eléctrico, etc.; o desprenderse directamente como calor. (Figura 4.1) Calor H2O CO2 ATP Degradación de Alimentos Energía ADP Mecánico Eléctrico Trabajo Químico Osmótico CALOR Figura 4.1 : Laguna José, Piña Enrique, Bioquímica de Laguna) En bioquímica y nutrición se emplea como unidad de energía la Kilocaloría (kcal). Una kilocaloría es igual a 1000 calorías, y una caloría es equivalente a la cantidad de calor PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 190 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA requerida para subir 1ºC. (de 14.5 a 15.5ºC) 1 g de agua. (3) VALOR CALÓRICO DE LOS ALIMENTOS Los alimentos pueden medirse por sus calorías, o sea, por el calor almacenado en ellos. El método más común utilizado para medir el valor calórico es la calorimetría directa, empleando la bomba calorimétrica, este es el aparato utilizado para medir el valor energético total de los nutrimentos, y se estima midiendo la cantidad de calor (número de calorías) generado por una cantidad determinada de alimento al ser quemados dentro de dicha bomba (una cámara insulada); es decir, mide el calor de combustión liberado por los alimentos. (3;5) Valores de los Nutrientes: La energía liberada de cada gramo de hidrato de carbono a medida que se oxida a dióxido de carbono y agua es de 4.1 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 191 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Calorías, y la liberada de la grasa es de 9.3 calorías. La energía liberada del metabolismo de las proteínas medias de la dieta a medida que cada gramo se oxida a dióxido de carbono, agua y urea es de 4.35 calorías. Estos valores medios varían, ya que en el tubo digestivo no todas las sustancias se absorben de igual manera, por lo tanto, redondeando dichos valores, la energía media disponible a nivel fisiológico de cada gramo de dichos alimentos es: Hidratos de carbono Grasas Proteínas Calorías 4 9 4 En promedio, un individuo recibe aproximadamente 15% de su energía de las proteínas, un 40% de las grasas, y un 45% de los hidratos de carbono. (5;65) Si se conoce la composición de un alimento, en términos de los hidratos de carbono, proteínas y grasas, estos valores se usan para estimar su valor calórico. Por ejemplo, PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 192 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA el valor calórico de medio aguacate mediano que contiene aproximadamente 6.5 gramos de hidratos de carbono, 2.4 gramos de proteínas y 18.4 gramos de grasas, puede calcularse como sigue: (65) Hidratos de Carbono Proteínas Grasas 6.5mg x 4 2.4mg x 4 18.4mg x 4 TOTAL = = = = 26. 0 Calorías 9.6 Calorías 156.6 Calorías 201.2 Calorías Necesidades diarias de proteínas: Diariamente se degradan y utilizan para producir otras sustancias químicas 20 a 30 gramos de proteínas corporales; por lo tanto, todas las células deben continuar formando nuevas proteínas que tomen el lugar de aquellas que se han destruido, por lo que se hace necesario un aporte de proteínas con la dieta. Una persona media puede mantener un depósito normal de proteínas siempre que el aporte diario este por encima de 30 a 55 gramos. Sin embargo algunas proteínas tienen cantidades inadecuadas de ciertos aminoácidos esenciales PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 193 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA y por tanto no se pueden utilizar para formar las proteínas corporales, denominadas proteínas dichas proteínas parciales, y son cuando las están presentes en grandes cantidades en la dieta, la necesidad diaria de proteínas en la dieta es mucho mayor de lo normal. Las proteínas de origen animal son más completas que las de origen vegetal. (3;27;65) Hidratos de carbono y grasas como “ahorradores de proteínas”: Cuando la dieta de un individuo contiene abundancia de hidratos de carbono y grasas, casi toda la energía del cuerpo deriva de estas dos sustancias y poca lo hace de las proteínas. Por tanto, los hidratos de carbono y las grasas son ahorradores de proteínas. (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 194 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Medición de la energía producida por el cuerpo (gasto calórico): El metabolismo representa el conjunto de reacciones físicas y químicas que tienen lugar en las células de los tejidos vivos, mediante el cual se produce y mantiene material viviente organizado, e incluye la utilización de las sustancias nutricias (hidratos de carbono, grasas y proteínas) con el fin de producir energía útil para las funciones vitales del organismo. (3;65) Metabolismo total (MT): en estado de equilibrio, la producción de energía en el organismo iguala a la energía dispersada en forma de calor. El gasto de energía depende de los factores constantes relacionados con el metabolismo basal y de los variables dependientes de la actividad muscular o del consumo alimenticio. Entre estos últimos destaca la acción dinámica específica o efecto termogénico de los alimentos, y la actividad física. (5) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 195 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA En resumen podemos decir que: MT = MB + ETC + AF Siendo estas: Metabolismo Basal (MB): es la cantidad mínima de calorías necesarias para que puedan realizarse todas las funciones esenciales y las reacciones químicas mientras la persona está descansando o en un estado de quietud. La TMB es la parte más grande del metabolismo y representa el 65%-75% de todas las calorías quemadas en un día. Si el peso magro o muscular se pierde en el cuerpo a través de un incremento en el metabolismo proteico, la tasa metabólica basal decrece. Esto sucede a menudo cuando una persona sigue una dieta estricta. El cuerpo es forzado a lo que se conoce como "un balance negativo del nitrógeno", que se refiere a que más proteínas son PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 196 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA pérdidas de las que son reemplazadas debido a una menor cantidad de proteínas/ingreso de energía. Este desbalance causa una pérdida gradual de la masa grasa o muscular y por lo tanto una reducción de la tasa del metabolismo basal. (65) Entre los factores que modifican la intensidad del metabolismo basal tenemos: • Movimiento humano (ejercicio o actividad física): Luego de una sesión de ejercicio, el metabolismo basal se mantiene elevado por un determinado período de tiempo. • Tamaño y constitución del cuerpo: El metabolismo basal es mayor en individuos con una constitución física musculosa, y es menor en personas obesas; esto se debe a que los músculos son tejidos relativamente activos en comparación con el tejido adiposo, el cual es de escasa actividad metabólica. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 197 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA • Efecto termogénico de los alimentos (acción dinámica específica): Después de ingerir una comida aumenta el metabolismo; esto es causado principalmente por las distintas reacciones químicas asociadas con la digestión, la absorción y el almacenamiento de los alimentos en el organismo. • Edad y crecimiento: Los niños tienen un elevado metabolismo basal; esto se debe a la gran intensidad de las reacciones celulares, y a la rápida síntesis de material celular y al crecimiento del organismo. Por el otro lado, en la edad adulta el metabolismo basal desciende porque decrece la masa celular activa y porque en muchos casos aumenta la grasa corporal total. (26;65) • Sexo (Género): Por lo regular, el hombre tiene un mayor metabolismo basal que la mujer, porque éste cuenta con menos cantidad de tejido adiposo y más masa muscular, comparado con la mujer. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 198 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA • Secreción de hormonas por ciertas glándulas endocrinas: La tiroxina aumenta el metabolismo. Si la secreción de esta hormona disminuye, el metabolismo basal se reduce también. Además, la adrenalina (secretada por la médula adrenal) causa una elevación en el metabolismo. • Clima: El metabolismo basal es mucho menor en regiones tropicales que en las frías. • Sueño: Durante el sueno el metabolismo disminuye, debido a un mayor grado de relajamiento muscular y emocional. • Desnutrición: Una desnutrición prolongada puede disminuir el metabolismo drásticamente, debido a la falta de alimento en la célula. • Fiebre: Cualquiera que fuera su causa, la fiebre aumenta el metabolismo basal. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 199 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA • Embarazo: Durante el último trimestre de la embarazada hay un aumento en el metabolismo basal, ya que el feto y la placenta incrementan su actividad metabólica debido a que van creciendo, y porque los tejidos maternales lo hacen de igual modo. Medición de la Energía Gastada: Calorimetría Directa: involucra la medición de la cantidad de calor producido por el organismo durante cierto tiempo. En este método, la cantidad total de calor que liberan las células durante su metabolismo se mide en un calorímetro. Calorimetría Indirecta: el método más sencillo de medir el metabolismo basal en forma indirecta, esto es, mediante la medición del consumo de oxígeno. Se basa en el hecho de que las reacciones metabólicas del cuerpo en que se libera energía depende de un continuo suministro de oxígeno. Se ha estimado que por cada litro de oxígeno que se consuma, 5 kilocalorías se generan cuando los PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 200 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA hidratos de carbono, grasas y proteínas se metabolizan en las células. (65) Efecto térmico de la comida (ETC): el cuerpo usa la energía para digerir y absorber los nutrientes presentes en los alimentos que comemos. La tasa de energía usada por el ETC está alrededor del 10%, que puede incrementarse dependiendo de la composición de cada comida, siendo muy discreto para los carbohidratos, intermedio para las grasas y muy elevado para las proteínas. Actividad física (AF): la cantidad de energía que el cuerpo quema durante las actividades diarias como el ejercicio, la recreación, el trabajo en la oficina, el trabajo en la casa, etc. Las actividades físicas diarias representan el 20-40% de las calorías quemadas cada día. Esta parte varía dependiendo de cuan activo es un individuo cada día. Una persona sedentaria requerirá menos calorías para PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 201 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA mantener su peso en relación a un trabajador que labora en una construcción. (26;65) BALANCE CALÓRICO La Ecuación del Balance Energético Esta ecuación establece que el peso corporal se mantendrá constante cuando la ingesta calórica (la energía química potencial de los alimentos ingeridos diariamente) es igual al gasto calórico (energía gastada durante el transcurso del día). (20;65) Balance Energético = Energía ingresa - Gasto energético Tipos de Balance Calórico (o Energético) Balance Energético: ocurre cuando las calorías ingeridas se aproximan a las calorías gastadas durante el curso del día, manteniéndose de esta manera el peso estable. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 202 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Balance Energético Positivo: en este, se ingieren más calorías que las gastadas, y como consecuencia se aumenta de peso, ya que el exceso de calorías se almacena en forma de grasa en los depósitos del tejido adiposo corporal. Se ha estimado que por cada 3,500 Calorías que se consuman en exceso, l libra de grasa (0.45 kg) se almacena en el cuerpo. Balance Energético Negativo: si por el contrario, el consumo total de calorías es menor en relación al gasto, el individuo pierde peso. Si el déficit energético es de 3,500 Calorías, l libra de grasa se pierde. La pérdida en peso puede ser causado por un aumento en el ejercicio físico o una disminución en el consumo de calorías. (22;26) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 203 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Métodos clínicos y experimentales para determinar la utilización metabólica de las proteínas, los hidratos de carbono y grasas: Es importante determinar las tasas relativas de utilización de las proteínas, hidratos de carbono y grasas, con este propósito se emplean dos métodos principales: 1. Determinación de la tasa de metabolismo proteico en el organismo.- la proteína media de la dieta contiene aproximadamente un 15% de nitrógeno. Durante el metabolismo proteico, aproximadamente el 90% de este nitrógeno se excreta en la orina en forma de urea, ácido úrico, creatinina y otros productos nitrogenados menos importantes. El 10% restante se elimina por las heces. De manera que es posible determinar de forma muy sencilla la tasa de descomposición de proteínas en el organismo, mediante la valoración de la cantidad de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 204 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA nitrógeno en la orina, añadiendo después un 11% por el nitrógeno excretado en las heces, y finalmente multiplicando por 6.25 para determinar la cantidad total de metabolismo proteico en gramos por día. Así; 8 gramos de nitrógeno en la orina cada día significa que se han metabolizado aproximadamente 55 gramos de proteínas. (3) Si la ingesta diaria de proteínas es menor que su metabolismo diario, se dice que la persona tiene un equilibrio de nitrógeno negativo, y su almacén corporal de proteínas decrece cada día. 2. Utilización relativa de grasas e hidratos de carbono “cociente respiratorio”.- cuando los hidratos de carbono se metabolizan con el oxígeno, por cada molécula de oxígeno consumida se forma exactamente una molécula de dióxido de carbono. Esta proporción entre el dióxido de carbono producido y el oxígeno utilizado se denomina cociente PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 205 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA respiratorio, por lo tanto, el cociente respiratorio para los hidratos de carbono es 1. Cuando las células corporales oxidan grasa, se forma aproximadamente 70 moléculas de dióxido de carbono por cada 100 moléculas de oxígeno consumidas; por tanto el cociente respiratorio para las grasas es de 0.7. De forma similar, cuando las células oxidan proteínas, el cociente respiratorio medio es de 0.8. El coeficiente respiratorio en una persona que ingiere una dieta mixta es 0.82. (3;5) Para comprender como se emplea el cociente respiratorio para la determinación de la utilización relativa de los alimentos, debemos considerar el “el cociente de intercambio respiratorio” (salida de dióxido de carbono por los pulmones dividido por la captación de oxígeno durante el mismo periodo). En el periodo de 1 hora o más, el cociente de intercambio respiratorio se iguala exactamente PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 206 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA con el cociente respiratorio medio de las reacciones metabólicas de todo el organismo. Mediante el estudio del cociente respiratorio se han llegado a importantes conclusiones, entre estas tenemos: Inmediatamente después de una comida, casi todo el alimento que se metaboliza son hidratos de carbono, de modo que el cociente respiratorio en ese momento es de 1. De 8 a 10 horas después de una comida, el cuerpo ya ha empleado la mayor parte de los hidratos de carbono de fácil disposición, y el cociente respiratorio se aproxima al del metabolismo de la grasa: 0.7. En la diabetes mellitus no tratada, las células corporales emplean pocos hidratos de carbono bajo cualquier condición, ya que la insulina es necesaria para ello. De modo que cuando la diabetes es grave, el cociente respiratorio permanece la mayoría del PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 207 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA tiempo cercano al del metabolismo de las grasas: 0.7. (3) 3. Valor calórico del oxígeno.- al oxidar carbohidratos hasta CO2 y H2O se produce aproximadamente 5.0 kcal por cada litro de oxígeno utilizado. Cuando se oxidan grasas, 1 litro de oxígeno sirve para producir 4,68kcal., y cuando se trata de proteínas, el valor calórico del oxígeno es de 4,48kcal por litro. En una dieta mixta se obtiene un valor calórico por litro de oxígeno de 4,825kcal. (5) Regulación de la ingesta alimenticia. Hambre: significa ansia de alimento, se asocia a varias sensaciones objetivas, tales como, contracciones rítmicas intensas denominadas contracciones de hambre, o dolores con sensación de estiramiento o torsión llamadas dolores PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 208 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA de hambre. Incluso después de extirpar el estómago, las sensaciones físicas del hambre persisten, y la ansia por el alimento continúa. Apetito: se lo usa a menudo con el mismo sentido que el hambre, habitualmente implica el deseo por un tipo específico de alimento en lugar de alimentos en general. Por lo tanto, el apetito ayuda a una persona a elegir la cantidad de alimento a ingerir. Saciedad: es lo opuesto del hambre, consiste en una sensación de satisfacción en la búsqueda de alimento; es el resultado de una comida satisfactoria, sobre todo cuando los depósitos nutricionales de la persona, el tejido adiposo y el glucógeno, ya están llenos. (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 209 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Centros neuronales de regulación de la ingesta alimenticia: Centros del hambre y de la saciedad.Los núcleos laterales del hipotálamo son los encargados de regular la ingesta alimenticia, por lo que se los conoce como centros del hambre; por el contrario, los centros ventromediales del hipotálamo regulan la saciedad y se conocen como centros de la saciedad. El centro del hambre hipotalámico lateral, actúa mediante impulsos motores, y en especial bajo impulsos emocionales. El centro de la saciedad opera para dar al animal una sensación de satisfacción nutricional, que inhibe de forma secundaria al centro del hambre.(3) Factores que regulan la cantidad de alimento ingerido: Podemos dividir la regulación de la cantidad de alimento ingerido en: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 210 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 1. Regulación de la energía (regulación largo plazo) Un animal que ha sido expuesto a un ayuno prologado durante mucho tiempo y al que se presenta una cantidad limitada de alimento come una cantidad mucho mayor que un animal que ha seguido una dieta regular. Por el contrario, un animal al que se ha forjado a comer durante varias semanas come muy poco cuando se le permite comer de acuerdo a sus propios deseos. De este modo, el mecanismo de control de la ingestión de alimento esta relacionado con el estado nutricional del cuerpo. Algunos factores nutricionales que controlan el grado de actividad del centro del hambre son los siguientes. (3) Efectos de las concentraciones de glucosa, aminoácidos y lípidos sobre el hambre y la ingestión de alimento: las teorías glucostáticas, aminostáticas y lipostáticas. Desde hace tiempo, se sabe que una reducción de la concentración sanguínea PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 211 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA de glucosa produce hambre, lo que ha llevado a la conocida teoría glucostática del hambre y de la regulación de la ingestión de alimentos. Estudios similares han demostrado más recientemente el mismo efecto para la concentración sanguínea de aminoácidos y de productos del metabolismo de los lípidos como los cetoácidos y algunos ácidos grasos, lo que conduce a las teorías aminostáticas y lipostática de la regulación. Interrelación entre la temperatura y la ingestión de alimentos. Cuando un animal se expone al frió, tiende a comer en exceso; cuando se expone al calor, tiende a comer menos. Esto esta producido por la interacción, dentro del hipotálamo, entre el sistema regulador de la temperatura y el sistema de regulación de la ingestión de alimento. Esto es importante porque el aumento de la ingestión de alimento en el frío: 1) aumenta su tasa metabólica, y 2) proporciona más PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 212 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA grasa para el aislamiento, lo que en ambos casos tiende a corregir el estado de enfriamiento. (3) 2. Regulación de la ingestión de alimento (regulación a corto plazo) Cuando el hambre mueve a comer a una persona, se generan mecanismos capaces de lograr que la persona deje de comer cuando ha ingerido alimentos en cantidad suficiente, no se trata del mecanismo de retroacción de energía expuesto anteriormente, porque todo él tarda horas antes de que se absorban cantidades suficientes de factores nutritivos en la sangre para que se produzca la inhibición necesaria de la ingesta de alimentos. Es importante que la persona no coma en exceso, e incluso que coma una cantidad de alimento que se aproxime a sus necesidades nutricionales. Algunas de estas señales o mecanismos de retroacción rápida son los siguientes: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 213 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Llenado gastrointestinal. Cuando el tubo digestivo se distiende, especialmente el estomago y el duodeno, se transmiten señales inhibidoras de estiramiento, principalmente a través del vago, para suprimir el centro del hambre, reduciendo el deseo de comer. Factores humorales (colecistocinina, glucagón, y e hormonales insulina). La colecistocinina (hormona gastrointestinal) liberada en respuesta a la presencia de grasas en el duodeno, tiene un efecto directo sobre los centros de la ingestión de alimentos para reducir una ingestión adicional. La presencia de alimento en el estómago y en el duodeno hace que el páncreas secrete cantidades significativas de glucagón e insulina, que suprimen las señales neurógenas de ingestión de alimento. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 214 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Medida del alimento por receptores orales: cuando una persona con una fístula esofágica come grandes cantidades de alimento, aunque este se pierda de inmediato al exterior, el nivel de hambre disminuye después de haber pasado una cantidad razonable de alimento a través de la boca. Este efecto se produce a pesar de que el tubo digestivo no se llena, por lo tanto factores orales como la masticación, salivación, deglución y el sabor “miden” el alimento a medida que pasa a través de la boca, y después de pasar una cierta cantidad de este, el centro hipotalámico del hambre se inhibe. Sin embargo este tipo de inhibición es mucho menos intensa y duradera que el llenado gastrointestinal, durando entre 20 y 40 minutos. (3) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 215 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA CONTROL DEL PESO Componentes Estructurales Principales del Ser Humano El organismo humano se encuentra constituido fundamentalmente de músculos, huesos y grasa. Dentro de los principales depósitos de grasa corporal tenemos: Grasa Esencial: Es aquella almacenada en el tuétano de los huesos, corazón, pulmones, hígado, bazo, intestinos, músculos y tejidos grasos del sistema nervioso central. Esta grasa se requiere para una función normal en la fisiología del organismo. La grasa esencial en las mujeres es mucho mayor que en los hombres, ya que éstas cuentan con grasa almacenada en las glándulas mamarias y en la región de la cadera (pelvis) y muslos, cuyos depósitos son imprescindibles durante el embarazo y para una normal PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 216 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA función de las hormonas femeninas (de modo que halla una regular menstruación). (32) Grasa Almacenada: Es aquella que se acumula en el tejido adiposo, e incluye los tejidos grasos que protegen los diferentes órganos internos contra cualquier trauma y la grasa subcutánea. En varones, la grasa almacenada abarca un 12% y en las mujeres un 15 % (32) SOBREPESO: Uno de los problemas más comunes asociado al estilo de vida actual es el exceso de peso; este es uno de los principales factores de riesgo en el desarrollo de muchas enfermedades crónicas. El sobrepeso es un estado anormal caracterizado por la acumulación excesiva de grasa en el organismo. El concepto de sí una persona está excedida de peso, varía PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 217 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA con la raza, sexo, edad, época y el lugar. En términos generales es más frecuente en las mujeres y después de los 35 años (aunque puede darse a cualquier edad). (74;75) Los nuevos estudios científicos y ciertos datos estadísticos han demostrado que los riesgos para salud del exceso de grasa corporal pueden estar asociados a pequeños incrementos de peso y no sólo a una obesidad pronunciada. Para determinar el peso adecuado de una persona, se mide simplemente la relación entre peso y altura, que se denomina Índice de Masa Corporal (IMC). El IMC es una útil herramienta que es utilizada comúnmente por médicos y otros profesionales de la salud para determinar la prevalencia de peso por debajo de lo PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 218 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA normal, exceso de peso y obesidad en adultos. Se obtiene dividiendo el peso en kilogramos de una persona entre el cuadrado de su altura en metros (kg/m2). (32;74) Se considera que hay exceso de peso y obesidad cuando el IMC es respectivamente superior a 25 y 30. Normalmente, se considera que un IMC es saludable cuando está entre 18,5 y 25, que es de riesgo cuando es de 25-29 y de alto riesgo cuando es superior a 30. Valores límites del IMC (kg/m²) Peso insuficiente <18,5 Normopeso 18,5 - 24,9 Sobrepeso grado I 25 - 26,9 Sobrepeso grado II 27 - 29,9 Obesidad de tipo I 30 - 34,9 Obesidad de tipo II 35 - 39,9 Obesidad de tipo III (mórbida) 40 - 49,9 Obesidad de tipo IV (extrema) >50 Pero el IMC no nos facilita información sobre la cantidad total de grasa, ni sobre cómo dicha grasa está distribuida en nuestro cuerpo, lo cual es importante, ya que el exceso de grasa abdominal puede tener consecuencias negativas para la salud. (74;75) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 219 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Una forma de determinar la distribución de la grasa es medir el perímetro de la cintura. El perímetro de la cintura no tiene nada que ver con el peso, y es un método simple y práctico de identificar qué personas tienen sobrepeso. Si el perímetro de la cintura es superior a 94-102 cm en el caso de los hombres y a 80-88 cm en las mujeres, significa que hay un exceso de grasa abdominal, que puede suponer un mayor riesgo incluso aunque su IMC sea normal. (74) Según lo que mida el perímetro de la cintura, se divide a estas personas en dos categorías: Las que tienen una distribución androide de la grasa (normalmente conocida como forma de "manzana"), lo que significa que la mayoría de su grasa corporal es intraabdominal y se acumula en el estómago y el pecho, y supone que corran mayor riesgo de desarrollar enfermedades relacionadas con la obesidad. Y las personas con una distribución ginoide de la grasa (normalmente conocida como forma de "pera"), lo que significa que la mayor parte de la grasa corporal está PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 220 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA acumulada en las caderas, los muslos y los glúteos, y supone que pueden aparecer problemas mecánicos (articulaciones, interior de los muslos) en casos extremos. Normalmente, la distribución de grasa en los hombres obesos es en forma de "manzana" y en las mujeres en forma de "pera". (Figura 4.2) (22) Figura 4.2: (www.iml,es) La dinámica del equilibrio energético: El principio fundamental del equilibrio energético es: Cambios en reservas = ingesta energética (calorías) - gasto energético energéticas (grasa) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 221 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Hay varios factores que influyen en el exceso de peso y la obesidad, entre ellos la predisposición genética, los factores medioambientales y conductuales, el envejecimiento, y los embarazos. Lo que está claro es que la obesidad no siempre es consecuencia de un abuso del consumo de alimentos apetecibles, o de la falta de actividad física. También pueden influir los factores biológicos (hormonas, genética), el estrés, los medicamentos y el envejecimiento. (22;64;65;66) Los factores dietéticos y la frecuencia de ejercicio físico tienen una gran influencia en la ecuación del equilibrio energético. De hecho, las características más estrechamente asociadas al aumento de la prevalencia de la obesidad en todo el mundo son las dietas altas en grasas y excesivamente energéticas, y el sedentarismo. La ganancia de peso no es brusca, sino que puede dividirse en tres fases consecutivas: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 222 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA a) Fase estática preobesa: cuando el individuo mantiene un balance positivo pero un peso constante. b) Fase dinámica: se produce un incremento progresivo de peso por el balance energético positivo. Puede durar varios años y muchas veces presenta fluctuaciones a consecuencia de los esfuerzos por recuperar el peso inicial por parte del paciente. c) Fase estática obesa: se recupera el balance energético pero el peso es mayor que en la fase preobesa, y el organismo tiende a mantener el nuevo peso alcanzado. La dieta tiene una fuerte influencia en el balance energético y puede considerarse como el factor modificable más importante. (74) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 223 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA OBESIDAD: Es el estado del organismo caracterizado por exagerada acumulación y almacenamiento de grasa en el cuerpo. Estándares de Obesidad Varones: Mayor o igual a 20% de grasa. Mujeres: De 28% a 30% o más de grasa. Causas de la obesidad Desequilibrio Calórico (Balance Calórico Positivo): El ingreso calórico excesivo y la escasa actividad física es el mecanismo mas importante en la producción de obesidad Anormalidades Endocrinas: El hipotiroidismo reduce el metabolismo basal (y el gasto calórico), PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 224 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA acumulando así exceso de calorías, las cuales se convierten en grasa. Hipercelularidad (Exceso de Adipocitos o Células Grasas): El número de adipocitos (células grasas) tienden a multiplicarse rápidamente si hubo una alimentación excesiva durante los primeros años de vida; ya en la edad adulta, las células grasas quedan fijas, lo cual hace difícil el control de peso. Factores Genéticos: La persona endomórfica (muy redondeada y barrigón) tiende a comer en exceso y a ser obeso, en comparación con el ectomorfo (flaco y frágil) el cual tiende a mantenerse delgado. Problemas Emocionales: Una persona en tensiones o ansiosa trata de aliviar sus problemas a través de la comida, en donde su consumo representa un placentero pasatiempo. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 225 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Tipo de Trabajo: Las amas de casa, los cocineros y aquellos que manipulan alimentos "no pueden resistir la tentación" de picar y probar alimentos constantemente. Pobreza: Algunas familias con poco ingreso económico compran alimentos baratos, los cuales tienden a ser altos en azúcares simples y en grasas saturadas. (22;65) Patrones de Alimentación en el Infante: En algunos ambientes familiares los padres fuerzan la alimentación de sus hijos, aunque sean sanos, quieren verlos "bien gordos". La Familia y Hábitos de Alimentación: Si los padres tienen la costumbre de comer grandes cantidades de alimentos en la mesa y éstos son obesos, dicho ambiente transmite al niño el hábito de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 226 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA comer en exceso y ello resulta posteriormente muy difícil de vencer. Susceptibilidad a desarrollar obesidad: SUSCEPTIBILIDAD GENÉTICA: Se han realizado estudios en familias obesas, gemelos y adopciones con el fin de averiguar el grado de herencia de la distribución grasa y obesidad. Se ha observado una asociación mayor entre gemelos idénticos que en gemelos no idénticos. Estudios en familias han determinado que la herencia genética sería responsable del 30% de la obesidad de un individuo. De la misma forma, el grado de grasa corporal de un individuo adoptado se correlaciona hasta en un 30% con el de sus padres biológicos, pero no lo ha sido con su familia adoptiva. Parece que la herencia genética sería, también, parte responsable de la cantidad de grasa abdominal hasta en un 50-60%. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 227 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Aunque no se conocen todos genes implicados, ni cómo actúan e interactúan para su desarrollo, existen diferentes mecanismos por los que la susceptibilidad genética podría influir en el control del peso corporal: tendencia a un bajo nivel de metabolismo basal, bajo nivel de utilización de grasas por el organismo, pobre control del apetito, sensibilidad a la insulina disminuida, propensión a la actividad física espontánea, composición muscular, etc. (22) SUSCEPTIBILIDAD NO GENÉTICA: a) Sexo: En la mujer existen una serie de procesos fisiológicos que contribuyen a un mayor depósito de grasa en las mujeres, y que son fundamentales para mantener la capacidad reproductiva. En la pubertad las mujeres muestran una preferencia por el consumo de carbohidratos mientras que los varones prefieren el consumo de proteínas; posteriormente se incrementa el PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 228 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA consumo de grasas en ambos sexos, pero es más precoz e intensa en las mujeres. b) Raza: Existen varios grupos étnicos que tienen una especial susceptibilidad al desarrollo de obesidad cuando se exponen a un ambiente inadecuado. Entre éstos destacan los indios y aborígenes de zonas rurales los cuales abandonan su estilo de vida tradicional a favor de una dieta y vida sedentaria propia de la sociedad industrializada. Existen varios periodos de la vida en los que existe una mayor predisposición a la ganancia de peso y el desarrollo posterior de obesidad. En el niño: La nutrición durante la vida intrauterina influye en el tamaño, composición, distribución corporal y capacidad para la utilización de los nutrientes en la vida adulta. Tras el nacimiento, después de un aumento del PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 229 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA peso corporal durante el primer año, el índice de masa corporal disminuye para aumentar nuevamente en el periodo conocido como de rebote adiposo (4 a 8 años); en los niños en los que el rebrote aparece más pronto hay un mayor riesgo de obesidad persistente. En el adulto: El peso suele incrementarse en las mujeres tras los sucesivos embarazos, aunque depende del peso ganado en la gestación. Así existe una ganancia neta de aproximadamente 1 Kg de media respecto del peso antes de la gestación. La menopausia afecta a la ingesta y el consumo energético, sobre todo por disminución de la actividad física. Otras situaciones: El abandono del hábito tabáquico suele producir un incremento de peso, sobre todo en los fumadores importantes (>15 cigarrillos/día), por un menor gasto energético y mayor ingesta para compensar la abstinencia. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 230 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA El consumo de alcohol provoca incremento de peso (sobre todo de grasa abdominal) porque la grasa de los alimentos es acumulada al no ser utilizada por el metabolismo, sin embargo el alcoholismo crónico suele producir bajo peso por déficit alimenticio total. El uso de forma mantenida de diversos fármacos promueve la ganancia de peso: antidepresivos tricíclicos, litio, sulfonilureas, anticonceptivos, insulina, beta-bloqueantes, corticoides, ciertos anticonvulsivantes y neurolépticos, entre otros. (22;66) Clasificación de la Obesidad: A lo largo de los años se han realizado varias clasificaciones de la obesidad. Las diferentes clasificaciones son complementarias y necesarias en la evaluación clínica de cada paciente con obesidad. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 231 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Clasificación celular: Según las características del tejido adiposo. Esta clasificación está en desuso ya que no implica diferente abordaje o riesgo de enfermedad. Se definen dos tipos: Obesidad hipertrófica: se produciría en la etapa adulta y por lo cual no sería susceptible de producirse la multiplicación de las células grasas. Por tanto, el tejido adiposo se caracterizaría por tener adipocitos en número normal pero de mayor tamaño al estar cargados de grasa. Obesidad hiperplásica: aquella que se produce en la etapa de formación del tejido adiposo. Este se caracterizaría por un aumento del número de células grasas, aunque son de un tamaño normal. Se la consideró responsable de la obesidad infantil y de la PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 232 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA adolescencia, y de peor pronóstico que la hipertrófica. (22) Clasificación según el estado nutricional: Depende del IMC (visto anteriormente). Clasificación anatómica: Proviene de finales de los años 1940s. Se basa en la diferente distribución de la grasa. En función de dicha determinación, se distinguen la siguiente clasificación de distribución grasa: Distribución androide, central, visceral o abdominal (forma de manzana): el exceso graso se localiza preferentemente en cara, tórax y abdomen. Distribución ginecoide o periférica (forma de pera): la grasa se acumula fundamentalmente en cadera y muslos. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 233 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Distribución homogénea o generalizada: la grasa se distribuye de forma homogénea. (22) Los peligros de la obesidad: 1. Enfermedades cardiovasculares, accidentes cerebro-vasculares y alteraciones venosas: La obesidad por sí sola constituye un factor de riesgo para presentar enfermedades cardiovasculares (angina, infartos, insuficiencia cardiaca, hipertrofia miocárdica. Se ha observado que el incremento del IMC (mayor o igual a 27 Kg/m2) y la ganancia de peso después de los 18 años se asocia con un aumento del riesgo de enfermedades cerebro-vasculares. En los pacientes con obesidad existen alteraciones en la circulación venosa de retorno así como de la circulación linfática, produciéndose edema y síndrome PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 234 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA varicoso, siendo más frecuente en mujeres con obesidad ginecoide. El riesgo de trombosis venosa profunda aumenta con el peso del individuo, pero sin relación con el tipo de distribución grasa. (47;63) 2. Hipertensión Arterial: La obesidad constituye un factor de riesgo tanto para su aparición como para su progresión. Así, la hipertensión arterial es 2.5 veces más frecuente en pacientes con obesidad que en individuos con peso normal; de la misma forma, aproximadamente el 50% de los hipertensos son obesos. Sin embargo la prevalencia de hipertensión arterial en la obesidad varía con la edad, el sexo y la raza. El riesgo de hipertensión depende de la distribución de la grasa corporal, siendo mayor en aquellos con incremento de la grasa abdominal. Sin embargo, los mecanismos causantes del aumento de presión arterial PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 235 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA en los pacientes obesos todavía no son del todo conocidos. (22;47;63) 3. Diabetes: Son muchos los estudios que relacionan el exceso de peso con un aumento de Diabetes Mellitus tipo 2, siendo la obesidad el factor de riesgo más importante para su desarrollo. La obesidad resistencia a la insulina e incremento de los niveles en sangre de esta hormona secretada por el páncreas; a pesar del incremento de la insulina, ésta no es capaz de normalizar los niveles de glucosa en sangre. Al disminuir el peso mejoran las cifras de glucemia y se optimiza el comportamiento de la insulina. Estos cambios muchas veces ya se producen con pérdidas moderadas de peso, que oscilan entre un 5 y un 10%. (22;33) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 236 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 4. Problemas en el Aparato Respiratorio: la obesidad puede producir alteraciones de la función pulmonar. En general el paciente con obesidad (por el mayor contenido de grasa en la pared torácica) moviliza menos los pulmones, lo que produce una disminución del volumen y de la circulación pulmonar. El problema pulmonar más importante de la obesidad es el Síndrome de Apnea del sueño (SAOS), este aparece entre el 25-40% de los individuos con obesidad mórbida, y en un 10% de la obesidad grave. Es más frecuente en varones y mujeres posmenopáusicas. El SAOS además de empeorar la calidad de vida del paciente puede producir, cuando está evolucionado, insuficiencia respiratoria, hipertensión arterial e insuficiencia cardiaca. (22) 5. Alteraciones articulares y óseas: El exceso de peso provoca alteraciones sobre el sistema esquelético, ya que el sistema osteo-articular no está diseñado para PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 237 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA soportar sobrepesos importantes. La obesidad provoca una erosión constante sobre la articulación, que degenera con mayor rapidez y que da como resultado final una artrosis, sobre todo de rodillas, caderas, tobillos y en columna, sobretodo en mujeres con obesidad de tipo ginecoide, aunque la frecuencia de artrosis en articulaciones que no soportan carga como las manos también está incrementada; en los niños en edad de crecimiento la obesidad puede producir deformidades. En los individuos con obesidad la masa ósea está aumentada, desconociéndose la causa exacta, y disminuye al bajar peso. De tal forma se puede decir que la obesidad protege de la osteoporosis.(22,75) 6. Alteraciones endocrinológicas, reproducción y embarazo: Las alteraciones endocrinológicas son numerosas y afectan a cualquier sistema endocrino. Los sujetos con obesidad pueden mostrar alteración del PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 238 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA metabolismo del cortisol (con un efecto de acumulación de grasas). En los varones con obesidad la producción de testosterona por los testículos puede verse reducida. La mujeres obesas presentan niveles elevados de testosterona, destacando una de las alteraciones ginecológicas más comunes asociada a la obesidad, el llamado síndrome de anovulación crónica o síndrome de ovarios poliquísticos (SOP). La obesidad en el embarazo constituye un factor de riesgo para el desarrollo de diabetes gestacional e hipertensión arterial del embarazo, infecciones del tracto urinario, colelitiasis y complicaciones vasculares como la trombosis venosa. Además, un elevado IMC previo a la gestación, se asocia a una mayor frecuencia de macrosomía (fetos de mayor tamaño a lo normal, de más de 4.0 Kg). (3;22) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 239 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 7. Dislipemia: Las personas obesas, secundariamente al estado de resistencia a la insulina e incremento de los niveles en sangre de insulina, tienden a presentar diversas alteraciones lipídicas: elevación de las concentraciones de colesterol total, colesterol LDL y triglicéridos, y valores bajos de colesterol HDL. Además, el colesterol LDL modifica su estructura hacia partículas pequeñas y densas. Este perfil se asocia a un nivel elevado de riesgo cardiovascular, al facilitarse la aterogénesis (depósitos grasos en la arteria que provocan una disminución de su calibre). La disminución de peso tiende a producir normalización de los parámetros alterados, descendiendo los triglicéridos y el colesterol LDL, y aumentando el colesterol HDL. (3;22) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 240 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 8. Problemas Psicológicos : La persona joven que se sabe gorda tiene un sentido de inferioridad, cree que no puede participar en las actividades sociales y se avergüenza. 9. Alteraciones del aparato digestivo: La colelitiasis es la afección del sistema hepático-biliar más frecuente de la obesidad, sobre todo en la mujer. El riesgo incrementado está en relación con el aumento de producción hepática de colesterol y eliminación de una bilis rica en sales de colesterol, con el mayor tamaño y menos movilidad de la vesícula. La pérdida rápida de peso (más de 1.5 Kg/semana) facilitan la formación de cálculos pudiendo provocar cólicos biliares, por lo que se recomienda la pérdida moderada y progresiva. La esteatosis hepática (hígado graso) se relaciona claramente con obesidad, diabetes e hipercolesterolemia. No causa síntomas, reflejándose PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 241 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA únicamente en los análisis de función hepática por un aumento ligero de las transaminasas. (63) 10. Hiperuricemia: La obesidad se relaciona con un aumento de ácido úrico y éste, a su vez, puede provocar ataques de gota. Parece estar relacionado de forma directa con la elevación de la insulina. 11. Alteraciones oncológicas: La obesidad se asocia a una mayor mortalidad por cáncer de próstata y colon y recto en varones, mientras que en las mujeres (sobre todo posmenopáusicas) la mortalidad se eleva en el cáncer de útero, ovario, endometrio, mama y vesícula biliar. El cáncer de próstata de sujetos obesos es más benigno, determinando un menor crecimiento y frecuencia de metástasis, que en individuos sin obesidad. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 242 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 12. Alteraciones dermatológicas: La aparición de estrías cutáneas es frecuente y reflejan la tensión de la piel por los depósitos de grasa subcutánea. El hirsutismo (incremento en las mujeres de pelo en regiones propiamente masculinas) se produce con mayor frecuencia en mujeres con obesidad abdominal por aumento de la producción de testosterona. La acantosis nigricans se asocia al incremento de hiperinsulinemia, resistencia y a se la insulina caracteriza e por hiperpigmentación de cuello, axila, codos y superficies de extensión de los miembros. (22) El grado de riesgo depende entre otras cosas de la cantidad relativa de exceso de peso, la localización de la grasa corporal, cuánto se ha subido de peso durante la edad adulta y la cantidad de actividad física. La mayoría de estos problemas pueden mejorarse adelgazando un poco PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 243 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA (entre 10 y 15%), especialmente si también se aumenta la actividad física. (22) FALTA DE PESO: Para diagnosticar a una persona con falta de peso, se establecen ciertos criterios, entre ellos se encuentra: Si el peso de la persona está más de 10 cifras por debajo de su peso ideal. Si los huesos asoman por doquier en el cuerpo y los músculos no cubren la espalda. Los músculos y las nalgas con protección elástica. Si la cara tiene apariencia delgada y alargada. El peso bajo puede ser causado por enfermedades crónicas, problemas emocionales, desnutrición, alguna deficiencia en su capacidad para asimilar los nutrimentos, ejercicio/actividad excesiva, falta de apetito, dietas peligrosas - no científicas y anorexia nervosa. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 244 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA La falta de peso puede predisponer la falta de nutrientes en el cuerpo, ocasionando varias condiciones, tales como: Enfermedades respiratorias (tuberculosis). Frecuentes infecciones (por baja resistencia inmunológica). Fatigabilidad. Diarrea. (65;66) CAPITULO V ANÁLISIS PRÁCTICO Muestreo: Se trabajó seleccionando a 82 pacientes que cumplían con las especificaciones planteadas para esta tesis: Tener de 20 a 50 años de edad No haber sido diagnosticados como diabéticos PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 245 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA No encontrarse bajo tratamiento con corticoides o inmunosupresores. Sin embargo, durante el análisis se determinó que dos de los pacientes presentaban niveles elevados de glicemia, por lo que fueron excluidos del grupo de estudio, quedando establecido el tamaño de muestra en 80 pacientes. Las muestras de sangre fueron tomadas a los pacientes en ayunas, el muestreo se dio en el lapso de una semana, recopilando la información de los pacientes en la siguiente hoja de datos: # de muestra Nombre Edad (Años) Sexo Peso (Kg) Estatura (metros) IMC Patologías que presenta el paciente actualmente Una vez recopilados los datos de nombre, edad y si padecen alguna patología, se procedió a pesar y medir a cada uno de los pacientes; se calculó su índice de masa PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 246 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA corporal para posteriormente clasificarlos en dos grupos: pacientes con sobrepeso y pacientes con peso normal. Cada día se tomaba las muestras y se procedía a dejarlas en reposo hasta que se forme totalmente el coagulo, de tal forma que se evite la hemólisis, la cual podía dar lugar a valores erróneos en las pruebas realizadas. Una vez formado el coágulo se procedió a separar los sueros y a realizar los análisis respectivos. Métodos: La determinación de insulina se llevó a cabo en el analizador IMMULITE (Figura 5.1), este equipo emplea como metodología, el Inmunoensayo por Quimioluminiscencia, para realizar estudios de hormonas, marcadores oncológicos, de alergias, anemias y de metabolismo óseo. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 247 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA El sistema IMMULITE es 100% automático, de acceso aleatorio continuo para la realización de inmunoensayos y ensayos inmunométricos quimioluminiscentes. Cuenta con lector de código de barra que reconoce muestras y reactivos y su acceso aleatorio permite incorporar muestras rápidas en cualquier momento sin detener el proceso. Utiliza reactivos de calibración con curvas maestras, lo que aumenta la calidad y confiabilidad de los resultados. Es un método de lectura que se basa en el principio de emisión luminosa a través de una reacción (EnzimaSustrato), esta emisión de luz es medida por un tubo fotomultiplicador en el luminómetro, con lo cual se efectúan lecturas exactas de la energía producida por la reacción. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 248 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA En ciertas mediciones, la sensibilidad analítica es de gran importancia para el diagnóstico, como es el caso del TSH ultrasensible. En este caso el método alcanza una sensibilidad de 0,002 Ul/ml. El sistema IMMULITE utiliza perlas de plástico específicas al ensayo recubiertas de anticuerpo como fase sólida, un reactivo marcado con fosfatasa alcalina y un substrato de enzima quimioluminiscente. La perla esta contenida en una unidad de prueba patentada. La unidad de prueba sirve como el vaso de reacción para la reacción inmune, los procesos de incubación, de lavado y el desarrollo de la señal. El sistema IMMULITE realiza automáticamente todo el proceso de ensayo. Después de incubar la muestra con el reactivo de fosfatasa alcalina, la mezcla de reacción liquida contenida en la unidad de prueba se separa rápidamente de la perla cuando esta se lava y la unidad de prueba gira a gran velocidad sobre su eje vertical. Todo el contenido de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 249 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA los fluidos se transfiere a una cámara de desecho coaxial localizada en la unidad de prueba. La perla queda sin marca residual suelta. La marca limitada se cuantifica mediante un substrato que produce luz y la computadora del sistema elabora informes impresos de cada muestra. El sistema IMMULITE tiene dos modos de operación: estándar y turbo en esencia el modo turbo opera de igual forma que el estándar excepto por que el primer resultado aparece en menor tiempo. Esto permite una verdadera funcionalidad para situaciones de urgencia como los marcadores cardiacos o la detección de embarazo El sistema en modo estándar maneja una capacidad de procesamiento de hasta 120 pruebas por hora, 42 minutos para un ensayo de un ciclo o 72 minutos para un ensayo de dos ciclos y procesa hasta 5 unidades de prueba por cubeta de muestra. En modo turbo su capacidad de procesamiento es de 80 pruebas por hora menor a 15 minutos para un ensayo de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 250 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA un ciclo o menor a 22 minutos para un ensayo de dos ciclos y hasta 5 unidades de prueba por cubeta de muestra. La prueba se realiza como se detalla en el (Anexo # 1) Técnicas: Determinación cuantitativa de Insulina: Número de Catálogo; LKIN1 (100 test). Código del Test: INS Color: Naranja Para su uso en el diagnóstico in vitro con los analizadores IMMULITE e IMMULITE 1000, para la medición cuantitativa de insulina en suero o en plasma heparinizado. (Anexo # 2) Principio del análisis: IMMULITE / IMMULITE 1000 Insulina es un ensayo inmunométrico con dos sitios de unión, quimioluminiscente un fase sólida. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 251 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Toma de la muestra: En la toma de muestras, es muy importante evitar la hemólisis, que puede conllevar resultados extremadamente bajos. Las muestras ictéricas, lipémicas, o ampliamente contaminadas pueden dar resultados erróneos. La centrifugación de las muestras de suero antes de que se forme el coagulo puede ocasionar la presencia de fibrina. Para evitar resultados erróneos debidos a la presencia de fibrina asegurarse que se ha formado el coagulo completamente antes de centrifugar las muestras. Los tubos para recoger sangre de distintos fabricantes pueden producir valores diferentes, dependiendo del material del tubo y de los aditivos. Los tubos que contiene EDTA no son aptos para el análisis ya que producen descenso en los valores. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 252 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Volumen requerido: 100 ul de suero o plasma heparinizado. (El recipiente de la muestre debe contener, como mínimo, 250 ul más que el volumen total requerido.) Ensayo: Para obtener el funcionamiento optimo es necesario realizar, todos los procedimientos del mantenimiento general según lo definido en el manual del operador de IMMULITE o IMMUIITE 1000 Inspeccionar visualmente cada unidad de reacción para asegurarse que hay una bola antes de introducirla en el sistema. El recipiente de la muestra debe contener como mínimo 250 ul más que el volumen total requerido. Cada soporte de recipientes de muestras puede acompañarse de cuatro unidades de reacción como máximo. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 253 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Determinación cuantitativa de glucosa Principio del método: La glucosa oxidasa (GOD) cataliza la oxidación de glucosa a ácido glucónico. El peróxido de hidrógeno (H2O2), producido se detecta mediante un aceptor cromogénico de oxigeno, fenol-ampirona en presencia de peroxidasa (POD): p-D-Glucosa + 02 + H20 → Ácido glucónico + H2O2 H202 + Fenol + Ampirona → Quinona + H2O La intensidad del color formado es proporcional a la concentración de glucosa presente en la muestra ensayada. Significado clínico: La glucosa es la mayor fuente de energía para las células del organismo; la Insulina facilita la entrada de glucosa en las células. La diabetes mellitus es una enfermedad que cursa con una hiperglucémia, PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 254 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA causada por un déficit de insulina. El diagnostico clínico debe realizarse teniendo en cuenta todos los datos clínicos y de laboratorio. (Anexo # 3) VALORES DE REFERENCIA: Suero o plasma: 60- 11Omg/dL = 3,33-6.10 mmol/L Formas de Control: 1. Muestreo: durante el muestreo se selecciono específicamente a los pacientes que cumplieran con las especificaciones planteadas, además se tomo con mucha precisión su talla y peso. Se cuido que las muestras no se hemolizaran para evitar errores en el análisis posterior. 2. Práctica: se realizo la calibración del equipo siguiendo las especificaciones detalladas en el manual. Se verifico las fechas de caducidad de los reactivos. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 255 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Se atempero cada reactivo antes de su uso. Se verifico que cada unidad de análisis se encuentre en buen estado. Se emplearon copas cuyo código de barras se encontraba en perfecto estado. Se realizo duplicados de siete muestras tomadas al azar para corroborar los resultados. # de muestra 6 32 51 55 66 72 79 Primera determinación Insulina uUI/ml 9.8 18.0 5.4 24.7 3.6 3.7 7.6 Duplicado Insulina uUI/ml 9.9 17.8 5.6 25.2 3.3 3.1 7.5 Se utilizo 300 uL de muestra más de lo requerido por la técnica. 3. Análisis de resultados: al analizar los resultados se observo que dos de los pacientes tenían sus niveles de PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 256 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA glucosa considerablemente elevados por lo que se volvió a realizar resultados; dichos el análisis confirmándose los datos fueron descartados por encontrarse fuera de las especificaciones establecidas para el estudio. Para llegar a establecer las conclusiones de nuestro estudio se utilizo análisis estadístico descriptivo, análisis grafico y la prueba T para medias de dos muestras emparejadas corroborando las hipótesis planteadas al inicio del estudio. DATOS OBTENIDOS EN LA PRÁCTICA Tabla #1 # de muestra 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Edad IMC 24 42 20 36 31 21 23 26 42 44 21 35 28 32 31 22.4 29.75 25.86 20.93 25.24 21.84 22.42 23.99 26.66 20.28 23.97 26.26 30.30 24.91 26.12 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA Glicemia (mg/dL) 79.5 83.7 60.6 69.9 70.6 71.6 70.4 62.3 71.6 78.2 68.9 75.4 86.3 71.2 80.5 Insulina (uUI/ml) 4.6 <2 3.1 4.2 16.6 9.8 4.0 6.7 <2 6.4 8.4 9.0 12.8 7.9 10.9 257 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 33 24 23 26 25 24 21 32 36 21 44 43 47 32 22 44 27 28 38 38 45 33 43 44 29 26.65 27.24 27.68 28.54 23.97 20.08 25.25 27.63 25.77 25.16 24.33 26.78 32.68 22.72 22.20 34.48 24.24 24.56 40.26 29.83 27.03 22.22 33.24 30.92 23.72 73.60 82.00 88.00 96.30 92.80 75.40 96.10 82.20 82.20 87.30 90.01 95.30 85.13 91.00 118.50 93.08 101.00 106.9 91.30 94.00 77.70 100.01 101.82 88.90 89.02 4.9 15.1 15.5 13.9 9.7 3.8 5.8 2.8 9.9 15.1 6.8 4.4 4.8 3.7 15.5 22.6 18.0 10.5 27.8 7.8 4.7 3.1 23.1 4.3 6.9 Continuación de la Tabla #1 # de muestra 41 Edad IMC 29.23 Glicemia (mg/dL) 80.31 Insulina (uUI/ml) 11.4 22 42 43 27 26 22.22 27.04 68.75 88.01 5.6 <2 44 45 46 47 48 49 50 51 22 21 24 40 44 30 32 21 21.11 20.38 21.37 33.39 25.39 22.20 28.40 90.20 91.13 94.00 106.33 84.51 86.00 92.26 91.00 3.3 3.5 4.7 16.0 4.1 2.2 9.1 5.4 52 53 54 55 41 29 26 25 25 89.24 86.51 91.90 79.42 64.41 7.7 9.4 15.1 24.7 5.3 73.02 5.2 56 57 30 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 30.72 28.20 30.55 32.16 32.40 23.21 20.41 258 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 25 26 21.75 19.66 19.92 22.79 22.01 26 41 22 20 20.14 19.09 21.64 23.23 25 29 33 36 27.54 23.96 19.48 30.27 24.45 22 26 40 44 45 29.68 22.19 28.76 46 46 47 21.21 34.24 50 41 35.23 27.74 24.92 23.83 44 45 48 63.48 81.39 67.90 69.99 79.99 81.16 65.11 96.76 90.22 73.95 92.78 73.95 90.30 79 81.20 80.80 78.41 72 92 115.30 105.02 77.62 86 5.6 <2 <2 5.0 4.2 5.5 5.6 9.0 3.6 9.8 3.5 4.2 17.2 9.8 3.7 8.3 3.5 7.0 13.9 27.6 8.1 7.6 3.4 ANÁLISIS ESTADÍSTICO DESCRIPTIVO Para realizar el análisis, se dividió a la población por edades, tomando como intervalo 5 años de edad entre cada grupo, obteniéndose los siguientes resultados: Tabla # 2 EDAD 20-25 IMC GLICEMIA INSULINA 23.89 81.84 8.0 3.48 19.09 32.4 13.31 60.6 118.5 5.5 3.1 24.7 ANA. ESTADÍSTICO MEDIA DESVIACIÓN ESTANDAR MÍNIMO MÁXIMO 24.41 84.75 7.8 MEDIA PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 259 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 26-30 31-35 36-40 41-45 46-50 4.14 19.48 32.16 12.72 62.3 106.9 5.1 2 18 25.34 82.70 7.2 2.08 22.22 28.4 10.20 70.6 100.01 4.4 2.8 16.6 29.71 86.85 13.2 6.09 20.93 40.26 12.50 69.9 106.33 7.8 4.2 27.8 27.76 87.19 8.8 4.10 20.28 35.23 12.1 69.99 115.3 7.8 2 27.6 27.15 82.39 6.8 5.56 21.21 34.24 6.92 72 92 4.0 3.4 13.9 DESVIACIÓN ESTANDAR MÍNIMO MÁXIMO MEDIA DESVIACIÓN ESTANDAR MÍNIMO MÁXIMO MEDIA DESVIACIÓN ESTANDAR MÍNIMO MÁXIMO MEDIA DESVIACIÓN ESTANDAR MÍNIMO MÁXIMO MEDIA DESVIACIÓN ESTANDAR MÍNIMO MÁXIMO INTERPRETACIÓN DE RESULTADOS: Según el análisis estadístico descriptivo, basado en la Tabla # 2, tomando los datos de la población en general, podemos deducir que: 1. El IMC tiende ha incrementarse con la edad, presentándose los valores más elevados en la población PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 260 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA comprendida entre los 30 y 40 años de edad, sin embargo, a partir de los 40 años de edad los valores de IMC tienden a estabilizarse. 2. Los valores promedio de glicemia en la población estudiada, se encuentran dentro de los límites normales (80-110mg/dL), sin apreciarse variaciones significativas. 3. Los niveles más elevados de insulina se presentan en la población comprendida entre los 36 y 40 años de edad, la misma que presenta los valores más elevados de IMC, lo cual ratifica nuestra hipótesis: "La secreción de insulina se incrementa a medida de que aumenta el IMC" PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 261 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA GRAFICO # 1 REPRESENTACIÓN DEL IMC SEGÚN LA EDAD IMC 35,00 33,00 31,00 IMC 29,00 27,00 25,00 23,00 21,00 19,00 20 21 22 23 24 25 26 27 28 29 30 31 32 33 35 36 38 40 41 42 43 44 45 46 47 48 50 EDAD IMC EDAD 23.00 24.55 23.70 25.05 22.77 24.08 24.4 23.23 27.43 25.3 31.3 25.68 25.91 24.03 26.26 24.74 35.05 31.83 28.74 28.205 30.01 25.86 27.3 25.475 26.945 23.83 34.24 20 21 22 23 24 25 26 27 28 29 30 31 32 33 35 36 38 40 41 42 43 44 45 46 47 48 50 Datos de Referencia Tabla #1 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 262 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA GRAFICO # 2 VARIABILIDAD DE NIVELES DE GLUCOSA SEGÚN LA EDAD 88 GLICEMIA mg/dL 86 84 EDAD 22.5 27.5 32.5 37.5 42.5 47.5 82 80 GLICEMIA 80.26 83.89 86.97 82.03 84.37 81.84 Datos de Referencia Tabla #1 78 76 22,5 27,5 32,5 37,5 42,5 47,5 EDAD GLICEMIA PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 263 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA GRAFICO #3 VARIABILIDAD DE NIVELES DE INSULINA SEGÚN LA EDAD 12 INSULINA uUI/ml 11 EDAD 22.5 27.5 32.5 37.5 42.5 47.5 10 9 8 INSULINA 6.8 5.9 6 11.8 7.1 7.2 Datos de Referencia Tabla #1 7 6 5 22,5 27,5 32,5 37,5 EDAD PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 42,5 47,5 INSULINA 264 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA ANALISIS GRÁFICO DE LOS RESULTADOS Se dividió a la población por edades (Datos de Referencia Tabla #1), tomando como intervalo 5 años de edad entre cada grupo, obteniéndose los siguientes resultados: 20 – 25 AÑOS Tabla # 3 Edad 20 21 22 23 24 25 IMC 23 24.55 23.70 25.05 22.77 24.08 Glicemia 70.88 84.34 92.36 79.20 82.73 73.04 Insulina 4.3 8 7.6 9.8 7.1 10.2 GRAFICO # 4 VARIACION DEL IMC SEGÚN LA EDAD 20-25 AÑOS 26 25 IMC 24 IMC 23 22 21 20 20 21 22 23 24 25 EDAD GRAFICO # 5 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 265 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA VARIACIÓN DE LA GLICEMIA SEGÚN LA EDAD 20-25 AÑOS GLICEMIA mg/dL 94,00 90,00 86,00 Glicemia 82,00 78,00 74,00 70,00 20 21 22 23 24 25 EDAD GRAFICO # 6 VARIACIÓN DEL INDICE DE INSULINA SEGÚN LA EDAD 20-25 AÑOS 11 INSULINA uUI/ml 10 9 8 7 Insulina 6 5 4 3 20 21 22 23 24 25 EDAD INTERPRETACIÓN DE RESULTADOS: Según las gráficas obtenidas, podemos observar que los pacientes, cuyas edades se encuentran comprendidas entre 20 y 25 años: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 266 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 1. Ningún paciente de este grupo presenta sobrepeso, sin embargo, algunos se encuentran muy cerca del límite máximo (24.9). (Gráfico # 4) 2. Todos los pacientes presentan valores de glicemia dentro de los rangos normales (70-110mg/dL), presentando los valores más elevados los pacientes de 22 años. (Gráfico #5) 3. Los niveles de insulina observados se encuentran dentro de los rangos normales, sin embargo, se observa los valores más elevados en los pacientes de 21, 23 y 25 años, los mismos que a su vez presentaron los valores más elevados de IMC del grupo. (Gráfico # 6) 26-30 AÑOS Tabla # 4 Edad 26 27 28 29 30 IMC 24.40 23.23 27.43 25.30 21.92 Glicemia 80.25 84.87 96.60 90.76 91.38 Insulina 6.6 11.8 11.7 8.4 5.6 GRAFICO # 7 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 267 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA VARIACIÓN DEL IMC SEGÚN LA EDAD 26-30 AÑOS 28 27 26 IMC 25 24 IMC 23 22 21 20 26 27 28 29 30 EDAD GRAFICO # 8 VARIACIÓN DE LA GLICEMIA SEGÚN LA EDAD 26-30 AÑOS GLICEMIA mg/dL 98 94 90 86 Glicemia 82 78 74 70 26 27 28 29 30 EDAD PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 268 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA GRAFICO # 9 INSULINA uUI/ml VARIACIÓN DEL INDICE DE INSULINA SEGÚN LA EDAD 26-30 AÑOS 12,0 11,0 10,0 9,0 8,0 7,0 6,0 5,0 4,0 3,0 Insulina 26 27 28 29 30 EDAD INTERPRETACIÓN DE RESULTADOS: Según las gráficas obtenidas, podemos observar que los pacientes, cuyas edades se encuentran comprendidas entre 26 y 30 años: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 269 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 1. En los grupos de pacientes comprendidos entre 28 y 29 años existe sobrepeso. (Gráfico # 7) 2. Todos los pacientes presentan valores de glicemia dentro de los rangos normales (70-110mg/dL), presentando los valores más elevados los pacientes de 28 y 30 años. (Gráfico # 8) 3. Los niveles de insulina observados se encuentran dentro de los rangos normales, sin embargo, se observa los valores más elevados en los pacientes de 28 y 29 años, mismos que a su vez presentaron los valores más elevados de IMC del grupo. (Gráfico # 9) 4. El nivel de insulina promedio en los pacientes de 27 años se encuentra elevado, debido a que una de las pacientes (muestra # 32) presentaba un nivel de insulina elevado debido a que se encuentra en estado de gestación, lo cual puede alterar los niveles normales de insulina. (gráfico # 9) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 270 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 31-35 AÑOS Tabla # 5 Edad 31 32 33 35 IMC 25.68 25.92 24.03 26.26 Glicemia 75.55 84.17 87.94 75.40 Insulina 13.8 5.9 3.9 9.0 GRAFICO # 10 VARIACIÓN DEL IMC SEGÚN LA EDAD 31-35 AÑOS 28 27 26 IMC 25 IMC 24 23 22 21 20 31 32 33 35 EDAD VARIACIÓN DE LA GLICEMIA SEGÚN LA EDAD 31-35 AÑOS GRAFICO # 11 94,00 GLICEMIA mg/dL 90,00 86,00 Glicemia 82,00 78,00 74,00 70,00 31 32 33 35 EDAD PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 271 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA VARIACIÓN DEL INDICE DE INSULINA SEGÚN LA EDAD 31-35 AÑOS GRAFICO # 12 INSULINA uUI/m 13.0 11.0 9.0 Insulina 7.0 5.0 3.0 31 32 33 35 EDAD INTERPRETACIÓN DE RESULTADOS: Según las gráficas obtenidas, podemos observar que los pacientes, cuyas edades se encuentran comprendidas entre 31 y 35 años: 1. Las tres cuartas partes de la población presenta sobrepeso. (Gráfico #10 ) 2. Todos los pacientes presentan valores de glicemia dentro de los rangos normales (70-110mg/dL), presentando los PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 272 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA valores más elevados los pacientes de 32 y 33 años. (Gráfico # 11) 3. Los niveles de insulina observados se encuentran dentro de los rangos normales, sin embargo, se observa los valores más elevados en los pacientes de 31 y 35 años, los mismos que a su vez presentaron valores elevados de IMC. (Gráfico #12) 36-40 AÑOS Tabla # 6 Edad 36 38 40 IMC 24.75 35.05 31.83 Glicemia 75.35 92.65 98.32 Insulina 8.0 17.8 16.6 IMC VARIACIÓN DEL IMC SEGÚN LA EDAD 36-40 AÑOS 36 34 32 30 28 26 24 22 20 GRAFICO # 13 IMC 36 38 40 EDAD GRAFICO # 14 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 273 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA VARIACIÓN DE LA GLICEMIA SEGÚN LA EDAD 36-40 AÑOS GLICEMIA mg/dL 98,00 94,00 90,00 86,00 Glicemia 82,00 78,00 74,00 70,00 36 38 40 EDAD PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 274 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA GRAFICO # 15 VARIACIÓN DEL INDICE DE INSULINA SEGÚN LA EDAD 36-40 AÑOS 19.0 INSULINA uUI/ml 17.0 15.0 13.0 11.0 Insulina 9.0 7.0 5.0 3.0 36 38 40 EDAD INTERPRETACIÓN DE RESULTADOS: Según las gráficas obtenidas, podemos observar que los pacientes, cuyas edades se encuentran comprendidas entre 36 y 40 años: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 275 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 1. Los pacientes de este grupo presentan un IMC considerablemente elevado, llegando en su mayoría a un franco sobrepeso. (Gráfico #13) 2. Todos los pacientes presentan valores de glicemia dentro de los rangos normales (70-110mg/dL), presentando los valores más elevados los pacientes de 40 años. (Gráfico #14) 3. Los niveles de insulina observados se encuentran dentro de los rangos normales, sin embargo, se observa los valores más elevados en los pacientes de 38 y 40 años, los mismos que a su vez presentaron los valores más elevados de IMC del grupo. . (Gráfico #15) 41- 45 AÑOS Tabla # 7 Edad 41 42 43 44 45 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA IMC 28.74 28.21 30.01 26.80 27.21 Glicemia 91.51 77.65 98.56 88.39 78.84 Insulina 13.4 2.0 13.8 8.9 5.3 GRAFICO # 16 276 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA VARIACIÓN DEL IMC SEGÚN LA EDAD 41-45 AÑOS 30 IMC 28 IMC 26 24 22 20 41 42 43 44 45 EDAD GRAFICO # 17 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 277 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA VARIACIÓN DE LA GLICEMIA SEGÚN LA EDAD 41-45 AÑOS GLICEMIA mg/dL 98.00 94.00 90.00 86.00 Glicemia 82.00 78.00 74.00 70.00 41 42 43 44 45 EDAD PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 278 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA GRAFICO # 18 VARIACIÓN DEL INDICE DE INSULINA SEGÚN LA EDAD 41-45 AÑOS 16.0 INSULINA uUI/ml 14.0 12.0 10.0 8.0 Insulina 6.0 4.0 2.0 0.0 41 42 43 44 45 EDAD INTERPRETACIÓN DE RESULTADOS: Según las gráficas obtenidas, podemos observar que los pacientes, cuyas edades se encuentran comprendidas entre 41 y 45 años: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 279 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 1. Todos los pacientes de este grupo presentan sobrepeso. (Gráfica # 16) 2. Todos los pacientes presentan valores de glicemia dentro de los rangos normales (70-110mg/dL), presentando los valores más elevados los pacientes de 41 Y 43 años. (Gráfica # 17) 3. Los niveles de insulina observados se encuentran dentro de los rangos normales, sin embargo, se observa los valores más elevados en los pacientes de 41 Y 43 años, los mismos que a su vez presentaron los valores más elevados de IMC del grupo. (Gráfica # 18) 46 – 50 AÑOS Tabla # 8 Edad 46 47 48 50 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA IMC 25.48 26.95 23.83 34.24 Glicemia 79.61 78.57 86.00 92.00 Insulina 5.9 5.9 3.4 13.9 280 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA GRAFICO # 19 IMC VARIACIÓN DEL IMC SEGÚN LA EDAD 46-50 AÑOS 36 34 32 30 28 26 24 22 20 IMC 46 47 48 50 EDAD VARIACIÓN DE LA GLICEMIA SEGÚN LA EDAD 46-50 AÑOS GRAFICO # 20 GLICEMIAmg/dL 94.00 90.00 86.00 82.00 Glicemia 78.00 74.00 70.00 46 47 48 50 EDAD PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 281 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA GRAFICO # 21 VARIACIÓN DEL INDICE DE INSULINA SEGÚN LA EDAD 46-50 AÑOS INSULINA uUI/ml 14.0 12.0 10.0 Insulina 8.0 6.0 4.0 2.0 46 47 48 50 EDAD INTERPRETACIÓN DE RESULTADOS: Según las gráficas obtenidas, podemos observar que los pacientes, cuyas edades se encuentran comprendidas entre 46 y 50 años: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 282 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 1. Las tres cuartas partes de los pacientes de este grupo presentan sobrepeso. (Gráfica # 19) 2. Todos los pacientes presentan valores de glicemia dentro de los rangos normales (70-110mg/dl), presentando los valores más elevados los pacientes de 48 y 50 años. (Gráfica # 20) 3. Los niveles de insulina observados se encuentran dentro de los rangos normales, sin embargo, se observa los valores más elevados en los pacientes de 50 años, los mismos que a su vez presentaron los valores más elevados de IMC del grupo. (Gráfica # 21) ANÁLISIS ESTADÍSTICO En base a los datos obtenidos, y tomando en cuenta que se trata de un “Estudio Comparativo” entre dos grupos dados, PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 283 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA hemos considerado pertinente analizar los datos mediante la “prueba T para dos muestra emparejadas” En primer lugar se clasificó a la población de acuerdo a su edad en 6 grupos; posteriormente, estos grupos se subdividieron tomando en cuenta el género de los mismos, obteniéndose los siguientes datos: COMPARACIÓN DEL IMC ENTRE HOMBRES Y MUJERES Tabla # 9 EDAD 22.5 27.5 32.5 37.5 42.5 47.5 IMC ♂ 24.10 25.82 25.32 24.23 28.24 35.43 IMC ♀ 23.31 23.91 25.40 30.88 25.91 26.02 GRAFICO # 22 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 284 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA RELACIONES DEL IMC ENTRE VARONES Y MUJERES 37,00 35,00 VARONES 33,00 MUJERES IMC 31,00 29,00 27,00 25,00 23,00 21,00 19,00 20 25 30 35 40 45 50 EDAD Ho: El IMC de los varones es menor o igual al de las mujeres Hi: El IMC de los varones es mayor o igual al índice de masa corporal de las mujeres a cualquier edad. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 285 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Significación estadística: Prueba t para medias de dos muestras emparejadas varones Media Varianza Observaciones Estadístico t P(T<=t) una cola Valor crítico de t (una cola) mujeres 27.19 25.905 18.53672 6 0.61127959 0.28386764 2.01504837 7.14659 6 Error: 0.05 Considerando que el valor crítico de t es mayor que el estadístico, es decir, que no existen diferencias estadísticamente significativas, se acepta la hipótesis nula como certera, y se rechaza la hipótesis alternativa: El IMC de los varones es menor o igual al de las mujeres. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 286 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA COMPARACIÓN DE NIVELES DE INSULINA ENTRE HOMBRES Y MUJERES Edad Tabla # 10 Insulina (uUI/ml)♂ 22.5 27.5 32.5 37.5 42.5 47.5 Insulina (uUI/ml)♀ 8.1 3.5 5.6 7.0 8.9 5.6 8.4 6.4 16.6 5.2 7.2 GRAFICO # 23 INSULINA uUI/ml RELACIÓN ENTRE NIVELES DE INSULINA EN MUJERES Y VARONES 16,0 14,0 12,0 10,0 8,0 6,0 4,0 2,0 Insulina (uUI/ml)♂ Insulina (uUI/ml)♀ 20 25 30 35 40 45 50 EDAD Ho: Los niveles de insulina en las mujeres son > o = a los de los varones Hi: Los niveles de insulina de las mujeres son < a los de los varones PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 287 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Significación estadística: Prueba t para medias de dos muestras emparejadas varones mujeres 6.62161905 8.408333333 4.52593215 22.50493056 5 5 -0.72747113 0.25361606 2.13184678 Media Varianza Observaciones Estadístico t P(T<=t) una cola Valor crítico de t (una cola) Error: 0.05 Considerando que el valor crítico de t es mayor que el estadístico, es decir, que no existen diferencias estadísticamente significativas, se acepta la hipótesis nula como certera, y se rechaza la hipótesis alternativa: Los niveles de insulina de las mujeres son > o = a los de los varones. COMPARACIÓN DE NIVELES DE GLICEMIA ENTRE HOMBRES Y MUJERES Tabla # 11 Edad 22.5 27.5 Glicemia (mg/dL) ♂ 78.79 80.45 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA Glicemia (mg/dL)♀ 81.73 87.33 288 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 32.5 37.5 42.5 47.5 87.17 71.92 88.64 86.77 92.15 80.10 81.84 GRAFICO # 24 RELACIÓN GLICEMIA vs EDAD EN HOMBRES Y MUJERES 95,00 GLICEMIA mg/dL 90,00 Glicemia (mg/dL) ♂ 85,00 Glicemia (mg/dL)♀ 80,00 75,00 70,00 20 25 30 35 40 45 50 EDAD Ho: El nivel de glicemia en los varones es menor o igual que el de las mujeres. Hi: El nivel de glicemia en los varones es siempre mayor que el de las mujeres Significación estadística: Prueba t para medias de dos muestras emparejadas varones mujeres 81.393 85.6148 45.830345 23.1229412 5 5 -0.89085836 0.21167394 Media Varianza Observaciones Estadístico t P(T<=t) una cola PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 289 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Valor crítico de t (una cola) 2.13184678 Error: 0.05 Considerando que el valor crítico de t es mayor que el estadístico, es decir, que no existen diferencias estadísticamente significativas, se acepta la hipótesis nula como certera, y se rechaza la hipótesis alternativa: El nivel de glicemia en los varones es menor o igual que el de las mujeres. RELACION ENTRE IMC, INSULINA Y GLICEMIA VS EDAD PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 290 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA EN HOMBRES Y MUJERES Tabla # 12 Edad IMC ♂ 22.5 27.5 32.5 37.5 42.5 47.5 25.23 23.08 25.32 24.23 27.38 Glicemia (mg/dL) ♂ 78.79 80.45 87.17 71.92 88.64 Insulina (uUI/ml) ♂ 8.1 3.5 5.6 7.0 8.9 IMC ♀ 20.95 23.42 25.82 30.27 27.07 26.05 Glicemia (mg/dL) ♀ 81.73 87.33 86.77 92.15 80.10 81.84 Insulina (uUI/ml) ♀ 5.6 8.4 6.4 16.6 5.2 7.2 GRAFICO # 25 RELACIÓN IMC e INS vs EDAD EN HOMBRES Y MUJERES IMC ♂ 30,00 IMC ♀ IMC e INS 26,00 22,00 Insulina (uUI/ml)♂ 18,00 Insulina (uUI/ml)♀ 14,00 10,00 6,00 2,00 20 25 30 35 40 45 50 EDAD GRAFICO # 26 RELACION INS-GLICEMIA vs EDAD EN HOMBRES Y MUJERES Glicemia (mg/dL) ♂ 105,00 90,00 Glicemia (mg/dL)♀ INS - GLI 75,00 60,00 Insulina (uUI/ml)♂ 45,00 30,00 Insulina (uUI/ml)♀ 15,00 0,00 20 25 30 35 40 45 50 EDAD PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 291 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA COMPARACIÓN DE NIVELES DE INSULINA EN PACIENTES CON NORMO-PESO Y SOBREPESO Tabla # 13 EDAD 22.5 27.5 32.5 37.5 42.5 47.5 IMC NP 21.69 20.55 23.23 20.93 24.05 22.41 INSULINA NP 5.0 4.1 3.6 4.2 7.5 6.2 IMC SP 31.56 31.36 28.40 28.91 29.25 31.50 INSULINA SP 15.1 8.8 9.1 14.3 7.9 8.7 RELACIÓN DE LA INS EN PACIENTES CON NORMO-PESO Y SOBREPESO GRAFICO # 27 INSULINA uUI/ml 16.0 14.0 12.0 INSULINA NP 10.0 INSULINA SP 8.0 6.0 4.0 2.0 20 25 30 35 40 45 50 EDAD Ho: INS en pacientes con SP es < o = a la INS en pacientes con NP Hi: INS en pacientes con SP es > a la INS en pacientes con NP Significación estadística: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 292 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Prueba t para medias de dos muestras emparejadas Media Varianza Observaciones Estadístico t P(T<=t) una cola Valor crítico de t (una cola) INS PN INS SP 5.09166667 10.6503968 2.19352778 10.0146994 6 6 -3.44270166 0.00919086 2.01504837 Error: 0.05 Considerando que el valor crítico de t es menor que el estadístico, es decir, que existen diferencias estadísticamente significativas, se rechaza la hipótesis nula, y se acepta la hipótesis alternativa como certera: Los niveles de Insulina en pacientes con sobrepeso son mayores a los presentados en pacientes con peso normal. COMPARACIÓN DE NIVELES DE GLICEMINA EN PACIENTES CON NORMO-PESO Y SOBREPESO Tabla # 14 Edad 22.5 27.5 32.5 37.5 42.5 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA Glicemia NP 77.28 82.86 90.61 69.90 78.31 Glicemia SP 85.11 89.21 82.93 86.08 95.05 293 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 47.5 79.60 85.21 GRAFICO # 28 RELACIÓN ENTRE NIVELES DE GLICEMIA vs EDAD EN PACIENTES CON SOBREPESO Y CON PESO NORMAL 100,00 Glicemia NP GLICEMIA mg/dL 95,00 Glicemia SP 90,00 85,00 80,00 75,00 70,00 65,00 20 25 30 35 40 45 50 EDAD Ho: Los niveles de glicemia en pacientes con sobrepeso son < o = a los obtenidos en pacientes con peso normal Hi: Los niveles de glicemia en pacientes con sobrepeso son > a los obtenidos en pacientes con peso normal. Significación estadística: Prueba t para medias de dos muestras emparejadas Media Varianza Observaciones Estadístico t P(T<=t) una cola Valor crítico de t (una cola) Peso normal Sobrepeso 79.7592857 87.2637222 46.5703745 18.7059745 6 6 -2.06470043 0.0469351 2.01504837 Error: 0.05 PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 294 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Considerando que el valor crítico de t es menor que el estadístico, es decir, que existen diferencias estadísticamente significativas, se rechaza la hipótesis nula, y se acepta la hipótesis alternativa como certera: Los niveles de glicemia en pacientes con sobrepeso son > a los obtenidos en pacientes con peso normal. CAPITULO VI CONCLUSIONES Mediante nuestro estudio pudimos determinar que: Los niveles de Insulina en pacientes con sobrepeso son mayores a los presentados en pacientes con peso normal; esto no indica precisamente que los pacientes con sobrepeso presenten valores de insulina superiores a los normales, sino más bien, nos demuestra que esta variación es gradual, a medida que aumenta el ÌMC se va PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 295 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA incrementando los niveles de insulina, tal y como se expuso en el capítulo número 4. Los niveles de insulina de las mujeres son mayores o iguales a los de los varones; esto no se ve influenciado directamente por el índice de masa corporal (se citará posteriormente), sino más bien, a que las mujeres tienden a ser más sedentarias, presentan mayor depósito de grasa en el organismo (caderas y cintura) y a variaciones hormonales propias del género. El IMC de los varones es menor o igual al de las mujeres (tomando como referencia la población que partició de este estudio), ya estadísticamente que no significativas existen que variaciones determinen lo contrario. Pese a que los niveles de IMC presentados en mujeres y hombres de estos no 30 y 40 años difieren considerablemente, deben PATRICIA DELGADO TORRES LORENA BRAVO MEDINA de tomarse como un hecho 296 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA representativo, pues tal variación se puede deber a los cambios hormonales propios de las mujeres a dicha edad. El IMC tiende ha incrementarse con la edad, principalmente porque se dan cambios en el ritmo de vida, cambios hormonales propios de la menopausia, las mujeres aumentan de peso después de ser madres, entre otros varios factores. A pesar de lo expuesto anteriormente, dichos valores tienden a estabilizarse a partir de los 45 años. El nivel de glicemia en los varones es menor o igual que el de las mujeres, dicha variación podría deberse principalmente al tipo de dieta de ambas partes, ya que las mujeres tendemos consumir mayor cantidad de carbohidratos y a realizar menos actividad física que los hombres. A demás el hecho de que las mujeres tienden más a realizar las denominadas “dietas rápidas”, hace que la homeostasis propia del organismo se altere y se refleje PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 297 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA como en este caso, con variaciones en los niveles de glicemia. Los niveles de glicemia en pacientes con sobrepeso son mayores a los encontrados en pacientes con peso normal, ya que como se explicó en el capítulo 4, el sobrepeso influye considerablemente en el metabolismo. En estado de gestación los niveles de insulina tienden a incrementarse independientemente del IMC, debido a que en dicho estado, además de incrementarse la masa muscular, la insulina actúa como hormona de crecimiento fenal. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 298 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA RECOMENDACIONES Cuando se realice cualquier análisis en el IMMULITE se recomienda seguir en orden las especificaciones detalladas en el manual. No colocar demasiadas muestras a la vez, ya que en caso de que se produzca algún fallo en el equipo estas se perderían. La medición de concentración de glucosa se debe realizar lo mas pronto posible ya que a medida me transcurre en tiempo los resultados varían considerablemente. Para la determinación de insulina no utilizar sueros hemolizados lipémicos ni ictéridos ya que se producen cambios en los resultados. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 299 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Se recomienda a los pacientes que participaron en este estudio tener una vida mas activa, llevar una mejor selección del tipo de alimentación que consumen para tratar de llegar a un IMC saludable y así evitar futuras complicaciones en su salud. Sería bueno que se continuara realizando este tipo de estudios en grupos de pacientes comprendidos en otras edades, de tal modo que se obtengan datos que demuestren el estado nutricional de la población en general. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 300 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA BIBLIOGRAFÍA 1. De Robertis D.P. Eduardo, Biología Celular y Molecular, Duodécima Edición, Editorial “El Ateneo”, Buenos Aires – Argentina, 1998. 2. Gonzáles Bahamonde Germán, Métodos Estadísticos y Principios de Diseño Experimental, Universidad Central del Ecuador, Quito – Ecuador. 3. Guyton Hall, Tratado de Fisiología Médica, Décima Edición, Editorial Mc Graw-Hill Interamericana, Madrid España, 2001. 4. IMMULITE®, Automotor Unmunoasside sistem, Operador's Manual. Copyricht1991-2005 by Dyagnostic Products Corporation. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 301 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 5. Laguna José, Piña Enrique, Bioquímica de Laguna, Quinta Edición, Editorial El Manual Moderno, México D.F. 6. Lebovitz HE., Manual de Resistencia a la Insulina, Editorial Science Press Brasil, Brasil 2003. 7. Murria K. Robert, Mayes A. Meter, Granner Daryl K., Rodwell W. Victor, Bioquímica de Harper, 14ª Edición, Editorial El Manual Moderno, México D.F. 8. Orrego M. Arturo, Fundamentos de Medicina “Endocrinología”, Tercera Edición, Corporación para Investigaciones Biológicas, Medellín Colombia. 9. Robbins Stanley L., Cotran Ramzi S., Kumar Vinay, M.D., Patología Estructural y Funcional, Quinta Edición, Editorial Interamericana, Madrid España, 1992. 10. Segatore Luigi Dr., Diccionario Médico Teide, Editorial Teide, Barcelona España. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 302 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 11. Varios autores, Enciclopedia Autodidáctica Océano, Grupo Editorial Océano, Barcelona España, 1990 12. Varios Autores, Manual Merck, Editorial OCEANO, Barcelona España, 1997. 13. Vera Vargas Francisco Dr., Resistencia a la Insulina y Diabetes Mellitus, Sociedad Ecuatoriana de Endocrinología Núcleo del Guayas, 2004 Páginas de Internet: 14. http://anm.encolombia.com/medicina23201articuloscien.htm 15. http://bvs.sld.cu/revistas/ali/vol15_1_01/ali09101.htm 16. http://cbs.xoc.uam.mx/3rafase/obesidad/unidad3.htm 17. http://elmundosalud.elmundo.es/elmundosalud/2005/11/ 03/oncodudasypreguntas/1131012570.html 18. http://es.wikipedia.org/wiki/Glicemia PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 303 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 19. http://fbio.uh.cu/metabol/metabolismoglucosa.htm 20. http://groups.msn.com/mundociclista/balanceenergtico. msnw 21. http://scielo-mx.bvs.br/scielo.php 22. http://www20.brinkster.com/ladietetica/Tablas/calorias2. htm 23. http://www.abcmedicus.com/articulo/pacientes/1/id/379/ pagina/1/glicemia que_es.html 24. http://www.abcysonline.com/QuimioluminiscenciaEs.asp ?MyParamMenu=30 25. http://www.americanheart.org/presenter.jhtml?identifier= 3018675 26. http://www.anabolandia.com/articulo-gasto-calorico.html 27. http://www.aula21.net/Nutriweb/lasnecesidenerg.htm 28. http://www.buenasalud.com/lib/ShowDoc.cfm?LibDocID =3360&ReturnCatID=344 29. http://www.bvs.sld.cu/revistas/end/vol9_1_98/end06198 .htm PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 304 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 30. http://www.bvs.sld.cu/revistas/end/vol11_1_00/end0510 0.htm 31. http://www.cfnavarra.es/salud/anales/textos/vol21/suple 3/suple9.htm 32. http://www.csalto.net/control%20peso/plan.htm 33. http://www.diabetes.org/espanol/diabetes-tipo2/insulina.jsp 34. http://www.diariosalud.cm 35. http://www.drscope.com/pac/mg-2/5/mg2t5_p43.htm 36. http://www.enbuenasmanos.com/articulos/muestra.asp? art=123 37. http://www.enbuenasmanos.com/articulos/muestraSub. asp?sub=0708 38. http://www.encolombia.com/medicina/sociedadescien/di abetes2042-sobrepeso1.htm 39. http://www.espalda.org/divulgativa/su_espalda/sobrepe so.asp 40. http://www.eufic.org/sp/quickfacts/obesidad.htm 41. http://www.eSDLMS.com PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 305 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 42. http://www.fao.org/docrep/v4700s/v4700s0c.htm 43. http://www.fciencias.unam.mx/Cursos/Biologia/Animales II/horm.html 44. http://www.geocities.com/HotSprings/Spa/2007/concept os_generales_endocrino.htm#_Toc488814293 45. http://www.ilustrados.com/publicaciones/EpyFyupAZVw ByjoaNb.php 46. http://www.indstate.edu/thcme/mwking/steroidhormones.html 47. http://www.infonutricion.com/obesidad/s02_4.htm 48. http://www.kidshealth.org/parent/en_espanol/nutricion/o verweight_obesity_esp.html 49. http://www.klip7.cl/herbalife/info/boletin.htm 50. http://www.labguemes.com.ar/areas.html 51. http://www.labnutricion.cl/257,2,Estado Nutricional Normal 52. http://www.labnutricion.cl/homa_normal.htm 53. http://www.laboratorioramos.com.mx/tecnologia.htm#3 54. http://www.medidores.com/div.medica_dpc_3.html PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 306 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 55. http://www.medidores.com/pdf_medica/Immulite_1000_ MIYMSA.pdf 56. http://www.medilegis.com/BancoConocimiento/R/Rev_ci rugiaN3dic_obesidad/revicionobesidad.htm 57. http://www.monografias.com/trabajos11/quimilu/quimilu. shtml 58. http://www.monografias.com/trabajos14/endocrino/endo crino.shtml 59. http://www.monografias.com/trabajos14/insulina/insulin a.shtml 60. http://www.nlm.nih.gov/medlineplus/spanish/ency/article /003101.htm 61. http://www.nutrar.com/detalle.asp?ID=1262 62. http://www.ondasalud.com/edicion/noticia/0,2458,15067 4,00.html 63. http://www.roemmers.com.ar/infovida/obesidad.asp 64. http://www.saludalia.com 65. http://www.saludmed.com/Salud/Nutricion/BalEnerg.htm l PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 307 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 66. http://www.saludmed.com/Salud/Nutricion/Obesidad.ht ml 67. http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S 071775262004000100008& lng=es&nrm=iso&tlng=es 68. http://www.solociencia.com/medicina/sistemaendocrino-generalidades.htm 69. http://www.solociencia.com/medicina/sistemaendocrino-hormonas.htm 70. http://www. studentconsult.com 71. http://www.uned.es/pea-nutricion-y-dieteticaI/guia/diabetes/prodinsu.htm 72. http://www.uv.es/garoa2/estresyadiccion/psicoendocrin ologia.htm 73. http://www.wachtower.org.langvajes/español/medicacare-and/blood.htm 74. http://www.xenicare.com.ec/calorias_gasto_metabolism o.php 75. http://www.zonadiet.com/alimentacion/l-sobrepeso.htm PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 308 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA ANEXO # 1 MANEJO DEL IMMULITE La prueba se realiza de la siguiente manera: 1. Se enciende el equipo IMMULITE, se deja que este se caliente por el lapso aproximado de 1 hora. 2. Se procede a encender el monitor y la impresora, y se los deja así por unos 40 minutos aproximadamente. 3. Mientras esperamos que los equipos estén listos para poder utilizarlos, se debe reconstituir los reactivos (se explicará posteriormente) 4. Una vez transcurrido el tiempo necesario para la utilización del equipo, procedemos a calibrar el equipo, para esto, primeramente debemos ingresar los códigos de barras de los reactivos que vamos a emplear, colocamos los reactivos en el carrusel de reactivos asegurándonos de que las tapas estén bien abiertas. Cargamos la plataforma de carga con las copas que contienen los reactivos (LINL,LINH, LINC1,LINC2) y las PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 309 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA muestras a procesar. Junto a cada copa colocamos una unidad de análisis (perlas). 5. Una vez cargado el carrusel, procedemos a ingresar los datos de las muestras a analizar, presionamos Data Entry, e ingresamos los siguientes datos: Número de copa Nombre del paciente (o reactivo en la calibración) Fecha Observaciones: aquí se debe especificar la prueba a realizar 6. Cuando ya se haya ingresado todos los datos, presionamos “Go” en el panel del IMMULITE, las muestras empezaran a correr y aparecerá el siguiente cuadro en la pantalla: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 310 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 7. Esperamos a que el equipo realice la prueba y nos permita visualizar los resultados. ANEXO # 2 Determinación cuantitativa de Insulina: Resumen y Explicación del Test: La insulina humana es una hormona polipeptídica producida por las células beta del páncreas y cuya función es ser el principal regulador del almacenamiento y la producción de hidratos de carbono. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 311 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Su secreción se estimula por un aumento de la cantidad de glucosa en sangre, produciendo niveles más altos de insulina y más asimilación de la glucosa por parte de los tejidos, seguido de un descenso del nivel de insulina al mismo tiempo que disminuye el nivel de glucosa. En muchas situaciones, especialmente en casos de insulinoma y diabetes, esta relación se deteriora. La insulina tiende a circular a niveles inadecuadamente elevados un pacientes con tumores pancreáticos que segregan insulina, por lo que dichos tumores pueden provocar hipoglucemia; por consiguiente, los inmunoensayos de insulina a veces empleados junto con dosis provocadoras de tolbutamida o calcio desempeñan un papel fundamental en la identificación de insulinomas. El hallazgo de hipoglucemia en estado de ayunas asociado con una concentración de insulina en suero inadecuadamente elevada se considera diagnostico. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 312 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Los niveles de insulina no figuran en la subclasificación de diabetes elaborada por el National Diabetes Data Group (Grupo Nacional de Datos sobre la Diabetes). Sin embargo, cuando se obtienen en el transcurso de un análisis de tolerancia a la glucosa, parecen tener algún valor pronóstico para predecir los beneficios de la terapia de insulina y la probabilidad de progresión para la dependencia de insulina y complicaciones características de la diabetes. La aplicación de inmunoensayos de insulina a pacientes que ya estén siguiendo una terapia con insulina se complica, porque esta terapia provoca la formación de anticuerpos anti insulina que pueden interferir con el ensayo. Ciclos de incubación: 1 x 60 minutos. Volumen requerido: 100 ul de suero o plasma heparinizado. (El recipiente de la muestre debe contener, como mínimo, 250 ul más que el volumen total requerido.) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 313 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Conservación: 7 días a 2-8°C, o 3 meses a -20ºC Reactivos: y Mantener a 2--8°C. y Siga las precauciones universales y manipule todos los componentes como si fueran capaces de transmitir agentes infecciosos. Sustrato quimioluminiscente: evitar la contaminación y exposición a la luz directa del sol. Agua: Use agua destilada o desionizada. Materiales Suministrados: Los componentes representan un juego completo. Las etiquetas incluidas en la caja son necesarias para el ensayo. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 314 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Unidades de análisis de Insulina (LIN1) Cada unidad etiquetada con un código de barras contiene una bola recubierla de anticuerpos monoclonales murinos antiinsulina. Estable a 2-8ºC hasta la fecha de caducidad. LKIN1: 100 unidades. Esperar a que las bolsas de las unidades de análisis alcancen la temperatura ambiente antes de abrirlas. Ábralas cortando por el extremo superior, dejando el borde del cierre de cremallera intacto. Vuelva a cerrar las bolsas herméticamente para protegerlas de la humedad. Vial de reactivo de Insulina (LIN2) Con códigos de barras. 7,5 ml de fosfatasa alcalina (de intestino de ternera) conjugada con anticuerpos policlonales de oveja anti-insulina y fosfatasa alcalina (de intestino de ternera) conjugada con anticuerpos monoclonal de ratón antiinsulina en solución tampón, con conservante. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 315 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA Guardar tapado y refrigerado: estable a 2-8°C hasta la fecha de caducidad. Se recomienda utilizarlo antes de que pasen 30 días después de abrirlo cuando se guarda según lo indicado. LKIN1: 2 viales Ajustadores de Insulina (LINL, LINH) Dos viales (bajo y alto) de insulina liofilizada en una matriz sérica no humana, con conservante. 30 minutos como mínimo antes de su uso, reconstituir cada vial añadiendo 4, 0 ml de agua destilada o desionizada. Mezcle por agitación o inversión suave. Alicuotar y congelar; estable a -20ºC durante 60 días tras su reconstitución. LKIN1: 1 juego. Controles de Insulina (LINC1-2) Dos viales de insulina liofilizada en una matriz serica no humana con conservante. Reconstituir cada vial añadiendo 4, 0 ml de agua destilada o desionizada. Mezcle por PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 316 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA agitación o inversión suave. Alicuotar y congelar; estable a -20ºC durante 60 días tras su reconstitución. Componentes del Kit que se suministran por separado: Diluyente de Insulina (LINZ) Para la dilución manual de las muestras de los pacientes. Un vial que contiene humano (con 25 ml de una matriz de suero no conservante), libre de insulina, con conservante. Estable a 2-8ºC durante 30 días después de abrirse, o hasta 6 meses (alicuotados) a -20°C: - LSUBX: Substrato quimioluminiscente - LPWS2: Lavado de sonda - LKPM: Kit de limpieza de sonda - LCHx-y: Soportes de recipientes de muestras (con códigos de barras) LSCP: Recipientes de muestras (desechables) PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 317 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA - LSCC: Tapas para los recipientes de muestras (opcionales) También es necesario: - Pipetas de transferencia de muestras - Agua destilada o desionizada Intervalo de ajuste recomendado: 2 semanas Muestras para control de calidad : usar los controles de insulina del kit Valores esperados: Promedio de 8.9 uUI/ml – 28.4 uUI/ml Cada Laboratorio deberá establecer sus propios rangos Características Analíticas: PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 318 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA - Rango de Calibración: Hasta 300 ulU/ml (WHO NIBSC 1st IRP 66/304). - Sensibilidad: 2 ulU/ml - Efecto de gancho a altas dosis: Ninguno hasta 70 000 ulU/ml. - Precisión: Las muestras fueron analizadas por duplicado durante 20 días, en dos tandas de trabajo por día, para un total de 40 tandas y 80 replicados. - Especificidad- El ensayo es específico para insulina - Bilirrubina: Una ictericia grave (hasta 100 o 200 mg/l de bilirrubina) puede provocar un descenso en los valores. - Hemólisis: Puede causar una bajada de los valores. - Lipemia: la presencia de triglicéridos puede causar una baja de los valores. PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 319 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA ANEXO # 3 Determinación cuantitativa de glucosa Reactivos: R1 Tampón. R2 Enzimas GLUCOSE CAL TRIS pH 7,4. 92 mmol/L Fenol 0,3 mmol/L Glucosa oxidasa (GDO)15000 U/L Peroxidasa 1000U/L (POD) 2,6 mmol/L Patrón primario 100mg/dl acuoso de Material adicional: - Espectrofotómetro o analizador para lecturas a 505 nm. - Cubetas de 1,0 cm de paso de luz. - Equipamiento habitual de laboratorio. Muestras: Suero o plasma, libre de hemólisis; el suero debe separarse lo antes posible del coágulo. Estabilidad: La glucosa en suero o plasma es estable 3 días a 2-8°C, PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 320 /2006 UNIVERSIDAD DE CUENCA FACULTAD DE CIENCIAS QUIMICAS ESCUELA DE BIOQUÍMICA Y FARMACIA 1. Condiciones de! ensayo: - Longitud de onda: ............... 505nm - Cubeta:.... ......................1 cm paso de luz - Temperatura....................... 37°C / 15-25°C 2. Ajustar el espectrofotómetro a cero frente al blanco de agua destilada. 3. Pipetear en una cubeta Blanco Patrón Muestra RT (mL) 1,0 1,0 1,0 Patrón (uL) - 10 -- Muestra (uL) ~ - 10 4. Mezclar e incubar 10 minutos a 37°C ó 30 min a temperatura ambiente (15-25°C). 5. Leer la absorbancia (A) del Patrón y la muestra, frente al Blanco de reactivo. El color es estable como mínimo 30 minutos. Cálculos: (A) Muestra x 100 ( conc patrón) = mg/dL de Glucosa (A)Patrón PATRICIA DELGADO TORRES LORENA BRAVO MEDINA 321 /2006