Pharmaton complex comprimidos efervescentes
Anuncio

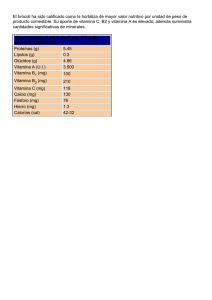
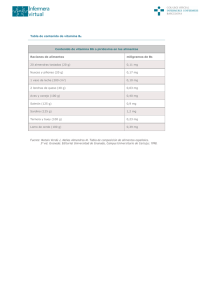
RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO (FICHA TECNICA) 1. NOMBRE DEL MEDICAMENTO PHARMATON COMPLEX comprimidos efervescentes 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por comprimido efervescente Extracto etanólico seco estandarizado de raíz de Panax Ginseng G115 (5:1) 40 mg (equivalente a 1,6 mg de ginsenósidos) Bitartrato de 26 mg deanol………………………………………… Retinol (DOE) (vitamina 1.500UI A)………………………………... (como palmitato de retinol) Mononitrato de tiamina (vitamina B1)……………………... 2 mg Riboflavina (DOE) (vitamina B2)………………………….. 2 mg Hidrocloruro de Piridoxina (vitamina B6)…………………. 1 mg Cianocobalamina (DOE) (vitamina B12)…………………... 1 microgramo Acido ascórbico (DOE) (vitamina 60 mg C)………………………. Colecalciferol (DOE) (vitamina D3)……………………….. 200 UI Alfa-Tocoferol (vitamina 10 mg E)………………………………... (como d-l-alfa-acetato de tocoferol) Nicotinamida 15 mg (DOE)……………………………………….. Pantotenato de calcio 10 mg (DOE)……………………………….. Rutósido 20 mg (DOE)…………………………………………….. (como sulfato de sodio de rutina) Hierro 10 mg ……………………………………………………… (como sulfato de hierro II) Calcio 90,6 mg ……………………………………………………… (como carbonato, glicerofosfato, fluoruro y pantotenato de calcio) Fósforo 70 mg …………………………………………………….. (como glicerofosfato de calcio y de magnesio) Flúor ………………………………………………………. 0,2 mg (como fluoruro de calcio) Cobre 1 mg ………………………………………………………. (como sulfato de cobre II) Potasio ……………………………………………………... (como cloruro de potasio y acesulfamo de potasio) Manganeso ………………………………………………… (como sulfato de manganeso II) Magnesio …………………………………………………... (como glicerofosfato de magnesio) Zinc ………………………………………………………… (como sulfato de zinc) 8 mg 1 mg 10 mg 1 mg Excipientes: (ver relación en 6.1) 3. FORMA FARMACÉUTICA Comprimidos efervescentes 4. DATOS CLÍNICOS 4.1 Indicaciones terapéuticas Prevención de estados carenciales de vitaminas y minerales. Estados pasajeros de agotamiento y decaimiento. Convalecencias. 4.2 Posología y forma de administración Vía oral. Adultos y niños mayores de 15 años: La dosis habitual recomendada es de 1 comprimido al día, administrado preferiblemente por la mañana, con el desayuno. En caso necesario puede aumentarse la dosis a 2 comprimidos, uno por la mañana con el desayuno y otro al mediodía con la comida. El comprimido debe disolverse en una cantidad suficiente de agua y esperar a que cese completamente el burbujeo antes de su ingestión. No debe tomarse de forma continuada. 4.3 Contraindicaciones Hipersensibilidad a alguno de los componentes. Trastornos del metabolismo del calcio. Insuficiencia cardíaca, renal, hepática o biliar. Hipertensión. Estados de ansiedad o excitabilidad. Enfermedad de Leber. Hipervitaminosis o exceso de minerales u oligoelementos en sangre u orina, o durante el tratamiento con retinoides o vitamina D. Ulcera gastroduodenal. Epilepsia. Pharmaton Complex no debe administrarse a niños menores 15 años. 4.4 Advertencias y precauciones especiales de empleo No exceder la dosis recomendada (ver apartado 4.2. Posología y forma de administración y apartado 4.9. Sobredosificación) No deberá utilizarse como sustitutivo de una dieta equilibrada y deberán tenerse en cuenta otros aportes de vitaminas y minerales. Se debe tener en cuenta el contenido en flúor de esta especialidad cuando se ingieran otros productos o alimentos que lo contengan o si el agua de abastecimiento local contiene una cantidad superior a 0,7 mg/l o ppm. Se debe administrar con precaución en los siguientes casos: - Historia de formación de cálculos renales, ya que el ácido ascórbico, el calcio y los fosfatos pueden potenciar su formación. - Parkinson tratado con levodopa no asociado a carbidopa (ver apartado 4.5. Interacciones con otros medicamentos y otras formas de interacción). - Pacientes tratados con digitálicos, ya que el calcio, el magnesio y la vitamina D pueden modificar sus efectos (ver apartado 4.5. Interacciones con otros medicamentos y otras formas de interacción). Advertencia sobre algunos de sus componentes Este medicamento contiene como excipiente aspartamo. Las personas afectadas de fenilcetonuria tendrán en cuenta que cada comprimido del mismo contiene 10,10 mg de fenilalanina. Por contener potasio, es perjudicial para pacientes con dietas pobres en potasio. El exceso de potasio puede producir molestias de estómago y diarreas. Este medicamento por contener 235,5 mg de sodio por comprimido puede ser perjudicial en pacientes con dietas pobres en sodio. 4.5 Interacciones con otros medicamentos y otras formas de interacción Este preparado puede interaccionar con: - Glucósidos digitálicos, ya que podría producirse toxicidad por digital o arritmias cardíacas debido al calcio, al magnesio y a la vitamina D. - Fenitoína, neomicina, etidronato, penicilamina, colestiramina, colestipol, parafina líquida o aceite mineral: puede verse modificada su absorción o la de alguno de los componentes de Pharmaton complex, por lo que si se administran conjuntamente con esta especialidad, deben distanciarse las tomas al menos 2 ó 3 horas. - Levodopa (no asociada a carbidopa), ya que la piridoxina, a dosis altas, puede revertir los efectos de la levodopa, lo cual no ocurre con la asociación de levodopa-carbidopa. - Ácido acetohidroxámico, ya que produce quelación del hierro y otros metales pesados, pudiendo disminuir la absorción intestinal de todos ellos. - Isotretionina, ya que pueden producirse efectos tóxicos auditivos junto con el retinol. - Tetraciclina, ya que puede producirse hipertensión intracraneal benigna junto con el retinol y además, disminuye la absorción del hierro, del zinc y del calcio. - Antiácidos que contienen aluminio o magnesio, ya que junto con la vitamina D puede aumentarse la toxicidad del aluminio y las concentraciones de magnesio, especialmente en pacientes con insuficiencia renal crónica. - Anticonvulsivos del grupo hidantoína o barbitúricos o primidona, ya que pueden reducir el efecto de la vitamina D. - Antidepresivos, anticoagulantes orales, dosis altas de salicilatos, sulfamidas, trimetoprim/sulfametoxazol o anticonceptivos hormonales ya que con dosis altas de vitamina C puede verse modificada la acción de estos medicamentos. Interferencias con pruebas diagnósticas: pueden aparecer resultados erróneos en la determinación de la glucosa en orina, incluyendo las pruebas con tiras reactivas, debido a la presencia de ácido ascórbico, riboflavina, nicotinamida y sulfato ferroso; ésto deberá ser tenido en cuenta especialmente en el caso de pacientes diabéticos. Piridoxina: en el caso de determinaciones de urobilinógeno que utilizan el reactivo de Erlich pueden producirse resultados falsamente positivos. Tiamina (generalmente sólo se produce con dosis altas): en la determinación de concentraciones séricas de teofilina por el método espectrofotométrico de Schack y Waxler puede producir interferencias; en la determinación de ácido úrico en orina por el método del fototungstato o de urobilinógeno utilizando el reactivo de Ehrlich, pueden producirse resultados falsamente positivos. 4.6 Embarazo y lactancia Como con cualquier medicamento, antes de administrar Pharmaton Complex durante el embarazo o la lactancia, se debe valorar la relación beneficio/riesgo. No son necesarias dosis altas de Vitamina C en el embarazo (ver apartado 4.3 Contraindicaciones). Por lo que respecta a la Vitamina C, durante el embarazo, en condiciones normales, no son necesarias dosis superiores a 100 mg al día, en cualquier caso, siempre por indicación del médico. Aunque no hay evidencia de efectos perjudiciales, no ha sido establecida la seguridad fetal con las dosis altas de Vitamina C. 4.7 Efectos sobre la capacidad para conducir y utilizar maquinaria No se han descrito. 4.8 Reacciones adversas Reacciones de hipersensibilidad a alguno de sus componentes. En algunos casos, hipertensión, nerviosismo, insomnio, edema. En casos raros se han descrito reacciones digestivas tales como náuseas, vómitos y dolor de estómago. Asimismo, existe el riesgo de formación de cálculos y de precipitar ataques agudos de gota en individuos predispuestos. En caso de observarse la aparición de reacciones adversas debe suspenderse el tratamiento y notificarse al sistema de Farmacovigilancia. 4.9 Sobredosificación A dosis elevadas del preparado podrían producirse o agravarse: - hiperuricemia o gota, debido a la nicotinamida y la cianocobalamina - úlcera péptica y alteraciones hepáticas, debido al hierro y la nicotinamida - diarrea, cálculos renales y calambres abdominales, debido a dosis superiores a 1 g por día de Vitamina C - vómitos, dolor de cabeza, somnolencia y diarrea, debido a una toxicidad crónica por ingesta diaria prolongada de cantidades muy elevadas de vitamina A (25 comprimidos) y de vitamina D (5 comprimidos). - cuadro de sobrestimulación cerebral con insomnio y aumento de la irritabilidad, dolor de cabeza, mareo, edema, alteraciones digestivas, alteraciones menstruales y sensación dolorosa en las mamas, debido al ginseng. Otros síntomas de una sobredosificación serían: estreñimiento, sabor metálico, hipertensión, ictericia, descamación de la piel, manchas de color amarillo-anaranjado en la piel, color azula do de las palmas de las manos. 5.PROPIEDADES FARMACOLÓGICAS 5.1 Propiedades farmacodinámicas A13A: Tónicos y reconstituyentes (Código ATC: A11AA) Pharmaton Complex contiene una asociación de vitaminas, minerales y oligoelementos en cantidades que cubren las Raciones Diarias Recomendadas. Estos componentes intervienen en su mayor parte como constituyentes de enzimas o coenzimas en numerosas funciones del organismo, tales como el metabolismo de hidratos de carbono, grasas, aminoácidos, ácidos nucleicos, formación de huesos, transmisión nerviosa y mantenimiento del equilibrio ácido-base. Además, contiene extracto estandarizado de ginseng G115 y deanol que ejercen un efecto tónico general. 5.2 Propiedades farmacocinéticas Debido a que el extracto estandarizado de ginseng G115 es un extracto complejo, que contiene más de 200 sustancias identificadas, la realización de estudios farmacocinéticos es muy compleja. Sin embargo, se han realizado estudios farmacocinéticos de los ginsenósidos individuales purificados en diversas especies animales. La biodisponibilidad determinada en ratones, utilizando Ginsenósido Rg1 marcado radiactivamente (C14), originado a partir de extracto estandarizado de ginseng G115, resultó ser del 30 %. Tras la administración intraperitoneal, dependiendo de la especie animal y del tipo de ginsenósido, se determinaron las vidas medias de Ginsenósido Rg1 y Rb1 siendo éstas de 27 minutos y 14.5 horas, respectivamente. Las vitaminas se absorben fácilmente en el tracto gastrointestinal. Su metabolismo es hepático y la eliminación es renal (en el caso de las hidrosolubles) y fecal (en el caso de las liposolubles). Las sales minerales se absorben en el intestino, eliminándose por orina y heces. El deanol muestra una buena absorción por vía oral y se elimina por vía urinaria. Atraviesa la barrera hematoencefálica cuando se administra por vía oral o intraperitoneal. 5.3. Datos preclínicos sobre seguridad Ginseng La DL50 del extracto estandarizado de ginseng G115 por vía oral es superior a 5g/kg en rata y ratón y superior a 2g/kg en cerdo miniatura. La influencia del extracto estandarizado de ginseng G115 en la reproducción, fue estudiada en 2 generaciones de ratas Sprague-Dawley. Se alimentaron a animales de ambos sexos con una dieta control o con una dieta complementada con extracto estandarizado de ginseng G115, a dosis de 1,5, 5 o 15 mg/kg de peso corporal al día. Los parámetros de la reproducción y la lactancia en los grupos tratados fueron comparables para las dos generaciones de madres y cría s. No se observaron variaciones relacionadas con el tratamiento en el peso corporal semanal de los animales, consumo de alimentos, parámetros hematológicos y exámenes oftalmológico, histopatológico y macroscópico. La administración de extracto estandarizado de ginseng G115 a ratas Wistar y conejos hembra de Nueva Zelanda embarazadas no causó anormalidades en el desarrollo fetal. Las ratas fueron tratadas con 40 mg/kg/día durante los primeros 15 días tras el apareamiento y los conejos hembra fueron tratados con 20 mg/kg/día del 7º al 16º día tras el apareamiento. La obtención de los fetos fue por cesárea el día 21 en ratas y el 27 en conejos hembras. No se observaron anormalidades en los fetos de ambas especies. Deanol La DL50 del deanol administrado por vía oral fue de 3,1 g/kg en ratones y de 2,6 g/kg en ratas. En estudios de toxicidad subaguda y crónica llevados a cabo en diversas especies animales, se concluyó que el deanol mostraba una buena tolerancia, teniendo en cuenta las dosis mucho más elevadas utilizadas en los estudios con respecto a la dosis terapéutica. Vitaminas La dosis causante de toxicidad aguda en humanos adultos es para la vitamina D y la vitamina A, de 25.000-50.000 U.I y 300.000-900.000 U.I., respectivamente. La dosis causante de toxicidad crónica es de 2.000 U.I. para la vitamina D y de 100.000 U.I. para la vitamina A. 6.DATOS FARMACÉUTICOS 6.1 Relación de excipientes Gelatina, sacarosa, almidón de maíz, d,l-alfa-tocoferol, aceite de soja parcialmente hidrogenado, citrato de sodio, ácido cítrico, maltodextrina, hidrógenocarbonato de sodio, aspartamo (E-951), acesulafamo de potasio, sorbitol (E-490), povidona, macrogol 6000, estearato de magnesio, aromas de naranja, mandarina y limón. 6.2 Incompatibilidades No aplicable 6.3 Período de validez 2 años 6.4 Precauciones especiales de conservación No conservar a temperatura superior a 30ºC. Mantener el envase perfectamente cerrado. 6.5 Naturaleza y contenido del recipiente Frasco de polipropileno con tapón de polietileno y agente desecante. Envases conteniendo 15 comprimidos efervescentes. 6.6 Instrucciones de uso y manipulación Ver apartado 4.2. Posología y forma de administración. 7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN BOEHRINGER INGELHEIM ESPAÑA, S.A Prat de la Riba, s/n Sector Turó de Can Matas 08190 Sant Cugat del Vallès (Barcelona). 8. NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN: 65.378 9. FECHA DE LA PRIMERA AUTORIZACIÓN: Abril 2003 10. FECHA DE LA REVISIÓN DEL TEXTO: Abril 2003