pdf - SEQ
Anuncio

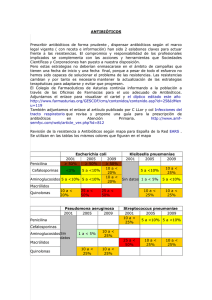
Rev Esp Quimioterap, Marzo 2006; Vol.19 (Nº 1): 14-20 © 2006 Prous Science, S.A.- Sociedad Española de Quimioterapia Revisión Impacto ecológico del tratamiento antibiótico de las infecciones odontológicas J.J. Granizo1, M.J. Giménez2, A. Bascones3 y L. Aguilar2 1Unidad de Epidemiología, Fundación Jiménez Díaz, Madrid; de Microbiología, Facultad de Medicina, Universidad Complutense, Madrid; 3Departamento de Estomatología III, Facultad de Odontología, Universidad Complutense, Madrid 2Departamento INTRODUCCIÓN La elevada prevalencia de las infecciones odontológicas las sitúan como primera causa de patología infecciosa en la comunidad (1), aunque desde el punto de vista terapéutico sólo aproximadamente el 10% de los antibióticos se emplea para tratar y prevenir este problema y sus consecuencias (2, 3). Ante la indicación de un tratamiento antimicrobiano, la elección del régimen antibiótico debe basarse en el espectro de cobertura de los posibles agentes etiológicos, en la actividad intrínseca frente a ellos, en la seguridad y tolerabilidad para el paciente, en la garantía de cumplimiento de la prescripción por parte del paciente que ofrece al prescriptor el régimen prescrito y, por último, en la capacidad de seleccionar bacterias resistentes y el impacto sobre el medio ambiente (impacto ecológico) del tratamiento indicado (4). La antibioticoterapia puede seleccionar resistencias tanto en la flora patógena (que pueden implicar fracaso terapéutico, aunque no existen datos en la literatura que permitan concluir un grave problema de resistencias en odontología) (5) como en la flora normal del paciente (sobrecrecimiento de especies intrínsecamente resistentes o sobrecrecimiento de subpoblaciones que por mutación de- sarrollan resistencia). La flora normal, microbiota humana, es parte integrante del ser humano. Debido a que la flora normal actúa como control de crecimiento de microorganismos oportunistas, su acción defensiva se denomina “resistencia a la colonización”. El ser humano tiene por cada célula eucariota diez procariotas como parte integrante de su cuerpo. Estas últimas constituyen la microbiota humana, la flora normal de la piel y las mucosas de las vías respiratorias altas, y la orofarínge, el intestino grueso y la vagina. Cada uno de estos nichos ecológicos tiene una flora particular que hay que respetar. Sin embargo, la administración de agentes antimicrobianos de manera terapéutica o profiláctica causa alteraciones en el balance ecológico entre el huésped y su microbiota (6). Por todo lo dicho, en la elección de un tratamiento antimicrobiano hay que valorar no sólo los efectos sobre los agentes etiológicos a erradicar, sino también los efectos sobre el ser humano: – El efecto sobre la célula eucariota humana, que será considerado un efecto adverso ya que los antibióticos están diseñados para actuar sobre estructuras de la célula procariota. 2006; Vol. 19 (Nº 1) Impacto ecológico del tratamiento antibiótico de las infecciones odontológicas – El efecto sobre la microbiota humana, que se puede definir como el impacto ecológico del tratamiento. Muchas veces la calificación de un organismo como patógeno o como flora normal depende de su localización en el cuerpo humano. Así, Streptococcus pneumoniae puede ser parte de la flora normal en la nasofaringe o el aislamiento más prevalente en la neumonía adquirida en la comunidad, dependiendo de si se encuentra en las vías respiratorias altas en el primer caso o en el parénquima pulmonar en el segundo. Los estreptococos del grupo viridans también son parte de la flora orofaríngea habitual, o agentes de las bacteriemias transitorias y de las infecciones a distancia que se producen tras manipulaciones odontológicas en el huésped con factores de riesgo. De la misma forma, Escherichia coli es parte integrante de la flora normal del intestino grueso, pero también es el agente más frecuente de la cistitis no complicada en la comunidad. Estos tres microorganismos se suelen tomar como índice del impacto ecológico del antibiótico en la flora normal respiratoria y orofaríngea, en el primer y segundo caso, e intestinal en el tercero. Los tratamientos antibióticos administrados para un determinado proceso infeccioso (por ejemplo, una infección odontológica) pueden seleccionar resistencias en bacterias de la microbiota humana (por ejemplo, E. coli en el intestino o los estreptococos de la faringe), que a su vez pueden producir, por la presencia de condiciones predisponentes, infecciones (por ejemplo, urinarias o respiratorias) en el huésped en que se ha seleccionado la resistencia o en otros al transmitirse la subpoblación bacteriana seleccionada. Estas infecciones pueden ser más difíciles de tratar por el simple hecho de que el agente etiológico portará genes de resistencia. Por tanto, también podemos considerar la resistencia como un grupo de genes (al final, en cada caso en particular, es un gen el que la codifica) en la microbiota humana. Estos genes pueden ser adquiridos, seleccionados por tratamientos antibióticos y transmitidos entre bacterias que forman parte de la flora normal, manteniéndose en esta situación o influyendo en el tratamiento antibiótico, al crear las bacterias de la flora normal infecciones por cambio de nicho ecológico, como hemos comentado anteriormente. Por ello, cuando se habla del impacto ecológico del tratamiento parece que debemos referirnos a la acción de los distintos antibióticos sobre dicho pool de genes que pone a disposición de las bacterias los mecanismos de resistencia a los antibióticos que se utilizan para tratar las infecciones comunitarias (7). 15 Desde el punto de vista epidemiológico de las resistencias (adquiridas, seleccionadas, transmitidas) en la comunidad, el peso específico de las infecciones que puedan producir las bacterias portadoras de resistencia es distinto según la bacteria diana de que se trate, ya que la transmisibilidad de los S. pneumoniae (como causa de infección respiratoria) seleccionados es mucho mayor que la de E. coli como agente de infección urinaria que produce la infección a partir de la propia flora intestinal. Además, parece que los neumococos resistentes tienen un mayor potencial de transmisión entre individuos que los sensibles (8, 9). Este hecho es importante ya que el 85% a 90% del consumo de antibióticos se produce en la comunidad, y el 80% de éste es para infecciones respiratorias (10) (que deberá cubrir las resistencias seleccionadas), seguido en segundo lugar, pero muy a distancia, de la infección urinaria, que supone en España un 12% de las consultas de los médicos de atención primaria (11). En resumen, para definir el concepto de impacto ecológico (7) podemos recurrir a las tres acepciones que tiene el término “ecología” en el diccionario de la Real Academia Española: 1) Ciencia que estudia las relaciones de los seres vivos entre sí y con su entorno. 2) Parte de la sociología que estudia la relación entre los grupos humanos y su ambiente, tanto físico como social. 3) Defensa y protección de la naturaleza y del medio ambiente. Cuando se habla del impacto ecológico de un tratamiento antibiótico las tres acepciones tienen sentido, ya que el impacto ecológico de un antibiótico se medirá por el efecto que éste ocasiona en la relación del paciente con su microbiota (acepción 1), que se engloba en un proceso dinámico de intercambio con otros seres de su entorno (acepción 2), por lo que el respeto a la flora del paciente incide positivamente en la protección de este “micromedio” ambiente (acepción 3). SELECCIÓN DE RESISTENCIAS EN LAS BACTERIAS ÍNDICE DE LA MICROBIOTA HUMANA Y POTENCIAL ECOLÓGICO DE LOS TRATAMIENTOS ANTIBIÓTICOS Si queremos estudiar el impacto ecológico del tratamiento antibiótico, necesitamos estudiar datos de los factores que crean la alteración ecológica, es decir, datos de los tratamientos antibióticos, analizando un gran número 16 J.J. Granizo, M.J. Giménez, A. Bascones y L. Aguilar de personas y de aislamientos de las bacterias índice de la microbiota humana que puedan aportarnos información sobre marcadores de resistencia. Para evaluar el impacto ecológico se utilizan los marcadores de resistencia: la penicilina para el grupo de los betalactámicos, la eritromicina para el grupo de los macrólidos y el ciprofloxacino para las quinolonas. El análisis de los marcadores de resistencia de grupo es válido desde el punto de vista epidemiológico, aunque no desde el punto de vista clínico, para el que sería necesario analizar cuáles son los antibióticos más activos de cada grupo. La relación entre consumo de antibióticos y resistencia a estos marcadores se escenifica en el llamado “círculo vicioso de las resistencias” (12, 13): 1) El consumo selectivo de determinados antibióticos tendrá un efecto particular y exclusivo sobre el aumento de la CMI (concentración mínima inhibitoria del crecimiento bacteriano) a escala poblacional de los marcadores de resistencia. 2) El incremento en la CMI de los marcadores de resistencia no influye por igual sobre todos y cada uno de los antibióticos agrupados en la misma familia. 3) Los antibióticos menos influidos por el incremento de resistencia a su marcador serán aquellos cuyo consumo, a su vez, seleccionará menos resistencia; cerrándose de esta manera el círculo. Hasta ahora, la respuesta al problema de la resistencia ha sido la disminución no selectiva de la prescripción antibiótica global para reducir el efecto de la presión de selección (14). A pesar de ello, la resistencia parece difícil de desplazar. Otra aproximación complementaria debería ser la utilización de compuestos con gran actividad intrínseca que pudieran cortar el círculo en sus tres fases: 1) haciendo que la CMI del marcador de resistencias no aumente, 2) sufriendo menos variaciones la CMI del compuesto utilizado al no ser influida por la CMI del marcador, y 3) evitando la utilización de fármacos más selectores y con ello la selección de resistencias. Con respecto a los estreptococos como bacterias índice de la flora orofaríngea, se ha relacionado el consumo de antibióticos (como única causa) con las resistencias en las especies S. pyogenes y S. pneumoniae (15), tanto desde un punto de vista temporal (16, 17) como geográfico (18, 19), estando las resistencias a los macrólidos en estas dos especies localmente ligadas (20). Mientras que la imputabilidad a las aminopenicilinas de la selección de resistencias en S. pneumoniae es mucho más baja (17, 19), los fármacos que seleccionan más resistencias a la penicilina y los ma- REV ESP QUIMIOTERAP crólidos son los macrólidos de administración una o dos veces al día en S. pneumoniae y S. pyogenes (17, 19), y en menor grado en S. pneumoniae las cefalosporinas orales de administración dos veces al día, pero no son fármacos de elección en odontología (5). Estos hechos tienen traducción en las especies del grupo viridans del género Streptococcus, en las cuales la alta resistencia a los macrólidos (eritromicina, claritromicina) (21) se asocia frecuentemente a alta resistencia a las tetraciclinas (22) y a la clindamicina y los azálidos (azitromicina) (23). Así, en España se ha descrito una alta prevalencia de bacteriemias iatrogénicas orales causadas por estreptococos resistentes a la eritromicina (40,8%) y la clindamicina (21%), siendo la mayoría de los aislamientos sensibles a las aminopenicilinas (24). Tomando E. coli como bacteria índice de la flora intestinal, los macrólidos y los cetólidos son respetuosos, ya que este microorganismo es resistente a estos compuestos. Las quinolonas, sin embargo, han seleccionado un alto grado de resistencia (4), pero estos compuestos no están indicados en odontología (5). Mientras la amoxicilina puede haber seleccionado altas tasas de resistencia en E. coli por producción de betalactamasas, la sensibilidad a amoxicilinaácido clavulánico es muy alta. Considerando que el consumo de antibióticos en odontología supone aproximadamente el 10% del consumo de antibióticos en la comunidad, como se ha comentado, es posible sospechar un cierto grado de imputabilidad, quizá no despreciable, en la selección de resistencias por tratamientos antimicrobianos de las infecciones odontológicas. HÁBITOS DE PRESCRIPCIÓN, AUTOMEDICACIÓN Y REPERCUSIÓN ECOLÓGICA Hemos visto que los distintos antibióticos tienen distinto potencial de selección de resistencias: los macrólidos de vida media larga y las cefalosporinas de segunda generación tienen más importancia que las aminopenicilinas en la resistencia a la penicilina y los macrólidos de S. pneumoniae, como representante de la flora orofaríngea. Por otra parte, las resistencias a la amoxicilina y las quinolonas son altas en E. coli como representante de la flora intestinal, mientras que son bajas para amoxicilina-ácido clavulánico. Hay una moderada discrepancia (entre el 20% y el 30%) entre el consumo de antibióticos según la Información Terapéutica del Sistema Nacional de Salud (ITSNS) y el Internacional Marketing Services (IMS) en casi todas las familias de antimicrobianos, excepto en el caso de las aminopenicilinas, en que las diferencias llegan a ser del 200% 2006; Vol. 19 (Nº 1) Impacto ecológico del tratamiento antibiótico de las infecciones odontológicas (25). Esto es explicable por el consumo derivado del ejercicio privado y por el autoconsumo, que no son recogidos por la ITSNS (sólo contempla las prescripciones hechas con receta médica en el sistema sanitario público), pero sí por el IMS, ya que éste recoge una estimación de ventas totales en función de la encuesta de mercado que se apoya en la producción, exportación e importación, y que recoge datos sistemáticos y completos de las compañías farmacéuticas, almacenistas, muestra de farmacias y de prescripción en la práctica privada. Es curioso que, con respecto a los estreptococos, los antibióticos que presentan menor potencial de selección de resistencias (las aminopenicilinas) son los que más se utilizan en el ejercicio privado y en la automedicación. Por ello es muy importante conocer los hábitos de prescripción y de automedicación. USO DE ANTIMICROBIANOS EN INFECCIONES ODONTOLÓGICAS La odontología es una especialidad de ejercicio predominantemente privado, con un componente asistencial público muy pequeño y limitado a algunas afecciones y segmentos de edad. Aun así, este ejercicio dentro de la sanidad pública tiene pocos años, pues la cartera de servicios de estomatología es dispar por comunidades (26). En 1993 había censados en España 12.247 estomatólogos (31,3 profesionales por 100.000 habitantes), cifra que se elevó a 17.358 en el año 2000 (43,9 profesionales/100.000 habitantes) (27). Relacionando los datos del IMS (28) y los datos básicos de la salud y los servicios sanitarios en España (27), en el año 2003 la tasa de prescripción relacionada con la odontología fue de 197,5 prescripciones por odontólogo y año. En ese mismo año, sólo en el sistema público había unos 28.000 médicos en atención primaria (27), con una tasa de 72,1 prescripciones por médico y año, cifra que sería mucho más reducida si se hubiera tenido en cuenta en el cómputo de prescriptores a los médicos generales privados. Según los datos del IMS, en el año 2005 el 12,4% de los antibióticos se utilizaron para el tratamiento de infecciones odontológicas (28). Aproximadamente el 62% de la prescripción fue realizada por odontólogos, el 36% por médicos generales y el 2% por otros facultativos. Tanto en el caso de los odontólogos como en el de los médicos generales, la prescripción más frecuente es la de betalactámicos seguida de los macrólidos, suponiendo la suma de las dos familias aproximadamente un 93% del total de las prescripciones. De las realizadas por odontólogos, el 71% corresponden a betalactámicos (23% amoxicilina- 17 ácido clavulánico y 48% amoxicilina) y el 22% a macrólidos (19% espiramicina y 3% otros) (28). De las prescripciones realizadas por los médicos generales, el 59% corresponden a betalactámicos (41% amoxicilina-ácido clavulánico y 16% amoxicilina) y el 35% a macrólidos (33% espiramicina y 2% otros) (28). Analizando estos datos al detalle (test de χ2) se observa que los odontólogos prescriben de manera significativa (p <0.001) más aminopenicilinas que los médicos generales en este tipo de infecciones (71% vs. 57%), mientras que estos últimos prescriben de manera significativa (p <0.01) más macrólidos (35% vs. 22%). Dentro de las aminopenicilinas, el patrón de prescripción es significativamente (p <0.001) diferente para los dos grupos: los odontólogos prescriben más amoxicilina que amoxicilina-ácido clavulánico (48% vs. 23%), mientras que los médicos generales prescriben más amoxicilina-ácido clavulánico que amoxicilina (41% vs. 16%). Por último, dentro de los macrólidos, el porcentaje de prescripción que supone la espiramicina es similar en ambos grupos de prescriptores (85% para odontólogos versus 95% para médicos generales; p >0.01). Cuando se toma como bacteria índice S. pneumoniae, parece que los odontólogos utilizan con mayor frecuencia compuestos (aminopenicilinas) de menor impacto ecológico que los médicos generales, que utilizan más macrólidos. Sin embargo, hay que tener en cuenta que el macrólido más utilizado es con diferencia la espiramicina, cuyo consumo global en nuestro país en DDD/1000 habitantes/día ha permanecido constante (alrededor de 0,5) durante la pasada década (25), por lo que no se le puede imputar de manera directa la selección de resistencias en esta bacteria diana. Quizá sí pueda tener cierto grado de imputabilidad cuando se considera su efecto aditivo con otros macrólidos en la selección de resistencia en S. pneumoniae (17, 25), ya que el mecanismo de resistencia a los macrólidos más prevalente en este grampositivo en España es el fenotipo MLSB (el 35% de los neumococos en nuestro país son resistentes a los macrólidos, y de ellos el 95% presenta este fenotipo de resistencia) (29), que afecta a los macrólidos de 14, 15 y 16 átomos, las lincosamidas y las estreptograminas. Las resistencias a los macrólidos como la azitromicina en bacterias del género Streptococcus, como las del grupo viridans, son altas y dependientes de la especie, variando entre un 18% en S. sanguis y un 48% en S. mitis, como se vio en un estudio que analizaba aislamientos de líquido crevicular en pacientes con periodontitis (30). Cuando se toma como bacteria índice E. coli, parece que los médicos generales utilizan con mayor frecuencia en las infecciones odontológicas compuestos de menor impacto ecológico (amoxicilina-ácido clavulánico y macrólidos) que los odontólogos, que utilizan más amoxicilina que 18 J.J. Granizo, M.J. Giménez, A. Bascones y L. Aguilar su asociación con ácido clavulánico. No podemos dejar de volver a mencionar que el mayor problema con respecto a E. coli es la alta tasa de resistencia a las quinolonas, aunque no está en relación con el consumo en las infecciones odontológicas, ya que estos compuestos no se utilizan en esta indicación. De los antibióticos que se emplean, los macrólidos respetan la flora de E. coli (que es resistente a ellos), mientras que la tasa de resistencias a amoxicilinaácido clavulánico se mantiene baja. Por el contrario, quizá sí puede influir en las altas tasas de resistencia a la amoxicilina en E. coli el consumo de amoxicilina para las infecciones odontológicas. Además de que su uso puede presentar aspectos negativos desde el punto de vista ecológico, su gran empleo no deja de ser sorprendente, ya que en muchos casos los odontopatógenos producen betalactamasas, como es el caso de Prevotella spp. (30), al igual que otras bacterias saprófitas de la cavidad bucal, lo que podría inactivar la acción de este compuesto sobre los odontopatógenos si no se asocia a un inhibidor de estas enzimas como el ácido clavulánico. OTROS FACTORES A CONSIDERAR El impacto ecológico de un tratamiento es importante, influyendo no sólo la elección del antibiótico sino también su dosificación para cada paciente, que finalmente seleccionarán o no bacterias resistentes. La elección de la dosificación adecuada debe realizarse basándose en consideraciones farmacodinámicas con respecto a los microorganismos que hay que erradicar (el primer parámetro para la elección de un tratamiento antibiótico es la predicción de su eficacia). La farmacodinamia especifica el valor de la “relación entre los parámetros farmacocinéticos séricos y la sensibilidad in vitro” que predice la eficacia: a) Porcentaje del intervalo de dosificación en que la concentración supera la CMI, que debe ser superior al 40% a 50% para los betalactámicos, los macrólidos y las lincosamidas. b) Relación del área bajo la curva de las concentraciones séricas/CMI, que debe ser superior a 25 para los azálidos (azitromicina). Las concentraciones antibióticas en el fluido gingival son similares o superiores a las séricas, como se ha visto en el caso de amoxicilina-ácido clavulánico (31), espiramicina y metronidazol (32). Se han publicado trabajos que aplican los conceptos farmacodinámicos a los tratamientos de las infecciones odontológicas, analizando distintos antibióti- REV ESP QUIMIOTERAP cos frente a los cinco aislamientos más prevalentes (pero no frente a todas las bacterias implicadas) en las infecciones odontológicas (Streptococcus grupo viridans, Peptostreptococcus spp., Prevotella intermedia, Porphyromonas gingivalis y Fusobacterium nucleatum) (33, 34). Sólo amoxicilina-ácido clavulánico a dosis de 875/125 mg cada 8 horas, o la nueva formulación de 2000/125 mg cada 12 horas, así como la clindamicina a dosis de 300 mg cada 6-8 horas, cumplen los requisitos farmacodinámicos. Sin embargo, la clindamicina no cubre adecuadamente los géneros Staphylococcus, Streptococcus y Peptostreptococcus, que presentan un grado de resistencia no despreciable (5). El metronidazol, los macrólidos y la espiramicina no cubren todos los grampositivos (Streptococcus y Peptostreptococcus) y estos dos últimos antibióticos tampoco cubren Fusobacterium (33, 34). CONCLUSIONES Las recomendaciones acerca de la utilización de los antibióticos en el tratamiento y la profilaxis de las infecciones odontológicas no pueden basarse en ensayos clínicos (ni por ende en la medicina basada en la evidencia), ya que los ensayos clínicos con antibióticos en afecciones dentarias responden poco a los criterios metodológicos requeridos, y además no son lo suficientemente numerosos para establecer conclusiones (5). Por ello, la estrategia general de prescripción antibiótica terapéutica o profiláctica se basa en acuerdos profesionales y documentos de consenso (2, 3). En estos documentos, la elección de tratamientos se basa en la probada seguridad y tolerabilidad para el paciente de los antimicrobianos recomendados y la garantía de cumplimiento de la prescripción para la consecución del valor adecuado de los parámetros farmacodinámicos que predice la erradicación de los microorganismos diana. Como último parámetro no debería olvidarse el comentado impacto ecológico. A pesar de la existencia de estos documentos de consenso y del distinto impacto ecológico, los datos sugieren que existen diferencias en los antimicrobianos prescritos para el tratamiento de las infecciones odontológicas según el prescriptor. Aunque la prescripción de aminopenicilinas es la más frecuente en ambos grupos (odontólogos y médicos generales), la de aminopenicilinas es significativamente mayor por parte de los odontólogos y la de macrólidos es significativamente mayor por parte de los médicos generales, a pesar de que en España estos fármacos no son adecuados frente a las bacterias del género Streptococcus. Asimismo, dentro de las aminopenicilinas, la prescripción 2006; Vol. 19 (Nº 1) Impacto ecológico del tratamiento antibiótico de las infecciones odontológicas de amoxicilina-ácido clavulánico es significativamente mayor por parte de los médicos generales, mientras que la de amoxicilina sola es significativamente mayor por parte de los odontólogos, a pesar de la producción de betalactamasas por muchos odontopatógenos y otras bacterias de la flora normal oral. Quizá sería necesario un esfuerzo de trabajo en común y la unificación de criterios entre los distintos profesionales. La ecología es el respeto al medio ambiente. Desde un punto de vista egoísta, el cuidado de nuestro micromedio ambiente, nuestra microbiota, que forma parte de nosotros mismos, debería ser importante. Por ello, el conocimiento del potencial ecológico de los distintos compuestos es importante y debería ser un factor (aunque no el principal) a considerar a la hora de elegir un tratamiento antibiótico. Aunque el mayor efecto sobre la microbiota humana lo produce el tratamiento de las infecciones respiratorias adquiridas en la comunidad, que representa la mayor parte del consumo de antibióticos, y la contribución del tratamiento de las infecciones odontológicas es mucho menor, no deberíamos olvidar la ecología en nuestra labor sanitaria diaria, aunando así esfuerzos entre todos. AGRADECIMIENTOS Al Dr. J.E. Martín y al Dr. J. Prieto por las interesantes conversaciones a lo largo de la redacción de este manuscrito y su revisión crítica. Correspondencia: Lorenzo Aguilar, Departamento de Microbiología, Facultad de Medicina, Universidad Complutense, Avda. Complutense s/n, 28040 Madrid. BIBLIOGRAFÍA 1. Matesanz, P., Figuero, E., Giménez, M.J. y cols. Del conocimiento de la etiología bacteriana al tratamiento y prevención de las infecciones más prevalentes en la comunidad: Las infecciones odontogénicas. Rev Esp Quimioterap 2005; 18: 136-145. 2. Bascones Martínez, A., Aguirre Urizar, J.M., Bermejo Fenoll, A. y cols. Documento de consenso sobre el tratamiento antimicrobiano de las infecciones bacterianas odontogénicas. Med Oral Patol Oral Cir Bucal 2004; 9: 363-369. 3. Gutiérrez, J.L., Bagan, J.V., Bascones, A. y cols. Documento de consenso sobre la utilización de profilaxis antibiótica en cirugía y procedimientos dentales. Med Oral Patol Oral Cir Bucal 2006; 11: E188-205. 4. Barberán, J., Giménez, M.J., Aguilar, L., Prieto, J. Evidencia científica y concepción global del tratamiento empírico de la infección de vías respiratorias bajas en la comunidad. Rev Esp Quimioterap 2004; 17: 317-324. 5. Prescription des antibiotiques en odontologie et stomatologie. Recommandations et argumentaire. Agence Française de Sécurité Sanitaire des Produits de la Santé (www.afssaps.sante.fr) 2001. 19 6. Sullivan, A., Edlund, C., Nord, C.E. Effect of antimicrobial agents on the ecological balance of human microflora. Lancet Infect Dis 2001; 1: 101-114. 7. Aguilar, L., Giménez, M.J. A la búsqueda del mínimo impacto ecológico del tratamiento antibiótico de la infección respiratoria de la comunidad en España. En: García Rodríguez, J.A., Prieto Prieto, J. (Eds.). Mejora de la calidad de los antimicrobianos. Recomendaciones SEQ. Grupo Ars XXI de Comunicación, Barcelona 2006; 135-153. 8. Arason, V.A., Kristinsson, K.G., Sigurdsson, J.A., Stefansdottir, G., Molstad, S., Gudmundsson, S. Do antimicrobials increase the carriage rate of penicillin resistant pneumococci in children? Cross sectional prevalence study. BMJ 1996; 313: 387-391. 9. Dancer, S.J. The problem with cephalosporins. J Antimicrob Chemother 200; 1: 463-478. 10. Huovinen, P., Cars, O. Control of antimicrobial resistance: Time for action. The essentials of control are already well known. BMJ 1998; 317: 613-614. 11. Libro Blanco: Uso racional de la antibioticoterapia en el tratamiento de las infecciones de vías urinarias bajas en España. Liade, Madrid 2001. 12. Aguilar, L., García-Rey, C., Giménez, M.J. Presión antibiótica, desarrollo de resistencias en Streptococcus pneumoniae y fracaso clínico: Un círculo no tan vicioso para algunos antibióticos. Rev Esp Quimioterap 2001; 14: 17-21. 13. Aguilar, L., Giménez, M.J., García-Rey, C., Martín, J.E. New strategies to overcome antimicrobial resistance in Streptococcus pneumoniae with betalactam antibiotics. J Antimicrob Chemother 2002; 50 (Suppl. S2): 93-100. 14. Livermore, D.M. The need for new antibiotics. Clin Microbiol Infect 2004; 10 (Suppl. 4): 1-9. 15. García-Rey, C., Fenoll, A., Aguilar, L., Casal, J. Effect of social and climatological factors on antimicrobial use and Streptococcus pneumoniae resistance in different provinces in Spain. J Antimicrob Chemother 2004; 54: 465-471. 16. Granizo, J.J., Aguilar, L., Casal, J., Dal-Re, R., Baquero, F. Streptococcus pyogenes resistance to erythromycin in relation to macrolide consumption in Spain (1986-1997). J Antimicrob Chemother 2000; 46: 959-964. 17. Granizo, J.J., Aguilar, L., Casal, J., García-Rey, C., Dal-Re, R., Baquero, F. Streptococcus pneumoniae resistance to erythromycin and penicillin in relation to macrolide and beta-lactam consumption in Spain (1979-1997). J Antimicrob Chemother 2000; 46: 767-773. 18. García-Rey, C., Aguilar, L., Baquero, F., Casal, J., Martín, J.E. Pharmacoepidemiological analysis of provincial differences between consumption of macrolides and rates of erythromycin resistance among Streptococcus pyogenes isolates in Spain. J Clin Microbiol 2002; 40: 2959-2963. 19. García-Rey, C., Aguilar, L., Baquero, F., Casal, J., Dal-Re, R. Importance of local variations in antibiotic consumption and geographical differences of erythromycin and penicillin resistance in Streptococcus pneumoniae. J Clin Microbiol 2002; 40: 159-164. 20. Gómez-Lus, R., Granizo, J.J., Aguilar, L., Bouza, E., Gutiérrez, A., García-de-Lomas, J., The Spanish Surveillance Group for Respiratory Pathogens. Is there an ecological relationship between rates of antibiotic resistance of species of the genus Streptococcus? J Clin Microbiol 1999; 37: 3384-3386. 21. Rodríguez-Avial, I., Rodríguez-Avial, C., Culebras, E., Picazo, J.J. In vitro activity of telithromycin against viridans group streptococci and Streptococcus bovis isolated from blood: Antimicrobial susceptibility patterns in different groups of species. Antimicrob Agents Chemother 2005; 49: 820-823. 20 J.J. Granizo, M.J. Giménez, A. Bascones y L. Aguilar 22. Rodríguez-Avial, I., Rodríguez-Avial, C., Culebras, E., Picazo, J.J. Distribution of tetracycline resistance genes tet(M), tet(O), tet(L) and tet(K) in blood isolates of viridans group streptococci harbouring erm(B) and mef(A) genes. Susceptibility to quinupristin/dalfopristin and linezolid. Int J Antimicrob Agents 2003; 21: 536-541. 23. Tomás, I., Limeres, J., Diz, P. Antibiotic prophylaxis. BDJ 2005; 198: 60-61. 24. Tomás, I., Álvarez, M., Limeres, J. y cols. In vitro activity of moxifloxacin compared to other antimicrobials against streptococci isolated from iatrogenic oral bacteremia in Spain. Oral Microbiol Immunol 2004; 19: 331-335. 25. Granizo Martínez, J.J. Resistencia de los gérmenes más prevalentes en aislamientos de infección respiratoria adquirida en la comunidad a los antimicrobianos y su relación con el consumo de fármacos más empleados en el tratamiento de la infección respiratoria en la comunidad. Dpto. de Microbiología, Facultad de Medicina, Universidad Complutense de Madrid, Septiembre, 2004. 26. Vida, J. Las carteras de servicios sanitarios: Concreción, racionalización y articulación del contenido de las prestaciones sanitarias. Derecho y Salud 2005; 13: 17-34 27. Datos básicos de la salud y los servicios sanitarios en España 2003. http://www.msc.es/estadEstudios/estadisticas/home.htm 28. Intercontinental Marketing Services Ibérica S.A., Madrid, España, 2005. REV ESP QUIMIOTERAP 29. Pérez-Trallero, E., García-de-la-Fuente, C., García-Rey, C. y cols., Spanish Surveillance Group for Respiratory Pathogens. Geographical and ecological analysis of resistance, coresistance and coupled resistance to antimicrobials in respiratory pathogenic bacteria in Spain. Antimicrob Agents Chemother 2005; 49: 1965-1972. 30. Maestre, J.R., Giménez, M.J., Bascones, A. y cols. Odontopathogen susceptibility to amoxicillin/clavulanic acid and other common antibiotics used in odontology. 7th Congress of Chemotherapy and Infection, Florence. J Chemother 2005; 17 (Suppl. 3): 91. 31. Bascones, A., Mansó, F. Infecciones odontógenas en la cavidad bucal y región maxilofacial. Av Odontoestomatol 1994; 10 (Supl. A): 5-26. 32. Poulet, P.P., Duffaut, D., Barthet, P., Brumpt, I. Concentrations and in vivo antibacterial activity of spiramycin and metronidazole in patients with periodontitis treated with high-dose metronidazole and the spiramycin/metronidazole combination. J Antimicrob Chemother 2005; 55: 347-351. 33. Isla, A., Canut, A., Rodríguez-Gascon, A. y cols. Análisis farmacocinético/farmacodinámico (PK/PD) de la antibioterapia en odontoestomatología. Enferm Infecc Microbiol Clin. 2005; 23: 116-121. 34. Isla, A., Canut, A., Gascón, A.R. y cols. Pharmacokinetic/pharmacodynamic evaluation of antimicrobial treatments of orofacial odontogenic infections. Clin Pharmacokinet 2005; 44: 305-316.