T 3. Lipidos
Anuncio

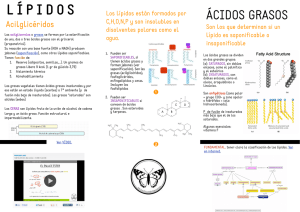
Bloque I: Lípidos BIOLOGÍA DE 2º DE BACHILLERATO 1. BASE FÍSICO QUIMICA DE LA VIDA. 1. 4. LÍPIDOS CONTENIDOS 1.4.1. Concepto y clasificación. 1.4.2. Ácidos grasos: estructura y propiedades. 1.4.3. Triacilglicéridos y fosfolípidos: estructura, propiedades y funciones. 1.4.4. Carotenoides y esteroides: propiedades y funciones. ORIENTACIONES 1. Definir qué es un ácido graso y escribir su fórmula general. 2. Reconocer a los lípidos como un grupo de biomoléculas químicamente heterogéneas y clasificarlos en función de sus componentes. Describir el enlace éster como característico de los lípidos. 3. Destacar la reacción de saponificación como típica de los lípidos con ácidos grasos. 4. Reconocer la estructura de triacilglicéridos y fosfolípidos y destacar las funciones energéticas de los triacilglicéridos y las estructurales de los fosfolípidos. 5. Destacar el papel de los carotenoides (pigmentos y vitaminas) y esteroides (componentes de membranas y hormonas). 1.4.1.CONCEPTO Y CLASIFICACIÓN Los lípidos son biomoléculas orgánicas, compuestas por C, H y O, y en algunos casos, pueden contener también P y N. Constituyen un grupo de sustancias muy heterogéneo que comparten las siguientes propiedades: • No son solubles en agua y otros disolventes polares, pero si son solubles en disolventes orgánicos, como el benceno, el éter o acetona. • Presentan un aspecto graso, es decir, poseen un brillo característico y son untuosos al tacto. • Poco densos. Dada la diversidad de lípidos existente se pueden hacer múltiples clasificaciones. La clasificación más aceptada actualmente se basa en su estructura molecular; estableciéndose los siguientes grupos: • Lípidos saponificables (ésteres de ácidos grasos): a. Simples (sólo contienen C, H y O): Acilglicéridos (aceites, mantecas y sebos) y ceras. b. Complejos (también tienen N y P). Son los lípidos de membrana: Fosfoglicéridos (fosfolípidos) y esfingolípidos. • Lípidos insaponificables (sin ácidos grasos en su molécula): a. Carotenoides (Como xantofilas y los carotenos). b. Esteroides (como la vitamina D y el colesterol). 1.4.2. ÁCIDOS GRASOS Estructura y clasificación. Los ácidos grasos, son moléculas que poseen una larga cadena lineal hidrocarbonada, de 14 a 22 C, que adopta estructuralmente forma de zig-zag debido a la simetría de sus enlaces, por lo general presentan un número par de átomos de carbono, y con un grupo carboxilo en el primer carbono de la molécula. Los más frecuentes presentan de 16 a 18 átomos de carbono. Son poco abundantes en estado libre y se obtienen mediante hidrólisis de otros lípidos. Se diferencian en la cadena carbonada, ya que todos poseen grupo carboxilo. Existen dos tipos de ácidos grasos, los saturados, cuando la cadena sólo tiene enlaces simples, y los insaturados, si la cadena presenta uno o varios enlaces dobles o triples entre los átomos de carbono. Algunos ácidos grasos son esenciales para los organismos, que no son capaces de sintetizarlos y tienen que ingerirlos en su dieta. Para los humanos son esenciales los ácidos grasos insaturados linoleico, linolénico y araquidónico (se designan con el término de vitamina F). Los contienen los aceites de semillas (maíz, girasol, etc.) y las grasas de los pescados azules, como por ejemplo el jurel. Propiedades de los ácidos grasos: • Propiedades físicas de los ácidos grasos - Carácter anfipático. Los ácidos grasos poseen en su molécula dos zonas diferentes: una zona polar, el grupo carboxilo (-COOH), que puede establecer puentes de hidrógeno con otras moléculas polares, como el agua, y una zona apolar, la cadena carbonada, fuertemente hidrófoba que tiende a formar enlaces por fuerzas de Van der Waals con otras cadenas semejantes. Debido a esta característica, al entrar en contacto con agua, los ácidos grasos orientan las cabezas polares hacia ella mientras que las colas apolares se sitúan en posición opuesta. Debido al gran tamaño de la fracción hidrófoba son insolubles en agua. - Punto de fusión. El tener o no dobles enlaces determina la forma, recta o doblada, de la molecula y, por lo tanto, su punto de fusión. Este depende de la longitud de la cadena y del grado de insaturación que presente. En los ácidos grasos saturados el punto de fusión aumenta con el número de átomos de carbono, porque a mayor número de átomos de carbono mayor número de enlaces por fuerzas de Van der Waals y mayor gasto de energía para conseguir la fusión. En los ácidos grasos insaturados los puntos de fusión son más bajos porque los dobles enlaces dificultan la formación de enlaces por fuerzas de van der Waals, por eso tienen un punto de fusión más bajo y estan fundidos a tª ambiente (aceites), los saturados están solidos (mantecas y sebos). Podemos decir que a temperatura ambiente, los ácidos grasos saturados son sólidos y los insaturados líquidos. Punto Nº de átomos Nombre trivial Estructura de carbono de fusión Ácidos grasos saturados Ácido láurico 12 CH3-(CH2)10-COOH 44,2 Ácido mirístico 14 CH3-(CH2)12-COOH 54,0 Ácido palmítico 16 CH3-(CH2)14-COOH 63,0 Ácido esteárico 18 CH3-(CH2)16-COOH 69,6 Ácido araquídico 20 CH3-(CH2)18-COOH 76,5 Ácido lignocérico 24 CH3-(CH2)22-COOH 86,0 Ácidos grasos insaturados Ácido palmitoleico 16 CH3-(CH2)5-CH=CH-(CH2)7-COOH -0,5 Ácido oleico 18 CH3-(CH2)7-CH=CH-(CH2)7-COOH 13,4 Ácido linoleico 18 CH3-(CH2)4-CH=CH-CH2-CH=CH-(CH2)7-COOH -3,0 Ácido linolénico 18 CH3-CH2-CH=CH-CH2-CH=CH-CH2-CH=CH(CH2)7-COOH -11,0 Ácido araquidónico 20 CH3-(CH2)4-CH=CH-CH2-CH=CH-CH2-CH=CHCH2-CH=CH-(CH2)3-COOH -49,5 Los acidos grasos saturados, debido a la forma recta de su molecula, pueden enpaquetarse más densamente por las Fuerzas de Wan der Waals y enlaces hidrofóbicos. Es por esto que las sustancias que los contienen son solidas (sebos) a la Tª ambiente Las Fuerzas de Van der Waals Estas fuerzas son las responsables de muchos fenómenos físicos y químicos como la adhesión, rozamiento, difusión, tensión superficial y la viscosidad. Son fuerzas de estabilización molecular (dan estabilidad a la unión entre varias moléculas), también conocidas como atracciones intermoleculares o de largo alcance y son las fuerzas entre moléculas (fuerzas entre molecula-molecula). Son mas débiles que las internas ya que dependen exclusivamente del tamaño y forma de la molécula pudiendo ser de atracción o de repulsión. Son tan débiles que no se las puede considerar un enlace, como el enlace covalente o iónico, solo se las considera una atracción. Para tener una idea de la poca fuerza que tienen, si un enlace covalente tuviera una fuerza de 100, las de van der Waals serían de valor 1 (100 veces menor). Propiedades químicas de los ácidos grasos - Esterificación. Los ácidos grasos se unen a alcoholes mediante enlace covalente y forman un éster, desprendiéndose una molécula de agua. Es la reacción que se establece al reaccionar el grupo hidroxilo de un alcohol y el carboxilo de un ácido graso. R1-COOH + HO-CH2-R2 ────► R1-COO-CH2-R2 + H2O Ácido graso Alcohol Éster Agua - Saponificación. Por hidrólisis alcalina, los ésteres dan lugar a jabón (sal del ácido graso). R1-COO-CH2-R2 + NaOH ────► R1-COONa + HO-CH2-R2 Éster Álcali Jabón Alcohol - Autoxidación. Los ácidos grasos insaturados se pueden oxidar espontáneamente, originando aldehídos donde existían los dobles enlaces. La posterior polimerización de estos aldehídos genera el proceso conocido como enranciamiento. Para evitar esta reacción, los organismos disponen de sustancias antioxidantes, la más común de las cuales es la vitamina E, que se encuentra en el aceite de oliva virgen. 1.4.3. Acilglicéridos, ceras y fosfolípidos. • Estructura de los acilgicéridos Son lípidos saponificables formados por la esterificación de una molécula del alcohol glicerina con 1, 2 o 3 ácidos grasos. Según esto, tenemos: monoacilglicéridos, diacilgicéridos y triacilglicéridos. Las cadenas de los acidos grasos pueden ser iguales o diferentes, saturadas o insaturadas • Propiedades de los acilglicéridos • • • • Son insolubles en agua. Son saponificables frente a bases. Se hidrolizan por acción de las enzimas lipasas. Su punto de fusión depende de la longitud de la cadena y de su grado de insaturación. • Clasificación: • • Aceites (grasas líquidas). Se encuentran en las plantas oleaginosas, bien en el fruto (aceite de oliva) o en la semilla (aceite de girasol). Su fluidez se debe a la presencia de ácidos grasos insaturados. • Mantecas o sebos (grasas sólidas). Como la grasa de cerdo. Los ácidos grasos son saturados. Funciones de los acilglicécridos • • • Reserva energética. Son las moléculas que generan más cantidad de energía: un gramo de grasa metabolizado produce 9 Kcal. más del doble que un gramo de glúcido (3,75 Kcal/g). Actúan como amortiguadores mecánicos en algunos órganos. Aislantes térmicos (panículo adiposo de los animales). Ceras Son moléculas sólidas que resultan de la esterificación de un ácido graso de cadena larga con un alcohol monovalente también de cadena larga (28-30 carbonos). Solidas a tª ambiente, bajo punto de fusión. Debido a su elevado grado de insolubilidad las ceras desempeñan principalmente una función de protección, por lo que pueden aparecer recubriendo la superficie de órganos vegetales (fruto, tallo), como impermeabilizante de algunas estructuras tegumentarias de los animales (por ejemplo, las plumas de las aves) o en los panales construidos por las abejas. • Fosfolípidos: estructura, propiedades y funciones • Estructura molecular de los fosfolípidos Los fosfolípidos más importantes son triésteres de glicerina, pero de los tres ácidos unidos a ella, dos son ácidos grasos y el tercero es un ácido ortofosfórico, ésta molécula se denomina ácido fosfatídico. Su unión posterior con un aminoalcohol origina el fosfolípido completo. Propiedades de los fosfolípidos Los fosfolípidos se caracterizan por su comportamiento anfipático, es decir, tienen una parte polar (y, por tanto, soluble en agua) y otra apolar (insoluble). La primera corresponde a la posición donde se sitúan el ácido ortofosfórico y el aminoalcohol, mientras que la segunda corresponde al resto de la molécula (ácidos grasos). En medio acuoso se disponen formando bicapas, en las cuales las cabezas polares quedan en contacto con el agua y las colas apolares enfrentadas entre sí. Funciones de los fosfolípidos De su comportamiento anfipático deriva su función biológica estructural. Todas las membranas celulares están constituidas por una doble capa fosfolípidica en la que las colas apolares de ambas capas quedan enfrentadas entre sí, mientras que las cabezas polares se orientan hacia el medio externo e interno, ambos acuosos. 1.4.4.Carotenoides y esteroides Son lípidos insaponificables, los cuales no contiene ácidos grasos en su composición, y por tanto, no llevan a cabo la reacción de saponificación. • Terpenos: propiedades y funciones. Son polímeros de la molécula isopreno. Están ampliamente difundidos en la naturaleza y tiene una gran importancia biológica. Dentro de este grupo se encuentran: los aceites esenciales de las plantas que les confieren olor y sabor característicos; pigmentos como el fitol que forma parte de la clorofila, la vitamina A o retinol, que interviene en los procesos de visión, la vitamina E o antioxidante, y la vitamina K que es antihemorrágica; pigmentos que colaboran con la clorofila en la fotosíntesis, como las xantofilas y los carotenos, de estos últimos el β caroteno es precursor de la vitamina A. Los carotenoides son tetraterpenos. • Esteroides: propiedades y funciones. Derivan del esterano (ciclopentano perhidrofenantreno). Comprenden moléculas muy activas biológicamente: - El colesterol. Confiere estabilidad a las membranas de las células animales. También se encuentra en el plasma unido a proteínas. Es precursor de otros esteroides como los que figuran a continuación. - Hormonas suprarrenales: aldosterona (favorece retención de agua y Na y la eliminación de K en el riñón); cortisol (regula el metabolismo de los glúcidos). - Hormonas sexuales: Progesterona (hormona del embarazo), testosterona (regula caracteres sexuales masculinos) y estrógenos (regulan caracteres sexuales femeninos). - Sales biliares, que provocan la emulsión de las grasas durante los procesos digestivos. - 7-deshidrocolesterol, molécula que se transforma en la vitamina D3 por la acción de los rayos ultravioleta. La vitamina D favorece la mineralización de los huesos. Su carencia ocasiona raquitismo. • Funciones de los lípidos - Reserva energética: Grasas y aceites. - Estructural: Glicerofosfolípidos, esfingolípidos y colesterol. Formadores de membranas. - Protectora. Ceras y acilglicéridos. Protección mecánica y evitan pérdida de agua. - Transportadora. Lipoproteinas. Transportan lípidos en la sangre. - Reguladora o biocatalizadora: Como precursores de vitaminas y diversas hormonas. - Absorben energía de la luz: Pigmentos fotosíntéticos. Vocabulario • Anfipático. • Carboxilo. • Ester. • Grasa. • Hidrófilo. • Hidrófobo. • Lipófilo. • Lipófobo. • Micela. • Saponificación