Reproduccion 2
Anuncio

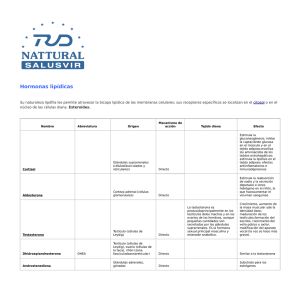
Células de Leydig Síntesis de testosterona regulada por LH Efectos agudos: StAR y esterasas Efectos tróficos: Aumenta la expresión de enzimas esteroidogénicas Estimula la Síntesis de colesterol Aumenta la expresión de receptores para LDL Su falta por HPX o inmunoneutralización provoca: Atrofia de las células de Leydig Pérdida de REL Disminuye la expresión de las enzimas Cit P450scc y Cit P450c17 aunque no desaparecen completamente Tratamiento con LH en: Animales intactos: aumenta todo Animales HPX: restaura todo Animales intactos con exceso de LH: desensibilización Célula de Leydig Relación de Leydig y Sertoli Condición: Pretratamiento de testículos por 48 hs con medio de cultivo o con FSH Pretratamiento Tratamiento Testosterona Medio de cultivo Medio de cultivo control Medio de cultivo LH aumenta FSH LH aumenta mas FSH Medio de cultivo control FSH NO TIENE EFECTO SI SE INCUBAN CÉLULAS DE LEYDIG SOLAS Relación de Leydig con Sertoli Co-cultivo de células de Leydig y Sertoli por 48 hs con: Medio de cultivo: Testosterona control LH dosis máximas: aumenta LH y FSH dosis máximas: aumenta mas FSH dosis máximas: control Medios condicionados de células de Sertoli tratadas con FSH se obtiene: SSP: proteína estimulante de la esteroidogénesis que aumenta la expresión de enzimas esteroidogénicas Otros reguladores de las Células de Leydig Prolactina: receptor de LH IGF-1 LH-dependiente: Promueve reposición de células de Leydig E2: inhibe el efecto de IGF-1 Células de Sertoli Características Constituyen la barrera hematotesticular por uniones estrechas Sincronizan la espermatogénesis Producen: ABP que transporta Testosterona Expresan 5-reductasa: Testosterona a 5-DHT Expresan aromatasa: Testosterona a Estradiol Expresan Inhibina Poseen receptores para FSH pero no para LH FSH: es el factor trófico de estas células. Células de Sertoli ABP: androgen binding protein Transporte de testosterona a epidídimo. FSH: estimula su síntesis. HPX o inmunoneutralización de FSH: disminuye ABP. Inmunoneutralización de LH: también disminuye ABP en circulación. FSH: estimula la secreción a la luz tubular Testosterona: estimula la secreción por la membrana basolateral Células de Sertoli Aromatasa: Su expresión depende de FSH Actividad importante durante período prepuberal. Comienzo pubertad: disminuye su actividad y disminuye estradiol CONSECUENCIA Se desinhibe la proliferación y diferenciación de las células de Leydig. 5-reductasa: Su expresión depende de FSH Regula la actividad de los andrógenos sobre las células de Sertoli. Células de Sertoli Inhibina: Estructura dimérica Su expresión depende de FSH Proteína termolábil que disminuye en criptorquidia. Asociada a aumento de FSH. Inhibe secreción de FSH estimulada por GnRH Factores inductores de la meiosis reduccional Su expresión depende de andrógenos Células de Leydig: Andrógenos Andrógenos: Testosterona: induce la diferenciación del conducto de Wolff en sus diferentes áreas: conducto eferente, epidídimo, conducto deferente, vesícula seminal. 5-DHT: induce la virilización externa (seno urogenital expresa 5-reductasa). De su presencia depende la diferenciación a escroto, pene, uretra, próstata. Estado diferenciado y funcional. Testosterona es el andrógeno testicular mas abundante con ritmos circadianos muy marcados Células de Leydig: Andrógenos Hormona activa en post púberes: Músculo: testosterona, no expresa 5-reductasa. Reproductor: 5-DHT, tienen 5-reductasa Tejido adiposo y algunas áreas cerebrales: aromatizan a estrógenos. Epidídimo Función: maduración espermática. Epidídimo Cambios a lo largo del epidídimo: 1. Motilidad: espermatozoides de cabeza con movimiento circular (temporal) espermatozoides de cola: movimiento direccional Por una proteína que induce la motilidad direccional, andrógeno dependiente (SMP) 2. Metabólicos: 3. Estructurales: 4. Reconocimiento especie-específica (glicoproteínas) 5. Capacidad fecundante: testicular vs cola del epidídimo CAPACITACION: en útero Epidídimo 5-DHT es la hormona activa Castración: regresión del epitelio secretor pérdida de receptores de andrógenos pérdida de 5-reductasa Tratamiento con testosterona: no restaura la funcionalidad: ABP Próstata: inhibidores de 5-reductasa Vesícula seminal: ídem epidídimo Músculo esquelético y cardíaco: hipertrofia pero no hiperplasia Hígado: dimorfismo andrógeno dependiente. Enzima 15-hidroxilasa Metabolismo lipídico: LDL y triglicéridos aumentan HDL disminuye Glándula mamaria: ginecomastia, relación T/E 2 Vello y 5-reductasa: hirsutismo SISTEMA NERVIOSO DIMORFISMO Núcleo Sexual dimórfico del área preóptica: Rata: 7 veces mas grande en ♂ que ♀ ORX de ♂ (orquiectomía) perinatal adulto con núcleo de ♀ ORX de ♂ perinatal + Testosterona adulto con núcleo de ♂ Free Martin ♀ perinatal + Testosterona adulto con núcleo de ♂ ♀ perinatal + Estradiol adulto con núcleo de ♂ ORX de ♂ perinatal + Estradiol adulto con núcleo de ♂ ROL DE AROMATIZACION A: Macho adulto B: Hembra adulta NÚCLEO SEXUAL DIMÓRFICO DEL ÁREA PREÓPTICA ♂>♀ C: Hembra expuesta a estrógenos D: Hembra expuesta a testosterona MASCULINIZACIÓN POR: C.- ESTRÓGENOS D.- TESTOSTERONA SISTEMA NERVIOSO Amígdala Medial Area extrahipotalámica que controla el comportamiento sexual Mayor tamaño y mayor número de sinápsis en el ♂ Feromonas y órgano vomeronasal ROL DE AROMATIZACION: NO Andrógenos y hembras adultas SISTEMA NERVIOSO Centro tónico y centro cíclico del HIPOTALAMO Áreas que controlan la producción de GnRH Centro tónico: Hipotálamo Medio Basal (en ♀ y ♂) Centro cíclico: Hipotálamo anterior (solo en ♀) ROL DE AROMATIZACION para la pérdida del centro cíclico OTRAS AREAS DIMORFICAS Núcleo espinal bulbar: inerva el cuerpo cavernoso ♀ tienen 1/3 de las motoneuronas que el ♂ Testosterona determina el número de neuronas 5-DHT determina el tamaño neuronal ROL DE 5-reducción Deficiencia de andrógenos Mutación del receptor de andrógenos a: macho; b: hembra OTRAS AREAS DIMORFICAS Gánglio cervical superior: inerva la glándula tiroides ♀ tiene menor tamaño que en el ♂ ♀ + Testosterona: aumenta el número de neuronas Pero no el tamaño neuronal que depende de 5-DHT ♀ sin 5-reductasa en el gánglio LIBIDO Andrógeno dependiente ♂ de rata castrados: disminuye comportamiento sexual Tratamiento con testosterona: restaura la libido Tratamiento con testosterona + inhibidores de aromatasa: se restaura parcialmente el comportamiento sexual Tratamiento con testosterona + inhibidores de 5reductasa restaura parcialmente el comportamiento sexual Se requiere 5-reducción y aromatización ¿QUÉ DETERMINA LA DIFERENCIACION SEXUAL EN MAMIFEROS? Genes SRY Genes SRY: responsables de la determinación testicular REGION DETERMINANTE DEL SEXO GONADAL Bipotencialidad Señal de dimorfismo gonadal Células de Sertoli agregadas en forma de cordones Testículo Fetal Humanos: 51 dpo Rata: 13 dpc Ovario humano: 224 dpo folículos primordiales 11 12 12,5 13 Células de Pre-Sertoli secretan Hormona anti Mulleriana (dímero glicosilado) Castración in utero de ♂ Fenotipo ductal femenino DESARROLLO FENOTIPO ♀ NO DEPENDE DE LAS GONADAS Células de Pre-Sertoli secretan Hormona anti Mulleriana 11.5 dpc en rata 49 dpo en humanos Sensibilidad del Conducto de Muller Hasta 13 dpc en rata Hasta 51 dpo en humanos Células de Pre-Sertoli secretan Hormona anti Mulleriana Castración in utero de ♂ Fenotipo ductal femenino DESARROLLO FENOTIPO ♀ NO DEPENDE DE LAS GONADAS La organización testicular es independiente de las células germinales Células de Pre-Leydig secretan Testosterona 19 dpc en rata 98 dpo en humanos Derivadas de las células de la cresta neural Por lo menos dos generaciones Fetales; Postpuberales Desarrollo inicial LH-independiente Células de Pre-Leydig secretan Testosterona Castración in utero de ♂ No involuciona el Conducto de Muller No desarrolla el Conducto de Wolff Tratamiento con antagonistas del receptor de andrógenos Involuciona el Conducto de Muller No desarrolla el Conducto de Wolff Testículo Células de Sertoli Células de Leydig Hormona Anti Mulleriana DHT testosterona 5-reductasa Conducto de Muller (ducto paramesonéfrico) Conducto de Wollff (ducto paramesonéfrico) Regresión Ducto eferente Epidídimo Ducto deferente Vesícula seminal Ducto eyaculatorio Seno urogenital indiferenciado Pene, escroto Próstata, uretra Estímulos externos e internos Hipotálamo Medio basal (centro tónico) Fotoperíodo 5 sentidos GnRH (en circulación atrofia gonadal) Hipófisis (gonadotrofos) LH Células de Leydig Testosterona Caracteres Sex 2rios Testosterona Feedback FSH + Meiosis reduccional Células de Sertoli ABP 5-reductasa Aromatasa Inhibina LH: sobre GnRH Soma: síntesis Preterminal: secreción Estradiol y testosterona: sobre GnRH Soma: síntesis Estradiol y testosterona: sobre LH Síntesis GnRH sobre GnRH Inhibina: sobre FSH Síntesis Pulsatilidad intrínseca Como se modifica la frecuencia de los pulsos? Neuronas GnRH con receptores para GnRH Acoplados a Gi y a Gs Concentraciones nM: se acopla a Gs Concentraciones μM: se acopla a Gi Control autocrino Estructura GnRH Polipéptido de 10 aminoácidos 3 genes distintos gnrh1, gnrh2 y gnrh3 3 sistemas con distinta localización Sistema 1: hipofisotropo piroGlu-His-Trp-Ser-Tyr-Gly-Leu-Arg-Pro-Gly-NH2 mGnRH Prepúber: 5-reductasa Pubertad 17β-deshidrogenasa (LH)