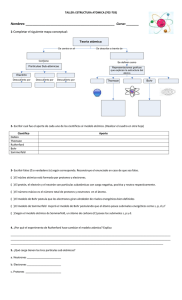
El modelo atómico de Bohr funcionaba muy bien para el
Anuncio

modificó el modelo atómico de Bohr, en el cual los electrones sólo giraban en órbitas circulares, al decir que también podían girar en órbitas elípticas más complejas y calculó los efectos relativis atomo El átomo es la unidad de materia más pequeña de un elemento químico que mantiene su identidad o sus propiedades, Insuficiencias del modelo de Bohr El modelo atómico de Bohr funcionaba muy bien para el átomo de hidrógeno, sin embargo, en los espectros realizados para átomos de otros elementos se observaba que electrones de un mismo nivel energético tenían distinta energía, mostrando que existía un error en el modelo. Su conclusión fue que dentro de un mismo nivel energético existían subniveles, es decir, energías ligeramente diferentes. Además desde el punto de vista teórico, Sommerfeld había encontrado que en ciertos átomos las velocidades de los electrones alcanzaban una fracción apreciable de la velocidad de la luz. Sommerfeld estudió la cuestión para electrones relativistas. y que no es posible dividir mediante procesos químicos. Está compuesto por un núcleo atómico, en el que se concentra casi toda su masa, rodeado de una nube de electrones. El núcleo está formado por protones, con carga positiva, y neutrones, eléctricamente neutros.nota 1 Los electrones, cargados negativamente, permanecen ligados a este mediante la fuerza electromagnética. Los átomos se clasifican de acuerdo al número de protones y neutrones que contenga su núcleo. El número de protones o número atómico determina su elemento químico, y el número de neutrones determina su isótopo. Un átomo con el mismo número de protones que de electrones es eléctricamente neutro. Si por el contrario posee un exceso de protones o de electrones, su carga neta es positiva o negativa, y se denomina ion. El nombre átomo proviene del latín atomum, y éste del griego ἄτομον, sin partes; también, se deriva de «a» (no) y «tomo» (divisible); no divisible.1 El concepto de átomo como bloque básico e indivisible que compone la materia del universo fue postulado por la escuela atomista en la Antigua Grecia. Sin embargo, su existencia no quedó demostrada hasta el siglo XIX. Con el desarrollo de la física nuclear en el siglo XX se comprobó que el átomo puede subdividirse en partículas más pequeñas.2 3 Los átomos son objetos muy pequeños con masas igualmente minúsculas: su diámetro y masa son del orden de la billonésima parte de un metro y cuadrillonésima parte de un gramo. Solo pueden ser observados mediante instrumentos especiales tales como un microscopio de efecto túnel. Más de un 99,94%