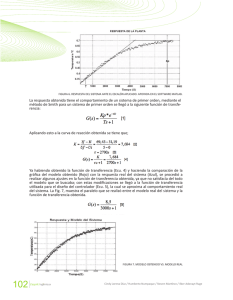
CAPITULO I Y II
Anuncio

PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR SEDE IBARRA PUCE - SI ESCUELA DE CIENCIAS AGRÍCOLAS Y AMBIENTALES E.C.A.A. INFORME FINAL DE TESIS PREVIO A LA OPTENCIÓN DEL TÍTULO DE INGENIERÍA AGROPECUARIA TÍTULO: “CARACTERIZACIÓN MOLECULAR DE LA COLECCIÓN DE AJIES (Capsicum spp) y CALABAZAS (Cucurbita spp.) DEL BANCO DE GERMOPLASMA DEL INSTITUTO NACIONAL AUTÓNOMO DE INVESTIGACIONES AGROPECUARIAS (INIAP), ECUADOR.” AUTORA: Diana M. Farinango Cervantes ASESOR: Biol. Galo Pabón. IBARRA- 2007 AUTORIA Declaro que la presente investigación es de total responsabilidad de la autora …………………………………… Diana María Farinango Cervantes C.I. 100211737-0 2 PRESENTACIÓN La presente investigación titulada “Caracterización Molecular de la Colección de Ajíes (Capsicum spp. L.) y Calabazas (Cucurbita spp. L.) del Banco de Germoplasma del Instituto Nacional Autónomo de Investigaciones Agropecuarias (INIAP), Ecuador.” está conformada por cinco capítulos que se detalla a continuación. El Capítulo I, está conformado por: planteamiento del problema el mismo que detalla los problemas relacionados con los cultivos de ají y calabazas, debido a la pérdida de variedades puras y la proliferación de plagas y enfermedades; justificación se menciona la importancia de la caracterización molecular para identificar material promisorio, así como la conservación de germoplasma; objetivos se plantea estudiar la variabilidad genética de la colección de ají y calabazas mediante la caracterización molecular empleando la técnica de RAPDs. En el Capítulo II, se detalla la revisión bibliográfica de los cultivos de ají y calabazas y la técnica molecular RAPDs, obtenida en libros y páginas web disponibles. En el Capítulo III, se describe la metodología como: los protocolos empleados en la fase experimental y el análisis estadístico aplicado a los resultados obtenidos. En el Capítulo IV, se presenta los resultados obtenidos y una discusión referente a la caracterización morfológica y molecular. El Capítulo V comprende, conclusiones y recomendaciones del presente estudio. 3 DEDICATORIA A DIOS por darme la fuerza necesaria para seguir adelante. A mis padres Carlos y María, quienes supieron guiarme e inculcarme valores morales y éticos durante mi formación profesional, así como también por todo el apoyo que me brindaron durante los momentos más difíciles de mi vida. Gracias por todo su apoyo y amor A mi hermano Danny por el cariño y la amistad brindada, a demás de ser mi motivación. A la memoria de mi abuelita Flora por su cariño, cuidado y dedicación mientras estuvimos juntas. 4 AGRADECIMIENTO Al culminar la presente tesis de grado, misma que es requisito fundamental para la obtención del título profesional de Ingeniería Agropecuaria, quiero dejar constancia de mi más sincero agradecimiento a la Universidad Católica del Ecuador Sede Ibarra por haberme formado profesionalmente durante 6 años; junto a todos aquellos docentes quienes con su tiempo y conocimiento supieron inculcarme los más altos valores morales y éticos. Al INIAP y especialmente al DENAREF por el apoyo brindado para la ejecución de la presente investigación. Al Ing. César Tapia, Biol. Gabriela Piedra, y al Dr. Eduardo Morillo por la asistencia técnica recibida durante la realización de esta investigación. Así también a todo el personal técnico del DENAREF por el compañerismo y amistad brindados. Al Biol. Galo Pavón por la amistad y apoyo al aportar con sus conocimientos técnicos en el desarrollo de esta tesis. A mis compañeros y amigos de la promoción 2000”B” quienes con sus consejos supieron alentarme durante el difícil camino de mi carrera profesional. A mis amigas Doris, Priscila y Anita quienes me apoyaron en todo momento compartiendo sus conocimientos y sobre todo su amistad. 5 RESUMEN Esta investigación que consta de dos partes fue desarrollada en el Departamento Nacional de Recursos Filogenéticos y Biotecnología (DENAREF) del INIAP. La primera parte se centra a la caracterización molecular de 71 accesiones de ají (Capsicum spp), en cambio en la segunda se caracteriza a 25 accesiones de calabazas (Cucurbita spp). Se utilizaron cuatro análisis, análisis de agrupamiento (UPGMA), análisis de coordenadas principales (PCO), boostrap, y análisis de varianza molecular (AMOVA). Los resultados más sobresalientes son: para ají, el análisis UPGMA determinó 5 gurpos sugiriendo una estrecha relación genética entre las 6 especies, así también el análisis PCO determinó 5 grupos donde a demás identificó al ecu 2261 como una mezcla varietal entre las especies C. annum y C. chinense, al igual que al ecu 12846 como otra mezcla varietal de las especies C annum y C. baccatum; por otra parte el análisis boostrap determinó la robustez estadística de los ecus 5429, 5444, 5445, 5462, 5463, 5371 de la especie C. annum con un valor de 81%; el análisis AMOVA determinó que un 23% de la varianza aporta a la diferenciación de las 5 especies analizadas, mientras que el 77% aporta a la diversidad intraespecífica. Los resultados para calabazas son: el análisis UPGMA determinó 4 grupos sugiriendo una diferenciación genética entre las especies analizadas, el análisis PCO determinó 3 grupos donde se observa una significativa diferencia a nivel molecular de cada una de las especies, el análisis boostrap determinó una robustez estadística de la especie C. pepo con un valor de 72%, por último el análisis AMOVA determinó que un 38% de la varianza aporta a la diferenciación de las 3 especies, mientras que el 62% aporta a la diversidad intraespecífica. Palabras Claves: UPGMA, PCO, Boostrap, AMOVA. 6 ABSTRACT This research consisting in two parts was carried out at the National Department of Phylogenetic Resources and Biotechnology (DENAREF) of INIAP. The first part was focussed on the molecular characterization of 71 assents of red hot chilli pepper (Capsicum spp.), and in the second one 25 assents of pumpkins (Cucurbita spp.) were characterized. Four kinds of analysis were used, grouping analysis (UPGMA), main coordinates analysis (PCO), boostrap and molecular varieties analysis (AMOVA). The most outstanding results were: for red hot chilli pepper, the analysis UPGMA determined 5 groups suggesting a narrow genetic relationship between the 6 species, as well as the analysis PCO determined 5 groups where ecu 2261 as a mixture of several kinds of varieties was identified between the species C. annum and C. chinense, as well as ecu 12846 as a mixture of varieties of the species C. annum and C. baccatum. On the other hand, the boostrap analysis determined the statistic robustness of the ecus 5429, 5444, 5445, 5462, 5463, 5371 and the species C. annum with the value 81%. The AMOVA analysis determined that 23% of the kinds of varieties contribute to the differentiation of the 5 analysed species, while 77% contributes to the intraspecific diversity. The result for pumpkins are: the UPGMA analysis determined 4 groups suggesting a genetic differentiation between the analysed species, PCO analysis determined 3 groups where a notable difference at a molecular level of each of the species is observed, the boostrap analysis determined a statistic robustness of the species C. pepo with the value 72%, and finally the AMOVA analysis determined that 38% of the variety contributes to the differentiation of the 3 species, while 62% are contributed by the intraspecific diversity. 7 PORTADA…………………………………………………………………………...1 PRESENTACIÓN…………………………………………………………………..3 DEDICATORIA……………………………………………………………………...4 AGRADECIMIENTO………………………………………………………………..5 RESUMEN…………………………………………………………………………..6 Abstrac……………………………………………………………………………….7 INDICE……………………………………………………………………………….8 CAPÍTULO I INTRODUCCIÓN 1.1 PLANTEAMIENTO DEL PROBLEMA……………………………………...15 1.2 JUSTIFICACIÓN……………………………………………………………..17 1.3 OBJETIVOS…………………………………………………………………..19 1.3.1 OBJETIVO GENERAL………………………………………………19 1.3.2 OBJETIVOS ESPECÍFICOS……………………………………….19 1.4 HIPÓTESIS……………………………………………………………………19 CAPÍTULO II MARCO TEÓRICO 2.1 CULTIVO DE AJÍ (Capsicum L.) 2.1.1 Origen, taxonomía e importancia del cultivo de ají……………………..20 2.1.2 Clasificación taxonómica…………………………………………………..21 2.1.3 Descripción botánica……………………………………………………….21 2.1.4 Ecología y adaptación……………………………………………………..23 2.1.5 Métodos de propagación…………………………………………………..23 2.1.6 Prácticas culturales y producción…………………………………………24 2.1.7 Control de principales plagas y enfermedades…………………………24 2.1.8 Tecnología de cosecha y poscosecha…………………………………...25 2.1.9 Formas de utilización ……………………………………………………...25 2.2 CULCTIVO DE CALABAZAS (Cucurbita spp.) 2.2.1 Origen, taxonomía e importancia del cultivo de calabazas………….26 2.2.2 Clasificación taxonómica: según Jeffrey (1990) ………………………27 2.2.3 Descripción botánica………………………………………………………27 2.2.4 Ecología y adaptación……………………………………………………..29 2.2.5 Métodos de propagación………………………………………………….30 2.2.6 Prácticas culturales y producción………………………………………...30 2.2.7 Control de principales plagas y enfermedades…………………………30 2.2.8 Tecnología de cosecha y poscosecha…………………………………..30 8 2.2.9 Formas de utilización………………………………………………………31 2.3 Caracterización molecular…………………………………………………...33 2.3.1 Marcadores moleculares………………………………………………......33 2.3.2 Reacción en cadena de la polimerasa (PCR)…………………………...35 2.3.3 Polimorfismo del ADN amplificado al azar (RAPDs)……………………37 2.3.4 Ventajas de los RAPDs……………………………………………………39 2.3.5 Desventajas de los RAPDs………………………………………………..40 2.3.6 Relación entre caracterización morfológica y molecular……………….40 CAPÍTULO III MATERIALES Y MÉTODOS 3.1 MATERIALES 3.1.1 DE CAMPO………………………………………………………………….42 3.1.1.1 Insumos……………………………………………………………………42 3.1.1.2 Herramientas……………………………………………………………..42 3.1.1.3 Recurso humano…………………………………………………………42 3.1.1.4 Material de oficina………………………………………………………..42 3.1.2 DE LABORATORIO………………………………………………………..43 3.1.2.1 Materiales de Laboratorio……………………………………………….43 3.1.2.2 Reactivos………………………………………………………………….44 3.2 MÉTODOS…………………………………………………………………….45 3.2.1. UBICACIÓN………………………………………………………………..45 3.2.2. DESCRIPCIÓN DE LA INVESTIGACIÓN………………………………45 3.2.2.1 Caracterización molecular………………………………………………45 3.2.2.2 Primers evaluados……………………………………………………….51 3.2.3. Análisis estadístico para datos moleculares…………………………..52 3.2.3.1 Análisis PCO……………………………………………………………...55 3.2.3.2 Análisis de varianza molecular (AMOVA)……………………………..55 3.2.3.3 Boostrap…………………………………………………………………..55 3.2.4. Relación de datos morfológicos y moleculares………………………...56 CAPÍTULO IV RESULTADOS Y DISCUCIÓN 4.1 Resultados y discusión………………………………………………………57 4.1.1 Datos pasaporte (Género Capsicum.)……………………………………57 4.1.2 Género Capsicum L………………………………………………………..57 4.1.2.1 Caracterización molecular de Capsicum L……………………………57 4.1.2.2 Productos de amplificación……………………………………………...59 9 4.1.2.3 Similitud genética………………………………………………………...60 4.1.2.4 Análisis de agrupamiento (UPGMA)…………………………………...60 4.1.2.5 Análisis de coordenadas principales (PCO)…………………………..63 4.1.2.6 Distancia genética de nei………………………………………………..66 4.1.2.7 Análisis de Varianza Molecular (AMOVA)…………………………….66 4.1.2.8 Correlación entre marcadores morfológicos y moleculares………....67 4.2.1 Datos pasaporte (Género Cucurbita.)……………………………………68 4.2.2 Género Cucurbita L……………………………………………………......68 4.2.2.1 Caracterización molecular de Cucurbita L……………………………68 4.2.2.2 Productos de amplificación……………………………………………...69 4.2.23 Similitud genética…………………………………………………………70 4.2.2.4 Análisis de agrupamiento (UPGMA)…………………………………...70 4.2.2.5 Análisis de coordenadas principales (PCO)…………………………..72 4.2.2.6 Distancia genética de nei……………………………………………….74 4.2.2.7 Análisis de varianza molecular (AMOVA)…………………………….74 4.2.2.8 Correlación entre marcadores morfológicos y moleculares………...75 4.3 Hipótesis………………………………………………………………………75 CAPÍTULO V CONCLUSIONES Y RECOMENDACIONES 5.1 Conclusiones género (Capsicum L.)………………………………………..76 5. 2 Conclusiones género (Cucurbita L.)……………………………………….78 5.3 Recomendaciones …………………………………………………………...79 10 Lista de Cuadros Cuadro 4.1 Rendimiento de ADN de 71 accesiones de Capsicum L. de germoplasma del DENAREF – INIAP…………………………………………58 Cuadro 4.2 Lista de primers analizados (C. capsicum L)59 Cuadro 4.3 Lista de los 5 primers polimórficos seleccionados con sus respectivas secuencias de nucleótidos, rango de amplificación y número de polimorfismos evaluados (C. capsicum L.)…………………………………...59 Cuadro 4.4 Matriz de distancia genética de nei. ………..66 Cuadro 4.5 Análisis de bandas binarias por población…67 Cuadro 4.6 Rendimiento de ADN de 25 accesiones de Cucurbita L. de germoplasma del DENAREF – INIAP………………………………………….68 Cuadro 4.7 Lista de primers analizados (C. cucurbita L)69 Cuadro 4.8 Lista de los 8 primers polimórficos seleccionados con sus respectivas secuencias de nucleótidos, rango de amplificación y número de polimorfismos evaluados (C. cucurbita L.)……………………………………69 Cuadro 4.9 Matriz de distancia genética de nei…………74 Cuadro 4.10 Análisis de bandas binarias por población…74 11 Lista de Figuras Figura 3.1 Extracción del ADN genómico………………47 Figura 3.2 Cuantificación de ADN en geles de agarosa………………………………………...49 Figura 3.3 Scriniing de Capsicum, primers OPA12, OPA18, OPA 20, OPAN 02, OPAS 01; scriniing para cucúrbitas primers OPA 09, OPA 12, OPA 19, OPAC 03, OPAC 05, OPAC 08, OPAC 09, OPAC 11……………………..51 Figura 3.4 Figura 3.4. Evaluación de primers, scriniing de capsicum y cucúrbitas ………………………53 Figura 4.1 Perfiles RAPDs obtenidos en Capsicum L. con el primer OPA – 20. Carriles 1 – 29 ADN amplificado. A la izquierda el tamaño en pares de bases (pb) de algunas bandas polimórficas evaluadas. (M) Marcador. Ecu 2231, Ecu 2233,Ecu 2236, Ecu 2242, Ecu 2243, Ecu 2249, Ecu 2252, Ecu 2258, Ecu 2259, Ecu 2261, Ecu 2262, Ecu2263, Ecu 2264, Ecu 2265, Ecu 2266, Ecu 2267, Ecu 2268, Ecu 2269, Ecu 2270, Ecu 2271, Ecu 3834, Ecu 5347, Ecu 5357, Ecu 5429, Ecu 5444, Ecu 5445, Ecu 5462, Ecu 5463, Ecu 5371…………………………………………….60 Figura 4.2 Dendograma en base a datos moleculares de la colección de Ají (Capsicum L.) usando el coeficiente de Jaccard, agrupamiento UPGMA y Boostrap. ……………………………………62 12 Figura 4.3 Distribución en el plano definido por el primer y segundo eje (C1 y C2) del PCO basado en el coeficiente de similitud de Jaccard en la comparación dos a dos de 71 accesiones de ají (Capsicum L.) con 36 polimorfismos RAPDs………………………………………….65 Figura 4.4 Perfiles RAPDs obtenidos en Cucurbita L. con el primer OPAC – 11. Carriles 1 – 25 ADN amplificado. A la izquierda el tamaño en pares de bases (pb) de algunas bandas polimórficas evaluadas. (M) Marcador, (-) Control Negativo, Ecu 4976, Ecu 4977, Ecu 4978, Ecu 4979, Ecu 4980, Ecu 4981, Ecu 4983, Ecu 4984, Ecu 4992, Ecu 5308, Ecu 5309, Ecu 5310, Ecu 5311, Ecu 5312, Ecu 5313, Ecu 5326, Ecu 5329, Ecu 5330, Ecu 5338, Ecu 5343, Ecu 12382, Ecu 12393, Ecu 12399, Ecu 12400, Ecu 12408…………………………….70 Figura 4.5 Dendograma en base a datos moleculares de la colección de calabazas (Cucurbita L.) usando el coeficiente de Jaccard, agrupamiento UPGMA y boostrap. …………72 Figura 4.6 Distribución en el plano definido por el primer y segundo eje (C1 y C2) del PCO basado en el coeficiente de similitud de Jaccard en la comparación dos a dos de 25 accesiones de calabazas (Cucurbita L.) con 36 polimorfismos RAPDs…………………………………………73 13 Lista de Anexos Anexo 1 Datos pasaporte de la colección nacional de Capsicum L. Anexo 2 Matriz básica de datos (MBD) generada a partir de datos moleculares de Capsicum L. Anexo 3 Matriz de similitud generada a partir de datos moleculares de Capsicum L. Anexo 4 Registro fotográfico de Capsicum L. Anexo 5 Datos pasaporte de la colección nacional de Cucurbita L. Anexo 6 Matriz básica de datos (MBD) generada a partir de datos moleculares de Cucurbita L. Anexo 7 Matriz de similitud generada a partir de datos moleculares de Cucurbita L. Anexo 8 Registro fotográfico de Cucurbita L. 14 CAPÍTULO I INTRODUCCIÓN 1.1 PLANTEAMIENTO DEL PROBLEMA La zona andina constituye uno de los principales centros de diversificación y domesticación de plantas cultivadas en el mundo. Es así que la diversidad y disponibilidad de recursos vegetales de interés económico sea más grande en países como Ecuador; donde la agricultura ha tenido un proceso dinámico de desarrollo y modernización, contribuyendo a que desaparezcan especies de importancia económica (Tapia et al. 1996). Los ajíes pertenecen al orden Solanales, familia solanaceae, y género Capsicum; se adapta a climas tropicales húmedos y suelos con buen drenaje, puede ser utilizado desde condimento en los alimentos hasta la medicina, además de tener un alto potencial para ser utilizado en la elaboración de productos deshidratados, de ahí su importancia para el cultivo de este género. El cultivo de calabazas que pertenece al orden violaceae, familia cucurbitaceae, y género Cucurbita L., se adapta a ecologías diferentes y suelos bien abonados, es consumido en sopas, dulces, etc; así como también puede ser aplicado en la medicina; sin embargo la importancia económica de este cultivo no es tan representativa como el ají. Estos son dos ejemplos representativos de la gran variabilidad genética y morfológica en casi todo el mundo, principalmente en Perú y Bolivia. En la actualidad la diversidad de estas especies ha disminuido drásticamente debido a diferentes causas como por ejemplo la creencia de que estas especies atraen a culebras, la influencia de la cultura occidental, así como la erosión genética que produce la pérdida de recursos 15 filogenéticos o germoplasma vegetal, lo que constituye una amenaza a la seguridad alimentaria local y regional. De acuerdo a datos presentados en un seminario con comunidades de Cotacachi, se puede apreciar que en estos dos cultivos existe una disminución marcada de los nombres vulgares o tradicionales con que se conoce a estos productos (Tapia, C. 2004, citado por Pavón, G. 2004) Por otra parte la utilización de marcadores moleculares basados en caracteres morfológicos particularmente en plantas se ha empleado desde que el hombre practica la agricultura, y ha seleccionado individuos con características que forman la base de fitomejoramiento de una variedad y con una propiedad agronómica específica. (1) En el Ecuador la investigación científica apenas ha iniciado por lo que, los resultados en muchos casos son únicamente preliminares, es así que el Instituto Nacional de Investigaciones Agropecuarias (INIAP) ha conformado un Banco de Germoplasma el cual esta en proceso activo de caracterización, evaluación y potenciación genética desde 1980. La caracterización morfoagronómica y molecular son fundamentales, ya que permiten la identificación de materiales promisorios para fitomejoradores, agricultores conservacionistas, con el fin de estimular su uso en la agricultura, la industria, etc. 16 1.2 JUSTIFICACIÓN Los problemas agronómicos relacionados con producción, adaptabilidad, patología y entomología pueden ser mejorados a través de la identificación de materiales promisorios de cada uno de estos cultivos. El potencial genético que representan las especies de ajíes y calabazas son, entre otros cultivos, afectados por la erosión genética, por lo que es urgente plantear estrategias y métodos que permitan proteger estos recursos genéticos. Ya que estos cultivos son importantes en la seguridad alimentaria, así como en la economía a pesar de la marginación de algunas de sus especies. La colección, caracterización, evaluación y conservación de germoplasma es base primordial para rescatar y difundir las especies y variedades que pertenecen a estos géneros y utilizarlas a demás en proyectos de Turismo Comunitario, que actualmente se desarrollan en comunidades agrupadas de la Unión de Organizaciones Campesinas de Cotacachi (UNORCAC). Es por eso que a través de esta investigación se puede establecer semejanzas y diferencias entre diferentes tipos y variedades de dichos cultivos de una misma especie, permitiendo desarrollar estrategias que potencien aun más su uso dentro de una política de desarrollo sustentable. Es así que para recuperar y promover estos cultivos se puede establecer las características sistemáticas de los grupos, especies, variedades, tipos, etc; su nominación científica (revisión taxonómica) así como las semejanzas y diferencias categóricas que se establecen a través de una caracterización molecular. Ya que con la utilización de nuevas técnicas de biología molecular se puede explorar la variación de secuencias a nivel de ADN de cada uno de los individuos en estudio permitiendo distinguir entre genotipos estrechamente 17 relacionados. Lo que permite establecer una relación más especificas entre cada una de las especies a través de una caracterización morfológica y molecular. Permitiendo crear estrategias de desarrollo sustentable a través de bases científicas. El Departamento Nacional de Recursos Fitogenéticos y Biotecnología (DENAREF) del INIAP dispone de una colección de 71 entradas de ají y 25 entradas de calabazas, mismos que fueron descritos completamente para ampliar el conocimiento de estos cultivos y sus propiedades, permitiendo al investigador plantear trabajos de selección, bioprospección, mejoramiento, etc. 18 1.3 OBJETIVOS 1.3.1 OBJETIVO GENERAL Estudiar la variabilidad genética de 71 accesiones de Capsicum spp. L. (Ajíes) y 25 accesiones de Cucurbita spp. L. (Calabazas) del Banco de Germoplasma del INIAP, mediante la caracterización molecular de sus genotipos. 1.3.2 OBJETIVOS ESPECÍFICOS Caracterizar molecularmente el germoplasma recolectado mediante la técnica de amplificación de ADN al azar (RAPDs) de 71 accesiones de ají y 25 accesiones de calabazas. Determinar la variabilidad genética de los géneros Capsicum. y Cucurbita. Determinar correlaciones entre caracteres morfológicos y moleculares utilizando técnicas de análisis multivariado. 1.4 HIPÓTESIS Las entradas de la colección nacional de ají y calabazas del INIAP presentan variabilidad genética. 19 CAPÍTULO II MARCO TEÓRICO 2.1 Cultivo de ají (Capsicum L.) 2.1.1 Origen, taxonomía e importancia del cultivo de ají El cultivo de Capsicum se remonta a la época precolombina, a través de expediciones arqueológicas realizadas en Tehuacán, México se encontró restos de chile fechados entre 5 y 7 mil años A. C. De igual manera en Sudamérica, se encontraron restos en Ancón y Huaca Prieta en Perú con fechas de más de 2 mil años A. C. (Pozo O., et al., 1991) De acuerdo a bases arqueológicas las especies cultivadas de Capsicum se desarrollaron en tres centros de origen: a) C. annuum en México y Guatemala, b) C. chinense y C. frutescens en la cuenca del Amazonas, y por último c) C. baccatum y C. pubescens en Bolivia y Perú. (Pozo O., et al., 1991) El género Capsicum, al cual pertenece el ají abarca entre 20 y 30 especies originarias de las regiones tropicales y subtropicales de América, probablemente en Perú y Bolivia, ya que se ha encontrado semillas ancestrales de más de 7000 años. (2) Después del descubrimiento de América, estas especies principalmente Capsicum annum, han sido llevadas a distintas regiones del mundo y han pasado a ser el principal condimento de comidas típicas de muchos países. A pesar de que su cultivo es reducido; se encuentra ampliamente extendido, siendo China, Estados Unidos y México los principales productores a nivel mundial. (2) 20 2.1.2 Clasificación taxonómica Según Cronquist (1981): Reino: Plantae División: Magnoliophyta Clase: Magnoliopsida Orden: Solanales Familia: Solanaceae Género: Capsicum L. 2.1.3. Descripción Botánica Son plantas de crecimiento simpodial, sus tallos y ramas se forman de nudos superiores donde generalmente existen yemas floríferas y dos ramillas que forman un dicasio (Cronquis A, 1981, citado por Pavón G. 2004). La rama más grande continúa con su crecimiento, en cuyo nudo superior se repite la norma de inflorescencias y ramas, las hojas son elípticas con ápice agudo y base asimétrica (Brako y Zaruchi, 1993). Generalmente tiene dos flores por nudo con pedicelos erectos o doblados en la antesis, su cáliz es cupular, glabro, con dientes cortos y prominentes. Corola amarillo verdosa, blanco lechoso o morado, anteras azules. Los frutos maduros presentan constricción anular en la unión con el pedicelo, y la pulpa es firme de color rojo o amarillo y, a veces, blanco (Judd et al., 1999) A continuación se describen las principales especies de mayor explotación: Capsicum annuum: Es la especie que presenta mayor variabilidad en cuanto a forma, tamaño y color de frutos. En México se tiene la mayor variabilidad de formas cultivadas y sus parientes silvestres. (Pozo O., et al., 1991) Pozo (1991), cita a Pickersgill (1971) quién propone a C.annumm var. aviculare como la progenitora silvestre de C. annuum domesticada. 21 La planta es herbácea, de hábito perenne en condiciones naturales, pero cultivada como anual en la mayoría de los casos. El sistema radical es pivotante, alcanzando entre 0,7 y 1,2 m de profundidad y un diámetro de 0,5 a 0,9 m alrededor del eje central, las raíces adventicias se generan bajo el hipocótilo. El tallo presenta ramificación dicotómica y sobre las ramas se disponen hojas de tamaño medio, enteras, de forma oval-oblonga, glabras y de color verde intenso. Las flores son perfectas y se presentan solitarias en las axilas de las ramificaciones; su cáliz es dentado, a demás posee cinco pétalos de color blanco y anteras amarillenta-azules o púrpuras. Después de un proceso de autofecundación se inicia el desarrollo del fruto que constituye el órgano de consumo de la especie. (3) Capsicum baccatum L.: Comprende un conjunto de plantas herbáceas de diferente porte y tamaño, con período de vida generalmente menor a un año. Su crecimiento es simpodial; los tallos y ramas se forman de sectores en cuyo nudo superior hay, por lo general, yemas floríferas y dos ramillas que forman un dicasio, una de ellas más desarrollada que la opuesta. La rama más grande continúa el crecimiento y en su nudo superior se repite la norma de inflorescencia y ramas. (4) Hojas generalmente elípticas, con el ápice agudo y la base asimétrica, aunque existe bastante variación. Dos flores por nudo, rara vez una, con pedicelos erectos o doblados en la antesis. El cáliz es cupular, glabro, con los dientes muy cortos y prominentes. Corola amarillo verdosa, ocasionalmente entre blanco lechoso o morado y las anteras azules. Cáliz de los frutos maduros, generalmente con una constricción anular en la unión con el pedicelo; las venas no se prolongan en los dientes; márgenes doblados hacia arriba. Fruto de pulpa firme, rojo o amarillo y, a veces, blanco. (5) Capsicum chinense. Se caracteriza principalmente por la ausencia de cáliz dentado, la corola es de color blanca opaca y su fruto presenta constricción entre la base del cáliz y el pedúnculo. Las formas cultivadas de esta especie 22 son de gran importancia en el mercado mundial lo que le permite competir con la especie C. annuum. (Pozo O., et al., 1991) Capsicum frutescens. Esta especie está muy relacionada con C. chinense, siendo difícil la distinción entre ellas; se caracteriza por presentar corolas de color blanco verdoso, frutos decíduos, no presenta constricción entre la base del cáliz y el pedúnculo. El tipo de chile denominado “tabasco” es el más representativo de la especie, fue introducido de México a Luisiana, EE.UU en 1888; lo cual marco el inicio de la mundialmente famosa “salsa tabasco”. (Pozo O., et al., 1991) Capsicum pubescens. Fue descrita por primera vez por Ruiz y Pavón en 1799, sin embargo permaneció desconocida fuera de Sudamérica hasta la primera mitad del presente siglo, presenta una distribución muy amplia y gran variabilidad genética. Presenta flores de color violeta de forma campanada, la semilla es rugosa de color negro. Según varios investigadores, esta especie fue introducida a México y América Central entre 1930 y 1940. (Pozo O., et al., 1991) El gran problema que presenta esta especie, es que, sus características son silvestres (picante, fruto hueco, planta perenne, abundantes semillas). (6) 2.1.4 Ecología y adaptación Este género se adapta a climas tropicales húmedos con y sin estación seca marcada. Crece bien en condiciones de alta humedad relativa, y altitudes entre el nivel del mar y los 2500 m. s. n. m. Los suelos sueltos con buen drenaje, disminuyen el riesgo de la enfermedad producida por el Fusarium sp. y la marchitez causada por Phytophthora sp. (Bukasov,M:S, 1981). 2.1.5 Métodos de propagación Se propaga por semilla, la germinación se produce a los 15 a 17 días y, después de crecer por 20 a 25 días, se trasplanta a viveros. Se recomienda 23 germinar las semillas en almácigo, trazándose surcos de un centímetro de profundidad y espaciados cada 10 cm. (IPGRI, AVRDC y CATIE, 1995). 2.1.6 Prácticas culturales y producción Después de 45 a 60 días, se trasplantan al sitio definitivo plantas con una altura aproximada de 15 cm. Generalmente el distanciamiento es de un metro entre surcos y 0,5 a 0,6 m entre plantas. (León, J. 1987.) Debe tener buen control de malezas, especialmente hasta la floración y las primeras etapas de fructificación. Al momento del trasplante debe recibir un aporque, efectuándose dos a tres aporques adicionales (IPGRI, AVRDC y CATIE, 1995). 2.1.7 Control de principales plagas y enfermedades Además de ser un cultivo sensible a las bajas temperaturas, es muy susceptible a los hongos como (Phytophthora sp.) que produce la muerte de las plantas cuando éstas ya están fructificando. Esta situación obliga a utilizar el sistema de almácigo y trasplante para su cultivo. Los almácigos deben sembrarse en un suelo o substrato desinfectado. (7) Otra enfermedad que tiene el ají común es la podredumbre del tallo, originada por el hongo Sclerotium rolfsii, que ataca a nivel del suelo. Se controla rotando cultivos y evitando los suelos pesados con mal drenaje. (León, J. 1987.) También es atacada por el perforador del fruto Gnorischema gudmanella, polilla cuyas larvas minan las hojas y penetran en los frutos, y el pulgón Macrosiphurn euphorbidae, que succiona la savia, produciendo amarillamiento, deformación de hojas y brotes, pudiendo marchitar la planta; estas plagas transmiten virus ya que producen un medio adecuado principalmente para el desarrollo del hongo de la fumagina (León, J. 1987.) 24 2.1.8 Tecnología de cosecha y poscosecha En las condiciones actuales no se tienen cuidados especiales durante la cosecha, que se realiza de manera esporádica, ya que no existe un gran mercado para los frutos. El período de cosecha puede durar entre 60 días, en las variedades más herbáceas, hasta varios meses en las variedades herbáceas con tallo leñoso. (IPGRI, AVRDC y CATIE, 1995) 2.1.9 Formas de utilización Presenta múltiples usos, desde condimentos en los alimentos, hasta las aplicaciones medicinales; pasando por la obtención de materia prima, con niveles artesanales e industriales. Se emplea mundialmente en la industria farmacéutica y de alimentos. (Collazos et al., 1975). Recientemente, se ha incorporado la capsaicina, una amida aromática, en los repelentes atomizadores que se expenden para autodefensa. A demás sus múltiples variedades, como por ejemplo largos carnosos, dulces, picantes, etc; pueden cultivarse a nivel industrial, obteniendo productos como condimentos, conservas, pastas, salsas que son muy populares en países de Hispanoamérica como México. Así también puede ser utilizado como estimulante digestivo, para el dolor de cabeza, e incluso para tratar heridas y otras enfermedades de animales. (2), (8) Esta especie, puede ser consumida en fresco, deshidratado ahumado, en salsas, encurtidos, también se puede utilizar como colorante y saborizante. (Pozo O., et al., 1991) Por otra parte el uso de material genético sirve para buscar nuevas fuentes de resistencia a enfermedades fungosas y virosas que atacan al chile como por ejemplo Redondo (1979) detectó 19 colectas de C. annuum denominados “Criollos de Morelos” con resistencia al hongo Phytophthora capsici Leo., que causa la enfermedad denominada “marchites del chile”. (Pozo O., et al., 1991) 25 2.2 Cultivo de calabazas. (Cucurbita spp..) 2.2.1 Origen, taxonomía e importancia del cultivo de calabazas Basándose en evidencias fotogeográficas y en relaciones huésped – parásito se ha sugerido el sur y centro de México como centro de origen de este género, sin embargo algunas especies como C. maxima son nativas de América del Sur. (Nuez F. et. al., 2000) El centro y sur de México forman parte de la región conocida como Mesoamérica, centro de diversidad genética de cerca de 50 especies cultivadas, convirtiéndose en uno de los cultivos originarios más importantes de dicha región. (Hernández S., 1991) Las especies domesticadas de Cucúrbitas son probablemente las plantas más antiguas cultivadas en América, así por ejemplo de acuerdo a evidencias arqueológicas donde se encontró restos de semillas, pedúnculos y cáscara de C. pepo, indican la existencia de poblaciones silvestres de esta especie en México y al este de EE.UU. al rededor de 10000 y 30000 años. (Nuez F. et. al., 2000) Según Lira. R, 1990, la especie C. pepo pudo haberse domesticado cuando menos en dos ocasiones y regiones diferentes, teniendo en cada caso como posibles progenitores a C. fraterna y C. texana respectivamente. Por otra parte la especie C. moschata se cultivaba en México, América del Sur y el sudoeste de los EE.UU en tiempos precolombinos. Sin embargo el ancestro silvestre de esta especie aun se desconoce. Por último la especie C. argyrosperma fue domesticada al parecer al sur de México existiendo evidencias arqueológicas de su cultivo hace 5200 años A.C.. Poblaciones silvestres de la subespecie sororia, que se encuentran en México y América Central dieron lugar a la subespecie domesticada argyrosperma. (Nuez F. et. al., 2000) 26 2.2.2 Clasificación taxonómica: Según Jeffrey (1990): Reino: Plantae División: Magnoliophyta Clase: Magnoliopsida Orden: Violaceae Familia: Cucurbitaceae Género: Cucurbita L. 2.2.3 Descripción Botánica Son plantas monóicas o dioicas, y raramente hermafroditas; rastreras, trepadoras o subarbustivas, las flores pueden ser actinomorfas o ligeramente zigomorfas masculinas o estaminadas poseen estambres en forma de columna donde los filamentos y las anteras se hallan soldados, mientras que las flores femeninas o pistiladas son solitarias con tres estaminoides, un estilo corto y tres a cinco estigmas bilobados; presentan un ovario ínfero tricarpelar con 4 a 5 carpelos en posición horizontal, (Lira. R, 1995 y Nuez. F. et. al., 2000). La corola es de forma tubular – campanulada, los colores van desde amarillo pálido hasta amarillo anaranjado brillante. (Lira. R 1995). Los tallos son híspidos o escabrosos, huecos, angulosos y con tendencia a producir raíces en los nudos (Cronquist A, 1981.).Los frutos de plantas cultivadas son del tipo pepo teniendo una gran variedad de formas, tamaños, colores, texturas, etc. Las plantas silvestres son relativamente uniformes en cuanto a su forma, coloración y tamaño. (Bailey, s/a; Judd et al., 1999. y Lira. R 1995). El género presenta zarcillos ramificados, que en los tipos semierguidos están abortados; las hojas son de lámina simple y lobuladas (Lira R, 1990). Entre las especies cultivadas más importantes para la alimentación se encuentran C. moschata, C. pepo, C. maxima, C. mixta, C. ficifolia, C, argyrosperma, mismas que se describen a continuación. 27 Cucurbita argyrosperma: Presenta dos sub-especies: Argyrosperma, formada por cuatro variedades -argyrosperma, callicarpa, stenosperma y palmieri-, tres de las cuales incluyen a todos los tipos cultivados, mientras que la cuarta corresponde a poblaciones espontáneas del noroeste de México, generalmente conocidas bajo el nombre Cucurbita palmieri L.H. Bailey; y Sororia, que comprende poblaciones silvestres con amplia distribución desde México hasta Nicaragua. (León J, 1987.). Las especies C. palmeri Bailey y C. sororia Bailey fueron clasificadas como taxones infraespecíficos de C. argyrosperma. (Merrick y Bates, 1989). Son plantas herbáceas, rastreras o trepadoras no muy vigorosas, sus raíces son fibrosa, el tallo es angular, las hojas están sobre los pecíolos, sus lóbulos son obtusos, triangulares y apiculados, los zarcillos son desarrollados presentando de dos a cuatro ramificaciones pubescentes, las flores son estaminadas, su receptáculo es campanulado, la corola es de color amarillo con blanco y anaranjado en el limbo, el fruto usualmente conserva la forma del ovario. (Lira R, 1995) Cucurbita moschata: Se conocen como zapallos, es de gran importancia aquí y en otras zonas del mundo. Sus hojas son aterciopeladas, orbiculares, con 5-7 lóbulos redondeados y poco pronunciados, no erguidas y con pequeñas manchas blanquecinas en la unión de las nervaduras, las que son producidas por una delgada capa de aire bajo la epidermis (Lira R, 1990). La flor es amarilla y tubular. El pedúnculo es anguloso, acampanado o ensanchado en su unión con el fruto. (León J, 1987) Producen frutos que son frecuentemente grandes, pueden ser de forma aplanada, redondeada, oval, o con cuello curvo. En norteamérica se reconocen tres tipos comerciales como son “Cheese” de fruto oblongo, “Crookneck” de fruto redondo y, “Bell” de fruto cilíndrico o acampanado. (Robinson y Decker Walters, 1997) 28 Cucurbita pepo: Dentro de esta especie, se ha definido dos subespecies, la Subs. pepo y la Subs. ovífera. Cucúrbita pepo es altamente polimórfico ya que presenta una diversidad de frutos mayor que la de cualquier otra especie de la familia de las Cucurbitáceas. (Nuez. F, 2000.) Son plantas rastreras, trepadoras o subarbustivas, anuales. Sus raíces son fibrosas, el tallo es angular, las hojas reencuentran sobre los pecíolos, los zarcillos presentan de dos a seis ramificaciones, sus flores son estaminadas y pistiladas, la corola es de color anaranjado. (Lira R, 1995) Los frutos pueden ser verdes, amarillos, anaranjados, blancos, veteados, de formas planas, redondeadas, ovales, alargadas, etc. Por tal razón en función de la forma del fruto se clasifican en : “Pumpkin” fruto redondo de color naranja, “Scallop” fruto pequeño y aplanado, “Acorn” fruto pequeño u asurcado, “Crookneck” fruto alongado, “Straightneck” fruto cilíndrico, “Vegetable marrow” fruto cilíndrico, “Cocozelle” fruto largo y cilíndrico, “Zucchini” fruto largo y cilíndrico. (Paris, 1986) 2.2.4 Ecología y adaptación En función de su adaptación ecológica, las especies del género Cucúrbita puede dividirse en dos grupos: especies mesofíticas, aquí se incluyen las especies cultivadas más importantes y especies silvestres ya que poseen raíces fibrosas; se distribuyen desde el sudeste de EE.UU hasta el centro de Argentina, por debajo de elevaciones de hasta 1300m. Las especies xerófitas que poseen raíces carnosas y almacenan reservas, se adaptan a regiones más áridas o zonas de elevada altitud desde el sudoeste de EE.UU. hasta el sur de México. (Merrick. L., 1995) Por otra parte según Bailey, s/a (1999), el género Cucúrbita se adapta a diferentes climas, como los trópicos húmedos de América del sur o las zonas templadas y frías. 29 2.2.5 Métodos de propagación Se propaga por semillas. La siembra se hace directamente en el campo definitivo, colocando tres semillas por sitio. Después de 15 días se elimina una de estas plantas. (Esquina-Alcazar y Gulik, 1983). Se recomienda humedecer las semillas el día anterior a la siembra en una solución con fungicidas para lograr una germinación más uniforme (Lira R, 1990). 2.2.6 Prácticas culturales y producción La siembra se efectúa al inicio de la estación lluviosa en camas levantadas, para evitar el exceso de agua. Los frutos se empiezan a cosechar de los cuatro a seis meses, dependiendo de la variedad (Esquina-Alcazar y Gulik, 1983). El abonamiento debe efectuarse hasta los 50 días de la siembra, después de este período la planta no muestra respuesta significativa en rendimiento (Lira R, 1990). 2.2.7 Control de principales plagas y enfermedades En zonas agrícolas bajo riego, tienen problemas con el pique o gusano barrenador de tallos (Melittia cucurbitae); el gusano barrenador de los frutos y guías (Diaphania nitidalis), y la mosca minadora (Liriomyza sp.). (León J, 1987). Entre las principales enfermedades tenemos chupadera (Rhizoctonia solani, Fusarium sp.), el oidium (Erisiphe cichoracearum), el mildiu (Pseudoprerenospora cubensis) y la cercosporiosis (Cercospora citrulina). (Lira R, 1990). 2.2.8 Tecnología de cosecha y poscosecha La cosecha se realiza manualmente, cuando la cáscara está verde y dura. No existe tecnología específica para la poscosecha. Los frutos se conservan 30 bien por 15 a 30 días en lugares frescos y ventilados y por 90 días cuando son almacenados a 10ºC y 75% de humedad relativa. (Lira R, 1990) 2.2.9. Formas de utilización Según el modo de consumo se clasifica en “calabazas de verano” y “calabazas de invierno”, dependiendo de si el fruto se consume en estado inmaduro o maduro respectivamente. Las calabazas de verano suelen ser de carne blanca o amarilla, corresponde a la especie C. pepo, mientras que las de invierno que poseen carne naranja, pueden ser de las especies C. pepo, C. moschata, o C. argyrosperma. (Robinson y Decker - Walters, 1997) Las calabazas de verano poseen un gen dominante que determina la dureza de la cáscara con el fin de consumir el fruto antes de que comience la lignificación de la corteza, pueden ser consumidos hervidos o fritos; mientras que las calabazas de invierno generalmente se consumen asadas. Sin embargo de todas las especies se puede hacer pasteles y dulces, o semillas tostadas. (Robinson y Decker - Walters, 1997) A demás, según Lira R. (1995), la pulpa de los frutos maduros, es consumida como dulce, los tallos tiernos, flores y los frutos inmaduros se consumen como verdura cocida, frita, etc. La cáscara dura se utiliza como recipiente en las zonas rurales. En la medicina los usos se presentan en el cuadro 2.1: 31 Cuadro 2.1. Usos en la medicina. PAÍS O REGIÓN ESPECIES PARTES USADAS Brasil C. moschata Fruto Diurético Semilla Tenífugo y Vermífugo China C. moschata USOS O PROPIEDADES Raíz Dolor de dientes Flores Tónico estomacal Semilla Curación de hemorroides y anemia Tratamiento de asma bronquial C. pepo Colombia Jamaica Fruto C. máxima Semilla Vermífugo C. moschata Raíz Febrífugo C. moschata Semilla Diurético C. pepo Península de C. argyrosperma Yucatán C. moschata C. pepo Raíz Mordedura de serpientes Enfermedades de la piel Hojas Jugo para curar granos y erupciones de la piel Flores Estimulante del apetito Fruto Resina, jugo de cáscara y pulpa para quemaduras y llagas. El fruto de C. moschata se considera pectoral, refrescante, y útil para enfermedades del cuero cabelludo. semilla Antihelmíntico, tenífugo, vermífugo, gelactógeno, y el aceite para curar hemorroides y heridas. México C. moschata en general C. pepo Venezuela C. moschata C. pepo Semilla Antihelmíntico Semilla Fiebres eruptivas y el aceite para úlceras Fuente: (Lira, R 1995) Puede ser considerado importante desde el punto de vista nutricional, cultural y en ciertos casos económicos, ya que ciertas especies han representado parte fundamental de la dieta y otros aspectos de la vida humana (Lira R, 1995) A sí por ejemplo las semillas presentan altos contenidos de aceites (más de 39%), proteínas (44%) y fósforo (1%); los ápices de las guías, así como las flores y frutos tiernos y maduros, destacan por sus contenidos de calcio y fósforo (Lira R, 1990). 32 2.3 Caracterización molecular Corresponde a una serie de técnicas que permite detectar diferencias a nivel de las secuencias de ADN. Mediante el análisis molecular se puede evitar la influencia del ambiente en la variabilidad, a este efecto se lo conoce como neutralidad de los caracteres moleculares. (Ferreira y Grattapaglia, 1998) Entre las numerosas aplicaciones de estas técnicas se puede conocer y caracterizar el contenido genético de los organismos. Así también resulta ser útil en estudios de mapeo genético, filogenia, sistemática molecular, mejoramiento asistido por marcadores moleculares, e identificación varietal. (Ferreira y Grattapaglia, 1998) La caracterización molecular emplea como herramienta útil a los marcadores moleculares en el proceso de obtención y caracterización genética de nuevas variedades, detección de patógenos, controles sanitarios y de calidad de la cadena agroalimentaria; así como también en la detección y cuantificación de organismos genéticamente modificados mediante marcadores de Reacción en cadena de la Polimeraza (PCR). (Nuez y Carrillo, 2000) 2.3.1 Marcadores Moleculares “Tradicionalmente los marcadores utilizados en estudio de genética y mejoramiento eran aquellos controlados por genes asociados a caracteres morfológicos en general fenotipos de fácil identificación visual que contribuyeron significativamente al desarrollo teórico del análisis de ligamiento y en la construcción de las primeras versiones de mapas genéticos. Sin embargo el bajo número de estos marcadores y la posibilidad de interferencia epistática o ambiental limitaban su uso”. (9) Con la llegada de las técnicas modernas de la biología molecular, surgieron diversos métodos de detección de polimorfismo genético directamente a nivel de ADN, permitiendo que estos marcadores generalmente puedan 33 acelerar los programas de mejoramiento genético (Ferreira y Grattaplaglia 1998). Marcador molecular es cualquier fenotipo molecular, oriundo de la expresión de un gen o de segmentos específicos de ADN que puede ser detectado y su herencia monitoreada. Es así que un marcador molecular recibe el nombre de marcador genético cuando su comportamiento se rige de acuerdo con las leyes básicas de la herencia mendeliana. (Ferreira y Grattaplaglia 1998). Así también un marcador molecular es cualquier característica química o molecular medible que es heredada según el Modelo Mendeliano Simple (Walton, 1993 citado por Tapia, 1998), incluyendo tanto a los que analizan directamente los ácidos nucleicos (ADN y RNA), como también a los que analizan los productos del ADN como son las proteínas (principalmente las isoenzimas). Los marcadores moleculares son biomoléculas que se pueden relacionar con un rasgo genético, que son las proteínas (antígenos e isoenzimas) y el ADN (genes conocidos o fragmentos de secuencia y función desconocida). Cuando varios marcadores moleculares se asocian inequívocamente con un rasgo genético, se dice que forman un QTL (loci de rasgos cuantitativos o cuantificables). (10) Un buen marcador molecular debe reunir una serie de características para maximizar su utilidad: así por ejemplo, debe tener buena distribución a lo largo del genoma, un alto grado de polimorfismo, así como también la técnica para analizar el marcador debe ser rápida, práctica y debe poder repetirse con fiabilidad en otros laboratorios. (11) Hay que tomar en cuenta que los marcadores moleculares no son afectados por el medio ambiente, ya que se basan en las propiedades del ADN y la información genética no cambia aunque las plantas estén sujetas a condiciones extremas y variadas. Al igual que los marcadores morfológicos y 34 bioquímicos, los marcadores moleculares detectan la variación natural entre individuos. Una ventaja puede ser la posibilidad de analizar locis únicos (regiones únicas en el genoma) o locis múltiples (regiones repetidas a través del genoma). (1) Para analizar el ADN, se dispone de ciertas técnicas moleculares tales como: los RFLP (Fragmentos de Restricción de ADN de Longitud Polimórfica), marcadores basados en la Reacción de la Cadena de la Polimerasa (PCR), o sea RAPD (ADN polimórfico amplificado al azar), microsatélites, minisatélites y AFLP (Fragmentos Amplificados de ADN de Longitud Polimórfica), permitiendo obtener un muestreo extensivo de los genomas a nivel de ADN, sin la influencia ambiental. “Esta información se interpreta analizando cada marcador como un carácter fenotípico distinto e independiente de los demás”. (Caetano-Anolis, 1993, Tapia, 1998, Yaguachi y; Medina, 2003) “Los marcadores genéticos, son abundantes en el estudio de una población segregante, son neutros, con mínimo o nulo efecto epistático o pleiotrópico. No presentan efecto ambiental, y si el ambiente tiene alguna influencia, como puede ser el caso de las proteínas, la influencia es de tipo cuantitativo, no cualitativo. Pueden ser extraídos de semilla o de partes vegetativas en los primeros estadios del desarrollo de la planta. (Nuez y Carrillo, 2000) 2.3.2 Reacción en cadena de la polimerasa (PCR) La Reacción en Cadena de la Polimerasa (PCR), es una técnica desarrollada por Kary Mullis en 1983, misma que consiste en la síntesis enzimática in vitro de secuencias específicas de ADN, en presencia de la enzima Taq polimerasa, esta enzima es un tipo de ADN polimerasa termoestable aislada de la eubacteria termofílica Thermus aquaticus. La PCR, se basa en el apareamiento y polimerización enzimática de un par de oligonucleótidos utilizados como iniciadores “primers” delimitando la 35 secuencia de ADN de doble cadena de la amplificación (Ferreira y Grattapaglia, 1998). Cada ciclo de PCR consta de tres etapas: 1) Denaturación o desnaturalización La desnaturalización del ADN de doble cadena se produce al incrementar la temperatura a rangos de 92 a 95ºC. Es aquí donde los enlaces de hidrógeno, que unen las cadenas y que individualmente son débiles, se rompen. Luego las dos cadenas de ADN disociadas permanecen libres hasta que la temperatura sea reducida para facilitar el anillamiento de los primers. 2) Anillamiento o complementación “Permite la hibridación de los primers con su secuencia complementaria en el ADN molde. En esta fase la temperatura depende de la secuencia de nucleótidos del primer pero generalmente está entre 37 y 60ºC.” 3) Elongación “Se incrementa la temperatura para activar la Taq polimerasa, para realizar la extensión de la nueva cadena incorporando desoxirribonucleótidos a partir de cada terminal 3’ de los primers, produciendo una cadena complementaria al ADN molde en la región limitada por los primers.” Luego de 30 ciclos de amplificación se obtiene aproximadamente 106 moléculas de una secuencia específica de nucleótidos. Para visualizar estos fragmentos amplificados se realiza una electroforesis en el gel de agarosa tiñendo los fragmentos con bromuro de etidio, que produce fluorescencia anaranjada cuando se expone a la luz ultravioleta. (Weising et al, 1994; Ferreira & Grattapaglia, 1998; Willians et al., 1993) 36 2.3.3 Polimorfismo del ADN amplificado al azar (RAPDs) (Random Amplified Polymorphic DNA) utiliza la tecnología de PCR modificada, trabaja con un solo primer de secuencia aleatoria que está formada por 10 nucleótidos que le permiten unirse en muchos loci diferentes debido a su menor especificidad para luego amplificar secuencias de ADN al azar. (Phillips, 1998) La asunción de heredabilidad tiene dos componentes: fidelidad de la transmisión y modo de herencia de los caracteres en cuestión. El conocimiento de estos dos componentes es una información crítica para RAPDs, ya que este marcador es expresado de forma dominante. (Jeffreys et al., 1988; Hadrys et al., 1992; Riedy et al., 1992) La repetibilidad es un problema en el uso de RAPDs ya que puede ser muy sensitiva a las condiciones en las que se lleva a cabo. Es por eso que se debe estandarizar todas las condiciones experimentales utilizadas durante la amplificación con el fin de reducir la falta de repetibilidad inherente a la técnica. (Dowling ert al., 1996; Bachmann, 1994; Hadrys et al., 1992) Los RAPDs pueden no ser independientes cuando los fragmentos amplificados están asociados con frecuencias repetitivas del genoma, cuando las relaciones alélicas son desconocidas, o cuando existe la formación de heteroduplex. (Ayliffe et al., 1994; Danforth & Freeman-Gallant, 1996; Felsenstein, 1985) La homología de los fragmentos RAPDs asume que estos fragmentos amplificados son únicos (Hadrys et al., 1992). Sin embargo para probar esta asunción se ha sugerido herramientas como el análisis southernblot usando el producto RAPD como sonda en la hibridación, o bien la digestión con enzimas de restricción par observar perfiles de bandas congruentes. (Dowling et al., 1996 Fritsh & Rieseberg, 1992; Rieseberg, 1996) 37 El análisis de RAPDs requiere de cinco elementos básicos que son descritos a continuación: ADN molde: Se conforma por el ADN de doble cadena que proviene del organismo que se desea analizar, es decir que el ADN utilizado por la Taq polimerasa como molde sintetiza nuevas cadenas polinucleótidas. (Yaguachi y Medina, 2003) A demás depende de las técnicas de extracción y almacenamiento; siendo de 10 a 50 ng/50 ml (volumen de reacción) como concentraciones óptimas. (Tapia, 1998 citado por Yaguachi y Medina, 2003). Primer o iniciador: Generalmente están constituidos por una cadena de 10 nucleótidos, contienen más de un 50% de bases de guanina, y citosina para su buen funcionamiento (Weising et al., 1994, Tapia, 1998, Yaguachi y Medina, 2003). “Gallardo y Moyano (2002) citan a Entrala quien afirma que para elegir un primer para amplificar un fragmento de ADN se toma en cuenta lo siguiente”: 1) La longitud de cada primer debe comprender entre 18 y 24 bases, ya que los primers de mayor longitud no aumenta el rendimiento, mientras que los más cortos carecen de especificidad. 2) “Ambos primers deben tener una temperatura similar a (-5ºC de diferencia)”. 3) “La relación bases púricas: pirimidínicas debe ser 1:1 (máximo 40 – 60%)” 4) “La secuencia de los primers debe comenzar y terminar con 1 – 2 bases púricas. 5) “Para evitar la formación de dímeros de primers es necesario comprobar que estos no contengan secuencias complementarias entre sí. 38 .Desoxinucleótidos Trifosfatos : “Tapia (1998), menciona a Estrella el cual se expresa que se requieren concentraciones adecuadas de dATP, dGTP, dCTP, y dTTP para la síntesis de la cadena”. Solución del bufer: Generalmente deben tener iones de potasio y magnesio en concentraciones óptimas, así como también deben ser calibradas a un pH de 8,3; para obtener bandas fuertes se aplica un amplio rango de concentraciones de magnesio, obteniendo cambios cualitativos de los patrones de bandas. Taq polimerasa: Es una enzima termoestable extraída de la bacteria Thermus aquaticus su función es restituir la doble cadena de ADN a través de una síntesis que parte de un punto determinado que es fijado por el primer. (Willians et al., 1993; Wolf et al., 1993; Tapia, 1998) Para que la técnica de RAPDs sea eficiente se toma en cuenta cuatro factores: 1) Número de ciclos de amplificación. 2) Cantidad de ADN inicial. 3) Longitud del ADN. 4) Temperatura. (Phillips et al., 1995; Tapia, 1998.) 2.3.4 Ventajas de los RAPDs Las ventajas más importantes de esta técnica se basan en su simplicidad, rapidez y bajo costo, ya que utiliza pequeñas cantidades de ADN que generan numerosos polimorfismos distribuidos por todo el genoma. A si también se puede realizar un muestreo de regiones de ADN altamente repetitivo como de regiones de ADN de copia única. 39 “Esta técnica no requiere del desarrollo previo de una biblioteca de sondas específicas, ni poseer información previa de la secuencia genética del organismo objetivo de estudio”. Se realiza aproximadamente en tres horas permitiendo manejar simultáneamente un gran número de muestras sin utilizar el ADN recombinante ni de radioactividad, ya que no se utiliza sondas ni procesos de autoradiografía. El bajo costo de esta técnica se debe a que no se requiere de instalaciones de laboratorio sofisticados. (Ferreira & Grattapaglia, 1998) “A demás estos marcadores fueron más eficientes que los RFLPs en el mareamiento de polimorfismos ligados a loci de resistencia a enfermedades y más eficientes en tiempo y mano de obra. Los segmentos RAPDs una vez amplificados y separados por electroforesis pueden ser fácilmente aislados del gel”. (Ferreira & Grattapaglia, 1998, Yaguachi y Medina, 2003) 2.3.5 Desventajas de los RAPDs “Se obtiene poca información genética por locus, los genotipos heterocigotos no pueden ser discriminados directamente de los homocigóticos, limitación conocida como “dominancia””. (Ferreira &Grattapaglia, 1998) “Otra desventaja puede ser el inconveniente de una baja consistencia (repetitiva), sin embargo empleando una metodología controlada y constante (termociclador, tipo y concentración de reactivos, etc) se puede conseguir resultados satisfactorios”. ((12) citado por Chalampuente y Prado, 2005) 2.3.6 Relación entre caracterización morfológica y molecular Es necesario establecer el grado de concordancia entre los caracteres morfológicos y marcadores moleculares, ya que estas dos técnicas maximizan la información y la utilidad de las colecciones de germoplasma. 40 Los caracteres morfológicos son influenciados por el medio ambiente siendo algunos de ellos poco convenientes para el estudio de la biodiversidad; mientras que los marcadores moleculares no consideran las interacciones del genotipo con el medio ambiente, es por eso que la combinación de estos dos métodos provee un amplio y real conocimiento de la diversidad de especies. (Hillis, 1987). Para comparar matrices de datos moleculares se utiliza los coeficientes de similitudes en base a Jaccard o Nei, mientras que para datos morfológicos se realiza una transformación (Z) en cada característica y luego se ejecuta una transformación de rangos o análisis de componentes principales. Este tipo de comparación da como resultado la identificación de correlaciones entre caracteres morfológicos y moleculares. (Mantel, 1967) 41 CAPÍTULO III MATERIALES Y MÉTODOS 3.1 MATERIALES 3.1.1 DE CAMPO 3.1.1.1 Insumos ♦ Semillas de 71 accesiones de Capsicum y 25 accesiones de Cucúrbitas del Banco Nacional de Germoplasma del INIAP ♦ Humus 3.1.1.2 Herramientas ♦ Palas ♦ Macetas plásticas ♦ Regaderas ♦ Invernadero 3.1.1.3 Recurso humano ♦ Técnicos INIAP ♦ Tesista 3.1.1.4 Material de oficina ♦ Computadora ♦ Hojas ♦ Cámara fotográfica ♦ Otros 42 3.1.2 DE LABORATORIO 3.1.2.1 Materiales de laboratorio ♦ Sílica gel ♦ Papel toalla ♦ Papel aluminio ♦ Papel filtro ♦ Papel cera (parafilm) ♦ Micro filtros ♦ Tijeras ♦ Pinzas ♦ Gradillas ♦ Guantes ♦ Mascarillas ♦ Morteros y pistilos ♦ Tubos eppendorf de 2, 1.5 y 0.6 ml ♦ Tubos PCR ♦ Puntas amarillas ♦ Puntas azules ♦ Erlenmeyer de vidrio de 250 y 1000 ml ♦ Vasos de precipitación ♦ Balanza eléctrica ♦ Vortex ♦ Micro pipetas ♦ Micro centrífuga ♦ Micro estufa ♦ Baño María ♦ Termocicladores MJPT100 ♦ Cámara de electroforesis ♦ Cámara de luz UV ♦ Refrigerador 43 3.1.2.2 Reactivos ♦ Buffer de extracción de ADN (Tris, EDTA, Na CL, SDS, PVP, CITAB, B. Mercapto etanol). ♦ Acetato de Potasio ♦ Acetato de Sodio ♦ Acetato de Amonio ♦ Etanol, Isopropanol ♦ CIA ♦ EtOH NaAC ♦ Tris – EDTA (TE) ♦ Tris – Ácido Acético – EDTA (TAE) ♦ ARNasa ♦ Aceite Mineral ♦ Agarosa ♦ Bromuro de etidio ♦ Blue Juice ♦ Marcador ♦ Buffer 5X ♦ Primer RAPDs ♦ dNTPs ♦ Taq polimerasa 44 3.2 MÉTODOS 3.2.1. UBICACIÓN Provincia: Pichincha Cantón: Mejía Parroquia: Cutuglahua Sitio: Instituto Nacional Autónomo de Investigaciones Agropecuarias (INIAP). Departamento Nacional de Recursos Fitogenéticos y Biotecnología (DENAREF). Estación Experimental Santa Catalina (EESC), Quito. 3.2.2. Descripción de la investigación 3.2.2.1 Caracterización molecular A) Extracción del ADN genómico Para la extracción de ADN en Capsicum, se probó con varios protocolos de extracción tales como: Extracción de ADN (Mariack), extracción de ADN de Yuca (Colombo 1998), y Colombo (1998) modificado por Piedra* (2004, comunicación personal). Hasta que finalmente se definió el protocolo de extracción de ADN de Yuca (Colombo 1998) para las especies en estudio, el mismo que se detalla a continuación. (Figura 3.1) El buffer de este protocolo consta de: Tris pH 8 (1M), NaCl 5M, EDTA Ph 8 (0.5M), CTAB, Agua estéril autoclavada. Se tomo de 3 a 5 hojas jóvenes, las cuales fueron secadas en sílica gel, durante 1 semana aproximadamente; hasta que estén completamente secas. Se vierte 0.5 g de tejido seco de cada accesión en tubos eppendorf de 2ml, a esto se le añade 1ml de buffer precalentado, más 25 ul de B. 45 mercapto etanol, y se agita suavemente hasta que la mezcla se torne homogénea. Las muestras se incubaron en baño maría a 65ºC durante dos horas, debiendo agitarlas cada 30 minutos. Luego se centrifugó a 14000 rpm durante 10 minutos, se transfiere el sobrenadante a tubos nuevos de 2 ml; para luego aforar los tubos a 1 ml con el buffer de extracción, a demás de agregar 1 ml de CIA; agitar suavemente. Se centrifugó una vez más a 4000 rpm por 15 minutos ó a 14000 rpm por 5 minutos. Se captura el sobrenadante sin contaminarla con la interfase, para luego adicionar 1 ml de buffer de extracción más 1 ml de CIA, y centrifugarlo a 14000 rpm por 5 minutos; retirando nuevamente el sobrenadante a tubos nuevos. Seguidamente se adiciona 800 ul de isopropanol frío (igual volumen de sobrenadante). Centrifugando de inmediato a 12000 rpm durante 15 minutos, debiendo chequear cada 2 minutos. Se retira el isopropanol del pelet, y se lava con 1 ml de etanol 70%. Se puede secar a temperatura ambiente o en micro estufa por 30 minutos a una temperatura de 37ºC. Finalmente se resuspendió el ADN en 100 ul de TE a temperatura ambiente por toda la noche. Es necesario resaltar que en el presente proceso el ADN de varias accesiones se mostró contaminado, para corregir tal circunstancia se realizó una limpieza con Acetato de Amonio; el cual se describe a continuación. Se adiciona a los tubos 350 ul de acetato de amonio 7.5M, y se agita suavemente. Luego se da un vórtex y se centrifuga a 14000 rpm durante 5 minutos. Se transfiere el sobrenadante a tubos nuevos y se añade 700 ul de isopropanol frío, para luego agitarlo suavemente. Se vuelve a centrifugar a 14000 rpm por cinco minutos. 46 Finalmente al pelet precipitado se le añade 250 ul de etanol 70%, agitándolo suavemente; para luego eliminar el etanol y dejar secar el pelet. El pelet es resuspendido 50 o 100 ul de TE. Y conservado a -20ºC hasta su utilización. Sílica Gel Maceración de Tejido Centrífuga Centrífuga Formación del Pelet Lavado de Pelet con Etanol al 70% Mezcla Homogenea Baño María Sobrenadante + 1ml de buffer y1ml de CIA Micro estufa 37ºC Pelet Seco (ADN) Figura 3.1. Extracción del ADN genómico. Para la extracción de ADN en cucúrbitas se siguió el protocolo Dellaporta et al, mismo que está conformado por: Tris pH 8, EDTA, NaCl, SDS al 20%, y agua destilada estéril. 47 La deshidratación de hojas, y macerado se procesan igual que en capsicum, variando únicamente en el tiempo de secado del material vegetal ya que las hojas son más gruesas. Se procedió a macerar el tejido deshidratado, del cual se tomo alrededor de 0.1 gr adicionando PVP que es un antioxidante, para luego ser vertidos en tubos eppendorf de 2 ml. Se añade 30ul de B. mercaptoetanol (antioxidante), 200ul de SDS, y se aforó la muestra a 2 ml con el buffer de extracción. Se agitaron los tubos hasta que la mezcla se torne homogénea. Luego se incubó a 65ºC en baño maría por 20 minutos. Los tubos fueron retirados para dejar enfriar a temperatura ambiente, luego se añadió 300ul de acetato de potasio 5M, se mezclo; e inmediatamente se incubó en hielo por 30 minutos. Una vez que las muestras están a temperatura ambiente, se centrifugaron a 10000 rpm durante 10 minutos. El sobrenadante fue filtrado a tubos nuevos, a los cuales se les añadió 0.7 vol de Isopropanol frío. Es decir que en 500 ul de sobrenadante se añadió 350 ul de isopropanol y se agitaron suavemente. Una vez más las muestras fueron incubadas a – 20ºC durante una hora. Posteriormente se centrifugaron a 10000 rpm por 10 minutos, los contaminantes son eliminados, dejando el pelet o pastilla, mismo que fue secado en la micro estufa a 37ºC. Luego de secado el pelet se disolvió en 700 ul de TE, se dejó a baño maría por 30 minutos para minimizar el tiempo. El ADN volvió a ser precipitado adicionando 0.1 vol. de acetato de sodio (Na Ac) 3M y 0.7 vol. de isopropanol frío. Es decir que en 750 ul de ADN disuelto en TE, se adicionó 75 ul de NaAc 3M y 525 ul de isopropanol. Debe ser agitado suavemente. Se centrifugo por última vez a 12000 rpm durante 10 minutos, debiendo chequearse cada tres minutos. Seguidamente se lavó el pelet con 350 ul de etanol 70%. Y se secón en la micro estufa. 48 Una ves seco el pelet se agrego 100 ul de TE, esto es de acuerdo al tamaño del pelet. Y se sometió a baño maría a una temperatura de 65ºC durante 30 minutos. Las muestras al ser enfriadas se les dio un vórtex para homogenizar el ADN. Finalmente se verifico y cuantifico cada una de las muestras. Al igual que en capsicum, el ADN de varias accesiones se mostró contaminado, por lo que se aplicó una limpieza con Acetato de Amonio; el cual ya fue descrito anteriormente. B) Cuantificación de ADN La integridad y concentración del ADN fueron analizadas por electroforesis en geles de agarosa 0,8% en tampón TAE 1X y cuantificadas comparativamente por la intensidad de sus bandas con las del estándar ADN Low Mass Ladder (10068-013, INVITROGEN) Una vez listo el gel se mezclaron en parafilm: 4 ul de ADN de cada muestra, con 1 ul de blue juice. El volumen de carga fue 2 ul a partir del segundo poso, una vez cargadas todas las muestras se colocó en el primer poso 2ul de marcador ADN Low Mass Ladder Posteriormente se llevó el gel a la cámara de luz ultravioleta. La concentración de ADN de cada una de las muestras se estandarizó diluyéndolo en tampón TE 0,1M tartrazine, hasta lograr una concentración final de 5 ng/ul tanto para cucúrbitas como para Capsicum. (Figura 3.2) 49 Gel Agarosa +TAE 1X Mezcla en Parafilm Cámara de Luz Ultravioleta Figura 3.2. Cuantificación de ADN en geles de agarosa C) Reacción RAPDs Se utilizó tubos PCR, y en cada uno de estos se colocó alícuotas de 2 ul de ADN (5 ng/ul) para cucúrbitas y 3 ul de ADN (5 ng/ul) para Capsicum. Se preparo una mezcla con los siguientes componentes para los dos géneros: Componentes 1Rx 5X buffer 2,2 ul Primer (1,0 uM) 0,4 ul DNTPs (2,5 mM cada uno) 0,8 ul Taq polimerasa (5U/ul) 0,13 ul H2O ultra pura 2,3 ul Volumen final 5,83 ul Luego se extrajo 5,4 ul de la mezcla y se coloco en los tubos PCR tanto para las 25 muestras de cucúrbitas, como para las 71 muestras de Capsicum, la reacción fue cubierta con una gota de aceite mineral con el fin de evitar su evaporación. Estas reacciones fueron amplificadas en un termociclador MJ – Research, de acuerdo al siguiente programa: 50 PASOS TEMPERATURA TIEMPO 1 2 Denaturación inicial Denaturación cíclica 94 94 5 min. 30 seg. 3 Anillamiento 42 1 min. 4 Elongación 72 2 min. 40 veces el paso 2 hasta el paso 4 6 Elongación final 72 7 min. 7 Conservación de la muestra 4 5 min. Se usó el 1 Kb DNA Ladder Marker (10381-010 INVITROGEN) como marcador de referencia en los productos amplificados, estos fueron visualizados en geles de agarosa al 2% en tampón TAE 1X con bromuro de etidio. La electroforesis se realizó a 110 V. finalmente las bandas de ADN fueron visualizadas bajo un transiluminador UV, a la vez que fueron documentadas. 3.2.2.2 Primers evaluados Se realizó un sondeo preliminar (screening), donde se probaron 145 primers pertenecientes a los Kits OPA, OPAC, OPAN, OPAM, OPR, OPS, OPW, OPAA, de Operon Technologies. Para esta prueba se escogieron cinco accesiones morfológicamente diferentes de cada género. Como resultado se seleccionaron cinco primers para Capsicum y ocho primers para cucúrbitas, que presentaron polimorfismos reproducibles y confiables, los mismos que se emplearon para la amplificación del ADN de las 71 accesiones de capsicum y las 25 accesiones de cucúrbita respectivamente estudiadas. (Figura 3.3) 51 Scriniing de Capsicum Scriniing de Cucúrbitas Figura 3.3. Scriniing de Capsicum primers OPA 12, OPA18, OPA 20, OPAN 02, OPAS 01; scriniing para cucúrbitas primers OPA 09, OPA 12, OPA 19, OPAC 03, OPAC 05, OPAC 08, OPAC 09, OPAC 11 3.2.3. Análisis estadístico para datos moleculares La codificación de bandas polimórficas se evaluaron a través de las variables presencia (1) o ausencia (0), los cuales se registraron por inspección en una matriz de datos binarios en el programa NTEDIT del paquete estadístico NTSYS pc ver.2,0 (Applied Biostatistis Inc, 1998), que es un programa utilizado para determinar similitudes genéticas entre especies, basándose en caracteres moleculares. Es importante mencionar que no se tomo en cuenta polimorfismos que involucren datos dudosos (9). (Figura 3.4) Los tamaños de las bandas polimórficas se calcularon mediante la aplicación LENGTH (Templeton 1988), expresándose en pares de bases (pb). La principal ventaja de esta codificación es que proporciona el mismo peso a 52 todos los individuos independientemente del número de bandas. El número de locus es el número de bandas diferentes observadas en el germoplasma en estudio. Al comparar dos accesiones, los estados posibles a un mismo locus son: ACCESION Y ACCESION X + - + A C b d Es necesario recalcar que el número de dobles ausencias (carácter <<d>>) corresponde al número de locus homocigotos para el alelo nulo en dos individuos ya que solo informa sobre la ausencia del alelo amplificado, por tanto no es considerado como una evidencia de similitud entre dos accesiones. Es así que la selección del índice de similaridad sobre este tipo de marcadores moleculares tiene que basarse en características de la técnica utilizada. Codificación de Bandas Polimórficas (Presencia (1), Ausencia (0), y Dudoso (9) en Capsicum Codificación de Bandas Polimórficas (Presencia (1) y Ausencia (0), en Cucúrbitas Figura 3.4. Evaluación de primers, scriniing de capsicum y cucúrbitas 53 A) Matriz de similitud y distancias Empleando un coeficiente de asociación para cuantificar el parecido o similitud entre dos muestras, debido a la naturaleza de la información proporcionada por los RAPDs se empleo el algoritmo de Jaccard. Esto permitió calcular la similitud genética entre pares de accesiones mediante la opción SIMQUAL del paquete estadístico NTSYS. La base molecular para la presencia de una banda RAPDs aún no está claramente entendida, sin embargo se considera que la ausencia de una banda compartida no necesariamente implica un ancestro común o similitud genética entre muestras, clones o accesiones. Es así que el coeficiente de Jaccard fue considerado como el mejor algoritmo para obtener una matriz de similitud y distancia en este estudio, debido a que no se considera a la ausencia de banda entre dos muestras como elemento a favor de la similitud entre ellas. El coeficiente de Jaccard se expresa de la siguiente manera: Mxy F= (Mt – Mxyo) Donde: F = Coeficiente de Jaccard Mxy = Número de fragmentos compartidos entre dos accesiones Mt = Número total de bandas en la matriz de datos Mxyo = Número de bandas en la matriz Sobre la matriz obtenida se aplicó la técnica Cluster análisis empleando el método de agrupamiento UPGMA (media Aritmética No Ponderada; (Sneath & Sokal, 1973) mediante la opción de SAHN CLUSTERING del paquete estadístico NTSYS. 54 Y a través de la opción TREE DISPLAY se visualizaron los agrupamientos o relaciones entre entradas de la colección generando diagramas arborescentes o dendrogramas que demuestran las relaciones genéticas entre accesiones. 3.2.3.1 Análisis de la PCO La estructuración de la diversidad genética, puede ser visualizada a través de un análisis multivariado en coordenadas principales (PCA). El PCO es un método de ordenación homólogo al análisis de componentes Principales (PCA) adaptado especialmente a datos cualitativos. “Al igual que el análisis de componentes principales, este método indica cuantos factores independientes explican la diversidad total, que fracción de la diversidad es explicada y el peso de estos factores (factor loading). El análisis PCO no utiliza la distancia euclideana y posibilita la representación de variables e individuos en un mismo campo de proyección (plotting). (Crisci 1983, citado por Piedra 2002). 3.2.3.2 Análisis de varianza molecular (AMOVA) Este análisis utiliza datos crudos o una matriz de distancia ya calculada, permite diferenciar genéticamente a cada especie a demás de identificar los polimorfismos existentes. El PhiPt es considerado como una medida que facilita la comparación entre datos codominantes, haploides y binarios, es decir que es considerado como un parámetro de diferencia genética entre especies. (Flanagan N., 2005 (13)) 3.2.3.3 Boostrap Consiste en tomar muestras (con reemplazamiento) de elementos que constituyen la muestra original. Cada genotipo es expresado en n bandas donde son elegidas aleatoriamente. Cada muestra da información para todos 55 los genotipos dando lugar a una matriz de similaridad y una matriz de distancia. (Duque, 1998) Con un número adecuado de muestras se puede calcular un promedio de distancias entre i y j dando una opinión objetiva sobre la significancia y fuerza de las ramas que contienen a los diferentes grupos. (Duque, 1998) 3.2.4 Relación de datos morfológicos y moleculares. Para el estudio de la diversidad genética de un cultivo se utiliza avanzadas técnicas moleculares, así como también rasgos morfológicos. Sin embargo la diversidad molecular no considera las interacciones genotipo por medio ambiente; por lo que estas dos técnicas se complementan una con otra. (Taba, 1991) Al comparar matrices de datos se debe calcular para caracteres moleculares, distancias genéticas o coeficientes de similaridad utilizando algoritmos principalmente de Jaccard o Nei; mientras que los datos morfológicos son estandarizados. Una vez obtenidas las matrices de los dos tipos de caracteres se comparan con el comando MXCOMP del sotware NTSYS-pc (Rohlf, 1990) o mediante el estadístico Mantel (Mantel, 1967), este tipo de comparación da como resultado la identificación de correlaciones entre los caracteres morfológicos y moleculares. Este análisis utiliza matrices de distancia moleculares “X” obtenidas con el coeficiente de Jaccard y las morfológicas “Y” obtenidas con el coeficiente de Gower; y se las correlaciona entre ellas con el valor estadístico Mantel que se define como: Z= j k X jk Y jk Donde: X jk y Y jk = son elementos de js líneas y ks columnas de Xnxn y Ynxn respectivamente, y k es < j. 56 CAPÍTULO IV 4.1 Resultados y discusión Los resultados se presentan de forma separada para cada género, iniciando por Capsicum L., que es el género que agrupa a los ajíes y luego Cucurbita L. que agrupa a las calabazas. Posteriormente se hace una discusión de nuestros resultados para cada una de las especies. 4.1.1 Datos pasaporte (Género Capsicum.) Las accesiones de Capsicum fueron colectadas en ocho provincias de la Sierra ecuatoriana tanto del norte (Carchi, Imbabura, Pichincha), centro (Chimborazo y Tungurahua), sur (Azuay y Loja), y en la zona oriental (Napo). A demás se incluyen países como Bolivia, México y Perú. Las colectas están comprendidas entre los 1200 y 3500 de altitud m.s.n.m Los datos pasaporte de las accesiones analizadas se detallan en el anexo 1. 4.1.2 Género Capsicum L. De las 73 accesiones inicialmente sembradas bajo invernadero en el INIAP, los (ecu-12860 y 12863), no germinaron por presentar contaminación de semillas, por lo que fueron excluidas del análisis molecular, por tanto los datos moleculares registrados para las 71 accesiones restantes se muestran en el anexo 2. 4.1.2.1 Caracterización molecular de Capsicum L. Con una modificación del protocolo de extracción ADN de yuca Colombo modificado por Piedra se obtuvo un ADN de buena calidad, con rendimientos que oscilaron entre 1.66 y 50 ug/muestra, con una media de 6.13 ug/muestra de ADN. (cuadro 4.1). 57 Cuadro 4.1. Rendimiento de ADN de 71 accesiones de Capsicum L. de Germoplasma del DENAREF – INIAP. ENTRADA RENDIMIENTO ENTRADA ADN ug/muestra ECU - 2231 RENDIMIENTO ADN ug/muestra 12.5 ECU - 12833 5 ECU - 2233 8.33 ECU - 12834 2.5 ECU - 2236 8.33 ECU - 12835 3.33 ECU - 2242 6.25 ECU - 12839 3.33 ECU - 2243 5 ECU - 12840 50 ECU - 2249 3.33 ECU - 12841 2.5 ECU - 2252 2.5 ECU - 12842 3.33 ECU - 2258 2.5 ECU - 12843 5 ECU - 2259 12.5 ECU - 12844 5 ECU - 2261 5 ECU - 12845 3.33 ECU - 2262 3.33 ECU - 12846 1.66 ECU - 2263 6.25 ECU - 12847 2.5 ECU - 2264 1.66 ECU - 12848 5 ECU - 2265 1.66 ECU - 12849 8.33 ECU - 2266 1.66 ECU - 12851 2.5 ECU - 2267 1.66 ECU - 12852 3.33 ECU - 2268 6.25 ECU - 12853 5 ECU - 2269 5 ECU - 12854 4.16 ECU - 2270 5 ECU - 12855 3.33 ECU - 2271 1.66 ECU - 12857 6.25 ECU - 3834 8.33 ECU - 12859 6.25 ECU - 5347 8.33 ECU - 12861 3.33 ECU - 5357 12.5 ECU - 12862 2.5 ECU - 5429 12.5 ECU - 12864 3.33 ECU - 5444 12.5 ECU- 12865 3.33 ECU - 5445 3.33 ECU - 12866 16.66 ECU - 5462 2.5 ECU - 12867 2.5 ECU - 5463 8.33 ECU - 12868 2.5 ECU - 5371 8.33 ECU - 12869 2.5 ECU - 5528 6.25 ECU - 12870 4.16 ECU - 5529 5 ECU - 5530 6.25 ECU - 6222 5 ECU - 6233 12.5 ECU - 6225 6.25 ECU - 7019 25 ECU - 11991 5 ECU - 11992 1.66 ECU - 11993 5 ECU - 12831 5 ECU - 12832 3.33 Media= 6.13 58 4.1.2.2 Productos de amplificación En un sondeo preliminar de 73 primers RAPDs se seleccionaron 5 primers OPA–12, OPA–18, OPA–20, OPAN–02, OPAS–01, que generaron alrededor de 98 bandas RAPDs, de los cuales 36 se consideraron polimórficas, con una tasa de polimorfismo de 2,3 polimorfismos por primer. El numero de bandas osciló entre 1 a 23 productos RAPDs obtenidos y el tamaño de las bandas varió entre 250 pb a 1640 pb para Capsicum. (cuadro 4.2 y 4.3). En la figura 4.1 se muestra un ejemplo de la amplificación obtenida. Cuadro 4.2. Lista general de primers analizados. (C. capsicum L.) # Primer # Primer # Primer # Primer # Primer 1 2 3 4 5 6 7 8 9 10 11 OPA-05 OPA-06 OPA-09 OPA-12 OPA-13 OPA-14 OPA-15 OPA-17 OPA-18 OPA-19 OPA-20 12 13 14 15 16 17 18 19 20 21 22 OPAC-01 OPAC-03 OPAC-05 OPAC-06 OPAC-08 OPAC-09 OPAC-11 OPAC-12 OPAC-13 OPAC-15 OPAC-16 27 28 29 30 31 32 33 34 35 36 37 OPAN-02 OPAN-03 OPAN-04 OPAN-07 OPAN-09 OPAN-10 OPAN-11 OPAN-12 OPAN-13 OPAN-14 OPAN-17 40 41 42 43 44 45 46 47 48 49 50 OPAM-01 OPAM-02 OPAM-03 OPAM-04 OPAM-05 OPAM-06 OPAM-07 OPAM-08 OPAM-09 OPAM-10 OPAM-12 58 59 60 61 62 63 64 65 66 67 68 OPAS-01 OPAS-02 OPAS-03 OPAS-04 OPAS-05 OPAS-06 OPAS-07 OPAS-08 OPAS-09 OPAS-10 OPAS-11 23 OPAC-17 38 OPAN-18 51 OPAM-13 69 OPAS-12 24 OPAC-18 39 OPAN-20 52 OPAM-14 70 OPAS-13 25 OPAC-19 53 OPAM-15 71 OPAS-14 26 OPAC-20 54 OPAM-16 72 OPAS-15 55 OPAM-17 73 OPAS-16 56 OPAM-18 57 OPAM-20 Cuadro 4.3. Lista de los 5 primers polimórficos seleccionados con sus respectivas secuencias de nucleótidos, rango de amplificación y número de polimorfismos evaluados (C. capsicum L.) Secuencia de Nucleótidos Nº de productos Rango de Amplificación 5' - 3' obtenidos (pb) (pb) OPA - 12 OPA - 18 OPA - 20 OPAN - 02 TCGGCGATAG AGGTGACCGT GTTGCGATCC CACCGCAGTT 9 – 23 5 – 18 1 – 13 5 – 21 300 - 1600 300 - 1030 400 - 1640 250 - 1050 940, 799, 682, 560, 478, 343, 301 1005, 824, 681, 565, 545, 506, 436, 334 1532, 1108, 854, 657, 623, 421 1067, 927, 774, 707, 592, 452, 394, 309, 265 OPAS - 01 CTACTGCGCT 1 – 17 350 - 1640 1830, 1093, 799, 733, 593, 480 Primer Polimorfismos evaluados 59 M 29 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 3054 pb 2036 pb 1636 pb 1018 pb 506 pb 396 pb 344 pb 298 pb Figura 4.1. Perfiles RAPDs obtenidos en Capsicum L. con el primer. OPA - 20 Carriles 1 – 29 ADN amplificado. A la izquierda el tamaño en pares de bases (pb) de algunas bandas polimórficas evaluadas. (M) Marcador. Ecu 2231, Ecu 2233, Ecu 2236, Ecu 2242, Ecu 2243, Ecu 2249, Ecu 2252, Ecu 2258, Ecu 2259, Ecu 2261, Ecu 2262, Ecu 2263, Ecu 2264, Ecu 2265, Ecu 2266, Ecu 2267, Ecu 2268, Ecu 2269, Ecu 2270, Ecu 2271, Ecu3834, Ecu 5347, Ecu 5357, Ecu 5429, Ecu 5444, Ecu 5445, Ecu 5462, Ecu 5463, Ecu 5371. 4.1.2.3 Similitud genética Los valores de similitud obtenidos en la comparación dos a dos entre las entradas de Capsicum varían entre 0,00 a 0,86 con un valor medio de 0,43. Los valores obtenidos son similares a otros resultados tales como en cacao (0,49) (Colombo et al., 2000), tomate de árbol (0,54) (Chalanpuenta D., Prado P., 2005), oca (0,72) (Piedra G., 2002). (anexo 3) 4.1.2.4 Análisis de agrupamiento (UPGMA) Al igual que en el caso de la caracterización morfoagronómica de Tomate de árbol, (Chalanpuenta D., Prado P., 2005), en el género Capsicum no se observa una correspondencia con el agrupamiento morfológico ya que con los resultados del análisis de agrupamiento se ubican en mismo cluster accesiones que son diferentes morfológicamente. Esto sugiere que hay una estrecha relación genética entre cada una de las especies, En cuanto a la robustez de los grupos descritos el análisis boostrap determinó la robustez estadística de los ecus 5429, 5444, 5445, 5462, 5463, 5371 que pertenecen a la especie C. annum con un valor de 81. Mientras que los ecus 2262 y 2263 que pertenecen a la especie C. pubescens 60 25 26 27 28 presentan un valor de 77 que también es significativo. Por último el resto de accesiones presentan un valor de 58 que es medianamente significativo. Esto quiere decir que los porcentajes más altos demuestran que las accesiones que representan a las dos especies C. annum y C. pubescens se pueden considerar como las más puras del resto de accesiones a pesar de que se encuentran agrupados en el mismo cluster con diferentes especies. figura 4.2 Sin embargo en otros estudios realizados los resultados boostrap son más significativos, así por ejemplo en la colección de P. tuberosus en las entradas TC525, TC118 y en el grupo de chuines las líneas TC353 y TC354 obtuvieron un valor de 100% (Tapia C., 1998) El dendograma generado a partir del análisis UPGMA dividió a las 71 entradas de Capsicum en 5 grupos principales representados con los códigos A, B, C, D y E en la figura 4.2 Grupo A: Este grupo está formado por nueve entradas de las cuales 6 son C. bacatum, 1 es sp., 1 es C. frutescens, y 1 es C. annum. Grupo B: Está formado por treinta y cuatro entradas, donde 21 son C. pubescens, 1 es C. baccatum, 10 son C. annum, y 2 pertenecen a C. frutescens. Grupo C: Se forma por diecisiete entradas; 11 son C. annum, 5 son C. chinense, y 1 es sp. Grupo D: Está formado por diez entradas, de las cuales 6 son C. pubescens, 3 C. annum, y 1 C. chinense. Grupo E: Está formada únicamente por una sola entrada que pertenece a C annum. 61 Figura 4.2 Dendograma en base a datos moleculares de la colección de ají (Capsicum L.) usando en coeficiente de Jaccard, agrupamiento UPGMA y boostrap. 62 4.1.2.5 Análisis de coordenadas principales (PCO) La variabilidad representada por los dos primeros vectores se puede observar en la figura 4.3. El primer vector, que representa el 9,8% de la variabilidad total dentro del grupo 1, está formado por dos especies, la especie C. annum que agrupa a los ecus 5529, 5530, 12840, 12843, 12847 y 12855, y la especie C. chinense que agrupa a los ecus 12841, 12842, 12845, 12848 y 12853. La relación entre estas dos especies se debe a que comparten características morfológicas al presentar frutos alargados y redondos, ligera pubescencia en tallo y corrugación en corte transversal del fruto. EL ecu (12846) al no saber de que especie es, se puede sugerir que es una mezcla varietal, ya que comparte características como fruto alargado, y ligera pubescencia en tallos; siendo estas las principales similitudes entre las especies C. annum y C chinense del resto de especies. anexo 4 Así también en la parte inferior de este mismo vector, tenemos al grupo dos que está conformado por la especie C. annum con los ecus 6222, 6223 y 7019 y a la especie C. pubescens con los ecus 12835 y 12839. La relación entre estas dos especies es que presentan un fruto alargado. A demás se observa un grupo de entradas, los ecus 2231, 2233, 2236, 2242, 2269 y 3834 que corresponden a la especie C. baccatum, y los ecus 11993, 12831, 12833, 12834 y 12870 que pertenecen a la especie C annum. Se sugiere que existe una mezcla varietal de la especie C. baccatum en relación a la especie C. annum ya que esta última de acuerdo con el análisis boostrap es considerada una especie pura; sin embargo la especie C. baccatum comparte caracteres morfológicos como frutos alargados y corrugación transversal del fruto, siendo esta la razón por las cual se encuentran agrupadas en un mismo cluster. anexo 4 Por otra parte el ecu (2261 no está identificado) que también se encuentra en la zona intermedia del eje, puede ser otra mezcla varietal de las especies C. annum, y C. baccatum, ya que comparte características morfológicas de las mismas; como es la forma del fruto que es alargado. Cabe mencionar 63 que esta accesión no fue analizada morfológicamente, pero si fue tomada en cuenta para el análisis molecular. En el vector 2 que está representado con un 7.7% de la variabilidad total observada, forma el grupo cuatro, que pertenece a la especie C. pubescens con los ecus 2243, 2249, 2252, 2258, 2262, 2263, 2264, 2265, 2266, 2267, 2270 y 2271; así como también la especie C. baccatum con el ecu 2268. En este grupo es importante mencionar que de acuerdo al análisis boostrap la especie C. pubescens se considera pura, por tanto la presencia de un ecu de la especie C. baccatum sugiere que se debe a un mal etiquetado, ya que el ecu 2268 tiene más características morfológicas y moleculares de la especie C. pubescens así por ejemplo presenta frutos ligeramente alargados, corrugación intermedia longitudinal del fruto, floración y fructificación tardía. Este grupo difiere significativamente del resto de accesiones. Finalmente el grupo cinco que se encuentra en una zona intermedia está conformado por la especie C. pubescens con los ecus 11991, 11992, 12832, 12844, 12849, 12851, 12852, 12857, 12861, 12865, 12866, 12867, 12869; la especie C. frutescens con los ecus 2259, 5347 y 5357, la especie C. annum con los ecus 5371, 5429, 5444, 5445, 5462, 5463, 5528, 6225, 12854, 12859, 12864 y 12868; y la especie C. chinense con el ecu 12862. En este caso de igual manera se sugiere una mezcla varietal entre las especies C. pubescens y C. annum, ya que las características morfológicas que comparten se basan en que poseen frutos alargados y, la escasa pubescencia en hojas; la relación de estas dos especies con la especie C. chinense se basa en el color de anteras que puede ser morado claro u oscuro. Por otra parte cabe mencionar que el ecu 12682 que pertenece a la especie C. chinense puede estar mal etiquetado ya que sus características morfológicas como corrugación en corte transversal del fruto, floración y fructificación tardía corresponden a los ecus 5528, 12854, 12859 y 12868 que pertenecen a la especie C. annum, debido a que se encuentran agrupadas en el mismo cluster. anexo 4 64 Así como en el caso de este género Capsicum, que el análisis PCO permitió sugerir que existen mezclas varietales entre especies, de igual manera en otras investigaciones como en oca (Oxalis tuberosa Mol.) (Piedra G. 2002) se pudo distinguir posibles híbridos; al igual que en P. tuberosus (Tapia C. 1998). De ahí la importancia de este análisis. Figura 4.3. Distribución en el plano definido por el primer y segundo eje (C1 y C2) del PCO basado en el coeficiente de Similitud de Jaccard en la comparación dos a dos de 71 accesiones de ají (Capsicum L.) con 36 polimorfismos RAPDs. 65 4.1.2.6 Distancia genética de nei Este análisis se realizó en las 69 accesiones, ya que los ecus (2261 y 12846) no tienen identificación de especie. (cuadro 4.4) Cuadro 4.4 Matriz de distancia genética de nei. A B 0,232 0,035 0,092 0,108 C 0,215 0,358 0,282 F 0,130 0,168 P 0,248 0.00 C. annum (A) C. baccatum (B) C. chinense (C) C. frutescens (F) C. pubescens (P) Como se puede observar en el cuadro, este análisis nos permite ver a que distancia genética se encuentra una especie de la otra con el fin de ver cuanta diferencia o similitud hay entre cada una de ellas. Así por ejemplo, la mayor distancia corresponde a C. baccatum con 0,232, con respecto a C. chinense; por otra parte, las distancias genéticas entre las especies analizadas son de diferente orden y sus diferencias son medianamente significativas. 4.1.2.7 Análisis de varianza molecular (AMOVA) La descomposición de la varianza mediante el AMOVA determinó que un 23% de la varianza aporta a la diferenciación de las 5 especies analizadas, mientras que el 77% aporta a la diversidad intraespecífica. El mayor número de bandas binarias que fue de 34, y la frecuencia de bandas mayores al 5% que fue de 30 se obtuvo en la especie C. pubescens, seguido de la especie C. annum con 31 y 27 respectivamente, luego la especie C. baccatum con 25; la especie C. frutescens con 11 y finalmente la especie C. chinense con 9 respectivamente. (cuadro 4.5) 66 Cuadro 4.5 Análisis de bandas binarias por población Población No. Bandas No. Frecuencia de Bandas. >= 5% No. Bandas Privadas C. annum C. C. C. C. baccatum chinense frutescens pubescens 31 25 9 11 34 27 0 25 1 9 0 11 0 30 0 Por otra parte se identifico una banda exclusiva de una determinada taxa para la especie C. baccatumen. Es así que, de acuerdo a estos resultados la diferenciación genética entre especies es medianamente significativa. Los valores de PhiPT demuestran que la diferenciación genética entre la especie C. baccatum y C. chinense es altamente significativa una de la otra con un valor de 0,440 en relación al resto de especies, ya que la diferencia genética de las especies C. annum, C. pubescens y C. frutescens no es significativo. 4.1.2.8 Correlación entre marcadores morfológicos y moleculares El valor de correlación (r) obtenido a partir de este análisis fue de 0.25 (p=0.60) que es un valor bajo al igual que el obtenido en tomate de árbol (Chalanpuente D. Prado P., 2005) y otras investigaciones (Beer et al., 1993 y Scout et al., 1997), en comparación con otros estudios de caracterización (Tapia, 1998) y (Piedra G. 2002) que son moderadamente significativos; por tanto este resultado sugiere una correlación baja entre ambos tipos de información (morfológica y molecular). Los valores de PhiPT permiten corroborar que la relación entre la fase morfológica y el análisis molecular no es significativa. 67 4.2.1 Datos pasaporte (Género Cucurbita.) De las 25 accesiones de Cucúrbitas en estudio, solo cinco fueron colectados en Ecuador, específicamente en la Provincia de Loja. Las 20 restantes proceden de varios países de América, Asia, Europa y África. Las colectas realizadas en la Provincia de Loja, comprenden altitudes entre los 1200 y 2010 m.s.n.m. (anexo 5) 4.1.4 GÉNERO Cucurbita L. De las 30 accesiones de esta especie, cinco fueron eliminados por escasez de semilla en el Banco de Germoplasma del INIAP, por lo que fueron excluidas del análisis molecular. Los datos moleculares registrados para las 25 accesiones restantes se muestran en el anexo 6. 4.2.2.1 Caracterización molecular de Cucurbita L. Con el protocolo de extracción de ADN de Caña de Azúcar de Dellaporta et.al, se logro obtener un ADN de buena calidad, con rendimientos que oscilaron entre 1.66 y 50 ug/muestra, con una media de 11.83 ug/muestra de ADN (cuadro 4.6). Cuadro 4.6. Rendimiento de ADN de 25 accesiones de Cucúrbita L. de germoplasma del DENAREF – INIAP. ENTRADA CANTIDAD ENTRADA CANTIDAD ADN(ug) ADN(ug) ECU - 4976 ECU - 4977 ECU - 4978 ECU - 4979 ECU - 4980 ECU - 4981 ECU - 4983 ECU - 4984 ECU - 4992 5 5 5 5 3.32 6.25 3.32 12.5 3.32 ECU - 5326 ECU - 5329 ECU - 5330 ECU - 5338 ECU - 5343 ECU - 12382 ECU - 12393 ECU - 12399 ECU - 12400 ECU - 5308 16.6 ECU - 12408 5 Media = 11.83 ECU - 5309 25 ECU - 5310 ECU - 5311 ECU - 5312 16.6 25 16.6 ECU - 5313 25 50 3.32 25 3.32 12.5 5 5 1.66 1.66 68 4.2.2.2 Productos de amplificación En un sondeo preliminar de 30 primers arbitrarios se seleccionaron 8 primers (OPA–09, OPA–12, OPA–19, OPAC–03, OPAC–05, OPAC–08, OPAC–09, OPAC–11), que generaron alrededor de 98 bandass RAPDs de los cuales 51 se consideraron polimórficas, con una tasa de polimorfismo de 2,04 polimorfismos por primer. El número de bandas oscilo entre 3 a 18 productos RAPDs obtenidos y el tamaño de las bandas varió de 250 a 1640pb (cuadro 4.7 y 4.8). En la figura 4.4 se muestra un ejemplo de la amplificación obtenida. Cuadro 4.7. Lista de primers ensayados en el screening de polimorfismo en C. cucurbita L. # Primer # Primer # Primer 1 OPA 06 11 OPAC 01 21 OPAC 17 2 OPA 09 12 OPAC 03 22 OPAC 18 3 OPA 12 13 OPAC 05 23 OPAC 19 4 OPA 13 14 OPAC 08 24 OPAC 20 5 OPA 15 15 OPAC 09 25 OPAN 02 6 OPA 15 16 OPAC 11 26 OPAN 03 7 OPA 17 17 OPAC 12 27 OPAN 04 8 OPA 18 18 OPAC 13 28 OPAN 07 9 OPA 19 19 OPAC 15 29 OPAN 09 10 OPA 20 20 OPAC 16 30 OPAN 10 Cuadro 4.8. Lista de los 8 primers polimórficos seleccionados con sus respectivas secuencias de nucleótidos, rango de amplificación y número de polimorfismos evaluados (C. cucurbita L.) Secuencia de Nº de Rango de Nucleótidos productos Amplificación 5' - 3' obtenidos (pb) OPA – 09 GGGTAACGCC 3 – 14 300 - 1030 1053, 905, 825, 757, 520, 370 OPA - 12 TCGGCGATAG 4 – 13 300 - 1500 1370, 1175, 1067, 815, 689, 520, 462, 410 OPA - 19 CAAACGTCGG 3 – 13 250 - 1640 1327, 1213, 1065, 979, 736, 680, 654, 558 OPAC - 03 CACTGGCCCA 6 – 18 250 - 1500 1577, 1162, 1106, 713, 679, 615, 528 OPAC - 05 GTTAGTGCGG 6 – 17 350 - 1020 942, 756, 683, 590, 491, 469, 449 OPAC - 08 TTTGGGTGCC 3 – 11 450 - 1050 1233, 894, 852, 535 OPAC - 09 AGAGCGTACC 4 – 12 400 - 1100 1164, 972, 751, 690, 608 OPAC - 11 CCTGGGTCAG 6 –15 450 - 1100 1246, 1131, 982, 857, 687, 551 Primer Polimorfismos evaluados (pb) 69 M 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 (-) 3054 pb 2036 pb 1636 pb 1018 pb 506 pb 396 pb 344 pb 298 pb Figura 4.4. Perfiles RAPDs obtenidos en Cucurbita L. con el primer. OPAC - 11 Carriles 1 – 25 ADN amplificado. A la izquierda el tamaño en pares de bases (pb) de algunas bandas polimórficas evaluadas. (M) Marcador, (-) control negativo, Ecu 4976, Ecu 4977, Ecu 4978, Ecu 4979, Ecu 4980, Ecu 4981, Ecu 4983, Ecu 4984, Ecu 4992, Ecu 5308, Ecu 5309, Ecu 5310, Ecu 5311, Ecu 5312, Ecu 5313, Ecu 5326, Ecu 5329, Ecu 5330, Ecu 5338, Ecu 5343, Ecu 12382, Ecu 12393, Ecu 12399, Ecu 12400, Ecu 12408. 4.1.4.3 Similitud genética Los valores de similitud obtenidos en la comparación dos a dos entre las entradas de Cucúrbitas varían entre 0,21 a 0,89 con un valor medio de 0,55. Los valores obtenidos son similares a otros resultados tales como para cacao (0,49) (Colombo et al., 2000), tomate de árbol (0,54) (Chalanpuenta D., Prado P., 2005), oca (0,72) (Piedra G., 2002). (anexo 7) 4.1.4.4 Analisis de agrupamiento (UPGMA) Del agrupamiento UPGMA se observa una correspondencia con el agrupamiento morfológico, sugiriendo una diferenciación genética entre las especies analizadas. En cuanto a la robustez de los grupos descritos, el análisis boostrap determinó la robustez estadística de la especie C. pepo con un valor de 72 y de C. moschata con 70. 70 En otros estudios realizados los resultados boostrap son más significativos, así por ejemplo en la colección de P. tuberosus en las entradas TC525, TC118 y en el grupo de chuines las líneas TC353 y TC354 obtuvieron un valor de 100% (Tapia C., 1998), en el género Capsicum los ecus 5429, 5444, 5445, 5462, 5463, 5371 que pertenecen a la especie C. annum 81%. El dendograma generado a partir del análisis UPGMA dividió a las 25 entradas de Cucúrbitas en 4 grupos principales representados con los códigos 1, 2, 3, y 4 en la figura 4.5. Grupo 1: Este grupo está formado por dos entradas que pertenecen a la especie C. pepo. Grupo 2: Está formado por ocho entradas, pertenecientes a la especie C. pepo. Grupo 3: Se forma por diez entradas; pertenecientes a la especie C. moschata. Grupo 4: Está formado por cinco entradas, que pertenecen a la especie C. argyrosperma. 71 Figura 4.5. Dendograma en base a datos moleculares de la colección de Calabazas (Cucurbita L.) usando en coeficiente de Jaccard y el agrupamiento UPGMA. 4.2.2.5 Análisis de coordenadas principales (PCO) La variabilidad representada por los dos primeros vectores se puede observar en la figura 4.6. El primer vector, que representa el 18% de la varianza total pertenece a la especie C. pepo, mismo que está conformado por los ecus 4976, 4977, 4978, 4979, 4980, 4981, 4983, 4984, 4992 y 12382; es necesario mencionar que este último ecu en el análisis morfológico, se agrupó en la especie C. moschata, no así en el molecular. anexo 8 72 A demás, se puede observar un grupo de entradas correspondientes a los ecus 5326, 5329, 5330, 5338, 5343 de la especie C. argyrosperma, localizados en una posición intermedia del eje entre el vector 1 y 2 respectivamente. En el vector 2 que está representada con un 13% de la variabilidad total observada, agrupa a los ecus 5308, 5309, 5310, 5311, 5312, 5313, 12393, 12399, 12400 y 12408 que corresponden a la especie C. moschata. anexo 8 Finalmente de acuerdo a este análisis se puede observar que cada especie está agrupada en un mismo cluster, por lo que difiere significativamente a nivel molecular una especie de la otra. Mientras que en otros cultivos como en el caso del género Capsicum se sugiere que existen mezclas varietales entre especies, o mala etiquetación de las mismas; así también, en otras investigaciones como en oca (Oxalis tuberosa Mol.) (Piedra G. 2002) se pudo distinguir posibles híbridos; al igual que en P. tuberosus (Tapia C. 1998). Figura 4.6. Distribución en el plano definido por el primer y segundo eje (C1 y C2) del PCO basado en el coeficiente de Similitud de Jaccard en la comparación dos a dos de 25 accesiones de calabazas (Cucurbita L.) con 51 polimorfismos RAPDs. 73 4.1.2.6 Distancia genética de nei Este análisis se realizo en las 25 accesiones de calabazas. (cuadro 4.9) Cuadro 4.9. Matriz de distancia genética de nei. A M 0,324 0,372 P 0,362 0.00 Especie C. argyrosperma (A) C. moschata (M) C. pepo (P) En este análisis podemos observar la diferencia genética entre cada especie, así por ejemplo; la mayor distancia corresponde a C. pepo con 0,372, con respecto a C.argyrosperma. Sin embargo las distancias genéticas entre las especies analizadas son del mismo orden y sus diferencias no parecen significativas. 4.2.2.7 Análisis de varianza molecular (AMOVA) La descomposición de la varianza mediante el AMOVA determino que un 38% de la varianza aporta a la diferenciación de las 3 especies analizadas, mientras que el 62% aporta a la diversidad intraespecífica. El mayor número de bandas binarias así como la frecuencia de bandas mayores al 5% por especie! que fue de 45, se obtuvo en la especie C. pepo , seguido de la especie C.moschata con 42 y finalmente la especie C argyrosperma con 35 respectivamente (cuadro 4.10) Cuadro 4.10 Análisis de bandas binarias por especie Población No. Bandas No. Frecuencia de Bandas. >= 5% No. Banda Privadas C. C. C. argyrosperma moschata pepo 35 42 45 35 0 42 1 45 2 74 Por otra parte se identificaron bandas exclusivas de un determinado taxa, así por ejemplo una para la especie C. moschata y dos para C. pepo. Los valores de PhiPT demuestran que cada especie se identifica significativamente una de la otra, siendo la más alta diferencia genética entre la especie C. moschata y C. pepo con un valor de 0,390. 4.2.2.8 Correlación entre marcadores morfológicos y moleculares El valor de correlación (r) obtenido fue de 0.49 (p=0.002), que es un valor relativamente bajo en comparación con otros estudios de caracterización (Chalanpuente D., Prado P., 2005); (Tapia, 1998 y Piedra G. 2002), lo que sugiere una correlación moderada entre ambos tipos de información (morfológica y molecular). Sin embargo con los valores de PhiPT permite corroborar que la relación entre la fase morfológica y el análisis molecular es significativa. Otros autores reportan así mismo correlaciones moderadas (ej, oca, Piedra G. 2002 y jícama, Tapia C. 1998), y correlaciones bajas (tomate de árbol, Chalanpuente D., Prado P., 2005). 4.3 Hipótesis Una vez obtenidos y discutidos los resultados de la colección nacional de ají y calabazas, se confirma la variabilidad genética. 75 CAPÍTULO V CONCLUSIONES Y RECOMENDACIONES 5.1 Conclusiones género (Capsicum L.) La caracterización molecular, diferencio cinco grupos que se conforman de la siguiente manera: (Grupo A, C. baccatum, C. frutescens, C. annum y sp), (Grupo B, C. pubescens, C. baccatum, C. annum, y C. frutescens), (Grupo C, C. annum, C. chinense, y sp.), (Grupo D, C. pubescens, C. annum, y C. chinense.), (Grupo E, C annum). No se obtuvo un agrupamiento definido de cada una de las especies, debido a la estrecha relación genética que existe entre las accesiones de Capsicum spp. La técnica RAPDs no detecto una mínima variación genética del germoplasma en estudio. El análisis “bosstrap” determinó a los ecus 5429, 5444, 5445, 5462, 5463, 5371 como las especies más puras al tener un porcentaje del 81%. El Análisis PCO detectó posibles mezclas varietales de los ecus 12846 y 2261. La PCO también detectó un mal etiquetado del ecu 2268 y 12682. La distancia de nei determinó que la mayor distancia genética está entre la especie C. baccatum y C. chinense con 0.232. El análisis AMOVA determinó que un 23% corresponde a la diferenciación genética entre especies, mientras que el 77% aporta a la diversidad intraespecífica. 76 El valor de correlación entre datos morfológicos y moleculares no fue significativo (0,25), demostrando un bajo grado de concordancia entre estas dos etapas. Los análisis empleados para la obtención de resultados moleculares en ají son fundamentales para la identificación de la variabilidad genética. 77 5. 2 Conclusiones género (Cucurbita L.) En el género cucúrbitas se identificó cuatro grupos: (Grupo A, C. pepo), (Grupo B, C. pepo), (Grupo C, C. moschata.), (Grupo D, argyrosperma.). Se obtuvo un agrupamiento definido tanto en el análisis UPGMA como en la PCO de cada una de las especies, debido a una marcada diferencia genética que existe entre estas. En este caso, la técnica RAPDs si detectó una variación genética. El análisis “bosstrap” determinó a los ecus 4976 y 4978 de la especie C. pepo como las más puras con un valor de 72%. La distancia de nei determinó que la mayor distancia genética está entre la especie C. pepo y C. argyrosperma con 0.372. El análisis AMOVA determinó que un 38% corresponde a la diferenciación genética entre especies, mientras que el 62% aporta a la diversidad intraespecífica. El valor de correlación entre datos morfológicos y moleculares fue relativamente bajo (0,49), demostrando una correlación moderada entre estas dos etapas. 78 5.3 Recomendaciones Realizar una nueva evaluación molecular principalmente del género capsicum, utilizando técnicas más eficientes en la detección de polimorfismos como son Microsatélites (Abrev. SSRs, del inglés Simple Sequence Repeats), AFLPs (Del inglés Amplified Fragment Length Polymorphism). Es importante para futuras investigaciones obtener una mayor cantidad de polimorfismos, ya sea de estas especies en estudio como de otras, ya que proporcionaría un mejor conocimiento de la variabilidad genética. Se recomienda evitar la mezcla de cultivares de distintas especies en un mismo sitio, ya que existen plantas alógamas como es el caso de las calabazas que intercambian material genético y producen mezclas varietales. Se debería establecer estrategias para la conservación in situ y ex situ tanto de cucúrbitas como de capsicum, para mantener la diversidad y evitar la erosión genética. Ya que en la actualidad es el principal problema debido a la introducción de nuevas variedades comerciales. 79 BIBLIOGRAFIA Applied Biostatistics Inc. 1998. NTSYS-pc manual. Exeter Software, Setauket, New York. Pp. 186. Ayliffe, M.; Lawrence,G.; Ellis,J. & Prior,A. 1994. Heteroduplex molecules formed between allelic sequences cause non-parental RAPD bands. Nucl. Acids Res. 22:1632-1636. Bailey, L:H (s/a). 1999. The domesticated cucurbits. First Papes. Gent. Herb, 2:32-34. Bachmann,K. 1994. Molecular markers in plant ecology. New Phytol. 126:403-418. Brako, L y J. L: Zaruchi. 1993. Catálogo de las Angiospermas y Gimnospermas del Perú. Missouri Boyanical Garden. St. Louis, Missouri, EE.UU. 1286p. Bukasov, M. S. 1981. Las plantas cultivadas en México, Guatemala y Colombia. CATIE-Turrialba, Costa Rica. Caetano-Anollis, G. 1993. Amplifying DNA with arbitrary oligonucleotide primers. In: PCR Methods and applications. Cold Spring Harbor Laboratory. pp. 85, 94. Colombo C., SecondG., Losada Valle T. et Charrier. A., 1998. Genetic diversity characterization of cassava cultivars (Manihot esculenta Crantz). I) RAPD markers. Genetics and Molecular Biology 21, 11 105 -113. Collazos, C., RL. White., H.S. White et al. 1975. La composición de los alimentos peruanos. Instituto de Nutrición. Minist. De Salud. Lima. 35 p. 80 Cronquist, A. 1981. An Integrated System of Classification of Flowering Plants. The New York Botanical Garden. Columbia University Press. New York, USA. Cueva, E. 1997. Recolección, clasificación y studio etnobotánico de los recursos fitogenéticos arbóreos y arbustivos nativos; Productores de frutos comestibles de la provincia de Loja, Facultad de Ciencias Agrícolas. p. 17, 20. Chalampuente, D. y Prado, P. 2005. Caracterización morfoagronómica y molecular de la colección de tomate de árbol (Cyphomandra betacea Sendt). Del Banco de Germoplasma del INIAP, Ecuador. Tesis de Grado. Danforth,B. & Freeman-Gallant, C. 1996. DNA fingerprinting data and the problem of non-independence among pairwise comparison. Molecular Ecology 5:221.227. Dellaporta, SL., J. Wood y J.B. Hicks. 1983 A plant DNA minipreparation: Versión II. Plant Molecular Biology Reporter 1 (14): 19 -21. Dowling, T., Moritz, C., Parmer, J. & Rieseberg, L. 1996. Nucleid acids III. Analysis of fragments and restriction sities. IN Molecular systematics. Hillis, D., Moritz, C & Mable, B. (eds) 1996. Second edition. Sinauer Associates, Inc., Suderland, USA. Pp 249-320. Duque, C. 1998. Métodos estadísticos aplicados en biología molecular. In: Curso superior de capacitación: métodos estadísticos para el análisis de datos en biología milecular. Universidad Nacional Costa Rica, CIAT. 1998. s.p. Esquina-Alcazar, J. T. y Gulik, F. J. 1983. Genetic Resources ofCucurbitaceae - a global report- Internacional Board for genetic Resources IBPGRE Secretarit. Rome, Italy. 81 Felsenstein, J. 1985 Confidence limits on phylogenies: an approachusing the bootstrap. Evolution 39:783-791. Ferreira, M., Grattapaglia, D. 1998. Introducción al Uso de Marcadores Moleculares en el Análisis Genético, EMBRAPA, Brasilia DF. Fritsh, P. & Rieseberg, L. 1992. High outcrossing rates maintain male and hermaphrodite individuals in populations of the flowering plant Datisca glomerata. Nature 359:633-636. Gower, J. 1967. A comparison of some methods of cluster analysis. Biometrics 23:623-637. Hadrys, H.; Balick, M. & Schierwater, B. 1992. Applications of random amplifiedpolymorphic DNA (RAPD) in molecular ecology. Molecular Ecology 1:55-63. Hernández S. 1991. Avances en el Estudio de los Recursos Fitogenéticos de México. Chapingo – México. Pag: 239 – 247. IPGRI. 1995. Molecular genetic techniques for plant genetic resource. Report of IPGRI Workshop, Roma, Italy. pp. 137. IPGRI, AVRDC y CATIE. 1995. Descriptores para Capsicum (Capsicum spp.). Instituto Internacional de Recursos Fitogenéticos, Roma, Italia; Centro Asiático para el Desarrollo de la Investigación relativos a los vegetales, Taipei, Taiwán y Centro Agronómico Tropical de Investigación y Enseñanza, Turrialba, Costa Rica. Jaramillo, S.; Baena, M. 2000. Módulo de Capacitación: conservación ex situ de recursos fitogenéticos. Quito, Ec., Instituo Internacional de Recursos Fitogenéticos (IPGRI) Grupo Américas. p. 22, 23. 82 Jarrín, F. y Velasco J. 1997. Protocolo de extracción de ADN (Ref: DNA fingerprinting in Plants and Fugi, pag. 559-560) CIP – Quito. Jeffrey, C. 1990. Systematic of the Cucurbitaceae. En: Biology and utilization of the Cucurbitaceae. Bates, D.M.; Robinson, R.W.; Jeffrey, C., eds. Cornell Univ. Press, Ithaca, New York, pp. 3 – 9. Jeffreys, A.; Royle, N.; Wilson, V. & Wong, Z. 1998. Sponteneous mutation rates to new length alleles at tandem-repetitive hypervariable loci in human DNA: Nature 332:278-281. Judd, S. Walter., C. S. Campwell, E. A. Kellogg & P. F. Stevens. 1999. Plant Systematics. A Phylogenetic Approach. Sinauer Associates, Inc. Souderland, Massachusetts USA. León, J. 1987. Botánica de los cultivos Tropicales. P. 386. IICA. San José, Costa Rica. Lira, R. 1990. Estudios Taxonómicos y Ecogeográficos de las Cucurbitáceas de Latinoamérica. 1er Reporte semestral (enero-agosto). CIRF, Roma. Lira – Saade, R. 1995. Estudios Taxonómicos y Ecogeográficos de las Cucurbitáceae Latinoamericanas de Importancia Económica. Roma, Italia, Pag 1, 15, 19. Mantel, N. 1967. The detection of disease clustering and a generalizad regresion approach. Cancer Res. 27:209-220. Merrick L.C. 1995. Squashes, pumpkins and gourds. En: Evolution of Crop Plants. Smart, J.; Simmonds, N.W., eds. Longman, Londres, pp. 97 – 105. Merrick L.C., Bates D.M. 1989. Classification and nomenclature of Cucurbita argyrosperma. Baileya, 23. 94 - 102 83 Morillo E., Biol. DEA. 2002 Protocolos de Marcadores Moleculares Compilado y Editado por Ecuador Morillo V. responsable de Laboratorio Molecular. Instituto Agropecuarias Nacional (INIAP), Autónomo Departamento de Nacional Investigaciones de Recursos Fitogenéticos y Biotecnología (DENAREF), Estación Experimental Santa Catalina. Quito – Ecuador. Nuez, F.; Carrillo, J. 2000. Los Marcadores genéticos en la mejora vegetal. Valencia, Esp. p. 134. Nuez, F.; Ruiz, J.; Valcárcel, V.; et al. 2000 . Colección de Semillas de Calabaza del Centro de Conservación y Mejora de la Agroviodiversidad Valenciana. Madrid, España.Pag 11 – 29. Pabón, G. 2006. Caracterización Morfológica Y Revisión Taxonómica de Capsicum spp. (Ajíes) y Cucurbita spp (Calabazas) en la Granja de la UNORCAC, Cantón Cotacachi. Tesis, Universidad Técnica del Norte. Instituto de Post-Grado , Maestría en Manejo de Recursos Naturales. Ibarra. Paris H.S. 1986. A proponed subespecific classification for Cucúrbita pepo. Phytologia, 61, 133 – 138. Pickersgill, B. 1971. Relationships between weedy and cultivated formsin some species of chili peppers (genus Capsicum). Evolution 25: 683 691 Piedra, G. 1999. Caracterización morfoagronómica y molecular de la colección de oca (Oxalis tuberosa Mol.) del banco de germoplasma de INIAP, Tesis de grado, Ecuador. 84 Piedra A. 2002. Caracterización morfológica y morfológica de la colección de oca Oxalis tuberosa del banco de germoplasma del INIAP. Tesis Lic. Biol. Quito, Ec., Pontificia Universidad Católica del Ecuador. p. 22, 70. Phillips, W. 1998. Marcadores moleculares en plantas. Laboratorio de Biotecnología CATIE. Turrialba, Costa Rica. Pp. 29. Phillips, W.; Rodríguez, H.; Fritz, P. 1995. Marcadores de ADN: Teoría, aplicaciones y protocolos de trabajo. Con ejemplos de investigaciones en cacao (Theobroma cacao). Unidad de Biotecnología, CATIE, Turrialba, Costa Rica. 183p. Pozo, O. et al., 1991. Avances en el Estudio de los Recursos Fitogenéticos de México. Chapingo – México. Pag: 217 - 236 Riedy, M.; Hamilton, W. & Aquadro, C. 1992. Excess of non-parental bands in offspring from known primate pedigrees assayed using RAPD PCR. Nucleid. Acids. Res. 20:918. Rieseberg, L. 1996. Homology among RAPD fragmentsin interspecific comparison. Molecular Ecology. 5:99-105. Robinson R.W., Decker Walters D.S. 1997. Cucurbits. CAB International,New York. Rohlf, J. 1990. NTSYS. Numerical Taxonomy and Multivariate Analysis System. Version 2.0. Department of Ecology and Evolution State University of New York. Sneath, H.F. & Sokal, R.R. 1973. Numerical taxonomy. The principles and practice of numerical classification. Eds. D. Kennedy; R.B. Park. San Francisco, W.H. Freeman. Pp.573. 85 Taba, S. 1991. Caracterización y evaluación de germoplasma de maíz. In Técnicas para el manejo y uso de recursos genéticos vegetales. Castillo, R. Estrela, J. Tapia C. eds. Editorial Porvenir. Quito, Ecuador. Pp. 161-166 Tapia, C. 1998. Caracterización morofológica y molecular de la diversidad genética de la colección de Pachyrhyzus tuberosus (Lam). Spreg. Del CATIE. Centro Agronómico Tropical de Investigación y Enseñanza. Tesis M. Sc. Turrialba, Costa Rica. Pp. 157. Tapia, C. 2004. Taller de devolución de conocimientos a las comunidades agrupadas en la UNORCAC. Cotacachi, 19 y 20 de marzo del 2004. Tapia, C.; Castillo, R.; &Mazón, N. 1996. Catálogo de recursos genéticos de raíces y tubérculos andinos en Ecuador. INIAP. Departamento Nacional de Recursos Fitogenéticos y Biotecnología. Quito, Ecuador. Pp. 178. Templeton, A. & Lawrance, J. 1988. FRAG-LENGTH III: algorithm for the calculation of molecular weights. Software distributed by the authors. Weising, K.; Nybom, H., Wolf, K. & Meyer, W. 1994. DNA dingerprinting in plants and fungi. CRC Press. London, UK. Pp 332. Williams, J. 1990. DNA polymorphisms amplified by arbitrary primers are useful asgenetic markers. Nucleic Acids Res. Pp 6531-6535. Williams, J. Rafalski, J. & Tingey, S. 1993. Genetic analisys using RAPD markers. Methods Enzymol. 218:704-740. Wolf, K.; Peters – Van Rijn, J. 1993. Rapad detection of genetic variability in chrysanthemun (Dendranthema grandiflora Tzvelev) using random primers. Heredity 71:335 – 341. 86 Yaguache, B. y Medina, D. 2003. Diversidad genética y filogenia de los géneros Carica y Vasconcellea del sur del Ecuador. Tesis de Grado. PAGINAS WEB 1) Avance y Perspectiva, Marcadores Moleculares, Hemeroteca Virtual ANUIES, Asociación Nacional de Universidades e Instituciones de EducaciónSuperior, 1997. Consultado 10 oct/2005, disponible en: http://www.hemerodigital.unam.mx/ANUIES/ipn/avanpers/ene97/vol1608/ sec_1.html 2) Calabazas, propiedades medicinales. 2006. Consultado 10 oct/2005, disponible en: http://www.botanical-online.com/medicinalscucurbitapepocastella.htm 3) Calabaza. 2006. Consultado 10 oct/2005, disponible en: http://www.puc.cl/sw_educ/hortalizas/html/aji/caracteristicas_aji.html 4) Pimiento Capsicum annum. 2006. Consultado 10 oct/2005, disponible en: http://www.cabexperu.com/Espanol/ProdNat/aji.htm 5) AJI (Mirasol y Panca). 2006. Consultado 15 oct/2005, disponible en: http://www.podernatural.com/Plantas_%20Medicinales/Plantas_P/p_pimiento _picante.htm 6) Estudio citogenética de Capsicum pubescens “Rocoto”. Guevara, Misael; Luis Tellería; Olga Bracamonte; Rosa Gonzales y Alberto López. 2006. Consultado 15 oct/2005, disponible en: http://www.unmsm.edu.pe/biologia/reunion/c4r33.htm 7) Cultivo de ají. 2006. Consultado 15 oct/2005, disponible en: http://www.tattersall.cl/revista/Rev185/cultivo.htm. 8) Capsicum pubescens. 2006. Consultado 15 oct/2005, disponible en: http://www.usuarios.lycos.es/rocotosalsa/#CUATRO 87 9) Yañez, O. Aislamiento y Caracterización de Marcadores Moleculares Microsatélites a Partir de la Construcción de Librerías Genómicas Enriquecidas de Camote (Ipomoeabatatas (L) (Lam). Consultado 15 oct/2005, disponible en: http://sisbib.unmsm.edu.pe/bibvirtual/tesis/Basic/Ya%C3%B1ez_A_V/indiceYa%C3%B1es.htm. 10) Claros, G. Marcadores moleculares: Que son, como se obtienen y para que valen, Málaga. Consultado 6 ene/2006, disponible en: http://www.ciencias.uma.es/publicaciones/encuentros/ENCUENTROS4 9/marcadores.html. 11) José A. Aranguren – Méndez1 y Jordi Jordana2. Utilización de marcadores de ADN (Microsatélites) en Poblaciones de Animales Domésticos en Peligro de Extinción. Consultado 6 ene/2006, disponible en: http://www.cecalc.ula.ve/AVPA/articulos_libres/AVPAconservacion.pdf. 12) Dorado, G,; Caballero, L.; Muñoz, J. Capítulo 7. Capítulo. “Fingerprinting” Mediante Marcadores Moleculares en Biotecnología: Descripción, Amplificaciones y Perspectivas. Consultado 6 ene/2006, disponible en: http://www.webcd.usal.es/web/transgen00/Unidades/documento01/caba llero/cap7.htm 13) Incola S. Flanagan. 2005. Gen AIEx Genetic Análisis in Excel Versión 6. Consultado 30 oct/2006, disponible en: http:/www.anu.edu.au/BoZo/GenAIEx/. 14) M. Carme de Vicente Coll (Dra. C. B.); y otros. 1994 – 1996. Identificación varietal en frutales de hueso y pepita con el uso de marcadores moleculares. IRTA Cataluña. Consultado 6 ene/2006, disponible en: http://www.alpha1.inia.es:8081/SEARCH/BASIS/resulp/fqma/proyecto/D DD/94079.pdf 88 ANEXOS Género Cucurbita L. Anexo 1. Datos pasaporte de la colección nacional de Capsicum L. Código de Banco (ECU) Genero Especie Nombre común No. Colector Colector Localidad Observaciones 2 231 Capsicum baccatum Ají ECU-05-0005 C. Nieto ECU, Cotopaxi, Salcedo, Salcedo, 2 600 msnm, 00.55S, 79.36W Planta verde intenso, frutos pequeños. 2 233 Capsicum baccatum Ají ECU-06-0007 C. Nieto, E. Peralta ECU, Chimborazo, Guamote, La Matriz, Matriz, 3 063 msnm, 01.55S, 78.42W Frutos rojos, largos y delgados. 2 236 Capsicum baccatum Ají ECU-19-0010 2 242 Capsicum baccatum Ají ECU-06-0016 C. Nieto, E. Peralta ECU, Chimborazo, Penipe, Penipe, 2 460 msnm, 01.33S, 78.31W 2 243 Capsicum pubescens Ají ECU-04-0017 R. Castillo ECU, Carchi, Montúfar, Pioter, Pioter, 3 378 msnm, 00.39N, 77.47W 2 249 Capsicum pubescens Ají ECU-11-0023 A. Ortega, R. Castillo, J. Sánchez ECU, Loja, Gonzanamá, Gonzanamá, Gonzanamá, 2 045 msnm, 04.13S, 79.25W 2 252 Capsicum pubescens Ají ECU-11-0026 A. Ortega, R. Castillo, J. Sánchez ECU, Loja, Gonzanamá, Gonzanamá, Gonzanamá, 2 045 msnm, 04.13S, 79.25W 2 258 Capsicum pubescens Ají rocoto ECU-0032 R. Castillo, G. García, M. Holle ECU, Loja, Loja, Yangana, Yangana, 1 200 msnm, 04.24S, 78.28W 2 259 Capsicum frutescens Ají dulce ECU-0033 M. Holle, R. Castillo, F. Vivar ECU, Loja, Calvas, El Lucero, El Lucero, 1 200 msnm, 04.24S, 79.28W 2 261 Capsicum spp. PER-0035 R. Castillo, E. Peralta PER, Cusco, Cusco, Cusco, 3 500 msnm 2 262 Capsicum pubescens Chauchamushuri ECU-0036 ECU, Tungurahua, Patate, Hacienda San Luis, 2200 msnm, 01.18S, 78.30W R. Castillo, J. ECU, Imbabura, Otavalo, San Pablo, Gualabí, Ochoa 2 780 msnm, 00.10N, 78.12W Fruto muy aromático. Fruto rojo, pequeño. Fruto grande, alargado. Continuación Anexo 1. 2 263 2 264 Capsicum pubescens Capsicum pubescens Ají rocoto ECU-0037 Ají poncho amarillo ECU-0038 R. Castillo, J. ECU Ochoa E. Peralta, C. ECU, Azuay, Oña, Oña, Baijón, 2 372 msnm, Nieto 03.27S, 79.09W 2 265 Capsicum pubescens Ají rocoto ECU-0039 E. Peralta, C. Nieto ECU, Loja, Saraguro, Saraguro, Saraguro, 2 500 msnm, 04.24S, 79.28W 2 266 Capsicum pubescens Ají ECU-0040 E. Peralta, C. Nieto ECU, Loja, Saraguro, La Matriz, San Francisco, 2 500 msnm, 04.24S, 79.28W 2 267 Capsicum pubescens Ají redondo ECU-0041 E. Peralta, C. Nieto ECU, Loja, Saraguro, La Matriz, San Francisco, 2 500 msnm, 04.24S, 79.28W 2 268 Capsicum baccatum Ají rocoto ECU-0042 E. Peralta, C. Nieto ECU, Azuay, Sigsig, Gima, Hierbabuena, 3 000 msnm, 03.18S, 78.51W, 2 269 Capsicum baccatum Ají yunga ECU-0043 E. Peralta, C. Nieto ECU, Loja, Saraguro, El Tablón, San José, 2680 msnm, 03.30S, 79.22W 2 270 Capsicum pubescens Ají rocoto ECU-0044 E. Peralta, J. Tola ECU, Loja, Saraguro, Celán, Santa Rosa, 2620 msnm, 03.34S, 79.18W 2 271 Capsicum pubescens Ají ECU-0045 E. Peralta, J. ECU, Loja, Saraguro, Urdaneta, Baber, 2 640 Tola msnm, 03.36S, 79.11W 3 834 Capsicum baccatum Ají RC-1074 5 347 Capsicum frutescens Capsicum frutescens 5 357 R. Castillo ECU Frutos rojo intenso, de 1 cm de diámetro. PI-188477 MEX Cultivar Uvilla. PI-281396 MEX Continuación Anexo 1 5 429 5 444 5 445 5 462 5 463 5 371 5 528 5 529 5 530 6 222 Capsicum annuum Capsicum annuum Capsicum annuum Capsicum annuum Capsicum annuum Capsicum annuum Capsicum annuum Capsicum annuum Capsicum annuum Capsicum annum PI-511884 MEX PI-224405 MEX PI-260436 BOL PI-511879 MEX PI-511880 MEX PI-438657 MEX Cultivar Guajillo ancho. PI-438616 MEX Cultivar Xcatic. PI-5529 MEX Cultivar Dulce. PI-438662 MEX Cultivar Pimento. Ají rocoto CS-076 C. Tapia, J. Velásquez ECU, Napo, Quijos, Cuyuja, Cuyuja, 2 400 msnm 6 223 Capsicum annum Ají rocoto CS-077 C. Tapia, J. Velásquez ECU, Napo, Quijos, Cuyuja, Cuyuja, 2 400 msnm 6 225 Capsicum annum Ají CS-082 C. Tapia, J. Velásquez ECU, Napo, Quijos, Cuyuja, Cuyuja, 2 260 msnm 7 019 Capsicum annuum Ají rocoto JEE-023 J. Estrella ECU, Pichincha, Quito, San José de Minas, 2 450 msnm Planta de estructura arbórea. Frutos rojos brillantes. 11 991 Capsicum pubescens Ají rocoto WTS-9 K. Williams, C. Tapia ECU, Carchi, Tulcán, Malgonada, El Laurel, 2 490 msnm, 0.50.027N, 78.3.303W Fruto rojo intenso, 5-6 cm largo x 8 ancho, lobado en pedicelo, ápice hundido. Continuación Anexo 1. 11 992 Capsicum pubescens 11 993 Capsicum annuum Ají rocoto WTS-13 K. Williams, C. Tapia ECU, Imbabura, Cotacachi, Apuela, Santa Rosa, 1 660 msnm, 0.21.274N, 78.30.757W Fruto 6x4 cm., rojo brillante, cordado en pedicelo y hundido en ápice. Picante WTS-14 K. Williams, C. Tapia ECU, Imbabura, Cotacachi, Apuela, Santa Rosa, 1 660, 0.21.274N, 78.30.757W Fruto 6x2cm, rojo brillante, pedicelo obtuso y ápice punteado. Flor blanca. CTMTFP-001 C. Tapia, M. Tacán, F. Paredes Ecuador. Imbabura: Pimampiro, Pimampiro. Barrio San José. 0°22.844’N, 77°56.835W. 2 200 msnm. Tres meses de cultivo. Siembra: 30 x 50. 12 831 Capsicum annuum 12 832 Capsicum pubescens CTMTFP-008 C. Tapia, M. Tacán, F. Paredes Ecuador. Carchi. Tulcán, Maldonado, Bellavista. 0°50.552’ N, 78°04.003 W. 2 320 msnm. Poco picante. Altura: 80 cm. Pétalos blancos con base morada. 12 833 Capsicum annuum CTMTFP-014 C. Tapia, M. Tacán, F. Paredes Ecuador. Imbabura. Antonio Ante. Chaltura. El Rosario. 0°29.998’N, 78°11.588W. 2 190 msnm. Asociación con tomate de árbol. 12 834 Capsicum annuum CTMTFP-015 C. Tapia, M. Tacán, F. Paredes Ecuador. Imbabura. Urcuquí. Pablo Arenas. Plaza Barba Donoso. 0°29.998’N, 78°11.588’W. 2 210 msnm. 12 835 Capsicum pubescens CTMTFP-018 C. Tapia, M: Tacán, F. Paredes Ecuador. Imbabura. Urcuquí. Cahuasquí. Santo Domingo. 0°30.584’, 78°12.836’W. 2 245 msnm. La planta tiene cinco años de vida. 12 839 Capsicum pubescens M. Tacán, F. Paredes Ecuador. Loja. Paltas. Catacocha. Barrio Lourdes. 4°03.711’S, 79°38.917’W. 1 710 msnm. Tres plantas maduras ají Pubescens MTFP-002 Pubescens Continuación Anexo 1. 12 840 Capsicum annuum MTFP-003 M. Tacán, F. Paredes Ecuador. Loja. Paltas. Catacocha. Mercado Central. 4°03.711’S, 79°39.283’W. 1 710 msnm. 12 841 Capsicum chinense MTFP-004 M. Tacán, F. Paredes Ecuador. Loja. Paltas. Catacocha. Mercado Central.. 4°03.711’S, 79°39.283’W. 1 710 msnm. 12 842 Capsicum chinense MTFP-005 M. Tacán, F. Paredes Ecuador. Loja. Paltas. Catacocha. Centro Comercial Paltense. 4°03.711’S, 79°39.283’W. 1 710 msnm. Muy picante. Se puede localizar en le sector La Supa. Color amarillo. 12 843 Capsicum annuum MTFP-006 M. Tacán, F. Paredes Ecuador. Loja. Paltas. Catacocha. Centro Comercial Paltense. 4°03.711’S, 79°39.283’W. 1 710 msnm. Muy picante. 12 844 Capsicum pubescens MTFP-007 M. Tacán, F. Paredes Ecuador. Loja. Paltas. Catacocha. Centro Comercial Paltense. 4°03.711’S, 79°39.283’W. 1 710 msnm. MTFP-008 M. Tacán, F. Paredes Ecuador. Loja. Paltas. Catacocha. El Progreso. 4°03.533’S, 79°38.842’W. 1 700 msnm. MTFP-009 M. Tacán, F. Paredes Ecuador. Loja. Paltas. Catacocha. Barrio Santa Marianita. 4°03.287’S, 79°38.502’W. 1 640 msnm. Fruto alargado Pubescens 12 845 Capsicum chinense 12 846 12 847 Capsicum annuum MTFP-010 M. Tacán, F. Paredes Ecuador. Loja. Paltas. Catacocha. Chapongo. 4°02.539’S, 79°38.195’W. 1 570 msnm. 12 848 Capsicum chinense MTFP-011 M. Tacán, F. Paredes Ecuador. Loja. Paltas. Catacocha. Barrio Sigro. 3°59.525’S, 79°35.436’W. 1 800 msnm. Muy picante. Pequeño. Muy picante Continuación Anexo 1. 12 849 Capsicum pubescens MTFP-012 M. Tacán, F. Paredes Ecuador. Loja. Loja. Sucre. Plateado Bajo. Muy picante. Altura: 2 m 3°58.883’S, 79°13.876’W. 2 075 msnm. 12 851 Capsicum pubescens MTFP-014 M. Tacán, F. Paredes Ecuador. Loja. Loja. El Valle. Jipiro Alto. 3°58.087’S, 79°11.464’W. 1 940 msnm. El picante pasa rápido. 12 852 Capsicum pubescens MTFP-017 M. Tacán, F. Paredes Ecuador. Loja. Loja. Yangana. Yangana. 4°22.338’S, 79°10.481’W. 1 740 msnm. Picante. Altura: 1.50 m 12 853 Capsicum chinense MTFP-018 M. Tacán, F. Paredes Ecuador. Loja. Loja. Yangana. Yangana. 4°22.338’S, 79°10.481’W. 1 740 msnm. Suave. Altura: 1.50 m 12 854 Capsicum annuum MTFP-020 M. Tacán, F. Paredes Ecuador. Loja. Loja. Yangana. Yangana Centro. 4°21.913’S, 79°10.617’W. 1 655 msnm. 12 855 Capsicum annuum MTFP-021 M. Tacán, F. Paredes Ecuador. Loja. Loja. Yangana. Yongana Centro. 4°21.913’S, 79°10.617’W. 1 655 msnm. 12 857 Capsicum pubescens MTFP-023 M. Tacán, F. Paredes Ecuador. Loja. Loja. Yangana. Yangana Centro. 4°21.932’S, 79°10.544’W. 1 670 msnm. 12 859 Capsicum annuum MTFP-027 M. Tacán, F. Paredes Ecuador. Loja. Loja. Yangana. Barrio Soro. 4°21.984’S, 79°10.600’W. 1 650 msnm. Altura con guía: 4 m 12 861 Capsicum pubescens MTFP-029 M. Tacán, F. Paredes Ecuador. Loja. Loja. Malacatas. Centro. 4°13.123’S, 79°15.606’W. 1 395 msnm. Muy picante. M. Tacán, F. Paredes Ecuador. Loja. Loja. Malacatas. Santanilla. Picante. 4°13.422’S, 79°16.060’W. 1 450 msnm. Pubescens Pubescens Pubescens 12 862 Capsicum chinense MTFP-030 Pubescens Continuación Anexo 1. 12 864 Capsicum annuum MTFP-038 M. Tacán, F. Paredes Ecuador. Azuay. Gualaceo. Bulcay. Centro. 2°51.993’S, 78°46.634’W. 2 040 msnm. Rojo 12 865 Capsicum pubescens MTFP-039 M. Tacán, F. Paredes Ecuador. Azuay. Gualaceo. Bulcay. Centro. 2°51.993’S, 78°46.634’W. 2 040 msnm. Rocoto: rojo y pequeño M. Tacán, F. Paredes Ecuador. Azuay. Gualaceo. Bulcay. Centro. 2°51.993’S, 78°46.634’W. 2 040 msnm. Rocoto: rojo y grande M. Tacán, F. Paredes Ecuador. Azuay. Gualaceo. Bulcay. Centro. 2°51.993’S, 78°46.634’W. 2 040 msnm. Rocoto: verde y grande Pubescens 12 866 Capsicum pubescens MTFP-040 Pubescens 12 867 Capsicum pubescens MTFP-041 Pubescens 12 868 Capsicum annuum MTFP-045 M. Tacán, F. Paredes Ecuador. Tungurahua. Pelileo. Pelileo. San Blas. 1°19.964’S, 78°31.867’W. 2 350 msnm. 12 869 Capsicum pubescens MTFP-046 M. Tacán, F. Paredes Ecuador. Tungurahua. Pelileo. Pelileo. San Blas. 1°19.964’S, 78°31.867’W. 2 350 msnm. 12 870 Capsicum annuum M. Tacán, F. Paredes Ecuador. Tungurahua. Pelileo. Pelileo. Guadalupe. 1°20.081’S, 78°31.556’W. 2 350 msnm. Pubescens MTFP-049 Anexo 5. ECU Datos pasaporte de la colección nacional de Cucúrbita L. Género Especie Nombre común No. Colector Colector Localidad Observaciones Cultivar Yumurta. 4 976 Cucurbita pepo PI-173681 USDA TUR 4 977 Cucurbita pepo PI-181912 USDA SYR 4 978 Cucurbita pepo PI-5 3320 USDA HUN, Tapioszele Cultivar Ovari Feher. 4 979 Cucurbita pepo PI-508468 USDA COR, Seúl Cultivar Golden Zucchini. 4 980 Cucurbita pepo PI-418966 USDA CHN 4 981 Cucurbita pepo PI-357931 USDA YUG 4 983 Cucurbita pepo PI-234616 USDA ZAF 4 984 Cucurbita pepo PI-267757 USDA USA, Iowa Cultivar Long Green Bush. Cultivar Buff Pie. 4 992 Cucurbita pepo PI-234617 USDA ZAF Cultivar Skorsie. 5 308 Cucurbita moschata PI-371941 MEX 5 309 Cucurbita moschata PI-419083 CHN 5 310 Cucurbita moschata PI-288239 EGY 5 311 Cucurbita moschata PI-267754 ITA Cultivar Gian Spanish G8785. 5 312 Cucurbita moschata PI-244706 BRA Cultivar Paca 595. 5 313 Cucurbita moschata PI-234251 JPN Cultivar White Rind Sugar. 5 326 Cucurbita argyrosperma Cucurbita argyrosperma Cucurbita argyrosperma Cucurbita argyrosperma Cucurbita argyrosperma PI-512 12 6 MEX PI-438720 MEX PI-442237 MEX PI-458722 ARG PI-489692 GTM 5 329 5 330 5 338 5 343 Continuación Anexo 5. 12382 Cucurbita pepo 12 393 Lineño Cucurbita moschata 12399 Cucurbita moschata 2 de mate TACT-433 C. Tapia, T.Andres TACT-447 C. Tapia, T.Andres TACT-455 C. Tapia, T.Andres Ecuador, Loja, Catamayo,San Pedro de la Bendita Santiago, 2010 msnm, 03.59S, 79.30W Ecuador, Loja, Celica, Cerro Verde, 1300 msnm, 04.10S, 79.5 3W Ecuador, Loja, Gonzanamá, Sacapalca, La casa vieja, Duplicado para Cucurbit Network, New York, USA. Duplicado para Cucurbit Network, New York, USA. Duplicado para Cucurbit Network, New York, USA. 1500 msnm, 04.09S, 79.32W, 12400 Cucurbita moschata TACT-456 C. Tapia, T.Andres Ecuador, Loja, Catamayo, Poroto, 12 00 msnm, 04.02S,79,22W Duplicado para Cucurbit Network, New York, USA. Cucurbita moschata TACT-466 C. Tapia, T. Andres Ecuador, Loja, Vilcabamba, San Pedro de Vilcabamba, 1600msnm Duplicado para Cucurbit Network, New York, USA. 12408 Anexo 6. Matriz Básica de Datos (MBD) generada a partir de Datos Moleculares de Cucúrbita L. Nº ECU 1 4976 2 4977 3 4978 4 4979 5 4980 6 4981 7 4983 8 4984 9 4992 10 5308 11 5309 12 5310 13 5311 14 5312 15 5313 16 5326 17 5329 18 5330 19 5338 20 5343 21 12382 22 12393 23 12399 24 12400 25 12408 A9-1 0 1 1 1 1 1 1 1 1 1 1 1 1 0 1 1 1 1 0 0 0 0 1 1 1 A9-2 A9-3 0 0 0 0 1 0 0 0 0 1 1 1 1 1 1 1 1 1 1 1 0 1 1 1 1 A9-4 0 0 1 0 0 1 1 1 0 1 0 1 1 1 1 0 0 1 1 0 1 1 1 1 1 A9-5 0 0 1 1 1 1 1 1 1 1 1 1 1 1 0 1 0 0 0 0 1 1 1 1 1 0 0 0 0 0 1 0 1 1 1 1 1 1 1 1 1 1 1 1 1 0 1 1 1 1 A9-6 A 12 - 1 0 1 0 1 1 1 1 1 1 0 0 0 0 0 0 0 1 1 0 0 1 0 0 0 0 1 1 1 1 1 1 1 1 1 0 0 0 0 0 0 1 1 1 1 1 1 0 0 0 0 A 12 - 2 A 12 - 3 0 0 0 0 0 0 0 0 0 0 1 0 0 0 0 1 0 1 0 0 0 0 0 0 0 A 12 - 4 1 0 1 0 0 0 0 0 0 1 0 0 0 0 0 1 1 1 0 1 0 0 0 0 1 A 12 - 5 0 0 1 1 0 0 0 0 0 1 0 0 0 0 0 0 1 0 0 0 0 0 0 0 0 0 1 0 1 1 1 1 1 1 1 1 0 0 0 0 1 0 1 0 1 0 1 1 1 1 A 12 - 6 A 12 - 7 1 0 1 1 0 0 0 0 0 1 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 1 0 0 0 1 1 1 0 0 0 0 0 0 0 0 0 0 A 12 - 8 A 19 - 1 1 1 0 0 0 0 0 0 0 1 0 1 1 0 0 0 0 0 0 0 0 0 0 1 1 1 1 1 1 1 1 0 0 1 0 0 0 0 0 0 0 0 0 0 0 1 1 1 1 1 A 19 - 2 A 19 - 3 0 0 1 0 0 0 0 0 0 0 0 1 0 1 0 0 0 0 0 0 0 1 1 1 1 A 19 - 4 0 0 0 0 0 1 0 0 1 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 A 19 - 5 0 0 1 0 0 1 0 0 1 0 1 1 0 0 0 1 0 1 0 1 0 1 1 0 0 1 1 1 0 0 0 0 0 0 0 1 0 0 1 0 0 1 0 0 1 1 0 0 0 0 Continuación Anexo 6 A 19 - 6 A 19 - 7 0 0 0 0 0 0 0 0 0 1 1 0 0 1 0 1 1 1 1 1 0 0 0 0 0 0 1 0 1 0 0 1 1 0 1 1 1 1 0 0 0 0 0 0 0 0 1 1 1 1 A 19 - 8 AC 3 - 1 0 1 1 1 1 0 0 0 0 0 0 0 1 1 0 0 0 0 0 0 1 1 0 0 0 AC 3 - 2 0 0 0 0 0 0 0 0 0 1 1 1 0 0 0 1 0 0 1 0 0 0 0 0 0 AC 3 - 3 0 1 0 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 AC 3 - 4 0 0 0 0 0 0 0 0 0 0 1 0 0 0 0 1 1 1 1 1 0 0 0 0 0 AC 3 - 5 1 0 1 1 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 1 AC 3 - 6 0 0 0 0 0 0 0 0 0 1 1 1 1 1 0 0 1 1 1 1 0 1 1 1 1 AC 3 - 7 0 1 1 1 1 1 1 1 1 0 1 1 1 0 1 1 0 1 1 0 1 1 1 1 0 AC 5 - 1 0 0 0 0 0 0 0 0 0 1 1 1 1 1 1 0 0 0 0 0 0 1 1 1 1 0 1 1 1 1 1 1 1 1 0 0 0 0 0 0 0 0 0 0 0 1 0 0 0 0 AC 5 - 2 AC 5 - 3 0 0 0 0 0 1 1 1 1 1 1 0 1 1 0 0 0 0 0 1 0 0 0 0 0 AC 5 - 4 1 0 1 0 0 0 0 0 0 0 0 0 0 0 0 0 1 0 0 0 0 0 0 0 0 AC 5 - 5 0 1 1 1 1 1 1 1 1 1 1 1 1 1 1 0 0 0 0 0 1 1 1 1 1 AC 5 - 6 0 1 0 0 0 1 1 0 1 1 0 1 1 1 0 0 0 0 0 0 1 1 0 0 0 AC 5 - 7 1 1 0 0 0 0 0 0 0 0 0 0 1 0 0 0 0 0 1 0 0 1 1 1 1 AC 8 - 1 0 1 0 1 1 1 1 1 1 1 1 1 1 1 1 1 0 0 0 1 1 0 0 0 0 AC 8 - 2 1 1 0 1 1 1 1 1 1 0 0 0 0 0 0 0 0 0 0 0 1 1 1 1 1 0 0 0 1 0 0 1 1 1 1 1 1 0 1 0 0 1 1 1 1 0 0 0 0 0 Continuación Anexo 6 AC 8 - 3 AC 8 - 4 0 1 1 1 0 1 0 1 0 0 0 0 0 0 0 0 1 0 0 0 0 0 0 0 0 AC 9 - 1 0 1 0 1 1 1 1 1 0 0 0 0 0 0 0 0 1 0 0 0 1 1 0 0 0 AC 9 - 2 0 1 1 1 1 1 1 1 1 0 1 1 0 0 0 0 0 0 1 0 0 1 1 0 0 AC 9 - 3 0 1 0 0 0 0 1 1 1 1 1 1 1 0 0 0 0 0 0 0 0 0 0 0 0 AC 9 - 4 0 1 1 1 1 1 1 1 1 0 0 0 0 0 0 1 0 1 0 0 0 0 0 0 0 AC 9 - 5 1 1 1 0 0 0 0 0 0 0 0 0 0 0 0 0 1 0 0 0 0 0 0 0 0 AC 11 - 1 1 0 1 0 0 0 0 0 0 1 1 1 1 1 0 0 0 0 0 0 0 0 1 1 1 0 0 0 0 0 0 0 0 0 1 1 1 1 1 1 0 0 0 1 0 1 1 1 1 1 AC 11 - 2 0 0 1 1 1 1 1 1 1 1 1 1 1 1 1 0 0 0 1 0 0 1 1 1 1 AC 11 - 3 1 1 1 1 1 1 1 1 1 0 0 0 1 1 1 0 1 1 0 0 0 0 0 1 1 AC 11 - 4 1 1 1 1 0 1 1 1 1 0 0 0 0 0 0 0 1 0 0 0 0 0 0 0 0 AC 11 - 5 1 1 1 1 1 1 1 1 0 0 0 1 1 0 0 1 1 1 0 0 0 0 0 0 0 AC 11 - 6 0 1 0 1 1 1 1 1 1 1 1 1 1 1 1 0 1 1 1 1 1 1 1 1 1 Anexo 7. Matriz de similitud generada a partir de datos moleculares de Cucúrbita L. ECU-4976 ECU-4976 ECU-4977 ECU-4978 ECU-4979 ECU-4980 ECU-4981 ECU-4983 ECU-4984 ECU-4992 ECU-5308 ECU-5309 ECU-5310 ECU-5311 ECU-5312 ECU-5313 ECU-5326 ECU-5329 ECU-5330 ECU-5338 ECU-5343 ECU-12382 1 ECU-4977 0,3225806 1 ECU-4978 0,4285714 0,3783784 1 ECU-4979 0,2424242 0,625 0,5 1 ECU-4980 0,1666667 0,5862069 0,3636364 0,7037037 1 ECU-4981 0,1714286 0,5757576 0,4166667 0,625 0,6428571 1 ECU-4983 0,1470588 0,6129032 0,3243243 0,6666667 0,6296296 0,7241379 1 ECU-4984 0,1428571 0,59375 0,3513514 0,7 0,6071429 0,7586207 0,8846154 1 ECU-4992 0,1428571 0,5 0,3157895 0,5454545 0,5517241 0,7586207 0,6896552 0,6666667 1 ECU-5308 0,1081081 0,2380952 0,2142857 0,3 0,2432432 0,3 0,3888889 0,3783784 0,3421053 1 ECU-5309 0,0526316 0,2439024 0,1904762 0,275 0,2857143 0,3076923 0,3611111 0,3888889 0,3888889 0,6451613 1 ECU-5310 0,0833333 0,2820513 0,2564103 0,2820513 0,2941176 0,3513514 0,4117647 0,4 0,3611111 0,6666667 0,6333333 1 ECU-5311 0,1428571 0,3783784 0,25 0,3076923 0,3636364 0,3783784 0,4411765 0,4285714 0,3888889 0,59375 0,5151515 0,6896552 1 ECU-5312 0,0882353 0,2 0,2368421 0,2307692 0,2727273 0,2972973 0,3142857 0,3055556 0,3428571 0,5483871 0,516129 0,5333333 0,6206897 1 ECU-5313 0,0357143 0,2121212 0,1818182 0,25 0,36 0,3333333 0,3103448 0,3448276 0,3448276 0,3793103 0,3928571 0,4615385 0,56 0,5 1 ECU-5326 0,1 0,2222222 0,2285714 0,2571429 0,3571429 0,3333333 0,2727273 0,3030303 0,3030303 0,3333333 0,4827586 0,3548387 0,2647059 0,2121212 0,2307692 1 ECU-5329 0,2857143 0,3428571 0,3142857 0,3428571 0,28125 0,3055556 0,2857143 0,3529412 0,2432432 0,2702703 0,2777778 0,2162162 0,2105263 0,2647059 0,2068966 0,3448276 1 ECU-5330 0,1290323 0,2777778 0,25 0,3142857 0,3793103 0,3939394 0,375 0,40625 0,3636364 0,3142857 0,40625 0,3333333 0,2857143 0,2727273 0,3076923 0,6521739 0,5185185 1 ECU-5338 0,0714286 0,1388889 0,1111111 0,1714286 0,2068966 0,2058824 0,21875 0,25 0,2121212 0,3666667 0,4285714 0,3928571 0,3333333 0,3703704 0,3809524 0,375 0,3333333 0,4583333 1 ECU-5343 0,1111111 0,1714286 0,1111111 0,1714286 0,2068966 0,2424242 0,21875 0,25 0,2903226 0,3666667 0,4814815 0,2580645 0,2121212 0,3703704 0,2083333 0,5 0,44 0,5217391 0,4285714 1 ECU-12382 0,1428571 0,4827586 0,2727273 0,4333333 0,5416667 0,4827586 0,4642857 0,4 0,4 0,2285714 0,2352941 0,28125 0,3125 0,3448276 0,2916667 0,1666667 0,1875 0,1935484 0,2307692 0,1851852 1 ECU-12393 0,0882353 0,3333333 0,2368421 0,3333333 0,4 0,4117647 0,3529412 0,3428571 0,3428571 0,4117647 0,4242424 0,5333333 0,516129 0,4666667 0,3846154 0,25 0,1621622 0,2727273 0,3703704 0,2333333 0,4444444 ECU-12399 0,125 0,2702703 0,2777778 0,3055556 0,3666667 0,3823529 0,3235294 0,3529412 0,3529412 0,46875 0,5333333 0,6071429 0,5333333 0,4333333 0,4583333 0,3 0,1666667 0,3225806 0,3846154 0,2413793 0,3103448 ECU-12400 0,1935484 0,3333333 0,2702703 0,3333333 0,4 0,3714286 0,3529412 0,3823529 0,3428571 0,5 0,46875 0,5862069 0,6206897 0,4666667 0,5 0,25 0,1944444 0,3125 0,3703704 0,1935484 0,3 ECU-12408 0,2666667 0,2894737 0,2972973 0,3243243 0,34375 0,3243243 0,3055556 0,3333333 0,2972973 0,53125 0,4117647 0,516129 0,5483871 0,4516129 0,4230769 0,2424242 0,2222222 0,3030303 0,3103448 0,2258065 0,25 Continuación anexo 7 ECU-12393 ECU-12399 ECU-12400 ECU-12408 1 0,7916667 1 0,6923077 0,8695652 1 0,6071429 0,76 0,875 1