Hibridación Antes que nada, Química Orgánica es todo lo relacionado con... Química Orgánica
Anuncio

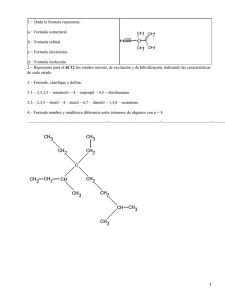
Hibridación Química Orgánica Antes que nada, Química Orgánica es todo lo relacionado con las sustancias orgánicas, es decir, todas aquellas que tienen Carbono en su composición molecular. El Carbono es un elemento muy importante debido a su gran capacidad de formar enlaces con otros elementos, y es debido a su gran diversidad el motivo por el cual una rama de la ciencia se encarga especialmente de su estudio. Una de las características especiales del carbono es su capacidad de Hibridación, la cual es un proceso mediante el cual se unen dos especies diferentes para formar una nueva. Hibridación SP del Carbono: En química, la hibridación ocurre entre orbitales, por ejemplo, la hibridación de los orbitales sp, en el Carbono: Para analizarla, primero se escribe su configuración electrónica: Carbono 6 !! !! !_____!_______ 1s 2s 2px 2py 2pz Para llevar a cabo la hibridación, y así el Carbono sea capaz de combinarse con otros elementos para formar alquinos, se pasa un electrón del orbital 2px al orbital 2pz: !! !!___ _____!_____!___ 1s 2s 2px 2py 2pz Luego, se pasa un electrón del orbital 2s al 2px !! ! !_____!_____!_ 1s 2s 2px 2py 2pz Por último, se renombran los orbitales: !! ! !_____!_____!_ 1s 2sp 2sp 2sp 2sp Hibridación SP2 del Carbono: Carbono 6 !! !! !_____!_______ 1 1s 2s 2px 2py 2pz Para llevar a cabo la hibridación, y así el Carbono sea capaz de combinarse con otros elementos para formar alquenos, se pasa un electrón del orbital 2py al orbital 2pz: !! !!___ !___________!___ 1s 2s 2px 2py 2pz Luego, se pasa un electrón del orbital 2s al 2py !! ! !_____!_____!_ 1s 2s 2px 2py 2pz Por último, se renombran los orbitales: !! ! !_____!_____!_ 1s 2sp2 2sp2 2sp2 2sp2 Hibridación SP3 del Carbono: Carbono 6 !! !! !_____!_______ 1s 2s 2px 2py 2pz Para llevar a cabo la hibridación, y así el Carbono sea capaz de combinarse con otros elementos para formar alcanos, se pasa un electrón del orbital 2s al orbital 2pz: !! !___ !_____!_____!___ 1s 2s 2px 2py 2pz Por último, se renombran los orbitales: !! ! !_____!_____!_ 1s 2sp3 2sp3 2sp3 2sp3 Mediante la hibridación, además de hacer posible la tetravalencia del Carbono, permite formar orbitales más estables, y éstos a su vez, enlaces más estables. Isomería Es la ciencia que estudia a los isómeros, que son compuestos que tienen la misma composición centesimal, pero difieren den algunas propiedades por una diferencia mínima en su estructura molecular. Isomería estructural o de Cadena: 2 C4H10: Butano = CH3 − CH2 − CH2 − CH3 IsoButano = Isomería de Grupo Funcional: C2H6O: CH3 − CH2 − OH CH3 − O − CH3 Isomería de Posición: C3H7Br: CH3 − CH − CH2 − Br Isomería Geométrica: Cis = Trans = Nomenclatura Para nombrar a los compuestos con carbono se siguen distintas reglas, dependiendo de los elementos que lo conformen. El nombre se asigna conforme a su complejidad, tal y como sigue en la tabla de abajo. Si en un compuesto hay dos o mas radicales, se nombrará de acuerdo con el radical más compuesto, y los otros serán secundarios. Grupo Funcional Alcoholes R − OH Alcohol Secundario Alcohol Terciario Ésteres Éteres R−O−R Cetonas Aldehídos Aminas Primarias Aminas Secundarias R − CH = O R − NH2 R − NH − R Aminas Terciarias 3 Ácidos Carboxílicos R − COOH Amidas Nitro N° Componentes 1 2 3 4 5 6 Prefijo Met Et Pro But Pent Hex N° Componentes 7 8 9 10 11 12 Prefijo Hept Oct Non Dec Undec Duodec Alcanos: • Encontrar la cadena más larga posible que contenga solo carbonos (ésta será la base) • Numerar buscando que el radical más complejo quede cerca • Nombrar la base, como se trata de alcanos, se pondrá el prefijo que indique el número de componentes de la cadena, con terminación ano • Nombrar las ramificaciones indicando su posición y colocando el prefijo que indique la cantidad de radicales presentes • Al final poner el nombre de la base. (se numeró de derecha a izquierda sobre la base de color turquesa) 3, 5, 6 − trimetil − 4 − etil − octano (se numeró de derecha a izquierda y de abajo a arriba) 6 − Bromo − 3, 7 − dimetil − 5 − isopropil − undecano. 4 (se numeró de izquierda a derecha) 3 − Flúor − 5 − Bromo − 2, 4 − metil − 4 − etil − octano. Alquenos: • Encontrar la cadena más larga posible que contenga solo carbonos y todos los dobles enlaces presentes • Numerar buscando que el radical más complejo quede cerca • Nombrar la base, como se trata de alquenos, se pondrá el prefijo que indique el número de componentes de la cadena, con terminación eno • Nombrar las ramificaciones indicando su posición y colocando el prefijo que indique la cantidad de radicales presentes • Al final poner el número del carbono en el cual se sitúa el doble enlace, y por último, el nombre de la base. (se numeró de arriba a abajo) 2,3, 6, 6 − tetrametil − 4 − octeno (se numeró de abajo a arriba) 1 − metil − 3 − secpentil − 1,3 − pentadieno (se numeró de arriba abajo, como el radical es demasiado complejo, se formó una cadena secundaria en color azul, y apartir de ella se nombraron otros radicales; esto se pone entre paréntesis) 5 2(4 − Cloro − 2,2 − dietil − pentil) − 1, 3 − butadieno Alquinos: • Localizar la cadena continua de carbonos más larga que contenga enlaces triples, utilizando las mismas raíces usadas en los alcanos, solo que con terminación ino, según sea el número de triples enlaces presentes, e indicando su posición. • Numerar buscando que el radical más complejo quede cerca • Nombrar las ramificaciones indicando su posición y colocando el prefijo que indique la cantidad de radicales presentes • Al final poner el número del carbono en el cual se sitúa el doble enlace, y por último, el nombre de la base. (se numeró de arriba abajo) 6 − Flúor − 5 Bromo − 7 − metil − 4 etil − 5,7 − dieno − 3 − octino. (se numeró de derecha a izquierda) 5 − Flúor − 4, 6 − dimetil − 5(Bromo metil) − 2 heptino (se numeró de derecha a izquierda) 3 − metil − 3 − etil − 4 − terbutil − 4 eno − 1 − pentino Benceno C6H6 El benceno es un compuesto aromático formado por seis átomos de Carbono y seis de Hidrógeno. La Aromaticidad estudia los compuestos del benceno y similares. El benceno, al combinarse con otros elementos, forma un gran número de solventes, desinfectantes y colorantes. Su estructura se asemeja a la de una tuerca de seis lados iguales. 6 Representaciones del Benceno Nombre si es base Representación Nombre si es ramificación Formado por: Usos: Halurobencenos X Halógenos (Flúor, Cloro, Bromo, Yodo) Solventes Tolueno Metil CH3 Solvente Fenol Hidroxi OH Primer desinfectante que existió Anisol Metoxi O − CH3 Solvente Anilina Amino NH2 Materia prima de colorantes y solventes NO2 Materia prima en la síntesis de numerosos compuestos aromáticos y explosivos CH = O Desinfectante y materia prima de colorantes O = COH Desinfectante y conservador de alimentos Nitrobenceno Benzaldehído Ácido Benzóico Nitro Al Oico 7 Benzamida −−− COONH2 Desinfectante y conservador. Nomenclatura de compuestos aromáticos: Según la posición de las ramificaciones en el anillo del benceno, se nombrará de la siguiente manera: Orto Meta Para O−M−P− 234 La nomenclatura por medio de números se llama IUPAC. Para nombrar a los compuestos aromáticos, se numera a partir de la ramificación más compleja, la cual será la base, y en sentido de las ramificaciones que tenfan más complejidad. Se pone primero la forma en la que se encuentran las ramificaciones, seguido por el nombre de la ramificación más pequeña, y por último el nombre del compuesto (Por ejemplo, orto − metil − anisol) 8 Base: Anisol Base: Ácido Benzóico IUPAC = 3 − etil − Anisol. IUPAC = Ácido 2 − Hidroxi − benzóico Común = Meta − etil − Anisol. Común = Ácido Orto − Hidroxi − Benzóico Nomenclatura de Aromáticos Poli sustituidos (se numeró a partir de COONH2 en sentido contrario a las manecillas del reloj) 2 − Cloro − 4 − isopropil − 5 − oico − benzamida (se numeró a partir del NH3 en sentido de las manecillas del reloj) 2, 5 − dicloro − 4 − metoxi − anilina 9 Alcoholes • Seleccionar la cadena continua de carbonos más larga y que contenga la mayor cantidad posible de grupos hidroxilo (OH). Ésta será la base de la molécula y se nombrara de la misma manera que el alcano, alqueno, alquino o hidrocarburo cícliclo, dando la terminación respectiva de los alcoholes (ol, diol, triol) de acuerdo con el número de OH's presentes, en indicar sus posiciones • Numerar la base, de modo que los OH's queden en la menor posición posible • Nombrar las ramificaciones. Terminar con el nombre de la base • Las ramificaciones que contienen OH's, se nombran anteponiendo el nombre del alquil, alquenil, alquinil o cicloalquil correspondiente la palabra hidroxi, dihidroxi, trihidroxi, según el número de OH's presentes, e indicando sus posiciones. (se numeró de izquierda a derecha) 6 − Bromo − 3 (hidroxi − 1 − etinol) − hexanopentanol − 1,2,4,5,5 (se numeró de derecha a izquierda) 4 − Bromo − 3,6,6 − trimetil − 3 − etinil − nonenopentanol − 1,1,1,2,5 (se numeró de abajo a arriba) Cis − 2, 4 − dimetil − 3(2 − metil − 1 − propeno) − 5,7 − octodiinotriol − 1,2,8. Éteres Sesigue el mismo proceso que con los alcoholes, solo que se le agrega a la cadena base el prefijo OXA, y sus posiciones se indican al final. Se identifican cuando la molécula posee las partículas R − O − R 10 (se numeró de derecha a izquierda) 2 − metil − 4 − hidroxi − oxapentano − 2. (se numeró de izquierda a derecha) 3 − metil − 2(2 − Bromo − 1 metil − etanil) − 5 − dioxahexeno − 1,2 (se numeró de derecha a izquierda) 6 − Flúor − 6 − metil − 3 − n − propil − 5 − oxi − etil − trioxapentano − 1,2,6. Aminas • Cuando la molécula contenga un solo grupo de amina, se nombrará por separado cada radical • Se ordenarán en orden creciente de complejidad y se terminará con la palabra amina • Hay aminas primarias (NH2), secundarias (NH) y terciarias (N) (se nombró en orden de complejidad) N − Etil − N − 1 − Bromo − etil − amina 11 (se numeró de abajo a arriba) 2, 5 − dimetil − 5(1 − metil − 2 − propenil) − 4 − etinil − 5 − oxi − hexano − amina − 3. 2 − Bromo − n − propil 1 − Flúor − 1 − propenil (se nombra en orden de complejidad alrededor del N) N − Bromo − N − 2 − Bromo − n − propil − N − 1 − Flúor − 1 − propenil − amina Aldehídos Los aldehídos se caracterizan por tener un doble enlace con el Oxígeno en su grupo funcional, el cual tiene que estar en sus orillas: R − CH = O. Se forman al reaccionar un alcohol primario con el oxígeno. Al finalizar se le agrega la terminación AL. (se numeró de derecha a izquierda) 3 − 7 − Dimetil − 2,6 − octadienal (se numeró de derecha a izquierda) 3 (2 − oxa − etil) 3 − hexenodial Cetonas Provienen de la oxidación de un alcohol secundario. Su terminación es ONA. 12 (se numeró de izquierda a derecha) 5 − Hidroxi − 3 − pentinona − 2 (se numeró de izquierda a derecha) 3 − amino − 2 (1 − ona − etil) − 4 − heptinodiona − 2,6 Ácidos Carboxílicos Se forman de la reacción de un aldehído con el Oxígeno, y entre su composición se encuentra la partícula R − COOH. Para nombrarlos, primero que nada se pone la palabra Ácido, seguido por los demás componentes como se ha venido nombrando hasta ahora, y al final, se le agrega la palabra ICO. (se numeró de derecha a izquierda) Ácido 3 − Bromo − 2 − hidroxi − pentanoico Ésteres Se forman de la reacción de un alcohol con un ácido carboxílico. Se identifica por poseer un Oxígeno en medio de la molécula, con una ramificación ácida y otra alcohólica. Para nombrarlo, primero se tiene que identificar la parte ácida, la cual llevará en su terminación la palabra ATO, y después se pone de y por último la parte alcohólica, a la cual se le pondrá la terminación ILO. 2 − Cloro − 4 − hidroxi − butanoato de etenilo 13 3 − Cloro − propanoato de 2 − hidroxi − 3 al − propilo. Amidas Se forman de la reacción de una amina y un ácido carboxílico. Para ello, el grupo CONH2 debe de ir en una orilla. Para nombrarlas se sigue el mismo proceso que con los demás compuestos, y al final se le agrega la palabra AMIDA. (se numeró de derecha a izquierda) oico − propanoamida (se numeró de izquierda a derecha) 6 − Bromo − 2,3 − dimetil − 3 − amino − 4 ona − 5 (2− hidroxi − 1 − oxi − etil) − heptanodiamida (se numeró de derecha a izquierda) 3 − Cloro − 3 − metil − hexanodiamida Macromoléculas: Carbohidratos: Fórmula = Cn(H2O)n. Los carbohidratos se forman de la unión de un aldehído o una cetona + alcohol. Se dividen en 3 tipos: 14 • Monosacáridos: De un solo Carbono (Como la Glucosa) • Oligosacáridos: De 2 hasta 10 Carbonos (Glucosa + Fructosa) • Polisacáridos: De más de 11 Carbonos Proteínas: Son macromoléculas formadas por polipéptidos, y éstos son formados por aminoácidos: Al unir un par de aminoácidos se forma un enlace peptídico Lípidos Grupo heterogéneo, formado por CHO, y forman la membrana celular (grasas). Sirven como energía de reserva. Se dividen en dos: simples y complejos. También se clasifican en saturados, como las grasas, e insaturadas, como los aceites. Química Orgánica 15