Aspectos perioperatorios de la implantación de un estimulador vagal
Anuncio
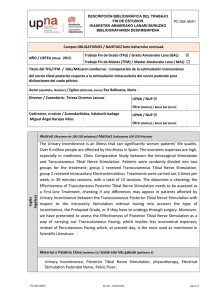
Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. (Rev. Esp. Anestesiol. Reanim. 2010; 57: 431-438) FORMACIÓN CONTINUADA Formación acreditada Aspectos perioperatorios de la implantación de un estimulador vagal F. Iturri Clavero1, A. González Uriarte1, G. Tamayo Medel1,2, I. C. Pomposo Gaztelu3, M. Cano Dorronsoro1,2, A. Martínez Ruiz1 Servicio de Anestesiología y Reanimación. Hospital de Cruces. Baracaldo. Bizkaia. 2Departamento de Farmacología. Universidad del País Vasco. EHU-UPV. 3Servicio de Neurocirugía. Hospital de Cruces. Departamento Cirugía. Universidad del País Vasco. EHV-UPV. Baracaldo. Bizkaia. 1 Resumen La estimulación vagal se ha convertido en una modalidad importante en el tratamiento de la epilepsia refractaria, que sigue siendo su indicación principal. Sus indicaciones terapéuticas se han visto ampliadas, siendo aprobado para el tratamiento de la depresión mayor. En la actualidad siguen en estudio otras posibles indicaciones como la obesidad mórbida, la enfermedad de Alzheimer, síndromes de dolor crónico y algunos trastornos neuropsiquiátricos. En este artículo se revisan los aspectos perioperatorios de este procedimiento terapéutico, lo cual permitirá un mejor y más integral manejo del mismo. Palabras clave: Epilepsia. Tratamiento. Estimulación del nervio vago. Perioperative considerations in vagal nerve stimulator implantation Summary Vagal nerve stimulation has become an a important tool in the treatment of refractory epilepsy, which continues to be the main indication for this technique. Other therapeutic indications are emerging, however, and vagal nerve stimulation has now been approved for major depression. Additional possible uses under study include morbid obesity, Alzheimer disease, chronic pain syndromes, and certain neuropsychologic disorders. This review considers perioperative aspects relevant to using this therapeutic procedure with a view to facilitating better and more integrated management of its application. Key words: Epilepsy. Therapeutics. Vagal nerve stimulation. 1. Introducción 2. Estimulación del nervio vago 3. Efectos secundarios de la estimulación vagal 4. Consideraciones anestésicas 5. Visita preanestésica 6. Intraoperatorio 7. Mantenimiento de la anestesia 8. Postoperatorio inmediato 9. Consideraciones clínicas en el paciente portador del dispositivo 1. Introducción La estimulación vagal es una modalidad de tratamiento, no farmacológica y no destructiva de la epilepsia farmacorresistente, que fue aprobada por la FDA en Correspondencia: Dr. Fernando Iturri Clavero C/ Iparbide, 17, 3ºC. 48991 Algorta. Bizkaia E-mail: [email protected] Aceptado para su publicación en mayo de 2010. 39 1997. La estimulación del nervio vago mediante un sistema programable implantado se ha convertido en una modalidad importante en el tratamiento de la epilepsia refractaria, que sigue siendo su indicación principal. Posteriormente sus indicaciones terapéuticas se ampliaron en 2005 y fue aprobado para el tratamiento de la depresión mayor. En la actualidad siguen en estudio otras posibles indicaciones como la obesidad mórbida, la enfermedad de Alzheimer, síndromes de dolor crónico y algunos trastornos neuropsiquiátricos. Debido al creciente número de pacientes a los que se implanta o que son portadores de un estimulador vagal, el anestesiólogo puede encontrarlos en su ámbito de trabajo y debe conocer su manejo. El objetivo de este artículo es revisar los aspectos perioperatorios de este procedimiento terapéutico. 2. Estimulación del nervio vago El estimulador vagal es un dispositivo que consta de un generador de pulsos, semejante a un marcapasos cardiaco, y de un cable que posee en su extremo proximal de tres formaciones helicoidales (un electrodo 431 Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Rev. Esp. Anestesiol. Reanim. Vol. 57, Núm. 7, 2010 positivo, uno negativo y uno de anclaje) (Fig. 1) que se colocan abrazando al nervio vago para su estimulación. En el otro extremo el cable finaliza en dos conectores (positivo y negativo) para el generador. Quirúrgicamente, el nervio vago izquierdo es aislado dentro de la vaina carotídea entre la vena yugular y la arteria carótida. La exposición de aproximadamente 3 cm del vago es suficiente para la colocación de los electrodos. Una vez aislado el nervio, se crea un bolsillo subcutáneo por encima de la fascia pectoralis mediante una incisión en la parte anterior del tórax. Algunos autores sugieren la implantación submuscular debajo del pectoral en pacientes pediátricos, en especial en aquellos con retraso mental o hiperactivos, para evitar que la manipulación del estimulador pueda dañarlo2. Mediante un dispositivo, antes del cierre, se comprueba el generador, así como la impedancia de todas las conexiones, realizándose en este momento un test de prueba. Se ha comprobado que en modelos animales la estimulación del nervio vago derecho e izquierdo tiene igual efecto en el control de las crisis epilépticas. La estimulación bilateral no parece aportar mayores beneficios. Por otra parte, los cambios en el EEG inducidos por la estimulación vagal son semejantes en ambos hemicórtex. En general3, el dispositivo se coloca preferentemente en el nervio vago izquierdo. Esta elección del nervio vago izquierdo se basa en la asimetría de ambos nervios vagos con respecto a la inervación cardiaca. El nervio vago izquierdo conduce la mayoría de las fibras parasimpáticas que inervan, con escasa densidad, los Fig. 1. Estimulador del nervio vago en el momento de su implante quirúrgico. 432 ventrículos, y el nervio vago derecho conduce la mayoría de las fibras parasimpáticas que inervan más densamente las aurículas4. No se conoce con precisión el mecanismo por el cual la estimulación del nervio vago izquierdo presenta efecto antiepiléptico. Se ha postulado que los estímulos eléctricos podrían inhibir la sincronización en distintos núcleos que deben descargar al unísono para que la actividad eléctrica cerebral normal se convierta en una crisis epiléptica. Aunque varios mecanismos podrían explicar no sólo su efecto antiepiléptico, sino el resto de sus efectos beneficiosos. El estudio del mecanismo de acción ha sido objeto de extensa revisión por algunos autores5. 3. Efectos secundarios de la estimulación vagal Cardiacos La afirmación de que la estimulación del nervio vago izquierdo no produce efecto cronotrópico6-8 parece contradecir el principio probado de que la activación vagal produce bradicardia9, y ha sido explicada por la asimetría de la inervación cardiaca vagal10. Sin embargo, Frei et al11 publicaron un estudio en el cual observaron que, separando los periodos de activación del estimulador de aquellos en los que el sistema no funcionaba, la estimulación del nervio vago izquierdo producía bradicardia y disminución de la variabilidad del ritmo cardiaco. Posteriormente en otro artículo12 ampliando esta serie, los mismos autores concluyeron que la estimulación del nervio vago izquierdo a alta intensidad tiene efectos complejos sobre el ritmo cardiaco espontáneo y sobre la variabilidad del mismo, mostrando además una gran diversidad interindividual. Se ha publicado una serie de cuatro casos de asistolia durante la estimulación intraoperatoria del nervio vago izquierdo 13, cifrando los autores el riesgo de padecer una asistolia en un 0,1%, en base a la exposición de más de 3.000 pacientes a esta técnica. Asconapé et al14 analizaron las posibles causas de dos episodios de bradicardia y de una asistolia en el periodo intraoperatorio de la colocación de un estimulador de nervio vago. Uno de los posibles mecanismos podría ser la posición inadecuada de los electrodos por su colocación invertida (el electrodo negativo debe ser craneal). Dicha colocación, en estudios animales, aumenta de forma significativa la afectación cardiaca15. Otras posibilidades son su colocación proximal a la salida de los nervios cardiacos superior e inferior, o la estimulación colateral de estas ramas, que estaría favorecida por la presencia de sangre o suero salino que actuarían como conductores. 40 Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. F. ITURRI CLAVERO ET AL– Aspectos perioperatorios de la implantación de un estimulador vagal Un aspecto relevante es la posibilidad de que la técnica anestésica fuera un fenómeno coadyuvante. Morris16 presentó un caso de asistolia entre 28 estimuladores colocados, lo cual supone una incidencia del 3,6%, 6 veces superior a la media publicada. Aunque una posibilidad que explicaría los casos descritos por Tatum13 sería la sensibilidad a la estimulación vagal, una hipótesis alternativa enunciada por Lesser17 sería que los pacientes tienen una sensibilidad incrementada al estar con anestesia general, con la consecuente inhibición de las respuestas del tronco de encéfalo, incluidas las respuestas a la estimulación vagal. Respiratorios Se ha evidenciado durante los periodos de estimulación que la estimulación vagal crónica empeora los síntomas del síndrome de apnea obstructiva del sueño (SAOS). La primera comunicación sobre las alteraciones de la respiración durante el sueño fue publicada por Malow18 en una serie de 4 pacientes. Posteriormente otros autores han confirmado esta impresión inicial. Marzec19 comunica que hasta en un tercio de los pacientes de su serie existen cambios significativos en el índice apnea-hipopnea, este efecto era moderado en la mayoría de los casos. Sin embargo, los dos pacientes que presentaban historia de SAOS desarrollaron índices de apnea-hipopnea mayores de 10. En el postoperatorio inmediato se han descrito casos de parálisis de cuerda vocal izquierda con una frecuencia estimada en el 1%1. También se ha descrito ronquera con una incidencia en torno al 0,5%. La disfunción de la musculatura laríngea y de las cuerdas vocales aumenta el riego de aspiración. 4. Consideraciones anestésicas La implantación del estimulador vagal puede realizarse con anestesia regional20, sin embargo, suele realizarse con anestesia general por la posibilidad de que una crisis epiléptica durante el periodo intraoperatorio, pudiera comprometer la cirugía21-23. 5. Visita preanestésica Dentro de la valoración de estos pacientes para la implantación de estimuladores del nervio vago es importante conocer y revisar la patología médica asociada a la epilepsia, así como la posible presencia de síndromes que incluyen la epilepsia como una de sus manifestaciones, por ejemplo, la esclerosis tuberosa, que supone en una serie de casos infantiles de los 41 autores una proporción muy importante. Debemos conocer asimismo, el tipo de crisis, su frecuencia, y la presencia o ausencia de aura o de factores desencadenantes. Es necesario conocer el tratamiento al que el paciente esta sometido, y dentro de éste, es de importancia fundamental conocer el tratamiento anticomicial. Una gran proporción de los pacientes sometidos a la colocación de un estimulador vagal presentan epilepsia refractaria, por lo cual suelen estar en tratamiento con múltiples fármacos antiepilépticos. Se sabe que algunos anticomiciales como la fenitoína, la carbamazepina y el fenobarbital, son potentes inductores de las enzimas microsomales hepáticas, como el citocromo p450, y pueden alterar el metabolismo de los fármacos utilizados durante el procedimiento anestésico. De hecho, se ha constatado un incremento en la necesidad de opioides y la posibilidad de presentar resistencia a los bloqueantes neuromusculares24,25. Los anticomiciales pueden afectar también a estos fármacos causando una sobre expresión (“up-regulation”) de los receptores de la acetilcolina en la unión neuromuscular26,27. Esta variabilidad en la respuesta hace más necesaria una estrecha monitorización de la respuesta neuromuscular en estos pacientes. Otros posibles efectos secundarios de los fármacos anticomiciales deben tenerse en cuenta (Tabla 1). Entre ellos cabe destacar la presencia de acidosis metabólica asintomática sin anión Gap producida por el topiramato, como consecuencia de la inhibición de la anhidrasa carbónica28 y la disfunción plaquetaria asociada al ácido valproico con el riesgo de trastornos hemorrágicos29. El tratamiento anticomicial debe mantenerse hasta el momento de la cirugía30. Premedicación La premedicación es ventajosa dadas las alteraciones del comportamiento que padecen muchos de estos pacientes31-34. Las benzodiacepinas son útiles por ser capaces de disminuir la actividad convulsiva. Además poseen un antagonista específico si se presenta depresión respiratoria. Una excepción la constituyen los pacientes con síndrome de Lennox-Gastaut, en los que las benzodiacepinas pueden inducir crisis25,35. El midazolam es uno de los fármacos más frecuentemente utilizados, especialmente en niños y por vía intranasal, aprovechando su menor latencia, la ausencia de metabolismo de primer paso y los efectos clínicos más predecibles que por vía oral o rectal36-38. La vía intranasal ofrece una forma de premedicación más cómoda en la habitación y facilita el traslado posterior al área quirúrgica, evitando el llanto de la separación y por tanto la hiperventilación asociada, en este tipo de pacientes. 433 Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Rev. Esp. Anestesiol. Reanim. Vol. 57, Núm. 7, 2010 TABLA 1 Posibles efectos secundarios de los fármacos anticomiciales Nombre comercial Fármaco Efectos secundarios Epanutin Fenitoína Rubio Neosidantoína Sinergina Tegretol Carbamazepina (Alter, Normon) Depakine Depamide Luminal, Gardenal, Gatrusminal Luminaletas Crisomet, Labileno, Lamictal Fenitoína Carbamazepina Hiperplasia gingival, hirsutismo, anemia megaloblástica, rash cutáneo, ataxia, mareo, diplopía, nistagmo. Ataxia, mareo, diplopía, anemia, aplásica, rash, Síndrome Steven Johnson, leucopenia. Ácido Valproico Valproamida Fenobarbital Náuseas, vómitos, hepatotoxicidad, trombopenia, pancreatitis, encefalopatía, temblor. Derivado del ácido valproico, mismos efectos secundarios. Sedación, depresión del sistema nervioso central (SNC), anemia megaloblástica. Lamotrigina Rash cutáneo. Anomalías hepáticas alteraciones hemáticas. Edema facial, Precaución en asociación con ácido valproico, el cual duplica la concentración sanguínea de lamotrigina. Acidosis metabólica somnolencia, ataxia y confusión. Neutropenia, disminución de hemoglobina en sangre, reducción del campo visual. Somnolencia, psicosis. Náuseas, vómitos, cefalea, parkinsonismo. Topamax Sabrilex Topiramato Vigabatrina Etoxusimida Faes Zarontin Mysoline Taloxa Etoxusimida Primidona Felbamato Neurontin, Gabatur Gabapentina (Alter. Bexal, géminis, Kern, Ratiopharm, Rubio) Zonegran Rivotril Gabapentina Zonisamida Clonazepan Ospolot Gabitril Sultiamo Tiagabina Trileptal Keppra Oxcarbazepina Levetiracetam Similar a Fenobarbital. Insomnio, cefalea, anorexia, somnolencia, emesis, pérdida de peso y mareos incidencia relativamente alta de anemia aplásica algunas veces fatal y alteración hepática. Somnolencia, ataxia y mareos. A altas dosis puede producir, flatulencia, diarrea y mioclonias. Nefrolitiasis, anorexia, náuseas y ataxia. Somnolencia, fatiga, mareo, hipotonía muscular, trastornos de la coordinación. Raros trastornos sanguíneos. Alteración de las pruebas hepáticas. Hiperventilación, inquietud, ataxia, parestesias. Mareos, náuseas, astenia, intranquilidad, alteración en la concentración, letargia y depresión. Mareos, cefalea, diplopía, náuseas, emesis, ataxia e hiponatremia, rash. Astenia, incoordinación, labilidad emocional y ansiedad. La canalización de una vía intravenosa puede retrasarse hasta que ha producido su efecto la premedicación31,33,40. Se debe disponer de una vía IV antes de la inducción debido al elevado riesgo de complicaciones como arritmias y crisis convulsivas40,41. Debido a que la cirugía para la colocación de los electrodos en el nervio vago se desarrolla en íntima proximidad a la arteria carótida y a la vena yugular, se debe disponer de una vía que nos permita una administración rápida de volumen. En cuanto a la profilaxis antibiótica, la tasa de infección en el estudio clínico previo a la aprobación fue de 1,1%, posteriormente en una serie de 100 casos pediátricos se comunicó una tasa del 3%42. El germen más frecuentemente identificado fue el Staphylococcus aureus43. El tratamiento antibiótico profiláctico comienza en el preoperatorio y se mantiene durante las 24 horas postoperatorias68. 6. Intraoperatorio La elección del agente inductor en estos pacientes viene condicionada por dos aspectos fundamentales, por una 434 parte el estado funcional del paciente, y por otro los efectos pro o anticonvulsivantes de los distintos fármacos. Propofol. El uso de propofol en pacientes epilépticos es controvertido, con varios casos publicados en los que se comunica un efecto proconvulsivante45-48. Por el contrario, reduce la duración de las convulsiones durante la terapia electroconvulsiva49. Además, ha sido usado como tratamiento en pacientes con estatus epiléptico50-52. La preocupación sobre su seguridad en este tipo de pacientes no ha sido completamente aclarada53, y dicha controversia se ve reflejada en las recomendaciones contradictorias sobre su uso en pacientes epilépticos54-56. Una revisión sistemática de los fenómenos similares a convulsiones (“seizure-like”), es decir convulsiones, mioclonias y opistótonos, durante la anestesia con propofol muestra que suelen ocurrir principalmente durante la inducción y la educción, esto es, cuando hay cambios rápidos en la concentración del fármaco57. Existen casos descritos de este fenómeno que se presentaron varios días después de la administración de propofol en individuos susceptibles58. La relevancia clínica de estos movimientos y de 42 Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. F. ITURRI CLAVERO ET AL– Aspectos perioperatorios de la implantación de un estimulador vagal los cambios en el patrón de EEG no están claros. En pacientes epilépticos sometidos a resección del lóbulo temporal no se encontraron diferencias en la actividad epileptiforme entre tiopental y propofol en el electrocorticograma59. Esto sugiere que el propofol no tiene mayor efecto proconvulsivante que el tiopental. Habiéndose sugerido su uso en pacientes sometidos a cirugía de la epilepsia60. El primer estudio prospectivo sobre el uso del propofol en niños con epilepsia y dificultad de aprendizaje, ofrece nuevas perspectivas sobre el efecto del propofol en el EEG. Sus resultados parecen demostrar que el propofol es un agente hipnótico-sedante con propiedades anticonvulsivantes61. Etomidato. El etomidato presenta efecto tanto pro, como anticonvulsivante. A dosis altas suprime, mientras que a dosis bajas induce actividad motora involuntaria. Tanto la dosis, como la velocidad de administración determinan su efecto sobre el umbral convulsivo62. Ha sido usado para activar el registro electroencefalográfico de focos epileptógenos63. Por el contrario existen publicaciones de su uso para el tratamiento con éxito del estatus epiléptico64. Barbitúricos. En dosis terapéuticas anestésicas, los barbitúricos muestran un potente efecto anticonvulsivante. Además no se han publicado crisis clínicas, ni a nivel de EEG tras la administración de barbitúricos en pacientes no epilépticos65. Muchos estudios clínicos aportan evidencias sobre la eficacia anticonvulsivante de los barbitúricos a dosis anestésicas66. Sin embargo, cuando se administra a dosis bajas (subanestésicas), incluso el tiopental puede desencadenar actividad comicial clínicamente evidente67. Ketamina. La ketamina activa focos epilépticos en pacientes epilépticos. Se han documentado crisis clínicas tras la administración parenteral de ketamina tanto en pacientes epilépticos, como en no epilépticos62. La ketamina, por tanto, debería ser evitada en estos pacientes68,69. Opiáceos. Los opiáceos son capaces de producir actividad epileptiforme. Tanto el fentanilo, como el sufentanilo han mostrado causar actividad epileptiforme en el EEG, en dosis moderadas o grandes, en pacientes no epilépticos70. El alfentanilo es también capaz de inducir actividad epileptiforme en pacientes epilépticos71. El remifentanilo a dosis altas activa el sistema límbico, sin inducir crisis clínicas72. Halogenados. Todos los agentes inhalatorios modernos son capaces de inducir complejos de ondasupresión a dosis hemodinámicamente aceptables. El isoflurano, aunque usado como terapia en los casos de estatus epiléptico también ha sido asociado a actividad epileptiforme en pacientes epilépticos73. Es conocida la actividad epileptiforme en el EEG, tanto en niños como en adultos, durante la inducción con sevoflura43 no74,75. Asimismo, se ha comunicado con este agente la inducción de actividad epileptógena durante los niveles quirúrgicos de anestesia tanto en pacientes epilépticos como no epilépticos76,77. Sin embargo, los fenómenos “seizure-like” con sevoflurano se producen especialmente en individuos sensibles, por ejemplo en niños con tratamiento anticomicial o bien con antecedentes de convulsiones febriles 78. Los cambios se observan también con altas concentraciones de anestésico durante la inducción inhalatoria, pero a pesar de ello, la morbilidad del EEG epileptógeno no ha sido probada78. Las recomendaciones sugieren que la anestesia con sevoflurano parece ser segura incluso en pacientes epilépticos, si se evita la hiperventilación que rebaja el umbral convulsivo y se administran concentraciones inferiores a 1,5 CAM79. Bloqueantes neuromusculares. No se ha comunicado crisis clínicas o electroencefalográficas con ninguno de ellos usado a dosis clínicas. Se considera que el atracurio en infusión continua reduce el umbral de convulsión mediante la acumulación de su metabolito laudanosina. Esto no parece representar un problema relevante en su uso en quirófano desde el punto de vista clínico. 7. Mantenimiento de la anestesia El mantenimiento de la anestesia puede llevarse a cabo mediante el uso de sevoflurano, desflurano o isoflurano asociado a oxígeno y óxido nitroso o bien a oxígeno y aire. Si la función cardiaca no está comprometida, podemos usar propofol para mantener la hipnosis. Se debe evitar la hiperventilación y la hipoventilación en estos pacientes, dado que tanto los niveles bajos como altos de carbónico pueden favorecer la aparición de crisis comiciales. Los casos de asistolia se han relacionado con la dosis test. La dosis test supone una estimulación durante aproximadamente 15 seg a 1 mA, 500 μseg y 20 Hz. En pacientes portadores de un estimulador vagal que van a ser sometidos a una anestesia, Morris16 plantea la administración de un fármaco antimuscarínico profiláctico, así como la necesidad de disponer de un marcapasos temporal. En nuestra experiencia hemos administrado atropina de forma profiláctica, previa al test intraoperatorio, sin que apareciera bradicardia significativa en ningún caso de nuestra serie. 8. Postoperatorio inmediato El postoperatorio puede verse complicado por la posibilidad de aparición de crisis comiciales. Es aconsejable mantener al paciente cuidadosamente analge435 Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Rev. Esp. Anestesiol. Reanim. Vol. 57, Núm. 7, 2010 siado y euvolémico, con el fin de evitar que se desarrolle taquipnea que a su vez podría desencadenar crisis epilépticas40,80. Las crisis se deben sospechar en aquellos casos de despertar retrasado o de cambios inesperados en el nivel de conciencia. Otras complicaciones postoperatorias inmediatas son los hematomas peritraqueales por lesión de la arteria carótida o de la vena yugular. La aparición de dificultad respiratoria y/o el incremento de circunferencia cervical deben hacernos pensar en la existencia de un hematoma cervical. El tratamiento puede requerir una intubación de secuencia rápida y una revisión quirúrgica urgente de la herida. La lesión unilateral del nervio vago puede causar disnea y ronquera. Podemos diagnosticar esta incidencia mediante una laringoscopia directa o fibróptica1. 9. Consideraciones clínicas en el paciente portador del dispositivo La mayoría de los efectos viscerales durante la terapia con estimulación del nervio vago izquierdo, ocurren durante estados inusuales, tales como la anestesia general80 o en pacientes con ciertas condiciones comórbidas no relacionadas directamente con su epilepsia de base. SAOS La incidencia de SAOS en pacientes con epilepsia refractaria ha sido establecida en un 33%82. Esta cifra es muy alta, ya que en la población normal oscila entre un 5 y un 9%. Además se ha evidenciado que la estimulación vagal crónica empeora los síntomas de SAOS durante los periodos de estimulación. El SAOS es considerado un factor de riesgo de morbimortalidad perioperatoria83-87. Las primeras 24 horas postoperatorias han sido establecidas como las de mayor riesgo88. Las recomendaciones para el manejo de estos pacientes han sido recogidas en las guías de la Sociedad Americana de Anestesiólogos (ASA) para el manejo de los pacientes con SAOS89. Vía aérea. La estimulación vagal crónica ha sido asociada a varios tipos de disfunción laringofaríngea, siendo el más frecuente las alteraciones de la voz. Varios estudios como el de Zalvan90 han examinado a los pacientes con alteraciones de la voz durante la estimulación del nervio vago. En dichos estudios se ha documentado un desplazamiento medial del cartílago aritenoides y de la cuerda vocal izquierda durante el periodo de estimulación. En el estudio citado, en 2 pacientes adultos la cuerda vocal se desplazaba a la línea media y permanecía allí inmóvil durante el periodo de la estimulación90. En un estudio posterior el grupo de Lundy91 demostró que las 436 cuerdas vocales se desplazan hacia la línea media con la estimulación vagal a frecuencias de 40 Hz. Estos investigadores se dieron cuenta de que la dirección del movimiento de las cuerdas vocales es dependiente de la frecuencia de estimulación. A frecuencias de 20 Hz la estimulación del nervio vago produce abducción de la cuerda vocal. Estas diferencias de comportamiento posiblemente sean debidas a las diferencias en la respuesta de los músculos faríngeos a cada frecuencia. Un caso importante desde el punto de vista anestésico es el publicado por Bernards92, en el cual, un paciente portador de un estimulador vagal como tratamiento de una epilepsia refractaria, sin clínica de alteración de la vía aérea superior secundaria al mismo, desarrollo una obstrucción intermitente de la vía aérea objetivada mediante visión fibróptica a través de la mascarilla laríngea, mientras era sometido a una anestesia general y a ventilación con dicha mascarilla. Los periodos de obstrucción coincidían con los de estimulación vagal, mientras que la obstrucción cedía en los periodos de reposo. Otras consideraciones Si se precisa desfibrilación o cardioversión eléctrica de un paciente portador de un estimulador vagal existe la posibilidad de dañar el circuito. El fabricante (Cyberonics, Houston, EEUU) recomienda usar la mínima cantidad de energía eficaz en cada caso y colocar las palas del desfibrilador tan lejos del generador y de los electrodos como sea posible. Además se deben colocar las palas de modo que el vector de desplazamiento de la corriente sea perpendicular al sistema de estimulación vagal. El bisturí eléctrico o la ablación por radiofrecuencia pueden dañar el circuito. Aunque según el fabricante no es preciso desconectar el sistema, las maniobras para evitar dañar el circuito son similares a las que se toman con un marcapasos. A la hora de canalizar una vía central, lógicamente evitaremos la colocación en la vena yugular izquierda. Podemos observar interferencias eléctricas en el electrocardiograma, en pacientes con el dispositivo ya colocado, durante los periodos de estimulación. Apagar o no el generador durante la cirugía El fabricante del sistema no lo recomienda, sin embargo son varios los autores que sugieren esta posibilidad 92-94. Si decidimos intubar a estos pacientes debemos considerar la posible lesión de la cuerda vocal por la aducción intermitente de la misma contra el tubo endotraqueal. Además debemos considerar que la mayoría de los efectos viscerales están descritos en pacientes con anestesia general14. Bernards92, afirmó 44 Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. F. ITURRI CLAVERO ET AL– Aspectos perioperatorios de la implantación de un estimulador vagal que sería prudente apagar el sistema, si se decide ventilar a estos pacientes con una mascarilla laríngea. Para desconectar el sistema sólo debemos mantener un imán durante unos 65 segundos. Independientemente de si lo desconectamos o no deberemos consultar con un neurólogo para comprobar su funcionamiento y reprogramarlo una vez finalizada la cirugía. Así pues podemos concluir que la colocación de los dispositivos de estimulación vagal constituyen una importante herramienta terapéutica en pacientes con epilepsia refractaria a tratamiento convencional y a un número creciente de enfermedades. El conocimiento de los aspectos perioperatorios que rodean al paciente permite un mejor y más integral manejo del mismo. BIBLIOGRAFÍA 1. Hatton KW, McLarney JT, Pittman T, Fahy BG. Vagal nerve stimulation: overview and implications for anesthesiologists Anesth Analg. 2006;103(5):1241-9. 2. Álvarez LA, Dean P, Jayakar P, Duchowny M, Resnick T, Dunoyer C, et al. Epilepsy treatment by vagal stimulation. Rev Neurol. 1999;29(4):385-7. 3. McGregor A, Wheless J, Baumgartner J, Bettis D. Right-sided vagus nerve stimulation as a treatment for refractory epilepsy in humans. Epilepsia. 2005;46(1):91-6. 4. Saper CB, Kibbe MR, Hurley KM, Spencer S, Holmes HR, Leahy KM, et al. Brain natriuretic peptide-like immunoreactive innervation of the cardiovascular and cerebrovascular systems in the rat. Circ Res. 1990;67(6):1345-54. 5. Henry TR. Therapeutic mechanisms of vagus nerve stimulation. Neurology. 2002;59(Suppl. 4):S3-S14. 6. Handforth A, DeGiorgio CM, Schacter SC, Uthman BM, Naritokn DK, Tecoma ES, et al. Vagus nerve stimulation therapy for partial onset seizures: a randomized active control trial. Neurology. 1998;51(1):48-55. 7. Kamath MV, Upton RAM, Talalla A, Fallen EL. Neurocardiac responses to vagoafferent electrostimulation in humans. Pacing Clin Electrophysiol. 1992;15:1581-7. 8. Setty AB, Vaughn BV, Quint SR, Robertson KR, Messenheimer JA. Heart period variability during vagal nerve stimulation. Seizure. 1998; 7(3):213-7. 9. Levy MN, Martin P. Parasympathetic control of the heart. En: Randall WC, ed. Nervous control of cardiovascular function. New York: Oxford University Press. 1984. pp. 69-94. 10. Armour JA, Hopkins DA. Anatomy of the extrinsic efferent autonomic nerves and ganglia innervating the mammalian heart. En: Randall WC, ed. Nervous control of cardiovascular function. New York: Oxford University Press. 1984. pp. 20-45. 11. Han P, Frei MG, Osorio I. Probable mechanisms of action of vagus nerve stimulation in humans with epilepsy: is the heart a window into the brain? Epilepsia. 1996;37(5 suppl):83S. 12. Frei MG, Osorio I. Left vagus nerve stimulation with the neurocybernetic prosthesis has complex effects on heart rate and on its variability in humans. Epilepsia. 2001;42(8):1007-16. 13. Tatum WO, Moore DB, Stecker MM, Baltuch GH, French JA, Ferreira JA, et al. Ventricular asystole during vagus nerve stimulation for epilepsy in humans Neurology. 1999;52(6):1267-9. 14. Asconape JJ, Moore DD, Zipes DP, Hartman LM, Duffell WH. Bradycardia and asystole with the use of vagus nerve stimulation for the treatment of epilepsy: a rare complication of intraoperative device testing. Epilepsia. 1999;40(10):1452-4. 15. Smith CD, Bourland JD, Foster KS, Geddes LA, Schoenlein WE. The chronaxie and propagation velocity of canine vagus nerve fibers in vivo. Datos de los archivos de Cyberonics, Inc. 45 16. Morris C, Farling P. Remifentanil slows more than seizures. Br J Anaesth. 2003;91(2):301. 17. Lesser RP. Ventricular asystole during vagus nerve stimulation for epilepsy in humans. Neurology. 2000;54(3):776. 18. Malow BA, Edwards J, Marzec M, Sagher O, Fromes G. Effects of vagus nerve stimulation on respiration during sleep: a pilot study. Neurology. 2000;55:1450-54. 19. Marzec M, Edwards J, Sagher O, Fromes G, Malow BA. Effects of vagus nerve stimulation on sleep-related breathing in epilepsy patients. Epilepsia. 2003;44(7):930-5. 20. Penry JK, Dean JC. Prevention of intractable partial seizures by intermittent vagal stimulation in humans: preliminary results. Epilepsia. 1990;31(suppl 2):S40-3. 21. Tarver WB, George RE, Maschino SE, Holder LK, Wernicke JF. Clinical experience with a helical bipolar stimulating lead. Pacing Clin Electrophysiol. 1992;15(10 Pt 2):1545-56. 22. Reid SA. Surgical technique for implantation of the neurocybernetic prosthesis. Epilepsia. 1990;31(suppl 2):S38-9. 23. Landy HJ, Ramsay RE, Slater J, Casiano RR, Morgan R. Vagus nerve stimulation for complex partial seizures: surgical technique, safety, and efficacy. J Neurosurg. 1993;78(1):26-31. 24. Kofke WA, Tempelhoff R, Dasheiff RM. Anesthetic implications of epilepsy, status epilepticus, and epilepsy surgery. J Neurosurg Anesthesiol. 1997;9(4):349-72. 25. Modica PA, Tempelhoff R, White PF. Pro- and anti-convulsant effects of anesthetics (Part II). Anesth Analg. 1990;70(4):433-44. 26. Kim CS, Arnold FJ, Itani MS, Martyn JA. Decreased sensitivity to metocurine during long term phenytoin therapy may be attributable to protein binding and acetylcholine receptor changes. Anesthesiology. 1992;77(3):500-6. 27. Melton AT, Antognini JF, Gronert GA. Prolonged duration of succinylcholine in patients receiving anticonvulsants: evidence for mild upregulation of acetylcholine receptors? Can J Anaesth. 1993;40(10):939-42. 28. Groeper K, McCann ME. Topiramate and metabolic acidosis: a case series and review of the literature. Paediatr Anaesth. 2005;15(2):167-70. 29. Soriano SG, Bozza P. Anesthesia for epilepsy surgery in children. Childs Nervous System. 2006;22(8):834-43. 30. Roizen MF, Fleisher LA. Anesthetic implications of concurrent diseases. En: Millar RD, ed. Miller’s anestesia. 6th ed. Philadelphia, PA: Elsevier, Churchill Livingstone; 2005. pp. 1017-149. 31. Shenkman Z, Rockoff MA, Eldredge EA, Korf BR, Black PM, Soriano SG. Anaesthetic management of children with tuberous sclerosis. Paediatr Anaesth. 2002;12(8):700-4. 32. Lee JJ, Imrie M, Taylor V. Anaesthesia and tuberous sclerosis. Br J Anaesth. 1994;73(3):421-5. 33. Cote CJ, Todres ID, Ryan JF, Goudsouzian NG. A practice of anesthesia for infants and Children 3rd ed. Philadelphia, Pa: WB Saunders; 2001. pp. 45, 184-185, 573. 34. Cray SH, Dixon JL, Heard CM, Selsby DS. Oral midazolam premedication for paediatric day case patients. Paediatr Anaesth. 1996;6(4):265-70. 35. Modica PA, Tempelhoff R, White PF. Pro- and anti-convulsant effects of anesthetics (Part I). Anesth Analg. 1990;70(4):303-15. 36. Scott JL, Smith MS, Sanford SM, Rosenthal RE, Smith JP, Feied CF, et al. Effectiveness of transnasal butorfanol for the treatment of musculoskeletal pain. Am J Emerg Med. 1994;12(4):469-71. 37. Walbergh EJ, Wills RJ, Eckhert J. Plasma concentrations of midazolam in children following intranasal administration. Anesthesiology. 1991;74(2):233-5. 38. Rey E, Delauney L, Pons G, Murat I, Richard MO, Saint-Maurice C. Pharmacokinetics in midazolam in children: Comparative study of intranasal and intravenous administration. Eur J Clin Pharmacol. 1991;41(4):355-7. 39. Saint-Maurice C, Meistelman C, Rey E, Esteve G, de Leuture D, Bouvier d’Yvoire H. The pharmacokinetics of rectal midazolam for premedication in children. Anesthesiology. 1986;65(6):536-8. 40. Septer S, Thompson ES, Willemsen-Dunlap A. Anesthesia concerns for children with tuberous sclerosis. AANAJ. 2006;74(3):219-25. 41. Morgan GE, Mikhail MS, Murray MJ. Clinical Anesthesiology. 3rd ed. New York, NY: Mc-Graw-Hill; 2002. pp. 857-62. 42. Murphy JV, Torkelson R, Dowler I, Simon S, Hudson S. Vagal nerve stimulation in refractory epilepsy: the first 100 patients receiving vagal nerve stimulation at a pediatric epilepsy center. Arch Pediatr Adoles Med. 2003;157(6):560-4. 437 Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Rev. Esp. Anestesiol. Reanim. Vol. 57, Núm. 7, 2010 43. Patel NC, Edwards MS. Vagal nerve stimulator pocket infections. Pediatr Infect Dis J. 2004;23(7):681-3. 44. Meilán ML, Quecedo Gutiérrez L. Estimulación vagal en la epilepsia: Consideraciones anestésicas. Disponible en: www.uam.es/departamentos/medicina/anesnet/forconred/neuro/vago/vago.pdf 45. Hickey KS, Martin DF, Chuidian FX. Propofol-induced seizure-like phenomena. J Emerg Med. 2005;29(4):447-9. 46. Saunders PR, Harris MN. Ophistotonus and other unusual neurological sequelae after outpatient anaesthesia. Anaesthesia. 1990;45(7):552-7. 47. Sutherland MJ, Burt P. Propofol and seizures. Anaesth Intensive Care. 1994;22(6):733-7. 48. Hodkinson BP, Frith RW, Mee EW. Propofol and the electroencephalogram. Lancet. 1987;26(2):1518. 49. Simpson KH, Halsall PJ, Carr CM, Stewart KG. Propofol reduces seizure duration in patients having anaesthesia for electroconvulsive therapy. Br J Anaesth. 1988;61(3):343-4. 50. van Gestel JPJ, Blussé van Oud-Ablas HJ, Malingré M, Ververs FFT, Braun KPJ, van Nieuwenhuizen O. Propofol and thiopental for refractory status epilepticus in children. Neurology. 2005;65(4):591-3. 51. Rosetti AO, Reichhart MD, Schaller MD, Despland PA, Bogousslavsky J. Propofol treatment of refractory status epilepticus. A study of 31 episodes. Epilepsia. 2004;45(7):757-63. 52. Stecker MM, Kramer TH, Raps EC, O'Meeghan R, Dulaney E, Skaar DJ. Treatment of refractory status epilepticus with propofol: clinical and pharmacokinetic findings. Epilepsia. 1998;39(1):18-26. 53. Niermeijer JM, Uiterwald CS, Van Donselaar CA. Propofol in status epilepticus: little evidence, many dangers? J Neurol. 2003;250(10):1237-40. 54. Anonymous. Disoprivan 1%. En: Walker G, ed. ABPI Compendium of Data Sheets and Summaries of Product Characteristics, 1998-99. London: Datapharm Publications; 1998. pp. 1093-4. 55. Committee ADRA. Propofol convulsions. Australian Adverse Drug Reaction Bulletin. 1993: 7. 56. Borgeat A, Wilder-Smith OHG, Suter PM. The nonhypnotic therapeutic applications of propofol. Anesthesiology. 1994;80(3):642-56. 57. Walder B, Tramèr M, Seeck M. Seizure-like phenomena and propofol. Neurology. 2002;58(9):1327-32. 58. Thomas JS, Boheimer NO. An isolated grand mal seizure 5 days after propofol anaesthesia. Anaesthesia. 1991;46(6):508. 59. Hewitt PB, Chu DL, Polkey CE, Binnie CD. Effect of propofol on the electrocorticogram in epileptic patients undergoing cortical resection. Br J Anaesth. 1999;82(2):199-202. 60. Engelhard K. Werner C. Inhalational or intravenous anesthetics for craniotomies? Pro inhalational. Curr Opinion Anaesthesiol. 2006;19(5):504-8. 61. Meyer S, Shamdeen MG, Kegel B, Mencke T, Gottschling S, Gortner L, et al. Effect of propofol on seizure-like phenomena and electroencephalographic activity in children with epilepsy vs children with learning difficulties. Anaesthesia. 2006;61(11):1040-7. 62. Bhagat H, Dash HH. Anaesthesiologist´s role in the management of an epileptic patient. Indian J Anaesth. 2006;50(1):20-6. 63. Ebrahim ZY, DeBoer GE, Luders H, Hahn JF, Lesser RP. Effect of etomidate on the electroencephalogram of patients with epilepsy. Anesth Analg. 1986;65(10):1004-6. 64. Yeoman P, Hutchinson A, Byrne A, Smith J, Durham S. Etomidate infusions for the control of refractory status epilepticus. Intensive Care Med. 1989;15(4):255-9. 65. Roper SN, Alphin RS Epilepsy Surgery. Clinical Neuroanesthesia 2nd ed. Churchill Livingstone inc; 1998. pp 367-401. 66. Lowenstein DH, Aminoff MJ, Simon RP. Barbiturate anesthesia in the treatment of status epilepticus: clinical experience with 14 patients. Neurology. 1988;38(3):395-400. 67. Kofke WA, Dasheiff RM, Dong ML, Whitehurst S, Caldwell M. Anesthetic care during thiopental tests to evaluate epileptic patients for surgical therapy. J Neurosurg Anesthesiol. 1993;5(3):164-70. 68. Ferrer-Allado T, Brechner VL, Dymond A, Cozen H, Crandall P. Ketamine induced electroconvulsive phenomena in the human limbic and thalamic regions. Anesthesiology. 1973;38(4):333-44. 69. Bennett DR, Madsen JA, Jordan WS, Wiser WC. Ketamine anesthesia in brain-damaged epileptics: electroencephalographic and clinical observations. Neurology. 1973;23(5):449-60. 70. Kearse LA Jr, Koski G, Husain MV, Philbin DM, McPeck K. Epileptiform activity during opioid anesthesia. Electroencephalogr Clin Neurophysiol. 1993;87(6):347-9. 438 71. Ross J, Kearse LA Jr, Barlow MK, Houhton KJ, Cosgrove GR. Alfentanil-induced epileptiform activity: a simultaneous surface and depth electroencephalographic study in complex partial epilepsy. Epilepsia. 2001;42(2):220-5. 72. Kofke WA, Attaallah AF, Kuwabara H, Garman RH, Sinz EH, Barbaccia J, et al. The neuropathologic effects in rats and neurometabolic effects in humans of large-dose remifentanil. Anesth Analg. 2002;94(5):1229-36. 73. Iijima T, Nakamura Z, Iwao Y, Sankawa H. The epileptogenic properties of the volatile anesthetics sevoflurane and isoflurane in patients with epilepsy. Anesth Analg. 2000;91(4):989-95. 74. Vakkuri A, Yli-Hankala A, Sarkela M, Lindgren L, Hennander S, Korttila K. Sevoflurane mask induction of anaesthesia is associated with epileptiform EEG in children. Acta Anaesthesiol Scand. 2001;45(7):805-11. 75. YLi-Hankala A, Vakkuri A, Sarkela M, Lindgren L, Korttila K, Jantti V. Epileptiform electroencephalogram during mask induction of anesthesia with sevoflurane. Anesthesiology. 1999;91(6):1596-603. 76. Jääskeläinen S K, Kaisti K, Suni S, Hinkka S, Scheinin H. Sevoflurane is epileptogenic in healthy subjects at surgical levels of anesthesia. Neurology. 2003;61(8):1073-8. 77. Kurita N, Kawaguchi M, Hoshida T, Nakase H, Sakaki T, Furuya H. The effects of sevoflurane and hyperventilation on electrocorticogram spike activity in patients with refractory epilepsy. Anesth Analg. 2005;101(2):517-23. 78. Constant I, Seeman R, Murat I. Sevoflurane and epileptiform EEG changes. Pediatr Anesth. 2005;15(4):266-74. 79. Engelhard K, Werner C. Inhalational or intravenous anesthetics for craniotomies? Pro inhalational. Curr Opinion Anaesthesiol. 2006;19(5):504-8. 80. Diaz JH. Perioperative management of children with congenital phakomatoses. Paediatr Anaesth. 2000;10(2):121-8. 81. Lewis ME, Al-Khalidi AH, Bonser RS, Clutton-Brock T, Morton D, Paterson D, et al. Vagus nerve stimulation decreases left ventricular contractility in vivo in the human and pig heart. J Physiol. 2001;534(Pt 2):547-52. 82. Malow BA, Levy K, Maturen K, Bowes R. Obstructive sleep apnea is common in medically refractory epilepsy patients. Neurology. 2000;55(7):1002-7. 83. Boushra NN. Anaesthetic management of patients with sleep apnoea syndrome. Can J Anaesth. 1996;43(6):599-616. 84. Ogan OU, Plevak DJ. Anesthetic safety always an issue with obstructive sleep apnea. J Clin Monit Comput. 1998;14(1):69-70. 85. Catley DM, Thornton C, Jordan C, Lehane JR, Royston D, Jones JG. Pronounced, episodic oxygen desaturation in the postoperative period: its association with ventilatory pattern and analgesic regimen. Anesthesiology. 1985;63(1):20-8. 86. Ostermeier AM, Roizen MF, Hautkappe M, Klock PA, Klafta JM. Three sudden postoperative respiratory arrests associated with epidural opioids in patients with sleep apnea. Anesth Analg. 1997; 85(2):452-60. 87. Reeder MK, Muir AD, Foex P, Goldman MD, Loh L, Smart D. Postoperative myocardial ischaemia: temporal association with nocturnal hypoxaemia. Br J Anaesth. 1991;67(5):626-31. 88. Gupta RM, Parvizi J, Hanssen AD, Gay PC. Postoperative complications in patients with obstructive sleep apnea syndrome undergoing hip or knee replacement: a case-control study. Mayo Clin Proceed. 2001;76(9):897-905. 89. American Society of Anesthesiologists Task Force on Perioperative Management of Patients with Obstructive Sleep Apnea. Practice guidelines for the perioperative management of patients with obstructive sleep apnea: a report by the American Society of Anesthesiologists task force on perioperative management of patients with obstructive sleep apnea. Anesthesiology 2006;104:1081-93. 90. Zalvan C, Sulica L, Wolf S, Cohen J, González-Yanes O, Blitzer A. Laryngopharyngeal dysfunction from the implant vagal nerve stimulator. Laryngoscope. 2003;113(2):221-5. 91. Lundy DS, Casiano RR, Landy HJ, Gallo J, Gallo B, Ramsey RE. Effects of vagal nerve stimulation on laryngeal function. J Voice. 1993;7(4):359-64. 92. Bernards CM. An unusual cause of airway obstruction during general anesthesia with a laryngeal mask airway. Anesthesiology. 2004;100(4):1017-8. 93. Tovey G, Griffiths R. Vagal nerve stimulators and anaesthesia. Anaesthesia. 2001;56(7):703-4. 94. Aziz E, Radcliffe JJ. Vagal nerve stimulators and anaesthesia. Anaesthesia. 2001;56(12):1209-10. 46
 0
0
Anuncio
Documentos relacionados
Descargar
Anuncio
Añadir este documento a la recogida (s)
Puede agregar este documento a su colección de estudio (s)
Iniciar sesión Disponible sólo para usuarios autorizadosAñadir a este documento guardado
Puede agregar este documento a su lista guardada
Iniciar sesión Disponible sólo para usuarios autorizados