Presentación de PowerPoint
Anuncio
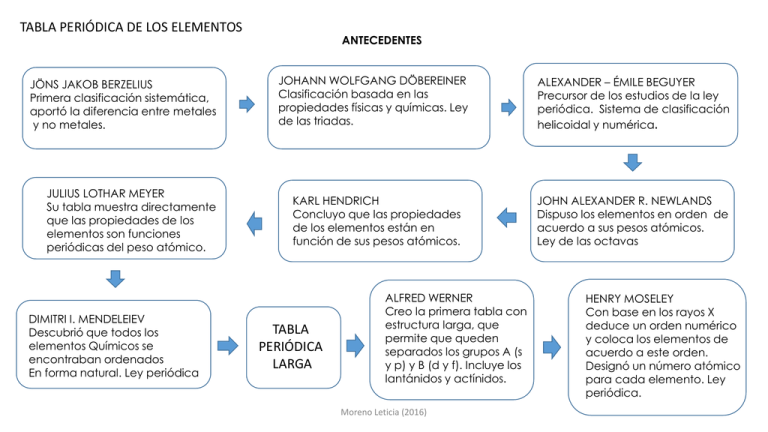
TABLA PERIÓDICA DE LOS ELEMENTOS JÖNS JAKOB BERZELIUS Primera clasificación sistemática, aportó la diferencia entre metales y no metales. JULIUS LOTHAR MEYER Su tabla muestra directamente que las propiedades de los elementos son funciones periódicas del peso atómico. DIMITRI I. MENDELEIEV Descubrió que todos los elementos Químicos se encontraban ordenados En forma natural. Ley periódica ANTECEDENTES JOHANN WOLFGANG DÖBEREINER Clasificación basada en las propiedades físicas y químicas. Ley de las triadas. KARL HENDRICH Concluyo que las propiedades de los elementos están en función de sus pesos atómicos. TABLA PERIÓDICA LARGA ALFRED WERNER Creo la primera tabla con estructura larga, que permite que queden separados los grupos A (s y p) y B (d y f). Incluye los lantánidos y actínidos. Moreno Leticia (2016) ALEXANDER – ÉMILE BEGUYER Precursor de los estudios de la ley periódica. Sistema de clasificación helicoidal y numérica. JOHN ALEXANDER R. NEWLANDS Dispuso los elementos en orden de acuerdo a sus pesos atómicos. Ley de las octavas HENRY MOSELEY Con base en los rayos X deduce un orden numérico y coloca los elementos de acuerdo a este orden. Designó un número atómico para cada elemento. Ley periódica. BERZELIUS DÖBEREINER Ley de las triadas: En su clasificación de las tríadas, Döbereiner explicaba que el peso atómico promedio de los pesos de los elementos extremos, es parecido al peso atómico del elemento de en medio. Por ejemplo, para la tríada cloro, bromo, yodo, los pesos atómicos son aproximadamente 35, 80 y 126; si sumamos 35 + 126 y dividimos entre 2, obtenemos 80 (aproximadamente), el peso atómico de 80 es el bromo. ALEXANDER – ÉMILE BEGUYER El creó la tabla periódica. En 1862, Chancourtois construyó una hélice de papel, en la que estaban ordenados por pesos atómicos (masa atómica) los elementos conocidos, arrollada sobre un cilindro vertical. Se encontraba que los puntos correspondientes estaban separados unas 16 unidades. Los elementos similares estaban prácticamente sobre la misma generatriz, lo que indicaba una cierta periodicidad, pero su diagrama pareció muy complicado y recibió poca atención. Moreno Leticia (2016) JOHN ALAEXANDER R. NEWLANDS Al disponer los elementos en orden de acuerdo con sus pesos Atómicos, observó que ocho elementos retirados de un elemento tenían propiedades físicas y químicas similares. JULIUS LOTHAR MEYER Anexó la gráfica de volúmenes atómicos, la cual es una manifestación de propiedades tales como: volatilidad, fusibilidad, maleabilidad y fragilidad. Se basó principalmente en las propiedades físicas. DIMITRI IVÁNOVICH MENDELEIEV Se baso principalmente en las propiedades químicas de los elementos. Moreno Leticia (2016) ALFRED WERNER Hace coincidir la estructura electrónica de los elementos con Su colocación dentro de la tabla. HENRY G. J. MOSELEY La tabla periódica actual se basa en gran medida en la tabla Periódica de Moseley. Moreno Leticia (2016) PERIODOS 1) 2) 3) 4) 5) 6) 7) ESTRUCTURA Son líneas horizontales en la tabla periódica y son 7 Los elementos que constituyen un periodo tienen propiedades progresivas a través de la tabla. El número del periodo determina el numero del último nivel de energía principal. Contiene solo al hidrógeno y al helio, llena al subnivel 1s Contiene 8 elementos, desde el litio hasta el neón. Llena los subniveles 2s y 2p. Contiene 8 elementos desde el sodio hasta el Aragón. Llena los subniveles 3s y 3p. Contiene 18 elementos desde el potasio hasta el criptón. Llena los subniveles 4s 3d y 4p. Contiene 18 elementos desde el rubidio hasta el xenón. Llena los subniveles 5s, 4d y 5p. Contiene 32 elementos desde el cesio hasta el radón. Llena los subniveles 6s, 4f, 5d y 6p. Contiene 32 elementos desde el francio hasta el elemento 118. Llena los subniveles s, 5f, 6d y 7p. Moreno Leticia (2016) BIBLIOGRAFÍA Chang, R., Química Ed. Mc Graw Hill (1998) Ebbing, D., Química General Ed. Mc Graw Hill (1997) Mortimer, C. ,Química Grupo Editorial Iberoamericano (1990) Daub, G., Seese, S., Química Ed. Pearson Educación, 7ª. Edición Sherman, A.,Sherman, J., Russikoff, L., Conceptos Básicos de Química, 1a. Ed.CECSA (2001) Resumen y adaptación: Mtra. Leticia Judith Moreno Mendoza Moreno Leticia (2016)