Micosis pulmonar por Paracoccidioides brasiliensis: confusión
Anuncio

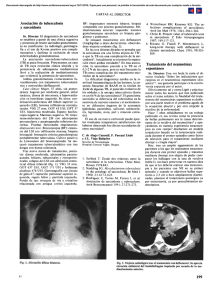
Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Radiología. 2011;53(6):560---563 www.elsevier.es/rx COMUNICACIÓN BREVE Micosis pulmonar por Paracoccidioides brasiliensis: confusión peligrosa con sarcoidosis M. Pujol-Riqué a,∗ , S. Ruiz a , C. Alonso-Tarrés b y C. Cañete c a Servicio de Diagnóstico por la Imagen, Hospital General de l’Hospitalet, L’Hospitalet de Llobregat, Barcelona, España Microbiología, Consorci de Laboratoris Intercomarcal, Hospital General de l’Hospitalet, L’Hospitalet de Llobregat, Barcelona, España c Servicio de Neumología, Hospital General de l’Hospitalet, L’Hospitalet de Llobregat, Barcelona, España b Recibido el 31 de marzo de 2010; aceptado el 8 de julio de 2010 Disponible en Internet el 6 de mayo de 2011 PALABRAS CLAVE Paracoccidioidomicosis; Paracoccidiodes brasiliensis; Micosis sistémica; Infección fúngica pulmonar KEYWORDS Paracoccidioidomycosis; Paracoccidiodes brasiliensis; Systemic mycosis; Fungal lung infection Resumen Se presenta el caso de un paciente de origen sudamericano con una enfermedad pulmonar diagnosticada inicialmente de sarcoidosis y tratado con corticoides. A pesar de una mejora inicial, el paciente fue empeorando hasta que por fin el cuadro se atribuyó a una paracoccidioidomicosis. Esta micosis sistémica tiene rasgos comunes con la sarcoidosis, pero el tratamiento difiere hasta el punto de que los corticoides pueden poner en peligro la vida del paciente. © 2010 SERAM. Publicado por Elsevier España, S.L. Todos los derechos reservados. Pulmonary mycosis caused by Paracoccidioides brasiliensis: dangerous confusion with sarcoidosis Abstract We present the case of a patient from South America with a lung disease that was initially diagnosed as sarcoidosis and treated with corticoids. Despite an initial improvement, the patient worsened gradually until his condition was finally attributed to paracoccidioidomycosis. This systemic mycosis has features in common with sarcoidosis, but the treatment differs drastically because corticoids can place the patient’s life at risk. © 2010 SERAM. Published by Elsevier España, S.L. All rights reserved. Introducción ∗ Autor para correspondencia. Correo electrónico: [email protected] (M. Pujol-Riqué). La paracoccidioidomicosis es la micosis sistémica más frecuente en Latinoamérica y está causada por Paracoccidioides brasiliensis. Se adquiere por vía inhalatoria y el hongo alcanza los pulmones, donde desarrolla la infección primaria y puede diseminarse a otros órganos1 . Esta 0033-8338/$ – see front matter © 2010 SERAM. Publicado por Elsevier España, S.L. Todos los derechos reservados. doi:10.1016/j.rx.2010.07.014 Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Micosis pulmonar por Paracoccidioides brasiliensis: confusión peligrosa con sarcoidosis Figura 1 En la radiografía de tórax se observó una enfermedad pulmonar difusa con abundantes nódulos mal delimitados y un discreto predominio en campos medios. infección suele ser subclínica o poco sintomática, pero en algunos casos progresa hacia lesiones graves y en pacientes inmunodeprimidos puede ser mortal. Descripción del caso Paciente de 48 años de origen ecuatoriano residente en España en los últimos seis años, sin haber visitado su país desde entonces. Entre sus antecedentes destacaban el tabaquismo y que trabajó en una zona selvática del Brasil. Consultó por tos de dos meses de evolución, con expectoración hemoptoica y sudoración nocturna en los últimos días. El paciente estaba afebril y el hemograma no mostró alteraciones. Tenía placas induradas y sobreelevadas en el tronco de meses de evolución. En la radiografía de tórax se observaron abundantes nódulos mal delimitados que afectaban a ambos pulmones de manera simétrica, con predominio en los campos medios (fig. 1). También existía un índice cardiotorácico discretamente aumentado. En la tomografía computarizada (TC) se comprobó que los nódulos tenían una distribución difusa, ocupando también zonas peribroncovasculares y subpleurales (fig. 2A). Estos nódulos eran de tamaños dispares, siendo los mayores algo superio- 561 res al centímetro. Muchos de ellos estaban mal delimitados, con áreas en vidrio esmerilado adyacentes. También existían opacidades lineales y engrosamientos cisurales y de las paredes bronquiales, así como alteración de la arquitectura del parénquima pulmonar. Se identificaban adenopatías mediastínicas e hiliares bilaterales (fig. 2B). El cuadro se atribuyó a una sarcoidosis grave estadio II al detectar en una biopsia transbronquial y cutánea granulomas epitelioides no necrosantes y estar elevada la enzima conversora de la angiotensina (54 u/L). Se empezó tratamiento con prednisona por vía oral (40 mg/día). Otras pruebas resultaron negativas (PPD, tinción y cultivo de bacterias/micobacterias/hongos habituales de esputo, aspirado y lavado broncoalveolar, marcadores tumorales, HIV, ANCA, ANA). Los cultivos micológicos se descartaron a los 30 días de incubación. Tras una mejora inicial, a las seis semanas el paciente empeoró clínicamente, presentando tos, disnea, fiebre y leucocitosis con neutrofilia (14.820/l). En la gasometría se constató una insuficiencia respiratoria. En una nueva TC se identificó la progresión de la enfermedad. Los nódulos habían crecido hasta formar en algunas zonas agrupaciones con aspecto de consolidación y estaban claramente cavitados en muchos casos (fig. 2C). Al revisar la TC previa, se observaron pequeñas cavitaciones en algunos nódulos que habían pasado desapercibidas. En vista del empeoramiento y teniendo en consideración la procedencia del paciente, se remitieron nuevas muestras respiratorias para estudio microbiológico, observándose abundantes levaduras de diversos tamaños con gemaciones múltiples compatibles con Paracoccidiodes brasiliensis en dos muestras de esputo (fig. 3). El paciente tuvo una buena evolución clínica después de empezar el tratamiento con anfotericina B liposomal intravenosa (4 mg/kg/día) y de suspender los corticoides. Fue dado de alta del hospital a las dos semanas con tratamiento con itraconazol por vía oral (100 mg/día) hasta completar seis meses. Los cultivos de las muestras respiratorias (esputos, aspirado y lavado broncoalveolar) fueron positivos para el hongo tras seis a ocho semanas de incubación y se negativizaron al mes del tratamiento antifúngico. Una resonancia magnética (RM) reveló una displasia arritmogénica del ventrículo derecho sin aparente relación con la infección y causante de la cardiomegalia. Al año de seguimiento el paciente está asintomático y con una función pulmonar casi normal (FEV1 78% del teórico), aunque en Figura 2 A) TCMD inicial, ventana pulmonar. Nódulos pulmonares (puntas de flecha) y opacidades lineales (flechas cortas). Se identifican engrosamientos cisurales (flecha larga). B) TCMD inicial, ventana mediastínica. Adenopatías en región paratraqueal dcha y ventana aortopulmonar (*). C) TCMD después del tratamiento con corticoides. Muchos nódulos han crecido y algunos han cavitado (puntas de flecha). Hay conglomerados nodulares con aspecto de consolidación (flecha). Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. 562 Figura 3 Fotomicrografía de esputo (tinción de Gram 1.000x y examen en fresco con KOH 400x en el recuadro), donde se observa una gran cantidad de levaduras de distintos tamaños (flechas) y gemación multipolar formando la imagen característica de timón de barco (*). la radiografía torácica persisten muchas lesiones, poniendo de manifiesto que existía un gran componente de fibrosis pulmonar en el momento del diagnóstico. Discusión La paracoccidioidomicosis es una infección propia de países latinoamericanos, que se extiende desde el sur de México hasta Argentina y Uruguay. Se han descrito pocos casos en las islas del Caribe y según parece ninguno en Chile1 . Las zonas endémicas tienen temperaturas suaves y abundantes bosques con inviernos cortos y veranos lluviosos. Su prevalencia es muy variable y desconocida en muchas zonas, superando el 50% en campesinos de áreas rurales de Brasil2 . Se ha establecido una clasificación de los estadios clínicos en infección, enfermedad aguda/subaguda, enfermedad crónica y enfermedad residual. La forma aguda es propia de pacientes jóvenes de ambos sexos y afecta típicamente al sistema reticuloendotelial (ganglios linfáticos, hígado, bazo), mientras que la forma crónica suele darse en varones adultos y provoca predominantemente lesiones pulmonares y mucocutáneas, como ocurrió con el paciente presentado. Actualmente se considera que la paracoccidioidomicosis es una enfermedad multiorgánica donde predominan las lesiones pulmonares, que son la causa más importante de morbimortalidad. La diseminación ocurre tanto por vía linfática como hematógena y se han descrito también alteraciones en huesos, sistema nervioso central, riñones y característicamente glándulas suprarrenales, pudiendo existir síndrome de Addison3 . La forma crónica es la más frecuente, siendo un motivo de consulta común las úlceras de mucosa oral de larga evolución, y con menos frecuencia lesiones cutáneas y manifestaciones respiratorias1 . En nuestro país se han descrito muy pocos casos de enfermedad importada, habiéndose producido confusiones con la sarcoidosis en las formas pulmonares4 . Uno de los pacientes murió tras la administración de glucocorticoides5 . Esta M. Pujol-Riqué et al confusión también ocurre en los países endémicos, siendo la sarcoidosis una entidad que forma parte del diagnóstico diferencial2 . En los casos leves y moderados se recomienda tratar la enfermedad con itraconazol o ketoconazol, mientras que la anfotericina B se reserva para los casos graves6 . Los individuos infectados pueden identificarse mediante pruebas serológicas o cutáneas (intradermorreacción), aunque son poco accesibles en países no endémicos. A menudo el diagnóstico se hace mediante el examen microscópico de fluidos biológicos o de una biopsia tisular2 , donde se identifican levaduras de pared gruesa con gemación múltiple formando la característica imagen de «timón de barco». Si no se sospecha esta posibilidad y se omite el examen microscópico adecuado (examen en fresco, preferiblemente con microscopio de contraste de fases, y tinciones argénticas o PAS), el hongo puede pasar desapercibido. El cultivo de las muestras también es diagnóstico, pero se necesita más de un mes de incubación. Se obtienen colonias de levaduras a 37 ◦ C y de hongos filamentosos a temperatura ambiente (dimorfismo térmico) en medios de cultivo habituales como el agar sangre y el agar glucosado de Sabouraud, respectivamente1 . Recientemente se ha descrito una técnica diagnóstica por reacción en cadena de la polimerasa en muestras de secreciones respiratorias, tejidos afectados y sangre, que permitiría un diagnóstico rápido con una alta sensibilidad7 . La gammagrafía con Ga67 ha sido empleada para monitorizar la actividad de la infección durante el tratamiento6 . Los hallazgos tomográficos en la paracoccidioidomicosis pulmonar sintomática son muy variados8 . En pacientes sin tratamiento específico, son frecuentes las opacidades en vidrio deslustrado y los nódulos, mientras que en pacientes tratados predominan los engrosamientos septales, además de ser también prevalentes el enfisema cicatricial y los engrosamientos murales bronquiales, probablemente representando un estadio más avanzado de la enfermedad. El tamaño de los nódulos varía desde pequeños nodulillos centrilobulillares hasta nódulos de varios centímetros, pudiendo cavitar, estar rodeados por un halo hipodenso o tener una densidad central en vidrio deslustrado y periférica más densa (halo inverso). Todos estos tipos de nódulos pueden coincidir en un mismo paciente y en un mismo momento de la infección. Las adenopatías, incluyendo las intratorácicas, también aparecen en las formas crónicas, aunque su frecuencia es menor que en las presentaciones agudas juveniles. En el caso descrito estaban presentes en el mediastino y ambos hilios, lo que en parte propició la confusión diagnóstica con la sarcoidosis. En este paciente también destaca la presencia de importantes lesiones pulmonares residuales, comunes en infecciones activas de larga evolución a pesar del tratamiento antifúngico, especialmente cuando existe una participación parenquimatosa extensa9 . Según algunos autores, las lesiones mucosas son propias de estadios iniciales, mientras que las cutáneas, como las presentes en este paciente, indican un estadio avanzado y un peor pronóstico1 . Las escasas manifestaciones clínicas de la forma pulmonar impiden a menudo un diagnóstico temprano. Los nódulos pulmonares también se observan en infecciones por otros hongos dimórficos o en la tuberculosis. La asociación entre paracoccidioidomicosis y tuberculosis no es infrecuente, lo que a veces dificulta el diagnóstico2 . Documento descargado de http://www.elsevier.es el 20/11/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato. Micosis pulmonar por Paracoccidioides brasiliensis: confusión peligrosa con sarcoidosis Existen otras entidades no infecciosas que se manifiestan igualmente con nódulos pulmonares múltiples entre las que se encuentra la sarcoidosis. En concreto, existe un tipo de sarcoidosis nodular grande que se ajustaría a las lesiones del paciente presentado, pero es poco frecuente, y todavía menos la cavitación10 . En la sarcoidosis pulmonar suele identificarse un patrón reticulonodular con nódulos inferiores a 5 mm, bilateral y simétrico, afectando característicamente a las zonas de drenaje linfático de campos pulmonares medios. En sujetos provenientes del continente americano, donde hay zonas endémicas para hongos patógenos sistémicos, ante la presencia de lesiones pulmonares, especialmente si son nodulares, hay que pensar en ellos para realizar un diagnóstico correcto y sobre todo no hay que confundir el cuadro con una sarcoidosis. Diagnósticos de infecciones infrecuentes en nuestro medio pueden ser cada vez más habituales por la llegada de numerosos inmigrantes. Autorías Todos los autores han leído y aprueban la versión final del artículo. 1. Responsable de la integridad del estudio: MPR. 2. Concepción del estudio: no se trata de un trabajo de investigación. 3. Diseño del estudio: no se trata de un trabajo de investigación. 4. Obtención de los datos: MPR, SR, CAT, CC. 5. Análisis e interpretación de los datos: no se trata de un trabajo de investigación. 6. Tratamiento estadístico: no se trata de un trabajo de investigación. 7. Búsqueda bibliográfica: MPR, SR, CAT. 8. Redacción del trabajo: MPR. 9. Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: SR, CAT, CC. 10. Aprobación de la versión final: MPR, SR, CAT, CC. 563 Conflicto de intereses Los autores declaran no tener ningún conflicto de intereses. Bibliografía 1. Restrepo A, Tobón AM, Agudelo CA, Ochoa JE, Rosero DS, Osorio ML, et al. Co-existence of integumentary lesions and lung X-ray abnormalities in patients with paracoccidiodomycosis (PCM). Am J Trop Med Hyg. 2008;79:159---63. 2. Blotta MH, Mamoni RL, Oliveira SJ, Nouer AS, Papaiordanou PM, Goveia A, et al. Endemic regions of paracoccidioidomycosis in Brazil: a clinical and epidemiological study of 584 cases in the Southeast region. Am J Trop Med Hyg. 1999;61:390---4. 3. Leal AM, Bellucci AD, Mugglia VF, Lucchesi FR. Unique adrenal gland imaging features in Addison’s disease caused paracoccidioidomycosis. AJR Am J Roentgenol. 2003;181:1433---4. 4. Botas-Velasco M, Jover-Díaz F, Ortiz de la Tabla-Duccase V, Martínez-García C. Paracoccidioidomicosis importada en España. Enferm Infecc Microbiol Clin. 2010;28:259---60. 5. López J, Blanco JJ, Santos C, Calvo M. Infección por Paracoccidioides brasiliensis en un inmigrante venezolano. Med Clin (Barc). 2005;125:139. 6. Ramírez-Olivencia G, Ramírez-Rubio O, Rivas P, Herrero MD, Puente S. Paracoccidioidomycosis in a spanish missionary. J Travel Med. 2010;17:139---40. 7. Buitrago MJ, Merino P, Puente S, Gómez-López A, Arribi A, Zancope-Oliveira RM, et al. Utility of real-time PCR for the detection of Paracoccidioides brasiliensis DNA in the diagnosis of imported paracoccidioidomycosis. Med Mycol. 2009;47:879---82. 8. Souza Jr AS, Gasparetto EL, Davaus T, Escuissato DL, Marchiori E. High resolution CT findings of 77 patients with untreated pulmonary paracoccidioidomycosis. AJR Am J Roentgenol. 2006;187:1248---52. 9. Tobón AM, Agudelo CA, Osorio ML, Álvarez DL, Arango M, Cano LE, et al. Residual pulmonary abnormalities in adult patients with chronic paracoccidioidomycosis: prolonged follow-up after itraconazole therapy. Clin Infect Dis. 2003;37:898---904. 10. Miller BH, Rosado-de-Christenson ML, McAdams HP, Fishback NF. Thoracic sarcoidosis: radiologic-pathologic correlation. Radiographics. 1995;15:421---37.