Técnica de Melles
Anuncio

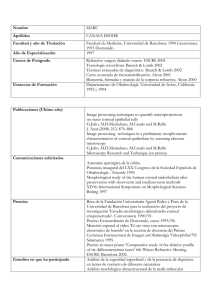
Capítulo 8 Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles — Maniobras y Signos para visualizar la Profundidad de la Incisión — Técnica Quirúrgica de Melles para la DALK • Viscodisección — Complicaciones — Resultados — Experiencia Personal — Bibliografía Capítulo 8 Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles Alberto Villarrubia, Juan José Pérez Santonja, Antonio Hidalgo, Elisa Palacín Los trabajos publicados por Gerrit Melles desde 1999 han supuesto una cierta popularización del procedimiento de DALK. La originalidad de su técnica consiste en la descripción de una serie de maniobras para visualizar la profundidad de la disección lamelar durante la cirugía (1) basándose en un abordaje posterior (a diferencia de todas las técnicas descritas hasta ahora que usan un abordaje anterior para alcanzar el plano predescemético); para ello, emplea una serie de signos que se producen después de llenar la cámara anterior (CA) con aire: en condiciones normales es difícil distinguir la superficie posterior de la córnea durante el acto quirúrgico debido a que el índice de refracción es similar en la córnea y en el humor acuoso (HA); sin embargo, al intercambiar aire por HA en la CA, se crea una interfase óptica en la superficie posterior de la córnea que nos permite conocer a qué profundidad nos encontramos. Comentaremos en primer lugar cuáles son los signos y maniobras que nos permitirán conocer la profundidad de la disección; a continuación, describiremos la técnica quirúrgica de Melles para la DALK con aportaciones de nuestra experiencia personal; posteriormente hablaremos de las complicaciones tanto intra como postoperatorias para pasar a analizar los resultados publicados y nuestra modesta experiencia personal. caso de 30 gauge) a través de una paracentesis. La burbuja de aire en la CA actúa como un espejo convexo por lo que, si nos acercamos a la cara anterior de la córnea con un cuchillete, veremos dos imágenes especulares del mismo (fig. 1): una es la imagen reflejada desde la superficie corneal anterior y la otra desde la superficie corneal posterior: de este modo, podemos hacernos una idea del espesor corneal el cual es la mitad de la distancia entre la punta del cuchillete y la imagen reflejada desde la superficie posterior corneal («mirror effect» o «signo del espejo»). Cuando comenzamos a introducir el cuchillete en el espesor del estroma corneal, podemos observar un reflejo de luz especular y semicircular cerca de la punta del cuchillete: este reflejo se produce debido a la indentación de tejido durante la realización de la incisión («indentation effect» o «signo de la indenta- Maniobras y Signos para visualizar la Profundidad de la Incisión Para conseguir con éxito la profundidad adecuada donde comenzar la disección, la primera maniobra que realizamos es un intercambio de HA por aire con una cánula roma (en nuestro Fig. 1: «Mirror effect» o «signo del espejo»: el espesor corneal puede estimarse calculando el punto medio entre la punta real del cuchillete sobre la cara anterior de la córnea (1) y su imagen especular desde la cara posterior (2). 112 8. Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles Fig. 2: «Indentation effect» o «signo de la indentación»: la banda oscura existente entre la punta del cuchillete y el reflejo especular de luz va haciéndose cada vez menor a medida que penetramos en la profundidad del estroma corneal (A,B,C). En la última imagen (D), se puede ver el signo del pliegue, señal de que hemos alcanzado la MD. ción»). El espacio que existe entre la punta del cuchillete y el reflejo de luz es el tejido de córnea aún no penetrado por el cuchillete: este espacio puede ser objetivado por el cirujano como una banda oscura que se encuentra justo alrededor de la punta del cuchillete. El grosor de esta banda oscura disminuye a medida que vamos avanzando con el cuchillete en las capas más profundas del estroma (fig. 2). Cuando el cuchillete se aproxima a la superficie posterior (fig. 3), pueden apreciarse unos pequeños pliegues en la zona más profunda del tejido corneal («folding effect» o «signo de los pliegues»). A medida que el cuchillete está más profundo, aumenta el número, anchura y movi- lidad de los pliegues: estos signos se pueden usar como indicadores de la cercanía de la punta del cuchillete a la superficie corneal posterior, o sea, a la membrana de Descemet (MD). Técnica Quirúrgica de Melles para la DALK Nosotros realizamos este técnica desde un abordaje temporal o temporal-superior (de igual forma que se hace en una facoemulsificación estándar) ya que es importante sentirse cómodo a la hora de manejar todos los instrumentos. Pensamos que un abordaje superior como describe 8. Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles 113 Fig. 3: «Folding effect» o «signo de los pliegues»: a medida que el cuchillete se aproxima a la MD, se pueden apreciar pequeños pliegues en el tejido corneal posterior alrededor de la punta del cuchillete. Melles en su artículo original (2) dificulta la comodidad para maniobrar con las diferentes espátulas. La cirugía se inicia abriendo la conjuntiva en el sitio elegido y realizando una incisión escleral de unos 5 mm de longitud y unas 250 micras de profundidad a 1 mm del limbo; es interesante cauterizar todos los vasos de la zona para evitar la entrada de sangre en la interfase durante las maniobras de disección ya que esto puede dificultar la visualización. Bien con un cuchillete calibrado de 3,2 mm similares a los que se usan para crear la incisión en la cirugía de facoemulsificación o bien con un cuchillete tipo Crescent, se diseca un túnel escleral hasta que entramos mínimamente en estroma corneal. A continua- ción, se realiza una paracentesis con un cuchillete de acero de 15° a unos 3 sectores horarios en sentido de las agujas del reloj: en nuestra experiencia, esta paracentesis debe tener el tamaño justo para permitir la entrada de una cánula de 30 gauge ya que, si es mayor, el aire tenderá a escapar de la CA. A través de la paracentesis y con una cánula de 30 gauge, aspiramos HA de la CA para que nos permita introducir una burbuja de aire con la misma cánula; el aire es inyectado hasta que toda la CA está completamente llena y el ojo tiene una presión firme. Nosotros solemos hidratar la paracentesis una vez conseguida la burbuja de aire con el objetivo de que éste no escape de la CA con las maniobras de disección. 114 8. Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles A través del tunel escleral que previamente hemos realizado, se introduce la primera de las espátulas diseñadas por Melles (2110, DORC Internacional b.v., Zuidland, Holanda) la cual es, realmente, un cuchillete romo (fig. 4-B). Este instrumento se debe ir acercando hacia la MD hasta que conseguimos visualizar los pliegues de la misma. Para ello, debemos ir observando los tres signos descritos en el epígrafe anterior (figs. 1, 2 y 3). Consideramos este paso el más importante de toda la cirugía ya que es en este momento donde debemos alcanzar el plano predescemético. Una vez conseguida la profundidad de disección deseada, cambiamos a la segunda espátula de Melles (fig. 4-C): con ella comenzamos la disección de la MD realizando movimientos laterales que, en un primer momento, serán de amplitud muy limitada hasta que vayamos creando un espacio suficiente que nos permita realizar movimientos más amplios con los que llegaremos al limbo a ambos lados de la incisión. Es difícil establecer normas sobre cómo realizar la disección: los movimientos deben ser suaves, intentando visualizar siempre los pliegues que se producen en la MD y sin inclinar la espátula hacia abajo; con experiencia se puede conseguir cierta soltura en estas maniobras si bien nunca deben realizarse de forma brusca para evitar una perforación. Si esta se produjera (contingencia muy posible al operar un queratocono), se podrá objetivar inequívocamente ya que el aire pasa de la CA al plano de disección: si después de la perforación la CA permanece formada y considera- Fig. 4: Juego de espátulas diseñado por Gerrit Melles para la disección de la MD (2110, DORC Internacional b.v., Zuidland, Holanda). mos que el ojal permitirá una buena aposición de la córnea donante, podremos continuar la disección; de lo contrario, es preferible reconvertir a una queratoplastia penetrante (QPP). Con esta segunda espátula conseguiremos disecar unos 180° de tejido corneal. A partir de aquí, usaremos la tercera de las espátulas de Melles (fig. 4-D) para terminar la disección de toda la córnea hasta el limbo en sus 360°. Con las maniobras descritas lo que hemos conseguido es crear un espacio virtual completo entre el estroma profundo y la MD y, a continuación, se debe extraer aire de la CA a través de la paracentesis para bajar la presión intraocular (PIO) y poder realizar con comodidad el siguiente paso. A través del bolsillo escleral creado inicialmente, introducimos viscoelástico de forma suave y controlada: iremos viendo como la MD se separa del estroma profundo y se crea una especie de «pseudocámara anterior» (fig. 5). A nosotros nos parece una buena maniobra dar un punto de nylon en la incisión antes de comenzar la inyección de viscoelástico ya que de esta manera se evita que éste escape a través del túnel escleral. Finalizada la «formación» de esta «segunda cámara anterior», podemos pasar a la trepanación. Habitualmente existe viscoelástico sobre la superficie ocular debido al escape que ocurre a través de la incisión; por ello, consideramos importante limpiarlo con una hemosteta de merocel para poder obtener una correcta succión. Colocamos el trépano (en nuestro caso, de Hessburg-Barron) centrado sobre la superficie anterior corneal y aplicamos la succión. Una vez asegurada la succión procedemos a la trepanación hasta que aparece viscoelástico: en este momento hemos alcanzado el bolsillo estromal disecado. Liberamos la succión y retiramos el trépano. Con tijeras corneales (las que habitualmente use cada uno en una QPP), se procede a completar la disección del disco corneal anterior intentando que las hojas de las tijeras se mantengan perpendiculares a la superficie corneal (de la misma forma que en una QPP) pero con especial cuidado de no perforar la MD en este momento: para ello es útil ayudarse con más viscoelástico inyectado entre la MD y el estroma profundo disecado. 8. Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles 115 Fig. 5: «Pseudocámara Anterior» creada por inyección de viscoelástico en el espacio virtual existente entre el estroma profundo y la MD. Cuando se ha retirado el botón corneal del receptor, se lava completamente el viscoelástico que queda sobre la MD y se pasa al manejo y sutura del botón donante: estas maniobras no difieren en nada de lo ya expuesto en el capítulo anterior y remitimos al lector a dicho epígrafe. En la figura 6 se resume en 9 imágenes los pasos realizados con esta técnica. Fig. 6: Técnica de Melles para DALK resumida en 9 pasos. (A) Inyección de aire en CA. (B) Buscando el plano predescemético con la 1.ª espátula de Melles. (C) Disección de 180 grados con la 2.ª espátula de Melles. (D) Disección de los 360 grados con la 3ª espátula de Melles. (E) Inyección de viscoelástico en el espacio virtual creado entre el estroma profundo y la MD para crear una seudocámara anterior. (F) Trepanación hasta que escape viscoelástico. (G) El botón receptor es retirado con tijeras teniendo cuidado de no lesionar la MD. (H) Sutura del botón donante al que previamente se ha retirado la MD. (I) Aspecto final. 116 8. Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles Viscodisección Usando los mismos principios descritos anteriormente para alcanzar el plano predescemético, Melles describió en 2000 su técnica de Viscodisección (3). La diferencia con la técnica de disección manual es que, en el caso de la Viscodisección se entra directamente con una aguja de 30 gauge unida a una jeringa llena de viscoelástico. Una vez alcanzado el plano predescemético (usando los tres signos ya conocidos: espejo-indentación-pliegues) se inyecta directamente viscoelástico para separar la MD del estroma suprayacente. A partir de aquí, la trepanación y sutura del botón donante no difieren en nada de lo ya descrito. Como ya se comentó en el capítulo anterior, en el artículo en el que Melles describe esta técnica (3) se produjo un 20% de perforación (5 ojos de 25) en ojos de banco. De los tres pacientes en los que la realizó in vivo, en uno se produjo una microperforación que condujo a una pseudocámara anterior y en otro la perforación fue considerada de suficiente tamaño como para reconvertir a QPP. Estos resultados han influido, probablemente, en que esta técnica no se haya abierto camino. Complicaciones La complicación más frecuente que puede ocurrir durante la cirugía es que, durante las maniobras de disección, se produzca una perforación (muy frecuente al operar un queratocono): como ya hemos comentado, cuando ocurre, el aire pasa de la CA al plano de disección; si después de la perforación la CA permanece formada y consideramos que el ojal permitirá una buena aposición de la córnea donante, podremos continuar la disección; de lo contrario, es preferible reconvertir a una queratoplastia penetrante (QPP). Para el manejo de las complicaciones postoperatorias (proliferación epitelial en la entrecara, rechazo estromal y epitelial, «pseudocámara anterior»), nos remitimos en todo a lo descrito en el capítulo 7. Se ha descrito una complicación directamente relacionada con esta técnica (4,5): el uso de aire intracamerular puede resultar en una midriasis media paralítica posiblemente producida por isquemia iridiana (síndrome de UrretsZavalia). Para intentar evitar esta contingencia, consideramos importante que el tiempo de disección, que es durante el cual el aire está a tensión en la CA, sea minimizado al máximo; por otra parte, es deseable dejar la mínima cantidad de aire posible en el postoperatorio en la CA así como intentar evitar su inyección en CA si se produce una «pseudocámara anterior». Resultados Melles (2) comunicó un 12% (3 ojos) de microperforación en 25 ojos de banco en los que realizó su técnica de disección lamelar profunda; en todos consiguió terminar la disección de la MD. En el mismo trabajo, publica 7 casos realizados in vivo: en 1 de ellos reconvierte a QPP y en otro se produce una microperforación que no precisa reconversión a QPP. Caporossi (6) ha comunicado un 10% de perforación con la técnica de Melles. En su trabajo original (2), Melles comunicó una MAVCC media de 0,7±0,3 (rango: 0,251,0) con un cilindro final que varió entre 1 y 3,5 dioptrías. La paquimetría central osciló entre 620 y 730 micras sin evidencia de edema epitelial o estromal. El seguimiento medio fue de 4,8±2,8 meses. Este mismo autor tiene reflejados sus últimos resultados en su página web (www.niioc.nl/edalkcrs/edalk.htm): en una serie de 68 ojos con un seguimiento de 12 meses, la MAVCC media fue de 0,8±0,1, el astigmatismo de 2,6±1,6 dioptrías, la paquimetría final de 660±50 micras y la densidad celular endotelial media de 2.240±475 células/mm2; en esta serie, la tasa de perforación fue de un 10% (7/68). Caporossi (6) ha comunicado sus resultados con esta técnica en 9 ojos con queratocono. El 78% de los ojos consiguió una agudeza visual corregida de 0,66 o mejor, la paquimetría postoperatoria media fue de 605±46 micras y la densidad celular endotelial media postoperatoria de 2.273±229 células/mm2. 8. Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles Los resultados respecto al endotelio corneal han sido favorables con esta técnica. Van Dooren (7) ha encontrado una pérdida de células endoteliales del 11% a los 6 meses, 13% a los 12 meses y 14,2% a los 24 meses de la cirugía. La pérdida endotelial entre los 12 y 24 meses fue sólo del 1,2%. Los autores concluyen que con esta técnica quirúrgica se produce una caída inicial de la densidad celular endotelial seguida de una pérdida celular fisiológica. Experiencia Personal En la tabla 1 se refleja la modesta experiencia personal con esta técnica de uno de los autores (AVC) en sus primeros 15 casos. Nos gustaría hacer los siguientes comentarios. De los 15 ojos en los que hemos intentado una DALK, en 3 de ellos (20%) no se ha conseguido debido a perforación intraoperatoria: pero hay que hacer notar que no fue en los primeros casos sino en 2 casos con queratocono (en los que existe la posibilidad de que hubiera roturas en la MD que pasaron inadvertidas en el estudio preoperatorio) y en un caso en el que la perforación estaba prácticamente asegurada ya que se trataba de un paciente con 2 descemetoceles. Aunque el queratocono supone una excelente indicación para la DALK, hay que resaltar que, cuando hay roturas en la MD, por ejemplo, cuando ha habido un hydrops previo, esta técnica debe contraindicarse pues la MD ya está rota antes de empezar la cirugía y es seguro que encontraremos una perforación. Para ilustrar los resultados de la DALK en el queratocono, haremos de nuevo referencia al trabajo de Watson y colaboradores (8): operaron 51 ojos con queratocono: en 26 utilizaron una técnica de DALK (hidrodelaminación de Sugita en 19 ojos y técnica de Melles en 7) y en 25 una QPP; la media de mejor agudeza visual corregida (MAVCC) en la QPP es mejor que en la DALK pero estas diferencias no son significativas; los resultados refractivos y la incidencia de complicaciones son similares en ambas técnicas; los autores concluyen finalmente que, en el tratamiento del queratocono, la QPP no debe ser la indicación inicial por defecto si no que la QPL (en este 117 caso, lamelar anterior profunda) puede ser una alternativa igualmente segura. En 3 casos más se ha producido una perforación intraoperatoria pero el resultado final ha sido exitoso: en 2 de ellos existió una seudocámara anterior resolviéndose una de ellas nada menos que al mes y medio de la intervención. Hay 4 ojos en los que existe una evidente limitación visual pero en ninguno de estos casos dicha contingencia está relacionada con la técnica; queremos decir con esto que la misma limitación se hubiera producido si se hubiera realizado una QPP: en el caso 4 la causa es un astigmatismo irregular por descentramiento; en el paciente número 6 existe una isquemia macular debido a una retinopatía diabética; el caso número 9 está pendiente de ser operado de catarata; por último, en el paciente número 10 existe un leucoma central después de un defecto epitelial persistente: en este paciente se está produciendo una vascularización de la entrecara (fig. 7). En 3 ojos existe una mejoría evidente después de que los propios pacientes manifestaran ser ojos amblíopes (en uno de ellos, debido al corto período de seguimiento, aún puede existir ganancia de MAVCC). Es importante destacar que el diagnóstico causal era herpético en 6 casos y, en 4 de ellos, existía vascularización profunda con adelgazamiento corneal y brotes de queratouveítis herpética (figs. 8 a 11: casos 2, 3, 5 y 12): estos casos presentan un alto riesgo de rechazo después de una QPP y en ninguno de Fig. 7: Vascularización que se está iniciando en la entrecara del paciente número 10 que presenta, además, un leucoma central debido a un defecto epitelial persistente. 118 8. Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles Tabla 1. Resumen de los 15 casos con más de un mes de evolución operados por el mismo autor (AVC) Nº Sexo Edad Ojo 1 Mujer Diagnóstico Fáquico Pseudofáquico MAVCC Evolución Preop (meses) MAVCC Postop Cil. Rx. Postop Cil. Topo Postop Incidencias Observaciones 69 OD Leucoma Postherpético sin Vacularización Pseudofáquico 0,1 36 0,65 4 3,75 (1) 2 Hombre 43 OI Leucoma Postherpético con Vacularización Profunda y Adelgazamiento Corneal Fáquico CD a 1 metro 30 1,0 1,75 3,25 (2) 3 Hombre 40 OD Leucoma Postherpético con Vacularización Profunda y Adelgazamiento Corneal Pseudofáquico 0,05 26 0,8 5 6,50 (3) 4 Hombre 33 OI Fáquico CD a 1 metro 12 0,1 No valorable 12 (4) Astigmatismo Irregular 5 OD Leucoma Postherpético con Vacularización Profunda y Adelgazamiento Corneal Fáquico 0,05 12 0,6 2,5 3,75 (5) Mujer 35 Leucoma Central Postcausticación Insuficiencia Límbica Parcial 6 Hombre 54 OD Leucoma después de Vitrectomía Posterior en un paciente Diabético Pseudofáquico 0,05 12 0,15 5 6,75 (6) 7 Hombre 22 OD Queratocono Fáquico 0,3 12 1,0 4 5 Perforación Intraoperatoria. Reconversión a QPP 8 Hombre 22 OI Leucoma Corneal después de Queratitis Infecciosa Postraumática en un paciente operado con LASIK Fáquico 0,15 9 0,7 2 2,75 9 Hombre 74 OD Leucoma Postherpético sin Vacularización Fáquico 0,05 9 0,15 No valorable 4,5 (9) 10 Hombre 50 OI Leucoma Corneal después de Queratitis Infecciosa Postraumática Fáquico 0,1 7 0,2 No valorable 5,50 Astigmatismo Irregular (10) 11 Hombre 28 OI Queratocono Fáquico 0,2 5 0,8 3 3,5 Perforación Intraoperatoria. Reconversión a QPP 12 Mujer 56 OD Leucoma Postherpético Vascularizado Fáquico CD a 1 metro 3 0,3 8 8 (12) 13 Hombre 21 OD Queratocono Fáquico 0,05 2 0,2 4,5 4,6 (13) 14 Hombre 35 OI Descemetoceles en Leucoma Postherpético con Vacularización Profunda Fáquico MM 2 0,4 6 8,75 QPP a los 7 días debido a perforación intraoperatoria y seudocámara anterior 15 Hombre 32 OD Ectasia Corneal Post-LASIK Fáquico 0,2 1,5 0,4 3 3 (15) MAVCC: Mejor Agudeza Visual con Corrección; Cil. Rx.: Astigmatismo Refractivo (dioptrías); Cil. Topo: Astigmatismo Topográfico (dioptrías); QPP: Queratoplastia Penetrante; MM: Movimiento de Manos; CD: Contar Dedos; SC: Sin Corrección. (1): microperforación con formación de seudocámara anterior y resolución a los 7 días tras inyección de SF6. Ambliopía: la MAVCC referida por la paciente era de 0,1; (2): brotes de queratouveítis herpética durante 15 años. Se produjo una queratitis estromal necrotizante a los 3 meses de la cirugía que requirió nuevo implante corneal; (3): microperforación sin formación de seudocámara anterior. Brotes de queratouveítis herpética durante 3 años. Extirpación de pterigium con implante de injerto limboconjuntival del ojo adelfo a los 15 meses de la cirugía. En tratamiento tópico por glaucoma, probablemente inducido por tratamiento prolongado con corticoides preoperatoriamente; (4): precisó implante de membrana amniótica en el mismo acto quirúrgico debido a insuficiencia límbica parcial. La limitación visual se debe a un astigmatismo irregular debido a descentramiento del injerto. Está pendiente de nueva queratoplastia; (5): brotes de queratouveítis herpética durante 4 años. Ambliopía: la MAVCC referida por la paciente era de 0,2; (6): la limitación visual se debe a isquemia macular debida a retinopatía diabética; (9): microperforación con formación de seudocámara anterior y resolución espontánea al mes y medio tras la intervención. La limitación visual se debe a una catarata que está pendiente de ser intervenida; (10): presenta una severa alteración de la superficie ocular por blefaritis. Precisó implante de membrana amniótica a los 2 meses de la cirugía debido a defecto epitelial persistente. La limitación visual se debe al leucoma residual central. Está pendiente de nueva queratoplastia; (12): brotes de queratouveítis herpética durante 2 años. Ambliopía: la MAVCC referida por la paciente era de 0,1. El astigmatismo es alto debido a que no ha sido retirada la sutura por lo que aún puede ganar MAVCC; (13): ambliopía: la MAVCC referida por el paciente era de 0,2. A los 2 meses de la cirugía ya se ha alcanzado su MAVCC. No ha sido retirada la sutura por lo que aún puede ganar MAVCC; (15): no ha sido retirada la sutura por lo que aún puede ganar MAVCC. 8. Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles 119 Fig. 8: Caso número 2. Leucoma postherpético vascularizado. (A y B) Aspecto preoperatorio. MAVCC: cuenta dedos a 1 metro. (C y D) Aspecto postoperatorio (obsérvese partículas en la entrecara). MAVCC: 1,0. Fig. 9: Caso número 3. Leucoma postherpético vascularizado. (A y B) aspecto preoperatorio. MAVCC: 0,05. (C y D) Aspecto postoperatorio. MAVCC: 0,8. 120 8. Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles Fig. 10: Caso número 5. Leucoma postherpético vascularizado. (A y B) Aspecto preoperatorio. MAVCC: 0,05 (ambliopía). (C y D) Aspecto postoperatorio. MAVCC: 0,6. Fig. 11: Caso número 12. Leucoma postherpético. (A y B) Aspecto preoperatorio. MAVCC: cuenta dedos a 1 metro (ambliopía). (C y D) Aspecto postoperatorio. MAVCC: 0,3 (tan sólo 3 meses de evolución: obsérvese aún los pliegues en la MD). 8. Queratoplastia Lamelar Anterior Profunda (DALK): Técnica de Melles nuestros 12 ojos se ha producido un episodio de rechazo estromal o epitelial (ni, por supuesto, endotelial). Nos parece interesante hacer mención a un caso de queratitis estromal necrotizante (paciente número 2) a los 3 meses de la cirugía inicial: este caso fue reintervenido mediante explante del injerto original e implante de un nuevo injerto y el resultado final es de MAVCC de 1,0. Por último, señalar que en los pacientes con más de 9 meses de evolución en los que el astigmatismo refractivo y topográfico es valorable, las cifras medias de estos son 3,37 (rango: 1,75-5) y 4,46 (rango: 2,75-6,75) respectivamente. Queremos por tanto hacer notar que, a pesar de que a primera vista los resultados puedan parecer desesperanzadores, no hay ningún caso en el que se haya producido un resultado no satisfactorio debido a la técnica en sí; más bien al contrario: casos en los que la posibilidad de rechazo endotelial estaba prácticamente asegurada con una QPP, han presentado un resultado altamente satisfactorio con la técnica DALK. 121 Bibliografía 1. Melles G, Rietveld F, Beekhuis WH, Binder PS. A technique to visualize corneal incision and lamellar dissection depth during surgery. Cornea 1999; 18: 80-86. 2. Melles GRJ, Lander F, Rietveld FJR, et al. A new surgical technique for deep stromal, anterior lamellar keratoplasty. Br J Ophthalmol 1999; 83: 327-333. 3. Melles GRJ, Remeijer L, Geerards AJM, Beekhuis WH. A quick surgical technique for deep, anterior lamellar keratoplasty using visco-dissection. Cornea 2000; 19: 427-432. 4. Minasian M, Ayliffe W. Fixed dilated pupil following deep lamellar keratoplasty (Urrets-Zavalia syndrome). Br J Ophthalmol 2002; 86: 115-116. 5. Maurino V, Allan B, Stevens J, Tuft S. Fixed dilated pupil (Urrets-Zavalia syndrome) after air/gas injection after deep lamellar keratoplasty for keratoconus. Am J Ophthalmol 2002; 133: 266-268. 6. Caporossi A, Simi C, Licignano R, et al. Air-guided manual deep lamellar keratoplasty. Eur J Ophthalmol 2004; 14: 55-58. 7. van Dooren BT, Mulder PG, Nieuwendaal CP, et al. Endothelial cell density after deep anterior lamellar keratoplasty (Melles technique). Am J Ophthalmol 2004; 137: 397-400. 8. Watson SL, Ramsay A, Dart JKG, Bunce C, Craig E. Comparision of Deep Lamellar Keratoplasty and Penetrating Keratoplasty in Patients with Keratoconus. Ophthalmology 2004; 111: 1676-1682.