Soluciones
Anuncio

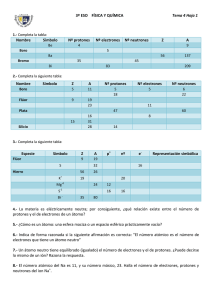
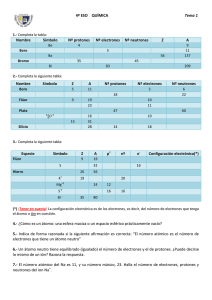
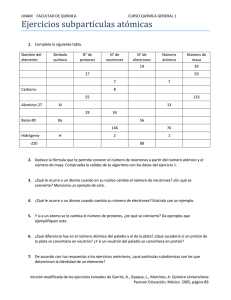
SOLUCIONES EJERCICIOS DE 4º ESO PROPUESTOS EN BACHILLERATO 1. a) Thomson en 1897. MedianTe sus experimentos con rayos catódicos en tubos de descarga de gases. b) La masa del protón y del neutrón son aproximadamente aguales. La masa del electrón es 1800 veces más pequeña. c) Protón y electrón tienen la misma cara en valor absoluto (1,6x10-19 C) , la del protón es + y la del electrón es - . El neutrón no tiene carga. 2. a) Por los grandes avances en la Física que hubo en la época, avances que fueron aplicados a indagar en la estructura interna del átomo. Los avances en electricidad permitieron a Thomson llevar a cabo sus investigaciones. El descubrimiento de la radiactividad (Becquerel 1896) permitió a Rutherford realizar su experimento de la lámina de oro. b) Porque seguían apareciendo fenómenos físicos y químicos que no podían ser explicados por los modelos vigentes. Además, se había demostrado que el átomo no era indivisible como se había pensado hasta entonces, por lo cual tenía sentido buscar hasta qué punto era divisible. Si el átomo tenía una estructura interna, podían buscarse los últimos constituyentes del átomo. 3. Thomson: El átomo es una masa positiva en la que están incrustados los electrones (partículas mucho más pequeñas con carga negativa). El número de electrones es el adecuado para compensar la carga positiva y que el átomo sea neutro. Rutherford: El átomo tiene una parte central (núcleo) donde se concentra casi toda la masa del átomo y tiene carga positiva. Alrededor, en una zona mucho más extensa (corteza) giran los electrones alrededor del núcleo debido a la fuerza eléctrica de atracción. La carga positiva del núcleo y negativa de los electrones se anulan. La gran diferencia entre ambos modelos es que en el de Thomson el átomo es macizo y en el de Rutherford es prácticamente hueco. 4. a) El primero fue Niels Bohr. Se apoya en los espectros atómicos. b) Las capas tienen más anergía a medida que nos alejamos del núcleo. 5. a) V ; b) V c) F (en el modelo actual no existe el concepto de órbita definida) ; d) V 6. 1cm = 0,01m =10-2 m 10-2 / 10-10 = 108 átomos (100000000 átomos) 7. a) 2 tipos. Unos positivos y otros negativos. b) Negativo = anión c) La descompensación entre el número de protones y el número de electrones del átomo. d) De ninguna forma, solo varía el número de electrones, no de protones ni de neutrones. 8. 46 neutrones ---> N=46 A=81 Z=A-N=81-46=35 ------35 protones 36 electrones Z=35 (Bromo) tiene 35 protones carga = (número protones) - (número electrones) = 35-36= -1 9. Z A Carga Tipo ión Protones neutrones electrones a) 8 16 -2 Anión 8 8 10 b) 28 58 +3 Catión 28 30 25 c) 30 64 +2 Catión 30 34 28 d) 35 75 -3 Anión 35 40 38 e) 48 114 +1 Catión 48 66 47 f) 80 202 +2 Catión 80 122 78 10. a) Un átomo de escandio que ha ganado dos electrones se ha convertido en un anión Sc3b) Al ganar 2 protones, un átomo ha pasado de tener un número atómico Z=4 a un número atómico Z=6 (Nota: lo normal no es que un átomo gane o pierda protones o neutrones, sino electrones, ya que son los más externos, en cuyo caso se forman iones, pero esto no afecta al número atómico ni al másico) c) La representación simbólica de un átomo de magnesio con 12 protones, 12 neutrones y 10 electrones es 2412Mg2+ 11. Isótopos son átomos del mismo elemento con distinto número de neutrones. Tienen igual número de protones (igual Z) y diferenta número de neutrones (y por lo tanto diferente A) p.ej. 168O y 178O 12. Porque son medias ponderadas de los diferentes isótopos del elemento, teniendo en cuaenta sus respectivas abundancias relativas. 13. 13153I tiene 53 protones y 78 neutrones. Son radioisótopos. El I-131 se utiliza para destruir células del tiroides en caso de hipertiroidismo o como radioterapia tras la extirpación de esta glándula por cáncer de tiroides. 14. A una representación de como están distribuidos los electrones en las capas de la corteza. 15. Es importante porque la configuración de los electrones más externos es la que determina las propiedades químicas del elemento. 16. a) El orbital 4s b) El orbital 3s c) Un orbital 3p d) Los orbitales 4d 2 17. He (2): 1s S(16): 1s2 2s2p6 3s2p4 Ca(20): [Ar] 4s2 Ni(28): [Ar] 4s2 3d8 Kr(36): [Ar] 4s2 3d10 4p6 Zr(40): [Kr] 5s2 4d2