DEMENCIA Y DOLOR Problema frecuente de diagnóstico complejo
Anuncio

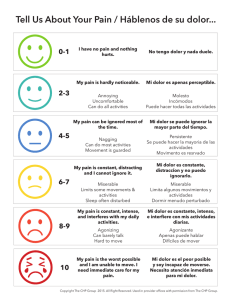
DEMENCIA Y DOLOR Problema frecuente de diagnóstico complejo Dra. Cristina Arotce Dra. Soad Ayul Departamento de Geriatría y Gerontología. Prof Dr Italo Savio Introducción La edad constituye un factor de riesgo para dolor y demencia. 60-80% de los pacientes con demencia experimentan dolor. En la demencia avanzada, los pacientes no pueden reportar dolor debido al déficit cognitivo y verbal propio de la enfermedad. Esto genera una infradetección y un infratratamiento del dolor. Hadjistavropuolos T, Herr K, Prkachin K, Craig K et al. Pain assessment in elderly adults with dementia. Lancet Neurol 2014; 13: 1216-27. Corbett A, Husebo B, Malcangio M, Staniland A, Cohen-Mansfield J et al. Assessment and treatment of pain in people with dementia. Nat Rev Neurol 2012; 8: 264-274. Husebo B, Kunz M, Achterberg W, Lobbezoo F et al. Pain Assessment and treatment challenges in patients with dementia. Z.Neuropsychol 2012; 23(4): 237-246. El dolor en la demencia o Un inadecuado diagnóstico y control del mismo genera mayor sufrimiento del paciente, sobrecarga del cuidador e incrementos de los costos sanitarios. Consecuencias del dolor no tratado en pacientes con demencia: FÍSICAS PSICOSOCIALES Dificultad para caminar y movilizarse Anorexia Alteración del sueño Agitación Vagabundeo Declinación funcional Delirium Agresión verbal Depresión Aislamiento social Shega J, Emanuel L, Vargish L, Levine S et al. Pain in persons with dementia: complex, common and challenging. The Journal of Pain 2007; 8: 373-378. El dolor en la demencia En el envejecimiento se producen alteraciones en los SNC y SNP relacionados con el procesamiento del dolor, y en los sistemas de control endógeno inhibitorio, disminuyendo el umbral del dolor. En los pacientes con demencia no se aprecian cambios en el umbral del dolor, pero si en la tolerancia del mismo. El componente sensorial está indemne, mientras que el componente afectivo del dolor se encuentra modificado. Alaba J, Arriola E, Navarro A, González M, Buiza C, Hernández C, Zulaica A. Demencia y dolor. Rev Soc Esp Dolor 2011; 18: 1-10. Percepción del dolor en la Enf Alzheimer Los pacientes con EA en una fase temprana reportan más dolor que aquellos en una etapa más avanzada de la enfermedad. Tienen el mismo umbral de dolor, pero una significativa mayor tolerancia al mismo. La capacidad analgésica del placebo desaparece en el paciente con EA. Los pacientes con EA parecen ser más sensibles al dolor agudo respecto al crónico. Alaba J, Arriola E, Navarro A, González M, Buiza C, Hernández C, Zulaica A. Demencia y dolor. Rev Soc Esp Dolor 2011; 18: 1-10. Valoración del dolor DEMENCIA Y DOLOR Instrumentos para medición del dolor → Instrumentos de autoreporte de dolor → Medidas de observación comportamental Escalas de autoreporte de dolor El componente del dolor que se mide frecuentemente a través de autoinformes es la INTENSIDAD DEL DOLOR. ESCALA DESCRIPTIVA VERBAL ESCALA NUMÉRICA 0 1 Ausencia de dolor 2 3 4 Dolor leve 5 6 7 Dolor moderado 8 ESCALA FACIAL DEL DOLOR Montes MJ, Retamoso I, Vazquez C. El dolor, un abordaje interdisciplinario. Zona Editorial. 2012. Montevideo, Uruguay. 9 10 Dolor intenso Medidas de observación comportamental EDAD (Escala de evaluación del dolor en ancianos con demencia) PADE (Pain Assessment for Dementia in the Elderly) RAPID (Rating Pain in Dementia) Escala de dolor de Abbey DOLOPLUS-2 PANAID (Pain Assessment in Advanced Dementia) PACSLAC (Pain Assessment Checklist for Seniors with Limited Ability to Communicate) NOPPAIN (Non-Communicative Patient`s Pain Assessment Instrument) DS-DAT (Discomfort in Dementia of the Alzheimer’s type) CNPI (Checklist of Nonverbal Pain Indicators) Hadjistavropuolos T, Herr K, Prkachin K, Craig K et al. Pain assessment in elderly adults with dementia. Lancet Neurol 2014; 13: 1216-27. Escala PACSLAC Pain Assessment Checklist for Senior with Limited Ability to Communicate Es considerada el gold standard para la evaluación del dolor en este grupo de pacientes. Está formada por 60 ítems agrupados en 4 categorías: expresión facial, movimientos del cuerpo, indicadores fisiológicos e indicadores psicosociales. Cada uno de los ítems puntúa en una escala dicotómica (presencia o ausencia). Se utiliza en trabajos de investigación. Desventajas: está en inglés y es muy larga. Escala DOLOPLUS 2 REACCIONES SOMÁTICAS 1. Quejas somáticas (0) Ninguna queja. (1) Quejas únicamente ante el estímulo. (2) Quejas espontáneas ocasionales. (3) Quejas espontáneas continuas. 2. Posiciones antálgicas en reposo (0) Ninguna posición antálgica. (1) El sujeto evita ciertas posiciones ocasionalmente. (2) Posición antálgica permanente y eficaz. (3) Posición antálgica permanente ineficaz 3. Protección de las zonas dolorosas (0) Ninguna protección. (1) Protección ante el estímulo que no impide continuar el examen o los cuidados. (2) Protección ante el estímulo que impide examinarlo. (3) Protección en reposo, en ausencia de todo estímulo. 4. Mímica (0) Mímica habitual. (1) Parece expresar dolor ante el estímulo. (2) Parece expresar dolor en ausencia de estímulo. (3) Inexpresiva en forma permanente (expresión fija, mirada vacía, atonía) 5. Sueño (0) Sueño habitual. (1) Dificultades para conciliar el sueño. (2) Despertar frecuente, agitación motora. (3) Insomnio con repercusión en las fases de vigilia. REACCIONES PSICOMOTORAS 6. Aseo y/o vestido (0) Sin cambios. (1) Algo disminuidas, lo realiza pero con precaución. (2) Muy disminuidas, aseo y/o vestido difíciles y parciales. (3) Imposibles, el enfermo se opone. 7. Movimientos (0) Sin cambios. (1) Activos limitados, el enfermo evita ciertos movimientos, disminuye su perímetro de marcha. (2) Activos y pasivos limitados, incluso con ayuda el enfermo reduce sus movimientos. (3) Imposible, toda movilización encuentra oposición. REACCIONES PSICOSOCIALES 8. Comunicación (0) Sin cambios. (1) Intensificada, la persona atrae la atención de manera inhabitual. (2) Disminuida, la persona se aísla. (3) Ausencia o rechazo de toda comunicación. 9. Vida social (0) Sin cambios. (1) Participación en las distintas actividades solo bajo estímulo. (2) Rechazo parcial de participación. (3) Ausencia de toda vida social. 10. Trastornos del comportamiento (0) Sin cambios. (1) TDC bajo estímulo. (2) TDC bajo estímulo y permanentes. (3) TDC permanentes, fuera de todo estímulo. Escala PANAID Pain Assessment in Advanced Dementia – Evaluación del dolor en la demencia avanzada 0 1 2 SCORE Respiración Normal Respiración ocasionalmente dificultosa. Períodos cortos de hiperventilación Respiración dificultosa y ruidosa. Largos períodos de hiperventilación. Respiración de Cheyne-Stokes. Vocalización Ninguna Gemidos o quejidos. Habla con volumen bajo o con desaprobación. Llamadas agitadas y repetitivas. Gemidos y quejidos en volumen alto. Llanto. Expresión facial Sonriente o inexpresivo Triste. Atemorizado. Ceño fruncido Muecas de disgusto o desaprobación Lenguaje corporal Relajado Tenso. Camina de forma angustiada. Inquieto con las manos. Rígido. Puños cerrados. Rodillas flexionadas. Agarra o empuja. Agresividad física Consolabilidad No necesita que se le consuele Se distrae o se tranquiliza hablándole o tocándolo Es imposible consolarlo o tranquilizarlo TOTAL Escala CNPI Checklist of Nonverbal Pain Indicators – Indicadores no verbales del dolor CONDUCTA CON MOVIMIENTO 1. VOCALIZACIONES (suspiros, lamentos, gritos, llanto) 2. MUECAS FACIALES (frente arrugada, ojos apretados, labios y dientes apretados) 3. TENSIÓN (sujetarse a los muebles, equipos, o sostener el área afectada durante el movimiento) 4. INQUIETUD (constante o intermitente cambio de posición, mecerse, movimientos con las manos, nunca quieto) 5. FROTARSE (masajeando el área afectada) 6. QUEJIDOS ORALES (palabras que describan desconfort o dolor, como ser “ay”, “ya está”, “no puedo más”) Score subtotal Score total EN REPOSO ¿Cual escala utilizar y cuando? NIVEL DE DETERIORO COGNITIVO ESCALAS Ninguno Leve Moderado Severo Escalas analógicas visuales (colores, termómetro) √ √ √ x Escalas numéricas √ √ x √ √ x x x √ x x √ Escalas faciales de dolor Escalas observacionales Coffey Alice et al. Palliative care for the person with dementia. Guidance document 4: Pain assessment and management. The Irish Hospice Foudation. 2015 ¿Cual escala observacional utilizar? Conclusiones: PACSLAC DOLOPLUS 2 Por presentar las mejores propiedades psicométricas en cuanto a validez, fiabilidad y homogeneidad en personas con demencia. Tratamiento farmacológico DEMENCIA Y DOLOR Consideraciones El manejo farmacológico del dolor en el anciano es complicado por el aumento de las reacciones adversas que se producen en general. Estas consideraciones son aún mayores en las personas con demencia, en relación a su vulnerabilidad neurológica, aumentando en ellos la sedación y los efectos secundarios. El efecto placebo desaparece con la afectación de las áreas frontales (funciones ejecutivas) en pacientes con Enfermedad de Alzheimer. Por lo que no es adecuado ni ético el uso de placebos para el control del dolor en estos pacientes. Consideraciones Tratar de identificar la causa del dolor, siempre que sea posible, y actuar sobre ella. Considerar medidas no farmacológicas antes de proceder al uso de fármacos del primer escalón analgésico de la OMS. A la hora de prescribir opioides, se debe comenzar con dosis bajas y aumentar lentamente (Start slow and go slow). Criterios de BEERS American Geriatrics Society 2015. Updated Beers criteria for potentially inaprpopiate medication in older adults. JAGS 63: 2227-2246 Criterios STOPP and START 1er escalón: Analgésicos no opioides No hay diferencias en cuanto a eficacia analgésica entre uno y otro fármaco. No es útil la asociación de dos AINEs, porque no se logra aumentar la eficacia analgésica y sí lo efectos secundarios. Los más gastrolesivos son el Ketoprofeno, el Ketorolac y el Piroxicam. Está indicado el uso de IBP (Omeprazol) en aquellos pacientes con FR para toxicidad gastrointestinal (todos). Paracetamol → Es el de elección por su mínima toxicidad gástrica y renal. → Es antipirético y analgésico. No posee actividad antiinflamatoria. → No se deben superar los 3g al día → Dosis tóxica: 10 g/día → Contraindicado en pacientes con insuficiencia hepática 2do escalón: Opioides menores Se debe empezar con dosis muy bajas y titular Tramadol → Dosis habitual es de 50 a 100mg c/4-6 hs → Dosis máxima en ancianos frágiles: 300 mg/día → Especial cuidado en pacientes con ISRS o ISRSN (Venlafaxina y Duloxetina) por el riesgo de aparición de un síndrome serotoninérgico. → Eficaz en el tto tanto del dolor agudo como del crónico. De elección en el tto del dolor crónico. 3er escalón: Opioides mayores Se requieren generalmente en casos excepcionales. A dosis bajas actúan como opioides menores. También producen efectos subjetivos como una sensación de bienestar y euforia, lo que contribuye a la acción analgésica. No tienen techo analgésico. Cuanto más dosis, más efecto analgésico. Las limitaciones están dadas por la aparición de efectos secundarios. Pergolizzi J, Boger R, Budd K, Dahan A, Erdine S et al. Consensus Statement: Opioids and the management of cronic severe pain in the eldely. Pain Practice 2008; 8 (4): 287-313. Potenciales beneficios y riesgos de los OPIOIDES en la demencia Potencial beneficio Potencial riesgo Dolor Disminuye la severidad Puede no disminuir la severidad pero sí exponer al paciente a potenciales riesgos Polifarmacia Reduce el uso de fármacos psicotrópicos Tal vez no cambia el número de fármacos recibidos. Seguramente requiera el agregado de laxantes. Sobrecarga del cuidador Disminuye Puede aumentar si hay preocupación sobre la posibilidad de dependencia/ adicción. Movilidad Mejora Aumenta el riesgo de caídas Función cognitiva No se conoce. Tal vez disminuya el riesgo de delirium Puede generar bradipsiquia al igual que sedación. Delirium es posible. Función psicológica Puede mejorar con la reducción del dolor Puede generar depresión y/o agitación Sueño Puede mejorar el sueño si éste se encontraba alterado por el dolor Alteración en la arquitectura del sueño Apetito Puede mejorar el apetito si éste se encontraba alterado por el dolor Nauseas y/o constipación puede generar alteraciones en el apetito Shega J, Emanuel L, Vargish L, Levine S et al. Pain in persons with dementia: complex, common and challenging. The Journal of Pain 2007; 8: 373-378. Coadyuvantes analgésicos Los coadyuvantes analgésicos (antiepilépticos, antidepresivos, neurolépticos, corticoides) forman parte del tratamiento integral del dolor crónico en especial en el dolor neuropático, donde son el tratamiento farmacológico de 1ra línea. Muchos de ellos también son eficaces en aliviar otros síntomas acompañantes del dolor tales como la depresión, ansiedad, trastornos del sueño, etc. La decisión de cual o cuales debemos emplear debe basarse no solo en la evidencia científica de su eficacia, el perfil de seguridad y la interacciones farmacológicas, sino en los síntomas que deseamos aliviar, la edad y comorbilidades del paciente, el costo y accesibilidad a la medicación. Conclusiones Existe una infradetección e infratratamiento del dolor en la demencia con graves repercusiones funcionales y sobre la calidad de vida. El dolor puede manifestarse como delirium o trastornos afectivos, siendo frecuente la presentación atípica. Evaluar el dolor en las personas mayores con demencia, especialmente en etapas avanzadas, es un reto. Se recomienda utilizar escalas de valoración del dolor adaptadas y validadas. Cada tratamiento debe ser individualizado. La elección más apropiada, la titulación lenta, el alcance de las dosis de mantenimiento adecuadas y la medición del impacto del tratamiento en cada paciente, son las premisas fundamentales. Muchas gracias..