CAPÍTULO 1 INTRODUCCIÓN 1.1 Antecedentes del Problema Por
Anuncio

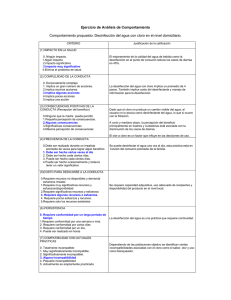
CAPÍTULO 1 INTRODUCCIÓN 1.1 Antecedentes del Problema Por mucho tiempo se han estudiado e investigado alternativas efectivas y de bajo costo para desinfectar agua para uso y consumo humano en situaciones en las que, por diversas razones, no se cuenta con un agua de calidad adecuada, como las que prevalecen en pequeñas comunidades y en situaciones de desastre. Las zonas rurales cuentan generalmente con insuficientes recursos sanitarios, energéticos, culturales y económicos y resultan ser las regiones más afectadas por el consumo directo de agua contaminada (Galal-Gorchev, 1996). El proceso de desinfección es clave en cualquier sistema de tratamiento de agua, ya que la generación de agua microbiológicamente segura depende en buena medida de él. Existen varios métodos tradicionales de desinfección y otros de relativa nueva aplicación. Algunos de los factores que influyen en la selección de un método o tecnología de desinfección para agua son costo, consumo energético, calidad del agua a tratar, entre otros. Por más de un siglo se ha utilizado cloro para desinfectar agua para uso y consumo humano. La aplicación de cloro contribuyó a disminuir de manera significativa la ocurrencia de enfermedades gastrointestinales tales como el cólera, la disentería, amebiasis, salmonelosis, shigellosis y hepatitis A. Sin embargo, en años más recientes se ha demostrado que la cloración puede resultar ineficiente para controlar la ocurrencia de algunos patógenos en el agua, tales como Giardia lamblia y Cryptosporidium parvum (Galal-Gorchev, 1996). Un ejemplo de método alternativo que se ha explorado para desinfectar agua con bajo costo y menores implicaciones ambientales adversas es la radiación solar, referida en ocasiones como SODIS (del Inglés, Solar Disinfection). El proceso de desinfección solar ha sido demostrado como un tratamiento efectivo para el consumo de agua contaminada con bacterias y virus patógenos. Este método es ideal cuando las condiciones económicas y socioculturales de la comunidad ponen en riesgo la sostenibilidad de otras alternativas de tratamiento y desinfección, como la filtración o el uso de cloro, aún cuando estas también sean reconocidas como simples y económicas. A la fecha existen muy pocos estudios acerca de la eficiencia que puede tener la SODIS para inactivar C. parvum, Giardia lamblia u otros patógenos protozoarios importantes (Saladin, 2004)). Algunos estudios han demostrado que la aplicación seriada de dos procesos de desinfección química (ozono y cloro, por ejemplo) puede resultar muy eficiente para inactivar C. parvum y G. lamblia. Se ha encontrado que una exposición limitada de estos patógenos a un oxidante “fuerte” como el ozono puede sensibilizarlos de manera importante a la acción germicida del cloro, de tal manea que las dosis de cloración pueden reducirse considerablemente. Una de las explicaciones propuestas sobre este fenómeno sugiere que los radicales OH• generados durante la ozonización alteran la permeabilidad de la membrana celular afectando directamente la estructura de los lípidos ahí contenidos. Una vez alterada la permeabilidad de la membrana, el cloro aplicado puede permear hacia el interior del organismo y dañarlo. Una alternativa interesante para generar radicales OH• es sin duda la fotocatálisis solar. Por ello se propone sustituir al proceso de ozonización por fotocatálisis solar para ser probada en un esquema secuencial como el descrito anteriormente. De aquí que el objetivo primordial de este trabajo de tesis sea evaluar el potencial germicida de la desinfección secuencial utilizando fotocatálisis solar seguida de cloro libre. 1.2 Importancia de la Desinfección de Agua El agua es un elemento natural indispensable para la vida y para la salud, el ser humano lo usa y lo consume diariamente. Existen diversas formas para extraerla de la tierra, sin embargo, estas aguas pueden contener restos de materia orgánica, desechos de fertilizantes o de productos industriales que la contaminan y que se convierten en un peligro potencial para la salud de las personas puesto que es un vehículo idóneo para transmitir enfermedades. Un requisito importante que debe cumplir el agua para ser considerada como “potable” es estar libre de microorganismos transmisores de enfermedades gastrointestinales y por ello es necesario someterlas, en ocasiones a tratamientos específicos (Saladin, 2001). Según reportes de la Organización Mundial de la Salud el consumo de agua contaminada, así como la disposición inadecuada de las aguas residuales, se encuentran entre las tres causas principales de muerte en el mundo. Tan sólo en América Latina y el Caribe la gastroenteritis y las enfermedades diarreicas son responsables de aproximadamente 200,000 muertes al año, sin incluir las ocasionadas por la fiebre tifoidea, la hepatitis y otras similares (Castro de Esparza, 1992). Por todo ello, la desinfección de agua forma parte importante del tren de tratamiento o serie de procesos/operaciones a que ésta debe someterse con la finalidad de reducir o eliminar toda una gama de posibles contaminantes microbiológicos contenidos en ella. 1.3 Procesos Tradicionales de Desinfección del Agua 1.3.1 Cloro El empleo de cloro para la desinfección de agua de consumo humano es una práctica aceptada en todo el mundo y ampliamente usada para controlar la ocurrencia de enfermedades gastrointestinales tale como el cólera. La cloración es una alternativa para la desinfección del agua ampliamente difundida en los países en desarrollo, dado que constituye la tecnología mas conocida por su eficacia, costos de su aplicación, así también por estar histórica y epidemiológicamente comprobada. En sus guías de calidad de agua, la OMS recomienda que, para tener la garantía sanitaria de la calidad del agua para consumo y para asegurar su efecto ante cualquier contaminación posterior, debe existir un promedio de 0.3 mg/L de cloro residual activo y una turbiedad menor de 1 UNT Unidad Nefelométrica de Turbiedad (Castro de Esparza, 1992). Se ha sabido ya por muchos años que el cloro reacciona con ciertos materiales orgánicos durante la desinfección de agua y crea trihalometanos (THMs), incluido en particular el cloroformo. Estudios toxicológicos demostraron que el cloroformo es carcinogénico para animales de laboratorios, aunque aplicado en niveles mucho mayores que los encontrados en agua potable. Los efectos tóxicos de los THMs incluyen afectación al sistema nervioso central, así como a las funciones del hígado y los riñones. Los temores de que lo THMs podrían ser cancerígenos en el ser humano llevaron a la Agencia de Protección Ambiental de los Estados Unidos (US EPA, por sus siglas en inglés) a fijar los límites reglamentarios para estos subproductos de desinfección (SPD) a 0.080 mg/L (80 partes por billón). En general, las desventajas más importantes que presenta la desinfección con cloro son las siguientes: El cloro residual, aún en bajas concentraciones, puede resultar nocivo a los organismos acuáticos. Todas las formas de cloro son corrosivas y potencialmente tóxicas. Como consecuencia, el almacenamiento, el transporte y el manejo presentan riesgos cuya prevención requiere de normas estrictas de seguridad. El cloro oxida ciertos tipos de materiales orgánicos del agua residual generando compuestos más peligrosos, por ejemplo trihalometanos (THMs). 1.3.1.1 Cloro libre: Se refiere a las especies de cloro en forma de Cl2, HOCl y OCl-, las cuales tienen capacidades germicidas diferentes en virtud a la cantidad de materia orgánica, presente en el agua y al pH de la misma. De las tres especies mencionadas, el ácido hipocloroso (HOCl) es la que tiene mayor capacidad para inactivar microorganismos patógenos en agua. Para procurar su predominio sobre las otras dos especies, es necesario procurar que el pH del agua se encuentre entre 5.0 y 7.5 unidades. 1.3.1.2 Cloraminas: Se refiere a las especies de cloro combinado que resultan de la mezcla de cloro libre y amonio (NH3). Tales especies son: monocloramina (NH2Cl), dicloramina (NHCL2) y tricloramina o tricloruro de nitrógeno (NCl3). Estás se usan comúnmente para mantener un residual de desinfectante durante la distribución de agua a través de las redes municipales. Contrario a lo observado con cloro libre, la aplicación de cloraminas resulta en poca formación de trihalometanos y ácidos haloacéticos. 1.3.1.3 Dióxido de Cloro (ClO2): Este desinfectante actúa como una excelente sustancia virucida, no reacciona con nitrógeno amoniacal para formar aminas doradas, tampoco reacciona con material oxidable para formar THMs, (e incluso destruye hasta 30% de los precursores de THMs) y es moderadamente eficaz contra G. lamblia y C. parvum. No obstante, este producto se descompone en subproductos inorgánicos: en clorito (ClO2 -) y en menor grado en ion de clorato (ClO3 -), los cuales son actualmente regulados debido a su toxicidad. En la Tabla 1.1 se muestra un cuadro comparativo de los procesos tradicionales de desinfección de agua descritos en este apartado. Tabla 1.1 Cuadro Comparativo de Desinfectantes de Agua Potable Desinfectantes Eficacia de Mantenimiento Estado de Remoción Remoción desinfección de residuos información de colores de olores en la comunes química del subproducto Cloro Bueno Bueno Adecuado Bueno Bueno Cloraminas Pobre Bueno Limitado Inadmisible Pobre Dióxido de cloro Bueno Inadmisible Adecuado Bueno Bueno Ozono Excelente Inadmisible Limitado Radiación Ultravioleta Acertado Inadmisible Nulo Excelente Excelente N/A N/A Fuente: Trussell, 1991. 1.3.2 Ozono La aplicación de ozono para desinfección de agua, así como para controlar su olor y sabor, es también tradicional. El ozono (O3) es un oxidante muy fuerte, que al entrar en contacto con microorganismos o compuestos orgánicos responsables de olor/sabor reacciona y las oxida dependiendo de su afinidad. A diferencia del cloro libre o combinado, el ozono no produce trihalometanos, ni ácidos haloacéticos. Sin embargo, la ozonización produce SPDs tales como bromatos y cianuros y varios precursores de otros subproductos relevantes. Además es importante reconocer que la aplicación de ozono como desinfectante requiere de una importante inversión de capital, puesto que el ozono se debe producir en el lugar por medio de una tecnología costosa que demanda mantenimiento y capacitación substancial de operadores. Así también promueve el crecimiento microbiano al reaccionar fácilmente con la materia orgánica más compleja, misma que puede descomponerla en compuestos más pequeños que sirven para aumentar los nutrientes en los abastecimientos de agua, por lo tanto puede mejorar el crecimiento microbiano en los sistemas de distribución de agua si en éste no se aplica algún residual de cloro libre para prevenirlo (Bulí y Kopfler, 1991). 1.3.3 Radiación Ultravioleta (UV) En este proceso incluye la exposición del agua a radiación UV (radiación UV-C, con longitud de onda de aproximadamente 254 nm), la cual inactiva diversos microorganismos alterando su información genética. La técnica se ha aplicado cada vez mas para el tratamiento tanto de agua residual como potable. Entre sus principales características, este proceso no requiere almacenamiento químico, manejo o equipo de alimentación y tampoco subproductos identificados de desinfección. No obstante, presenta altos costos de mantenimiento, importante inversión inicial, además de que su costo de operación también es importante. 1.4 Procesos de Oxidación Avanzada La mayoría de los procesos de oxidación avanzada pueden aplicarse para descontaminar agua a pequeña o mediana escala. Los métodos pueden usarse solos o combinados (entre ellos o con otros métodos convencionales) pudiendo ser aplicados también a contaminantes del aire y suelo. Los procesos avanzados de oxidación (PAOs) se basan en procesos fisicoquímicos que tienen la capacidad de producir cambios profundos en la estructura química de los contaminantes. El concepto fue inicialmente establecido por Glaze y colaboradores, quienes definieron los PAOs como procesos que involucran la generación y uso de especies transitorias poderosas, tales como los radicales hidroxilo (HO•). Este radical puede ser generado por medios fotoquímicos (incluida la luz solar) o por otras formas de energía, y posee alta efectividad para oxidar materia orgánica. Algunos PAOs recurren además a reductores químicos que permiten realizar transformaciones en contaminantes tóxicos poco susceptibles a la oxidación, tales como iones metálicos o compuestos halogenados (Doménech, Jardim y Litter, 2001). En general, los procesos avanzados de oxidación pueden clasificarse como fotoquímicos y no fotoquímicos. Tabla 1.2 Procesos de Oxidación Avanzada Procesos no fotoquímicos Procesos fotoquímicos - Ozonización en medio alcalino (O3/OH ) Oxidación en agua sub/y supercrítica Ozonización con peróxido de hidrógeno (O3/H2O2) Procesos fotoquímicos Fotólisis del agua en el ultravioleta de vacío Procesos Fenton (Fe2+/ H2O2) y relacionados (UVV) Oxidación electroquímica UV/peróxido de hidrógeno Radiólisis γ y tratamiento con haces de electrones UV/O3 Plasma no térmico Foto-Fenton y relacionadas Descarga electrohidráulica – Ultrasonido Fotocatálisis heterogénea Fuente: Doménech et al, 2001 1.5 Fundamentos de la Fotocatálisis Solar Una de las fuentes principales de energía para el desarrollo de la vida en el planeta es la radiación solar. La radiación solar se conforma por varias franjas o tipos de radiación: ultravioleta (UV), visible e infrarroja. Figura 1.1 Espectro Electromagnético (Zuloaga,2000) La capacidad germicida de la radiación solar se ha relacionado con la fracción ultravioleta de ésta. Por su parte, la fracción infrarroja contribuye notablemente a incrementar la temperatura del agua y con ello colabora a inducir condiciones adversas a los microorganismos patógenos que pudieran estar presentes en el agua. En lo referente a la fotocatálisis solar, esta técnica consiste en aplicar la energía solar para conseguir la degradación de los contaminantes por oxidación. La fotocatálisis solar es un proceso que se basa en la absorción directa o indirecta de energía radiante (visible o UV) por un sensibilizador. Este “fotocatalizador” es capaz de absorber la energía solar emitida, capturar fotones y con ello alcanzar estados electrónicos excitados. Cuando estos estados excitados se desactivan, se genera una especie orgánica agresiva que será encargada de atacar la materia orgánica, iniciando su degradación oxidativa. Los elementos necesarios para llevar a cabo la fotocatálisis solar son: Radiación solar, un agente oxidante (O2, H2O2, S2O82-) y un catalizador (Fe2+, Co2+,TiO2, Fe), entre otros). Los catalizadores empleados en fotocatálisis solar son materiales económicos, fáciles de conseguir e incluso muchos de ellos participan en procesos químicos de la naturaleza. Además, la mayoría de estos materiales pueden excitarse con radiación de no muy alta energía y pueden absorber parte de la radiación del espectro solar que incide sobre la superficie terrestre (λ > 310 nm), lo cual incrementa el interés para un posible aprovechamiento de la radiación solar. Los fotocatalizadores más investigados hasta el momento son los óxidos metálicos semiconductores de banda ancha y, particularmente, el TiO2, el cual presenta una elevada estabilidad química que lo hace apto para trabajar en un amplio rango de pH. La reacción Fenton es también ampliamente conocida y se refiere al uso de un metal (Fe2+, por ejemplo), el cual sirve como catalizador, que al ser combinado con un oxidante (H2O2, por ejemplo) contribuye a la formación de radicales con un elevado potencial de oxidación. Fe 2+ + H 2 O2 → Fe 3+ + HO • + HO − (1) Fe3+ + H 2O2 → Fe(OH )2 + + HO • + HO + (2) Fe(OH ) 2+ + hv → HO • + Fe 2+ (3) M .O. + HO • → productos de oxidación (4) Parece evidente que los procesos de fotocatálisis solar suponen una aplicación prometedora para descontaminar agua, no sólo por su potencial para degradar contaminantes biológicos y químicos sino también porque representan una tecnología ambientalmente más amigable que los procesos tradicionales. 1.6 Fundamentos de la Desinfección Secuencial La desinfección secuencial es un proceso en el cual los microorganismos son expuestos a un desinfectante primario con alta capacidad oxidativa, (i.e. ozono) y como segundo paso son expuestos a un desinfectante secundario “menos potente” (i.e cloro libre). Se ha observado que el pretratamiento en ocasiones, aplicado con el desinfectante “fuerte” sinergiza la acción germicida del desinfectante “débil” tornándolo más efectivo. Con el fin de ilustrar los efectos benéficos que se han reportado en esquemas de desinfección secuencial, se muestra a continuación una breve descripción de lo observado en otros estudios con la combinación de ozono/cloro libre aplicada a la inactivación de C. parvum. 1 0.1 N /No 0.01 0.001 0.0001 0 2 4 6 8 C × t (mg-min/L) Figura 1.2 Inactivación de Ooquistes de Crypstosporidium parvum con Ozono, pH=7.0 y 20°C. En la Figura 1.2 se ilustra la cinética de inactivación de ooquiste de C. parvum con ozono. De los datos mostrados puede observarse que la dosis de ozono requerida para disminuir la viabilidad de C. parvum en un 90% es de aproximadamente 2.2 mgmin/L. Si a una población de C. parvum se le aplicara una dosis semejante de ozono, y posteriormente la misma población fuera expuesta a cloro libre, entonces la cinética de inactivación con cloro sería muy similar a la que se muestra en la Figura 1.3. Como puede observarse, la aplicación limitada de ozono permite acelerar el proceso de inactivación con cloro de tal manera que, por ejemplo, las dosis requeridas para inactivar 99% de los ooquistes con cloro libre solo y con cloro libre secuencial difieren en un factor de 7 (C × t = 3500 mg-min/L para cloro libre solo vs C × t = 500 mg-min/L para cloro secuencial). 1 0.1 N /No Colo libre solo 0.01 Cloro libre despues de ozono 0.001 0.0001 0 1000 2000 3000 4000 5000 6000 C × t (mg-min/L) Figura 1.3 Ejemplo de los Efectos Sinérgicos Producidos por Ozono en la Subsecuente Aplicación de Cloro Libre para Inactivar Ooquistes de C. parvum. Los efectos sinérgicos producidos por el pretratamiento con ozono en la subsecuente desinfección con cloro libre son muy significativos. Otras combinaciones para las cuales se han detectado efectos similares son ozono/monocloramina, mientras que algunas otras como ClO2/COl y ClO2/NH2Cl no han mostrado efecto benéfico alguno.