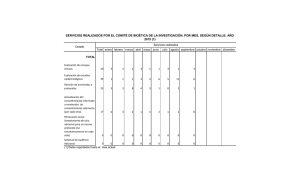
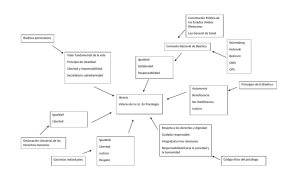
Modelos de Fundamentación en Bioética La
Anuncio

Modelos de Fundamentación en Bioética La investigación con seres humanos: análisis de un caso Charla - Taller Carolina Pallas [email protected] Departamento de Filosofía - Instituto de Profesores “Artigas” JORNADAS REGIONALES DE FILOSOFÍA Y DIDÁCTICA Young, Junio 2008 1 I- Ética y Moral: concepto y problemáticas II- Bioética: surgimiento, concepto y problemas III- Modelos de Fundamentación en Bioética * De Principios * Casuístico * Deliberativo, basado en DDHH IV- Taller: La investigación con seres humanos. Análisis de un caso 2 BIOÉTICA •Problemas éticos que se plantean en el contexto de la medicina y las ciencias biológicas. •Encyclopedia of Bioethics define la bioética como "el estudio sistemático de la conducta humana en el área de las ciencias de la vida y del cuidado sanitario, en cuanto que tal conducta se examina a la luz de los valores y de los principios morales". Tres grupos de condicionantes de su surgimiento: 1- El creciente y desmesurado tecnológico de los últimos 60 años; avance científico 2- El surgimiento de los derechos de los enfermos; 3- El cambio en los modelos de asistencia sanitaria y el debate sobre el derecho a la salud. 7 1962 Seattle Se crea un comité de legos para decidir qué pacientes tenían preferencia para beneficiarse de la entonces reciente máquina de hemodiálisis. ¿Por qué un avance médico debería crear una nueva discriminación médica? ¿Quién y cómo elegía a los candidatos? 8 1972 Se divulga el "caso Tuskegee", un estudio hasta entonces secreto, en el que 400 individuos de raza negra habían dejado de ser tratados contra la sífilis (a pesar de que ya existían tratamientos eficaces). "Comisión Nacional para la Protección de los sujetos humanos en el campo de las Ciencias Biomédicas y del Comportamiento”. "Informe Belmont“ (1978) con directrices para la protección de los individuos que participen como sujetos de experimentación en Biomedicina, basados en los principios de autonomía, beneficencia y justicia. 9 1967: primeros trasplantes de corazón, se plantea el problema de cómo definir la muerte clínica. 1968: la facultad de medicina de la Universidad de Harvard publica un artículo donde plantea el nuevo criterio basado en la muerte cerebral. Casos de coma irreversible animaron el debate sobre la eutanasia y el "derecho a la propia muerte". 1975 Karen Ann Quinlan entra en coma irreversible y queda en estado vegetativo persistente. Los padres piden que la desconecten del respirador artificial para que pueda morir en paz. Tras una denegación judicial, hay un recurso, en el que el Tribunal Supremo de Nueva Jersey autoriza la desconexión sobre la base del "derecho a una muerte digna y en paz". * Se reconocía por primera vez que la propia tecnología de soporte vital planteaba la cuestión sobre la eticidad o no de mantener en estado vegetativo a individuos que nunca volverían a tener una vida consciente. * Una de las recomendaciones del Tribunal Supremo fue la de que los hospitales creasen "Comités de ética" capaces de enfrentarse a este tipo de conflictos. 10 * Crisis del concepto paternalista de beneficencia médica: El médico ya no puede imponerse (siquiera benevolentemente) al paciente, sino que éste ha de ser informado, para que pueda ejercer sus irrenunciables derechos de autonomía y pueda conceder el consentimiento a los tratamientos. En 1972 se promulga en EE.UU. la Carta de los Derechos de los Enfermos. * Universalización de los servicios sanitarios: ¿Cómo financiar y distribuir equitativamente unos recursos limitados, y cómo regular el acceso a distintas tecnologías por parte de los ciudadanos. ¿Cómo se atienden las necesidades básicas sanitarias de todos los ciudadanos? Pero ¿qué son necesidades básicas? ¿Cómo se diferencia entre lo necesario y lo accesorio? 11 América Latina (referencia especial a otros determinantes propios por causas económico políticas) •Consumidores de tecnología que no producen. •Se realiza el 90% de las investigaciones que utilizarán el 10% de la población mundial no latinoamericana. •Falta de accesibilidad o inequidad en asistencia sanitaria. •Se transita un período de estabilización de las democracias. 12 “BIOÉTICA”: Triple acepción del término que habitualmente es terreno de superposición: a.- una nueva palabra, un neologismo 1971 por Van Rensselaer Potter “Bioethics: bridge to the future”: “...si hay dos culturas que parecen incapaces de hablar una a la otra , (ciencias y humanidades), y si esto es parte de la razón por la que el futuro se muestra tan incierto, entonces posiblemente deberíamos tender un puente hacia el futuro construyendo la disciplina bioética como un puente entre las dos culturas”. b.- una disciplina académica Refleja una nueva área de conocimiento interdisciplinar. c.- un nuevo discurso Reflejo de la conflictiva situación por la que atravesaba la sociedad civil en su relación con el Estado y con la ciencia. 13 La palabra bioética proviene de dos raíces griegas, ambas en crisis: El bios es un bios tecnocientífico, con el temor de que este no se vea reflejado en una mejora en las condiciones y la calidad de vida de los hombres en el planeta: ¿Es posible seguir adelante con el desarrollo de la tecnología o esta terminará con la vida humana en el planeta? El ethos - positivismo científico dominante bajo su modelo de racionalidad valorativamente neutral. - caída de los códigos únicos como referentes válidos para fundar la moralidad de la sociedad. - pérdida de la “legitimidad de obrar conforme a valores” poniendo en en crisis el significado mismo de la validez de la ética. 14 La bioética es una reflexión crítica sobre los conflictos éticos que emergen de la vida y la salud humana. La bioética tiene que enfrentar todos los problemas señalados sin olvidar su contextualización en prácticas político-sociales en las cuales aquellas cuestiones aparecen como conflictos entre diferentes concepciones morales. • polo de universalidad: sin el cual no tiene sentido lo moral. • polo contextual: sin el cuál son vacíos de contenido y referencia las normas. 15 Procedimientos de toma de decisión en Bioética Dos Modelos de Fundamentación Dominantes PRINCIPISMO: - de tipo deductivista: considera que la justificación de los juicios morales se hace en modo descendente a partir de principios y teorías éticas desde los cuales resulta posible llegar a establecer juicios morales sobre casos concretos. CASUÍSTICA: - de tipo inductivista: considera que la justificación de los juicios morales es de tipo ascendente a partir de la experiencia con casos particulares en sus contextos correspondientes y de la moral tradicional y sus juicios que llevan al reconocimiento de principios generales y teorías éticas. 16 El método casuístico. Albert Jonsen y Sthepen Toulmin: The abuse of casuistry (1988) Rechazan la posibilidad de una ética de carácter universal y valor absoluto. Las características de esta propuesta son: • Las decisiones se hacen caso a caso • las conclusiones son provisionales, atendiendo a la aparición de nuevas circunstancias que ayuden a matizar las opciones anteriores •enfoque no deductivista, sino analógico. Se recurre a máximas y valores generales que hay que ir comprendiendo al intentar estudiarlos y aplicarlos caso por caso •taxonomía de casos, según sus semejanzas y diferencias 17 Las decisiones se hacen caso a caso y las circunstancias deben ser tomadas en cuenta. cuenta ¿Qué condicionantes? - De la personalidad y de la psicología del paciente y que tienen que ver con su edad, grado de cultura, psicología y salud psíquica y mental; ¿quién? -De la naturaleza misma de la acción objeto de la evaluación: su dificultad, su complejidad, el temor que inspira en el sujeto, su novedad (el ¿qué?). Por ejemplo, una cosa es que una madre acepte una maternidad que se presenta como normal, y otra aceptarla cuando el feto se presenta n alguna discapacidad o cuando el embarazo implica riesgos para la vida misma e la madre. - Las circunstancias de lugar y de ambiente cultural tienen también su peso, por ejemplo el dar muerte a alguien por cuestión de honor en ciertos países (el dónde?). - Gran peso se le atribuye a la intencionalidad (el ¿por qué?) o motivación: ocurre con frecuencia que una acción concebida con un fin bueno provoca un daño real, y por tanto un mal objetivo. La eutanasia, por ejemplo, se configura hoy muy a menudo como un "acto piadoso”. - Otras circunstancias aluden también la experiencia y la literatura que tratan sobre el te-ma, como las que se refieren a la modalidad (el ¿cómo?) y a las circunstancias de tiempo (el ¿cuándo?). 18 El método principialista. Tom Beauchamp y James Childress, Principles of Biomedical (1979) Valor absoluto de la persona. El ser humano tiene dignidad, y no precio. Cuatro Principios: • Respeto a las Personas / Autonomía (Respetar el derecho inalienable de todo ser humano para decidir por sí, para sí y sobre sí mismo) • Beneficencia: hacer el bien • No maleficencia: no dañar • Justicia: reparto equitativo de cargas y beneficios evitando la discriminación 19 z Principio de autonomía o de libertad de decisión Se puede definir como la obligación de respetar los valores y opciones personales de cada individuo en aquellas decisiones básicas que le atañen vitalmente. Significa 4 cosas: z tratar a las personas como seres autónomos : acción autónoma no debe ser forzada, se decide por sí mismo que hacer: Se define “persona autónoma” como el individuo capaz de deliberar sobre sus objetivos personales y actuar bajo la dirección de esta deliberación z la libertad de decidir implica también tener opciones reales. z Se debe poseerse la información relevante. z los sujetos con autonomía disminuida debe ser objeto de protección. “sujetos vulnerables” * Restricción de la libertad o de autonomía: cuando se carece de capacidad cognitiva y emocional para tomar decisiones racionales. No implica propiamente violación de la autonomía. # “Paternalismo” * Consentimiento o Rechazo Informado * Veracidad * Confidencialidad 20 Principio de no maleficencia y Principio de beneficencia obligación de hacer el bien. El problema es que hasta hace poco, el médico podía imponer su propia manera de hacer el bien sin contar con el consentimiento del paciente (modelo paternalista). Por lo tanto, actualmente este principio viene matizado por el respeto a la autonomía del paciente, a sus valores, cosmovisiones y deseos. No es lícito imponer a otro nuestra propia idea del bien. z no hacer daño al paciente. Se trata de respetar la integridad física y psicológica de la vida humana. Es relevante ante el avance de la ciencia y la tecnología, porque muchas técnicas pueden acarrear daños o riesgos. En la evaluación del equilibrio entre daños-beneficios, se puede cometer la falacia de creer que ambas magnitudes son equivalentes o reducibles a análisis cuantitativo. z El principio positivo de beneficencia no es tan fuerte como el negativo de evitar hacer daño. No se puede buscar hacer un bien a costa de originar daños: por ejemplo, el "bien" de la experimentación en humanos (para hacer avanzar la medicina) no se puede hacer sin contar con el consentimiento de los sujetos, y menos sometiéndolos a riesgos desmedidos o infligiéndoles daños. 21 Principio de justicia z Consiste en el reparto equitativo (distribución justa) de cargas y beneficios en el ámbito del bienestar vital, evitando la discriminación en el acceso a los recursos sanitarios. Este principio impone límites al de autonomía, ya que pretende que la autonomía de cada individuo no atente a la vida, libertad y demás derechos básicos de las otras personas. Cuando a un paciente se le niega sin buenas razones un benéfico se comete una injusticia. ¿cuáles podrán ser las diferencias en el trato? Edad, experiencia, competencia, condición física. ¿cuáles diferencias son legítimas y cuáles no? Nuestra cultura ha sido más sensible al principio de autonomía, a costa del principio de justicia, pero es posible que la misma crisis ecológica nos obligue a cambiar este énfasis. La justicia e igualdad de los derechos de los seres humanos actuales y la preservación de condiciones viables y sostenibles para las generaciones futuras pueden hacer aconsejable, e incluso obligatoria, una cierta limitación del principio de autonomía, sobre todo en una sociedad de mercado que espolea el deseo desmedido de nuevos servicios y bienes, y en la que el individuo atomizado reclama ilimitadamente "derechos" de modo narcisista z 22 CRÍTICAS A LA CASUÍSTICA Lo que determina la tradición ¿puede por ello quedar legitimado como lo que debe hacerse? AL PRINCIPISMO Es insuficiente para el análisis contextual de ciertas realidades sociales complejas, en particular las latinoamericanas. Deja de lado los conflictos relacionados a la injusticia, la inequidad y la pobreza, se debe tomar en primer lugar en cuenta cuales son los derechos que en cada sociedad están siendo vulnerados. 23 Necesidad de redefinir el campo de estudio de la bioética en un análisis de la realidad política, económica, social y cultural de la región, que apunte a la construcción de un nuevo discurso, cuyos presupuestos serían los siguientes: • Que el mundo de hoy está regido por condiciones de desigualdad global, y por una distribución mundial y local de la riqueza injusta, no equitativa, y excluyente de grandes grupos sociales y • Que los problemas éticos que golpean la conciencia moral de la humanidad son principalmente la pobreza, la guerra y la violencia, el hambre y la exclusión de los bienes básicos de un importante porcentaje de la humanidad. 24 Toda toma de decisión ética envuelve un momento de universalidad y un momento de particularidad que son imprescindibles: - Porque si se anula el polo universal de confrontación con la validez racional universal la decisión pierde moralidad y queda a expensan de cualquier contingencia o interés subjetivo. Evitar la “relativización”: El problema es que si no hay “razones”, lo que decide es el juego de fuerzas y la balanza se inclina siempre en esos casos del lado del más poderoso. - Y si se anula la consideración de las circunstancias, la decisión se vacía de contenido real y muchas veces, con el paradójico resultado de no ser justa. Evitar la imposición de contenidos. 25 Proceso deliberativo que abarca un conjunto de pasos 1. Identificar conflictos morales. 2. Priorizar valores y/o principios en conflicto. 3. Optar. 4. Justificar la opción. Que a su vez permite: a.- Evitar el decisionismo, el reduccionismo y la improvisación. b.- Dar razón argumentativamente de las decisiones, lo que supone un uso público de la razón. c- Apostar a una racionalidad ética (ni soberbia ante demás saberes ni sumisa a la política, economía o la ciencia) y no estratégica • MODELO FUNDADO EN LOS DERECHOS HUMANOS. 26 ¿POR QUÉ FUNDADO EN LOS DERECHOS HUMANOS? 1. Es la constitución histórica que mejor da cuenta de un núcleo ético innegable de derechos humanos positivos y negativos. 2. Es una conquista histórica ganada en la lucha por el reconocimiento: universalidad ganada y no dada. 3. Es un proceso inacabado y abierto, deberá medirse en el terreno del diálogo crítico y confrontarse con culturas diferentes. Se distancia del modelo de principios. Permite abordar los problemas éticos en el contexto más amplio de las violaciones sistemáticas a otros derechos básicos como alimentación, seguridad social, vivienda que inciden en la salud de las personas y las poblaciones. No establece rango entre ellos, de modo que no puede aducirse que el cumplimiento de uno justifica actuar en detrimento del otro. 27 Problemas del modelo basado en DDHH: z Su naturaleza; son derechos morales o jurídicos. z Su fundamento filosófico; su capacidad de consenso en un debate abierto. z El debate en curso sobre universalismo o relativismo. 28 Taller: Modelos de Fundamentación en Bioética. La investigación con seres humanos. Análisis de un caso. Estudio de Willowbrook State School [1] La Escuela Estatal Willowbrook era una institució institución para chicos retrasados de Staten Island, Island, Nueva York. York. El nú número de sus residentes aumentó aumentó de 200, en 1949, a má más de 6000 en 1963. Se informó informó de casos de hepatitis entre los niñ niños, por primera vez, en 1949, y en 1954 el Dr. Saul Krugman y sus colegas, incluyendo a la Dra. Joan Giles y al Dr. Jack Hammond, Hammond, prestigiosos pediatras de reconocimiento internacional, empezaron empezaron a estudiar la enfermedad en la institució institución. De los 5200 residentes de Willowbrook durante una parte del estudio, 3800 eran retrasados mentales profundos, profundos, con coeficientes intelectuales de menos de 20. Ademá Además, al menos 3000 de los chicos no controlaban esfí esfínteres. Dado que la hepatitis infecciosa (tipo A) se transmite por ví niños susceptibles eran constantemente admitidos en la vía fecalfecal-oral, y dado que los niñ institució institución, la hepatitis contagiosa era permanente y endé endémica. Tal como el mismo Krugman describe la situació situación en 1971: “la hepatitis ví vírica era tan prevalente que los niñ niños susceptibles admitidos recientemente se infectaban en 6 a 12 meses despué después de entrar en la institució institución. Estos niñ niños eran una fuente de infecció infección para el personal que les atendí atendía y para las familias que les visitaban. Está Estábamos convencidos de que la solució solución del problema de la hepatitis en esta institució institución dependí dependía de adquirir conocimientos que llevaran al desarrollo de un agente agente inmunizador efectivo. Los logros con la viruela, la difteria, la poliomielitis y, má más recientemente, con el sarampió sarampión, proporcionaban elocuentes ilustraciones de este planteamiento” planteamiento”. Objetivo: Obtener conocimientos respecto al curso natural de la enfermedad (hepatitis) y su perí período de infectividad. infectividad. Método: Fueron incluidos un total de 750 niñ niños de la institució institución en un perí período de tiempo de casi 10 añ años. Se realizaron 5 estudios. Se incluyeron niñ ñ os entre 3 y 7 añ ñ os recié é n ingresados a la institució ó n. ni a reci instituci Fueron ingresados en una sala especial (unidad de hepatitis) donde donde recibí recibían una atenció atención especial y estaban especialmente protegidos del contagio de otras infecciones (shigelosis (shigelosis,, sarampió sarampión, etc.). Contaban con atenció atención especial de mé médicos y enfermeras. Los niñ niños fueron agrupados en cada uno de los estudios. Un grupo recibió recibió un preparado por ví vía oral que habí había sido elaborado a partir de la materia fecal de niñ niños infectados. A otro grupo se le inoculaba por ví vía intramuscular un preparado elaborado con suero de pacientes infectados con hepatitis. El diagnostico se realizó realizó con criterios clí clínicos y de laboratorio (serologí (serologías). Fueron registrados distintos hallazgos clí clínicos y de laboratorio. Y se realizó realizó un seguimiento pormenorizado de los pacientes, sus complicaciones complicaciones y su evolució evolución. [1] Material tomado de: http://www.redbioeticahttp://www.redbioetica-edu.com.ar 29 Consentimiento Informado: El CI fue solicitado inicialmente a los padres a través de una carta donde se les aportaba la información para ingresar al estudio. En una segunda etapa la información se suministraba en grupos de padres para que pudieran discutir y preguntar respecto a los aspectos que no estuvieran claros. La institución estaba sobre pasada de ingresos y en algunos casos se le negó lugar a padres por esta razón, posteriormente algunos de ellos recibieron una carta explicándoles que contaban con lugar para la internación de su hijo, pero solo en la Unidad de hepatitis, donde se desarrollaba la investigación. El trabajo contaba con la aprobación del Comité Universitario de Experimentación Humana, por el Departamento de Higiene mental del Estado de Nueva York y el Comité de Epidemiología de la Fuerzas Armadas y el Comando de Investigación Medica y desarrollo de las Fuerzas Armadas. De igual modo los investigadores afirmaron que obraron de acuerdo al código de ética de la Asociación Médica Mundial sobre Experimentación en Humanos (1956). La investigación se desarrolló entre mediados de los 50 y 1972. Justificación: Krugman fundamentó el estudio de la siguiente manera: “Es bien sabido que la hepatitis vírica en los niños es más leve y benigna que la misma enfermedad en los adultos. La experiencia ha revelado que la hepatitis en niños retrasados mentales institucionalizados es también leve, en contraste con el sarampión, que se convierte en una enfermedad más grave cuando ocurre en epidemias institucionales que afectan a retrasados mentales. Nuestra intención de exponer a un pequeño número de los niños admitidos recientemente (finalmente fueron implicados en total 750 a 800 niños) a cepas del virus de la hepatitis de Willowbrook, estaba justificada en nuestra opinión por las siguientes razones: 1) iban a exponerse inevitablemente a las mismas cepas en las condiciones naturales existentes en la institución; 2) se les admitiría en una unidad especial, bien equipada y con personal competente, donde serían aislados de la exposición a otras enfermedades infecciosas, prevalentes en la institución, es decir, shigellosis, parasitosis e infecciones respiratorias, por tanto su exposición en la unidad de hepatitis estaría asociada con menor riesgo que el tipo de exposición institucional en la que podían adquirirse múltiples infecciones; 3) probablemente iban a tener una infección subclínica seguida de una inmunidad para ese virus de la hepatitis; y 4) sólo se incluirían niños cuyos padres dieran su consentimiento”. 30 Cuestionario 1) ¿Considera que el riesgo a que se expone a los sujetos (niños) está justificado en función del objetivo del estudio? (palabras claves: objetivos del estudio, riesgo, beneficios del estudio). 2) ¿Considera que habría otra forma de obtener la información que se pretende alcanzar? (palabras claves: procedimiento, método). 3) A su entender la investigación, ¿sólo puede ser realizada en niños? (palabra clave: grupo vulnerable). 4) ¿Considera que el Consentimiento Informado (dado por los padres) es informado y voluntario? 5) Brevemente presente el modelo de justificación del investigador Krugman. 6) ¿Cuáles son las debilidades de este modelo? 31 Apoyo para la reflexión - 1 – * Distinción entre Investigaciones no terapéuticas e Investigaciones terapéuticas[1] Son investigaciones Clínicas, es decir, ocurren en probandos que están enfermos, por lo tanto tienen susceptibilidad aumentada y mayores riesgos de efectos negativos frente a cualquier sustancia que reciban. Se diferencian de las investigaciones no clínicas, porque estas se llevan a cabo en probandos sanos, para los cuales no hay beneficios, pero que están expuestos a riesgos supuestamente sustentables y predecibles en base a los estudios previos Investigaciones terapéuticas: cuando el estudio se relaciona con la enfermedad del paciente/probando Investigaciones no terapéuticas: se realiza en sujetos enfermos pero sobre una afección que no está relacionada con los probandos. 1) Siempre serán con riesgo mínimo. 2) El conocimiento a adquirir debe ser considerado de gran importancia. 3) Habrá un beneficio para los niños en general. 4) No hay otro modo de obtener la información. 5) La investigación no puede realizarse en personas autónomas. [1] Miguel Kottow. Kottow. Conflictos en ética de investigació investigación con seres humanos. Cád. Saú Saúde Pública 2005; 21:86221:862-869. 32 Apoyo para la reflexión - 2 – PAUTAS ÉTICAS INTERNACIONALES PARA LA INVESTIGACIÓN BIOMÉDICA EN SERES HUMANOS Preparadas por el Consejo de Organizaciones Internacionales de las Ciencias Médicas (CIOMS) en colaboración con la Organización Mundial de la Salud. Ginebra 2002 Pauta 8: Beneficios y riesgos de participar en un estudio En toda investigación biomédica en sujetos humanos, el investigador investigador debe garantizar que los beneficios potenciales y los riesgos estén razonablemente balanceados y que los riesgos hayan sido minimizados. · Las intervenciones o procedimientos que incluyan la posibilidad posibilidad de beneficio diagnóstico, terapéutico o preventivo directo para para el sujeto individual, a la luz de los riesgos y beneficios previstos, previstos, deben justificarse por la expectativa de que serán, al menos, tan ventajosas para él como cualquier otra alternativa disponible. disponible. Los riesgos de tales intervenciones o procedimientos ‘beneficiosos’ deben justificarse en relación con los beneficios esperados para el sujeto individual. · Los riesgos de intervenciones sin posibilidad de beneficio diagnóstico, diagnóstico, terapéutico o preventivo directo para el individuo deben deben justificarse en relación con los beneficios anticipados para la sociedad (conocimiento generalizable). Los riesgos de tales intervenciones deben ser razonables en relación con la importancia importancia del conocimiento que se espera obtener. Pauta 9: Limitaciones especiales del riesgo cuando se investiga en individuos incapaces de dar consentimiento informado Si existe una justificación ética y científica para realizar una investigación con individuos incapaces de dar consentimiento informado, el riesgo de intervenciones propias de la investigación investigación que no proporcionen la posibilidad de beneficio directo para el sujeto individual no debe ser mayor que el riesgo asociado asociado a un examen médico o psicológico de rutina de tales personas. Puede permitirse incrementos leves o menores por encima encima de tal riesgo cuando exista una fundamentación científica o médica superior para tales incrementos y cuando un comité de evaluación ética los haya aprobado. Pauta 13: Investigación en que participan personas vulnerables Se requiere una justificación especial para invitar a individuos vulnerables a participar como sujetos de investigación. En el caso caso de ser seleccionados, los medios para proteger sus derechos y bienestar bienestar deben ser aplicados estrictamente.[1] Pauta 14: Investigació Investigación en que participan niñ niños Antes de realizar una investigació investigación en la que participará participarán niñ niños, el investigador debe garantizar que: - la investigació investigación no podrí podría ser igualmente bien realizada con adultos; - el propó propósito de la investigació investigación es obtener conocimiento relevante sobre las necesidades de salud salud de los niñ niños; - el padre, madre o representante legal de cada niñ niño ha autorizado su participació participación; - el acuerdo (asentimiento) de cada niñ ñ o se ha obtenido teniendo en cuenta sus capacidades; y ni - la negativa de un niñ niño a participar o continuar en la investigació investigación será será respetada. 33 [1] Comentario sobre la Pauta 13: Son Son personas vulnerables las absoluta o relativamente incapaces de proteger sus propios intereses. Especí Específicamente, pueden tener insuficiente poder, inteligencia, educació educación, recursos, fuerza u otros atributos necesarios para proteger sus sus intereses. , Debate final: * Identifique los diferentes tipos de problemas detectados. Por ejemplo, pueden ser: clínicos, quirúrgicos, sociales, económicos o institucionales, legales y éticos. Preguntarse sobre lo que sucede y sus causas permite ampliar el campo de comprensión de los conflictos que se presentan. Problematizar la realidad significa adoptar una actitud crítica frente a ella y hace presente la necesidad necesidad de transformarla. Róvere define un problema como “una brecha entre una realidad o un aspecto de la realidad observada y un valor o deseo de cómo debe ser esa realidad para un determinado observador, observador, sea individual o colectivo”[1] colectivo”[1].. El problema es una construcció construcción subjetiva que realizan individuos frente a la realidad. Tipos de Problemas: Médicos: dicos: por ejemplo una duda en el diagnó diagnóstico o el pronó pronóstico realizado por los mé médicos tratantes que pueda modificar lo que se recomiende. Sociales: Sociales: cuando algú algún factor de la vida social del paciente determina su conducta. Por Por ejemplo, no se puede dar de alta a un paciente porque no tiene tiene a donde ir, a pesar de estar bien de salud. Institucionales: Institucionales: cuando las relaciones de poder o de sectores juegan un papel en en el aná análisis que estamos haciendo, por ejemplo existe un conflicto entre entre dos servicios que afecta el bienestar de un paciente. Éticos: aquellos en los que se pone de manifiesto una confrontació confrontación entre valores, derechos o principios en un acto, en un curso de de acció acción determinado o en un juicio moral sobre una conducta dada. Ellos pueden estar representados representados por una o por varias personas, por instituciones, o tal vez vez por la sociedad o el estado a travé través de sus normas. * Elija un problema ético e identifique los intereses en juego y quienes los representan, enuncie los conflictos existentes. * Detecte qué valores, principios y derechos se encuentran comprometidos en el problema seleccionado. ¿Existen conflictos entre estos valores, principios o derechos? * Establezca los cursos de acción posible y opte por uno de ellos. Justifique y argumente su decisión. * Prepare un breve informe para la defensa pública: esto quiere decir que usted está en condiciones de responder preguntas y posiciones contrarias a su decisión. [1] Mario Róvere. vere. Planificació Planificación Estraté Estratégica de Recursos Humanos en Salud. Serie Desarrollo de Recursos Humanos Nro. Nro. 96. O.P.S. O.P.S. 1993, pp. 7979-91. 34 Apoyo para el Debate * Pautas para el debate en el grupo[1] Cuando se realiza una deliberación entre varias personas sobre un tema de debate bioético se establece una situación que podríamos llamar situación dialógica. Para que el diálogo sea posible el debate llevado a cabo por el grupo deberá tener algunas reglas que faciliten la comunicación: z z z z z z z z z Todos pueden participar y dar sus opiniones, la participación estará libre de toda discriminación, la relación es de carácter democrático. Intenten respetar la exposición de cada uno (no interrumpir a los demás cuando hablan). Toda afirmación es susceptible de ser cuestionada (no hay dogmas). Cualquier proposición puede ser introducida al debate, para ello se deberán presentar razones, (justificación). No sostenga posiciones que no puedan ser defendidas con argumentos. Trate de no emplear las expresiones “porque sí”, “porque me parece”, “es así”. Intente un ejercicio de argumentación: a todo pregúntese por qué. Cada participante puede expresar sus deseos, necesidades y puntos de vista sin ningún tipo de prejuicios. Todos los participantes deberían ser tolerantes con las posiciones de los demás, aunque no estén de acuerdo. Evite dispersarse en temas derivados. Los relatos de experiencias deben tratar de limitarse a aquellos que enriquezcan la discusión. Intente encontrar puntos de acuerdo con los demás, no de confrontación. El grupo debe tratar de llegar a un consenso. De otro modo presentará dos mociones (en la presentación del caso). [1] Material Elaborado a partir de Dra. Susana Vidal: Instrumento para el seguimiento del Proceso Educativo de Comité Comités Hospitalarios de www.redbioetica--edu.com.ar Bioé http://www.redbioetica Bioética. http:// 35 DECLARACION DE HELSINKI DE LA ASOCIACION MEDICA MUNDIAL Principios éticos para las investigaciones médicas en seres humanos Adoptada por la 18ª Asamblea Médica Mundial Helsinki, Finlandia, Junio 1964 y enmendada por la 29ª Asamblea Médica Mundial Tokio, Japón, Octubre 1975 - 35ª Asamblea Médica Mundial Venecia, Italia, Octubre 1983 - 41ª Asamblea Médica Mundial Hong Kong, Kong, Septiembre 1989 - 48ª Asamblea General Somerset West, West, Sudáfrica, Octubre 1996 y la 52ª Asamblea General Edimburgo, Escocia, Octubre 2000 - Nota de Clarificación del Párrafo 29, agregada por la Asamblea General de la AMM, Washington 2002 - Nota de Clarificación del Párrafo 30, agregada por la Asamblea General de la AMM, Tokio 2004 A- INTRODUCCION 1. 2. 3. 4. 5. 6. 7. 8. 9. La Asociación Médica Mundial ha promulgado la Declaración de Helsinki Helsinki como una propuesta de principios éticos que sirvan para orientar a los médicos y a otras personas que realizan realizan investigación médica en seres humanos. La investigación médica en seres humanos incluye la investigación del del material humano o de información identificables. El deber del médico es promover y velar por la salud de las personas. personas. Los conocimientos y la conciencia del médico han de subordinarse al cumplimiento de ese deber. La Declaración de Ginebra de la Asociación Médica Mundial vincula vincula al médico con la fórmula "velar solícitamente y ante todo por la salud de mi paciente", y el Código Internacional de Ética Médica afirma que: "El médico debe actuar solamente en el interés del paciente al proporcionar atención médica médica que pueda tener el efecto de debilitar la condición mental y física del paciente". El progreso de la medicina se basa en la investigación, la cual, en último término, tiene que recurrir muchas veces a la experimentación en seres humanos. En investigación médica en seres humanos, la preocupación por el bienestar de los seres humanos debe tener siempre primacía sobre los intereses de la ciencia y de la sociedad. El propósito principal de la investigación médica en seres humanos humanos es mejorar los procedimientos preventivos, diagnósticos y terapéuticos, y también comprender la etiología y patogenia de las enfermedades. Incluso, los mejores métodos preventivos, diagnósticos y terapéuticos disponibles deben deben ponerse a prueba continuamente a través de la investigación para que sean eficaces, efectivos, accesibles y de calidad. En la práctica de la medicina y de la investigación médica del presente, presente, la mayoría de los procedimientos preventivos, diagnósticos y terapéuticos implican algunos riesgos y costos. La investigación médica está sujeta a normas éticas que sirven para para promover el respeto a todos los seres humanos y para proteger su salud y sus derechos individuales. Algunas poblaciones poblaciones sometidas a la investigación son vulnerables y necesitan protección especial. Se deben reconocer las necesidades necesidades particulares de los que tienen desventajas económicas y médicas. También se debe prestar atención especial a los que no pueden otorgar o rechazar el consentimiento por sí mismos, a los que pueden otorgar el consentimiento consentimiento bajo presión, a los que no se beneficiarán personalmente con la investigación y a los que tienen la investigación investigación combinada con la atención médica. Los investigadores deben conocer los requisitos éticos, legales y jurídicos para la investigación en seres humanos en sus propios países, al igual que los requisitos internacionales vigentes. vigentes. No se debe permitir que un requisito ético, legal o jurídico disminuya o elimine cualquiera medida de protección para para los seres humanos establecida en esta Declaración. 36 B- PRINCIPIOS BASICOS PARA TODA INVESTIGACION MEDICA 1010- En la investigación médica, es deber del médico proteger la vida, vida, la salud, la intimidad y la dignidad del ser humano. 1111- La investigación médica en seres humanos debe conformarse con los los principios científicos generalmente aceptados, y debe apoyarse en un profundo conocimiento de la bibliografía bibliografía científica, en otras fuentes de información pertinentes, así como en experimentos de laboratorio correctamente realizados y en animales, cuando sea oportuno. 1212- Al investigar, hay que prestar atención adecuada a los factores que puedan perjudicar el medio ambiente. Se debe cuidar también del bienestar de los animales utilizados en los experimentos. 1313- El proyecto y el método de todo procedimiento experimental en seres seres humanos debe formularse claramente en un protocolo experimental. Este debe enviarse, para consideración, consideración, comentario, consejo, y cuando sea oportuno, aprobación, a un comité de evaluación ética especialmente especialmente designado, que debe ser independiente del investigador, del patrocinador o de cualquier otro tipo de influencia indebida. Se sobreentiende que ese comité independiente debe actuar en conformidad conformidad con las leyes y reglamentos vigentes en el país donde se realiza la investigación experimental. experimental. El comité tiene el derecho de controlar los ensayos en curso. El investigador tiene la obligación de proporcionar proporcionar información del control al comité, en especial sobre todo incidente adverso grave. El investigador investigador también debe presentar al comité, para que la revise, la información sobre financiamiento, patrocinadores, afiliaciones institucionales, otros posibles conflictos de interés e incentivos incentivos para las personas del estudio. 14El protocolo de la investigación debe hacer referencia siempre a las consideraciones éticas que fueran del 14 caso, y debe indicar que se han observado los principios enunciados enunciados en esta Declaración. 1515- La investigación médica en seres humanos debe ser llevada a cabo cabo sólo por personas científicamente calificadas y bajo la supervisión de un médico clínicamente competente. competente. La responsabilidad de los seres humanos debe recaer siempre en una persona con capacitación médica, médica, y nunca en los participantes en la investigación, aunque hayan otorgado su consentimiento. 1616- Todo proyecto de investigación médica en seres humanos debe ser precedido de una cuidadosa comparación de los riesgos calculados con los beneficios previsibles para el individuo o para otros. Esto no impide la participación de voluntarios sanos en la investigación médica. El El diseño de todos los estudios debe estar disponible para el público. 1717- Los médicos deben abstenerse de participar en proyectos de investigación investigación en seres humanos a menos de que estén seguros de que los riesgos inherentes han sido adecuadamente adecuadamente evaluados y de que es posible hacerles frente de manera satisfactoria. Deben suspender el experimento experimento en marcha si observan que los riesgos que implican son más importantes que los beneficios esperados esperados o si existen pruebas concluyentes de resultados positivos o beneficiosos. 1818- La investigación médica en seres humanos sólo debe realizarse cuando cuando la importancia de su objetivo es mayor que el riesgo inherente y los costos para el individuo. Esto Esto es especialmente importante cuando los seres humanos son voluntarios sanos. 37 1919- La investigación médica sólo se justifica si existen posibilidades posibilidades razonables de que la población, sobre la que la investigación se realiza, podrá beneficiarse de sus resultados. 2020- Para tomar parte en un proyecto de investigación, los individuos individuos deben ser participantes voluntarios e informados. 21Siempre debe respetarse el derecho de los participantes en la investigación 21 investigación a proteger su integridad. Deben tomarse toda clase de precauciones para resguardar la intimidad de los individuos, la confidencialidad de la información del paciente y para reducir al mínimo las consecuencias consecuencias de la investigación sobre su integridad física y mental y su personalidad. 2222- En toda investigación en seres humanos, cada individuo potencial potencial debe recibir información adecuada acerca de los objetivos, métodos, fuentes de financiamiento, posibles conflictos conflictos de intereses, afiliaciones institucionales del investigador, beneficios calculados, riesgos previsibles e incomodidades incomodidades derivadas del experimento. La persona debe ser informada del derecho de participar o no en la investigación investigación y de retirar su consentimiento en cualquier momento, sin exponerse a represalias. Después de asegurarse asegurarse de que el individuo ha comprendido la información, el médico debe obtener entonces, preferiblemente por por escrito, el consentimiento informado y voluntario de la persona. Si el consentimiento no se puede obtener obtener por escrito, el proceso para lograrlo debe ser documentado y atestiguado formalmente. 23Al obtener el consentimiento informado para el proyecto de investigación, 23 investigación, el médico debe poner especial cuidado cuando el individuo está vinculado con él por una relación de dependencia dependencia o si consiente bajo presión. En un caso así, el consentimiento informado debe ser obtenido por un médico médico bien informado que no participe en la investigación y que nada tenga que ver con aquella relación. 2424- Cuando la persona sea legalmente incapaz, o inhábil física o mentalmente mentalmente de otorgar consentimiento, o menor de edad, el investigador debe obtener el consentimiento informado del del representante legal y de acuerdo con la ley vigente. Estos grupos no deben ser incluidos en la investigación a menos que ésta sea necesaria para promover la salud de la población representada y esta investigación no pueda pueda realizarse en personas legalmente capaces. 2525- Si una persona considerada incompetente por la ley, como es el caso de un menor de edad, es capaz de dar su asentimiento a participar o no en la investigación, el investigador investigador debe obtenerlo, además del consentimiento del representante legal. 2626- La investigación en individuos de los que no se puede obtener consentimiento, consentimiento, incluso por representante o con anterioridad, se debe realizar sólo si la condición física/mental física/mental que impide obtener el consentimiento informado es una característica necesaria de la población investigada. Las razones específicas por las que se utilizan participantes en la investigación que no pueden otorgar su consentimiento consentimiento informado deben ser estipuladas en el protocolo experimental que se presenta para consideración y aprobación aprobación del comité de evaluación. El protocolo debe establecer que el consentimiento para mantenerse en la investigación debe obtenerse a la brevedad posible del individuo o de un representante legal. 2727- Tanto los autores como los editores tienen obligaciones éticas. Al publicar los resultados de su investigación, el investigador está obligado a mantener la exactitud de los datos y resultados. Se deben publicar tanto los resultados negativos como los positivos o de lo contrario deben estar a la disposición del público. En la publicación se debe citar la fuente de financiamiento, afiliaciones afiliaciones institucionales y cualquier posible conflicto de intereses. Los informes sobre investigaciones que no se ciñan a los principios descritos en esta Declaración no deben ser aceptados para su publicación. 38 C- PRINCIPIOS APLICABLES CUANDO LA INVESTIGACION MEDICA SE COMBINA CON LA ATENCION MEDICA 2828- El médico puede combinar la investigación médica con la atención atención médica, sólo en la medida en que tal investigación acredite un justificado valor potencial preventivo, preventivo, diagnóstico o terapéutico. Cuando la investigación médica se combina con la atención médica, las normas normas adicionales se aplican para proteger a los pacientes que participan en la investigación. 2929- Los posibles beneficios, riesgos, costos y eficacia de todo procedimiento procedimiento nuevo deben ser evaluados mediante su comparación con los mejores métodos preventivos, diagnósticos y terapéuticos existentes. Ello no excluye que pueda usarse un placebo, o ningún tratamiento, en estudios estudios para los que no hay procedimientos preventivos, diagnósticos o terapéuticos probados. probados. A fin de aclarar más la posición de la AMM sobre el uso de ensayos ensayos controlados con placebo, la AMM publicó en octubre de 2001 una nota de clarificación del párrafo 29 3030- Al final de la investigación, todos los pacientes que participan participan en el estudio deben tener la certeza de que contarán con los mejores métodos preventivos, diagnósticos y terapéuticos terapéuticos probados y existentes, identificados por el estudio. 3131- El médico debe informar cabalmente al paciente los aspectos de la atención que tienen relación con la investigación. La negativa del paciente a participar en una investigación investigación nunca debe perturbar la relación médicomédico-paciente. 3232- Cuando en la atención de un enfermo los métodos preventivos, diagnósticos diagnósticos o terapéuticos probados han resultado ineficaces o no existen, el médico, con el consentimiento consentimiento informado del paciente, puede permitirse usar procedimientos preventivos, diagnósticos y terapéuticos terapéuticos nuevos o no comprobados, si, a su juicio, ello da alguna esperanza de salvar la vida, restituir la salud o aliviar el sufrimiento. Siempre que sea posible, tales medidas deben ser investigadas a fin de evaluar su su seguridad y eficacia. En todos los casos, esa información nueva debe ser registrada y, cuando sea oportuno, oportuno, publicada. Se deben seguir todas las otras normas pertinentes de esta Declaración. Nota de Clarificación del Párrafo 29 de la Declaración de Helsinki Helsinki La AMM reafirma que se debe tener muchísimo cuidado al utilizar ensayos con placebo y, en general, esta metodología sólo se debe emplear si no se cuenta con una terapia probada y existente. Sin embargo, los ensayos con placebo son aceptables éticamente en ciertos casos, incluso si se dispone de una terapia probada y si se cumplen las siguientes condiciones: - Cuando por razones metodológicas, científicas y apremiantes, su uso es necesario para determinar la eficacia y la seguridad de un método preventivo, diagnóstico o terapéutico o - Cuando se prueba un método preventivo, diagnóstico o terapéutico terapéutico para una enfermedad de menos importancia que no implique un riesgo riesgo adicional, efectos adversos graves o daño irreversible para los pacientes que reciben el placebo. Se deben seguir todas las otras disposiciones de la Declaración de Helsinki, en especial la necesidad de una revisión científica y ética apropiada. z Nota de Clarificación del Párrafo 30 de la Declaración de Helsinki Helsinki Por la presente, la AMM reafirma su posición de que es necesario durante el proceso de planificación del estudio identificar el acceso después del ensayo de los participantes en el estudio a procedimientos preventivos, preventivos, diagnósticos y terapéuticos que han resultado beneficiosos beneficiosos en el estudio o el acceso a otra atención apropiada. Los arreglos para para el acceso después del ensayo u otra atención deben ser descritos descritos en el protocolo del estudio, de manera que el comité de revisión ética ética pueda considerar dichos arreglos durante su revisión. z 39 Bibliografía: •Beauchamp, Tom L.; Childress, James F. Principles of Biomedical Ethics, New York, Oxford University Press, (1979), 1a.ed. (Trad.esp. de la 4ª edición, Principios de Etica Biomédica. Barcelona, Masson, 1999). •Boladeras, Margarita: Bioética, Ed. Síntesis, Madrid. 1999. •Brussino, S.: Bioética, deliberación y juicio razonable. En Luis G. Blanco (Comp.): “Bioética y Bioderecho. Cuestiones actuales”. Ed. Universidad, Buenos Aires, pp. 21-47, 2002 •Brussino, S.: Bioética, racionalidad y principio de realidad. Cuadernos de Bioética 0 (1996): 39-48. Argentina. http://cuadernos.bioetica.org/doctrina7.htm •Cechheto, S.: La Bioética como nuevo movimiento social. Quirón, (1996), 27 (1): 96-102. •Guariglia, O; Cuestiones Morales. Trotta, Madrid, 1996. •Habermas, J: Tres modelos normativos de Democracia (1992) en “La inclusión del otro. Estudios de Teoría Política”, Paidós, Barcelona, 1999. •Habermas, J: El futuro de la naturaleza humana. ¿Hacia una eugenesia libera? Paidós, Barcelona 2002. •Harris, H. Superman y la Mujer Maravilosa. Las dimensiones éticas de la biotecnología humana. Tecnos, , Madrid, 1998. •Informe Belmont: http://www.ecu.edu/irb/docs/Belmont%20Report_Spanish.pdf •Justo, Erazun, Villareal: La investigación participativa como derecho:¿posibilidad o utopía? Perspectivas Metodológicas, Vol. 4, 73-82, (2004). •Justo, Luis: Prioridades en investigación. Reflexiones desde América Latina. Presentación en la Conferencia sobre Investigaciones en Poblaciones Vulnerables. Foro Latinoamericano de Comités de Investigación en Salud. México. Setiembre (2004). http://e-ms.cilea.it/view/subjects/A3.html. •Luna, F – Rivera López, E (comp.) ; Los desafíos éticos de la genética humana. •Luna, F – Salles, A; “Bioética”. Introducción y selección de textos”. Ed. Sudamericana. 40 Buenos Aires, 1998. •Luna, F – Salles, A; “Decisiones de vida y muerte”. Introducción y selección de texto. Ed. Sudamericana. Buenos Aires, 2000. •Mª Teresa López de la Vieja: Principios Morales y casos Prácticos: Tecnos, 2000. •Nussbaum, M – Sunstein, C; Clones y Clones, Cátedra, España, 2000. •Pfeiffer M. L.: Educar para Respetar los Derechos, en Pfeiffer (ed) “Bioética. Estrategia de dominación para América Latina, Ed. Suarez, Mar del Plata, (2004). •Potter Van Rensselaer. Bioethics. Bridge to the Future. Prentice-Hall. Englewood Cliffs, New Jersey (1971), véase además Van Rensselaer Potter. Bioética Puente, Bioética Global y Bioética Profunda. Cuadernos del programa Regional de Bioética OPS/OMS, Nro 7, 1998. •Red Bioética de UNESCO: http://www.redbioetica-edu.com.ar. •Rotondo, M.T. Perspectivas Uruguayas para la RedBio. (2003). http://www.smu.org.uy/emc/novedades/be/redbio.pdf •Singer, P. (Ed.), “Compendio de Ética”. Alizana, Madrid, 2005. •Singer, P.. Ética práctica. Gran Bretaña, Cambridge University Press, 1995. •Singer, P; “Una vida ética. Escritos2. Tautus, , España 2002. •Tealdi, J. C.: Bioética y Derechos Humanos en América Latina. Conferencia en Bioética y Derechos Humanos -V Encuentro Nacional de Comités de Etica de la Salud y Reunión Regional de Derecho, Etica y Ciencia; Bio&Sur, Buenos Aires, 5 de octubre de (2001). •Tomás Garrido, G(coord.). Manual de Bioética. Ed. Ariel, España. 2001 (tiene aspectos científicos que sirven para aclarar conceptos) •Vázquez, R; (comp) Bioética y Derecho. Fundamentos y problemas actuales. FCE, , México, 1999 •Vidal, S.: Conflicto de intereses y políticas públicas. Revista Brasilera de Bioética, Vol. 1 (4): 386-400, (2005). •Vidal, S.: Ética o mercado. Una decisión urgente. Lineamientos para el diseño de normas éticas en investigaciones biomédicas en América Latina. En: Keyeux, G; Penchaszadeh, V.; Saada, A. (orgs.). “Investigación en seres humanos y políticas de salud pública”. Bogotá, 41 UNIBIBLOS. Serie “Publicaciones científicas”, Nº 2, (2006b).