REFRIGERANTES Y SU iMPACTO AMBIENTAL
Anuncio

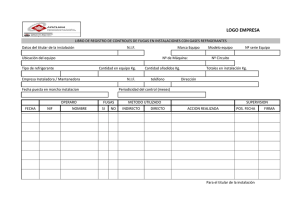
Universidad de Los Andes Facultad de Ciencias Departamento de Química Laboratorio de Organometálicos Refrigerantes y su Impacto Ambiental Por Ricardo R. Contreras 1. Refrigerantes. Un refrigerante es cualquier sustancia capaz de absorber calor de otra, v.gr., hielo, agua, aire, etc. Dado que la refrigeración mecánica se basa en la evaporación y la consiguiente condensación del fluido para absorber y disipar el calor. 1. Refrigerantes. Un refrigerante debe cumplir con: Características físicas para que pueda repetir el ciclo líquido a gas y gas a líquido. Adecuada temperatura y presión de servicio (=> economía, dieño, construcción y operación) Buen efecto refrigerante. 2. Efecto de Refrigeración El efecto de refrigeración de un refrigerante se mide en función de la cantidad de calor que es capaz de absorber desde que entra al evaporador como líquido, hasta que sale como vapor. El efecto de refrigeración se resume como la diferencia entre el calor que contiene el líquido y el calor contenido en el vapor después de pasar por el evaporador. 3. Punto de Ebullición: El punto de ebullición de un refrigerante a la temperatura ambiente es fundamental a la hora escoger el equipo requerido y el tipo de servicio en el cual será utilizado. Clasificación de Refrigerantes por P.F.: Temperaturas ultrabajas: < -65 ºF Temperaturas bajas: -65 ºF a –20 ºF Temperaturas intermedia: -20 ºF a +20 ºF Temperaturas altas: > +20 ºF 4. Coeficiente de Comportamiento: El coeficiente de comportamiento (C.C.) de un refrigerante es la medida de su eficiencia en utilizar la energía gastada en el compresor, en relación con la energía absorbida durante la evaporación. Mientras menos energía necesite el refrigerante para comprimirse, mayor será el C.C. Del sistema. 5. Densidad: Si el refrigerante es de alta densidad, al fluir en las tuberías tendrá mayor fricción y, por tanto, una caída de presión. Por esto, los refrigerantes de baja densidad tiene más ventajas y pueden ser un factor importante a la hora de seleccionarlos. 6. Calor específico del líquido: El efecto refrigerante es igual al calor de evaporación menos el calor perdido en enfriar el líquido desde la temperatura al entrar en el evaporador a la temperatura final. Mientras más pequeño sea el calor específico del refrigerante líquido, mayor será el efecto de refrigeración. 7. Temperatura y Presión Crítica. El refrigerante debe tener una temperatura crítica mayor que la más alta temperatura al salir del compresor. De otra manera la condensación no es posible. La temperatura crítica de la mayoría de los refrigerantes está por encima de la temperatura de condensación. La presión crítica también debe estar por arriba de la presión de condensación. 8. Punto de Congelación. Mientras que la mayoría de los refrigerantes tienen un punto de congelación menor que el punto de congelación del agua (-20 ºF a +10 ºF), cuando se requieren temperaturas extrabajas, se debe tener mucho cuidado al escoger el refrigerante. El punto de congelación de un refrigerante debe ser bastante menor que la más baja temperatura obtenida en el evaporador. 9. Estabilidad Química y Efecto de la Humedad Los refrigerantes deben ser Estables ante continuos cambios de presión y temperatura. Estables a la descomposición por contaminación con Aire, aceite o agua. No deben ser corrosivos. Alguno refrigerantes como el amoníaco reaccionan con la humedad formando el hidróxido de amonio de reacciona con las tuberías de Fe, Cu u aleaciones. 10. Relación Refrigerante – Aceite. Los refrigerantes deben ser químicamente estables en presencia de aceites lubricantes, y no afectar las propiedades fisicoquímicas del lubricante. 11. Otras características Toxicidad Inflamabilidad Detección de fugas Olor Costo y Disponibilidad. 12. Refrigerantes. Clasificación Grupo Refrigerante Fórmula I Amoniaco NH3 II Dióxido de Carbono CO2 III Dióxido de azufre SO2 Etano CH3CH3 Etileno CH2CH2 Propano CH3CH2CH3 Isobutano CH(CH3)3 Butano CH3(CH2)2CH3 IV hidrocarburos 12. Refrigerantes. Clasificación G ru p o F a m ilia H id r o c a r b u r o s C lo r a d o s R e f r ig e r a n t e F ó r m u la C lo r o m e t a n o C H 3C l C lo r o e t a n o C H 3C H 2C l D ic lo r o m e t a n o C H 2C l2 D ic lo r o e t e n o C H C lC H C l 2 T r ic lo r o e t e n o C H C lC C l 2 S e r ie d e m e t a n o s F re ó n 1 1 C C l3F T r ic lo r o m o n o f lu o r o m e ta n o V F re ó n 1 2 H id r o c a r b u r o s F lu o r a d o s C C l2F 2 d ic lo r o f lu o r o m e t a n o F re ó n 1 3 C C lF 3 m o n o c lo r o t r if lu o r o m e t a n o F re ó n 1 4 CF4 t e t r a f lu o r o m e t a n o F re ó n 2 1 C H C l2F d ic lo r o m o n o f lu o r o m e t a n o F re ó n 2 2 m o n o c lo r o d if lu o r o m e t a n o C H C lF 2 12. Refrigerantes. Clasificación G ru p o F a m ilia R e frig e ra n te F ó rm u la S e r ie d e e ta n o s F re ó n 1 1 3 C C l2F C C lF 2 T ric lo ro triflu o ro e ta n o F re ó n 1 1 4 C C lF 2C C lF 2 d ic lo ro te tra flu o ro e ta n o H id r o c a r b u r o s V F lu o r a d o s S e r ie d e lo s B r o m u ro s K u le n e 1 3 1 C B rF 3 B r o m o triflu o ro m e ta n o F re ó n 2 1 C H C l2F d ic lo ro m o n o flu o ro m e ta n o F re ó n 2 2 C H C lF 2 m o n o c lo ro d iflu o ro m e ta n o 7 4 .2 % VI A z e ó tr o p o s C a rre n e 7 F re ó n 1 2 2 5 .8 % d iflu o ro e ta n o V II O tr o s O x id o n itro s o N 2O F o rm a to d e m e tilo HCCOCH3 E tila m in a C H 3C H 2N H 2 M e tila m in a C H 3N H 2 12. Refrigerantes. Clasificación Bióxido de carbono (CO2): Su uso requiere de equipos muy pesados, en virtud de la excesiva presión que se requiere => alto costo. Es inodoros, incoloro. Es difícil detectar fugas No es tóxico, sin embargo en grandes concentraciones causa muerte por sofocamiento. No es inflamable. Es químicamente estable (no es corrosivo). 12. Refrigerantes. Clasificación Anhídrido Sulfuroso (SO2): Incoloro No es inflamable Sus fugas no perjudican los alimentos, al contrario los conservan. Combinado con aceites, produce un lodo que obstruye las tuberías. Es químicamente estable. Es muy tóxico, irrita membranas, mucosas y ojos. 12. Refrigerantes. Clasificación Hidrocarburos Incoloros Muy inflamables y explosivos No son tóxicos, pero si anestésicos No son corrosivos Son miscibles en aceites 13. Refrigerantes Clorofluorados, CFCs ó Freones: Los CFCs, o freones, en un principio los desarrolló Thomas Midgley en la década de 1930 como unos sustitutos estables, no tóxicos y no inflamables del amoníaco gaseoso utilizado hasta el momento en la refrigeración. 13. Refrigerantes Clorofluorados, CFCs ó Freones: No son tóxicos, ni irritantes, o inflamables. En condiciones normales, no son corrosivos. Son incoloros, inodoros Son Químicamente estables. No afectan a los lubricantes ni son afectados ellos, aunque sean más o menos miscibles. Mientras mayor sea el número hidrógenos, más inflamables serán. Tienen buenas cualidades térmicas. de 13. Refrigerantes Clorofluorados, CFCs ó Freones: Cl Cl CFCs Cl Cl F Cl F F R-11 Cl F R-13 F F F R-22 R-23 H F F R-134a R-134a Cl R-14 Cl F F F R-113 R-114 R-114 Cl F F H F R-31 Cl F Cl R-114 R-113 R-113 H H F F H H F F F F F H Cl R-21 F F F H F Cl R-12 Cl HCFs F Cl H H H Cl 40 H H F R-41 13. Refrigerantes CFCs, Halones y otros: R e frig e ra n te N o m b re Q u ím ic o F ó rm u la G ru p o 1 C F C -1 1 T ric lo ro flu o ro m e ta n o C C l3F C F C -1 2 D ic lo ro d iflu o ro m e ta n o C C l2F 2 G ru p o 2 H a lo n 1 2 1 1 B ro m o c lo ro d iflu o ro m e ta n o C F 2 C lB r H a lo n 1 3 0 1 B ro m o triflu o ro m e ta n o C F 3B r H a lo n 2 4 0 2 D ib ro m o te tra flu o ro e ta n o C 2F 4B r2 G ru p o 3 C F C -1 1 3 1 ,1 ,2 -T ric lo ro triflu o ro e ta n o C 2F 3C l3 C F C -2 1 1 H e p ta c lo ro flu o ro p ro p a n o C 3F C l7 C F C -2 1 7 C lo ro h e p ta flu o ro p ro p a n o C 3F 7C l G ru p o 4 T e tra c lo ru ro d e c a rb o n o te tra c lo ro m e ta n o C C l4 G ru p o 5 M e til C lo ro fo rm o 1 ,1 ,1 -tric h lo ro e th a n o C 2H 3C l3 G ru p o 6 M e til B ro m u ro B ro m o m e ta n o C H 3B r 13. Refrigerantes Clorofluorados, CFCs ó Freones Un gas refrigerante se comprime a líquido normalmente por un motor eléctrico y entonces circula por una espiral metálica de pequeño diámetro arrollada alrededor del espacio a ser enfriado Cuando se le permite al líquido expandirse a gas de nuevo, absorbe calor y enfría ese espacio. 13. Refrigerantes Clorofluorados, CFCs ó Freones El papel de los CFCs se ha extendido mucho en los últimos sesenta años. Además de su continua utilización en los frigoríficos y en los aparatos de aire acondicionado, se ha empleado también como: Solventes. Propelentes de aerosoles para productos tales como laca del pelo y desodorantes. Agentes espumantes para aislamiento en la industria de la construcción y embalajes para alimentos precocidos. 13. Refrigerantes Clorofluorados, CFCs ó Freones Los CFCs más comunes y más utilizados son el Freón-11 CFCl3 y el Freón-12, ambos se producen por la acción del fluoruro de hidrógeno sobre tetracloruro de carbono como se representa en la ecuación: Cl Cl Cl Cl + HF Cl 100 ºC [SbF 5 ] Cl Cl F + HCl 13. Refrigerantes Clorofluorados, CFCs ó Freones La cloración de metano produce una mezcla compleja de los productos, mono-, di-, tri- y tetraclorados que pueden ser separados por destilación. Los metanos clorados sirven de punto de partida en la síntesis industrial de los CFs y HCFs : H H Cl2 H H H Cl H Cl2 H H Cl H Cl2 H Cl Cl Cl Cl2 Cl Cl + HCl + HCl + HCl Cloruro de metilo Cloruro de metileno Cloroformo Cl Cl Cl + HCl Tetracloruro de carbono 13. Refrigerantes Clorofluorados, CFCs ó Freones La investigación desarrollada en el campo de los refrigerantes ha llevado a obtener otros tipos de compuestos como los HCFCs, compuestos parcialmente halogenados como el Refrigerante-22 CHClF2 o los HFC compuestos parcialmente halogenados que no contienen Cloro, elemento químico que como veremos más adelante ataca la capa de Ozono, entre éstos HFC tenemos al Refrigerante-134a CH2FCF3 . 14. Refrigerantes y la Capa de Ozono: ¿Como es que los CFCs, tan valiosos por su estabilidad, pueden ser responsables de la destrucción generalidad del ozono estratosférico? De hecho, tal y como predijo Mario J. Molina y F. Sherwood Rowland en 1974, es su estabilidad la que les hace ser tan peligrosos Los CFCs son virtualmente indestructibles en la troposfera (cerca del suelo) y por eso difunden muy lentamente a la estratosfera pueden ser degradados por la radiación ultravioleta en átomos de cloro libres y diversos radicales. Es este cloro atómico libre el que destruye al ozono. 14. Refrigerantes y la Capa de Ozono: El El98% 98%de delalaluz luzUltravioleta Ultravioletadel delsol solde deabsorbe absorbeaatravés travésde delala formación formaciónyydestrucción destruccióndel delozono ozonoatmosférico. atmosférico.El Elcambio cambioglobal global entre ozono y oxigeno es del orden de 300 millones de toneladas entre ozono y oxigeno es del orden de 300 millones de toneladas por pordía. día. 14. Refrigerantes y la Capa de Ozono: Las Lasreacciones reaccionesanteriores anterioresocurren ocurrenen enlalaestratósfera, estratósfera,zona zonade delala atmósfera atmósferadonde dondese seencuantra encuantralalamayor mayorconcentración concentraciónde deozono ozonoyy que quees esfrecuentemente frecuentementedenominada denominadaozonosfera. ozonosfera. 14. Refrigerantes y la Capa de Ozono: Efecto Efecto de de los los CFCs CFCs (R-11) (R-11) sobre sobre elel ozono ozono estratosférico. estratosférico. Se ha estimado que por cada Cl se degradan Se ha estimado que por cada Cl se degradan100 100millones millones de moléculas de ozono, que son removidas de moléculas de ozono, que son removidas de de lala atmósfera atmósferaen enprejuicio prejuiciode delalavida vidaen enlalatierra. tierra. 14. Refrigerantes y la Capa de Ozono: El Elagujero agujerode deozono ozonodel delaño año2000 2000ha hasido sidouno unode delos losmás más intensos que hasta ahora se ha registrado, alcanzó los intensos que hasta ahora se ha registrado, alcanzó los28 28 2, tomada por la NASA el 9/09/2000, los millones de Km 2 millones de Km , tomada por la NASA el 9/09/2000, los colores colores azules azules más más intensos intensos representan representan las las mayores mayores reducciones reduccionesde deozono ozono 14. Refrigerantes y la Capa de Ozono: Para evaluar el impacto que tienen sobre el ozono los CFCs, halones y productos similares se introdujo una nueva magnitud: el Potencial Destructor del Ozono (ODP). Se ha determinado en relación con el R-12, al que se ha dado arbitrariamente el valor de la unidad. Potencial Destructor del Ozono (ODP). Compuesto ODP Tiempo de vida (años) R-11 0,9 65 R-12 1,0 120 R-113 0,8 90 R-114 1,0 180 R-115 0,6 380 Halón 1211 3 21 Halón 1301 13 110 R-123 0,02 1,7 R-22 0,055 15,8 R-134a 0,00 15,6 R-225ca 0,025 2,8 14. Estrategias para preservar la capa de ozono Protocolo de Montreal y sus Enmiendas : 1987 - Documento original: Reducción escalonada de CFCs. Eliminación en un lapso de 5 años. 1990 - Enmienda de Londres: Eliminación total de CFCs adelantada a 1996 en países desarrollados. Reducción escalonada de HCFCs hasta su desaparición para el año 2030 en países desarrollados. 1995 - Enmienda de Viena: Desaparición de HCFCs para el año 2020. Incluye a países en desarrollo en programa de reducción de CFCs y HCFCs: · · · 2010 Eliminación de CFCs. 2015 Congelación de niveles de HCFCs. 2040 Eliminación de HCFCs Compromisos de reducción de sustancias destructoras del ozono (Protocolo de Montreal revisado) Porcentaje de reducción en Porcentaje de reducción en Compuesto países desarrollados países en vías de desarrollo CFC 100 % 1996 CCl4 100 % 1996 Halones 100% 1996 100% 1996 Metil cloroformo HBFC HCFC 100 % 1996 0% 1996 35 % 2004 65 % 2010 90% 2015 99,5 % 2020 100% 2030 0% 1999 50% 2005 85% 2007 100% 2010 85% 2005 100% 2010 0% 1996 50% 2005 100 % 2010 0 % 2003 30 % 2005 70% 2010 100 % 2015 0% 2016 100 % 2040 0 % 2016 100 % 2040 14. Estrategias para preservar la capa de ozono Los 33 países de Latinoamérica y la región del Caribe ratificaron tanto el Convenio de Viena de 1985, como el Protocolo de Montreal de 1987. Muchos de ellos han ratificado las enmiendas de Londres, 1990, Copenhague, 1992, Montreal, 1997, y Beijing, 1999. Solo cuatro países: República Dominicana, Guatemala, Honduras y Surinam, no se han adherido a ninguna de las enmiendas, y en todo el continente solo Chile ha firmado las cuatro. Dentro de la política prevista en el Protocolo de Montreal para esta región, se han comenzado ha realizar las primeras medidas de control. 14. Estrategias para preservar la capa de ozono La Lamayor mayorparte partede delos lospaíses países Latinoamericanos ha Latinoamericanosha respondido respondidosatisfactoriamente satisfactoriamente aalos losrequerimientos requerimientos del delProtocolo Protocolode de Montreal, Montreal,reduciendo reduciendoelel consume consumede deCFC, CFC,incluso inclusoen en los losplazos plazosprevistos. previstos. Expresado Expresadoen envolumen volumenglobal, global,en enrojo, rojo, países que han reducido su consumo. países que han reducido su consumo. En Enazul, azul,los losque queaún aúnlolomantiene mantienesobre sobre las previsiones las previsiones 14. Estrategias para preservar la capa de ozono: Reciclaje de CFCs. Tanques Tanquesde derecuperación recuperaciónyyreciclaje reciclajede deCFC. CFC.Esta Estaactividad actividadha ha permitido recuperar cantidades de estos productos, evitando permitido recuperar cantidades de estos productos, evitando así asísu suemsión emsiónaalalaatmósfera atmósfera(Kali-Chemie (Kali-Chemie 14. Estrategias para preservar la capa de ozono. Desarrollo de Refiregrantes alternativos: R e frig e ra n te R -1 2 R -2 2 R -5 0 2 S u s titu to T ip o C o m p o s ic ió n de G as R -A / R -B / R -C R -1 3 4 a HFC 134a 100 M P 3 9 (4 0 1 A ) HCFC 2 2 /1 5 2 a /1 2 4 5 3 /1 3 /3 4 P M 6 6 (4 0 1 B ) HCFC 2 2 /1 5 2 a /1 2 4 6 1 /1 1 /2 8 F X 5 6 (4 0 9 A ) HCFC 2 2 /1 4 2 b /1 2 4 6 0 /1 5 /2 5 G H G -1 2 (4 0 6 A ) HCFC 2 2 /1 4 2 b /6 0 0 a 5 5 /4 1 /4 A C 9 0 0 0 (4 0 7 C ) HFC 3 2 /1 2 5 /1 3 4 a 2 3 /2 5 /5 2 A Z 2 0 (4 1 0 A ) HFC 3 2 /1 2 5 5 0 /5 0 K L E A -6 6 (4 0 7 C ) HFC 3 2 /1 2 5 /1 3 4 a 2 3 /2 5 /5 2 H P 8 0 (4 0 2 A ) HCFC 2 2 /1 2 5 /2 9 0 3 8 /6 0 /2 H P 8 1 (4 0 2 B ) HCFC 2 2 /1 2 5 /2 9 0 6 0 /3 8 /2 R 6 9 S (4 0 3 A ) HCFC 2 2 /2 1 8 /2 9 0 7 5 /2 0 /5 R 6 9 L (4 0 3 B ) HCFC 2 2 /2 1 8 /2 9 0 5 6 /3 9 /5 F X 1 0 (4 0 8 A ) HCFC 2 2 /1 4 3 a /1 2 5 4 7 /4 6 /7 R-600a R-600a==Isobutano Isobutano(alternativa (alternativapara paraR-12) R-12) R-290 R-290==Propano Propano(alternativa (alternativapara paraR-22 R-22en enA/A) A/A) % 14. Aplicaciones de HCFC y HFC (Ver Tabla EPA) N o m b re del P ro d uc to H F C -2 3 H F C -1 2 5 H F C -1 3 4 a H F C -1 5 2 a A p lic a c io ne s c o m o R e frig e ra nte B a ja T e m p e ra tu ra . S u stitu ye a l C F C -1 1 3 B a ja y m e d ia te m p e ra tu ra . S u stitu ye a la m e zcla C F C -5 0 2 R e frig e ra ció n d o m é stica y co m e rcia l. A /A p a ra a u to m ó vile s. S u stitu to d e l C F C -1 2 M e d ia te m p e ra tu ra y A /A p a ra a u to m ó vile s. S u stitu to d e l C F C -1 2 H C F C -1 2 3 B a ja y m e d ia te m p e ra tu ra . R e frig e ra ció n co m e rcia l y A /A d o m é stico . S u stitu ye a la m e zcla C F C -5 0 2 R e frig e ra d o re s d e a g u a . S u stitu to d e l C F C -1 1 H C F C -1 2 4 R e frig e ra d o re s d e a g u a . S u stitu to d e l C F C -1 1 4 H C F C -2 2 A p lic a c io ne s c o m o p ro p e le nte O tra s a p lic a c io ne s E sp u m a s: p o lie stire n o , p o liu re ta n o , fe n ílica s E sp u m a s: p o lie stire n o , p o liu re ta n o , fe n ílica s E sp u m a s: p o lie stire n o , p o liu re ta n o , fe n ílica s P ro p e le n te p a ra p ro d u cto s fa rm a cé u tico s e n a e ro so l E sp u m a s: p o lie stire n o , p o liu re ta n o , fe n ílica s E sp u m a s: p o lie stire n o , p o liu re ta n o , fe n ílica s C o m p o n e n te d e m e zcla s lim p ia d o ra s In te rm e d ia rio q u ím ico S u p re sió n d e la lla m a e n a p lica cio n e s d e a e ro so l 14. Estrategias para preservar la capa de ozono. Desarrollo de Refrigerantes alternativos: Amoniaco: Con el estado del arte actual del área de Máquinas y Herramientas, el desarrollo de nuevos materiales y tecnologías, el amoniaco podría ser un buen sustituto para los refrigerantes clorados, pues las eventuales fugas de este gas pueden ser manejadas por la Naturaleza (ciclo del nitrógeno). 14. Estrategias para preservar la capa de ozono. Volver a una Refrigeración más ecológica: Refrigeración por Absorción. El Agua como Refrigerante El Amoníaco como Refrigerante 14. Refrigeración por absorción: Sistema Amoniaco / Agua 14. Refrigeración por absorción: Sistema Bromuro de Litio / Agua