Documento PDF - Banc de Sang i Teixits
Anuncio
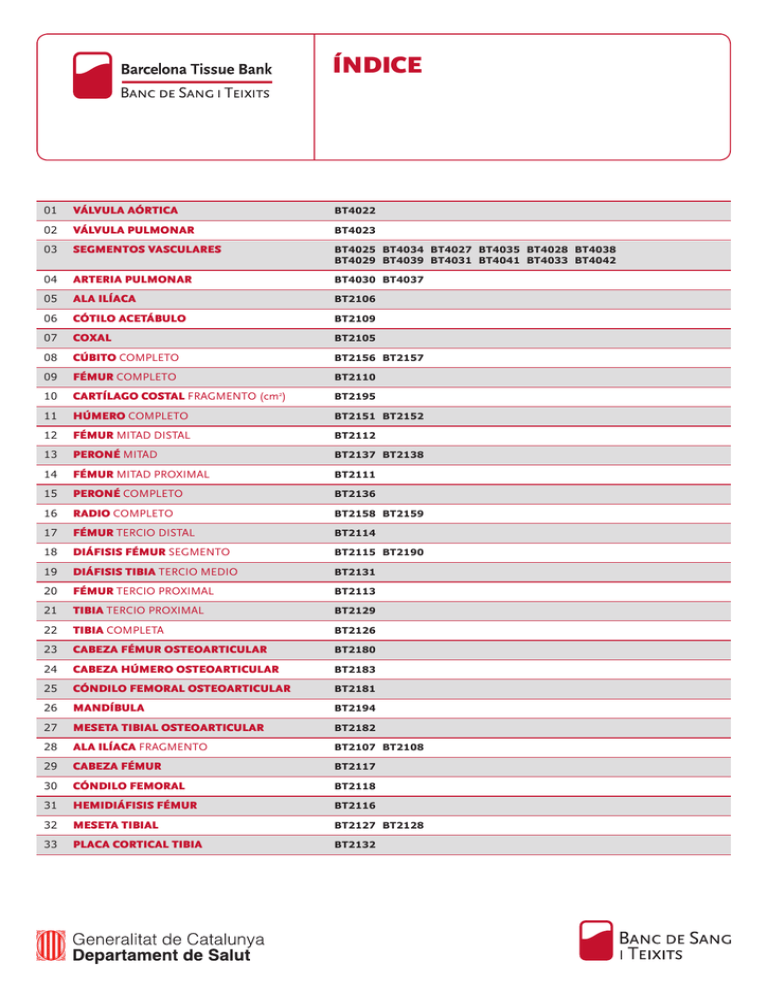
ÍNDICE 01 VÁLVULA AÓRTICA BT4022 02 VÁLVULA PULMONAR BT4023 03 SEGMENTOS VASCULARES BT4025 BT4034 BT4027 BT4035 BT4028 BT4038 BT4029 BT4039 BT4031 BT4041 BT4033 BT4042 04 ARTERIA PULMONAR BT4030 BT4037 05 ALA ILÍACA BT2106 06 CÓTILO ACETÁBULO BT2109 07 COXAL BT2105 08 CÚBITO COMPLETO BT2156 BT2157 09 FÉMUR COMPLETO 10 CARTÍLAGO COSTAL FRAGMENTO (cm ) BT2195 11 HÚMERO COMPLETO BT2151 BT2152 12 FÉMUR MITAD DISTAL BT2112 13 PERONÉ MITAD BT2137 BT2138 14 FÉMUR MITAD PROXIMAL BT2111 15 PERONÉ COMPLETO BT2136 16 RADIO COMPLETO BT2158 BT2159 17 FÉMUR TERCIO DISTAL BT2114 18 DIÁFISIS FÉMUR SEGMENTO BT2115 BT2190 19 DIÁFISIS TIBIA TERCIO MEDIO BT2131 20 FÉMUR TERCIO PROXIMAL BT2113 21 TIBIA TERCIO PROXIMAL BT2129 22 TIBIA COMPLETA BT2126 23 CABEZA FÉMUR OSTEOARTICULAR BT2180 24 CABEZA HÚMERO OSTEOARTICULAR BT2183 25 CÓNDILO FEMORAL OSTEOARTICULAR BT2181 26 MANDÍBULA BT2194 27 MESETA TIBIAL OSTEOARTICULAR BT2182 28 ALA ILÍACA FRAGMENTO BT2107 BT2108 29 CABEZA FÉMUR BT2117 30 CÓNDILO FEMORAL BT2118 31 HEMIDIÁFISIS FÉMUR BT2116 32 MESETA TIBIAL BT2127 BT2128 33 PLACA CORTICAL TIBIA BT2132 BT2110 2 ÍNDICE 34 FRAGMENTO ESPONJOSA PEQUEÑO BT2177 35 HUESO CORTICOESPONJOSO EN CHIPS CONGELADO BT2187 BT2188 36 BLOQUE ESPONJOSA APROXIMADAMENTE 15 cc BT2185 37 HUESO ESPONJOSO EN CHIPS CONGELADO BT2184 BT2186 38 TENDÓN AQUÍLEO BT2139 BT2140 BT2141 39 APARATO EXTENSOR RODILLA COMPLETO BT2122 40 TENDÓN CUADRICIPITAL BT2193 41 TENDÓN ROTULIANO BT2121 BT2123 BT2124 BT2125 42 INJERTOS TENDINOSOS SIN PASTILLA ÓSEA BT2174 BT2175 BT2170 BT2176 BT2171 BT2189 BT2172 BT2191 BT2173 BT2192 BT2174 43 INJERTOS MENISCALES BT2143 BT2144 BT2145 BT2146 BT2147 44 LABRUM ACETABULAR BT2148 45 FASCIA LATA CONGELADO BT2178 BT2179 46 HUESO ESPONJOSO EN CHIPS LIOFILIZADO BT1009 BT1010 BT3011 BT3012 BT3013 47 HUESO CORTICOESPONJOSO EN CHIPS LIOFILIZADO BT3026 BT3027 BT3028 BT3029 48 POLVO DE HUESO CORTICAL MINERALIZADO BT1002 BT1004 BT1016 BT1017 BT1018 BT1019 49 BLOQUE HUESO ESPONJOSO LIOFILIZADO BT1006 BT3023 BT3024 BT3025 50 CRESTA ILÍACA TRICORTICAL BT3015 BT3016 BT3017 BT3018 BT3019 51 CRESTA ILÍACA BICORTICAL BT3011 BT3014 52 PLACA CORTICAL LIOFILIZADA BT3020 BT3021 53 FASCIA LATA LIOFILIZADA BT1007 BT1008 BT3008 BT3009 BT3010 54 PERICARDIO BT3030 BT3031 55 POLVO DE HUESO CORTICAL DESMINERALIZADO BT1001 BT1003 BT1005 56 PASTA DE HUESO CORTICAL DESMINERALIZADO BT1012 BT1013 BT1014 BT1015 57 CÓRNEA BT7002 BT7003 BT7005 58 LAMELA BT7016 BT7017 59 ESCLERA BT7008 BT7009 BT7010 60 MEMBRANA AMNIÓTICA BT7013 BT7014 61 MEMBRANA AMNIÓTICA EXTRACTO BT7018 62 LIMBO ESCLEROCORNEAL EXPANSIÓN DE CÉLULAS BT7007 63 PIEL EN GLICEROL BT5003 BT5004 64 PIEL CRIOPRESERVADA BT5001 BT5005 65 MATRIZ DÉRMICA DESCELULARIZADA BT5006 BT5007 BT5008 66 TEJIDO BAJO DEMANDA Varias referencias Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits VÁLVULA AÓRTICA 01 BT4022 Especificaciones L Homoinjerto aórtico criopreservado. Consta de la válvula aórtica completa, la valva anterior de la válvula mitral y de una arteria aórtica de longitud variable que siempre incluye los senos coronarios. Medidas: • Diámetro valvular interno: 5-30 mm • Longitud arterial: 15-200 mm (L) (D) Aplicaciones clínicas D Recambio valvular aórtico. Especialmente indicado en: • Infecciones • Malformaciones congénitas • Pacientes jóvenes y mujeres en edad fértil, ya que no es necesario tratamiento anticoagulante 01 VÁLVULA AÓRTICA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en el quirófano utilizando técnicas estériles. Una vez se obtiene el tejido se preserva a 4ºC hasta su procesamiento. El procesamiento de la válvula aórtica incluye: una fase de descontaminación antibiótica (vancomicina, amikacina, metronidazol, ciprofloxacina y anfotericina B) previa al empaquetado del tejido en doble bolsa y solución crioprotectora con 10% de DMSO, la congelación programada y el almacenamiento en cuarentena hasta la revisión y aprobación de todos los controles de calidad realizados. Almacenamiento La preservación de los tejidos cardiovasculares se realiza en cubas de nitrógeno, a una temperatura de entre -140 y -196ºC. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga la integridad del empaquetado. Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) consiste en colocar el tejido con hielo seco (-80ºC) dentro de un contenedor externo, protegiendo su integridad en todo momento. La temperatura se mantiene dentro de los límites definidos durante 48 horas y se adjuntan instrucciones de uso y descongelación con la documentación del envío. Una vez los tejidos se han colocado en nieve carbónica no pueden ser devueltos a las cubas de nitrógeno debido a los daños que ocasionan los cambios de temperatura. En casos especiales el transporte se puede realizar en dry-shipper con nitrógeno en fase gas (-140ºC). facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. VÁLVULA PULMONAR 02 BT4023 Especificaciones L’ L’ L Homoinjerto pulmonar criopreservado. Consta de la válvula pulmonar completa, incluyendo el anillo miocárdico, mas un segmento de arteria pulmonar que puede incluir las ramas pulmonares (bifurcación). Medidas: • Diámetros del anillo valvular: 5-35 mm (D) • Longitud del tronco pulmonar: 15-50 mm (L) • Longitud de la rama pulmonar derecha / izquierda: 5-60 mm (cuando la bifurcación está conservada) (L’) Aplicaciones clínicas D Recambio valvular. Especialmente indicado en: • Operación de Ross (autoinjerto de válvula pulmonar en posición aórtica) • Infecciones • Malformaciones congénitas • Pacientes jóvenes y mujeres en edad fértil, ya que no es necesario tratamiento anticoagulante 02 VÁLVULA PULMONAR Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en el quirófano utilizando técnicas estériles. Una vez se obtiene el tejido se preserva a 4ºC hasta su procesamiento. El procesamiento de la válvula aórtica incluye: una fase de descontaminación antibiótica (vancomicina, amikacina, metronidazol, ciprofloxacina y anfotericina B) previa al empaquetado del tejido en doble bolsa y solución crioprotectora con 10% de DMSO, la congelación programada y el almacenamiento en cuarentena hasta la revisión y aprobación de todos los controles de calidad realizados. Almacenamiento La preservación de los tejidos cardiovasculares se realiza en cubas de nitrógeno, a una temperatura de entre -140 y -196ºC. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga la integridad del empaquetado. Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) consiste en colocar el tejido con hielo seco (-80ºC) dentro de un contenedor externo, protegiendo su integridad en todo momento. La temperatura se mantiene dentro de los límites definidos durante 48 horas y se adjuntan instrucciones de uso y descongelación con la documentación del envío. Una vez los tejidos se han colocado en nieve carbónica no pueden ser devueltos a las cubas de nitrógeno debido a los daños que ocasionan los cambios de temperatura. En casos especiales el transporte se puede realizar en dry-shipper con nitrógeno en fase gas (-140ºC). facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. SEGMENTOS VASCULARES 03 BT4025 BT4034 BT4027 BT4035 BT4028 BT4038 BT4029 BT4039 BT4031 BT4041 BT4033 BT4042 Especificaciones Ver la tabla a continuación. Aplicaciones clínicas En el tratamiento quirúrgico de las infecciones vasculares: • Aneurismas micóticos • Infecciones de prótesis vasculares Su aplicación también está asociada al trasplante de órganos, como alternativa a los segmentos vasculares del mismo donante. También aplica cuando hay falta de disponibilidad de injertos autólogos. BT4027 ­Código Descripción BT4031 Aorta ascendente BT4031 Longitud (L-cm) Diámetros (D-mm) Arco aórtico completo Proximal: 15-30 Distal: 10-25 BT4025 Aorta torácica 8-20 Proximal: 10-25 Distal: 9-22 BT4027 Bifurcación Inferior a 40 aorto-ilíaca corta Proximal: 10-15 Distal: 4-7 BT4033 Bifurcación Superior a 40 aorto-ilíaca femoral Proximal: 10-15 Distal: 3-6 BT4028 Arteria ilíaca Inferior a 40 Proximal: 5-9 Distal: 3 - 7 BT4034 Proximal: 5-9 Distal: 2-6 Arteria Superior a 40 ilíaca-femoral BT4039 Arterias ilíacas (2u) Inferior a 40 Proximal: 5-9 Distal: 3 - 7 BT4038 Proximal: 5-9 Distal: 2-6 Arterias Superior a 40 ilíaca-femorales (2u) BT4029 Arteria femoral Inferior a 40 Proximal: 3-7 Distal: 2-6 BT4035 Arteria femoral Superior a 40 Proximal: 3-7 Distal: 2-5 BT4042 Arterias femorales Inferior a 40 (2u) Proximal: 3-7 Distal: 2-6 BT4041 Arterias femorales Superior a 40 (2u) Proximal: 3-7 Distal: 2-5 03 SEGMENTOS VASCULARES Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en el quirófano utilizando técnicas estériles. Una vez se obtiene el tejido se preserva a 4ºC hasta su procesamiento. El procesamiento de la válvula aórtica incluye: una fase de descontaminación antibiótica (vancomicina, amikacina, metronidazol, ciprofloxacina y anfotericina B) previa al empaquetado del tejido en doble bolsa y solución crioprotectora con 10% de DMSO, la congelación programada y el almacenamiento en cuarentena hasta la revisión y aprobación de todos los controles de calidad realizados. Almacenamiento La preservación de los tejidos cardiovasculares se realiza en cubas de nitrógeno, a una temperatura de entre -140 y -196ºC. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga la integridad del empaquetado. Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) consiste en colocar el tejido con hielo seco (-80ºC) dentro de un contenedor externo, protegiendo su integridad en todo momento. La temperatura se mantiene dentro de los límites definidos durante 48 horas y se adjuntan instrucciones de uso y descongelación con la documentación del envío. Una vez los tejidos se han colocado en nieve carbónica no pueden ser devueltos a las cubas de nitrógeno debido a los daños que ocasionan los cambios de temperatura. En casos especiales el transporte se puede realizar en dry-shipper con nitrógeno en fase gas (-140ºC). facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. ARTERIA PULMONAR BT4030 04 BT4037 Especificaciones Arteria pulmonar: Tronco pulmonar (longitud entre 20-40 mm (L) y diámetro 20-30 mm (D)) con bifurcación en rama pulmonar derecha y izquierda. L D BT4030 Hemiarteria pulmonar derecha: Tronco pulmonar seccionado longitudinalmente (longitud entre 20-40 mm) y rama pulmonar derecha. Hemiarteria pulmonar izquierda: Tronco pulmonar seccionado longitudinalmente (longitud entre 20-40 mm) y rama pulmonar izquierda. Aplicaciones clínicas La principal aplicación de los parches pulmonares es la corrección de las malformaciones congénitas: • Tetralogía de Fallot • Atresia pulmonar • Truncus arteriosus • Estenosis de la raíz pulmonar • Reconstrucciones del tracto de salida del ventrículo derecho Código Descripción BT4030 Arteria pulmonar sin válvula BT4037 Hemiarteria pulmonar derecha BT4037 Hemiarteria pulmonar izquierda 04 ARTERIA PULMONAR Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en el quirófano utilizando técnicas estériles. Una vez se obtiene el tejido se preserva a 4ºC hasta su procesamiento. El procesamiento de la válvula aórtica incluye: una fase de descontaminación antibiótica (vancomicina, amikacina, metronidazol, ciprofloxacina y anfotericina B) previa al empaquetado del tejido en doble bolsa y solución crioprotectora con 10% de DMSO, la congelación programada y el almacenamiento en cuarentena hasta la revisión y aprobación de todos los controles de calidad realizados. Almacenamiento La preservación de los tejidos cardiovasculares se realiza en cubas de nitrógeno, a una temperatura de entre -140 y -196ºC. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga la integridad del empaquetado. Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) consiste en colocar el tejido con hielo seco (-80ºC) dentro de un contenedor externo, protegiendo su integridad en todo momento. La temperatura se mantiene dentro de los límites definidos durante 48 horas y se adjuntan instrucciones de uso y descongelación con la documentación del envío. Una vez los tejidos se han colocado en nieve carbónica no pueden ser devueltos a las cubas de nitrógeno debido a los daños que ocasionan los cambios de temperatura. En casos especiales el transporte se puede realizar en dry-shipper con nitrógeno en fase gas (-140ºC). facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. ALA ILÍACA BT2106 Especificaciones Ala ilíaca completa, seccionada por encima del acetábulo y a nivel de articulación sacroilíaca. Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Gran cantidad de hueso esponjoso en su interior • Posibilidad que el cirujano moldee el injerto • Posibilidad de escoger entre los lados derecho e izquierdo Aplicaciones clínicas • • • • • Cirugía tumoral Relleno de defectos óseos Artrodesis esquelética Aporte óseo en pseudoartrosis Cirugía de recambio protésico 05 05 ALA ILÍACA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 06 CÓTILO ACETÁBULO BT2109 Especificaciones D Fragmento óseo procedente del coxal, seccionado por encima del acetábulo y sínfisis del pubis. Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Posibilidad que el cirujano moldee el injerto • Posibilidad de escoger entre los lados derecho e izquierdo Aplicaciones clínicas • Cirugía de recambio protésico • Cirugía tumoral Código Dimensión D Diámetro acetabular 06 COTILO ACETÁBULO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 07 COXAL BT2105 Especificaciones Coxal preservado en su totalidad, seccionado a nivel de articulación sacroilíaca y sínfisis del pubis. A Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Posibilidad que el cirujano moldee el injerto • Posibilidad de escoger entre los lados derecho e izquierdo, así como del sexo masculino o femenino L D Aplicaciones clínicas • Cirugía tumoral Código Dimensión D Diámetro acetabular L Longitud proximal-distal A Longitud máxima anteroposterior 07 COXAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 08 CÚBITO COMPLETO BT2156 BT2157 Especificaciones Cúbito preservado en su totalidad con o sin presencia de inserción del tendón tricipital. A Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Posibilidad de escoger entre los lados derecho e izquierdo Aplicaciones clínicas • Cirugía tumoral • Aporte óseo en fracturas • Aporte óseo en pseudoartrosis We L A’ BT2156 Código Descripción BT2156 Cúbito completo BT2157 Cúbito completo + tendón tricipital Código Dimensión L Longitud total A Ancho epífisis proximal A’ Ancho epífisis distal We Diámetro externo diáfisis T Longitud tendón tricipital 08 CÚBITO COMPLETO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 09 FÉMUR COMPLETO BT2110 Especificaciones C Fémur preservado en su totalidad. Características: • Eliminación de las partes blandas • Aporte de un gran soporte estructural • Posibilidad por parte del cirujano de escoger entre los lados derecho e izquierdo Aplicaciones clínicas • Cirugía de recambio protésico • Cirugía tumoral L We A Código Dimensión L Longitud total C Diámetro cabeza femoral A Ancho epífisis distal Bmed Longitud anteroposterior cóndilo medial Blat Longitud anteroposterior cóndilo lateral We Diámetro externo diáfisis femoral 09 FÉMUR COMPLETO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. CARTÍLAGO COSTAL FRAGMENTO (cm2) BT2195 Especificaciones L A G Fragmento procedente del cartílago costal. Características: • Eliminación de las partes blandas • Preservación del pericondrio • Posibilidad de ser moldeado por parte del cirujano • Las medidas pueden ser variables (posibilidad de solicitar una medida concreta) Aplicaciones clínicas • Cirugía maxilofacial • Cirugía plástica y reconstructiva • Otorrinolaringología Código Dimensión L Longitud A Ancho G Grosor 10 10 CARTÍLAGO COSTAL FRAGMENTO (cm2) Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 11 HÚMERO COMPLETO BT2151 BT2152 Especificaciones D Húmero preservado en su totalidad con o sin presencia de inserciones musculares. Características: • Eliminación de las partes blandas • Aporte de un gran soporte estructural • En el caso del manguito rotador, presencia de inserciones musculares del subescapular, supraespinoso, infraespinoso y redondo menor • Posibilidad de escoger entre los lados derecho e izquierdo L We A BT2151 Aplicaciones clínicas • Cirugía de recambio protésico • Cirugía tumoral Código Descripción BT2151 Húmero completo BT2152 Húmero completo con manguito rotador Código Dimensión L Longitud total D Diámetro cabeza femoral A Ancho epífisis distal We Diámetro externo diáfisis femoral 11 HÚMERO COMPLETO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. FÉMUR MITAD DISTAL 12 BT2112 We Especificaciones Segmento óseo que incluye la epífisis distal del fémur con parte de la diáfisis. Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Posibilidad que el cirujano moldee el fragmento • Posibilidad de escoger entre los lados derecho e izquierdo L Aplicaciones clínicas • Cirugía de recambio protésico • Cirugía tumoral • Aporte óseo en fracturas Bmed/Blat Código Dimensión L Longitud total A Ancho epífisis distal Bmed Longitud anteroposterior cóndilo medial Blat Longitud anteroposterior cóndilo lateral We Diámetro externo diáfisis femoral Wi Diámetro interno diáfisis femoral 12 FÉMUR MITAD DISTAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 13 PERONÉ MITAD BT2137 BT2138 Especificaciones Segmento óseo que incluye la epísifis (proximal o distal) del peroné y parte de la diáfisis. L L Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Posibilidad que el cirujano moldee el injerto • Posibilidad de escoger entre proximal o distal y lados derecho e izquierdo Aplicaciones clínicas • Cirugía tumoral • Aporte óseo en fracturas • Artrodesis esquelética BT2138 BT2137 Código Descripción BT2137 Peroné mitad distal BT2138 Peroné mitad proximal Código Dimensión L Longitud total 13 PERONÉ MITAD Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. FÉMUR MITAD PROXIMAL 14 BT2111 Especificaciones C Segmento óseo que incluye la epífisis proximal del fémur con parte de la diáfisis. Características: • Eliminación de las partes blandas • Aporta de soporte estructural • Posibilidad que el cirujano moldee el fragmento • Posibilidad de escoger entre los lados derecho e izquierdo L Aplicaciones clínicas • Cirugía de recambio protésico • Cirugía tumoral • Aporte óseo en fracturas We Código Dimensión L Longitud total C Diámetro cabeza femoral We Diámetro externo diáfisis femoral Wi Diámetro interno diáfisis femoral (canal medular) 14 FÉMUR MITAD PROXIMAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 15 PERONÉ COMPLETO BT2136 Especificaciones Peroné preservado en su totalidad. Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Posibilidad que el cirujano moldee el injerto • Posibilidad de escoger entre los lados derecho e izquierdo Aplicaciones clínicas L • Cirugía tumoral • Aporte óseo en fracturas • Artrodesis esquelética Código Dimensión L Longitud total 15 PERONÉ COMPLETO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 16 RADIO COMPLETO BT2158 BT2159 Especificaciones Radio preservado en su totalidad, con o sin presencia de inserción del tendón bicipital. Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Posibilidad de escoger entre los lados derecho e izquierdo Aplicaciones clínicas • Cirugía tumoral • Aporte óseo en fracturas • Aporte óseo en pseudoartrosis Código Descripción BT2158 Radio completo BT2159 Radio completo + tendón bicipital Código Dimensión L Longitud total C Diámetro cabeza radial A Ancho epífisis distal We Diámetro externo diáfisis B Longitud tendón bicipital 16 RADIO COMPLETO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. FÉMUR TERCIO DISTAL 17 BT2114 We Especificaciones Fragmento óseo procedente de la epífisis distal del fémur. Está seccionado proximalmente a nivel de metáfisis femoral distal, incluyendo ambos cóndilos femorales. L Características: • Eliminación de las partes blandas • Hueso esponjoso en el interior aproximado de 120 cc • Posibilidad de escoger entre los lados derecho e izquierdo Aplicaciones clínicas Bmed/Blat • Cirugía de recambio protésico • Cirugía tumoral • Aporte óseo en fracturas Código Dimensión L Longitud total A Ancho epífisis distal Bmed Longitud anteroposterior cóndilo medial Blat Longitud anteroposterior cóndilo lateral We Diámetro externo diáfisis femoral Wi Diámetro interno diáfisis femoral 17 FÉMUR TERCIO DISTAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. DIÁFISIS FÉMUR SEGMENTO BT2115 BT2190 Especificaciones Fragmento cortical procedente de la diáfisis femoral. Características: • Ausencia de partes blandas • Ausencia de hueso esponjoso • Canal medular libre de médula ósea y restos celulares • Proporciona gran soporte estructural Aplicaciones clínicas • Aporte óseo en fracturas • Aporte óseo en pseudoartrosis • Cirugía de recambio protésico Código Descripción BT2115 Fémur tercio medio (diáfisis) BT2190 Segmento diafisario fémur (<10 cm) 18 18 DIÁFISIS FÉMUR SEGMENTO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. DIÁFISIS TIBIA TERCIO MEDIO BT2131 Especificaciones Fragmento cortical que incluye la totalidad de la diáfisis tibial. Características: • Ausencia de partes blandas • Ausencia de hueso esponjoso • Canal medular libre de médula ósea y restos celulares • Proporciona gran soporte estructural • Longitud mínima de 20 cm L Aplicaciones clínicas • Aporte óseo en fracturas • Aporte óseo en pseudoartrosis • Cirugía de recambio protésico Código Dimensión L Longitud total We Diámetro externo diáfisis proximal Wi Diámetro interno diáfisis proximal 19 19 DIÁFISIS TIBIA TERCIO MEDIO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. FÉMUR TERCIO PROXIMAL 20 BT2113 Especificaciones Fragmento óseo procedente de la epífisis proximal del fémur. Está seccionado distalmente a trocánter menor, incluyendo cabeza, cuello femoral y región trocantérea. C L Características: • Eliminación de las partes blandas • Hueso esponjoso en el interior aproximado de 120 cc • Posibilidad de escoger entre los lados derecho e izquierdo Aplicaciones clínicas • Cirugía de recambio protésico • Cirugía tumoral • Aporte óseo en fracturas We Código Dimensión L Longitud total C Diámetro cabeza femoral We Diámetro externo diáfisis femoral Wi Diámetro interno diáfisis femoral (canal medular) 20 FÉMUR TERCIO PROXIMAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. TIBIA TERCIO PROXIMAL 21 BT2129 Especificaciones Wp L Fragmento óseo procedente de la epífisis proximal de la tibia. Está seccionado distalmente a nivel de metáfisis tibial proximal, incluyendo ambos platillos tibiales. Características: • Eliminación de las partes blandas • En determinados casos se encuentra ausente la tuberosidad tibial anterior, así como las superfícies articulares (consultar) • Hueso esponjoso en el interior aproximado de 100 cc • Posibilidad de escoger entre lados derecho e izquierdo We Aplicaciones clínicas • Cirugía de recambio protésico • Cirugía tumoral • Aporte óseo en fracturas Código Dimensión L Longitud total Wp Ancho epífisis proximal APm Longitud AP cóndilo medial APl Longitud AP cóndilo lateral We Diámetro externo diáfisis tibial Wi Diámetro interno diáfisis tibial 21 TIBIA TERCIO PROXIMAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 22 TIBIA COMPLETA BT2126 Wp Especificaciones Tibia preservada en su totalidad. Características: • Ausencia de las partes blandas • En algunos casos está exenta de tuberosidad tibial anterior (consultar) • Proporciona gran soporte estructural • Existe gran cantidad de hueso esponjoso en el interior de sus epífisis • Posibilidad de seleccionar entre lados derecho e izquierdo We L Wd Aplicaciones clínicas • Cirugía de recambio protésico • Cirugía tumoral Código Dimensión L Longitud total Wp Ancho epífisis proximal Wd Ancho epífisis distal APm Longitud AP cóndilo medial APl Longitud AP cóndilo lateral We Diámetro externo diáfisis tibial 22 TIBIA COMPLETA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. CABEZA FÉMUR OSTEOARTICULAR 23 BT2180 Especificaciones C Fragmento óseo procedente del fémur. Incluye la cabeza femoral y parte del cuello, manteniendo el cartílago articular. Características: • Eliminación de las partes blandas • Aporte de soporte estructural • La cantidad de hueso esponjoso aproximadamente es de 30 cc • Posibilidad que el cirujano moldee el injerto Aplicaciones clínicas • Cirugía osteocondral • Mosaicoplastia Código Dimensión C Diámetro cabeza femoral 23 CABEZA FÉMUR OSTEOARTICULAR Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. CABEZA HÚMERO OSTEOARTICULAR 24 BT2183 Especificaciones C Fragmento óseo procedente del húmero. Incluye la cabeza humeral y ambas tuberosidades, manteniendo el cartílago articular. Características: • Eliminación de las partes blandas • Aporte de soporte estructural • La cantidad de hueso esponjoso aproximadamente es de 20 cc • Posibilidad que el cirujano moldee el injerto Aplicaciones clínicas • Cirugía osteocondral • Mosaicoplastia Código Dimensión C Diámetro cabeza humeral 24 CABEZA HÚMERO OSTEOARTICULAR Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. CÓNDILO FEMORAL OSTEOARTICULAR 25 BT2181 Especificaciones Fragmento óseo que incluye el cóndilo femoral. Está seccionado proximalmente a nivel de metáfisis y medialmente a nivel de escotadura intercondílea, manteniendo el cartílago articular. L Bmed/Blat Características: • Eliminación de las partes blandas • Aporte de soporte estructural • La cantidad de hueso esponjoso en el interior es aproximadamente de 60cc • Posibilidad que el cirujano moldee el fragmento • Posibilidad de seleccionar el cóndilo medial o lateral, derecho o izquierdo Aplicaciones clínicas • Cirugía osteocondral • Mosaicoplastia Código Dimensión L Longitud total A Ancho cóndilo Bmed o Blat Longitud AP cóndilo 25 CÓNDILO FEMORAL OSTEOARTICULAR Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. MANDÍBULA BT2194 Especificaciones Mandíbula preservada en su totalidad. Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Posibilidad que el cirujano moldee el injerto Aplicaciones clínicas • Cirugía tumoral • Aporte óseo en fracturas 26 26 MANDÍBULA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. MESETA TIBIAL OSTEOARTICULAR 27 BT2182 Especificaciones Fragmento óseo procedente de la epífisis proximal de la tibia. Está seccionado distalmente, a nivel de metáfisis tibial proximal y medialmente, a nivel de espacio intercondíleo, manteniendo el cartílago articular. Características: • Eliminación de las partes blandas • En determinados casos se encuentra ausente la tuberosidad tibial anterior (consultar) • La cantidad de hueso esponjoso en el interior es aproximadamente de 45 cc • Posibilidad que el cirujano moldee el injerto • Posibilidad de seleccionar meseta medial o lateral, derecha o izquierda Aplicaciones clínicas • Cirugía osteocondral • Mosaicoplastia Código Dimensión L Longitud total Wp Ancho replano tibial APm o APl Longitud AP cóndilo tibial 27 MESETA TIBIAL OSTEOARTICULAR Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 28 ALA ILÍACA FRAGMENTO BT2107 BT2108 Especificaciones Fragmento óseo procedente del ala ilíaca y seccionada por encima del acetábulo. A L Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Gran cantidad de hueso esponjoso en su interior Aplicaciones clínicas • • • • • Cirugía tumoral Relleno de defectos óseos Artrodesis esquelética Aporte óseo en pseudoartrosis Cirugía de recambio protésico Código Descripción Ancho (A-cm) Longitud (L-cm) BT2107 Ala ilíaca mitad ≥6 ≥8 BT2108 Ala ilíaca tercio ≥4 ≥8 28 ALA ILÍACA FRAGMENTO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. CABEZA FÉMUR 29 BT2117 Especificaciones Fragmento óseo procedente del fémur. Incluye la cabeza femoral y parte del cuello. C Características: • Eliminación de las partes blandas • Aporte de soporte estructural • La cantidad de hueso esponjoso es aproximadamente de 30 cc • Posibilidad que el cirujano triture el fragmento Aplicaciones clínicas • • • • • Cirugía de recambio protésico Aporte óseo en fracturas Aporte óseo en pseudoartrosis Artrodesis esquelética Relleno de defectos óseos Código Dimensión C Diámetro cabeza femoral 29 CABEZA FÉMUR Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. CÓNDILO FEMORAL 30 BT2118 Especificaciones Fragmento óseo que incluye el cóndilo femoral. Está seccionado proximalmente a nivel de metáfisis y medialmente a nivel de escotadura intercondílea. L Bmed/Blat Características: • Eliminación de las partes blandas • Aporte de soporte estructural • La cantidad de hueso esponjoso en el interior es aproximadamente de 60 cc • Posibilidad que el cirujano triture o moldee el fragmento • Posibilidad de seleccionar el cóndilo medial o lateral, derecho o izquierdo Aplicaciones clínicas • • • • • Cirugía de recambio protésico Aporte óseo en fracturas Relleno de defectos óseo Artrodesis esquelética Aporte óseo en pseudoartrosis Código Dimensión L Longitud total A Ancho cóndilo Bmed o Blat Longitud AP cóndilo 30 CÓNDILO FEMORAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. HEMIDIÁFISIS FÉMUR BT2116 Especificaciones Fragmento cortical procedente de la diáfisis femoral. L Características: • Ausencia de las partes blandas • Ausencia de hueso esponjoso • Proporciona gran soporte estructural • Forma semicircular Aplicaciones clínicas • • • • • Aporte óseo en fracturas Aporte óseo en pseudoartrosis Cirugía de recambio protésico Cirugía tumoral Artrodesis esquelética Código Dimensión L Longitud total 31 31 HEMIDIÁFISIS FÉMUR Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. MESETA TIBIAL BT2127 32 BT2128 Especificaciones Wp Fragmento óseo procedente de la epífisis proximal de la tibia. Está seccionado distalmente a nivel de metáfisis tibial proximal y medianamente a nivel de espacio intercondíleo. L Características: • Eliminación de las partes blandas • Ausencia de la tuberosidad tibial anterior, así como de las superficies articulares en determinados casos (consultar) • La cantidad de hueso esponjoso en el interior es aproximadamente de 45 cc • Posibilidad de seleccionar meseta medial o lateral, derecha o izquierda Aplicaciones clínicas BT2127 • • • • Cirugía de recambio protésico Cirugía tumoral Aporte óseo en fracturas Aporte óseo en pseudoartrosis Código Descripción BT2127 Meseta tibial interna BT2128 Meseta tibial externa Código Dimensión L Longitud total Wp Ancho meseta tibial APm o APl Longitud AP cóndilo tibial 32 MESETA TIBIAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 33 PLACA CORTICAL TIBIA BT2132 Especificaciones A L Fragmento cortical procedente de la diáfisis tibial. Características: • Ausencia de las partes blandas • Ausencia de hueso esponjoso • Proporciona gran soporte estructural • Forma aplanada Aplicaciones clínicas • • • • • Aporte óseo en fracturas Aporte óseo en pseudoartrosis Cirugía de recambio protésico Cirugía tumoral Artrodesis esquelética Código Descripción Longitud (L-cm) Ancho (A-cm) BT2132 Placa cortical tibia 20 2 PLACA CORTICAL TIBIA 33 Obtención del tejido Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. FRAGMENTO ESPONJOSA 34 PEQUEÑO BT2177 Especificaciones Fragmento óseo compuesto por hueso cortical y esponjoso. Normalmente procede de la metáfisis distal de la tibia. La cantidad aproximada de hueso esponjoso es de 15 cc. Características: • Eliminación de las partes blandas • Aporte de soporte estructural • Posibilidad que el cirujano triture o moldee el fragmento Aplicaciones clínicas • • • • • Cirugía de recambio protésico Aporte óseo en fracturas Relleno de defectos óseo Artrodesis esquelética Aporte óseo en pseudoartrosis 34 FRAGMENTO ESPONJOSA PEQUEÑO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. HUESO CORTICOESPONJOSO 35 EN CHIPS CONGELADO BT2187 BT2188 Especificaciones Hueso corticoesponjoso triturado obtenido de las alas ilíacas. Presentación de 15 y 30 cc. Características: • Fragmentos óseos libres de tejidos blandos • El hueso esponjoso tiene una buena incorporación en el receptor • Tiene una mayor resistencia mecánica por la presencia de hueso cortical • El tamaño de las partículas está entre 1-10 mm Aplicaciones clínicas • • • • • • Cirugía de recambio protésico Cirugía tumoral Aporte óseo en fracturas Aporte óseo en pseudoartrosis Relleno de defectos óseos Artrodesis esquelética Código Descripción BT2187 Chips corticoesponjosa triturada 15 cc BT2188 Chips corticoesponjosa triturada 30 cc 35 HUESO CORTICOESPONJOSO EN CHIPS CONGELADO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. BLOQUE ESPONJOSA APROXIMADAMENTE 15 cc 36 BT2185 Especificaciones Fragmento de hueso esponjoso procedente de la epífisis de huesos largos o vertebras lumbares. Características: • Fragmentos óseos libres de tejidos blandos • Buena incorporación del hueso esponjoso en el receptor • La cantidad aproximada de hueso esponjoso es de 15 cc • Ausencia de hueso cortical Aplicaciones clínicas • • • • • • Cirugía de recambio protésico Cirugía tumoral Aporte óseo en fracturas Aporte óseo en pseudoartrosis Relleno de defectos óseos Artrodesis esquelética 36 BLOQUE ESPONJOSA APROXIMADAMENTE 15 cc Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. HUESO ESPONJOSO EN CHIPS CONGELADO BT2184 37 BT2186 Especificaciones Hueso esponjoso triturado obtenido de las epífisis de los huesos largos y/o cuerpos vertebrales lumbares. Presentación de 15 y 30 cc. Características: • Fragmentos óseos libres de tejidos blandos • Ausencia de hueso cortical • Buena incorporación del hueso esponjoso en el receptor • El tamaño de las partículas está entre 1-10 mm Aplicaciones clínicas • • • • • • Cirugía de recambio protésico Cirugía tumoral Aporte óseo en fracturas Aporte óseo en pseudoartrosis Relleno de defectos óseos Artrodesis esquelética Código Descripción BT2186 Chips esponjosa triturada 15 cc BT2184 Chips esponjosa triturada 30 cc 37 HUESO ESPONJOSO EN CHIPS CONGELADO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 38 TENDÓN AQUÍLEO BT2139 BT2140 BT2141 Especificaciones Injerto tendinoso procedente del tendón aquíleo. Incluye pastilla ósea distal del calcáneo (exceptuando el tendón aquíleo sin pastilla). Características: • Eliminación de partes blandas musculares • Ausencia de lesiones, separación de fibras o hematomas • Posibilidad de adaptar, por parte del cirujano, el tamaño de la pastilla ósea del calcáneo según necesidades (exceptuando el tendón aquíleo sin pastilla) L Aplicaciones clínicas W • Ligamentoplastia • Reconstrucción tendinosa • Reconstrucción articular B A C BT2139 Pastilla calcáneo Código Descripción (cm) Longitud Ancho tendón tendón aquíleo (cm) aquíleo (cm) BT2139 Tendón aquíleo ≥ 1,0 x 1,0 x 2,5 ≥ 15 ≥ 1,0 BT2141 Tendón aquíleo mitad ≥ 1,0 x 1,0 x 2,5 ≥ 15 ≥ 1,0 BT2140 No aplica ≥ 15 ≥ 1,0 Tendón aquíleo sin pastilla ósea Código Dimensión L Longitud tendón aquíleo W Grosor tendón aquíleo A Longitud pastilla calcáneo B Ancho pastilla calcáneo C Grosor pastilla calcáneo 38 TENDÓN AQUÍLEO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. APARATO EXTENSOR RODILLA COMPLETO BT2122 Especificaciones Injerto osteotendinoso que incluye tercio proximal de tibia, tendón rotuliano, rótula y tendón cuadricipital. Q Características: • Eliminación de las partes blandas musculares • Ausencia de lesiones, separación de fibras o hematomas en las porciones tendinosas • Posibilidad de seleccionar los lados derecho e izquierdo R L Aplicaciones clínicas • Cirugía de recambio protésico • Reconstrucción articular T Código Dimensión L Longitud total aparato extensor Q Longitud tendón cuadricipital R Longitud tendón rotuliano T Longitud tercio proximal tibia 39 39 APARATO EXTENSOR RODILLA COMPLETO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. TENDÓN CUADRICIPITAL 40 BT2193 Especificaciones Injerto tendinoso procedente del tendón cuadricipital que incluye pastilla ósea distal de la rótula. Q L Características: • Eliminación de las partes blandas musculares • Ausencia de lesiones, separación de fibras o hematomas • Posibilidad de adaptar, por parte del cirujano, el tamaño de la pastilla rotuliana y tendón Aplicaciones clínicas A B • Ligamentoplastia • Reconstrucción articular C Código Dimensión L Longitud total Q Longitud tendón cuadricipital A Longitud pastilla ósea rótula B Ancho pastilla ósea rótula C Grosor pastilla ósea rótula 40 TENDÓN CUADRICIPITAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 41 TENDÓN ROTULIANO BT2121 BT2123 BT2124 BT2125 Especificaciones L R W C A B BT2124 Injerto tendinoso procedente del tendón rotuliano. Incluye pastilla ósea de la rótula y de la inserción tibial. Características: • Eliminación de las partes blandas musculares • Ausencia de lesiones, separación de fibras o hematomas • Posibilidad de adaptar, por parte del cirujano, el tamaño de las pastillas óseas rotuliana y tibial según necesidades • Posibilidad de incluir el tendón cuadricipital • Posibilidad de escoger entre los lados derecho e izquierdo (tendón rotuliano completo más cuadricipital, tendón rotuliano completo) Aplicaciones clínicas • Ligamentoplastia • Reconstrucción tendinosa • Reconstrucción articular Código Descripción Pastilla ósea tibial (ancho x grosor x longitud) (cm) Ancho pastilla ósea rótula (cm) Ancho Longitud tendón tendón rotuliano (cm) cuadricipital (cm) BT2124 Hemitendón rotuliano ≥ 0,8 x 1,2 x 2,5 ≥ 1,0 ≥ 1,0 No aplica BT2125 Hemitendón rotuliano + cuadricipital ≥ 0,8 x 1,2 x 2,5 ≥ 1,0 ≥ 1,0 ≥ 5,0 BT2121 Tendón rotuliano completo ≥ 2,0 x 1,2 x 2,5 ≥ 1,0 ≥ 2,0 No aplica BT2123 Tendón rotuliano completo + cuadricipital ≥ 2,0 x 1,2 x 2,5 ≥ 1,0 ≥ 2,0 ≥ 5,0 Código Dimensión L Longitud total R Longitud tendón entre pastillas W Ancho tendón rotuliano A Longitud pastilla ósea tibial B Ancho pastilla ósea tibial C Grosor pastilla ósea tibial Q Longitud tendón cuadricipital 41 TENDÓN ROTULIANO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 42 INJERTOS TENDINOSOS SIN PASTILLA ÓSEA BT2174 BT2175 BT2170 BT2176 BT2171 BT2189 BT2172 BT2191 BT2173 BT2192 BT2174 Especificaciones L Injertos tendinosos desprovistos de pastilla ósea. Características: • Eliminación de las partes blandas musculares • Ausencia de lesiones, separación de fibras o hematomas • Longitud mínima 20 cm • Grosor mínimo (doble haz) de 5 mm (con la excepción del plantar delgado y del tendón gracilis, cuyo grosor mínimo es de 3 mm) Aplicaciones clínicas • Ligamentoplastia • Reconstrucción articular Código Descripción Longitud Grosor total (doble haz) (cm) (mm) BT2171 Tendón peroneo largo ≥ 20 ≥5 BT2172 Tendón peroneo corto ≥ 20 No aplica BT2191 Tendón semitendinoso ≥ 20 ≥5 BT2173 Tendón tibial anterior ≥ 20 ≥5 BT2170 Tendón tibial posterior ≥ 20 ≥5 BT2189 Tendones pata de ganso ≥ 20 ≥5 BT2176 Tendón gracilis ≥ 20 ≥3 BT2192 Tendón palmar mayor ≥ 20 No aplica BT2174 Tendón extensor hallux ≥ 20 No aplica BT2175 Tendón flexor hallux ≥ 20 No aplica BT2142 Tendón plantar delgado ≥ 20 No aplica Código Dimensión L Longitud total W Grosor (doble haz) 42 INJERTOS TENDINOSOS SIN PASTILLA ÓSEA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. INJERTOS MENISCALES BT2143 BT2144 BT2145 BT2146 43 BT2147 Especificaciones Injerto fibrocartilaginoso que incluye menisco en su totalidad. Características: • Ausencia de lesiones o infiltrados hemáticos • Presencia de tejido blando en su periferia para facilitar la sutura en la cápsula articular • Posibilidad de escoger entre los lados derecho e izquierdo, medial o lateral • Presencia de fragmentos de platillo tibial manteniendo inserciones meniscales (menisco interno o externo con pastilla ósea) AP LM BT2145 Aplicaciones clínicas • Sustitución meniscal Código Descripción BT2147 Menisco externo con pastilla ósea BT2145 Menisco externo individualizado BT2146 Menisco interno con pastilla ósea BT2144 Menisco interno individualizado BT2143 Meniscos completos (interno y externo con meseta tibial) Código Dimensión AP Diámetro anteroposterior LM Diámetro lateromedial A Altura pastilla platillo tibial 43 INJERTOS MENISCALES Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. LABRUM ACETABULAR 44 BT2148 Especificaciones A’ Injerto que incluye labrum acetabular y fragmento óseo. D Características: • Ausencia de lesiones (traumáticas o degenerativas) o infiltrados hemáticos • En el acompañamiento del fragmento óseo manteniendo la inserción del labrum en su totalidad • Altura mínima del labrum acetabular 5 mm • Posibilidad de escoger entre los lados derecho e izquierdo Aplicaciones clínicas • Sustitución labrum acetabular Código Dimensión D Diámetro acetabular A’ Altura labrum acetabular LABRUM ACETABULAR 44 Obtención del tejido Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. FASCIA LATA CONGELADO BT2178 BT2179 Especificaciones Fragmento de fascia lata. Presentación en diferentes formatos. A L Características: • Fragmentos de fascia lata libre de otros tejidos • Ausencia de tejido graso • Ausencia de orificios y separación entre fibras • Actúa como membrana biológica Aplicaciones clínicas • • • • Cirugía urológica Cirugia maxilofacial Odontología Reconstrucción timpánica Código Descripción BT2178 Fascia lata BT2179 Fascia lata mitad Código Dimensión L Longitud AAncho 45 45 FASCIA LATA CONGELADO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis, HTLV I/ II Anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Finalmente se realiza el control microbiológico del tejido, que es almacenado a -80ºC en cuarentena, hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento El tejido se ha de mantener almacenado en el congelador hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a -80ºC. En caso de que se haya de mantener a -20/-40ºC, no se ha de superar el tiempo de almacenamiento más allá de cuatro meses. No utilizar el tejido en el caso que las bolsas de empaquetado no mantengan su integridad (exceptuando la bolsa externa de plástico). Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Transporte El tejido es empaquetado en una bolsa de plástico, una bolsa Tyvek y un contenedor plástico. El contenedor plástico es estéril así como la bolsa de Tyvek en su interior. El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el injerto empaquetado dentro de un contenedor de transporte que contiene hielo seco (dióxido de carbono sólido). Es un sistema de transporte validado que permite mantener las propiedades del injerto hasta la fecha y hora de entrega que constan en la etiqueta del paquete. PRECAUCIÓN: El hielo seco puede causar quemaduras. El producto debe ser desempaquetado empleando guantes de seguridad que permitan el manejo de productos a -80º C. Hay que evitar elevados niveles de dióxido de carbono, ya que pueden provocar asfixia. Por tanto, se debe tener la precaución de de abrir el embalaje en una dependencia con una ventilación adecuada. El hielo sobrante se puede dejar evaporar en un área ventilada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 46 HUESO ESPONJOSO EN CHIPS LIOFILIZADO BT1009 BT1010 BT3011 BT3012 BT3013 Especificaciones Hueso esponjoso triturado obtenido de las epífisis de los huesos largos y/o cuerpos vertebrales lumbares. Presentación de 2, 5, 10, 15 y 30 cc. Características: • Fragmentos óseos libres de tejidos blandos • Ausencia de hueso cortical • Buena incorporación del hueso esponjoso en el receptor • El tamaño de las partículas está entre 1-10 mm Aplicaciones clínicas • • • • • • Cirugía de recambio protésico Cirugía tumoral Aporte óseo en fracturas Aporte óseo en pseudoartrosis Relleno de defectos óseos Artrodesis esquelética Código Descripción Presentación (cc) BT1009 CAN2 - Esponjosa en chips 2 cc 2 BT1010 CAN5 - Esponjosa en chips 5 cc 5 BT3011 CAN10 - Esponjosa en chips 10 cc 10 BT3012 CAN15 - Esponjosa en chips 15 cc 15 BT3013 CAN30 - Esponjosa en chips 30 cc 30 46 HUESO ESPONJOSO EN CHIPS LIOFILIZADO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Seguidamente el tejido se somete a un proceso de liofilización en el cual se alcanza un porcentaje de agua residual inferior al 5%. Finalmente se realiza el control microbiológico del tejido. Se almacena a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits El tejido se ha de mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. No utilizar en caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con doble blíster. El que está directamente en contacto con el tejido es estéril. El más externo es estéril en su interior. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. HUESO CORTICOESPONJOSO 47 EN CHIPS LIOFILIZADO BT3026 BT3027 BT3028 BT3029 Especificaciones Hueso corticoesponjoso triturado obtenido de las alas ilíacas. Presentación de 5, 10, 15 y 30 cc. Características: • Fragmentos óseos libres de tejidos blandos • Buena incorporación del hueso esponjoso en el receptor • Mayor resistencia mecánica por presencia de hueso cortical • El tamaño de las partículas está entre 1-10 mm Aplicaciones clínicas • • • • • • Cirugía de recambio protésico Cirugía tumoral Aporte óseo en fracturas Aporte óseo en pseudoartrosis Relleno de defectos óseos Artrodesis esquelética Código Descripción Presentación (cc) BT3026 CE5 - Corticoesponjosa en chips 5 cc BT3027 CE10 - Corticoesponjosa en chips 10 cc 10 BT3028 CE15 - Corticoesponjosa en chips 15 cc 15 BT3029 CE30 - Corticoesponjosa en chips 30 cc 30 5 47 HUESO CORTICOESPONJOSO EN CHIPS LIOFILIZADO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Seguidamente el tejido se somete a un proceso de liofilización en el cual se alcanza un porcentaje de agua residual inferior al 5%. Finalmente se realiza el control microbiológico del tejido. Se almacena a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits El tejido se ha de mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. No utilizar en caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con doble blíster. El que está directamente en contacto con el tejido es estéril. El más externo es estéril en su interior. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. POLVO DE HUESO CORTICAL 48 MINERALIZADO BT1002 BT1004 BT1016 BT1017 BT1018 BT1019 Especificaciones Hueso cortical triturado obtenido de las diáfisis de los huesos largos (fémur, tibia y húmero). Presentación de 0,5, 1 y 2 cc. Características: • Fragmentos óseos libres de tejidos blandos • Ausencia de hueso esponjoso • Dos tamaños posibles de partículas: 250-850 o 500-850 micras Aplicaciones clínicas • • • • • Cirugía de elevación de seno Preservación tejido alveolar Relleno tras exodoncia Relleno de defectos óseos Reconstrucción maxilofacial Código Descripción Presentación (cc) Tamaño partícula (micras) BT1016 GC - Polvo cortical mineralizado 0,5 cc (0,25 - 0,85 mm) 0,5 250-850 BT1017 GC - Polvo cortical mineralizado 0,5 cc (0,50 - 0,85 mm) 0,5 500-850 BT1002 GC1 - Polvo cortical mineralizado 1 cc (0,25 - 0,85 mm) 1 250-850 BT1018 GC1 - Polvo cortical mineralizado 1 cc (0,50 - 0,85 mm) 1 500-850 BT1004 GC2 - Polvo cortical mineralizado 2 cc (0,25 - 0,85 mm) 2 250-850 BT1019 GC2 - Polvo cortical mineralizado 2 cc (0,50 - 0,85 mm) 2 500-850 48 POLVO DE HUESO CORTICAL MINERALIZADO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos son sometidos a un proceso de descontaminación que incluye una serie de procesos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente) por lo que pueden quedar trazas de estos agentes. Seguidamente el tejido se somete a un proceso de liofilización alcanzándose un porcentaje de agua residual inferior al 5%. Finalmente se realiza control microbiológico del tejido, que es almacenado a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga a la integridad del empaquetado. No utilizar en el caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con vial y bolsa de Tyvek. Son estériles el vial y la bolsa en su interior. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. BLOQUE HUESO ESPONJOSO LIOFILIZADO BT1006 BT3023 BT3024 49 BT3025 Especificaciones G L A BT3025 Fragmento de hueso esponjoso obtenido de las epífisis de huesos largos (fémur y tibia). Características: • Fragmentos óseos libres de tejidos blandos • Ausencia de hueso cortical • Buenas incorporación del hueso esponjoso en el receptor • Posibilidad de moldear el injerto por parte del cirujano Aplicaciones clínicas • • • • • Cirugía tumoral Aporte óseo en fracturas Aporte óseo en pseudoartrosis Relleno de defectos óseos Cirugía de elevación de seno Código Descripción Longitud (L-cm) Ancho (A-cm) Grosor (G-cm) BT1006 CUBE - Cubo esponjosa (1 x 1 x 1 cm) 1 1 1 BT3023 CANBLOCK1,3 - Bloque esponjosa (1,3 x 1,3 x 3 cm) 3 1,3 1,3 BT3024 CANBLOCK1,5 - Bloque esponjosa (1,5 x 1,5 x 3 cm) 3 1,5 1,5 BT3025 CANBLOCK2,0 - Bloque esponjosa (2 x 2 x 3 cm) 3 2 2 49 BLOQUE HUESO ESPONJOSO LIOFILIZADO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Seguidamente el tejido se somete a un proceso de liofilización en el cual se alcanza un porcentaje de agua residual inferior al 5%. Finalmente se realiza el control microbiológico del tejido. Se almacena a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits El tejido se ha de mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. No utilizar en caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con doble blíster. El que está directamente en contacto con el tejido es estéril. El más externo es estéril en su interior. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 50 CRESTA ILÍACA TRICORTICAL BT3015 A BT3016 BT3017 BT3018 BT3019 Especificaciones Fragmentos óseos obtenidos de la cresta ilíaca. Está compuesto por 3 caras corticales conteniendo en su interior hueso esponjoso. L G BT3018 Características: • Fragmentos óseos libres de tejidos blandos • Mayor resistencia mecánica por la presencia de hueso cortical • Buena incorporación en el receptor por la presencia de hueso esponjoso • Posibilidad de manipulación del injerto por parte del cirujano Aplicaciones clínicas • Artrodesis esquelética • Cirugía maxilofacial Código Descripción BT3015 ICW2 - Cresta ilíaca tricortical (1,2 x 3 cm) BT3016 Longitud (L-cm) Ancho (A-cm) Grosor (G-cm) ≥ 3 1,2 ≥ 0,8 ICW5 - Cresta ilíaca tricortical (1,5 x 3 cm) ≥ 3 1,5 ≥ 0,9 BT3017 ICW8 - Cresta ilíaca tricortical (1,8 x 3 cm) ≥ 3 1,8 ≥ 0,9 BT3018 ICW2_0 - Cresta ilíaca tricortical (2 x 3 cm) ≥ 3 2 ≥ 0,9 BT3019 ICW2_6 - Cresta ilíaca tricortical (2 x 6 cm) ≥ 6 2 ≥ 1,0 50 CRESTA ILÍACA TRICORTICAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Seguidamente el tejido se somete a un proceso de liofilización en el cual se alcanza un porcentaje de agua residual inferior al 5%. Finalmente se realiza el control microbiológico del tejido. Se almacena a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits El tejido se ha de mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. No utilizar en caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con doble blíster. El que está directamente en contacto con el tejido es estéril. El más externo es estéril en su interior. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 51 CRESTA ILÍACA BICORTICAL BT3011 L A BT3014 Especificaciones Fragmento óseo obtenido del ala ilíaca. Está compuesto por 2 caras corticales conteniendo en su interior hueso esponjoso. G BT3014 Características: • Fragmentos óseos libres de tejidos blandos • Mayor resistencia mecánica por la presencia de hueso cortical • Buena incorporación en el receptor por la presencia de hueso esponjoso • Posibilidad de manipulación del injerto por parte del cirujano Aplicaciones clínicas • Artrodesis esquelética • Cirugía maxilofacial Código Descripción BT1011 IS - Tira cresta ilíaca bicortical (2 x 2 cm) BT3014 IS26 - Tira cresta ilíaca bicortical (2 x 6 cm) Longitud (L-cm) Ancho (A-cm) Grosor (G-cm) 2 2 ≥ 0,5 ≥ 6 2 ≥ 0,5 51 CRESTA ILÍACA BICORTICAL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Seguidamente el tejido se somete a un proceso de liofilización en el cual se alcanza un porcentaje de agua residual inferior al 5%. Finalmente se realiza el control microbiológico del tejido. Se almacena a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits El tejido se ha de mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. No utilizar en caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con doble blíster. El que está directamente en contacto con el tejido es estéril. El más externo es estéril en su interior. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 52 PLACA CORTICAL LIOFILIZADA BT3020 BT3021 Especificaciones Placa de hueso cortical procedente de diáfisis de fémur o tibia. A L Características: • Fragmentos de óseos libre de tejidos blandos • Ausencia de hueso esponjoso • Mayor resistencia mecánica por presencia de hueso cortical • Posibilidad de manipulación del injerto por parte del cirujano BT3020 Aplicaciones clínicas • • • • • • Cirugía tumoral Cirugía de recambio protésico Aporte óseo en fracturas Aporte óseo en pseudoartrosis Relleno de defectos óseos Artrodesis esquelética Código Descripción Longitud (L-cm) Ancho (A-cm) BT3020 FSSP - Placa cortical femoral (2 x 12 cm) 12 2 BT3021 TSSP - Placa cortical tibial (1,5 x 10 cm) 10 1,5 52 PLACA CORTICAL LIOFILIZADA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Seguidamente el tejido se somete a un proceso de liofilización en el cual se alcanza un porcentaje de agua residual inferior al 5%. Finalmente se realiza el control microbiológico del tejido. Se almacena a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits El tejido se ha de mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. No utilizar en caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con doble blíster. El que está directamente en contacto con el tejido es estéril. El más externo es estéril en su interior. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 53 FASCIA LATA LIOFILIZADA BT1007 BT1008 BT3008 BT3009 BT3010 Especificaciones Fragmento de fascia lata. Presentación en diferentes formatos. A L Características: • Fragmentos de fascia lata libre de otros tejidos • Ausencia de tejido graso • Ausencia de orificios y separación entre fibras • Actúa como membrana biológica Aplicaciones clínicas BT3008 • Cirugia maxilofacial • Odontología • Reconstrucción timpánica Código Descripción Longitud (L-cm) Ancho (A-cm) BT1007 PFLS - Fascia lata periodontal (2,5 x 2,5 cm) 2,5 2,5 BT1008 FLR4.4 - Fascia lata liofilizada (4 x 4 cm) 4 4 BT3008 FLR - Fascia lata liofilizada (6 x 6 cm) 6 6 BT3009 FLM - Fascia lata mediana liofilizada (3 x 15 cm) 15 3 BT3010 FLL - Fascia lata grande liofilizada (> 70 cm2) ≥ 17 ≥7 53 FASCIA LATA LIOFILIZADA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Seguidamente el tejido se somete a un proceso de liofilización en el cual se alcanza un porcentaje de agua residual inferior al 5%. Finalmente se realiza el control microbiológico del tejido. Se almacena a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits El tejido se ha de mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. No utilizar en caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con doble blíster. El que está directamente en contacto con el tejido es estéril. El más externo es estéril en su interior. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 54 PERICARDIO BT3030 BT3031 Especificaciones Fragmento de pericardio humano. A L BT3031 Presentación en dos formatos: • Pericardio grande (PERI L): 6 x 6 cm • Pericardio mediano (PERI M): 3 x 5 cm Características: • Fragmentos de pericardio libre de otros tejidos • Ausencia de tejido graso • Ausencia de orificios y separación entre fibras • Actúa como membrana biológica Aplicaciones clínicas • Cirugia maxilofacial • Odontología • Reconstrucción timpánica Código Descripción Longitud (cm) Ancho (cm) BT3030 PERIL - Pericardio grande liofilizado (6 x 6 cm) 6 6 BT3031 PERIM - Pericardio medio liofilizado (3 x 5 cm) 5 3 54 PERICARDIO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. obtenidos asegurando su calidad, seguridad y eficacia. Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Seguidamente el tejido se somete a un proceso de liofilización en el cual se alcanza un porcentaje de agua residual inferior al 5%. Finalmente se realiza el control microbiológico del tejido. Se almacena a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits El tejido se ha de mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. No utilizar en caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con doble blíster. El que está directamente en contacto con el tejido es estéril. El más externo es estéril en su interior. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. POLVO DE HUESO CORTICAL 55 DESMINERALIZADO BT1001 BT1003 BT1005 Especificaciones Hueso cortical triturado obtenido de las diáfisis de los huesos largos (fémur, tibia y húmero). Presentación de 0,5, 1 y 5 cc. Características: • Fragmentos óseos libres de tejidos blandos • Ausencia de hueso esponjoso • El tamaño de las partículas óseas está entre 250-850 micras • Garantía de potencial osteoinductivo (test de osteoinducción “in vivo”) Aplicaciones clínicas • • • • • Cirugía de elevación de seno Preservación tejido alveolar Relleno tras exodoncia Relleno de defectos óseos Reconstrucción maxilofacial Código Descripción Presentación (cc) Tamaño partícula (micras) BT1001 DGC0.5 – Polvo cortical desmineralizado 0,5 cc 0,5 250 - 850 BT1003 DGC1 – Polvo cortical desmineralizado 1 cc 1 250 - 850 BT1005 DGC5 – Polvo cortical desmineralizado 5 cc 5 250 - 850 55 POLVO DE HUESO CORTICAL DESMINERALIZADO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Procesamiento Almacenamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Posteriormente se procede a la descalcificación del tejido obteniendo unos valores de Ca2+ residual <5%. Seguidamente el tejido se somete a un proceso de liofilización en el cual se alcanza un porcentaje de agua residual inferior al 5%. Finalmente se realiza el control microbiológico del tejido. Se almacena a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes (dentro de los controles de calidad se incluye un test de osteoinducción “in vivo”). El tejido se ha de mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. No utilizar en caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con vial o jeringa y bolsa de Tyvek. El vial o jeringa y la bolsa en su interior son estériles. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. PASTA DE HUESO CORTICAL 56 DESMINERALIZADO BT1012 BT1013 BT1014 BT1015 Especificaciones Pasta de hueso cortical triturado, obtenido de las diáfisis de los huesos largos (fémur, tibia, húmero), mezclado con glicerol. Presentación de 1, 2,5, 5 y 10 cc. Características: • Fragmentos óseos libres de tejidos blandos • Ausencia de hueso esponjoso • El tamaño de las partículas óseas está entre 250-850 micras • Garantía de potencial osteoinductivo (test de osteoinducción “in vivo”) Aplicaciones clínicas • • • • • Cirugía de elevación de seno Preservación tejido alveolar Relleno tras exodoncia Relleno de defectos óseos Reconstrucción maxilofacial Código Descripción Presentación (cc) BT1012 DBM Putty 1 cc Matriz ósea desmineralizada en pasta 1 BT1013 DBM Putty 2,5 cc Matriz ósea desmineralizada en pasta 2,5 BT1014 DBM Putty 5 cc Matriz ósea desmineralizada en pasta 5 BT1015 DBM Putty 10 cc Matriz ósea desmineralizada en pasta 10 56 PASTA DE HUESO CORTICAL DESMINERALIZADO Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a -80ºC hasta su procesamiento y preservación final. Procesamiento Almacenamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits Los tejidos se someten a un proceso de descontaminación que incluye una serie de tratamientos mecánicos y químicos (gentamicina, alcohol, peróxido de hidrógeno y detergente). Por este motivo, pueden quedar trazas de estos agentes. Posteriormente se procede a la descalcificación del tejido obteniendo unos valores de Ca2+ residual <5%. Seguidamente el tejido se somete a un proceso de liofilización en el cual se alcanza un porcentaje de agua residual inferior al 5%. Finalmente se realiza el control microbiológico del tejido. Se almacena a temperatura ambiente (4-30º), hasta la obtención del resultado del mismo. Tras el control de calidad final del tejido este queda disponible para su distribución y uso prescrito en pacientes (dentro de los controles de calidad se incluye un test de osteoinducción “in vivo”). El tejido se ha de mantener almacenado a temperatura ambiente (4-30º) hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. No utilizar en caso que alguno de los envoltorios no mantengan su integridad. Transporte El tejido es empaquetado con vial o jeringa y bolsa de Tyvek. El vial o jeringa y la bolsa en su interior son estériles. El transporte se realiza colocando el injerto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 57 CÓRNEA BT7002 BT7003 BT7005 Especificaciones Córnea fresca: Botón esclerocorneal (diámetro ≥17 mm) mantenido en hipotermia, con un contaje endotelial mayor o igual a 2.000 células/mm2. Córnea cultivada: Botón esclerocorneal (diámetro ≥17 mm) mantenido a temperatura ambiente en medio de cultivo con un contaje endotelial mayor o igual a 2.000 células/mm2. Córnea tectónica: Botón esclerocorneal (diámetro ≥17 mm) mantenido a temperatura ambiente con un contaje endotelial inferior a 2.000 células/mm2. BT7002 Aplicaciones clínicas Córnea fresca y córnea cultivada: • Queratoplastia penetrante • Queratoplastias lamelares posteriores y queratoplastias endotleilales • Trasplante de limbo (en donantes que cumplan criterios multitejidos) Córnea tectónica: • Queratoplastias lamelares anteriores • Finalidades tectónicas Código Descripción Presentación Temperatura de conservación BT7002 Córnea fresca Medio de mantenimiento 2ºC – 10ºC BT7003 Córnea cultivada Medio deturgescente Tª ambiente Medio de mantenimiento / Medio deturgescente 2ºC – 10ºC / Tª ambiente BT7005 Córnea tectónica 57 CÓRNEA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a 4ºC hasta su procesamiento en el Banco de Tejidos. Transporte Procesamiento y almacenamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decretoley 9/2014, para el procesamiento, preservación y Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Una vez aislado del globo ocular, el botón esclerocorneal se preserva en un medio que proporciona un ambiente adecuado para las células endoteliales y epiteliales. La córnea es evaluada mediante lámpara de hendidura y el contaje endotelial se realiza con microscopio especular. En el caso de la córnea cultivada al finalizar el periodo de preservación a 31ºC se realiza un nuevo contaje endotelial con microscopia óptica y el tejido se envía en medio deturgescente de transporte. El sistema de transporte validado, desde el Banco de Tejidos de Barcelona (BTB), para la córnea a 2-10º, consiste en colocar la córnea envasada con acumuladores de frío, dentro de un contenedor externo protegiendo su integridad en todo momento. La córnea cultivada se transporta y debe ser mantenida a temperatura ambiente hasta su uso. La fecha de caducidad del tejido figura en el etiquetado y en la documentación adjunta. El tejido no debe utilizarse si la integridad del envase no está preservada. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 58 LAMELA BT7016 BT7017 Especificaciones Lamela anterior: Córnea precortada a nivel del estroma corneal para la sustitución de la parte anterior de la córnea del paciente. La profundidad de la lamela anterior debe de ser indicada por el cirujano dentro del rango 130 µm - 450 µm. BT7016 BT7017 Lamela posterior: Córnea con contaje endotelial mayor o igual a 2.200 células/mm2 precortada a nivel estromal para sustitución de la parte posterior de la cornea del paciente. Si el cirujano no indica lo contrario, se suministran lamelas con grosor de 100 ± 30 µm. Aplicaciones clínicas Lamela anterior: • Queratoplastias lamelares anteriores (SALK, ALK, DALK) Lamela posterior: • Queratoplastias lamelares posteriores (DSAEK) Código Descripción BT7016 Lamela anterior BT7017 Lamela posterior 58 LAMELA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social, una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1/2 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos, se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a 4ºC hasta su procesamiento en el Banco de Tejidos. Procesamiento Todos los procesos realizados bajo el control del Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP), los requerimientos derivados de las autorizaciones de los medicamentos en investigación, los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. La lamela se obtiene tras cortar la córnea con microqueratomo semiautomático, colocándola en una cámara anterior artificial y midiendo su grosor con paquímetro ultrasónico. En función del valor obtenido, se escoge el cabezal de corte más adecuado para obtener la lamela corneal del grosor deseado. Almacenamiento Dependiendo del tipo de córnea de origen, el producto es mantenido a 2º-10ºC o a temperatura ambiente hasta su uso. La fecha de caducidad del tejido figura en el etiquetado y puede ser de 8 (lamela posterior) a 14 días (lamela anterior) siempre que se mantenga la integridad del empaquetado. Transporte La cornea pre-cortada se envía con la lamela anterior (cap) adherida a la lamela posterior dentro de un recipiente hermético (Chiron®) en medio nutritivo. Este recipiente es empaquetado y colocado dentro de un contenedor de transporte protegiendo su integridad en todo momento y manteniendo la temperatura requerida. La fecha de caducidad figura en la etiqueta y en la documentación adjunta. El producto no debe utilizarse si no se mantiene la integridad del envase. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 59 ESCLERA BT7008 BT7009 BT7010 Especificaciones Fragmentos de esclerótica. Aplicaciones clínicas BT7009 • • • • Reparaciones del globo ocular Escleritis necrotizante Adelgazamientos o perforaciones esclerales Recubrimiento de tubos de drenaje Código Descripción Presentación Temperatura de conservación BT7008 Esclera entera Etanol 70% Tª ambiente BT7009 Hemiesclera Etanol 70% Tª ambiente BT7010 Cuarto de esclera Etanol 70% Tª ambiente 59 ESCLERA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1/2 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos, se lleva a cabo dentro de las 24 horas posteriores al fallecimiento y se realiza utilizando técnicas estériles. Una vez el tejido es obtenido se preserva en cuarentena a 4ºC hasta su procesamiento en el Banco de Tejidos. Transporte Procesamiento y almacenamiento Todos los procesos realizados bajo el control del Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP), los requerimientos derivados Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits de las autorizaciones de los medicamentos en investigación, los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. El procesamiento del tejido escleral incluye la total eliminación de las estructuras internas del globo ocular así como de las inserciones musculares externas. La preservación se realiza en etanol 70% y se almacena en cuarentena hasta la revisión y aprobación de todos los controles de calidad realizados. El tejido escleral envasado se coloca dentro de un contenedor de transporte, protegiendo su integridad en todo momento y debe ser mantenido a temperatura ambiente hasta su utilización. La fecha de caducidad figura en la etiqueta y en la documentación adjunta. El producto no debe utilizarse si no se mantiene la integridad del envase. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. MEMBRANA AMNIÓTICA 60 BT7013 BT7014 Especificaciones Fragmentos de membrana amniótica presentados sobre un soporte de nitrocelulosa. Existen dos tipos de presentaciones, atendiendo a su tamaño: • Fragmentos de 2,5 cm de diámetro • Fragmentos de 4,5 cm de diámetro Aplicaciones clínicas • Uso oftalmológico en pacientes con defectos epiteliales de la córnea y de la conjuntiva: úlceras corneales, causticaciones en fase aguda, resecciones conjuntivales amplias • Coadyuvante en el trasplante de córnea y en casos en los que se prevean problemas de regeneración tisular o de cicatrización en el postoperatorio Código Descripción BT7014 Temperatura de conservación BT7013 Membrana amniótica 2,5 cm -80ºC BT7014 Membrana amniótica 4,5 cm -80ºC 60 MEMBRANA AMNIÓTICA Obtención del tejido El tejido procede de donantes con embarazo controlado y cesárea electiva. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIVAntígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBVDNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Una vez se recoge la placenta, se preserva en cuarentena a 4ºC hasta su procesamiento y preservación en el Banco de Tejidos. Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decretoley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits El procesamiento consiste en la separación de la membrana amniótica del corion. Los fragmentos obtenidos se congelan de forma controlada hasta -80ºC en una solución crioprotectora (RPMI + glicerol). Esta solución contiene un cóctel antibiótico (penicilina, estreptomicina y amfotericina B). Almacenamiento Cada fragmento de membrana amniótica es almacenado a -80ºC hasta su uso. La fecha de caducidad del tejido es de un año desde el procesamiento, siempre que se mantenga la integridad del empaquetado y la cadena de frío. El tejido no debe utilizarse en el caso que alguno de los recipientes no mantengan su integridad. Transporte El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) consiste en colocar el recipiente de la membrana dentro de un contenedor de transporte con hielo seco (-80ºC) protegiendo su integridad en todo momento. La temperatura se mantiene dentro de los límites definidos durante 48 horas. Se adjuntan instrucciones de uso y descongelación. La fecha de caducidad del producto se indica en la etiqueta y en la documentación adjunta. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. MEMBRANA AMNIÓTICA 61 EXTRACTO BT7018 Especificaciones El extracto de membrana es un producto liofilizado procedente de membrana amniótica. Cada vial se reconstituye en 4 ml de agua estéril y contiene la cantidad de extracto necesario para 5 días de tratamiento. La duración mínima del tratamiento es de 30 días (6 viales de extracto). Aplicaciones clínicas • • • • Uso oftalmológico en pacientes con defectos epiteliales en la córnea Casos de ojo seco secundario a síndrome autoinmune Úlceras corneales Coadyuvante en cirugías de trasplante de córnea, excisión de pterigion y simblefaron 61 MEMBRANA AMNIÓTICA EXTRACTO Obtención del tejido El tejido procede de donantes con embarazo controlado y cesárea electiva. El cribado serológico que por defecto se realiza es el siguiente: HIV-1/2 Anticuerpos, HIVAntígeno, HIV 1 -RNA, HBsAg, HBc Anticuerpos, HBVDNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Una vez se recoge la placenta, se preserva en cuarentena a 4ºC hasta su procesamiento y preservación en el Banco de Tejidos. El procesamiento consiste en la separación de la membrana amniótica del corion y la correspondiente descontaminación con antibióticos (penicilina, estreptomicina y amfotericina B). Posteriormente el tejido se somete a un proceso de triturado y centrifugación para obtener el extracto. El proceso concluye con la liofilización. Tras el control de calidad final del tejido, este queda disponible para su distribución y uso prescrito en pacientes. Almacenamiento Procesamiento Todos los procesos que realiza el Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP). También con los requerimientos derivados de las autorizaciones de los medicamentos en investigación, con los requerimientos establecidos en el Real Decretoley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, con los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits El extracto de membrana es almacenado a temperatura ambiente hasta su uso. La fecha de caducidad del producto es de 5 años desde su procesamiento, siempre que se mantenga a la integridad del empaquetado. El tejido no debe utilizarse si alguno de los envoltorios ha perdido su integridad. Transporte El extracto es empaquetado junto con todo el material necesario para su rehidratación. El transporte se realiza a temperatura ambiente colocando el producto empaquetado dentro de un contenedor protegiendo su integridad en todo momento. La fecha de caducidad del producto se indica en la etiqueta y en la documentación adjunta. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. LIMBO ESCLEROCORNEAL 62 EXPANSIÓN DE CÉLULAS BT7007 Especificaciones Células de limbo esclerocorneal. Características: • Expansión ex vivo de células del limbo esclerocorneal humano para uso autólogo. Aplicaciones clínicas • Insuficiencia límbica unilateral LSC 24 horas del aislamiento. LSC 7 días en cultivo celular, una vez establecido el crecimiento de las células. 62 LIMBO ESCLEROCORNEAL EXPANSIÓN DE CÉLULAS Obtención del tejido El tejido procede de pacientes a los que se les realiza una minuciosa evaluación de la historia médico-social y el siguiente cribado serológico: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1-RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. La obtención de la biopsia se realiza bajo anestesia local. Una vez obtenida, la biopsia es preservada a 4ºC en medio de transporte y enviada al Banco de Tejidos para su procesamiento inmediato. Procesamiento Las células del limbo esclerocorneal son obtenidas tras un proceso enzimático de la biopsia limbar. Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits La suspensión celular es expandida ex vivo a 37ºC y 5% de CO2 sobre un soporte de feeder layer. Posteriormente, estas células progenitoras se colocan sobre un sustrato y se implantan en el ojo dañado del propio paciente. Transporte El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) se realiza colocando el envase que contiene las células del limbo esclerocorneal en un contendedor de transporte que contiene acumuladores de frio, manteniendo las células entre 2º y 10ºC hasta su uso. La caducidad para su aplicación es de 6 h desde la preparación. La fecha y hora de preparación y caducidad se indican en la etiqueta y en la documentación adjunta. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 63 PIEL EN GLICEROL BT5003 BT5004 Especificaciones Tejido cutáneo en glicerol obtenido mediante dermatomo con grosor entre 0,5-1,5 mm. BT5003 • Piel entera glicerolizada • Piel mallada glicerolizada Aplicaciones clínicas • Apósito temporal en casos de grandes quemados • Úlceras con difícil cicatrización, úlceras por presión y pie diabético • Cubrimiento para cicatrices en zonas críticas BT5004 Código Descripción Temperatura de conservación BT5003 Piel plana glicerol 2ºC - 10ºC BT5004 Piel en malla glicerol 2ºC - 10ºC 63 PIEL EN GLICEROL Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1/2 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos, que se lleva a cabo dentro de las 24 horas posteriores al fallecimiento, se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva a 4ºC hasta su procesamiento. Procesamiento Todos los procesos realizados bajo el control del Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP), los requerimientos derivados de las autorizaciones de los medicamentos en investigación, los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits de tejidos y células con fines de trasplante, los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. El procesamiento de la piel incluye una primera fase de inmersión del tejido en glicerol estéril al 50%, seguida de una fase en glicerol estéril al 85 % y su almacenamiento definitivo refrigerado a hasta la revisión y aprobación de todos los controles de calidad realizados. Almacenamiento Mantener refrigerado hasta su uso. No utilizar en el caso que alguno de los envoltorios no mantengan su integridad. Transporte El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) consiste en colocar el injerto con acumuladores de frío dentro de un contenedor, manteniendo su integridad en todo momento. La fecha de caducidad del producto es de 5 años desde su procesamiento, la cual consta en la etiqueta y en la documentación adjunta. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 64 PIEL CRIOPRESERVADA BT5001 BT5005 Especificaciones Tejido cutáneo criopreservado obtenido mediante dermatomo con grosor entre 0,5-1,5 mm. BT5001 • Piel entera criopreservada • Piel mallada criopreservada Aplicaciones clínicas • Apósito temporal en casos de grandes quemados • Úlceras con difícil cicatrización, úlceras por presión y pie diabético • Cubrimiento para cicatrices en zonas críticas BT5005 Código Descripción Temperatura de conservación BT5001 Piel plana criopreservada -140ºC - -190ºC BT5005 Piel en malla criopreservada -140ºC - -190ºC 64 PIEL CRIOPRESERVADA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1/2 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos, que se lleva a cabo dentro de las 24 horas posteriores al fallecimiento, se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva a 4ºC hasta su procesamiento. Procesamiento Todos los procesos realizados bajo el control del Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP), los requerimientos derivados de las autorizaciones de los medicamentos en investigación, los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, los requerimientos de gestión de la calidad derivados Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits de las Normas ISO 9001 así como las especificaciones técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. El procesamiento de la piel incluye una fase de descontaminación antibiótica (penicilina, vancomicina y estreptomicina) previa al empaquetado del tejido en doble bolsa y solución crioprotectora con 10% de DMSO. Se procede a la congelación programada y almacenamiento en cuarentena hasta la revisión y aprobación de todos los controles de calidad realizados. Almacenamiento La preservación de los tejidos cutáneos criopreservados se realiza en cubas de nitrógeno, a una temperatura entre -140 y -196ºC. La fecha de caducidad del producto es de 5 años desde su procesamiento siempre que se mantenga la integridad del empaquetado. Transporte El sistema de transporte validado desde el Banco de Tejidos de Barcelona (BTB) consiste en colocar el tejido con hielo seco (-80ºC) dentro de un contenedor externo protegiendo su integridad en todo momento. La temperatura se mantiene dentro de los límites definidos durante 48 horas y se adjuntan instrucciones de uso y descongelación con la documentación del envío. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. 65 MATRIZ DÉRMICA DESCELULARIZADA BT5006 BT5007 BT5008 Especificaciones La matriz dérmica es tejido cutáneo. BT5006 BT5007 Características: • Tejido cutáneo sin epidermis • Mantenimiento de la membrana basal • Sin células en la dermis Aplicaciones clínicas BT5008 • • • • • • • Soporte y relleno en casos de pérdida de tejido blando Relleno y reconstrucción tras exodoncia Quemaduras en cara, cuello, manos Relleno de defectos óseos Reconstrucción maxilofacial Reconstrucción de la pared abdominal Cierre de heridas Código Descripción Dimensiones Grosor (cm) (mm) Temperatura conservación BT5006 Matriz dérmica acelular 2 x 1 0,5 – 1,5 Tª ambiente BT5507 Matriz dérmica acelular 3 x 3 0,5 – 1,5 Tª ambiente BT5008 Matriz dérmica acelular 5 x 11 0,5 – 1,5 Tª ambiente Consultar con el banco la posibilidad de otros tamaños 65 MATRIZ DÉRMICA DESCELULARIZADA Obtención del tejido El tejido procede de donantes a los que se les realiza una minuciosa evaluación de la historia médico-social y una exhaustiva exploración física. El cribado serológico que por defecto se realiza, es el siguiente: HIV-1/2 Anticuerpos, HIV-Antígeno, HIV 1/2 -RNA, HBsAg, HBc Anticuerpos, HBV-DNA, HCV-Anticuerpos, HCV-RNA, Syphilis y HTLV I/II anticuerpos. Asimismo se realiza el cribado microbiológico y las pruebas complementarias que se consideren necesarias. La extracción de los tejidos, que se lleva a cabo dentro de las 24 horas posteriores al fallecimiento, se realiza en quirófano utilizando técnicas estériles. Una vez el tejido es obtenido se preserva a 4ºC hasta su procesamiento. Procesamiento Todos los procesos realizados bajo el control del Banco de Tejidos de Barcelona (BTB) están sujetos a un Sistema de Calidad diseñado para cumplir con los requerimientos establecidos en los principios y guías de las Good Tissue Practices (GTPs) y las Normas de Correcta Fabricación de la Unión Europea (GMP), los requerimientos derivados de las autorizaciones de los medicamentos en investigación, los requerimientos establecidos en el Real Decreto-ley 9/2014, para el procesamiento, preservación y distribución de tejidos y células con fines de trasplante, los requerimientos de gestión de la calidad derivados de las Normas ISO 9001 así como las especificaciones Trazabilidad La utilización clínica de tejidos y células de origen humano proporciona grandes beneficios a los receptores. Como cualquier producto de origen humano, su uso no está exento de riesgos, que aunque poco frecuentes, pueden ser importantes. Es necesario un sistema robusto, capaz de ubicar, localizar e identificar las células y tejidos en cualquier parte del proceso, desde la donación hasta el receptor, para asegurar la intervención rápida. De esta forma, se puede prevenir un daño o riesgo potencial cuando se compromete la calidad y seguridad de los tejidos y células donados. Cada tejido es identificado con un código unívoco que permite el rastreo de origen a destino. Una vez el tejido es trasplantado, el código debe adjuntarse a la historia clínica del receptor. Es obligatorio informar al banco de tejidos de que el mismo ha sido trasplantado Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits técnicas de los propios productos obtenidos asegurando su calidad, seguridad y eficacia. Durante el procesamiento se procede a la eliminación de los fragmentos irregulares. Los tejidos son sometidos a un proceso de descontaminación mediante incubación en antibióticos (penicilina, vancomicina, estreptomicina y anfotericina B). Los fragmentos cutáneos se someten a un proceso de descelularización físico-química con detergentes y sin utilización de enzimas. Finalmente el tejido es almacenado a temperatura ambiente en cuarentena hasta la revisión y aprobación de todos los controles de calidad realizados. Almacenamiento Mantener almacenado a temperatura ambiente hasta su uso. El tejido es empaquetado con doble bolsa, siendo estéril la bolsa interna. No utilizar en el caso que alguno de los envoltorios no mantengan su integridad. Transporte El sistema de transporte validado por el Banco de Tejidos de Barcelona (BTB), consiste en colocar la matriz dérmica envasada en un contenedor externo, protegiendo su integridad en todo momento. La fecha de caducidad es de 5 años, desde su procesamiento, y figura en la etiqueta y en la documentación adjunta. facilitando NHC o iniciales del receptor. Si el tejido no es trasplantado también debe informarse al banco. Biovigilancia Ante la sospecha o evidencia de una reacción o efecto adverso grave en el receptor que pueda estar relacionado con la seguridad y calidad del tejido o células trasplantados, el facultativo debe ponerse inmediatamente en contacto con el banco de tejidos o con la autoridad sanitaria competente. Para cada tejido se facilita un formulario de notificación de reacción adversa o efecto adverso grave. Legislación reguladora de tejidos El Banco de Tejidos de Barcelona cuenta con la autorización administrativa nº E08796463 emitida por la autoridad competente. Las actividades reguladas incluyen la donación, obtención, evaluación, procesamiento, preservación, almacenamiento y distribución. Los tejidos humanos procesados bajo el control del banco cumplen los requisitos recogidos en la legislación española (Real Decreto ley 09/2014) y en la Directiva Europea 2004/23 y las directivas que la desarrollan 2006/17/EC, 2006/86/EC, 2012/39/EU. BTB sigue los estándares de las principales asociaciones científicas: Asociación Española de Bancos de Tejidos (AEBT), European Association of Tissue Banks (EATB), American Association of Tissue Banks (AATB), European Eye Bank Association (EEBA), y las recomendaciones de: Good Tissue Practices (Euro-GTP) y de la Guide to the quality and safety of tissues and cells for human application EDQM del Consejo de Europa. TEJIDO BAJO DEMANDA Varias referencias Algunos tejidos o servicios, ya sea por su escasa demanda o por la especificidad del tejido, están disponibles bajo petición expresa. Tejido cardiovascular El Banco de Tejidos de Barcelona, junto con los especialistas, tiene como objetivo encontrar la mejor solución para ofrecer el tratamiento más adecuado a cada paciente. Si lo que necesita no aparece en este catálogo, contacte con nosotros: [email protected] t 93 557 36 20 bancsang.net/banc-teixits BT4024 Válvula mitral BT4026 Aorta abdominal BT4032 Arteria axilar-humeral BT4040 Arterias axilares-humerales (2 u.) BT4036 Arteria carótida Tejido óseo congelado (GMP) BT2162Astrágalo BT2155 Cabeza de húmero BT2163Calcáneo BT2160 Clavícula BT2161Costilla BT2150Escápula BT2166 Falange mano BT2167 Falange pie BT2164 Metacarpiano BT2165 Metatarsiano BT2154 Húmero 1/2 distal BT2153 Húmero 1/2 proximal BT2134 Tibia 1/2 distal BT2133 Tibia 1/2 proximal BT2130 Tibia 1/3 distal BT2120Rótula BT2119 Cabeza de fémur (1/2) BT2135 Cuña tibial 66 66 TEJIDO BAJO DEMANDA Tejido óseo liofilizado BT3004 CAN_CUB5 - Cubos de esponjosa liofilizada 5 cc BT3005 CAN_CUB15 - Cubos de esponjosa liofilizada 15 cc BT3006 CAN_CUB10 - Cubos de esponjosa liofilizada 10 cc BT3007 CAN_CUB30 - Cubos de esponjosa liofilizada 30 cc BT3041 CL12 - Esponjosa taco cilíndrico BT3042 CL14 - Esponjosa taco cilíndrico BT3043 ID14 - Córtico-esponjosa en taco cilíndrico BT3045 FRAG_ESP_P_L - Fragmento de esponjosa pequeño BT3022 FC - Cóndilo femoral liofilizado BT3002 FH - Cabeza femoral liofilizada BT3044 FIBSP - Fragmento diáfisis peroné Tejido ocular y membrana amniótica BT7001 Globo ocular BT7011 Colirio de sérum autólogo (frasco) BT7012 Colirio de sérum alogénico (frasco) Tejido endocrino y reproductor Para más información: [email protected] t 93 557 3620 f 93 557 3621 bancsang.net/banc-teixits BT6001 Congelación de paratiroides BT6002 Descongelación de paratiroides BT6003 Congelación de semen BT6004 Descongelación de semen BT6005 Congelación de tejido ovárico BT6006 Descongelación de tejido ovárico BT6009 Entrega de una unidad criopreservada