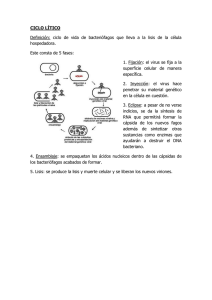
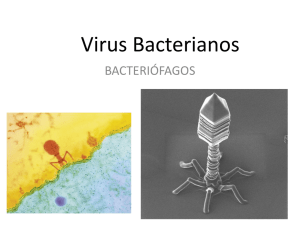
BACTERIOFAGOS
Anuncio

BACTERIOFAGOS 50 x 106 bacteriófagos /ml de agua de mar y cantidad equivalente en suelos Se estiman 1031 bacteriófagos en la Tierra 1 2 Bacteriófagos con Genoma de DNA dc • LÍTICOS : T1 ÆT7 – Se multiplican en Bacterias y matan la célula por lisis al final de su ciclo de vida • Virión complejo: cabeza icosaédrica, cola y fibras • DNA dc linear : 40.000 – 170.000 pb • LISOGÉNICOS (Atemperados) – Alternativamente pueden multiplicarse vía ciclo lítico o entrar en un estado quiescente en la célula donde la mayor parte de los genes no se expresan (lisogénicos) 3 Fagos Líticos Fago T7 • Virión – cabeza icosaédrica, cola corta – DNAdc linear 40.000pb – Genoma 97% codificante • Expresión génica – Genes inmediatos tempranos (RNA polimerasa del huésped): » Proteína inhibitoria del sistema de restricción de la célula huésped » RNA polimerasa T7 » Inhibición de RNA polimerasa de la célula huésped – Genes tempranos y tardíos (T7 RNA polimerasa) » Replicación del genoma (T7 DNA polimerasa) » Proteínas estructurales y ensamblado 4 Fagos Líticos • Replicación del Fago T7 – Origen de replicación único – formación de concatémeros – monómeros Æ endonucleasa específica 5 Uso de algunas características del fago T7 en Biología Molecular ¾ DNA polimerasa T7 Æ Enzima Sequenase (secuenciación de DNA) ¾RNA polimerasa T7 + promotor específicoÆ Vectores de expresión procariota 6 Fagos Líticos FagoT4 Virión Complejo (43 proteínas) -Cabeza icosaédrica -vaina -cuello -placa basal -fibras de la cola -DNAdc linear 170.000pb 7 Fagos Líticos ENTRADA Fago T4 -Adhesión a lipopolisacáridos de superficie -Inyección del material genético Infección viral Æ Degradación masiva del DNA de la célula huesped (nucleasas) Protección del DNA viral: base modificada 5 hidroximetilcitosina , con grupos hidroxilo glicosilados (DNA resistente a endonucleasas) 8 Fagos Líticos Infección del fago T4 Expresión génica en 3 fases (RNA pol de célula huésped + proteínas virales) 1er fase Æ RNA pol celular 2nda fase Æ RNA pol celular + proteínas virales 3ra fase Æ RNA pol celular + nuevo factor sigma 9 Bacteriófagos con Genoma a RNAsc (+) • • • • Icosaédricos Pequeños 26nm Infectan células F+ (pili) Regulación de la expresión por estructura secundaria del RNA – MS2 (E.coli)Æ Genoma de RNA + : 3500nt 5` lisis Prot de maduración cubierta replicasa 3` RNA genómico cad+ (RNAm) 10 Mapa genético y proceso de multiplicación del virus MS2 11 Bacteriófagos Icosaédricos con Genoma a DNA sc • Fago ϕX174 • • • • DNA sc circular 5300 nt 1er DNA secuenciado totalmente 25nm Icosaédrico DNAsc Enz.celulares genoma DNAsc RF DNAdc Replicación (circulo rodante) transcripción traducción Proteínas virales ensamblado 12 Fagos Líticos Terapia con Bacteriófagos Uso de Bacteriófagos en reemplazo o junto con antibióticos – Ventajas • Multiplicación dependiente de la presencia de bacteria blanco • No tóxicos • Específicos (rango estrecho de huésped) Æ no causan daño a la flora normal • Selección de fagos con receptor involucrado en virulencia – Desventajas • EspecíficosÆ hay que conocer previamente el agente infectivo 13 Fagos Lisogénicos •FAGOS LISOGÉNICOS (Atemperados) – Fago Lambda o lamboides » Inserción del genoma en sitios específicos del cromosoma del huésped – Fago Mu » Inserción del genoma en cualquier cromosoma del huésped » Transposición – Fago P1 » Profago no integrado » Mantenimiento como plásmido 14 Fagos Lisogénicos Fago lambda •Cabeza icosaédrica •Cola •1 única fibra •Genoma de ADNdc de 48.000pb •Extremos del genoma sc complementarios (extremos cos)Æ Circularización del genoma al ingresar a la célula y señales de empaquetamiento •Adsorción por unión a receptor: transportador maltosa 15 Fagos Lisogénicos Fago Lambda Eventos que llevan a la Lisogenia: -Circularización del genoma -Recombinación sitio específica (sitios att) -Represión de la expresión del genoma del fago Æ Expresión de Proteína represora Fin Lisogenia (Inducción del profago): -Destrucción de Proteína represora (Señal: condiciones adversas de crecimiento de las bacterias) 16 Fagos Lisogénicos Establecimiento de la Lisogenia o Ciclo Lítico Genes inmediatos tempranos = N y Cro Genes tempranos N, Cro, CII, CIII, CI Genes tardíos: Replicación, proteínas estructurales y lisis 17 Fagos Lisogénicos Usos en Biología Molecular del fago Lambda • Bibliotecas Genómicas • Bibliotecas de Expresión • Cósmidos 18 Cósmidos 19 Fagos Lisogénicos Genotipo y Fenotipo de Bacterias Lisogénicas ¾ Diversificación genómica (E.coli) ¾ Transmisión horizontal de factores de virulencia ÆTransformación de cepas no patógenas en patógenas Factores de virulencia localizados en genomas de bacteriófagos lisogénicos Æ codifican Proteínas que proveen a la bacteria mecanismos de: ¾Invasión de células huésped ¾Evitar defensas inmunes del huésped ¾Daño a células del huésped 20 Ejemplos de toxinas codificadas en bacteriófagos lisogénicos • Toxina colérica (ctxAB) Æ CTXΦ (Vibrio colera) • Toxina diftérica (tox) Æ β-phage (Corynebacterium diphteriae) • Shiga toxina (stx1, 2) Æ H-19B (E.coli) Inducción del profago Æ Multiplicación del virus (ciclo lítico) ¾ Aumento del número de copias del gen (Replicación) ¾Regulación positiva de la expresión Aumento de producción de toxina 21 Bacteriófagos Filamentosos DNA sc • M13, f1, fd (E.coli) • • • • Simetría helicoidal DNA sc circular Infectan células F+ Liberación de la célula sin lísis Æ ensamblado a nivel de membrana citoplasmática acoplado a transporte 22 RF DNAdc Replicación (circulo rodante) Enz. celulares genoma DNAsc transcripción traducción Proteínas virales Copias del genoma DNAsc Ensamblado en la membrana y translocación 23 Usos en Biología Molecular de los Fagos Filamentosos • Vectores de clonado y secuenciación Producción de DNA simple cadena Células infectadas mantenidas en cultivo Espacio intergénico que puede reemplazarse por DNA exógeno • Bibliotecas de Péptidos 24 Usos de virus en Biología Molecular ¾ Vectores de clonado – Secuenciación (M13) – Bibliotecas (fago lambda, cósmidos) ¾ Bibliotecas – Genómicas – Expresión – Péptidos (Fd) ¾ Vectores de Expresión – Baculovirus – Vaccinia ¾ Terapia Génica 25 Terapia Génica • Virus como vectores para transferencia de genes – Blanco principal Enfermedades monogénicas Æ reemplazo de genes alterados » Fibrosis quística (CFTR) » Factores de coagulación » Deficiencias en adenosin-desaminasa (inmunoincompetencia) Aplicación “ex vivo” o “in vivo” 26 Virus usados en terapia génica ¾ Retrovirus – – – – – MLV (virus de leucemia murina)Ævirus defectivos incompetentes en replicación Integración en el genoma de la célula huéspedÆ expresión a largo plazo Infectividad limitada a células en división Capacidad para gen exógeno limitada (8 Kb) Inactivación por complemento ¾ Adenovirus – – – – Sin integraciónÆ Expresión transiente Virus delecionados incompetentes para replicación Capacidad 7.5 Kb Receptores ubicuos ¾ Virus asociados a adenovirus – Integración en sitios específicos del genoma – Amplio rango de células blanco – No asociado a enfermedades ¾ Herpesvirus, Vaccinia, Syndbis virus 27