Ciclo del Si y el S
Anuncio
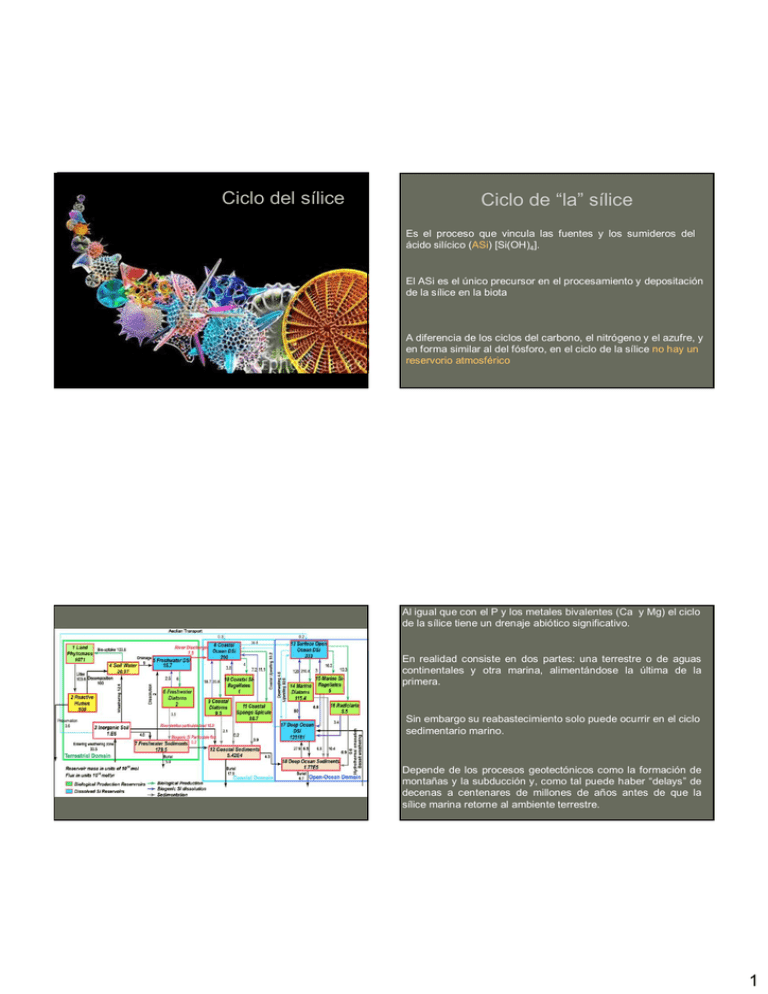
Ciclo del sílice Ciclo de “la” sílice Es el proceso que vincula las fuentes y los sumideros del ácido silícico (ASi) [Si(OH)4]. El ASi es el único precursor en el procesamiento y depositación de la sílice en la biota A diferencia de los ciclos del carbono, el nitrógeno y el azufre, y en forma similar al del fósforo, en el ciclo de la sílice no hay un reservorio atmosférico Al igual que con el P y los metales bivalentes (Ca y Mg) el ciclo de la sílice tiene un drenaje abiótico significativo. En realidad consiste en dos partes: una terrestre o de aguas continentales y otra marina, alimentándose la última de la primera. Sin embargo su reabastecimiento solo puede ocurrir en el ciclo sedimentario marino. Depende de los procesos geotectónicos como la formación de montañas y la subducción y, como tal puede haber “delays” de decenas a centenares de millones de años antes de que la sílice marina retorne al ambiente terrestre. 1 •Las pérdidas sustanciales de ASi biosférico a sumideros abióticos puede compensarse en la naturaleza por su gran abundancia en la corteza terrestre. Es el segundo elemento más abundante en la litosfera (28%; el Fe representa el 35%). En la corteza está presente como silicatos (cuarzo, feldespatos alcalinos y plagioclasas) Estos dos últimos son aluminosilicatos que contribuyen sustancialmente al contenido de Al en la corteza. Todos estos minerales se descomponen por procesos de meteorización Metamorfismo de carbonatos Meteorización La meteorización es fenómeno que más CO2 remueve de la atmósfera, (convierte el CO2 en HCO3- ) release Esta transferencia es una forma importante de control del contenido de CO2 de la atmósfera y por lo tanto del clima global. 2 La meteorización es una función compleja de lluvia, escorrentía, litología, temperatura, topografía y vegetación. La silicificación ocurre en 4 grupos de heterokontos Chrysophyceae (Parmales), Synurophyceae, Bacillariophyceae y Dictyochophyceae Las algas, las plantas y sus microbiotas asociadas afectan directamente la meteorización de los silicatos de diferentes maneras: • generación de quelatos: descomponen minerales y rocas por remoción de cationes metálicos • modificación del pH: producción de CO2 o de ácidos orgánicos como el acético, cítrico, fenólico, etc. • alteración de las propiedades físicas del suelo (particularmente las superficies expuestas de los minerales) Las diatomeas son los mayores contribuyentes a la biosilicificación, debido a que la sílice amorfa es un componente esencial de su pared celular. La disponibilidad de Si es un factor clave en la regulación del crecimiento de las poblaciones en la naturaleza. • Varios millones de años atrás, poco o nada de la vida estaba involucrado en la transformación del ASi en sílice amorfa (SiO2 nH2O) • Los ambientes en que se produjo la evolución geoquímica eran extremadamente ricos en ASi, en relación a las condiciones actuales. • Evidencia: fósiles de algas azules encerradas en sílex. O2 Como contrapartida, el uso de la sílice por las diatomeas domina su reciclado biogeoquímico el mar: cada átomo de Si meteorizado desde la tierra, pasa por las diatomeas un promedio de 39 veces antes de hundirse en el lecho marino 1% 2090 - 2450 MA 21% actual Concomitantemente aumenta el número de organismos capaces de convertir el ASi en sílice. 3 La condensación del ASi y la subsecuente polimerización para formar sílice biogénica, eventualmente resulta en una pérdida neta de ASi en la biosfera. La tasa de la reacción de condensación y polimerización es varios órdenes de magnitud mayor que la reacción inversa (regeneración del pool de ASi) Al aumentar las diatomeas y otras organismos Si-dependientes, se reduce significativamente la concentración del ASi ambiental. Los frústulos se forman en horas o días mientras que la tasa a la cual el ASi retorna a la biosfera via disolución de los frústulos de las diatomeas muertas mientras se hunden en la columna de agua es del orden de los 10-9 mmol m-2 seg-1. Una vez que los frústulos sedimentan, su sílice entra en el ciclo sedimentario de donde probablemente no vuelva a reaparecer en la biosfera por decenas de millones de años. Las diatomeas pueden dividirse en cualquier momento del día. Su independencia de la luz también se extiende a sus requerimientos de nutrientes La captación y acumulación de nitratos y ASi durante la noche utiliza el exceso de Corg sintetizado durante el día. El frústulo juega un rol en la adquisición de CO2. Facilita la conversión enzimática de bicarbonato en CO2 en la superficie celular, regulando el pH (funciona como un buffer) y por ende permitiendo una FS! más eficiente Constituyen un mecanismo de retroalimentación entre la variabilidad climática (disponibilidad de agua e input de ASi), la productividad de las diatomeas y el intercambio de CO2. Mientras que el ASi esté disponible, las diatomeas actúan como conducto para los nutrientes y el carbono hacia aguas profundas, en contraste con otras algas, que "atrapan" los nutrientes en un loop de regeneración en la superficie ↑ ↑ Organismos formadores de Si biogénica ↓↓ Ácido silícico ambiental CaSiO3 + CO 2 CaCO3 + SiO2 Meterorización ↑ ↑ Tasa de meteorización ↑ ↑ consumo de CO 2 ↓ ↓ concentración atmosférica de CO2 ↓ ↓ Efecto invernadero La proliferación de diatomeas y organismos formadores de Si biogénica contribuyó significativamente a la modificación del clima (enfriamiento) a través del ciclo biogeoquímico de la sílice Se estima que contribuyen al 45% de la producción primaria en los océanos, convirtiendolas en los jugadores más importantes en el ciclado de todos los elementos biológicos. Globalmente, captan y procesan 240 Tmol Si yr-1. Actualmente el riesgo para las diatomeas proviene del impacto del clima y fuentes antropogénicas. La reducción del input de sílice debido al endicamiento de ríos y a cambios en el uso del agua, así como los niveles crecientes del aporte inhibidor de amonio en los estuarios y costas adyacentes afectan el éxito de las diatomeas Las elevadas concentraciones de amonio de origen antrópico en algunos estuarios inhiben la captación de nitrato por las diatomeas que lo necesitan para tener sus altas tasas de crecimiento. 4 Como algas captadoras de ASi también debemos mencionar a los sílicoflagelados. Están adaptados para vivir tanto en aguas templadas como heladas. El estadio del ciclo más conocido es una célula desnuda con un esqueleto compuesto por sílice amorfa en una red de barras y espnas ordenadas como una canasta. Este esqueleto es muy suceptible a la disolución y por lo tanto su preservación está obstaculizada por procesos diagenéticos Su abundancia es relativamente baja comparada con otros microfósiles y su presencia no es común en el registro sedimentario. LAS ALGAS Y EL CICLO DEL AZUFRE La mayor parte del azufre de la Tierra está almacenado en rocas y minerales subterráneos, incluyendo las sales sulfatadas enterradas a grandes profundidades en los océanos El ciclo comienza con la meteorización de las rocas liberando el S almacenado CO2 SO2 atmosféricos En contacto con el aire se convierte en SO4 vulcanismo Emisión Depositación Gasificación Fertilizantes Depositación El SO4 es captado por plantas y otros organismos que lo convierten en formas orgánicas S4 SO Ingresa así en la cadena trófica y circula como alimento hasta que los organismos mueren y se descomponen Parte del S se libera otra vez como SO4 y otra parte entra a formar parte de los microorganismos descomponedores S4 y SO sedimentos Erosión SO2 Tierra y biosfera Escorrentía aguas servidas Ciclo sedimentario Ciclo hidrológico SO4 2oceánico Hay una variedad de fuentes naturales que emiten S directamente a la atmósfera, entre otras: • Erupciones volcánicas • Degradación química de materia orgánica en pantanos y pozas de marea • Evaporación del agua 5 CO2 SO2 atmosférico Eventualmente el S precipita en la tierra o cae con la lluvia Hay una pérdida continua de S de los ecosistemas terrestres por drenaje a los cuerpos de agua El gas SO2 o partículas de SO 42- pueden caer o llover desde la atmósfera S4 SO El S también entra a los océanos desde la atmósfera y una parte cicla a través de las comunidades, moviéndose a lo largo de la cadena trófica Las algas y las plantas los toman e incorporan en sus tejidos y pasan a integrar la cadena trófica hasta que mueren y son descompuestos S4 SO Las bacterias son importantes porque pueden transformar en el agua el azufre orgánico en gas H2S, sacándolo del ciclo. Esto puede obstaculizar el crecimiento algal en ambientes donde el S está limitado Una parte de este S es emitido otra vez a la atmósfera en el spray marino El resto se pierde en las profundidades, como sulfuro ferroso, responsable del color negro de la mayoría de los sedimentos marinos Todos los seres vivos requieren azufre como nutriente menor, en aproximadamente la misma proporción atómica que el fósforo. El azufre está presente en el agua en una relación de alrededor de un átomo de S a 100 átomos de Carbono (0.15– 1.96% peso seco) y el contenido de azufre varía con la especie, las condiciones ambientales y la época del año Estos gases pueden reingresar en la atmósfera, el agua y el suelo y continuar el ciclo El S es un elemento esencial para autótrofos y heterótrofos En su estado reducido, juega un rol importante en la estructura y función de las proteínas Tres de los aminoácidos más comunes (cisteina, cistina y metionina) contienen carbonos ligados con azufre También se lo encuentra en sulfolípidos, algunas vitaminas, esteres sulfatado y una variedad de otros compuestos. En estado oxidado, existe como sulfato y es la mayor causa de acidez en el agua de lluvia tanto la natural como la poluida. Las plantas, las algas y las bacterias, excepto algunas anaerobias que requieren S-2, tienen la habilidad de tomar, reducir y asimilar SO42- en aminoácidos y convertirlo en compuestos éster sulfatados Esta relación con la acidez lo hace importante en procesos geoquímicos, atmosféricos y biológicos como la meteorización natural de rocas, lluvia ácida y la tasa de desnitrificación. 6 El ciclo del azufre es otro de los ciclos elementales duramente perturbados por la actividad humana La emisión de S por actividad antrópica es igual o mayor que la natural Los volcanes inyectan intermitentemente compuestos azufrados en la atmósfera y una corriente continua de esos compuestos proviene de la actividad industrial Al igual que el nitrógeno, el azufre existe bajo diferentes formas, como gases o partículas de ácido sulfúrico La duración de muchos compuestos azufrados en el aire es relativamente corta (días) Sin embargo, hay procesos sedimentarios extremadamente lentos de erosión, sedimentación y exposición de rocas que contienen S. Mezclados con vapor de agua forman el smog de ácido sulf Compuestos volátiles de azufre, que son liberados en la atmósfera rica en oxígeno, son oxidados químicamente durante su estadía en la atmósfera y terminan como dióxido de azufre, ácido sulfúrico, sulfato particulado y sulfonato de metano Además de contribuir a la lluvia ácida, las gotas de ácido sulf Estos compuestos son removidos de la atmósfera y devueltos a la Tierra por forman una capa de neblina que refleja la radiación solar causando deposición húmeda y seca. un enfriamiento de la superficie terrestre Bajo condiciones óxicas, el estado oxidado del S en ácido sulfúrico es el más estable, el sulfato es la forma predominante de S en aguas y suelos óxicos Por lo tanto la reducción del sulfato a una especie más reducida de S es un prerequisito para la formación de compuestos volátiles y su emisión a la atmósfera Los procesos bioquímicos que llevan a esta reducción pueden ser considerados como los forzantes del ciclo atmosférico 7 Hay dos tipos de vías de reducción del sulfato que son importantes en el ciclo global: la reducción desasimilatoria y la asimilatoria . La 1ª es estrictamente anaeróbica y la realizan bacterias sulfatoreductoras para respirar en ambientes anóxicos, usando sulfato como último aceptor de electrones en lugar de oxígeno. Como la concentración de sulfato es alta en el agua de mar, este proceso es importante en ecosistemas marinos, incluyendo las marismas A diferencia de los animales que dependen de compuestos organosulfurados en su dieta, las bacterias, las algas, los hongos y las plantas pueden obtener S de la reducción asimilatoria para la síntesis de compuestos organosulfurados El SO42- es asimilado desde el ambiente, reducido dentro de las células y fijado en aminoácidos u otros compuestos orgánicos Este proceso ocurre en ambientes tanto óxicos como anóxicos Gran parte del Azufre reducido es fijado por procesos de asimilación intracelular y solo una fracción menor del S reducido se libera como compuestos gaseosos volátiles, mientras los organismos están vivos Luego de su muerte, la degradación microbiana libera al ambiente compuestos reducidos (principalmente bajo la forma de H2S, dimetil sulfuro [DMS] y también como sulfuros orgánicos. 8 Muchas algas marinas, microalgas (Prymnesiophyta, Dinophyta, diatomeas, Chrysophyta y Prasinophyta) y macroalgas (clorofitas y rodofitas) producen cantidades de dimetilsulfonio (DMSP) a partir de metionina Clima Pérdida a la atmósfera El DMSP es el precursor del DMS, que es un gas fuertemente oloroso y que es la mayor fuente de S atmosférico. Temperatura DMS Los organismos marinos producen casi la mitad del S biogénico emitido anualmente a la atmósfera y la mayor parte es producido como DMS. Como otros compuestos reducidos, el DMS se oxida rápidamente a dióxido de azufre que funciona como núcleo de condensación de nubes (CCN) y puede afectar el clima a escala global Otra peculiaridad: las aves usan DMS como una señal de alimentación, como las algas al ser consumidas por los peces liberan DMS, llaman la atención de las aves sobre la presencia de los peces DMSP en las algas Luz Nutrientes Transformación bacteriana DMSP libre PASTOREO, Muerte celular y lisis Sedimentación Ciclo del DMS (dimetil sulfuro) en el mar El DMSP puede funcionar como osmorregulador, para el control de la flotación, crioprotector y antioxidante Con la excepción de unas pocas cyanobacteria, las algas continentales no lo producen (usan glicerol) También se ha postulado que su producción está relacionada indirectamente con la el nitrógeno en las algas, como un reservorio del exceso de sulfato captado para la síntesis de nitrato reductasa o nitrogenasa Esto también podría ser cierto para las plantas con alta actividad de nitratoreductasa o con bacterias simbiontes fijadoras de N2 Calentamiento global 9 En esta etapa, los compuestos volátiles pueden escapar a la atmósfera. Sin embargo como ocurre en la vía desasimilatoria, los sulfuros liberados durante la descomposición son químicamente inestables en ambientes óxicos y son reoxidados a sulfatos por una variedad de microorganismos. El clivaje del DMSP por medio de la enzima DMSP liasa produce DMS y ácido acrílico. El DMSP también puede ser liberado durante la senecencia de las células del fitoplancton y se piensa que el pastoreo del zooplancton en células saludables también facilita la liberación de DMSP Una vez liberado de las células algales, el DMSP se convierte por acción bacteriana en DMS y acrilato 10