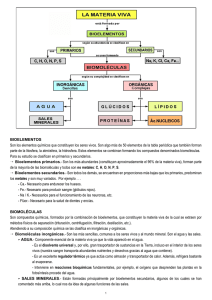
Bioelementos. Biomoléculas inorgánicas.
Anuncio

UD 1. LA MATERIA VIVA: BIOELEMENTOS Y BIOMOLÉCULAS. ANEXO: Tipos de enlaces y formas de representar las moléculas 1. BIOELEMENTOS O ELEMENTOS BIOGÉNICOS Son los elementos químicos que se encuentran en la materia viva. Clasificación Primarios. 96,2 % de la materia viva, Plásticos:Componentes fundamentales de las biomoléculas. C, H, O, N, P y S Secundarios: proporciones muy pequeñas, en forma iónica generalmente. de los bioelementos: Na+, K+, Cl-,Ca2+ y Mg2+ Oligoelementos: vestigiales(<0,1 %). Función catalítica. Fe, Cu, Zn, Mn y Co : indispensables (universales) B, Al, V, Mo, I y Si : variables (sólo están presentes en algunos organismos) 1.BIOELEMENTOS 1. BIOLELEMENTOS: PRINCIPALES CARACTERÍSTICAS DE LOS BIOELEMENTOS PRIMARIOS Aunque no son los más abundantes, se encuentran con facilidad en capas externas de la Tierra. Masa atómica pequeña (CHON), variabilidad de valencias Forman enlaces muy estables. Sus compuestos presentan polaridad solubles en agua (fácil incorporación y eliminación). C y N presentan la misma afinidad para unirse al O o al H por lo que pasan con la misma facilidad de estado oxidado a reducido. 1. BIOELEMENTOS: PROPIEDADES DEL CARBONO Átomo mayoritario en la materia viva (62%) idóneo para constituir los seres vivos debido a: Tetravalencia: Capacidad de unión entre sí: posee 4 electrones en su capa externa por lo que puede formar 4 enlaces covalentes muy estables. A través de enlaces covalentes simples, dobles o triples, dando lugar a cadenas lineales, ramificadas, cíclicas, con conformaciones tridimensionales algunas funciones requieren 3D Capacidad de unirse a otros elementos formando radicales muy diversos =O, -OH, -NH2 … Pueden formarse muchos compuestos químicos distintos posibilitan reacciones químicas de los seres vivos 2. BIOMOLÉCULAS Los bioelementos se unen entre sí para formar las moléculas que constituyen los seres vivos, llamadas biomoléculas. INORGÁNICAS: no exclusivas de los seres vivos Agua Sales minerales Algunos gases (CO2, O2) ORGÁNICAS: constituidas básicamente por polímeros de carbono. Exclusivas de los seres vivos. Glúcidos Lípidos Proteínas Ácidos Nucleicos 2. BIOMOLÉCULAS Átomos de los bioelementos Unidos por enlace iónico Sales minerales Agua Principios inmediatos no exclusivos de la materia viva Unidos por enlace covalente Glúcidos Lípidos Proteínas Nucleótido s Principios inmediatos exclusivos de la materia viva 2. BIOMOLÉCULAS: PROPIEDADES Su función depende de la forma y del tamaño (análisis químico y biológico). La mayoría son macromoléculas, en muchos casos polímeros formados por la unión de moléculas sencillas (monómeros). Formadas por esqueletos hidrocarbonados. Sustitución de hidrógenos grupos funcionales (propiedades f/q) 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA ESTRUCTURA H 2O Molécula DIPOLAR 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA PROPIEDADES Gran poder disolvente 2. Elevado calor específico 3. Elevado calor de vaporización 4. Gran conductividad 5. Elevada fuerza de cohesión y adhesión 6. Elevada tensión superficial 7. Reducida viscosidad 8. Mayor densidad en estado líquido que en estado sólido 9. Elevada reactividad química 1. 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA PROPIEDADES: gran poder disolvente NOTA: Solubilidad de las biomoléculas: * Son solubles: - Iones inorgánicos y orgánicos (grupos ácidos y aminos) - Las moléculas polares (alcoholes, tioles). * Son insolubles: - Las moléculas apolares (moléculas con mucho C e H). 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA P: gran poder de disolución Función relacionada: Transporte de sustancias Tanto el plasma sanguíneo en los animales como la savia en los vegetales contienen una altísima proporción de agua. 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA P: elevado calor específico, de vaporización y gran conductividad Función relacionada: Termorregulación El agua amortigua los cambios de temperatura. Frente a un cambio fuerte de Tª ambiental el agua del interior del ser vivo, permite que el cambio sea más lento y que se reparta por todo el cuerpo. 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA P: Elevada tensión superficial Función relacionada: este hecho es aprovechado para provocar deformaciones citoplasmáticas, para la ascensión de la savia bruta por los el xilema por el efecto de capilaridad*, para la formación de pseudópodos, etc,,, 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA P: Elevada cohesión y adhesión/ tensión superficial. Función relacionada: ascensión de la savia bruta por los el xilema por el efecto de capilaridad. Estructural actúa como esqueleto hidrostático en vegetales gracias a su incompresibilidad. (debido a cohesión) 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA P: reducida viscosidad Función relacionada: Lubricante. reduce el rozamiento entre estructuras deslizantes. Ej. Líquido sinovial en articulaciones 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA P: reactividad química (capacidad de disociarse en iones) Función: Produce hidrólisis, es decir, ruptura de enlaces moleculares por el agua. Disociación del agua Hidrólisis de un disacárido 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA P: mayor densidad en estado líquido que sólido. Función asociada: permite supervivencia de seres vivos acuáticos a temperaturas bajo cero. El agua líquida tiene una estructura polimérica y el hielo tiene una estructura reticular. 3. BIOMOLÉCULAS INORGÁNICAS: EL AGUA FUNCIONES BIOLÓGICAS Transportadora Termorreguladora Lubricante Bioquímica Estructural Otras funciones específicas: ascensión de savia bruta, absorción de sustancias por las raíces, permite la vida bajo la capa de hielo en ecosistemas acuáticos, etc… 3. BIOMOLÉCULAS INORGÁNICAS: LAS SALES MINERALES Sólidas o precipitadas: o Función estructural: CaCO3 forma el esqueleto de vertebrados, crustáceos, moluscos, corales, equinodermos… Ca3 (PO4)2 endurece huesos de vertebrados SiO2 endurece tallos de gramíneas, caparazón de diatomeas y radiolarios… Otras: otolitos (CaCO3) para mantener el equilibrio, partículas de magnetita para orientación… Disueltas en forma iónica. Estas últimas realizan las siguientes funciones: Regulan el equilibrio ácido-base Regulan los fenómenos osmóticos Función de regulación o catalítica Proporcionan estabilidad a los coloides 3. BIOMOLÉCULAS INORGÁNICAS: LAS SALES MINERALES REGULACIÓN DEL PH Ionización del agua y pH 3. BIOMOLÉCULAS INORGÁNICAS: LAS SALES MINERALES REGULACIÓN DEL PH LOS SISTEMAS TAMPÓN Mantienen constante el pH Suelen ser disoluciones de sales de ácidos o bases débiles, cuyo equilibrio químico es capaz de aceptar o ceder protones al medio. 3. BIOMOLÉCULAS INORGÁNICAS: LAS SALES MINERALES REGULACIÓN DEL PH 3. BIOMOLÉCULAS INORGÁNICAS: SALES MINERALES REGULACIÓN DE LOS PROCESOS OSMÓTICOS LOS SISTEMAS TAMPÓN (amortiguadores) Mantienen constante el pH Suelen ser disoluciones de sales de ácidos o bases débiles, cuyo equilibrio químico es capaz de aceptar o ceder protones al medio. Cuando aumentan los protones, el equilibrio se desplaza a la derecha Cuando disminuyen los protones, el equilibrio se desplaza a la izquierda 3. BIOMOLÉCULAS INORGÁNICAS: LAS SALES MINERALES Sistema tapón: Bicarbonato (en líquidos extracelulares) Capacidad de amortiguación: pH 7,4 3. BIOMOLÉCULAS INORGÁNICAS: LAS SALES MINERALES Sistema tapón: Fosfato (medio intracelular) pH 6,86 Capacidad de amortiguación: pH 6,86 3. BIOMOLÉCULAS INORGÁNICAS: LAS SALES MINERALES Según el movimiento de las partículas de soluto en el disolvente se pueden distinguir tres fenómenos: 3. BIOMOLÉCULAS INORGÁNICAS: SALES MINERALES REGULACIÓN DE LOS PROCESOS OSMÓTICOS Ósmosis: Es un tipo de difusión pasiva en la que se moviliza el agua. Tipos de disoluciones según su concentración: Hipertónica: más concentrada Isotónicas: igual concentración Hipotónicas: menos concentrada Movimiento de partículas: siempre desde la más concentrada a la más diluida. 3. BIOMOLÉCULAS INORGÁNICAS: SALES MINERALES REGULACIÓN DE LOS PROCESOS OSMÓTICOS FENÓMENOS OSMÓTICOS Efecto sobre las células Hipertónicas: Plasmólisis / crenación Isotónicas: Nada Hipotónicas: Turgencia o turgescencia / hemólisis 3. BIOMOLÉCULAS INORGÁNICAS: SALES MINERALES REGULACIÓN DE LOS PROCESOS OSMÓTICOS Turgescencia / Hemólisis Retracción / Crenación 3. BIOMOLÉCULAS INORGÁNICAS: SALES MINERALES FUNCIÓN CATALÍTICA Iones Función catalítica o reguladora Na+: Mantenimiento del equilibrio iónico en el medio extracelular Transmisión de la corriente nerviosa Mantenimiento del potencial de membrana en las células K+: Contracción muscular. Regulación de la actividad cardiaca Transmisión de la corriente nerviosa Ca2 +: Coagulación de la sangre Contracción muscular Transmisión sináptica Activador y cofactor de algunas enzimas Cl-: Mantenimiento del equilibrio iónico en el medio extracelular Transmisión de la corriente nerviosa Mantenimiento del potencial de membrana en las células 3. BIOMOLÉCULAS INORGÁNICAS: LAS SALES MINERALES LAS DISPERSIONES COLOIDALES Soluto no soluble (partículas de gran tamaño): no se dispersa homogéneamente. Id: Dispersan la luz. Turbidez. Estados: Sol: fluido Gel: gelatinoso (resistencia al movimiento del soluto) Sol Gel * La mayoría de las moléculas orgánicas forman dispersiones coloidales Las sales estabilizan dispersiones coloidales Ej jabones *Si se produce deshidratación, se coagula y deja de ser reversible. Apéndice: Fórmulas en química orgánica (tipos de representaciones moleculares) o Fórmula molecular TIPOS DE REPRESENTACIONES MOLECULARES FÓRMULA MOLECULAR FÓRMULA SEMIDESARROLLADA FÓRMULA DESARROLLADA REPRESENTACIONES ESPACIALES MODELO DE VARILLA MODELO COMPACTO