Trastornos del nervio óptico
Anuncio

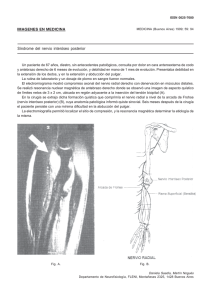
Capítulo 623 Trastornos del nervio óptico & e623-1 © ELSEVIER. Fotocopiar sin autorización es un delito. HIPOPLASIA DEL NERVIO ÓPTICO La hipoplasia del nervio óptico es una enfermedad no progresiva que se caracteriza por un número escaso de axones nerviosos, con normalidad de los elementos mesodérmicos y del tejido glial de soporte. En los casos típicos, la cabeza del nervio óptico es pequeña y pálida, con un halo peripapilar pálido o pigmentado (signo del doble anillo). Esta anomalía se asocia con defectos visuales y campimétricos de gravedad variable, desde ceguera hasta una visión normal o casi normal. Puede asociarse con anomalías sistémicas, sobre todo del sistema nervioso central (SNC). Son muy diversos los defectos del SNC que acompañan a la hipoplasia del nervio óptico, desde hidranencefalia o anencefalia hasta lesiones más focales compatibles con la vida, aunque también puede haber casos de hipoplasia unilateral o bilateral del nervio óptico sin defectos concomitantes. La hipoplasia del nervio óptico es la principal característica de la displasia septoóptica de De Morsier, un trastorno congénito en el que se asocian anomalías de estructuras de la línea media del encéfalo con hipoplasia del nervio, el quiasma y las cintillas ópticas; típicamente se encuentra agenesia del septo pelúcido, agenesia parcial o completa del cuerpo calloso y malformación del fórnix, con una cisterna quiasmática grande. Los pacientes pueden sufrir anomalías hipotalámicas y defectos endocrinos, desde panhipopituitarismo hasta deficiencia aislada de hormona del crecimiento, hipotiroidismo o diabetes insípida. La hipoglucemia y las convulsiones neonatales son signos de presentación importantes en los niños afectados (cap. 585). La RM es la técnica de elección para detectar anomalías del SNC en pacientes con hipoplasia del nervio óptico. Durante la RM, debe prestarse especial atención al infundíbulo hipofisario, donde puede hallarse ectopia de la hipófisis posterior. La ectopia hipofisaria posterior se observa en la RM como una ausencia del infundíbulo con un punto brillante anormal en el área del infundíbulo superior. Esta anomalía aparece en aproximadamente el 15% de los pacientes y sugiere deficiencia de las hormonas de la hipófisis posterior, por lo que deben realizarse estudios endocrinológicos. La hipoplasia sutil bilateral es difícil de diagnosticar, al no poderse comparar el aspecto de una papila con el otro ojo no afectado. Sin embargo, resulta importante establecer este diagnóstico para evitar confusiones con la atrofia óptica o el glaucoma y explicar la causa de la mala visión en un paciente que no responde a la terapia para la ambliopía. En los pacientes con hipoplasia del nervio óptico debe vigilarse de cerca la función endocrina. No se ha aclarado la etiología de la hipoplasia del nervio óptico. Los agentes que en las fases precoces de la gestación actúan sobre las estructuras de la línea media del SNC, causando daño axonal secundario o disrupción de los mecanismos normales de orientación neuronal del nervio óptico y las neuronas cerebrales, pueden explicar la asociación de estos trastornos. La hipoplasia del nervio óptico es más frecuente en hijos de madres diabéticas y se ha asociado con el consumo materno de fenitoína, quinina, LSD (dietilamida de ácido lisérgico) y alcohol durante el embarazo. Otros factores de riesgo son el trabajo de parto prematuro, la hemorragia vaginal gestacional, la baja ganancia de peso materna y la pérdida de peso durante el embarazo en las primíparas jóvenes. Los niños con leucomalacia periventricular muestran una forma atípica de hipoplasia del nervio óptico. Las papilas tienen un diámetro normal con una excavación grande. Esta forma de hipoplasia del nervio óptico se debe a degeneración transináptica de los axones ópticos causada por lesión bilateral primaria de las radiaciones ópticas (leucomalacia periventricular). [(Figura_1)TD$IG] Figura 623-1 Coloboma del nervio óptico. rretinianos y del iris. Los colobomas del nervio óptico pueden verse en numerosas anomalías oculares y sistémicas, como la asociación CHARGE (coloboma, cardiopatía [heart disease], atresia de coanas, retraso del crecimiento y el desarrollo y/o anomalías del sistema nervioso central, anomalías genéticas y/o hipogonadismo, malformaciones auditivas [ear anomalies] y/o hipoacusia). ANOMALÍA PAPILAR DE DONDIEGO DE DÍA La anomalía papilar de dondiego de día (morning glory) es una malformación congénita del nervio óptico caracterizada por una papila grande y excavada en forma de embudo con un reborde elevado, de manera que su aspecto recuerda al dondiego de día. Existe tejido glial blanquecino en la parte central de la papila. Los vasos retinianos son anormales, surgen de la periferia papilar y atraviesan radialmente el reborde rosáceo elevado. Suele haber moteado pigmentado del área peripapilar. La mayoría de los casos son unilaterales y las niñas se afectan dos veces más que los niños. La agudeza visual está en general muy reducida y se produce desprendimiento de retina en aproximadamente 1/3 de los casos. Se ha establecido una asociación entre esta anomalía y los encefaloceles basales en pacientes con alteraciones de la línea media. También se han observado anomalías de la circulación carotídea en pacientes con este trastorno papilar. La enfermedad de Moyamoya puede ser un hallazgo asociado. PAPILA INCLINADA La papila inclinada es una anomalía congénita en la que el eje vertical de la papila tiene una orientación oblicua, de forma que la porción temporal superior de la cabeza del nervio es más prominente y anterior que la porción nasal inferior. Los vasos retinianos emergen de la parte temporal superior de la papila más que de la zona nasal. A menudo se observa una semiluna o cono peripapilar y puede encontrarse astigmatismo miópico o defectos campimétricos asociados. Es importante la identificación clínica de este síndrome para evitar confusiones, debido a su aspecto y a los campos visuales, con el papiledema o tumores intracraneales. COLOBOMA DEL NERVIO ÓPTICO Los colobomas del nervio óptico pueden ser unilaterales o bilaterales. La agudeza visual varía desde normal hasta la ceguera completa. El coloboma se forma debido al cierre incompleto de la hendidura embrionaria. El defecto puede producir una excavación papilar parcial o total (fig. 623-1). También puede haber colobomas corio- DRUSAS DEL NERVIO ÓPTICO Las drusas del nervio óptico son cuerpos globulares acelulares que parecen proceder de derivados axoplásmicos de fibras nerviosas desintegradas. Las drusas pueden permanecer enterradas dentro del nervio, haciendo que se eleve la papila (lo que puede confundirse e623-2 & Parte XXIX Enfermedades oculares con un papiledema), o estar parcial o totalmente expuestas, viéndose como cuerpos refringentes en la superficie papilar. Se asocian con defectos del campo visual y con hemorragias espontáneas en la capa de fibras nerviosas peripapilares. A veces se heredan con un patrón autosómico dominante. Se han observado en niños con diversos trastornos neurológicos, como megalencefalia primaria, convulsiones, trastornos del aprendizaje, retraso mental, esquizofrenia, esclerosis tuberosa, síndrome de Down y tumores intracraneales. La ecografía B puede ayudar a identificar los casos en los que se sospechen drusas en la exploración clínica. PAPILEDEMA El término papiledema se reserva para describir la tumefacción de la cabeza del nervio óptico secundaria a aumento de la presión intracraneal (PIC). Sus manifestaciones clínicas consisten en borramiento edematoso de los límites de la papila, repleción o elevación de la cabeza del nervio óptico, obliteración parcial o completa de la excavación papilar, congestión capilar e hiperemia de la cabeza del nervio, ingurgitación venosa generalizada, pérdida del latido venoso espontáneo, hemorragias en la capa de fibras nerviosas y exudados peripapilares (v. fig. 584-2). En ocasiones, el edema se extiende a la mácula y adopta una forma de abanico o estrella. A veces se observan pliegues concéntricos en la retina peripapilar (líneas de Paton). Pueden producirse oscurecimientos transitorios de la visión, de pocos segundos de duración y asociados con cambios de postura. Sin embargo, la visión suele ser normal en el papiledema agudo. Por lo general, cuando se normaliza la PIC desaparece el papiledema en forma gradual a lo largo de 6-8 semanas. Sin embargo, el papiledema crónico por aumento prolongado de la PIC produce en ocasiones lesión permanente de fibras nerviosas, cambios atróficos en la papila, cicatrización macular y pérdida de visión. Se cree que la fisiopatología del papiledema es del siguiente modo: elevación de la presión del líquido cefalorraquídeo (LCR) subaracnoideo intracraneal, elevación de la presión del LCR en la vaina del nervio óptico, elevación de la presión tisular en el nervio óptico, estasis del flujo axoplásmico y tumefacción de las fibras nerviosas en la cabeza del nervio óptico, y cambios vasculares secundarios, con los típicos signos oftalmoscópicos de estasis venosa. En bebés y niños con aumento de la PIC pueden presentarse otros signos neuroftalmológicos, como parálisis del VI par con la consiguiente endotropia, retracción palpebral, paresia de la mirada superior, desviación tónica hacia abajo de los ojos y nistagmo convergente. La etiología del papiledema en la infancia suele corresponder a tumores intracraneales e hidrocefalia obstructiva, hemorragia intracraneal, edema cerebral traumático, meningoencefalitis y encefalopatía tóxica, y ciertos trastornos metabólicos. Cualquiera sea la causa, en ocasiones se modifican los signos papilares de hipertensión intracraneal por la distensibilidad del cráneo infantil. En ausencia de enfermedades asociadas con cierre precoz de las suturas y obliteración precoz de la fontanela (craneosinostosis, enfermedad de Crouzon y síndrome de Apert), los niños con aumento de PIC pueden no desarrollar papiledema. El diagnóstico diferencial incluye cambios estructurales de la papila (seudopapiledema, seudoneuritis, drusas y fibras mielinizadas), con los que puede confundirse, y la tumefacción papilar por hipertensión y diabetes mellitus. A menos que la mácula esté afectada por hemorragias o edema retiniano, la conservación de una buena visión central y la ausencia de defecto pupilar aferente (pupila de Marcus Gunn) sirven para diferenciar el papiledema agudo del edema de la cabeza del nervio óptico en la neuritis óptica aguda. El papiledema es una urgencia neurológica. Puede ir acompañado de otros signos de hipertensión intracraneal, como cefaleas, náuseas y vómitos. Deben realizarse pruebas de neuroimagen; si no se detectan masas intracraneales, se procederá a una punción lumbar con medición de la presión del LCR. NEURITIS ÓPTICA La neuritis óptica es cualquier inflamación, desmielinización o degeneración del nervio óptico con deterioro de su función. El proceso suele ser agudo, con pérdida de visión de progresión rápida. El comienzo de los síntomas visuales puede verse precedido o acompañado de dolor al mover el globo o a la palpación. Hay disminución de agudeza visual, alteraciones de la sensibilidad al contraste y la visión cromática, defecto pupilar aferente relativo y normalidad de la mácula y la retina periférica. Cuando se afecta la porción retrobulbar del nervio sin signos oftalmoscópicamente visibles de inflamación en la papila, se aplica el término de neuritis óptica retrobulbar. En la papilitis o neuritis óptica intraocular existen signos oftalmoscópicos de inflamación en la cabeza del nervio. Si se afectan la retina y la papila, se habla de neurorretinitis. En la infancia, la neuritis óptica puede aparecer como una enfermedad aislada o ser la manifestación de una enfermedad neurológica o sistémica. Puede ser secundaria a enfermedades inflamatorias, infecciones, exposición a toxinas o déficit de nutrientes. Entre las enfermedades inflamatorias se encuentran el lupus eritematoso sistémico, la sarcoidosis, la enfermedad de Behçet y la neuritis óptica autoinmunitaria. Entre las infecciones se deben tener en cuenta la tuberculosis, la sífilis, la enfermedad de Lyme, la meningitis, la encefalitis vírica y la infección por el VIH; la neuritis óptica también puede ser una reacción postinfecciosa. Entre las toxinas se encuentran el metanol, el plomo y el etambutol. El déficit nutricional más frecuente es la hipovitaminosis B12. La neuritis óptica también puede representar uno de los diversos trastornos desmielinizantes infantiles (caps. 593; 593.2). Aunque un porcentaje significativo de adultos que sufren un episodio de neuritis óptica terminan por desarrollar otros síntomas de esclerosis múltiple (EM), el riesgo parece ser bajo en los niños con este trastorno (riesgo de EM del 19% a los 20 años). La neuritis óptica bilateral en niños se asocia con neuromielitis óptica (enfermedad de Devic; cap. 593.2). Este síndrome se caracteriza por rápida pérdida de visión grave y bilateral acompañada de mielitis transversal y paraplejía. La neuritis óptica también es en ocasiones una complicación del tratamiento prolongado con dosis altas de cloranfenicol o vincristina. Suele ser necesaria una investigación neuropediátrica y oftalmológica exhaustiva, que incluya estudios como la RM y la punción lumbar. En la mayoría de los casos de neuritis óptica, la visión empieza a mejorar al cabo de 1-4 semanas y se normaliza después de varias semanas o meses. La evolución depende de la etiología. Aunque la visión central puede recuperarse por completo, es frecuente encontrar defectos permanentes en otras funciones visuales, como la sensibilidad al contraste, la visión cromática, la sensación de brillo y la percepción del movimiento. La neuritis óptica puede recidivar, sobre todo, aunque no siempre, en pacientes que padecerán EM. Un ensayo terapéutico ha demostrado que la metilprednisolona intravenosa a dosis elevada acelera la recuperación visual en adultos jóvenes y puede prevenir la aparición de EM en sujetos con riesgo. No deben emplearse corticoides por vía oral porque se asocian con un aumento significativo de la tasa de recurrencias de la neuritis óptica. Se desconoce hasta qué punto estos resultados pueden extrapolarse a la neuritis óptica infantil. En adultos con lesiones de la sustancia blanca en la RM, el tratamiento con interferón b (1a o 1b) reduce la incidencia de EM. NEUROPATÍA ÓPTICA DE LEBER La neuropatía óptica de Leber se caracteriza por pérdida repentina de la visión central en la 2.a o 3.a década de la vida, que afecta sobre todo a varones jóvenes. Se observa una típica microangiopatía telangiectásica peripapilar, no sólo en la fase presintomática de los ojos afectados, sino también en un gran número de familiares asintomáticos vinculados por la línea materna. La hiperemia papilar y el edema indican la fase aguda de pérdida visual. Por lo general se afecta un ojo antes que el otro. También hay defectos del campo Capítulo 623 Trastornos del nervio óptico & e623-3 visual y la visión cromática. Con el paso del tiempo suele instaurarse atrofia óptica progresiva y pérdida de visión. La angiopatía tortuosa se hace menos ostensible. Aunque la función visual por lo común se mantiene estable después de la pérdida inicial, por lo general se produce una recuperación considerable o incluso completa en hasta 1/3 de los pacientes. Esta recuperación puede tardar años o décadas desde el episodio inicial de pérdida visual. La angiopatía peripapilar, la ausencia de mejoría a corto plazo y el grado de simetría permiten distinguir la mayoría de los casos de enfermedad de Leber de la neuritis óptica de la EM. La neuropatía óptica de Leber se hereda de la madre y su causa radica en una mutación del ADN mitocondrial. Se han descrito múltiples mutaciones puntuales, observándose la mutación G1177A en el 50% de los casos. Debido a la naturaleza mitocondrial del trastorno, también pueden encontrarse alteraciones miocárdicas y de músculos esqueléticos, así como anomalías electrocardiográficas, en los individuos afectados. Se están realizando ensayos terapéuticos genéticos para prevenir la ceguera. ATROFIA ÓPTICA La atrofia óptica consiste en la degeneración de los axones del nervio óptico, con la correspondiente pérdida de función. Los signos oftalmoscópicos de atrofia óptica son palidez papilar y pérdida de sustancia en la cabeza del nervio óptico, a veces con aumento de la excavación. El defecto de visión asociado depende de la naturaleza y el sitio de la alteración o lesión primaria. La atrofia óptica es la expresión común de gran variedad de procesos patológicos congénitos o adquiridos. Puede ser de origen traumático, inflamatorio, degenerativo, neoplásico o vascular; los tumores intracraneales y la hidrocefalia son la principal causa de este trastorno en niños. En ocasiones, la atrofia óptica progresiva es hereditaria. La atrofia óptica infantil de herencia dominante es una lesión heredodegenerativa relativamente leve que tiende a progresar durante la infancia y la adolescencia. La atrofia óptica congénita autosómica recesiva es un trastorno raro presente al nacer o poco después, con un defecto de visión en general profundo. La atrofia óptica de Behr es hereditaria y se asocia con hipertonía de las extremidades, hiperreflexia tendinosa profunda, ataxia cerebelosa leve, cierto grado de retraso mental y posible oftalmoplejía externa. Afecta principalmente a niños de entre 3 y 11 años. Algunas formas de atrofia óptica heredodegenerativa se asocian con sordera neurosensorial, como ocurre en niños con diabetes mellitus de tipo 1. En ausencia de una causa evidente, la atrofia óptica infantil obliga a un estudio etiológico exhaustivo. © ELSEVIER. Fotocopiar sin autorización es un delito. GLIOMA DEL NERVIO ÓPTICO El glioma del nervio óptico (cap. 491), más correctamente denominado astrocitoma pilocítico infantil, es el tumor más frecuente del nervio óptico en niños. Este tumor neuroglial puede desarrollarse en la porción intraorbitaria, intracanalicular o intracraneal del nervio y afecta con frecuencia al quiasma. El tumor es un hamartoma citológicamente benigno que suele ser estacionario o de progresión lenta. Las principales manifestaciones clínicas de los tumores de la porción intraorbitaria del nervio son pérdida de visión unilateral, proptosis y desviación del ojo; puede aparecer atrofia óptica o congestión papilar. Hay que sospechar afectación quiasmática si existen defectos de la visión o el campo visual compatibles (es frecuente la hemianopsia bitemporal), aumento de la PIC, papiledema o atrofia óptica, disfunción hi- potalámica, disfunción hipofisaria y, en ocasiones, nistagmo o estrabismo. Los astrocitomas pilocíticos infantiles son más frecuentes en los pacientes con neurofibromatosis. El tratamiento de los gliomas ópticos en la actualidad es controvertido. Lo mejor suele ser la observación periódica con radiografías repetidas (preferiblemente con RM). El tratamiento debe reservarse a los pacientes sintomáticos o con gliomas del nervio óptico con signos de progresión en los estudios radiográficos. Puede ser aconsejable la resección quirúrgica si el tumor está confinado a la porción intraorbitaria, intracanalicular o prequiasmática del nervio óptico en un paciente con proptosis deformante y pérdida de visión completa o casi total del ojo afectado. Si se afecta el quiasma no suele estar indicado operar y en ocasiones se requiere radioterapia o quimioterapia. NEUROPATÍAS ÓPTICAS TRAUMÁTICAS El nervio óptico puede lesionarse por traumatismos directos o indirectos. El traumatismo directo se produce en heridas orbitarias penetrantes con sección o contusión del nervio. Las contusiones orbitarias también causan pérdida grave de visión si la fuerza del impacto se transmite al canal óptico y altera la irrigación de la porción intracanalicular del nervio. El tratamiento requiere a veces corticoides a altas dosis o descompresión del canal óptico. BIBLIOGRAFÍA Auw-Haedrich C, Staubach F, Witschel H: Optic disk drusen, Surv Ophthalmol 47:515-532, 2002. Balcer LJ: Optic neuritis, N Engl J Med 354:1273-1280, 2006. Birkebaek NH, Patel L, Wright NB, et al: Endocrine status in patients with optic nerve hypoplasia: relationship to midline central nervous system abnormalities and appearance of the hypothalamic-pituitary axis on magnetic resonance imaging, J Clin Endocrinol Metab 88:5281-5286, 2003. Garcia-Filion P, Fink C, Geffner ME, Borchert M: Optic nerve hypoplasia in North America: a re-appraisal of perinatal risk factors, Acta Ophthalmol 88:527-534, 2010. Hickman SJ, Dalton CM, Miller DH, et al: Management of acute optic neuritis, Lancet 360:1953-1962, 2002. Hu K, Davis A, O’Sullivan E: Distinguishing optic disc drusen from papilledema, BMJ 338:1207-1209, 2009. Lam BL, Feuer WJ, Abukhalil F, et al: Leber hereditary optic neuropathy gene therapy clinical trial recruitment, Arch Ophthalmol 128 (9):1129-1135, 2010. Massaro M, Thorarensen O, Liu GT, et al: Morning glory disc anomaly and moyamoya vessels, Arch Ophthalmol 116:253-254, 1998. Nicolin G, Parkin P, Mabbott D, et al: Natural history and outcome of optic pathway gliomas in children, Pediatr Blood Cancer 53:1231-1237, 2009. Optic Neuritis Study Group: Visual function 5 years after optic neuritis. Experience of the Optic Neuritis Treatment Trial, Arch Ophthalmol 115:1545-1552, 1997. Repka MX, Miller NR: Optic atrophy in children, Am J Ophthalmol 106:191-193, 1988. Skarf B, Hoyt CS: Optic nerve hypoplasia in children: association with anomalies of the endocrine and CNS, Arch Ophthalmol 102:62-67, 1984. Weiss AH, Beck RW: Neuroretinitis in childhood, J Pediatr Ophthalmol Strabismus 26:198-203, 1989.