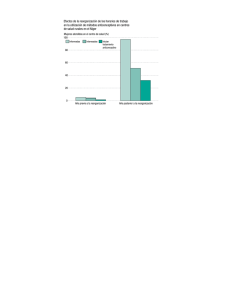
Estratégias para normalizar la representación sensorial
Anuncio

Mª Dolores Soler Plasticitat maladaptativa després d’una lesió neurològica. Noves estratègies d’abordatge Soler , M Dolors, Phy., PhD. Dep. Neuropsicosocial Fundació Institut Guttmann El cerebro responde a la percepción . No a la realidad. 1ª Premisa El dolor es una experiencia consciente. En contraste, pero a menudo erróneamente considerado análogo, la nocicepción puede existir fuera de la conciencia (Boly et al. Lancet Neurol., 2008). El cerebro responde a la percepción y a las expectativas... . No a la realidad. Henry Knowles Beecher (1904 – 1976) Beecher HK. Ethics and clinical research. The New England Journal of Medicine, 1966, 274: 1354–1360. El cerebro responde a la percepción . No a la realidad. Percepción de Dolor “La creencia habitual de que las heridas están asociadas inevitablemente al dolor, y de que cuanto mayor sea la herida peor será el dolor, no parece sostenerse a tenor de las observaciones realizadas en la zona de combate [...] No existe una relación simple ni directa entre la herida per se y el dolor experimentado. En gran medida, el dolor está determinado por otros factores, y aquí resulta de una gran importancia el significado de la herida [...] La respuesta del soldado herido era de alivio, de estar agradecido por escapar vivo del campo de batalla, incluso de euforia; [en cambio] para los [pacientes] civiles, la intervención quirúrgica era deprimente, un acontecimiento desastroso”. Beecher, H.K. and Sheik Adhith. Experimentation in man. Journal of the American Medical Association, 1959, 169 (5): 461–478. El cerebro responde a la percepción . No a la realidad. PUEDE EXISTIR PERCEPCIÓN y ACTIVACIÓN CEREBRAL SIN ESTIMULACIÓN EXTERNA Blankenburg F, Ruff CC, Deichmann R, Rees G, Driver J. The cutaneous rabbit illusion affects human primary sensory cortex somatotopically. PLoS Biol. 2006;4:e69. Neuroplasticidad y dolor tras lesión nerviosa. 2ª Premisa. El cerebro cambia cuando el dolor persiste Corteza cerebral (sensorial y motora) Aumento excitabilidad Cambios eficacia sináptica Reorganización mapas somatotópica 4 3 2 Núcleos del tronco cerebral Hiperexcitabilidad Cambios eficacia sináptica Reorganización de proyecciones aferentes Reorganización mapas aferentes Médula espinal Hiperexcitabilidad Descargas ectópicas Cambios en canales iónicos Reorganización proyecciones aferentes Sensibilización de neuronas espinales Cambios en la eficacia sináptica Disminución de neuronas inhibitorias 1 Núcleos del tálamo Hiperexcitabilidad Cambios en los canales iónicos Cambios eficacia sináptica Reorganización mapas de aferentes Neuronas nociceptivas Hiperexcitabilidad Descargas ectópicas Cambios en canales iónicos Cambios en neuropéptidos Navarro et al. Progr Neurobiol 2007 Plasticidad y dolor tras lesión nerviosa. Plasticidad maldaptativa El cerebro cambia cuando el dolor persiste La manifestación clínica de la sensibilización central , la alodinia y la hiperalgesia ocurrir con la activación repetida de nociceptores espinales y ofrece la ventaja biológica de aumentar la sensibilidad a las entradas periféricas. Este aumento de la sensibilidad optimiza la probabilidad de cicatrización de los tejidos y reduce al mínimo el riesgo de lesiones secundarias. Sin embargo, con el tiempo, la sensibilización puede perder su valor de adaptación y convertirse en si en un problema, como es el dolor crónico. La combinación de sensibilización y la desinhibición impulsan el cambio sistemático en el perfil de respuesta de las neuronas que representan el cuerpo. Este tipo de cambio, llamado reorganización cortical, se observó por primera vez en las principales áreas sensoriales y motoras de animales después de desaferenciación (Kaas et al., 1983; Merzenich et al., 1983, Endo et al., (2007; Cerveró 2008) Neuroplasticidad y dolor tras lesión nerviosa. El cerebro cambia cuando el dolor persiste V. Ramachandran 1999. Reorganización cortical y dolor neuropático: • desaferentización • Conexiones de aferencias mecanosensibles con neuronas corticales nocisensibles • Hiperexcitabilidad de neuronas corticales • Disminución del tono inhibitorio • "Incongruencia" del nuevo mapa sensorial con el esquema de acción motora Cambios en la organización cortical tras amputación Merzenich MM, et al. Somatosensory cortical map changes following digit amputation in adult monkeys. J Comp Neurol 1984; 224: 591–605. Neuroplasticidad y dolor tras lesión nerviosa. El cerebro cambia cuando el dolor persiste • La amputación o deaferentización de una extremidad suele producir sensaciones fantasma referidas a la extremidad perdida. • En 50‐80% de los amputados aparece dolor neuropático (dolor fantasma), intratable, durante años postamputación • La reorganización de estructuras centrales, debida a la ausencia de entradas sensoriales normales del territorio deaferentizado, se relaciona con la aparición de sensaciones fantasma Somatotopic referred sensations of the amputated hand in the arm stump Referred sensations in the phantom digits Ramachandran VS, Hirstein W. The perception of phantom limbs: The D. O. Hebb Lecture. Brain. 1998;121:1603-1630. Reorganización cortical en el dolor neuropático Tras una amputación de extremidad superior (deaferentación periférica), ocurren cambios funcionales en la representación somatotópica cortical: 1. 2. El área de representación de la región denervada se reduce de tamaño Áreas vecinas invaden el área vacante. Estos cambios corticales están relacionados con el dolor neuropático Existe una correlación entre la dimensión de la reorganización cortical y la intensidad de dolor Lotze M, Flor H, Grodd W, Larbig W, Birbaumer N. Phantom movements and pain: an fMRI study in upper limb amputees. Brain 2001; 124: 2268–77. Neuroplasticidad y dolor tras lesión nerviosa. El cerebro cambia cuando el dolor persiste Wrigley et al. Pain 2009 Neuroplasticidad y dolor tras lesión nerviosa. El cerebro cambia cuando el dolor persiste Soler MD, Kumru H, Vidal J, Pelayo R, Tormos JM, Fregni F, Navarro X, Pascual‐Leone A. Referred sensations and neuropathic pain following spinal cord injury. PAIN 2010; 150:192–198 Neuroplasticidad y dolor tras lesión nerviosa. El cerebro cambia cuando el dolor persiste Aprovechando la plasticidad cerebral para tratar a la persona con dolor Los cambios que se producen en el cerebro cuando el dolor persiste suponen una clara barrera para la recuperación exitosa. Sin embargo, la plasticidad que la sustenta sugiere que se puede modelar mediante tratamientos dirigidos. Tales tratamientos pueden agruparse en: Cognitivo‐conductual, Estrategias sensoriales y Estrategias motoras. Estrategias cognitivo‐conductual. Reacción ante el dolor Miedo. En pacientes con dolor existe miedo asociado al dolor y al movimiento. Miedo : potente motivador. Activa la percepción de amenaza de tu supervivencia. El cerebro quiere protegernos de cualquier cosa que suponga un peligro. Contribuye al modo en que te mueves, comportas y experimentas el dolor. El miedo puede depender poderosamente del contexto. Posibles miedos: Al dolor La gravedad de la causa del dolor A no saber la causa A que no le crean Ciertos movimientos, cualquier movimiento Re‐lesionarse o agravarse Tener mal aspecto, sobrepeso. Lo que los demás piensen No ser capaz de trabajar No percibir ingresos, no recibir una compensación Estrategias cognitivo‐conductual. Educación como herramienta fundamental Por qué es beneficiosa facilitar información/explicaciones sobre el dolor: 1. Aprender la fisiología del dolor disminuye el significado amenazante del dolor. La disminución de la amenaza reduce la activación de sistemas de protección como el sistema simpático, endocrino “y motor”. Esto puede redundar en el sistema inmunitario. 2. Combinar educación sobre el dolor+ abordajes orientados al movimiento mejora la capacidad física, reduce el dolor y mejora la calidad de vida. 3. El objetivo de entender la fisiología del dolor es facilitar un “aprendizaje profundo”, en el que la información se retiene, se comprende y se aplica a los problemas cotidianos. Saber únicamente lo que hay que hacer, pero sin entender el porqué, debe considerarse un aprendizaje superficial. La información se recuerda pero puede no entenderse ni se integra en ACTITUDES y CREENCIAS. Estrategias para normalizar la representación motora Modelo cortical del dolor patológico: The idea is that mirror therapy, graded motor imagery, and tactile training might correct cortical body maps, so as to remove the incongruence between motor Lacommands and sensory feedback.65 This notion was implied informally by interrupción de la representación propioceptiva (incongruencia sensorio‐ motora) puede ser una causa desencadenante del dolor. Ramachandran et al58 and posits that pain in the absence of ongoing tissue damage is (Harris, A. J. Cortical origin of pathological pain. Lancet,1999; 354: 1464–1466). caused by incongruence between motor intention and proprioceptive feedback. McCabe et al66 Crear una ilusión visual (y por lo tanto la retroalimentación positiva para la corteza motora) de la extremidad afectada en movimiento puede revertir procesos de reorganización cortical asociados a la presencia de dolor, reduciendo el dolor (Flor et al., 2000; Chan et al 2009). El visualizar el miembro en movimiento estaría restaurando una imagen corporal coherente, generando un feedback positivo (aferencia sensorial) en la corteza motora. Esta técnica también puede funcionar como un enfoque cognitivo que aumenta la excitabilidad cortical motora (Giraux, 2003; Garry 2005; Funase 2007). Estrategias para normalizar la representación motora mirror Diagrama de la terapia de espejo Ramachandran, V.S, D Rogers‐Ramachandran y S Cobb, 1995: “Touching the Phantom Limb” Nature, 377:487‐490 Estratégias para normalizar la representación sensorial Entrenar la representación sensorial requiere aportar estímulos al área afectada. Esta estimulación es más probable que induzca cambios en la representación cortical si la característica de la estimulación es importante para realizar una actividad, por ejemplo aprender a tocar un instrumento (Pascual‐Leone et al 2007; aprender Braille o desempaquetar alimentos (Jenkins et al 1990). Estrategias para normalizar la representación motora Chronic complex regional pain syndroms. Caccio A. et al. N Engl J Med 357;21. 2007 Giraux P, Sirigu A. Illusory movements of the paralyzed limb restore motor cortex activity. Neuroimage 2003;20:107‐111 Stroke. Caccio, et al. Neurorehabil Neural Repair. 2009;23:792‐799. Spinal cord injury. Moseley GL. Using visual illusion to reduce at‐level neuropathic pain in paraplegia. Pain 2007; 130: 294–8. Amputee. Flor H, Claudia Denke, Michael Schaefer, Sabine Grüsser. Effect of sensory discrimination training on cortical reorganisation and phantom limb pain. Lancet 2001; 357: 1763‐1764. Chan BL, Witt R, Charrow AP, Magee A, Howard R, Pasquina PF. et al. Mirror Therapy for phantom limb pain. N Engl J Med 2007;357: 2206‐2207. Brodie EE, Whyte A, Niven CA. Analgesia through the looking‐glass? A randomized controlled trial investigating the effect of viewing a 'virtual' limb upon phantom limb pain, sensation and movement. Eur J Pain 2007; 11:428‐36. MacIver K, Lloyd DM, Kelly S, Roberts N, Nurmikko T. Phantom limb pain, cortical reorganization and the therapeutic effect of mental imagery. Brain 2008;131:2181‐2191 Estrategias para normalizar la representación motora la MT se mostraba significativamente más efectiva que la imaginería motora, y reducía el dolor de manera significativa en un 88% de los pacientes, tras cuatro semanas de tratamiento. En una segunda fase, realizó un estudio cruzado mostrando una respuesta satisfactoria en el 92% de los pacientes. Cacchio A, De Blasis E, Necozione S, di Orio F, Santilli V. Mirror therapy for chronic complex regional pain syndrome type 1 and stroke. N Engl J Med. 2009;361:634‐636. Estrategias para normalizar la representación motora Cacchio A, De Blasis R, De Blasis V, Santilli V, Spacacca G. Mirror therapy in complex regional pain syndrome type 1 of the upper limb in stroke patients. Neurorehabil Neural Repair. 2009;23:792‐799. En un segundo ensayo aleatorizado con grupo control, Cacchio y col. confirmaron el efecto terapéutico de esta técnica, describiendo mejoras en la intensidad del dolor, en la alodinia al tacto, un aumento de la función motora en miembro superior, con persistencia de la mejoría durante más de 6 meses. Estrategias para normalizar la representación motora Emplearon (fMRI) para estudiar 13 pacientes con amputación de miembro superior y dolor, antes y después de un entrenamiento intensivo de 6 semanas en imagineria mental. Previamente al entrenamiento observaron una reorganización cortical en M1 y S1 que correlacionaba con la intensidad del dolor. Después del entrenamiento, los pacientes refirieron una reducción en la intensidad del dolor con su correspondiente eliminación en al reorganización cortical. Estratégias para normalizar la representación sensorial • Amputados entrenados en tarea de discriminación sensorial en el muñón • Se redució la intensidad de dolor fantasma • Retorno de reorganización cortical (labios/mano) • Estos datos se correlacionaron con el aprendizaje en la tarea de discriminación sensorial. Flor H, Claudia Denke, Michael Schaefer, Sabine Grüsser. Effect of sensory discrimination training on cortical reorganisation and phantom limb pain. Lancet 2001; 357: 1763‐1764. Estratégias para normalizar la representación sensorial Este estudio, utilizando imágenes de resonancia magnética funcional (fMRI), mostró que un uso frecuente y prolongado de prótesis mioeléctricas, en amputados del miembro superior, se correlacionaba negativamente con la reorganización cortical y dolor de miembro fantasma y positivamente con la reducción del dolor de miembro fantasma en el tiempo. Se compararon 5 sujetos que empleaban de manera continua las prótesis con 9 sujetos que las utilizaban de manera discontinua. Estrategias para normalizar la representación motora Ilusión visual Moltes gràcies per la seva atenció