ESPECTROMETRIA DE MASAS Espectrometría de masas atómica
Anuncio

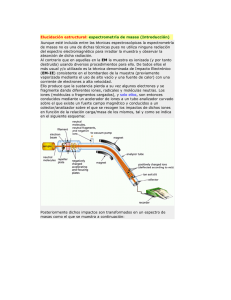
ESPECTROMETRIA DE MASAS • Se puede sub-dividir en dos áreas de aplicación: Espectrometría de masas atómica EMA: determinar cuali y cuantitativamente los elementos presentes en una muestra. Espectrometría de masas molecular EMM: análisis estructural de moléculas y determinación cuali y cuantitativa de mezclas complejas. Para cubrir los contenidos de Espectrometría de Masas en Análisis Instruemtnal III, el tema se dividirá en tres partes: • EM 1era. Parte: Espectrometría de masas atómica EMA. • EM 2da. Parte: Espectrometría de masas molecular EMM. • EM 3era. Parte: Analizadores de masas. Espectrometría de masas atómica EMA • Etapas de un análisis por EMA - Atomización - Conversión de los átomos en un flujo de iones (generalmente +1) - Separación de los iones según relación masa/carga (m/z) - Recuento del número de iones de cada tipo (medición de la corriente producida) 1 Pesos atómicos en EM • Peso atómico químico o peso atómico promedio de un elemento A = A1p1 + A2p2 + A3p3+…Anpn Donde A1, A2,.., An son las masas atómicas, en daltons, de n isótopos de un elemento y p1, p2,…,pn son las abundancias relativas de estos isótopos en la naturaleza. Pesos atómicos en EM • 1 uma (unidad de masa atómica) = 1 Da (daltons) • Al isótopo de C12 se le asigna una masa de 12 uma • La uma o Da es 1/12 de la masa de un átomo neutro de C12 • 1 uma = 1 Da = 1.66054x10-27 kg/átomo C12 Relación masa/carga • Se obtiene dividiendo la masa atómica o molecular m de un ión por el número de cargas z que tiene el ión. • Dado que en EM la mayoría de iones presentan una sola carga, el término m/z se simplifica utilizando el término masa 2 Tipos de espectrometría de masas atómica • Históricamente ionización térmica y fuente de chispa fueron los primeros, hoy desplazados por el plasma de acoplamiento inductivo Espectrómetros de masas • Instrumento que separa los iones que se desplazan rápidamente según se relación masa/carga, m/z. • Existen varios tipos; habitualmente en EMA se emplean tres: - espectrómetro de masa cuadrupolar - espectrómetro de masas de tiempo de vuelo - espectrómetro de masas de doble enfoque COMPONENTES DE UN ESPECTROMETRO DE MASAS 3 • Entrada: introducir la muestra (microgramos) en la fuente de iones donde los componentes se convierten en iones gaseosos. • La ionización puede ser por bombardeo con electrones, fotones, iones o moléculas; o por energía térmica o eléctrica. • La salida de la fuente de iones es un flujo de iones positivos o negativos gaseosos que son acelerados en el analizador de masas. • La función del analizador de masas es separar los iones según su relación m/z. Es análoga a la de un monocromador que separa λ de fotones. • El EM tiene un detector que convierte el haz de iones en corriente eléctrica para ser procesada (almacenada en memoria, mostrada en pantalla como picos, etc.) 4 • A diferencia de los espectrómetros ópticos, el EM requiere un complejo sistema de vacío para mantener una baja presión en todos los componentes, excepto el registro de datos • Bomba turbomolecular: 10-4 a 10-5 torr DETECTORES - A. Canal multiplicador de electrones: de dínodos discreto para detectar iones positivos; se parece a un fotomultiplicador G 107 A - B. Canal multiplicador de electrones: de dínodos contínuo G105. Estos dos tipos son los más usados -C. La copa de Faraday es menos usada -OTROS - Detector de centelleo: Fósforo cristalino produce destellos de luz -AgBr: placa fotográfica B C Los iones inciden sobre el electrodo colector. La jaula impide que salgan. La carga + de los iones se neutraliza con el flujo de electrones de tierra de la resistencia de carga. La caída de potencial resultante se amplifica con un amplificador de alta impedancia. Menos sensible que multiplicador de electrones, barata y sencilla. 5 Espectrometría de masas con plasma de acoplamiento inductivo (ICP-MS) • Una antorcha de ICP sirve como atomizador e ionizador. • Las muestras líquidas se introducen por nebulización; las sólidas por ablación (chispa o láser) o descarga luminiscente. • Los iones + producidos en la antorcha de ICP se introducen a través de una interfase de vacío diferencial unida al espectrómetro de masas • Espectros sencillos: consisten de una serie de picos de isótopos de cada elemento presente. • Permite análisis cuali y cuantitativo. • Se realiza una curva de calibración: - recuento de iones versus concentración - recuento iones del analito/recuento iones patrón interno versus concentración 6 • Parte crítica del instrumento: interfase que acopla la antorcha ICP (a presión atmosférica) con el espectrómetro de masas que trabaja a menos de 10-4 torr. • Acoplador de interfase de vacío diferencial Consiste de un cono de muestreo: cono de níquel refrigerado con agua con pequeño orificio (<1mm) por donde pasa el plasma caliente. Aquí el gas al enfriarse se expande y pasa por un agujero a un segundo cono (cono separador o skimmer) y a una cámara mantenida a una presión de 10-4 torr. • En la cámara los cationes se separan de los electrones y de las especies moleculares mediante un potencial negativo, y son acelerados y enfocados mediante una lente magnética de iones hacia la entrada del analizador de masas cuadrupolar. 7 Resolución de los ICP-MS • 3 a 300: esta capacidad permite separar iones que se diferencia de su relación m/z en una unidad • Pueden determinarse casi todos los elementos de la tabla periódica con límites de detección de 0.1 a 10 ppb. Espectro ICPMS de elementos de tierras raras. Las disoluciones contienen 1 ppm de cada elemento. 8 Límites de detección Límites de detección: barras negras ICPMS; barras rayadas ICP OES; barras grises ETAAS (emisión óptica en plasma de acoplamiento inductivo y absorción atómica electrotérmica). 9 Desventajas • Aunque originalmente se pensó que ICP-MS era un método libre de interferencias esa expectativa no se concretó y se encuentran serios problemas de interferencias en espectroscopía de masas atómica. Interferencias • No espectroscópicas: efectos de matriz similares a los que se producen en absorción y emisión atómica (Anal. Inst. II) • Espectroscópicas: cuando una especie iónica en el plasma tiene los mismos valores m/z que un ión del analito. Pueden ser de cuatro tipos. 1. 2. 3. 4. Iones isobáricos Iones poliatómicos o aductos Iones con doble carga Iones de óxidos refractarios Estudiar capítulos 11 y 20 del libro “Principios de Análisis Instrumental” SKOOG, HOLLER Y NIEMAN. Quinta edición. 10 Aplicaciones • Análisis elemental cuali y cuantitativo de todo tipo de muestras. • Elucidación estructural de moléculas orgánicas. • Medición de relaciones isotópicas: establecer la edad de materiales arqueológicos, enriquecer isotópicamente un material biológico para estudios clínicos. • Acoplado a cromatografía de gases o a cromatografía líquida de alta presión HPLC, permite la identificación y cuantificación de los compuestos presetnes en una mezcla. 11