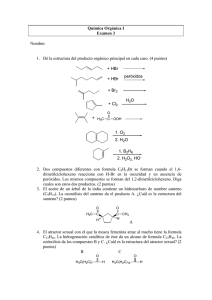
Examen BQOI Septiembre 1998
Anuncio

1. En prácticas se llevó acabo la preparación del aroma de plátano. Indique cual fue la reacción de síntesis y cual es la estructura del compuesto. La reacción de síntesis fue la esterificación de Fisher, de la siguiente manera. O CH 3 C OH Isoamílico 18ml Acético 23ml Secado O H3C CH 3 C O CH 2 CH 2 CH CH 3 CH 3 + CH 3 CH CH 2 CH 2-OH Ester (Acetato de Isoamilo) O H3C CH 3 C O CH 2 CH2 CH CH 3 MgSO4 + H2O deshidratación Ester (Acetato de Isoamilo) O H3C CH 3 C O CH 2 CH 2 CH CH 3 2. Ordene por acidez creciente: ácido acético, 1-butanol, fenol, n-butano y ácido tricloroacético. Justifique brevemente la respuesta. OH H3C H C H C CH 3 H H H H H H C < 3 C C C OH O < Cl O < H3C C OH < Cl C C OH Cl H H H n-butano 1-butanol fenol ácido acético ácido tricloroacético La explicación a esta ordenación es la siguiente; - El butano es un hidrocarburo, por tanto tiene todos los enlaces apolares, debido a esto es el menos ácido de todos - 1-butanol: la carga negativa de la base conjugada, por tanto carga negativa está sobre el oxígeno C4H9O-. - fenol: la base conjugada es más estable que el 1-butanol, ya que la carga negativa se encuentra repartida entre el oxígeno y el anillo aromático.(resonancia) - ácido acético: base conjugada muy estable, con formas resonantes equivalentes. O R C O O R C O - ácido tricloroacético: base muy estable como el ácido acético más el efecto inductivo de los átomos de cloro. 3. Ordene por densidad creciente y justifíquelo los compuestos de las dos series siguientes: a) yodometano, clorometano y bromometano; b) triclorometano, clorometano, tetraclorometano y diclorometano. ¿Qué compuestos de la serie b son más densos que el agua? 1.- Ordenar por densidad creciente; a) H3C Ι > H3C + H2O Br > H3C H2O Cl > H3C F Cl b) Cl Cl C Cl Cl > Cl CH > Cl CH 2 > Cl CH 3 Cl Cl H2O El Iodometano es el más denso, ya que es el compuesto con el halógeno más pesado de todos, seguido del Bromometano, Clorometano y Fluorometano, en la serie a). A medida que la cadena es más larga, el halógeno menos pesado o en menor proporción la densidad baja. A medida que la cadena es más corta, el halógeno más pesado o el halógeno se encuentra en mayor proporción la densidad es mayor. En la segunda serie el más denso es el tetraclorometano, ya que el halógeno está en mayor proporción que en los demás, y así descendiendo poco a poco de cloruros, es decir, el siguiente será el siguiente en cantidad de cloros, el triclorometano, después el diclorometano, y finalmente el clorometano como el menos denso, ya que su proporción de halógeno es la menor de todos. 2.- Que compuestos de la serie 2 son menos densos que el agua. Esto lo podemos comprobar de la siguiente manera: Un compuesto halogenado es menos denso que el agua cuando la proporción de halógeno en él, es menor al 70% de compuesto, es decir, que será más denso cuando el peso molecular del halógeno en el compuesto supere el 70% del peso molecular total del compuesto. Compuesto C-Cl4 HC-Cl3 H2C-Cl2 H3C-Cl PM 12 · 1 + 35.45 · 4 =153.8 12 · 1 + 1 · 1 + 35.45 · 3 =119.4 12 · 1 + 1 · 2 + 35.45 · 2 = 84.9 12 · 1 + 1 · 3 + 35.45 · 1 = 50.5 TOTAL PM ProporciónH 35.45 · 4 = 141.8 % 35.45 · 3 = 106.4 89.11% 35.45 · 2 = 70.90 35.45 · 1 = 35.45 HALÓGENO ALÓGENO Cl Cl Cl Cl C Cl > Cl CH > Cl CH 2 > Cl CH 3 Cl Cl H2O 4. ¿Cómo se puede determinar experimentalmente la estabilidad relativa del 1,3y el 1,4- ciclohexadienos?. ¿A qué es debido esta diferente estabilidad?. 1.- La estabilidad se puede medir experimentalmente midiendo los calores de hidrogenación de los cicloalquenos con un calorímetro, tras realizar esto llegaremos a la conclusión siguiente; a mayor calor desprendido en el proceso, menor es la estabilidad del compuesto cíclico. 2.- Esta diferencia de estabilidad se debe a la energía de conjugación o resonancia del dieno conjugado, los enlaces se hacen más fuertes tras la conjugación. 3-4 Kcal/mol Eresonancia 5. Sintetizar por dos vías diferentes a partir de tolueno y compuestos de uno y dos carbonos el 1-fenil-2-metil-2-propanol. 1ª Vía Cl2 CH 3 H CH 2 Cl luz, T-alta ICH3 - C C H CH 3 C CH 3 Eter seco CH 2 MgCl O H2O C C CH 3 CH 3 C CH 3 HgSO 4 OH CH 2 MgCl 1º) O Mg CH 3 C CH 2 + 2º) H3O CH 3 2ª Vía CH 2 MgCl O 1º) CO2 CH 2 C OH 2º) H+ O CH 2 C O CH 3 CH3-OH H+ O CH 2 C O CH 3 OH 1º) CH3-MgI CH 2 C CH 3 2º) H+ CH 3 6. A partir de tolueno obtener 1-(4-metilfenil)-1-(4-nitrofenil)metanona. CH 3 CH 3 HNO3 CH 3 NO 2 H2SO4 CH 3 + NO 2 COOH MnO 4- Separar CO-Cl SOCl2 OH -/ Calor NO 2 NO 2 NO 2 CH 3 O + C NO 2 AlCl 3 O H3C C NO 2 + Orto Cl 7. El tratamiento de cis-2-buteno con ácido fuerte y calor da lugar a una mezcla de trans- y cis-2-butenos. Explicar cual es el mecanismo de reacción, el isómero que predomina y porqué. Mecanismo: HC H3C CH CH 3 H H+ H -H+ + H H -H+ C + H3C H CH 3 CH 3 H3C Cis C H Trans Los dos estereoisómeros tienen en común el mismo carbocatión a través del cual se interconvierten del uno al otro. El isómero que predomina es el trans-, ya que se cumple la regla de Saytsev, la cual afirma que se formará el isómero más estable, y debido al efecto estérico es el más estable de los dos. 8. Deducir las fórmulas estructurales posibles para un hidrocarburo C9H8 que, conteniendo un grupo fenilo, da lugar a un compuesto carbonílico cuando es tratado con H2O / Hg2+ y reacciona con amiduro sódico. Justificar. - Grupo fenilo _ - Compuesto carbonílico que al tratarse con H2O / Hg2+ alquino - Reacciona con amiduro alquino terminal. Alquino terminal Estructura: CH2 Gr. Fenilo C C H 9. Indicar los productos de reacción silos hay de la 3-butin-2-ona con : a)borohidruro potásico; b)H2 / Pd Lindlar ;c) bromuro de metilmagnesio; d) HCl; e) hidroxilamina. O a) CH 3 CH C C CH CH 2 C C CH CH H O b) CH 3 C O c) CH3 C MgBr O d) CH 3 C Cl OH N e) CH 3 C CH C Oxima 10. Justifique en base al mecanismo de reacción la formación de los siguientes productos a partir de indeno: Cl HCl/BrNa + H2O O-H Br + - H+ H O + H H Cl- H Br - H2O H 11. Indique como puede llevarse a cabo la transformación del butanal en 2-etil-1,3hexanodiol (repelente de mosquitos). O CH 3 CH 2 CH 2 CH OH Aldólica CH 2 CH3 CH 2 CH 2 CH C CH 3 CHO H2 Pt CH 3 CH 2 CH CH CH CH 3 C H2C KBH4 CH 2 CH CH CH C CH 2 CH CH 3 12. Indique un método de preparación adecuado para: a) etoxietano; b) etoxibenceno; c)2-etoxi-2-metilpropano. CH 3 CH 2 OH OH Na CH 3 CH 2 O- O- NaOH C CH3CH2OH H+ CH 3 O ICH2CH3 SN CH 2 CH 3 O-CH 2-CH 3 CH 3 H2C ICH2CH3 CH 3 CH 2 O CH 2 CH 3 SN H3C C CH 3 CH 3 CH 3 CH 3 CH 2 OH 13. Na Br C CH 3 CH3 CH2 O- CH 3 NO reacciona SN Indique los productos que resultan al tratar consecutivamente el ciclopenteno con i)H2O / H+ ; ii) permanganato potásico; iii)HCN ; iv)H+/ calor; v)3H2/Pt. O H2O H+ KMnO4 HO HCN C CN H+ Calor N H2C 3H2 Pt OH 14. Diferencias entre polietileno de baja y alta densidad en cuanto a forma de preparación, estructura y aplicaciones. Diferencias respecto de: 1.- FORMACIÓN; (mecanismo) El polietileno de baja densidad se construye vía radicales (mediante peróxidos), mientras que el polietileno de alta densidad se forma por coordinación (con el catalizador de Ziegle-Natta). 2.- ESTRUCTURA; El polietileno de baja densidad es muy ramificado mientras que el polietileno de alta densidad es mas bien lineal. 3.- PROPIEDADES FÍSICAS; El polietileno de baja densidad tiene menor resistencia mecánica y una menor temperatura de reblandecimiento, mientras que su densidad es de 0,92, en cambio el NH 2 polietileno de alta densidad como su nombre indica tiene una densidad más alta de 0,96, y tiene un mayor empaquetamiento que el polietileno de baja densidad, lo que indica una mayor temperatura de reblandecimiento. 4.- FABRICACIÓN; El polietileno de baja densidad es más barato de producir, por lo que tiene un mayor volumen de producción, por otra parte el polietileno de alta densidad es más caro, al ser más complejo y su volumen de producción es mucho menor, esto se debe en gran medida a que este tipo de polietileno tiene una mayor temperatura de reblandecimiento y es mucho más difícil de tratar. 15. Estructura de los freones. Aplicaciones e impacto medioambiental. Los freones, también llamados clorofluorocarbonados. Estos compuestos se emplean como refrigerantes, solventes, y propulsores en los aerosoles. Siendo los más típicos el triclorofluorometano CFCl3 (denominado Freón – 11) y el diclorodifluorometano CF2Cl2 (Freón – 12). Los freones son tan buenos refrigerantes debido a que poseen una gran capacidad calorífica, lo que les permite pasar casi a temperatura ligeramente inferior a la ambiente de estado líquido a gas absorbiendo el calor del medio. Nomenclatura: - nº carbonos –1 Cl - nº hidrógenos +1 F C Cl - nº de fluor = F CF2Cl2 Freon - 12 Se creía que eran inertes, pero se ha demostrado que lo que realmente pasaba con los freones, era que se volatilizaban y se incorporaban a la atmósfera, donde se difundían sin sufrir alteraciones, llegando hasta la capa de ozono en la estratosfera, y lo que hace este freón que ha llegado hasta la estratosfera es iniciar reacciones en cadena de radicales libres, con la luz ultra violeta proveniente del sol sin filtrar por la atmósfera, que rompen el equilibrio natural del ozono. (1) Inicio de la cadena CF2Cl2 + hν (2) Propagación Cl· + O3 (3) de la cadena ClO· + O CF2Cl· + Cl· ClO· + O2 O2 + Cl· En la etapa inicial la luz ultra violeta provoca la ruptura homolítica de un enlace C-Cl del Freón. Siendo el átomo de cloro que se forma es verdadero causante del problema ya que es capaz de producir una cadena de reacciones que destruyen miles de moléculas de ozono rápidamente. 16. Diferencias estructurales entre una fibra y una resina. Ponga un ejemplo de poliester para ambos casos. *En las fibra existe un eje en el que se alinean las cadenas. ESTRUCTURA.- cadenas lineales con fuertes interacciones entre ellas pudiendo ser las interacciones por puentes de hidrógeno ó dipolo-dipolo. EJEMPLO.- Nylon 6. 5C 5C 5C O H H H H H O O O N C C C C C C N C N C N C H H H H H H H H H *Por el contrario en las resinas todo el polímero es una única unidad conectada mediante enlaces covalentes. Por tanto uniendo covalentemente una fibra, un elastómero o un plástico, generalmente se obtiene una resina, esto se realiza en dos etapas: 1.- Prepolimerización (se le da forma.) 2.- Fraguado: tras esta etapa el polímero no variará su forma. EJEMPLO.- Baquelita. OH OH OH OH OH OH HO 17. Polialcoholes industrialmente importantes y aplicaciones. Los polialcoholes son usados para OH CH 2 OH OH CH CH 2 la formación de : resinas de poliester Glicerina CH 2 OH OH CH 2 C CH 2-OH C O CH 2 CH CH 2 O C Pentaeritritol CH 2 OH CH 3-CH 2 C CH 2-OH O O CH 2 OH O CH 2 CH CH 2-OH O O resinas de polimetano Trimetilolpropano H3C CH 2 OH CH 3 O H O N C O O C NH O O C O CH3 O O C O O O NH C O O HN NH C O NH H3C O O OC O HN HN O C O O OC O O 18. Indique la secuencia industrial a partir del ciclohexano para la preparación del Nylon 6. OH OH O O2 N O H2NOH + Ciclohexano H N H2SO4 Nylon 6 e -Caprolactana Ciclohexanona 19. Principales productos derivados del etileno de importancia industrial. 1ª.- En un 60% son el PE, de alta y baja densidad y los oligómeros. H2C CH Los oligómeros lineales por adición de moléculas de etileno entre carbonos de entre C12-C24 (detergentes.) H 2ª.- oxicloración Cl2/O2 3ª.- 4ª.- PhH CH3-COOH O2 Cl H2C Ph CH 2 H 2C PVC CH CH 3 CH OAc -H2 Policloruro de vinilo Ph CH CH 2 (Son el poliestireno, porexpan, SBR, ABS, copolímeros.) poliacetato de vinilo y polivinil alcohol (PVA). OH OH 5ª.- 6ª.- H2C O O2/Ag O2 H2C CH 2 (óxido de etileno) O H3 C CH CH 2 (anticongelante) polietilenglicoles (disolventes) polietoxilatos O H 3C C OH Ácido etanoico 20. ¿Cuales son las características comunes más relevantes de las reacciones industriales que las diferencian de las reacciones generales de los grupos funcionales?. Las reacciones generales del grupo funcional son comunes para cualquier compuesto de la familia. • buscan rendimientos altos • reaccionan sin catalizador o con catalizador conocido • se hacen por cargas, se mezclan reactivos y especies hasta que reaccionan. En cambio las reacciones industriales (son específicas, catalítica y en continuo). • son específicas para cada producto. • • • • rentabilidad del proceso buscan el más barato. reacciones catalíticas, siendo el catalizador un secreto, o estando patentado. nunca se hacen por cargas son reacciones en continuo. se busca la rentabilidad del proceso, no el rendimiento alto. Ciclohexano 95% OH + O2 REACTOR O 5%