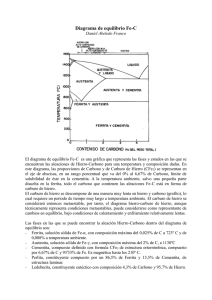
Capítulo 1: Fases y estructuras Diagrama de equilibrio Fe-C
Anuncio

Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
Capítulo 1: Fases y estructuras
Los aceros pueden tratarse térmicamente para producir una gran variedad de
microestructuras y propiedades. Los resultados deseados se obtienen a través del
calentamiento del acero en el rango de temperaturas donde una fase o una combinación de
fases es estable (así se producen cambios en la microestructura o en la distribución de fases),
y/o mediante el calentamiento o el enfriamiento en un rango de temperaturas en el cual
distintas fases son estables (produciendo así una beneficiosa transformación de fases). El
diagrama de equilibrio hierro-carbono (Fe-C) es sobre el cual se basan todos los tratamientos
térmicos de los aceros. Este diagrama de equilibrio define las regiones de composicióntemperatura donde varias fases de los aceros son estables, como así también, los límites de
equilibrio entre campos de fases. Aquí se describirán el diagrama Fe-C y las fases presentes en
aceros y aleaciones Fe-C.
Diagrama de equilibrio Fe-C
El diagrama Fe-C es un mapa que puede usarse para trazar la secuencia de operaciones
de un tratamiento térmico o termomecánico en un acero dado. El diagrama Fe-C se usará
sólo como una guía, dado que la mayoría de los aceros contienen otros elementos además del
carbono que modifican las posiciones de los límites de los campos de fases. El uso del
diagrama Fe-C es limitado a causa de que algunos tratamientos térmicos se realizan para
producir estructuras fuera de equilibrio, mientras que otros, apenas se acercan al mismo. No
obstante, el conocimiento de los cambios que tienen lugar en el acero cuando se acerca al
equilibrio en un dado campo de fase o de aquellos que resultan de una transformación de fase,
provee la base científica para los tratamientos térmicos de los aceros.
La Fig. 1.1 muestra el diagrama de equilibrio Fe-C para contenidos de carbono hasta
7%. Los aceros son aleaciones de Fe, C y otros elementos que contienen menos del 2% C,
frecuentemente 1% o menos. Por lo tanto, es de interés para los tratamientos térmicos de los
aceros la porción del diagrama por debajo del 2% C. Las aleaciones con más del 2% C se
clasifican como fundiciones. En la Fig. 1.1 se muestran dos diagramas, uno con líneas llenas
muestra el equilibrio entre Fe y Fe3C, mientras que el de líneas de trazos representa el
equilibrio entre el Fe y el grafito. El grafito es más estable que Fe3C y en periodos de tiempo
muy largos, el Fe3C se descompone a grafito. La grafitización, sin embargo, raramente ocurre
en aceros y así el diagrama Fe-Fe3C es el más adecuado para los tratamientos térmicos de los
aceros. En las fundiciones de Fe, el alto contenido de C y la presencia de elevados porcentajes
de Si (2-3.5%) promueven la formación de grafito.
El diagrama de la Fig. 1.1 es estrictamente válido a la presión de 1 atm. A valores de
presión mucho mayores los límites cambian y se presentan nuevas fases. Por ejemplo, en el
hierro puro a muy altas presiones se forma un cristal hexagonal compacto a partir del hierro
conocido como Fe ε.
La composición de las aleaciones Fe-C y de las fases del diagrama Fe-C se indican
convencionalmente en porcentaje en peso (el símbolo % representa el porcentaje en peso a
menos que se indique lo contrario). A veces es útil dar la composición en porcentaje atómico.
La forma de conversión de porcentaje en peso a atómico esta dada por:
% atC
átomosC
x100
átomosFe átomosC
1
Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
La aplicación de este cálculo a una aleación Fe-0.4C muestra que el 0.4% C en peso es
equivalente al 1.8 % atómico.
El arte y la ciencia de los tratamientos térmicos de los aceros se basan en la presencia
del campo de fase de la austenita en el sistema Fe-C. Mediante la transformación controlada
de la austenita durante el enfriamiento a otras fases se obtiene una gran variedad de
microestructuras y propiedades en los aceros.
El Fe es un elemento alotrópico, a la presión atmosférica puede existir en más de una
forma cristalina dependiendo de la temperatura: Fe (ferrita) hasta 912C, Fe (austenita)
existe entre 912 y 1394C, Fe (ferrita delta) existe desde 1394C hasta el punto de fusión del
Fe puro a 1538C. Los rangos de temperatura en los cuales las distintas formas cristalinas del
hierro son estables, forman el límite vertical izquierdo (Fe puro) en el diagrama de la Fig. 1.1.
Estructura cristalina del Fe
La estructura cristalina de la ferrita se caracteriza por una celda unitaria como la que se
muestra en la Fig. 1.2. La ferrita pertenece al sistema cúbico de cuerpo centrado (en inglés,
body centered cubic, bcc). Hay un total de dos átomos por celda unitaria, uno
correspondiente al centro de la celda y cada átomo de las esquinas es compartido por ocho
celdas vecinas o sea 1/8 átomo por las ocho esquinas del cubo hacen el segundo átomo
correspondiente por celda unitaria.
El parámetro de red de la Fe a temperatura ambiente es 2.86Å (0.286 nm). Las
diagonales de la celda unitaria corresponden a las direcciones de mayor compactación <111>,
son las direcciones en las cuales los átomos de Fe están en contacto unos con otros. En la
Fig. 1.2 se muestra una celda cúbica de cuerpo centrado en la cual cada átomo tiene ocho
vecinos más cercanos. En la estructura cristalina de empaquetamiento compacto cada átomo
tiene doce vecinos más cercanos y, por lo tanto, el Fe en la forma bcc tiene una estructura
más abierta o menos densa que la estructura del Fe que se describirá más abajo. La
diferencia de empaquetamiento atómico entre Fe y Fe es la que provoca la expansión
volumétrica que ocurre cuando el Fe transforma a Fe durante el enfriamiento.
La celda unitaria de Fe o austenita se muestra en la Fig. 1.3. La austenita también
pertenece al sistema cúbico, pero con la red centrada en las caras (en inglés, face centered
cubic, fcc). Hay en total cuatro átomos por celda unitaria: uno por los vértices de las celdas,
tres por los de las caras, medio átomo por cada cara, dado que éstos son compartidos por dos
celdas vecinas, por las seis caras resultan tres átomos.
El parámetro de red de la austenita es de 3.56 Å (0.356 nm), mayor que la ferrita. Sin
embargo, la estructura compacta y los cuatro átomos por celda unitaria hacen que la densidad
de la austenita sea mayor que la de la ferrita. Las diagonales de las caras correspondientes a las
direcciones <110>, son las direcciones de mayor compactación en la estructura fcc.
La austenita también puede caracterizarse como una estructura formada por el
apilamiento de planos compactos en una secuencia que se repite cada tres capas (ABCAB......).
La orientación de los planos compactos {111} relativa a la celda unitaria puede identificarse
fácilmente porque cada plano {111} se define por tres diagonales de las caras de la celda
unitaria. Los planos compactos en la austenita son extremadamente importantes, el
movimiento de las dislocaciones que hace posible la deformación plástica de la austenita
ocurre sobre los planos {111}, y la característica microestructural dentro de los granos,
conocida como macla, tiene como límites los planos {111}. En la austenita las maclas se
forman como resultado de fallas en el apilamiento de planos {111} causado por
recristalización y crecimiento de grano durante el calentamiento o recocido en el rango de
temperatura donde la austenita es estable.
2
Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
Figura 1.1- Diagrama de equilibrio Fe-C hasta 7% C. Las líneas llenas indican el diagrama Fe-Fe3C; las líneas
de trazos el diagrama Fe-grafito.
3
Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
Figura 1.2- Estructura cristalina cúbica de cuerpo centrado (body-centered cubic, bcc). A2 es un símbolo
(Strukturberich) de la estructura y W es un metal prototipo con estructura bcc. La ferrita en los aceros es bcc.
Figura 1.3- Estructura cristalina de cuerpo centrado en las caras (face-centered cubic, fcc). A1 es un símbolo
(Strukturberich) de la estructura y Cu es un metal prototipo con estructura fcc. La austenita en los aceros es fcc.
Finalmente, la tercera fase que puede formarse en el Fe puro es la ferrita , una
estructura cristalina cúbica centrada en el cuerpo que es cristalográficamente idéntica al Fe .
La ferrita se forma a una temperatura cercana a la del punto de fusión del Fe. Es
generalmente sólo de interés académico ya que en los tratamientos térmicos de los aceros al
carbono, ésta se reemplaza por la austenita a baja temperatura, siendo esta última estructura la
de comienzo de dichos procesos. Sin embargo, a causa de que la ferrita es la primera fase
que se forma durante la solidificación de los lingotes de Fe y acero y en las soldaduras, se la
puede asociar con modelos de segregación interdendrítica o gradientes de concentración de
aleantes y/o elementos de impurezas. El trabajado en caliente y la homogeneización de los
aceros en el rango austenítico generalmente reducen significativamente la segregación
producida durante la solidificación.
Efecto del carbono
El agregado de carbono al Fe produce varios cambios importantes en las fases y en el
equilibrio de fases descripto. La diferencia en la capacidad de la ferrita y la austenita para
acomodar los átomos de carbono resulta no sólo una característica importante del diagrama
Fe-C sino también en la formación del Fe3C. La estructura cristalina de la ferrita bcc y de la
austenita fcc, resulta modificada por la introducción de átomos de carbono dentro de los
intersticios o sitios intersticiales entre los átomos de Fe. La austenita y la ferrita en las
aleaciones de Fe-C y en los aceros son, por lo tanto, soluciones sólidas intersticiales.
4
Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
El carbono es un elemento que estabiliza la austenita y así amplía el rango de
formación de austenita en aceros. La Fig. 1.1 muestra que con el agregado de carbono, el
campo de la austenita se expande desde 912 a 1394C (rango del hierro puro) a un amplio
rango de temperaturas y composiciones. La máxima solubilidad del C en la austenita es de
2.11% a 1148ºC. La ferrita tiene menor capacidad de disolver carbono que la austerita y su
solubilidad decrece continuamente desde un máximo de sólo 0.02% C a 727C. La limitada
solubilidad del carbono en la ferrita es evidente por el pequeño campo de fase de la ferrita. La
Fig. 1.4 muestra una porción expandida del diagrama Fe-C en la región de bajo carbono que
muestra el rango de temperatura y composición de la ferrita. Se puede apreciar la disminución
de solubilidad del C con el descenso de la temperatura. A temperatura ambiente la solubilidad
del carbono en ferrita es casi despreciable.
En las aleaciones Fe-C y en aceros, cuando se excede el límite de solubilidad del
carbono en la austenita se forma una nueva fase, el carburo de Fe o cementita (Fe3C). La
cementita toma muchas formas, disposiciones y tamaños, que junto con la ferrita, contribuye
a la gran variedad de microestructuras encontradas en los aceros. Las variadas formas de la
cementita dependen directamente de la historia térmica o del tratamiento térmico.
Figura 1.4- Región rica en hierro del diagrama Fe-C mostrando la extensión del campo de fase de la ferrita y la
disminución de la solubilidad del carbono a medida que disminuye la temperatura.
Estructura cristalina en aleaciones Fe-C
La diferencia principal entre la estructura de la ferrita y la austenita en aceros y las
fases correspondientes al Fe puro es la introducción de los átomos de carbono. Hay dos tipos
5
Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
de huecos intersticiales donde se pueden ubicar los átomos de carbono en las estructuras bcc
y fcc. Las Figs. 1.5 y 1.6 muestran los huecos octaédrico y tetraédrico en las estructuras fcc y
bcc, respectivamente. Los dos tipos de huecos derivan su nombre del número de lados del
poliedro formado por los átomos de Fe que rodean un sitio dado. Un átomo de carbono
tiene seis vecinos más próximos en un sitio octaédrico y cuatro para un sitio tetraédrico.
El tamaño de los diferentes huecos varía considerablemente. En la austenita,
asumiendo átomos de Fe esféricos en contacto entre sí, un sitio octaédrico podría acomodar
un átomo de 0.052 nm de radio, pero un sitio tetraédrico podría sólo acomodar un átomo de
0.028 nm de radio. Los átomos de carbono tienen un radio de 0.07 nm, por lo tanto, son más
fáciles de acomodar en huecos octaédricos aunque se requiera alguna expansión de la red.
Figura 1.5- (a) Sitios intersticiales octaédrico y (b) tetraédrico en una estructura fcc.
Figura 1.6- (a) Sitios intersticiales octaédrico y (b) tetraédrico en una estructura bcc.
En la ferrita los sitios intersticiales son más pequeños, esto explica la limitada
solubilidad del carbono en esta fase. Un sitio tetraédrico en la ferrita podría acomodar un
átomo intersticial de 0.035 nm de radio y en un sitio octaédrico un átomo de sólo 0.019 nm
de radio. Los sitios octaédricos en la ferrita, sin embargo, no son simétricos (ver Fig. 1.6) y un
átomo de C debería desplazar severamente no sólo a dos átomos de Fe que están a una
distancia de a/2, sino también a aquellos que están a una distancia de a/√2. Los átomos de C
parecen preferir los sitios octaédricos y producen una distorsión severa de la red en las
6
Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
direcciones 100. En la ferrita, a causa del número limitado de átomos de C que pueden ser
acomodados, la red permanece esencialmente cúbica. Si un gran número de átomos de C
presente en la austenita resulta atrapado en huecos octaédricos por un enfriamiento rápido, la
estructura cúbica pasa a ser tetragonal. Esta última estructura tipifica la fase martensita y su
formación es el objetivo de los tratamientos térmicos de endurecimiento.
La cementita, es la fase que se forma cuando se excede la solubilidad del C en la ferrita
y en la austenita y es significativamente diferente de las soluciones sólidas intersticiales
descriptas previamente. La cementita es un compuesto con una relación específica de un
átomo de C a tres átomos de Fe y es llamada frecuentemente Fe3C. Contiene 6.67% C y
podría existir como una fase simple sólo en una aleación de esa composición, en contraste
con la ferrita o la austenita, las cuales pueden existir como una fase simple en una aleación en
un rango de contenido de C.
La cementita es ortorrómbica, con un parámetro de red a = 0.452 nm, b = 0.509 nm y
c = 0.674 nm. Esta celda unitaria contiene doce átomos de Fe y cuatro átomos de C. Las
posiciones de los átomos de C y Fe relativas a los ejes de la celda unitaria de la cementita se
muestran esquemáticamente en la Fig. 1.7.
Figura 1.7- Estructura cristalina ortorrómbica de la cementita. D011 es el símbolo (Strukturbericht) de la
estructura.
Efecto de los elementos aleantes
Hasta este punto se ha descripto el diagrama binario Fe-C y las estructuras cristalinas
de las fases que se forman en las aleaciones Fe-C. Sin embargo, los aceros contienen
elementos aleantes e impurezas que pueden formar nuevas fases o incorporarse en las
estructuras cristalinas de la austenita, ferrita y cementita. La incorporación se lleva a cabo
usualmente por el reemplazo de átomos de Fe si el átomo del elemento aleante o impureza
tiene aproximadamente el mismo tamaño que el primero, pero a veces ocupan sitios
intersticiales si ellos son significativamente más pequeños que los de Fe, como el caso del
nitrógeno. En algunas circunstancias, si la cantidad de elementos aleantes es suficiente, se
exceden los límites de solubilidad y pueden formarse otras fases distintas de las analizadas. Por
ejemplo, pequeñas adiciones de Cr a aleaciones de Fe-C a 890C mantienen la estructura de la
cementita, M3C (M significa una combinación de Cr y Fe), agregados mayores dan origen a la
forma M7C3 y cantidades aún mayores producen el carburo M23C6.
Algunos de los elementos presentes en aceros son estabilizadores de la austenita (Mn,
Ni, por ejemplo), otros son estabilizadores de la ferrita (Si, Cr y Nb) y algunos son fuertes
formadores de carburos (Ti, Nb, Mo y Cr si se presentan en cantidades suficientes). Los
7
Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
estabilizadores de la ferrita y la austenita expanden los respectivos campos de fases. Una
medida del efecto de un elemento aleante sobre el diagrama Fe-C, es si la temperatura
eutectoide (indicada por la horizontal de 727C) sube o baja por el agregado de dicho
elemento. Los estabilizadores de la austenita bajan la temperatura eutectoide y, por lo tanto,
expanden el rango sobre el cual la austenita es estable. La Fig. 1.8(a) muestra el cambio en la
temperatura eutectoide con el aumento del contenido de algunos elementos aleantes más
comunes. La Fig. 1.8(b) muestra el efecto de los elementos aleantes sobre el diagrama Fe-C,
se observa una disminución en el contenido de C de la austenita de composición eutectoide.
Los efectos mostrados en la Fig. 1.8 se representan ahora para el sistema Fe-Cr-C en la Fig.
1.9 y para el sistema Fe-C-Mn en la Fig. 1.10. En la Fig. 1.9 se muestra que debido a que el
cromo tiene un efecto muy fuerte como estabilizador de la ferrita y fuerte formador de
carburo, el campo de fase de la austenita se contrae con el aumento del contenido de Cr. En
la Fig. 1.10 se muestra el efecto del Mn, debido a que es un estabilizador de la austenita y un
elemento moderado en la formación de carburos, aumenta la estabilidad de la misma a
menores temperaturas en aceros de bajo carbono y extiende el campo austenita-cementita en
aceros de alto carbono hacia valores de menor contenido de carbono.
El efecto de los elementos aleantes sobre el campo de fase de la austenita se
determina usualmente por técnicas experimentales aunque se han usado también datos
termodinámicos para calcular el rango de estabilidad en aleaciones ternarias.
(a)
(b)
Figura 1.8- (a) Efecto de los elementos aleantes sustitucionales en la temperatura de transformación eutectoide
en aceros. (b) Efecto de los elementos aleantes sustitucionales en la composición eutectoide de carbono en
aceros.
Temperaturas críticas
Los límites entre los campos de fases del diagrama Fe-C mostrado en la Fig. 1.1 indica
las temperaturas para varias transformaciones de fases que pueden ocurrir en aleaciones Fe-C.
Por ejemplo, si una aleación Fe-0.5C fuera calentada desde la temperatura ambiente a una
velocidad extremadamente baja, algo de ferrita y toda la cementita transformarían a austenita a
727C y cerca de 860C, la última porción de ferrita transformaría completamente a austenita.
Las temperaturas de transformación son llamadas frecuentemente temperaturas
críticas y se determinan midiendo los cambios en la transferencia de calor o de volumen
cuando la muestra se calienta o enfría. Durante el calentamiento, el calor es absorbido y
ocurre la contracción de la muestra a medida que la ferrita y la cementita son reemplazadas
por la estructura compacta de la austenita. En el enfriamiento, el calor es liberado por la
8
Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
muestra y ocurre una expansión de volumen a medida que la austenita transforma en ferrita y
cementita. La absorción y liberación de calor durante la transformación de fase produce un
cambio en la pendiente, "o discontinuidad" sobre el gráfico de temperatura vs. tiempo. Se
utiliza la letra "A" como el símbolo que indica las discontinuidades térmicas que a su vez
identifican a las temperaturas críticas.
Hay tres temperaturas críticas de interés en el tratamiento térmico de los aceros: A1
corresponde al límite entre el campo ferrita-cementita y los campos que contienen austenita y
ferrita o austenita y cementita; A3 que corresponde al límite entre el campo ferrita-austenita y
el campo austenítico; y Acm corresponde al límite entre el campo de cementita-austenita y el
campo austenítico. Estas temperaturas asumen condiciones de equilibrio bajo largos periodos
de tiempo a temperatura constante o bajo velocidades de calentamiento o enfriamiento
extremadamente lentas. En estos casos, A1, A3, Acm se designan como Ae1, Ae2 y Aecm,
respectivamente, la letra “e” indica condiciones de equilibrio.
Las transformaciones que ocurren a A1, A3 y Acm se encuentran bajo control
difusional. Por lo tanto, las temperaturas críticas son sensibles a la composición y a las
velocidades de calentamiento y enfriamiento. Altas velocidades de calentamiento implican
menos tiempo para la difusión y tienden a incrementar las temperaturas críticas asociadas con
el equilibrio. De forma similar, altas velocidades de enfriamiento tienden a disminuir las
temperaturas críticas. El efecto de la velocidad de calentamiento o enfriamiento se define por
un nuevo juego de temperaturas críticas designadas "Ac" o "Ar" (para los cambios sobre el
enfriamiento o calentamiento, respectivamente). Esta terminología fue desarrollada por el
metalurgista francés Osmond. Ac es por arrêt chauffant y Ar por arrêt refroidissant. Por lo tanto,
como resultado del calentamiento o enfriamiento hay otros dos juegos de temperaturas
críticas Ac1, Ac3, Accm y Ar1, Ar3, Arcm, las cuales se muestran esquemáticamente en la Fig.
1.11.
Generalmente, las temperaturas críticas para un dado acero se determinan
experimentalmente. Sin embargo, se han desarrollado algunas fórmulas empíricas que
muestran el efecto de los elementos aleantes sobre las temperaturas críticas mediante análisis
de regresión de grandes cantidades de datos experimentales. Por ejemplo, Andren ha
desarrollado las siguientes fórmulas para Ac3 y Ac1 en grados centígrados:
Ac3 910 203 C 15.2 Ni 44.7 Si 104V 31.5Mo 13.1W
Ac1 723 10.7 Mn 16 .9 Ni 29.1Si 16.9Cr 290 As 6.38W
Estas fórmulas presentan otra manera de describir el efecto de los elementos aleantes
sobre el diagrama Fe-C y el comportamiento de transformación de los aceros. Los elementos
que estabilizan la austenita disminuyen Ac3 y Ac1 como evidencia de su contribución negativa
a la ecuación correspondiente, mientras que los elementos que estabilizan la ferrita o carburos
aumentan Ac3 y Ac1 y hacen una contribución positiva. El efecto de los elementos aleantes
sobre Ac3 se ha determinado también por cálculos termodinámicos.
9
Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
Figura 1.9- Efecto del contenido de cromo en el tamaño del campo austenítico.
Figura 1.10- Efecto del manganeso en el tamaño del campo austenítico.
10
Estructura y Propiedades de las Aleaciones-Facultad de Ingeniería-UNLP
Capítulo 1: Fases y estructuras
Figura 1.11- Temperaturas de aleaciones Fe-C de calentamiento (Ac), enfriamiento (Ar) y de equilibrio (A).
11