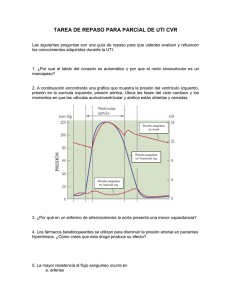
MONITOREO HEMODINÁMICO Presión arterial
Anuncio

MONITOREO HEMODINÁMICO La monitoría de las funciones vitales es esencial durante la vigilancia del paciente críticamente enfermo para el temprano reconocimiento de problemas fisiológicos o la implementación y seguimiento de medidas terapéuticas. El proceso incluye observación, vigilancia, instrumentación, interpretación y terapia. La monitoría puede ser invasiva o no invasiva. La invasiva, aquella que genera un riesgo potencial de daño, debe utilizarse sólo cuando con conocimientos adecuados se estime que el beneficio sobrepasa los riesgos ocasionados. Así, se usa en indicaciones precisas y debe ser removida inmediatamente cuando ya no sea requerida. En el presente capítulo se pretende explicar de una forma sencilla lo más importante de la monitorización hemodinámica haciendo énfasis en las indicaciones, contraindicaciones, limitaciones y riesgos de cada uno de los procedimientos e instrumentos usados. Presión arterial La presión arterial representa la presión lateral ejercida por el flujo sanguíneo sobre las paredes de las arterias. Durante el ciclo cardiaco, una onda de pulso resulta cuando el volumen sistólico del ventrículo izquierdo es eyectado hacia el árbol arterial. Los determinantes de la presión latido a latido son la elasticidad de las arterias, el volumen sanguíneo, el gasto cardiaco y la resistencia vascular periférica. La presión diastólica es un importante determinante de la perfusión coronaria. La presión arterial media representa el poder que dirige la fuerza hidrostática para realizar funciones de difusión y filtración. Tensión arterial no invasiva La tensión arterial se puede medir de manera indirecta a través de brazaletes inflables en las extremidades. Las presiones sistólica y diastólica se obtienen por auscultación de los ruidos de Korotkoff. La presión media puede ser calculada por una fórmula: TAM: PAD + 1/3 (PAS-PAD). Existen ya tensiómetros automáticos controlados por microprocesador que miden las ondas oscilantes del flujo sanguíneo durante la inflación y deflación del brazalete, midiendo la presión arterial sistólica, diastólica y media. En general se correlaciona bien con las técnicas invasivas pero pueden subestimar la presión sistólica entre 7 y 9 mm de Hg. El brazalete adecuado es el que tenga un ancho del 40 % de la circunferencia del brazo y de largo que sea suficiente para rodear el 60 % de la extremidad. Problemas La medición indirecta puede tener algunas limitaciones. Las medidas indirectas son dependientes de cambios en el flujo y el volumen y son frecuentemente más bajas que las medidas directas. Cuando se requieren medidas frecuentes, el brazalete puede no se desinflarse completamente alterando el retorno y por eso el paso de infusiones intravenosas localizadas en la misma extremidad. El temblor puede retrasar el desinflado y alterar la medición. Puede generar neurotrauma cuando el brazalete se coloca encima de una fibra nerviosa. En pacientes hemodinámicamente inestables puede subestimar los valores 2 de la presión. Si la extremidad está por encima o por debajo del nivel de la aurícula derecha puede haber error en la medición, esto se corrige sumando o restando 0.7 mm Hg por cada centímetro de desplazamiento del plano cardiaco. Tensión arterial invasiva Fig No. 1 Equipo de presión arterial invasiva Una cánula colocada percutáneamente en una arteria permite la monitorización de la presión sanguínea y da la posibilidad de obtener muestras de sangre arterial. La cánula es conectada a una línea llena con líquido que incorpora un dispositivo de flush continuo e intermitente que transmite la fuerza de la onda de pulso hasta un transductor de presión que convierte el desplazamiento mecánico de un cristal de silicón en señales eléctricas vistas en un monitor (Fig. 1). Indicaciones: 1. El monitoreo continuo de la presión arterial es esencial cuando se anticipan cambios hemodinámicos rápidos. • Cirugía mayor que implique grandes desplazamientos de líquidos y pérdidas sanguíneas • Cirugía vascular mayor • Procedimiento neuroquirúrgico mayor • Hipertensión arterial severa • Shock • Uso de agentes vasoactivos o inotrópicos intravenosos • Anestesia general en el paciente con enfermedad cardiovascular 2. Necesidad de muestras frecuentes de sangre arterial. • Seguimiento de gases arteriales en pacientes con enfermedades pulmonares sometidos a ventilación mecánica • Seguimiento de estado acido-base y/o lactato sérico en fases de reanimación. 3. Imposibilidad para la medición no invasiva (Ej: obesidad mórbida) 4. Uso de balón de contrapulsación intraaórtico. Precauciones (contraindicaciones): Las contraindicaciones son relativas y lo importante es tenerlas en cuenta para variar los sitios de inserción. • Coagulopatía. Se prefieren los sitios más periféricos que permitan una adecuada compresión. • Enfermedad vascular periférica severa. Se recomienda la canalización de arterias grandes como las femorales. • Obstrucción vascular proximal al sitio de inserción. • Ausencia de circulación colateral en el sitio de canulación • Lesiones en el sitio de canulación: Infección, dermatitis o quemaduras 3 Canalización Para la canulación se emplean catéteres # 20 o menores. Se puede realizar por técnicas por punción y por incisión quirúrgica. La técnica quirúrgica no es recomendada dado que es técnicamente más difícil, tiene mayor riesgo de complicaciones y rara vez se necesita por la posibilidad de múltiples sitios para puncionar. Son más recomendables los catéteres de teflón pues son más blandos y menos trombogénicos. Para la colocación de cualquier monitoria invasiva es obligatorio usar una técnica aséptica con el empleo de guantes, mascarilla, guantes, gorro, bata y campos estériles. Ténicas por punción Existen varias técnicas y cada persona debe encontrar la que más se le facilite. Canulación directa Luego de preparar adecuadamente el sitio, como se verá más adelante, se ubica la arteria por palpación. Con una aguja con catéter adaptado se hace la punción en un ángulo piel-aguja de 30º sobre la arteria y se introduce siguiendo la dirección de la misma hasta obtener retorno sanguíneo. El ángulo de la aguja se disminuye a 10º, la aguja se avanza 1 a 2 mm más para garantizar que el catéter esté intra-arterial y se desplaza solo el catéter sobre la aguja metálica hacia la arteria observando que exista salida de sangre. Transfixión Una vez localizada la arteria, ésta es atravesada avanzando la aguja hasta que no se obtenga retorno. La parte metálica se retira completamente y el catéter se va retirando lentamente hasta obtener retorno luego de lo cual se avanza de manera suave en un ángulo de 10º. Puede facilitar la maniobra el adaptar una jeringa pequeña al catéter. Se retira el catéter adaptado a la jeringa aspirando suavemente hasta obtener sangre, se inyecta la sangre al tiempo que se va introduciendo el catéter. Seldinger Luego de hallar la arteria y obtener retorno, se introduce una guía metálica a través de la aguja. Se retira la aguja sin perder vista la guía. Se introduce el catéter deslizándolo sobre la guía y una vez que esté adentro, se retira la guía. Sitios de canulación El sitio más adecuado para realizar la canulación es el que tenga circulación colateral, que evite acodamiento del catéter, que sea confortable para el paciente y de fácil acceso para el personal. Los sitios más Fig. No. 2 Arteria radial usados son las arterias radial, femoral y pedia. El sitio de punción deberá ser esterilizado y protegido con campos estériles. Arteria radial La arteria braquial tiene dos ramas que pasan por la muñeca, la radial y la cubital. Forman tres arcos 4 anastomóticos, superficial, profundo y dorsal. Sin embargo, hasta el 20% de la población normal no tiene arco superficial o dorsal. Para asegurar el flujo adecuado hacia la mano debe estar presente alguno de estos dos arcos. Antes de la canulación se recomienda evaluar la circulación colateral. Prueba de Allen: La mano es abierta y cerrada en varias ocasiones mientras se tienen comprimidas las arterias radial y cubital en la muñeca produciendo palidez palmar. Se suelta la cubital, cuando la palma se enrojece en < 7 segundos es normal, 8-14 segundos es equívoca y > 15 es anormal. La prueba puede tener falsos positivos y negativos hasta en el 14%, varios reportes muestran que aunque la maniobra de Allen sea anormal la posibilidad de isquemia distal es muy baja, se aconseja que si da anormal se haga una evaluación con doppler de la circulación colateral antes de la canulación. La arteria radial pasa lateral al tendón del flexor radial del carpo. Para la canulación, la muñeca se coloca sobre un pequeño rollo, la mano en dorsiflexión de 30-60º y se asegura la parte distal de la palma. El sitio de inserción se infiltra con 0.5 ml lidocaína usando una aguja # 25. Luego de lo cual se procede a la canalización. El catéter se fija con sutura y luego se cubre con vendaje de gasa estéril. (Fig. 2) Arteria femoral Es el segundo sitio de elección. El ligamento inguinal marca la Fig. No. 3 Arteria femoral salida de la arteria femoral desde la iliaca externa. La arteria es grande y fácilmente palpable bajo el ligamento inguinal cerca de la unión del tercio interno con el medio (Fig. 3). La punción debe hacerse unos centímetros caudalmente al ligamento para minimizar los riesgos de hemorragia retroperitoneal y perforación de vísceras. La aguja se dirige con el bisel hacia arriba en 45 grados en dirección cefálica. La guía metálica debe pasar fácilmente y nunca ser forzada pues se puede producir lesión del vaso. Varios estudios muestran que la frecuencia de complicaciones no es mayor que la radial. Sin embargo, se debe tener espacial cuidado cuando existe enfermedad vascular periférica por la posibilidad de producir embolismos de ateromas e isquemia distal. Arteria pedia La arteria pedia corre superficialmente en el dorso del pie y pasa lateral al tendón del extensor del pulgar. Tiene anastomosis con las arterias tibial y peronea. Su canalización tiene menor tasa de éxito debido a que la anatomía es más variable. El pie es colocado en flexión plantar y la aguja se inserta en ángulo de 10 a 20º siguiendo el trayecto del vaso. Al igual que con la mano es necesario realizar prueba para ver la circulación colateral comprimiendo la arteria pedia y tibial posterior. Debido a que es una vaso más pequeño tiene mayor incidencia de oclusión trombótica y no se recomienda en enfermedad vascular periférica. (Fig. 4) Fig. No. 4 Arteria pedia 5 Complicaciones La frecuencia de complicaciones de la monitoría invasiva de la presión arterial oscila entre15-40%, pero las clínicamente relevantes ocurren en menos del 5 % de los pacientes. Varían de acuerdo al sitio de Tabla 1. Complicaciones de la canalización canalización. Las complicaciones más arterial frecuentes se muestran en la tabla 1. • Dolor y edema Existen factores que se aumentan dichas • Trombosis complicaciones (Tabla 2). • Embolización • • • • Hematoma Infección asociada a catéter Pseudoaneurisma Trombocitopenia asociada a heparina Arteria radial • • Embolización cerebral Neuropatía periférica Arteria femoral • • • • Hemorragia retroperitoneal Perforación intestinal Pseudoaneurisma Fístula arteriovenosa Todas Infección Es la complicación importante más común. Puede generar bacteremia y llevar a sepsis. La ruta más común de migración es a través del túnel dérmico, por esta razón es tan importante la técnica aséptica para la canalización y el mantenimiento. Siempre que se sospeche se debe retirar el catéter. Trombosis e isquemia distal Su incidencia es de 5 a 25 %. Es común en radial y pedia. La infusión de heparina disminuye su aparición. Es muy importante la detección temprana de signos como dolor e isquemia. La isquemia clínica es poco Tabla 2. Factores que predisponen a las frecuente y la mayoría se resuelve dentro de las complicaciones de la canulación arterial tres semanas luego de retirar el catéter. Si no hay mejoría se debe recurrir a bloqueo • Cánulas muy grandes • Hipotensión simpático, trombolisis o embolectomía • Coagulopatía quirúrgica. La oclusión que requiere • Bajo gasto cardiaco intervención quirúrgica se presenta en menos • Múltiples punciones • Uso de vasopresores del 1 %. • • • • Aterosclerosis Estados hipercoagulables Flushing Canulación por método quirúrgico Embolización Embolización de coágulos o aire a la circulación proximal o distal puede ocurrir desde el sitio de canalización especialmente si se infunden líquidos con alta presión. Para minimizar el riesgo se hacen lavados de las líneas con pequeños volúmenes y baja presión. Hematoma La formación de hematomas puede ocurrir en cualquier sitio de punción arterial especialmente si existe coagulopatía. Para disminuir la posibilidad se hace compresión luego de cada punción y al retirar el catéter. La punción de la femoral puede llevar a sangrado hacia el retroperitoneo. Esto debe sospecharse cuando hay inestabilidad hemodinámica y disminución de la hemoglobina luego de la punción. Pseudoaneurisma Ocurre cuando hay una disrupción incompleta de la pared del vaso que permite escape de sangre hacia el tejido circundante lo que con el tiempo forma una cavidad sacular. Se presenta 2 a 3 semanas luego de la canulación. Requiere corrección quirúrgica. 6 Injuria nerviosa Injuria nerviosa puede ocurrir por trauma directo con la aguja durante múltiples intentos. Precauciones en la lectura La onda de la presión arterial se puede observar en la figura 5. Para evitar lecturas erróneas se debe calibrar el sistema teniendo como punto cero el nivel de la aurícula derecha y realizar periódicamente la prueba de la onda cuadrada con lo FIG No.6 Test de flush. que se detecta sobreamortiguamiento o subamortiguamiento. La prueba se realiza haciendo un lavado rápido con el flush A intermitente y observado la caída de la curva (Fig. 6). El sobre-amortiguamiento puede causar disminución de la presión arteria sistólica y aumento de la diastólica. Es causado por la presencia de burbujas de aire en el sistema, B trombos en la punta del catéter, presión baja del infusor, oclusión parcial del catéter o pérdidas del sistema. El sub-amortiguamiento genera aumento de la sistólica y disminución de la diastólica y es causado por líneas muy largas o la presencia de múltiples llaves en la línea. El sitio de inserción afecta las ondas y cifras de presión, así C cuanto más distal de la aorta, la onda sufre amplificación. Se va encontrar una presión sistólica más elevada y una A. Curva normal; B: curva amortiguada; C. Curva submuesca dicrótica más distal. La presión arterial media no amortiguada sufre alteración. Fig No.5 Curva arterial Catéter venoso central La inserción de un catéter en una vena de gran calibre es el método estándar para la monitorización de la PVC. Existen varias indicaciones para la colocación de un catéter venoso central (Tabla 3), pero se debe definir su utilidad en casos individuales. Es importante decir que la reanimación con volumen per se no es una indicación para CVC. Debido a que un catéter más largo y de menor diámetro presenta mayor resistencia al flujo. Canulación Las rutas más comunes para colocar un acceso venoso central incluyen las venas yugular interna, subclavia y femoral. La vía se elige teniendo en cuenta las características anatómicas del paciente, la presencia de lesión o infección en los sitios de acceso, la tolerancia del paciente a la posición requerida, la preferencia y experiencia del operador y la situación clínica que se desarrolla. 7 Técnica Tabla 3. Indicaciones para la canulación venosa central Siempre se debe informar al paciente sobre las indicaciones, riesgos y • Monitoreo hemodinámico molestias que se pueden presentar. Se − Cirugía mayor con gran intercambio de líquidos − Evaluación de volumen intravascular en falla deberá monitorizar con renal electrocardiograma continuo y tensión • Administración de nutrición parenteral arterial. • Administración de medicaciones o agentes No se debe olvidar la asepsia. Se infiltra irritantes el sitio de punción con lidocaína al 1-2%. • Drogas vasoactivas concentradas La técnica más usada para el paso del • Colocación de marcapaso cardiaco transvenoso • Terapia de reemplazo renal temporal catéter es la de Seldinger. Luego de • Aspiración de embolismo aéreo hacer la punción en el sitio elegido, se • Imposibilidad de acceso venoso periférico debe entrar aspirando por la jeringa conectada a la aguja hasta obtener retorno venoso. En algunos equipos es necesario retirar la jeringa, pero en otros trae un canal para pasar la guía metálica a través de ella. La guía se introduce entre 20 y 25 cm. Se retira la aguja. Se pasa un dilatador sobre la guía. Este solo debe pasar piel y tejido subcutáneo por el riesgo de lesión severa de los grandes vasos o del corazón. Finalmente el catéter es desplazado sobre la guía. Esta, nunca se debe perder de vista pues se corre el riego de que se desplace y se pierda o cause arritmias o trauma. La ubicación del paciente en Trendelemburg de 15 a 30º puede facilitar la canalización del vaso en accesos superiores mejorando el retorno venoso y disminuyendo el riesgo de embolismo aéreo. La ubicación de un rollo de tela debajo de la línea interescapular puede ayudar especialmente en los obesos. Vena yugular Interna Ventajas Localización anatómica predecible, marcas anatómicas fácilmente identificables, posibilidad de acceso intraoperatorio. Tiene bajo riesgo de neumotórax, posibilidad de fácil compresión en caso de sangrado. Es una vía recta hacia la vena cava superior, y por lo tanto es de elección para el paso de catéteres de arteria pulmonar y marcapasos transvenosos. Tiene alta frecuencia de éxito. Desventajas Las líneas anatómicas pueden no ser identificadas en pacientes obesos o edematizados, es menos confortable y ofrece más dificultad para su cuidado que el subclavio y cuando hay traqueostomía puede ser fácilmente infectado. Procedimiento Se puede hacer a través de tres vías: • Medial. Con la cabeza del paciente girada hacia el lado contralateral, se identifican los haces clavicular y esternal del músculo esternocleidomastoideo. Esto puede ser facilitado pidiendo al paciente que levante levemente la cabeza. Luego de adecuada anestesia local, una aguja de pequeño calibre es insertada justo inferiormente a la unión de los dos haces y avanzada hacia la tetilla ipsilateral con un ángulo de 30° con la piel. La vena debe ser puncionada al haber introducido la aguja menos de 3 cm si esto no ocurre se debe reposicionar la aguja. Si se obtiene retorno venoso se marca el sitio de entrada, se retira la aguja y siguiendo la misma dirección se hace la punción con la aguja del equipo para catéter central. (FIG. pendiente) 8 • Posterior. La aguja es insertada en la margen posterior del esternocleidomastoideo aproximadamente 4 cm sobre la unión esternoclavicular, que generalmente se corresponde con la unión de la vena yugular externa y la margen posterior del músculo, y se dirige al pezón contralateral en un ángulo de 10° a 15° con la piel. (FIG) • Anterior. La aguja se inserta en el borde medio del esternocleidomastoideo, lateral al pulso carotideo, a nivel del margen inferior en el cartílago tiroideo. La aguja luego se inclina en un ángulo de 30° con la piel y se debe dirige hacia el pezón ipsilateral. (FIG) Vena Subclavia Ventajas La vía subclavia tiene las ventajas de marcas óseas fácilmente identificadas, comodidad para el paciente, facilidad mayor de preparación y mantenimiento, y una incidencia más baja de colonización bacteriana del catéter. Es de elección cuando por colapso hemodinámico no puedan ser canalizadas vías periféricas dado que no se deja colapsar por los tejidos circundantes. Desventajas No se puede comprimir el sitio de punción en caso de sangrado. Mayor riesgo de neumotórax. Procedimiento La aguja se inserta, con un ángulo de 10° a 15° con la piel, 1 cm abajo de la unión del tercio interno con los dos tercios externos de la clavícula y se dirige hacia la fosa suprasternal. Debe evitarse un ángulo más grande pues se puede perforar la cúpula pulmonar. También puede puncionarse 1 cm debajo de la unión de los dos tercios proximales con el tercio distal de la clavícula. La malposición del catéter en la vena yugular interior es menos común con este acercamiento, pero se aumentan los riesgos de perforación de arteria de subclavia y la lesión del plejo braquial. Ubicación del catéter La punta del catéter debe terminar en la vena cava superior 3 a 5 cm antes de la unión con la aurícula derecha. La punta debe estar de 13 a 16 cm desde el sitio de inserción cuando se hace por el lado derecho y de 15 a 20 cm con inserciones izquierdas. La confirmación de la posición se hace con una radiografía de tórax. Vena femoral Ventajas La vena femoral puede ser canalizada sin riesgo de neumotórax y sin interferencia con la resucitación cardiopulmonar (CPR). La presión venosa central medida por esta vía se correlaciona bien con la medida por canalización superior. 9 Desventajas Retraso en la entrega de fármacos al corazón en estados de bajo flujo, interferencia en la medida por la movilidad del paciente y una proporción más alta de colonización bacteriana del catéter. Procedimiento La aguja debe insertarse a 1 cm internamente al pulso de la arteria femoral y 1 a 3 cm debajo del ligamento inguinal. Puncionar por encima del ligamento genera el riesgo de lesión visceral. Interpretación La presión venosa central (PVC) refleja la presión de la aurícula derecha y ésta a su vez la precarga ventricular pero, está determinada no solo por el volumen sanguíneo sino por el tono vascular y la función ventricular derecha. Para su interpretación es más importante la tendencia que un valor absoluto y en especial la respuesta a la infusión de volumen. No es una medida directa de la presión de llenado izquierda pero puede estimarla si hay buena función ventricular. Puede ser afectada por trombos en la vena cava, alteración de la presión intratorácica e hipertensión pulmonar. La presión venosa central tiene una curva característica con diferentes deflexiones (Tabla 4). Para la identificación de dichas ondas se debe hacer una correlación visual con el EKG. La curva puede ayudar al diagnóstico de algunas patologías. La ausencia de onda a ocurre en fibrilación o flutter auricular. Onda a grande o “en cañón” se presenta cuando la aurícula se contrae contra la válvula triscúspide cerrada como en bloqueo AV, arritmias ventriculares y ritmo Tabla 4. Ondas en la curva de PVC idioventricular. O cuando hay resistencia al vaciamiento auricular como en estenosis Onda Evento mecánico tricuspidea, hipertrofia ventricular derecha, a Contracción auricular estenosis pulmonar o hipertensión c Contracción ventricular isovolumétrica pulmonar. Onda V grande o en cañón se v Llenado sistólico auricular presenta si hay regurgitación tricuspidea o h Meseta diastólica x Relajación auricular cuando el ventrículo derecho disminuye su y Llenado ventricular temprano distensibilidad por isquemia o falla. Precauciones: • El síndrome de vena cava superior es una contraindicación para la canulación en el cuello, tórax y extremidades superiores. Se deben usar accesos de la parte inferior del cuerpo (femoral). • Si existe infección en el sitio de canulación se debe usar otro acceso. • En presencia de coagulopatía se deben usar accesos en donde sea fácil hacer compresión como el cuello y la región inguinal. 10 Complicaciones Tabla 5. Complicaciones de la inserción de CVC Las complicaciones son infrecuentes cuando se hace por personal adecuadamente entrenado y con la Durante la canulación técnica apropiada. Se pueden dividir en las producidas • Hematoma durante la inserción y durante la permanencia del • Fístula AV • Hemotórax catéter (Tabla 5). • Quilotórax La más frecuente es la punción arterial. Si ocurre, se • Neumotórax retira la aguja y se hace presión externa por al menos • Injuria nerviosa 5 minutos. Cuidado especial se debe tener cuando la • Ruptura cardiaca punción es de la arteria carótida especialmente • Embolismo aéreo • Ruptura del catéter o de la guía cuando se introduce el catéter, pues este tiene que ser removido y al hacerlo existe la posibilidad de Presencia del catéter • Trombosis hematoma con el riesgo de compromiso de la vía • Infección aérea lo que requiere intubación por eso vigilancia de • Arritmias • Hidrotórax vía aérea y neurológica. Neumotórax ocurre más frecuentemente cuando se hace por vía subclavia. Cuando se presenta neumotórax pequeños y el paciente permanece clínicamente estable, se debe manejar con observación y seguimiento radiográfico. Cuando el neumotórax es mayor del 20 %, el paciente se inestabiliza, está en ventilación mecánica o está programado para cirugía mayor se debe pasar un tubo de toracostomía. El taponamiento cardiaco por ruptura de la VCS, la aurícula o el ventrículo derechos se debe sospechar cuando hay colapso súbito luego de su colocación, ocasionalmente hay retraso en el diagnóstico. Esto hace justificada la realización rutinaria de Rx de tórax luego de paso de CVC para verificar su ubicación. La aparición de arritmias habla de la presencia del catéter en el ventrículo y es necesario retirarlo. La complicación tardía más importante es la infección. La infección asociada a catéter se presenta en un 5 % de pacientes con catéter venoso central, esto aumenta la estancia hospitalaria, el costo y la morbilidad del paciente por eso está justificado cada esfuerzo en prevenirla con adecuada técnica de inserción y mantenimiento. Catéter de arteria pulmonar (Swan-Ganz) El catéter de arteria pulmonar puede ayudar a establecer la naturaleza de problemas hemodinámicos, mejora la exactitud del diagnóstico y proporciona información que a menudo incita cambios en el tratamiento. Disminuye el riesgo de edema pulmonar y permite el uso racional de inotrópicos y vasoactivos. No obstante, su influencia en el resultado clínico permanece incierta. No hay datos concluyentes que demuestren mejoría. Incluso, algunos estudios han sugerido que el uso del catéter empeora el resultado. Esto puede ser debido a mala técnica en las mediciones y/o interpretación errónea lo que genera malas conductas terapéuticas. Está claro que el uso inapropiado y el pobre entendimiento del funcionamiento elevan la mortalidad. Indicaciones A pesar de su uso por casi un cuarto de siglo, las indicaciones aún no han sido científicamente establecidas. La decisión de colocarlo en el intraoperatorio debe estar basada en las características hemodinámicas del riesgo en cada caso 11 individual y en el entrenamiento del personal para su colocación, interpretación y manejo. Además debe ir precedida de una pregunta específica acerca de la hemodinamia del paciente que no sea respondida por otros métodos. Si su respuesta tiene trascendencia para el manejo, el catéter está indicado. Se usa en procedimientos quirúrgicos de alto riesgo de complicaciones hemodinámicas. El riesgo se determina en función del estado de salud del paciente y del procedimiento quirúrgico. Los pacientes de alto riesgo son los que tienen evidencia clínica de enfermedad cardiovascular significativa, disfunción pulmonar, falla renal u otra condición asociada con inestabilidad hemodinámica. El catéter ayuda en la detección de isquemia intraoperatoria de manera más precoz que el EKG mostrando elevación de la POAP o alteración del trazo con la elevación de las ondas A y V, pero no es tan sensible y específico como la ecocardiografía intraoperatoria. En general las indicaciones son: • • • • • • • Shock que no responde al tratamiento o en el que haya duda en el diagnóstico. Trauma mayor como guía para reemplazo de volumen y uso de apoyo hemodinámico. Infarto de miocardio con inestabilidad hemodinámica. Para diferenciar hipovolemia de shock cardiogénico. Edema pulmonar, para diferenciar si es cardiogénico o no cardiogénico (SDRA) y guiar su manejo. Cirugía de alto riesgo hemodinámico que involucre recambio alto de volemia. Pre-eclampsia severa con edema pulmonar y oliguria Cirugía cardíaca en pacientes con fracción de expulsión menor al 40 %, disquinesia ventricular izquierda, infarto miocárdico reciente o angina inestable, complicaciones post-infarto o reoperaciones. Descripción del catéter El catéter está hecho con pilivinilcloruro y dado que este material es trombogénico se recubre con heparina. Tiene Fig 7. Descripción del catéter de arteria pulmonar 110 cm de longitud y de 5 a 7.5 French de diámetro. Tiene marcas cada 10 cm para conocer la distancia que ha sido introducido. Tiene un balón a 2 mm de la punta. A 4 cm del orificio distal se ubica un termistor que permite la medición del gasto cardiaco por termodilución. Puede tener cuatro o cinco lúmenes. Uno de color azul termina a 30 cm de la punta y permite la medición de la presión venosa central. El lumen distal termina en la punta y mide la presión pulmonar y la presión de oclusión de la arteria pulmonar. Un lumen para inflar el balón y otro con conexión eléctrica hacia el termistor. El puerto accesorio sirve para infusión de líquidos y medicamentos. 12 Técnica de inserción El sitio de inserción se determina individualmente según los riesgos y ventajas para cada paciente. Las vías yugular interna derecha y subclavia izquierda permiten el paso más fácil del catéter hacia la arteria pulmonar. Antes del procedimiento se debe alistar todo el equipo para la inserción y la supervisión de las presiones. Se deben instalar y calibrar las líneas y los transductores de presión, purgar todas las vías e inflar el balón para descartar escapes. El catéter se pasa a través de un introductor, que debe tener 1 French de diámetro más que el catéter. La técnica de inserción del introductor a la vena es igual que para cualquier acceso venoso central, pero se debe hacer una pequeña insición en la piel para fácilitar su paso. La atención meticulosa a la técnica estéril es absolutamente necesaria. La inserción se facilita orientando el catéter de manera tal que su curva siga el curso que tomará hacia el corazón. Se infla el balón cuando la punta esté en la aurícula derecha (AD). La distancia aproximada a la AD varía según el sitio de inserción. Así por vía yugular interna será de 15 a 20 cm, subclavia 10 a 15 y femoral 30 a 40. Nunca se debe avanzar de este punto sin inflar el balón y si el catéter se va a reposicionar se debe desinflar. Al avanzar el catéter, es útil tener presente la "regla de los 10s" que da una pauta general para correlacionar los cambios anatómicos con los hemodinámicos. Así la AD estará a los 20 cm, el ventrículo derecho (VD) en 30 y la arteria pulmonar (AP) en 40 cuando se pasa por vía subclavia. El trazo de presión ayuda a confirmar la localización de la punta (Fig 7). Cuando el catéter entra al VD, el trazo registrará un aumento dramático en la presión sistólica. Fig 8. Cambios de la curva de presión a medida que se avanza el catéter de arteria pulmonar PAD: presión de aurícula derecha; PVD: presión de ventrículo derecho; PAP: presión de arteria pulmonar; POAP: presión de oclusión de arteria pulmonar 13 Ésta es la localización con el mayor riesgo de arritmias y por lo tanto se debe pasar rápidamente. Al llegar a la AP la presión diastólica se eleva y aparece una muesca dicrótica característica. Si se avanzan más de 15 cm del catéter y el trazo sigue constante con VD, el catéter se está enrollando en él. Se debe desinflar balón y retirarlo hasta la AD y reintentar el paso. De la AP, el catéter debe ser avanzado (con el globo inflado) hasta que se observe una caída en la presión sistólica. Ésta es la presión de oclusión de la arteria pulmonar (POAP). En este punto, el balón debe ser desinflado y el trazo de la presión arterial pulmonar (PAP) debe reaparecer. Si persiste el trazo de la POAP, el catéter debe ser retirado hasta que aparezca el de PAP. El catéter debe ubicarse para que la POAP se obtenga inflando el balón con un volumen de 1 a 1.5 ml. Si se necesita menor volumen indica que la punta está muy distal y existe el riesgo de ruptura arterial. Si se necesita mayor volumen indica que está muy proximal y puede deslizarse al VD con el riesgo de arritmias y de daño intracardiaco. Una vez se alcance la posición adecuada, es esencial asegurarlo para prevenir la migración. Se anota la distancia a la cual se encontró la POAP para detectar desplazamientos. Se confirma la posición del catéter con una radiografía de tórax. La punta del catéter debe estar de 3 a 5 centímetros de la línea media. Debe evaluarse la resistencia para inflar el balón, resistencia excesiva puede indicar mala posición de la punta y poca resistencia implica ruptura del balón. Valores medidos Varios parámetros hemodinámicos pueden ser medidos: gasto cardiaco y las presiones venosa central, arterial pulmonar y de oclusión de arteria pulmonar. Muestra sanguinea de la arteria pulmonar nos dará la saturación venosa mixta de oxígeno (SvO2) (Tabla 6). Tabla 6. Parámetros medidos Parámetro Rango normal TAM FC PVC PVD PAP PAPM POAP GC SvO2 80 – 102 60 – 100 0-8 25 / 0-4 15 - 25 / 8 – 15 10 – 20 6 – 14 4–7 70 – 80 mmHg L / min mmHg mmHg mmHg mmHg mmHg L / min % Presión aurícular derecha (PAD- PVC) TAM: Presión arterial media; FC: frecuencia cardiaca; PVC: Presión venosa central; PVD: Presión ventrículo derecho; Refleja el retorno venoso y la presión del PAP: Presión arterial pulmonar; PAPM: Presión arterial ventrículo derecho al final de la diástole. pulmonar media; POAP: Presión de oclusión de arteria pulmonar; GC: Gasto cardiaco; SvO2: saturación venosa La curva tiene normalmente tres mixta de oxígeno componentes positivos y dos desviaciones negativas que ya fueron descritas en un apartado anterior (Tabla 4). La PVC se aumenta en infarto ventricular derecho, hipertensión pulmonar, estenosis pulmonar, cortocircuitos de izquierda a derecha, valvulopatía tricuspidea, sobrecarga de volumen y disfunción del ventrículo derecho. Presión arterial pulmonar (PAP) Los componentes del trazo arterial pulmonar son sístole, diástole y la muesca dicrótica que representa el cierre valvular pulmonar. La presión pulmonar es menor que la sistémica. Se eleva con sobrecarga de volumen o aumentos de la resistencia vascular pulmonar como en hipertensión pulmonar primaria, embolismo pulmonar, 14 hipoxemia con vasoconstricción pulmonar, cortocircuitos de izquierda a derecha, insuficiencia cardiaca izquierda y enfermedad mitral. Fig 9. Medición de la POAP en en ciclo respiratorio Presión de oclusión de la arteria pulmonar (POAP) Se obtiene inflando el balón para interrumpir el flujo sanguineo a través de una rama de la arteria pulmonar. Esto crea una columna estática de sangre entre la punta del catéter y la aurícula izquierda. Con la oclusión el trazo cambia de presión de arteria pulmonar a presión auricular izquierda. La caida tiene un componente rápido que representa la presión a través de la arterias pulmonares y uno lento, la de las venas pulmonares. La razón para medir la POAP es que estima la PAI, lo que a su vez, estima la presión diástolica final del ventriculo izquierdo (PDFVI). La PDFVI es un índice de volumen diastólico final del ventrículo izquierdo (VDFVI). Así, la POAP es una medida de presión ventricular y no de volumen o precarga pero se asume que hay una relación directa entre las dos siempre que no haya alteraciones de distensibilidad y no haya ninguna obstrucción para el flujo entre las dos cavidades. Los datos sugieren que hasta el 50 % de las medidas son incorrectamente determinadas y/o mal-interpretadas resultando en terapeuticas inadecuadas. Para minimizar los errores se deben seguir las siguientes recomendaciones: • Calibrar el transductor con un punto ubicado en el cuarto espacio intercostal con línea media axilar. • Siempre se debe hacer con el paciente en supino. • Chequear la distensibilidad del sistema y corregir los errores como se explicó en el apartado de presión arterial invasiva (Fig. 6). • Corroborar que la punta esté en zona 3 de West para que refleje la presión vascular y no la alveolar (Tabla 7). • Medida la POAP al final de la espiración cuando la presión pleural haya retornado a la línea de base (Fig. 9). • Se mide en el punto medio entre la onda a y la x. Tabla 7. Verificación de posición en zona 3 Característica Contorno POAP PAPD vs POAP Ensayo de PEEP Variación respiratoria Localización de la punta Zona 3 Ondas a, c, v PAPD > POAP Zona 1 o 2 Plana PAPD < POAP ∆ POAP < ½ ∆ PEEP ∆ POAP > ½ ∆ PEEP ∆ PAPS / ∆ POAP ≤ 1 A nivel o bajo la AD ∆ PAPS / ∆ POAP > 1 Por encima de AD POAP: Presión de oclusión de arteria pulmonar; PAPD: Presión arterial pulmonar diastólica; PAPS: Presión arterial pulmonar sistólica. La PDFVI es mayor que la POAP cuando hay distensibilidad anormal o disfunción diastólica como en isquemia miocárdica y taponamiento cardíaco, así mismo, en la insuficiencia aórtica severa. Un neumotórax a tensión aumenta la POAP y disminuye 15 el VDFVI. La POAP puede exceder la presión diastólica final ventricular izquierda en pacientes con enfermedad pulmonar y falla respiratoria, debido a la constricción de venas pequeñas en segmentos hipóxicos del pulmón. Fig 10. Medición de la capilar pulmonar La POAP no es el único factor a tener en cuenta para la prevención del edema pulmonar. Se deben considerar además de la presión hidrostática, la permeabilidad de las membranas y la presión coloido-osmótica. A pesar de que en la mayoría de los casos la POAP se corresponde con la presión capilar pulmonar (Pc), determinante de la presión hidrostática, en situaciones de aumento de la resistencia vascular pulmonar, la Pc excede la POAP. Por esta razón un paciente puede tener POAP normal y tener edema pulmonar hidrostático. Para determinar la Pc, se debe tomar el punto en el cual luego de inflar el balón, la curva cambia de la fase de descenso rápido a la de descenso lento (Fig. 10). Asumir que la POAP es igual a la presión de cuña capilar, en algunos casos es erróneo. Se plantea que en ventilación mecánica con alto PEEP se altera la POAP, debido al aumento de la presión pleural. Sin embargo, dado que altos niveles se usan en pacientes con SDRA, que tienen baja distensibilidad pulmonar, la presión no será transmitida de gran forma hacia la vasculatura y por lo tanto no alterará de forma importante la medida. Es dificil estimar qué tanta presión será transmitida del alvéolo a la vasculatura. Un trabajo en animales demostró que había una diferencia importante entre la POAP y la PAI si había PEEP > 10 cm de H2O si los pulmones estaban sanos, pero cuando se medían en pulmones con injuria, la correlación fue excelente con PEEP hasta de 20 (Fig. 11). No se recomienda desconectar al paciente con PEEP para medir la POAP pues la situación hemodinámica varía por aumento del retorno venoso y se presenta hipoxia de la que será dificil recuperarlo. Fig 11. Diferencia entre la POAP y la PAI con aumentos del PEEP El valor absoluto de la POAP en la valoración de la precarga y por lo tanto en el manejo de la volemia, es menos importante que el cambio en respuesta al tratamiento. Así cuando el ventrículo está “lleno”, pequeños cambios de volumen incitan grandes cambios en la POAP sin mejorar el índice sistólico (IS). Para el manejo de líquidos se puede usar la “regla 7-3”. La configuración del trazo de la POAP es similar a la aurícula derecha con las ondas Tabla 8. La “regla 7-3” para el manejo de líquidos guiado por POAP POAP inicial (mmHg) Líquido (mL) < 10 10 – 15 > 15 200 mL en 10 min. 100 mL en 10 min. 50 mL en 10 min. Respuesta Terapia ↑ POAP > 7 ↑ POAP 3 – 7 Aún ↑ POAP > 3 ↑ POAP < 3 No require más líquidos Reevaluar en 10 minutos No require más líquidos Requiere más líquidos 16 a, x, c, v , y. Pero el retraso electromecánico es mayor debido al tiempo necesario para que los eventos mecánicos de la aurícula izquierda sean transmitidos a través de la vasculatura pulmonar hasta la punta del catéter. Como guía, la onda V está inmediatamente después de la onda T de un EKG simultaneo. La onda se eleva con aumentos de la resistencia al llenado ventricular izquierdo, como sucede en estenosis mitral, disfunción ventricular izquierda, sobrecarga de volumen e isquemia miocárdica. Las elevaciones en la onda de v representan una carga aguda de volumen a la aurícula izquierda como en defecto septal ventricular o regurgitación mitral. Esto hace que al inflar el balón no aparezca la curva característica y dé la impresión de no haber cuñado. Además, la POAP sobreestima la PAI. Para obviar este problema se debe reconocer la onda v con ayuda de un EKG. La POAP se mide al inicio de la onda V. Cálculo del gasto cardiaco Existen varios métodos para medir el gasto cardiaco. El método de dilución usa una concentración conocida de un indicador agregada a un líquido. Luego de un tiempo de mezcla, la dilución de dicho indicador medirá la cantidad de líquido a la que fue agregado. El catéter de arteria pulmonar usa el método de termodilución, usando el cambio de temperatura como indicador. Se inyecta rápidamente una cantidad conocida de líquido con una temperatura conocida a la AD a través del puerto proximal. Este se mezcla con la sangre y la enfría. El termistor que está en la punta del catéter mide el cambio de temperatura en la arteria pulmonar a medida que la sangre va pasando. Un computador grafica el cambio como curva de temperaturatiempo. El área bajo la curva es inversamente proporcional al gasto cardiaco (Fig. 12). La infusión se hace con 10 ml de dextrosa o solución salina con una temperatura menor, 10°C o más, que la del paciente. Debe infundirse en menos de 4 segundos e idealmente al final de la espiración. Siempre se toman tres o más medidas para luego promediarlas. Fig 12. Curva de gasto cadiaco (GC) medido por termodilución GC normal GC alto GC bajo La regurgitación tricuspidea produce un pico atenuado y una fase de lavado prolongada de la curva temperatura-tiempo lo que genera subestimación del gasto cardiaco. Los cortocircuitos intracardiacos producen medidas falsamente elevadas. Saturación venosa mixta (SVO2) La SVO2 refleja aspectos del balance tisular global de oxígeno. La SvO2 tiene relación directa con la saturación arterial de oxígeno, hemoglobina y gasto cardiaco y es inversamente proporcional al consumo de oxígeno (VO2). Asi, se disminuye si 17 disminuye el gasto cardiaco, la SaO2, el nivel de hemoglobina o porque aumenta el consumo de oxígeno. Cálculo de la saturación venosa mixta SvO2 = SaO2 VO2 GC x 1.34 x Hb SvO2: Saturación venosa mixta de oxígeno; SaO2: saturación arterial de oxígeno; GC: gasto cardiacco; Hb: hemoglobina. Para medirla, se aspira sangre desde el puerto distal del caterter de arteria pulmonar muy lentamente para no oxigenar la muestra. Una disminución indica que la entrega ha disminuido y por lo tanto que está alterado el metabolismo oxidativo de los tejidos o que el consumo ha aumentado. SvO2 se encuentra elevada en sepsis, cortocircuitos portocava, fístula A-V, pancreatitis, intoxicación por cianuro o monóxido de carbono o por una aspiración rapida a través del catéter. Variables derivadas A partir de las presiones medidas, gasto cardiaco y SVO2, se pueden obtener variables fisiológicas derivadas de fórmulas que intentan evaluar la postcarga (resistencia vascular sistémica y pulmonar) y la contractilidad (índice cardiaco, trabajo ventricular derecho e izquierdo). Es importante no caer en la “trampa” de tratar números y no pacientes por eso siempre se deben interpretar en el contexto clínico que se está presentando. Es recomendable el uso de índices dado que ajustan los valores a la superficie corporal del individuo. Las fórmulas y valores normales están en la tabla 9. Tabla 9. Parámetros derivados del catéter de arteria pulmonar Parámetro Fórmula Rango normal IC VS IS ITSVI ITSVD RVS IRVS RVP IRVP CaO2 DO2 VO2 GC / SC GC / FC VS / SC 0.0136 x IS X (TAM - POAP) 0.0136 x IS X (PAPM - PVC) 80 x (TAM-PVC) / GC RVS x SC 80 x (PAPM – POAP) / GC RVP x SC (Hb x 1.34 x SaO2) + (0.031 x PaO2) GC x CaO2 x 10 1.39 x Hb x (SaO2-SvO2) x GC x 10 2.5-4 L/min 60-100 mL 4 0-50 mL/m2 50-62 g.M/m2 5-10 g.M/m2 5 900 – 1200 dinas.seg/cm 1800 – 2500 dinas.seg/cm5/m2 100 - 250 dinas.seg/cm5 250 – 300 dinas.seg/cm5/m2 17 – 20 mL/dL 950 – 1100 mL / min 200 – 250 mL / min IC: Índice cardiaco; VS: Volumen sistólico; IS: Índice sistólico; ITSVI: índice de trabajo sistólico del ventrículo izquierdo; ITSVD: índice de trabajo sistólico del ventrículo derecho; RVS: resistencia vascular sistémica; IRVS: índice de resistencia vascular sistémica; RVP: resistencia vascular pulmonar; IRVP: índice de resistencia vascular pulmonar; CaO2: contenido arterial de O2; DO2: entrega de O2; VO2: consumo de O2. Interpretación de los datos Cuando los datos se analizan en forma conjunta, los pacientes se pueden clasificar en varios perfiles. Este esquema simple permite aclarar la etiología del proceso 18 Tabla 10. Perfiles hemodinámicos POAP IC TAM IRVS 6-14 2.5-4 80 - 100 1900-2500 Hipovolemia ↓ ↓ ↓ ↑ Sobrecarga ↑ ↑ ↑ N ↓/N ↑ ↓ ↓↓ Falla VI ↑ ↓ ↓ N/↑ Taponamiento cardiaco ↑ ↓ ↓ N/↑ Normal Shock distributivo POAP: Presión de oclusión de arteria pulmonar; IC: Índice cardiaco; TAM: Presión arterial media; IRVS: índice de resistencia vascular sistémica primario y así determinar la terapia (Tabla 10). El catéter ayuda en el diagnóstico de taponamiento cardiaco, evento en el cual se igualan todas las presiones diastólicas (AD, VD, PDAP y POAP) Complicaciones Las complicaciones se pueden presentar durante la inserción y por el mantenimiento y uso del catéter. Inserción del catéter En el apartado de catéter venoso central ya se trataron las complicaciones relacionadas con el acceso vascular. Los problemas asociados al paso del catéter son causados por trauma a los vasos y el corazón, que llevan a la ruptura o inflamación vascular, daño de la válvula tricúspide o arritmias. Estas complicaciones pueden ser reducidas asegurándose que el balón está inflado completamente después de entrar a la AD. Sin embargo, algunas complicaciones son inevitables. Por ejemplo, arritmias auriculares y ventriculares, ocurren comúnmente durante el paso del catéter a través de las cavidades cardiacas. La mayoría son auto-limitadas. El bloqueo de rama derecha se presenta en 5 % de inserciones, poniendo a pacientes con bloqueo de rama izquierda preexistente, en riesgo para bloqueo completo. Aunque el riesgo es bajo y generalmente temporal, no se debe insertar en tal situación. Si es mandatorio, se debe colocar un marcapaso externo o transvenoso temporal profiláctico, o usar un catéter con vía para marcapaso. Nudos del catéter alrededor de si mismo pueden ocurrir durante la inserción si se introduce gran longitud o si es repetidamente retirado y avanzado especialmente en presencia de cavidades derechas dilatadas. Esto se evita teniendo cuidado de no exceder la distancia prevista desde el punto de inserción a la arteria pulmonar. Para retirar el nudo se pasa una guía metálica a través del catéter siempre bajo visión fluoroscópica pues puede romper el catéter y causar lesión cardiaca. Si no se tiene éxito se pide interconsulta con cirugía vascular para extraerlo por venotomía o a radiología intervensionista. Uso y mantenimiento del catéter Se incluyen en este grupo la ruptura de la arteria pulmonar, el infarto pulmonar y los embolismos. La complicación más temida es la ruptura de la arteria pulmonar, con una mortalidad mayor al 30 %. Puede ocurrir durante la inserción pero se presenta principalmente por inflar el balón cuando el catéter está muy distal en la pulmonar. Los factores de riesgo para la ruptura son hipertensión pulmonar, edad avanzada, enfermedad válvular mitral, hipotermia y terapia anticoagulante. En estos casos, es 19 recomendable utilizar la presión diastólica de la pulmonar como aproximación a la POAP. Puede manifestarse de varias formas, si hay hemorragia hacia el árbol broncoalveolar habrá hemoptisis, si hay hemorragia parenquimal generará hemotórax, pero también puede formarse un coagulo en el sitio de perforación evitando el sangrado pero generando un seudoaneurisma. El manejo se hace de acuerdo a la presentación. El manejo de un paciente inestable se muestra en la figura 13. Si existe sospecha de ruptura por hemoptisis leve o pasajera se descartará siempre la presencia de seudoaneurisma. Un radiografía de tórax mostrará el “signo del halo”. Siempre hay que realizar angio-TAC o angigrafía pulmonar. Si se encuentra el seudoaneurisma, siempre se hace embolización o resección quirúrgica para evitar una ruptura posterior. La migración distal de la punta o el globo inflado por tiempo prolongado pueden generar infarto arterial pulmonar. Generalmente son pequeños y asintomáticos y diagnosticados solamente por radiografía de tórax. El tromboembolismo es una complicación infrecuente especialmente por el uso de catéteres recubiertos con heparina. Los pacientes con alto riesgo (estados hipercoagulables, inserciones traumáticas o permanencias prolongadas) deben ser considerados para anticoagulación sistémica. Trombos murales inducidos por inflamación o infección de una pared cardiaca ocurren en 33 %, vegetaciones estériles se ven hasta en el 90 % de los casos. La ruptura del balón y embolia de aire puede ocurrir si se sobrepasa el volumen aconsejado para su inflado. Catéteres nuevos Los catéteres con espectrofotometría fibróptica incorporan la supervisión oximétrica continua de saturación venosa mixta y del gasto cardiaco. Estos catéteres han demostrado buena correlación con la saturación medida por co-oximetría y el gasto por el método de bolos. Son más costosos y no han disminuido eventos hemodinámicos adversos, estancia en UCI o mortalidad frente al estándar. El catéter con termistor de respuesta rápida permite la medición de la fracción de eyección del ventrículo derecho (FEVD), con ésta se calcula el índice de volumen diastólico final del ventrículo derecho (IVDFVD) dividiendo el índice sistólico sobre la FEVD. Aunque la forma y geometría complejas del VD crean dificultades para la medición segura de la FEVD, ésta se ha correlacionado bien con mediciones hechas con ventriculografía nuclear o de contraste y ecocardiografía. Se ha sugerido que el IVDFVD es un mejor indicador de precarga y mejor guía para reanimación que la POAP especialmente en pacientes con trauma abdominal o conectados a ventilación mecánica con PEEP. El IVDFVD óptimo oscila entre 90 y 140 mL/m2. Ecocardiografía transesofágica La ecocardiografía transesofágica (ETE) intraoperatoria es un procedimiento relativamente nuevo. Es una herramienta especial y no una técnica intraoperatoria estándar. Es útil para determinar el gasto cardiaco, la función miocárdica y para optimizar el volumen circulante perioperatorio. La calidad mejorada de la imagen 20 acústica de la ETE permite diagnosticar isquemia miocárdica, confirmar la suficiencia de reconstrucciones valvulares y otras reparaciones quirúrgicas, determinar la causa de desórdenes hemodinámicos y otras complicaciones intraoperatorios. El acceso en tiempo real a esta información ha permitido a cirujanos corregir reparaciones inadecuadas antes de que los pacientes salgan del quirófano, ha reducido la necesidad de reoperaciones y ha facilitado la prevención y el tratamiento temprano de complicaciones perioperatorias. Otros dispositivos, tales como electrocardiografía y catéter de arteria pulmonar, pueden proporcionar el control continuo del funcionamiento cardiaco, pero no pueden proporcionar información importante como anormalidades del movimiento de la pared miocárdica o fuga perivalvular Indicaciones Las indicaciones en las que es útil mejorando el resultado son: Riesgo alto de isquemia, infarto miocárdico o disturbios hemodinámicos durante • el perioperatorio como en enfermedad coronaria, disfunción ventricular izquierda y cirugía de revasularización coronaria Evaluación intraoperatoria de disturbios hemodinámicos que no responden al • tratamiento en los que se desconocen la función ventricular y sus determinantes Reparo y reemplazo valvular • Cirugía para corrección de defectos congénitos cardiacos • Reparo quirúrgico de aneurismas cardiacos • Remoción quirúrgica de masas cardiacas • Detección de émbolos de aire durante cardiotomías • Evaluación de anastomosis durante trasplante cardiaco y/o pulmonar • Reparo quirúrgico de cardiomiopatía hipertrófica obstructiva • Reparo de disección aórtica torácica • Inestabilidad hemodinámica inexplicada en la unidad de cuidados intensivos • Aunque el procedimiento es generalmente seguro, la inserción apropiada del dispositivo requiere entrenamiento y habilidad. Hay algunos riesgos inherentes a su colocación, incluyendo trauma faringeo y/o laringeo, lesiones dentales, trauma de esófago, sangrado, arritmias y trastornos hemodinámicos. Es costoso y está disponible en pocos centros especializados. Resumen La monitoría de las funciones vitales es esencial para el temprano reconocimiento de problemas fisiológicos. El proceso incluye observación, vigilancia, instrumentación, interpretación y terapia correctiva. El uso de monitoría invasiva, presión venosa central, presión arterial no invasiva y catéter de arteria pulmonar solo debe usarse en situaciones que estén adecuadamente indicadas porque los datos aportados por ella cambiarán o facilitarán el manejo hemodinámico. La ecocardiografía trasesofágica intraoperatoria es una herramienta especial útil valorando la función miocárdica y la volemia; permite diagnosticar isquemia miocárdica, confirmar la suficiencia de reconstrucciones valvulares y otras reparaciones quirúrgicas. Siempre se deben conocer y manejar tempranamente las complicaciones presentadas. 21 Referencias 1. Mark J, Slaughter T and Reves J. Cardiovascular Monmitoring. En: Miller RD. Anestesia. Ed. Churchill Livingsqtone. 5a. ed. 2000. Pp: 1117-1206. 2. Vender J, Gilbert H. Monitoring the Anesthetized Patient. En: Barash P, Cullen B, Stoelting R. Clinical Anesthesia.Ed Lippincott-Raven. 3a. ed.1997.Pp 62141. 3. Reich D, Moskowitz D, Kaplan J. Hemodynamic Monitoring. En Kaplan JA. Cardiac Anestesia. Ed WB Saunders. 4a. ed. 1999. Pp: 321-357 4. Seneff MG. Central Venous Catheters. En Irwin R, Cerra F, Rippe J. Irwin and Rippe´s Intensive care Medicine. Ed. Lippincott-Raven. 4a. ed.1999. 17-35 5. Seneff MG. Arterial Line Placement and Care. En Irwin R, Cerra F, Rippe J. Irwin and Rippe´s Intensive care Medicine. Ed. Lippincott-Raven. 4a. ed.1999. 36-46. 6. Voyce S. Pulmonary Artery Catheters. En Irwin R, Cerra F, Rippe J. Irwin and Rippe´s Intensive care Medicine. Ed. Lippincott-Raven. 4a. ed.1999. 46-71 7. Kelly R, Lodato R, Schlichtig R, et al. Cardiovascular Monitoring. En Tobin M. Pinciples and Practice of Intensive Care Monitoring. Ed. McGraw-Hill.1998. 719-977 8. A Report by the American Society of Anesthesiologists Task Force on Pulmonary Artery. Practice Guidelines for Pulmonary Artery Catheterization Catheterization. Anesthesiology 1993;78:380-394 9. Turnan K., Carroll G., Ivankovich A. Pitfalls in Interpretation of Pulmonary Artery Catheter Data. Journal of Cardiothoracic Anesthesia. 1989 3(5):625-41. 10. A Report by the American Society of Anesthesiologists and the Society of Cardiovascular Anesthesiologists Task Force on Transesophageal Echocardiography. Practice Guidelines for Perioperative Transesophageal Echocardiography. Anesthesiology 1996: 84:986-1006.