clase-1.ppt
Anuncio

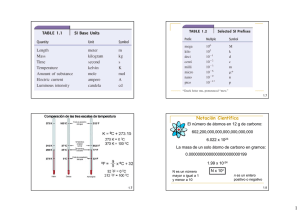
Química: el estudio de los cambios Raymond Chang; Capitulo 1, Las Herramientas de la Química La química es el estudio de la materia y de los cambios que experimenta. 1. La materia es cualquier cosa que ocupa un espacio y que tiene masa. 2. Una sustancia es una forma de materia que tiene una composición definida y propiedades características. agua, amoniaco, sacarosa, oro, oxígeno. 1.4 Una mezcla es una combinación de dos o más sustancias en la cual las sustancias conservan sus propiedades características. 1. Mezcla homogénea: la composición de la mezcla es la misma en toda la disolución. bebida no alcohólica, leche, soldadura 2. Mezcla heterogénea: la composición no es uniforme en todas partes. cemento, virutas de hierro en arena 1.4 Los medios físicos puede usarse para separar una mezcla en sus componentes puros. destilación imán 1.4 Un elemento es una sustancia que no se puede separar en sustancias más simples por medios químicos. • Se han identificado 115 elementos • 83 elementos se encuentran en forma natural en la Tierra oro, aluminio, plomo, oxígeno, carbono, • 32 elementos se han obtenido por medios científicos tecnecio, americio, seaborgio 1.4 Un compuesto es una sustancia formada por átomos de dos o más elementos unidos químicamente en proporciones definidas. Los compuestos sólo pueden separarse en sus componentes puros (elementos) por medios químicos. Agua (H2O) Glucosa (C6H12O6) Amoniaco (NH3) 1.4 Clasificación de la materia Materia Separación por Mezclas métodos físicos Sustancias puras Separación por Mezclas homogéneas Mezclas heterogéneas Compuestos métodos químicos Elementos 1.4 Los tres estado de la materia Sólido Líquido Gas 1.5 ¿Física o química? Una propiedad física no altera la composición o identidad de la sustancia. azúcar disuelta fusión de hielo en agua Una propiedad quimica altera la composición o identidad de la sustancia(s) involucrada(s). El hidrógeno se quema en presencia del aire para formar agua. 1.6 Materia: cualquier cosa que ocupa un espacio y tiene masa. Masa: medida de la cantidad de materia. La unidad SI de masa es el kilogramo (kg) 1 kg = 1000 g = 1 x 103 g Peso: fuerza que ejerce la gravedad sobre un objeto. peso = c x masa sobre la Tierra, c = 1.0 1 kg sobre la Tierra sobre la Luna, c ~ 0.1 0.1 kg sobre la Luna 1.7 Tabla 1.2 Unidades SI básicas Cantidad fundamental Nombre de la unidad Longitud metro Masa kilogramo Tiempo segundo Corriente eléctrica ampere Temperatura kelvin Cantidad de sustancia mol Intensidad luminosa candela Símbolo m kg s A K mol cd 1.7 Tabla1.3 Prefijos utilizados con unidades SI Prefijo Símbolo Significado TeraGigaMegaKilo- T G M k 1012 109 106 103 DeciCentiMilliMicro- d c m 10-1 10-2 10-3 10-6 NanoPico- m n p 10-9 10-12 1.7 Volumen: la unidad de volumen derivada del SI es el metro cúbico (m3). 1 cm3 = (1 x 10-2 m)3 = 1 x 10-6 m3 1 dm3 = (1 x 10-1 m)3 = 1 x 10-3 m3 1 L = 1000 mL = 1000 cm2 = 1 dm3 1 mL = 1 cm3 1 Litro Matraz volumétrico 1.7 Densidad: la unidad derivada del SI para la densidad es el kg/m3 1 g/cm3 = 1 g/mL = 1000 kg/m3 masa densidad = volumen m d= V Un pedazo de metal de platino con una densidad de 21.5 g/cm3 tiene un volumen de 4.49 cm3. ¿Cuál es su masa? m d= V m = d x V = 21.5 g/cm3 x 4.49 cm3 = 96.5 g 1.7 Comparación de las tres escalas de temperatura Punto de ebullición del agua K = 0C + 273.15 273 K = 0 0C 373 K = 100 0C Temperatura corporal normal Temperatura ambiente Punto de congelación del agua 0F = 9 x 0C + 32 5 32 0F = 0 0C 212 0F = 100 0C 1.7 Convertir 172.9 0F a grados Celsius. 9 = x 0C + 32 5 0F – 32 = 9 x 0C 5 0F 5 x (0F – 32) = 0C 9 0C = 5 x (0F – 32) 9 0C = 5 x (172.9 – 32) = 78.3 9 1.7 Notación científica El número de átomos en 12 g de carbono: 602,200,000,000,000,000,000,000 6.022 x 1023 La masa de un solo átomo de carbono en gramos: 0.00000000000000000000000199 1.99 x 10-23 N x 10n N es un número entre 1 y 10 n es un entero positivo o negativo 1.8 Notación científica 568.762 0.00000772 mover decimal a la izquierda mover decimal a la derecha n>0 n<0 568.762 = 5.68762 x 102 0.00000772 = 7.72 x 10-6 Adición o sustracción 1. Escribir cada cantidad con el mismo exponente n 2. Combinar N1 y N2 3. El exponente, n, permanece igual 4.31 x 104 + 3.9 x 103 = 4.31 x 104 + 0.39 x 104 = 4.70 x 104 1.8 Notación científica Multiplicación 1. Multiplicar N1 y N2 2. Sumar exponentes n1 y n2 División 1. Dividir N1 y N2 2. Restar exponentes n1 y n2 (4.0 x 10-5) x (7.0 x 103) = (4.0 x 7.0) x (10-5+3) = 28 x 10-2 = 2.8 x 10-1 8.5 x 104 ÷ 5.0 x 109 = (8.5 ÷ 5.0) x 104-9 = 1.7 x 10-5 1.8 Cifras significativas •Cualquier dígito que no es cero es significativo 1.234 kg 4 cifras significativas •Los ceros entre los dígitos no cero son significativos 606 m 3 cifras significativas •Los ceros a la izquierda del primer dígito no cero no son significativos 0.08 L 1 figura significativa •Si un número es mayor que 1, entonces todos los ceros a la derecha del punto decimal son significativos 2.0 mg 2 cifras significativas •Si un número es menor que 1, entonces sólo los ceros que están al final y en medio del número son significativos 0.00420 g 3 cifras significativas 1.8 ¿Cuántas cifras significativas están en cada una de las medidas siguientes? 24 mL 2 cifras significativas 3001 g 4 cifras significativas 0.0320 m3 3 cifras significativas 6.4 x 104 moléculas 2 cifras significativas 560 kg 2 cifras significativas 1.8 Cifras significativas Adición o sustracción La respuesta no puede tener más dígitos a la derecha del punto decimal que cualquiera de los números originales. 89.332 +1.1 90.432 3.70 -2.9133 0.7867 una cifra significativa después del punto decimal redondeo a 90.4 dos cifra significativa después del punto decimal redondeo a 0.79 1.8 Cifras significativas Multiplicación o división El número de cifras significativas en el resultado está determinado por el número original que tiene el número más pequeño de figuras significativas. 4.51 x 3.6666 = 16.536366 = 16.5 3 cifra sig redondeo a 3 cifra sig 6.8 ÷ 112.04 = 0.0606926 = 0.061 2 cifra sig redondeo a 2 cifra sig 1.8 Cifras significativas Números exactos Obtenidos por definición o al contar varios objetos, pueden considerarse formados por un número infinito de cifras significativas. ¿El promedio de tres longitudes medidas; 6.64, 6.68 y 6.70? 6.64 + 6.68 + 6.70 = 6.67333 = 6.67 = 7 3 Porque 3 es un número exacto 1.8 Exactitud: cuán cercana está una medición del valor real de la cantidad medida. Precisión: cuánto concuerdan dos o más mediciones de una misma cantidad. exactitud y precisión buenas exactitud deficiente y buena precisión exactitud y precisión deficientes 1.8 El método del factor unitario para la resolución de problemas 1. Determine qué factor(es) unitario de conversión se necesita. 2. Lleve las unidades a través del cálculo 3. Si todas las unidades se cancelan excepto para la unidad(es) deseada, entonces el problema se resolvió correctamente. ¿Cuántos mL están en 1.63 L? 1 L = 1000 mL 1000 mL 1.63 L x = 1630 mL 1L 2 1L L 1.63 L x = 0.001630 1000 mL mL 1.9 La velocidad del sonido en el aire es aproximadamente 343 m/s. ¿Cuál es esta velocidad en millas por hora? metros a millas segundos a horas 1 mi = 1609 m 1 min = 60 s 1 mi 60 s m x x 343 s 1609 m 1 min 1 hora = 60 min 60 min mi x = 767 hora 1 hora 1.9